05_теории биологического окисления.pptx
- Количество слайдов: 23

Биологическое окисление

Окисление – это химическая реакция, включающая потерю атомом или молекулой одного или более электронов. Всегда является частью реакции ОКИСЛЕНИЯВОССТАНОВЛЕНИЯ, при которой эти электроны приобретаются другим атомом или молекулой. Раньше этот термин использовался в более узком смысле для обозначения реакции, при которой кислород взаимодействует с другим элементом или веществом, в результате чего образуется оксид.

Биологическое окисление – это совокупность реакций окисления, направленных на обеспечение организма энергией в доступной для использования форме (АТФ). Окисление органических соединений может быть связано: 1) с потерей электрона; 2) с отрывом водорода от окисляемого субстрата; 3) с замещением атомов на другие, более электроотрицательные атомы. Особенность биологического окисления: многократность передачи Н+ и ē (или только ē) от одного соединения (донора, восстановителя) к другому (акцептору, окислителю). Это обеспечивает постепенное высвобождение энергии: без взрыва и пламени, в водной среде, при нормальном давлении.

Все три типа реакций имеют место в живой клетке. Если акцептором водорода в реакциях дегидрирования служит не кислород, а какой-либо другой субстрат, то совокупность таких реакций называют анаэробным окислением. Анаэробное окисление – это процесс генерации водорода с участием никотинзависимых и флавинзависимых дегидрогеназ. Если же акцептором водорода является кислород и в продуктах реакции присутствует вода, то такие реакции называют аэробным окислением, или тканевым дыханием. Тканевое дыхание – это распад органических веществ в живых тканях, сопровождающийся потреблением кислорода

История развития учения о биоокислении 1) Антуан Лоран Лавуазье (1743— 1794), французский химик. указал на то, что жизнь возможна только в присутствии кислорода, отметил сходство между процессами горения угля и тканевым дыханием. Но уже тогда было очевидно, что биологическое окисление во многом отличается от процессов горения, а именно: оно протекает в необычных, очень «мягких» условиях - при сравнительно низкой температуре (370 С), без образования пламени и в присутствии воды как главного компонента человеческого организма.

2) Теория А. Н. Баха – «теория активации кислорода» или «перекисная теория» Алексей Николаевич Бах (1857 -1946) Согласно теории А. Н. Баха, в организме есть ферменты (оксигеназы), которые активируют кислород, образуя пероксиды, окисляя таким образом субстрат. Кислород воздуха не является активным окислителем, так как обе валентности кислорода взаимно насыщают друга: О=О. Для того чтобы кислород мог быть активным окислителем, он должен быть сперва активизирован, т. е. должна получиться молекула с подобного рода связями: — О —.

По Баху, окислительные ферменты оксидазы состоят из самоокисляющихся веществ, которые, присоединяя кислород воздуха, образуют перекисеобразные соединения. Под действием ферментов пероксидаз отщепляется активный атомарный кислород. Пероксидазы разлагают перекись водорода Н 2 О 2 на воду и активный атомарный кислород: Н 2 О 2 = Н 2 О + О Выделенный кислород уже окисляет соответственное вещество.

В дальнейшем оказалось, что действительно в клетках существует ферменты, способные активировать молекулярный кислород и использовать его для окисления ряда веществ. Существуют ферменты монооксигеназы, которые присоединяют к субстрату один атом кисло рода (SH +1/2 O 2 → SOH ) и диоксигеназы, которые присоединяют к субстрату 2 атома кислорода (S + O 2 → SO 2). Монооксигеназы и диоксигеназы катализируют реакции гидроксилирования стероидов, ксенобиотиков, но не принимают участия в процессах биологического окисления в митохондриях.

3) Теория В. И. Палладина – «теория активации водорода» Владимир Иванович Палладин (1859 -1922) По теории В. И. Палладина, окисление может происходить путем дегидрирования без участия кислорода при помощи посредников – акцепторов водорода, т. е. окисление происходит как в аэробных условиях, так и в анаэробных. Отнятие от веществ (субстратов) водорода происходит с участием специальных ферментов - хромогенов. После этого водород, по Палладину, может передаваться или на молекулу кислорода с образованием воды, или на другие молекулы, восстанавливая их.

Основные положения теории Палладина: 1. Непременным участником дыхания является вода. 2. Вода наряду с окисляемым субстратом выполняет роль донора водорода. 3. В процессе дыхания участвуют специфические активаторы водорода, отнимающие водород от субстрата. 4. Первые этапы дыхания являются анаэробными и не требуют присутствия молекулярного кислорода. 5. Молекулярный кислород используется на заключительном этапе дыхания для регенерации акцепторов водорода с образованием воды.
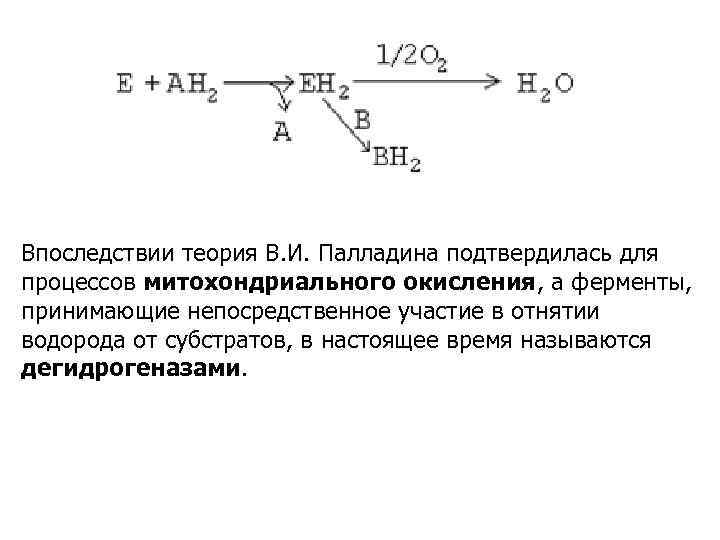
Впоследствии теория В. И. Палладина подтвердилась для процессов митохондриального окисления, а ферменты, принимающие непосредственное участие в отнятии водорода от субстратов, в настоящее время называются дегидрогеназами.
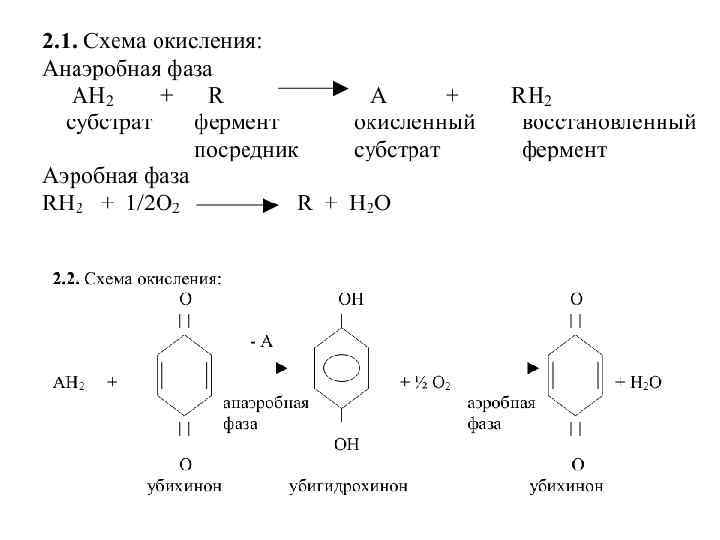
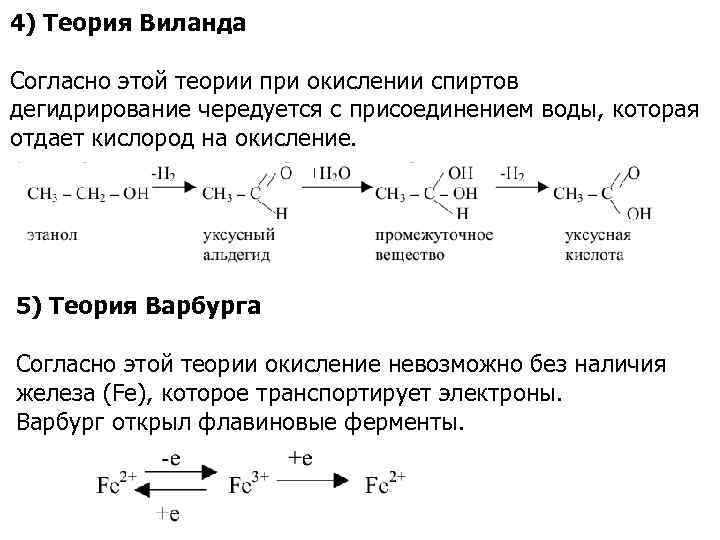
4) Теория Виланда Согласно этой теории при окислении спиртов дегидрирование чередуется с присоединением воды, которая отдает кислород на окисление. 5) Теория Варбурга Согласно этой теории окисление невозможно без наличия железа (Fe), которое транспортирует электроны. Варбург открыл флавиновые ферменты.

6) В 30 -х годах Энгельгардт наблюдал, что при тканевом дыхании накапливаются молекулы АТФ, т. е. показал связь тканевого дыхания с накоплением органического фосфата. 7) Белицер и Цыбакова показали, что тканевое дыхание связано с транспортом электронов и ввели коэффициент Р/О, который показывает число молекул АТФ, которое образуется на каждый поглощенный атом кислорода. 8) В 1961 – 1966 г. г. английский биохимик П. Митчел описал теорию окислительного фосфорилирования, связанную с транспортом протонов через сопряженную мембрану митохондрий, за что в 1978 г. получил Нобелевскую премию. Теория называется хемиосмотической.

Ферменты и коферменты, участвующие в биологическом окислении Перенос электронов от окисляемых субстратов к кислороду происходит в несколько этапов. В нём участвует большое количество промежуточных переносчиков, каждый из которых способен присоединять электроны от предыдущего компонента и передавать следующему. Так возникает цепь окислительно-восстановительных реакций.

Первичные акцепторы водорода окислительновосстановительных реакций относят к 2 типам дегидрогеназ: 1) никотинамидзависимым, содержащим в качестве коферментов производные никотиновой кислоты, 2) флавинзависимым, содержащим производные рибофлавина.
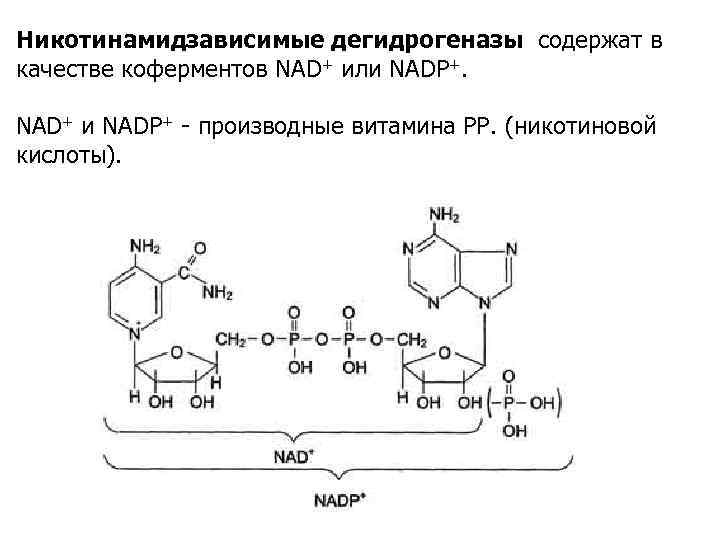
Никотинамидзависимые дегидрогеназы содержат в качестве коферментов NAD+ или NADP+. NAD+ и NADP+ - производные витамина PP. (никотиновой кислоты).
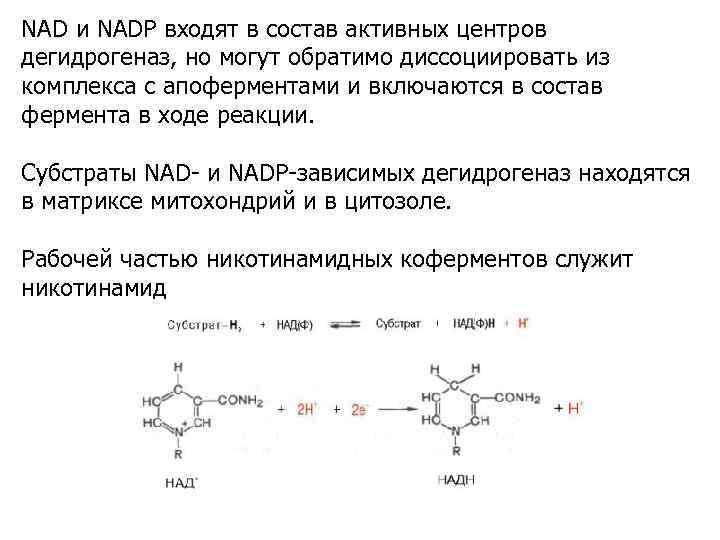
NAD и NADP входят в состав активных центров дегидрогеназ, но могут обратимо диссоциировать из комплекса с апоферментами и включаются в состав фермента в ходе реакции. Субстраты NAD- и NADP-зависимых дегидрогеназ находятся в матриксе митохондрий и в цитозоле. Рабочей частью никотинамидных коферментов служит никотинамид

Большинство дегидрогеназ, поставляющих электроны в ЭТЦ, содержат NAD+. Они катализируют реакции типа: R-CHOH-R 1 + NAD+↔ R-CO-R 1 + NADH + Н+. NAD+, присоединяя протоны и электроны от различных субстратов, служит главным коллектором энергии окисляемых веществ и главным источником электронов, обладающих высоким энергетическим потенциалом, для ЭТЦ. NADPH не является непосредственным донором электронов в ЦПЭ, а используется почти исключительно в восстановительных биосинтезах. Однако возможно включение электронов с NADPH в ЭТЦ благодаря действию пиридиннуклеотид трансгидрогеназы, катализирующей реакцию: NADPH + NAD+ ↔ NADP+ + NADH.
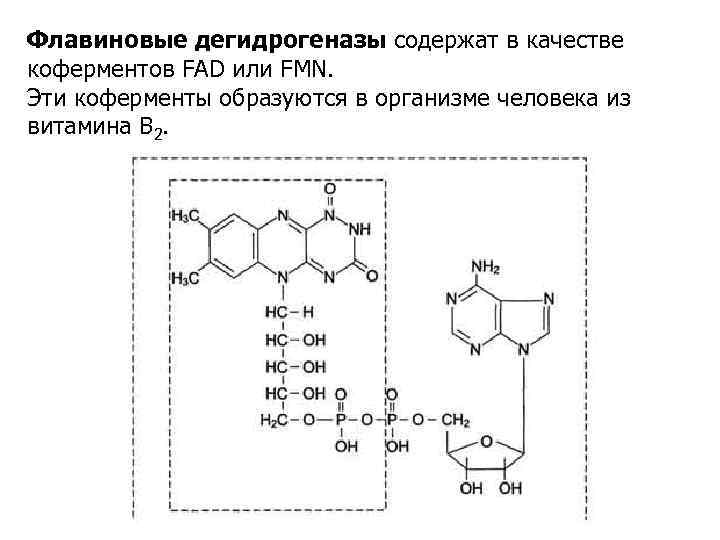
Флавиновые дегидрогеназы содержат в качестве коферментов FAD или FMN. Эти коферменты образуются в организме человека из витамина В 2.
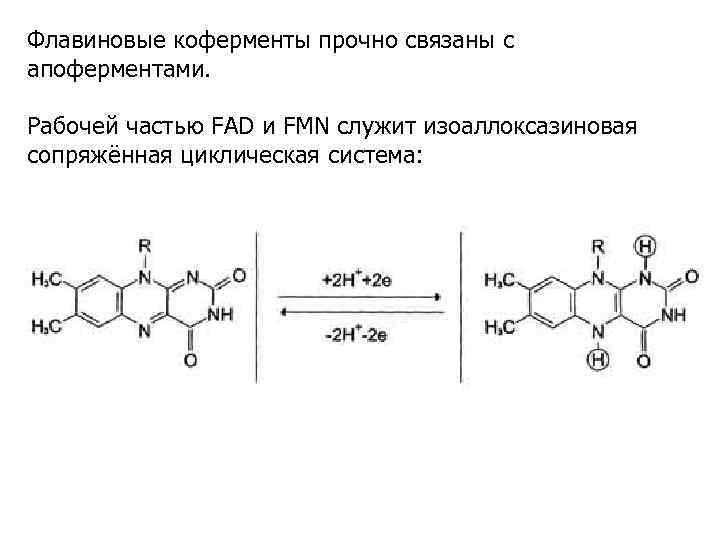
Флавиновые коферменты прочно связаны с апоферментами. Рабочей частью FAD и FMN служит изоаллоксазиновая сопряжённая циклическая система:

FAD служит акцептором электронов от многих субстратов в реакциях типа: R-CH 2 -R 1 + Е (FAD) ↔ R-CH=CH-R 1 + Е (FADH 2), где Е - белковая часть фермента. Большинство FAD-зависимых дегидрогеназ - растворимые белки, локализованные в матриксе митохондрий. Исключение составляет сукцинат-дегидрогеназа, находящаяся во внутренней мембране митохондрий. К FMN-содержащим ферментам принадлежит NADHдегидрогеназа, которая также локализована во внутренней мембране митохондрий; она окисляет NADH, образующийся в митохондриальном матриксе. Реакция протекает по уравнению: NADH + Н+ + Е (FMN) → NAD+ + Е (FMNH 2)
05_теории биологического окисления.pptx