биологическое окисление1.ppt
- Количество слайдов: 51

Биологическое окисление

Обмен энергии
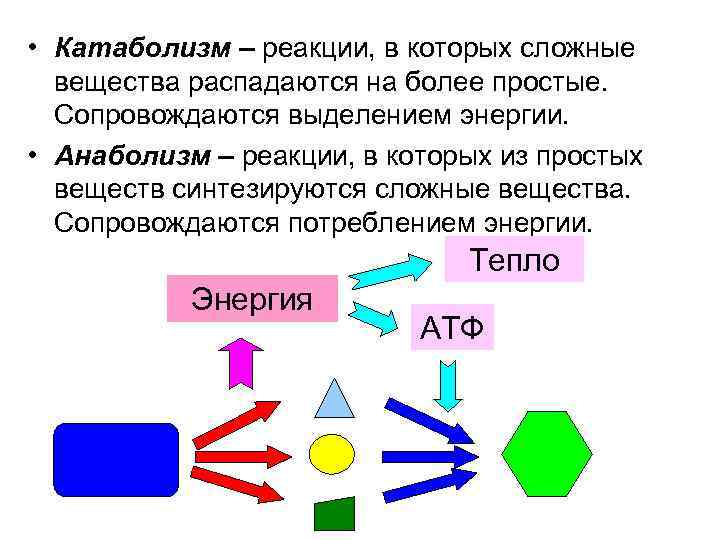
• Катаболизм – реакции, в которых сложные вещества распадаются на более простые. Сопровождаются выделением энергии. • Анаболизм – реакции, в которых из простых веществ синтезируются сложные вещества. Сопровождаются потреблением энергии. Тепло Энергия АТФ
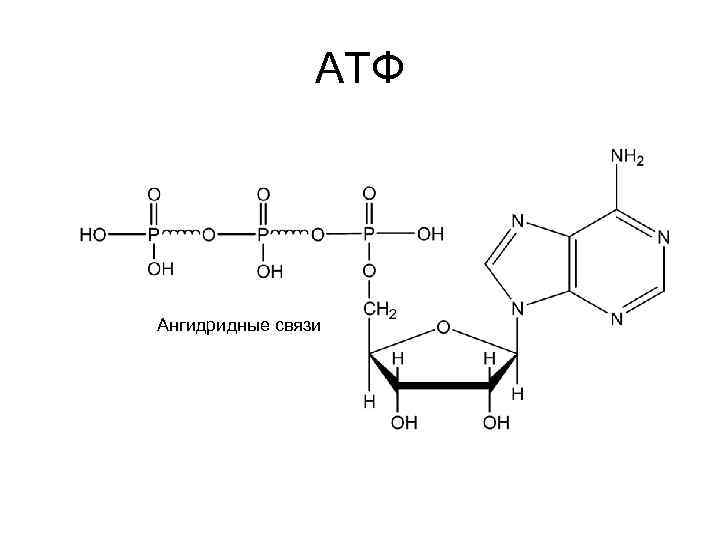
АТФ Ангидридные связи
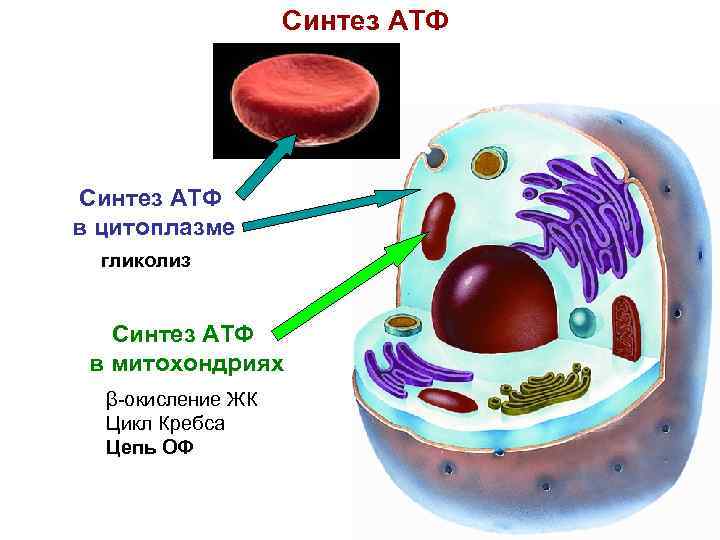
Синтез АТФ в цитоплазме гликолиз Синтез АТФ в митохондриях β-окисление ЖК Цикл Кребса Цепь ОФ
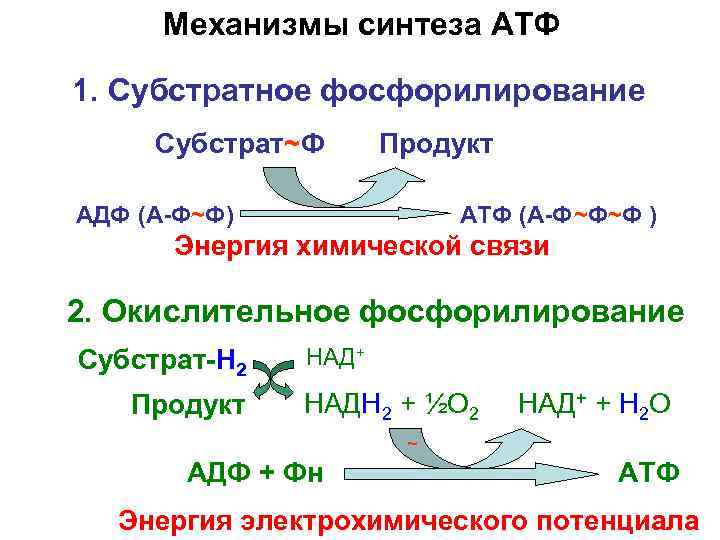
Механизмы синтеза АТФ 1. Субстратное фосфорилирование Субстрат~Ф Продукт АДФ (А-Ф~Ф) АТФ (А-Ф~Ф~Ф ) Энергия химической связи 2. Окислительное фосфорилирование Субстрат-H 2 Продукт НАД+ НАДН 2 + ½О 2 НАД+ + Н 2 О ~ АДФ + Фн АТФ Энергия электрохимического потенциала

Митохондрии Ключевую роль в энергетическом обмене клетки играют митохондрии 1. Наружная мембрана (содержит белок порин – поры 2 -3 нм, высокая проницаемость молекул до 5 к. Да. Также есть переносчики для крупных молекул) 2. Межмембранное пространство (1020 нм, состав похож на цитоплазму) 3. Внутренняя мембрана (имеет складки, содержит белки 70% (ферменты ЦОФ, транспортные), фосфолипид кардиолипин с 4 ЖК, непроницаема для протонов) 4. Матрикс (до 50% белков: ферменты ЦТК, β-окисления ЖК, АТ и др. , мт. ДНК, мт. РНК, рибосомы)

Митохондрии млекопитающих обычно содержат от двух до десяти идентичных копий кольцевых молекул ДНК У человека в митохондриях 16565 пар нуклеотидов и содержит 37 генов: • 13 кодируют биосинтез белков, • 22 являются матрицей для т. РНК, • 2 являются матрицей для р. РНК • • NADH-дегидрогеназа (комплекс I) Кофермент Q цитохром c редуктаза/Цитохром b (комплекс III) цитохром c оксидаза (комплекс IV) АТФ-синтаза (комплекс V) р. РНК т. РНК

История развития учения о биологическом окислении I. Антуан Лоран Лавуазье (1743 – 1794) – французский химик – в 1777 г. впервые правильно истолковал явление горения как процесс соединения веществ с О 2. Т. к. горение и дыхание сопровождаются потреблением О 2 и выделение СО 2, он предположил что, в их основе лежит один процесс. Но у дыхания были существенные отличия от горения, идёт: ü при низкой температуре; ü ü без пламени; в присутствии воды.

В конце XIX века русские исследователи А. Н. Бах и В. И. Палладин, работая независимо друг от друга, предложили 2 основные теории для объяснения процессов, протекающих в ходе биологического окисления. II. Алексей Николаевич Бах (1857 – 1946). В 1897 г сформулировал «ПЕРЕКИСНУЮ ТЕОРИЮ МЕДЛЕННОГО ОКИСЛЕНИЯ» , согласно которой молекула О 2 сначала активируется в результате разрыва одной его связи (-О-О-) и присоединения к органическим веществам – оксидазам. Активированный О 2 при взаимодействии с окисляемым веществом образует перекись.
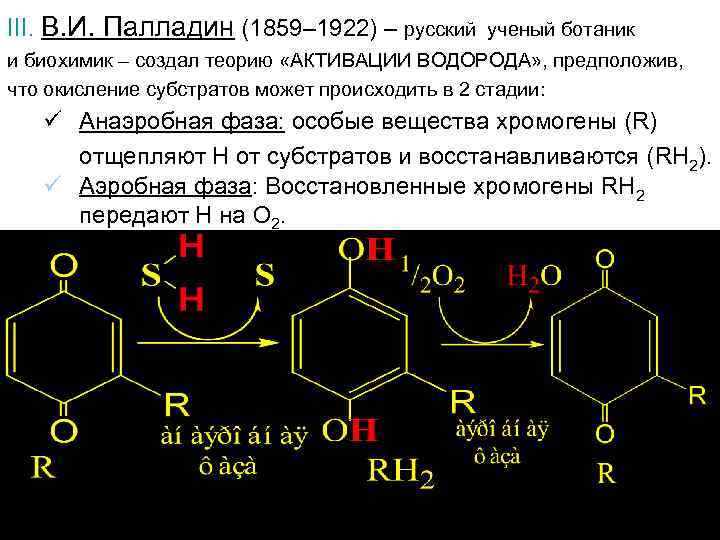
III. В. И. Палладин (1859– 1922) – русский ученый ботаник и биохимик – создал теорию «АКТИВАЦИИ ВОДОРОДА» , предположив, что окисление субстратов может происходить в 2 стадии: ü Анаэробная фаза: особые вещества хромогены (R) отщепляют Н от субстратов и восстанавливаются (RH 2). ü Аэробная фаза: Восстановленные хромогены RH 2 передают Н на О 2.

IV. В дальнейшем значительный вклад в исследование БО внесли ряд и других учёных. Вот некоторые из них: ü Кейлин Дейвид (1881 -1963) открыл цитохромы. Установил, что они способны передавать H+ и e- с окисляемого S на O 2. ü Шенбайн показал, что БО – каталитический процесс, в котором используется активный кислород. ü Отто Генрих Варбург открыл фермент(E) – цитохромоксидазу, работающую на заключительном этапе БО. Процесс БО представляет не только процессы дегидрирования, но и активирования О 2 железосодержащими E.

ü Генрих Отто Виланд установил, что процесс окисления может реализоваться в анаэробных условиях с использованием элементов воды.

Современные представления о биологическом окислении Согласно современной теории БО: 1. окисление происходит как в аэробных, так и в анаэробных условиях; 2. в аэробных организмах существует несколько путей использования О 2; 3. реакции БО необходимы для: ü получения энергии; ü синтеза новых веществ; ü разрушения чужеродных веществ; 4. БО является сложным, многостадийным процессом, в котором ведущую роль играют ферменты оксидоредуктазы.

Основные понятия БО Окислительно-восстановительные реакции (ОВР) – реакции, в которых меняется степень окисления субстрата за счет присоединения / отщепления: 1) 1 е-; Цит1(Fe 3+) + Цит2(Fe 2+) 2) 2 е- и 2 Н+; Субстрат-H 2 + R Цит1(Fe 2+) + Цит2(Fe 3+) Продукт + RH 2 3) атомов кислорода Субстрат-H 2 + ½O 2 Продукт + H 2 O
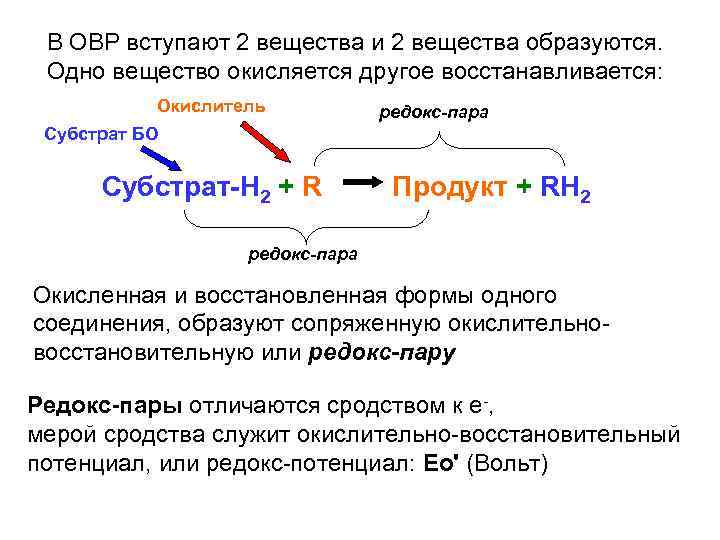
В ОВР вступают 2 вещества и 2 вещества образуются. Одно вещество окисляется другое восстанавливается: Окислитель редокс-пара Субстрат БО Субстрат-H 2 + R Продукт + RH 2 редокс-пара Окисленная и восстановленная формы одного соединения, образуют сопряженную окислительновосстановительную или редокс-пару Редокс-пары отличаются сродством к е-, мерой сродства служит окислительно-восстановительный потенциал, или редокс-потенциал: Ео' (Вольт)
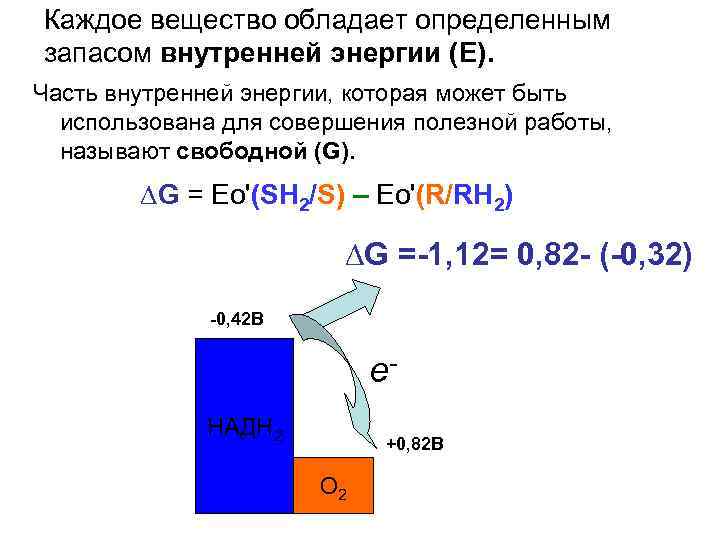
Каждое вещество обладает определенным запасом внутренней энергии (Е). Часть внутренней энергии, которая может быть использована для совершения полезной работы, называют свободной (G). ∆G = Ео'(SH 2/S) – Ео'(R/RH 2) ∆G =-1, 12= 0, 82 - (-0, 32) -0, 42 В е. НАДН 2 +0, 82 В О 2

Биологическое окисление (БО) - совокупность окислительно-восстановительных реакций в живых клетках. Особенности реакций БО: • протекают в аэробных и анаэробных условия; • катализируются оксидоредуктазами; • являются многостадийным процессом; • Существует несколько путей их использования: основной - синтез АТФ (90%), а также синтез новых веществ, разрушения ксенобиотиков и продуктов метаболизма. Субстрат БО – вещество, способное отдавать электрон. (вещества, способные вступать в реакции окисления) Субстрат-H 2

ü Дыхательная цепь – цепь переноса электронов. В переносе электронов от субстратов БО к О 2 принимают участие: 1. НАД– и НАДФ– зависимые ДГ; 2. ФАД– и ФМН– зависимые ДГ; 3. Цитохромы; 4. Коэнзим Q; 5. Белки, содержащие негеминовое железо.
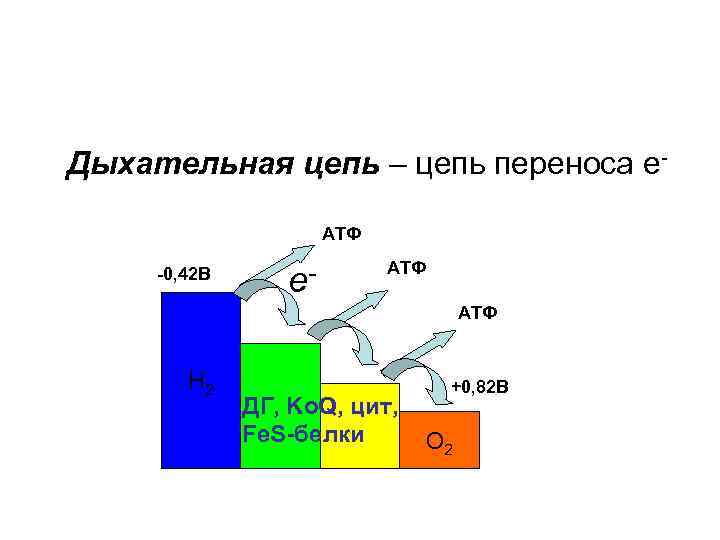
Дыхательная цепь – цепь переноса е. АТФ -0, 42 В е- АТФ Н 2 ДГ, Ko. Q, цит, Fe. S-белки +0, 82 В О 2

Пути использования О 2 в клетке В настоящее время выделено 4 основные пути использования О 2 в организме: 1. Оксидазный путь Функция: 90% О 2 используется для синтеза АТФ; 2. Монооксигеназный путь (Обеспечивает включение 1 атома кислорода в молекулу субстрата) Функции: ü синтез новых веществ (стероидные гормоны), ü обезвреживание ксенобиотиков и токсических продуктов обмена в митохондриях и ЭПР;

3. Диоксигеназный путь (Обеспечивает включение молекулы кислорода в молекулу субстрата) Функция: ü деградация АК; ü синтез новых веществ; 4. Свободно-радикальный путь Функции: ü внутриклеточное пищеварение; ü разрушение бактерий, вирусов, онко- и стареющих клеток; ü образование БАВ.
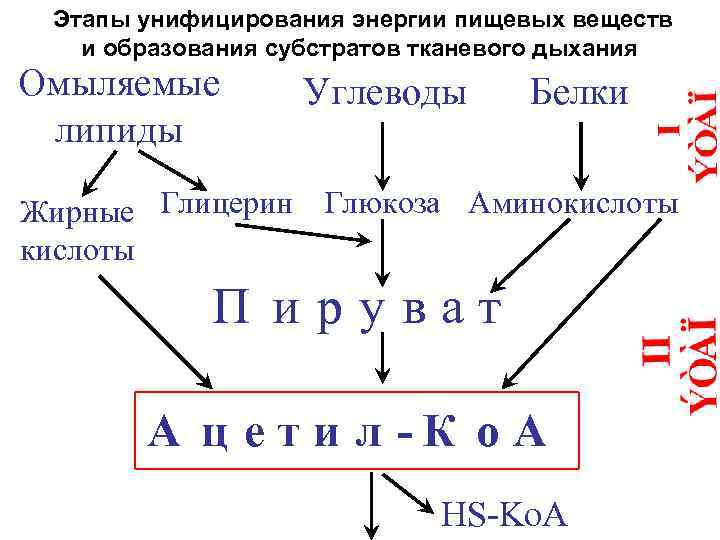
Этапы унифицирования энергии пищевых веществ и образования субстратов тканевого дыхания Омыляемые липиды Углеводы Белки Жирные Глицерин Глюкоза Аминокислоты П ируват А ц е т и л -К о А HS-Ko. A
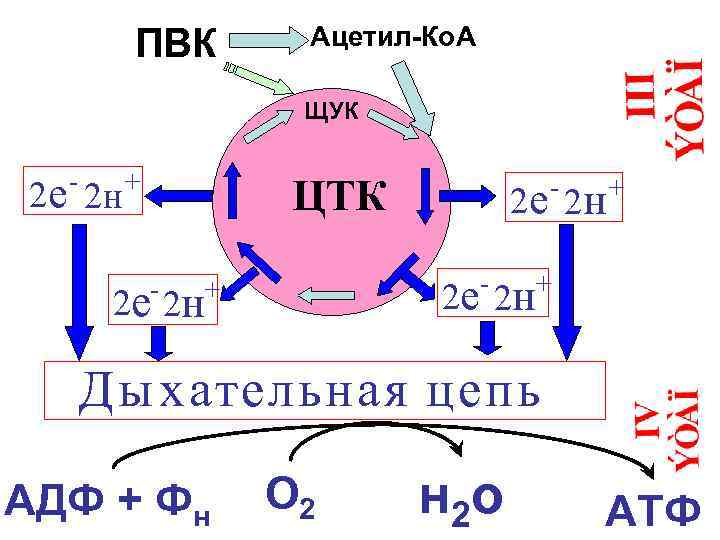
ПВК Ацетил-Ко. А ЩУК - 2 е 2 н + - ЦТК - 2 е 2 н - + + 2 е 2 н Д ы хательная цепь АДФ + Фн О 2 н 2 о АТФ
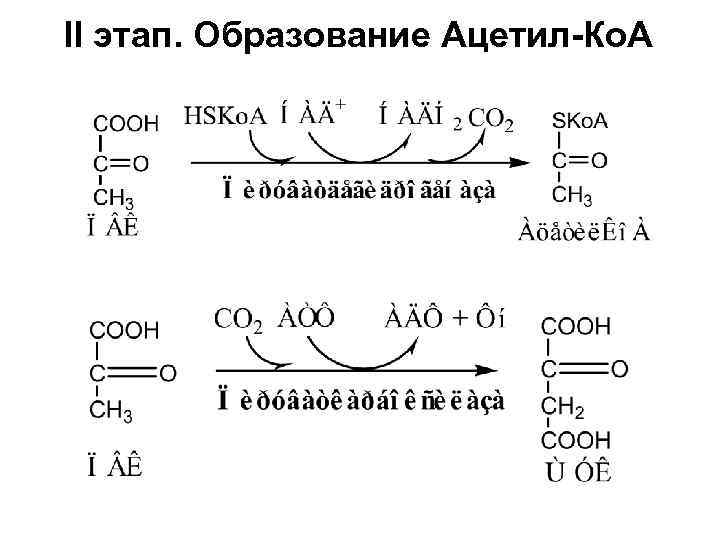
II этап. Образование Ацетил-Ко. А

III этап. Цикл Кребса (цикл трикарбоновых кислот) ü ЦТК является процессом окисления Ацетил–Ко. А - универсального продукта катаболизма углеводов, белков и омыляемых липидов; ü ЦТК протекает в митохондриях с участием 8 ферментов, которые локализованы в матриксе в свободном состоянии, или на внутренней поверхности внутренней мембраны; ü В ЦТК участвуют 5 витаминов В 1, В 2, РР, пантотеновая кислота и липоевая кислота в виде коферментов тиаминпирофосфата, ФАД, НАД+, Ко. А и липоата.

Н 2 О Цикл лимонной кислоты (цикл Кребса). Н 2 О Цис-аконитат Цитрат 3 2 Изоцитрат Н 2 О 4 1 HS-Ko. A НАД+ ИДГ Ацетил-Ко. А Оксалоацетат НАДН 2 СО 2 НАДН 2 -кетоглутарат 12 АТФ НАД+ МДГ НАД+ Малат 5 НАДН 2 НS-Ko. A 8 Н 2 О CO 2 Фумарат Е-ФАДН 2 Е-ФАД Сукцинил - Ко. А СДГ HS-Ko. A 7 6 Сукцинат H 3 PO 4 + ГДФ ГТФ
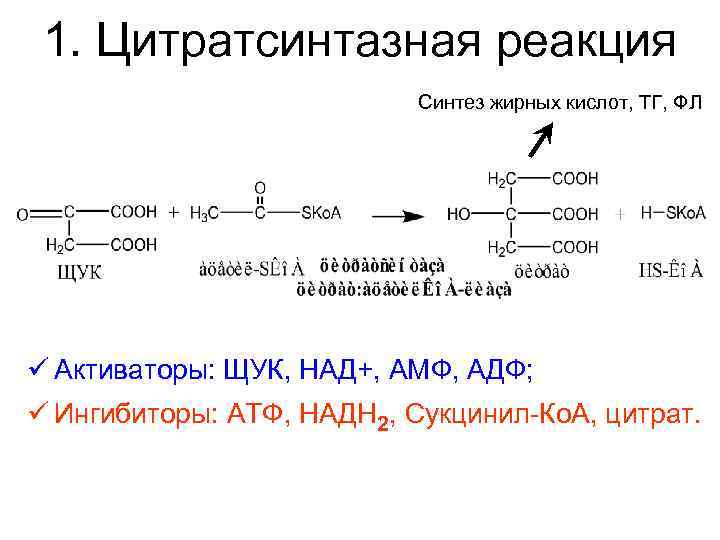
1. Цитратсинтазная реакция Синтез жирных кислот, ТГ, ФЛ ü Активаторы: ЩУК, НАД+, АМФ, АДФ; ü Ингибиторы: АТФ, НАДН 2, Сукцинил-Ко. А, цитрат.
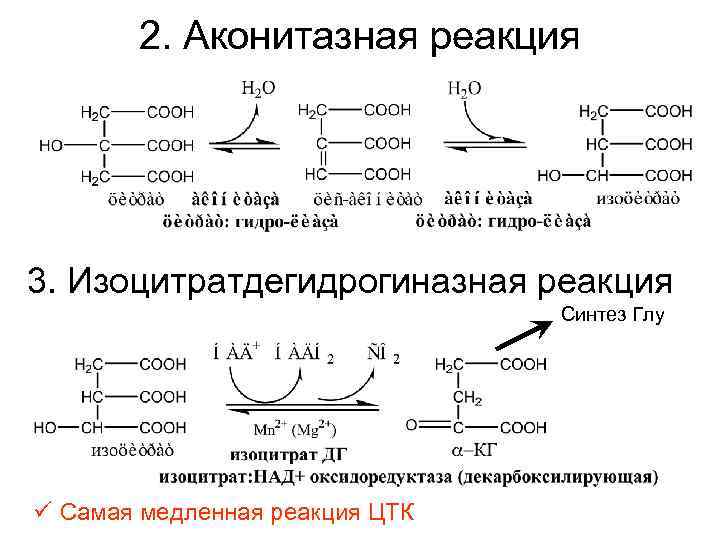
2. Аконитазная реакция 3. Изоцитратдегидрогиназная реакция Синтез Глу ü Самая медленная реакция ЦТК

4. α-Кетоглутаратдегидрогиназная Синтез гема реакция ü Активаторы: ионы Са; ü Ингибиторы: АТФ, сукцинил-Ко. А, НАДH 2; ü α-КГДГ комплекс состоит из 3 ферментов и содержит 5 коферментов: тиаминдифосфат, кофермент А, липоевая кислота, НАД+, ФАД.
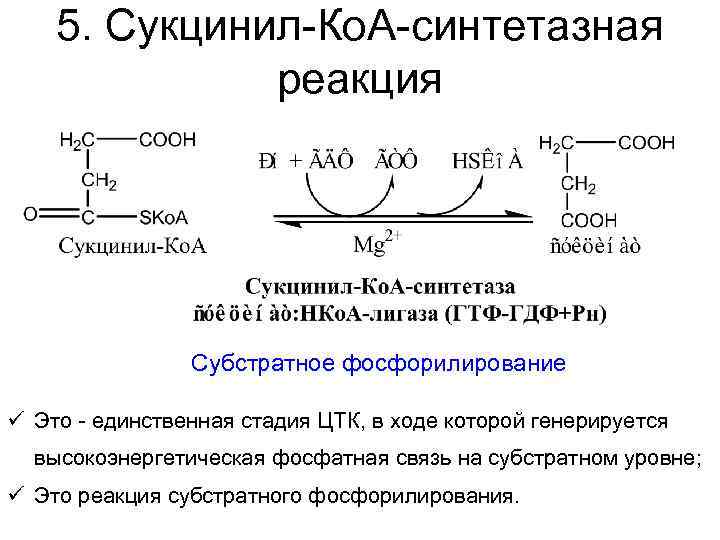
5. Сукцинил-Ко. А-синтетазная реакция Субстратное фосфорилирование ü Это - единственная стадия ЦТК, в ходе которой генерируется высокоэнергетическая фосфатная связь на субстратном уровне; ü Это реакция субстратного фосфорилирования.

6. Сукцинатдегидрогиназная реакция ü СДГ является флавопротеином, состоящим из 2 субъединиц: Fe 2 S 2 и Fe 4 S 4, одна из которых связана с ФАД; ü Ингибитор: ЩУК и Сукцинил–Ко. А.
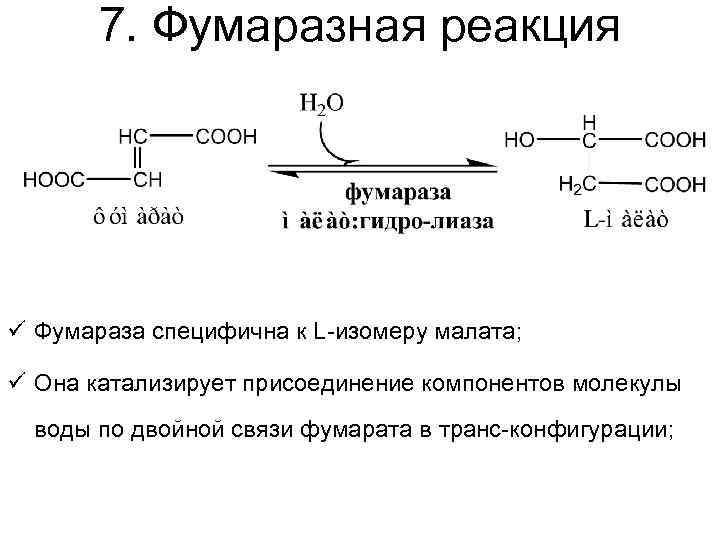
7. Фумаразная реакция ü Фумараза специфична к L-изомеру малата; ü Она катализирует присоединение компонентов молекулы воды по двойной связи фумарата в транс-конфигурации;
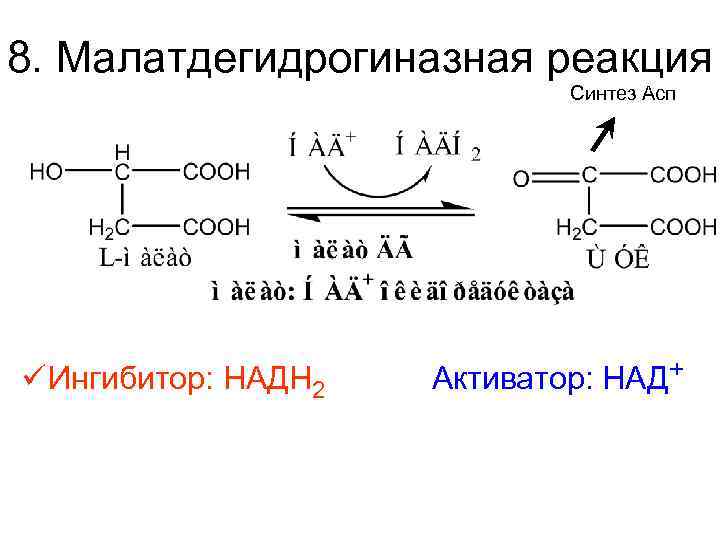
8. Малатдегидрогиназная реакция Синтез Асп ü Ингибитор: НАДН 2 Активатор: НАД+

Энергетический баланс одного оборота ЦТК • В 4 ОВР ЦТК образуются 3 НАДН 2 и 1 ФАДН 2, которые направляются далее в дыхательную цепь окислительного фосфорилирования. • В процессе окислительного фосфорилирования из 1 НАДН 2 образуется 3 АТФ, из 1 ФАДН 2 – 2 АТФ. • Из ГТФ, образующейся в ЦТК, синтезируется 1 АТФ: ГТФ + АДФ ГДФ + АТФ • Таким образом, за 1 цикл ЦТК из 3 НАДН 2, 1 ФАДН 2 и 1 ГТФ получается 12 АТФ.

Регуляция ЦТК 1. Регуляторные (ключевые, лимитирующие) ферменты: 1. Цитратсинтаза 2. изоцитрат ДГ 3. α-КГ ДГ 4. СДГ 2. Ингибирует – НАДН 2 и АТФ, которые являются продуктами ЦТК и дыхательной цепи 3. Активируют – НАД+ и АДФ 4. Первая - пусковая реакция ЦТК зависит от концентрации ЩУК, Ацетил-Ко. А

5. Стимулирует ЦТК гормон инсулин, а ингибирует – глюкагон 6. O 2 активирует ЦТК, переводя восстановленные формы НAДH 2, ФAДH 2 в окисленные 7. Аммиак связывает α–КГ и цикл блокируется

Биологическое значение ЦТК 1. образование водородных эквивалентов, которые в цепи ОФ обеспечивают синтез АТФ; 2. выполняет ведущую роль в: ü глюконеогенезе; ü переаминировании и дезаминировании АК; ü синтезе жирный кислот и липогенезе; ü синтезе гема. 3. интегрирует все виды обмена веществ

IV этап. Окислительное фосфорилирование История окислительного фосфорилирования В 1966 г. английский ученый Питер Денис Митчелл сформулировал хемиосмотическую гипотезу объясняющую принцип окислительного фосфорилирования. В 1979 г. - Нобелевская премия

Положения хемиосмотической теории • цепь реакций, осуществляющихся в процессе дыхания, представляет собой последовательность сменяющих друга протонов и электронов. • Белковые носители таким образом организованы во внутренней митохондриальной мембране, что переносят протоны через мембрану. • Поскольку митохондриальная мембрана не допускает пассивного тока протонов, в процессе дыхания генерируется электрохимическая разность потенциалов – мембранный потенциал. • Под ее действием протоны с внешней поверхности стремятся назад во внутриклеточное пространство. Именно этот поток протонов, который можно сравнить с электрическим током в батарее, и выполняет всю работу.
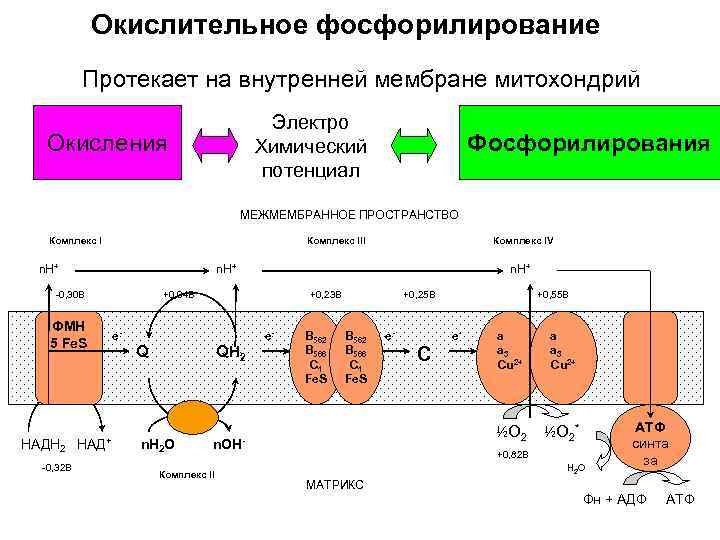
Окислительное фосфорилирование Протекает на внутренней мембране митохондрий Электро Химический потенциал Окисления Фосфорилирования МЕЖМЕМБРАННОЕ ПРОСТРАНСТВО Комплекс III n. Н+ -0, 30 В ФМН 5 Fe. S НАДН 2 НАД+ -0, 32 В Комплекс IV n. Н+ +0, 04 В +0, 23 В е- е- Q QН 2 n. Н 2 О B 562 B 566 C 1 Fe. S +0, 25 В B 562 B 566 C 1 Fe. S е- C a a 3 Cu 2+ ½О 2* n. ОН- Комплекс II е- +0, 55 В +0, 82 В Н 2 О МАТРИКС АТФ синта за Фн + АДФ АТФ
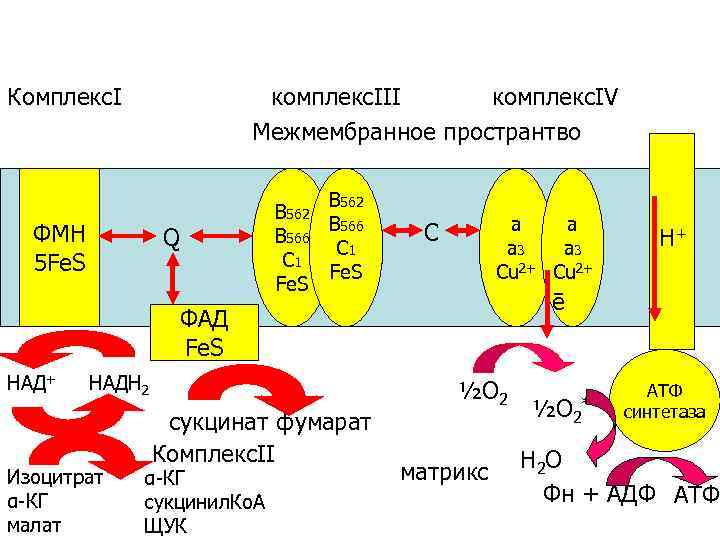
окисление КомплексΙ комплексΙΙΙ комплексΙV Межмембранное пространтво ФМН 5 Fе. S Q В 562 В 566 С 1 Fe. S а а а 3 Сu 2+ C ē ФАД Fe. S НАД+ НАДН 2 Изоцитрат α-КГ малат сукцинат фумарат КомплексΙΙ α-КГ сукцинил. Ко. А ЩУК Н+ ½О 2 матрикс ½О 2 * АТФ синтетаза Н 2 О Фн + АДФ АТФ
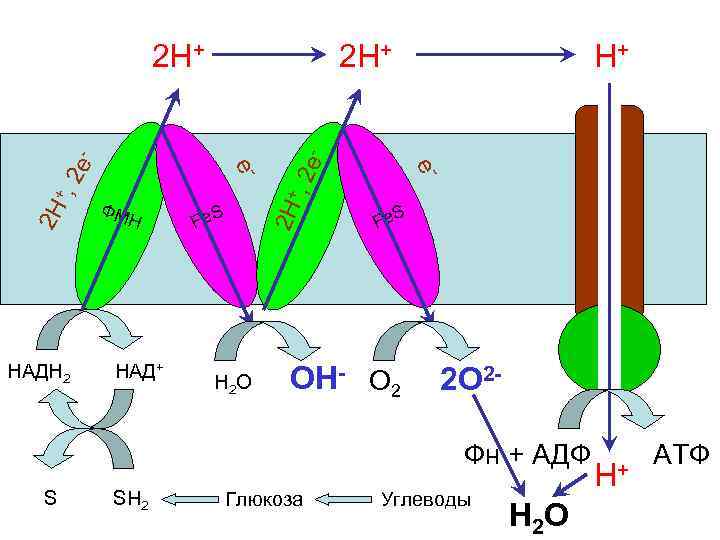
Н 2 О 2 Н + , 2 - НАДН 2 НАД+ Fe. S Н+ е - е ФМ Н 2 Н + , 2 е - 2 Н+ е- 2 Н+ Fe. S ОН- О 2 2 О 2 Фн + АДФ АТФ + S SH 2 Глюкоза Углеводы Н Н 2 О
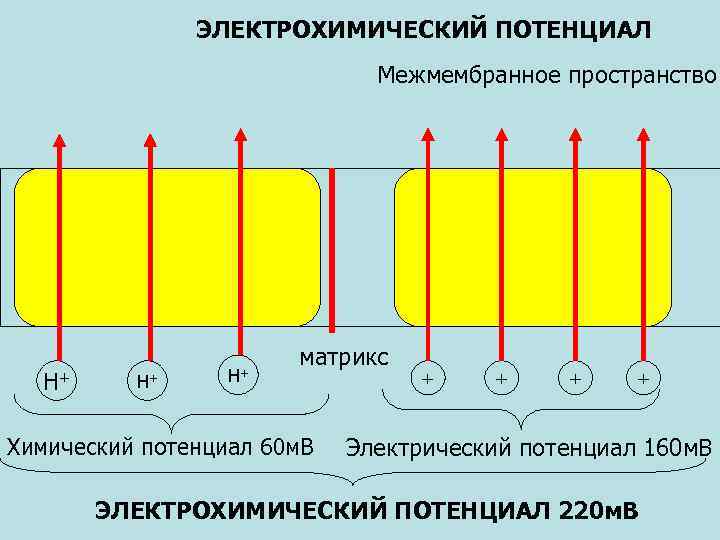
ЭЛЕКТРОХИМИЧЕСКИЙ ПОТЕНЦИАЛ Межмембранное пространство Н+ Н+ Н+ матрикс Химический потенциал 60 м. В + + Электрический потенциал 160 м. В ЭЛЕКТРОХИМИЧЕСКИЙ ПОТЕНЦИАЛ 220 м. В
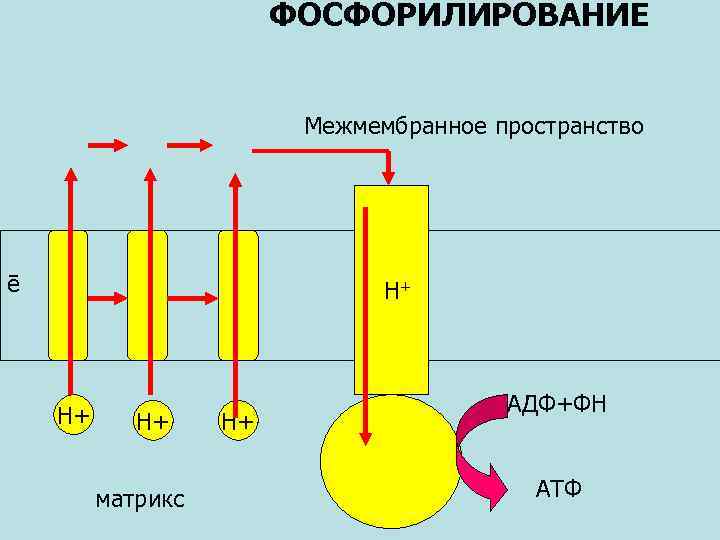
ФОСФОРИЛИРОВАНИЕ Межмембранное пространство ē Н+ Н+ Н+ матрикс Н+ АДФ+ФН АТФ
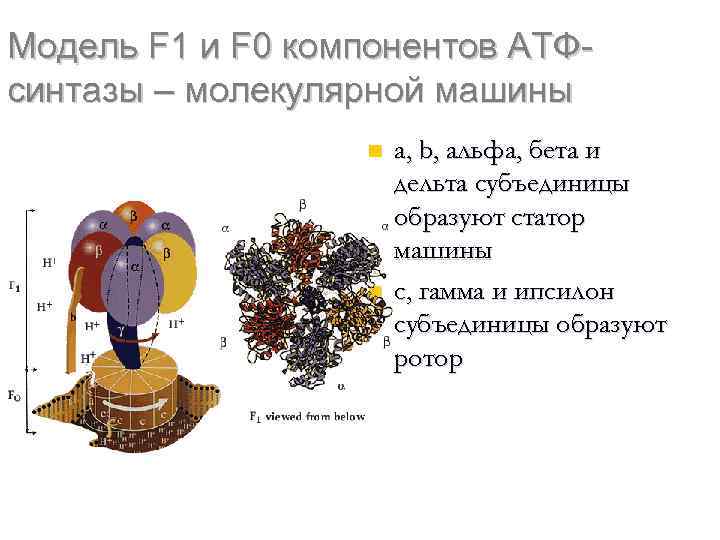
Модель F 1 и F 0 компонентов АТФсинтазы – молекулярной машины n n a, b, альфа, бета и дельта субъединицы образуют статор машины с, гамма и ипсилон субъединицы образуют ротор
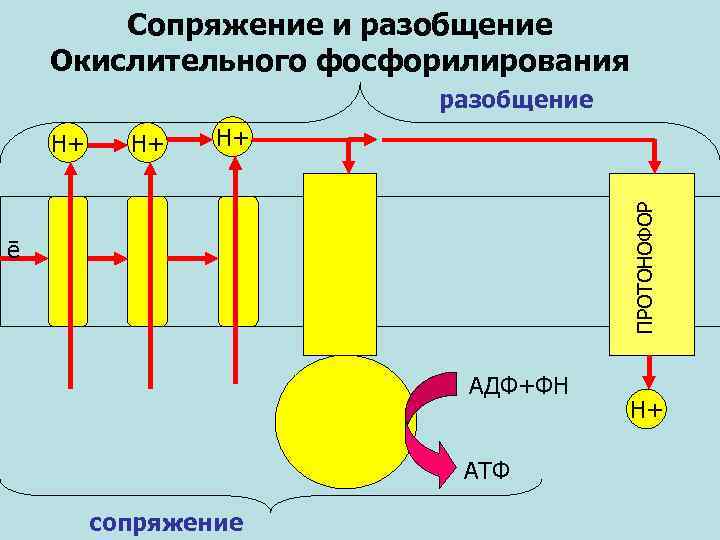
Сопряжение и разобщение Окислительного фосфорилирования разобщение Н+ Н+ ПРОТОНОФОР Н+ ē АДФ+ФН АТФ сопряжение Н+
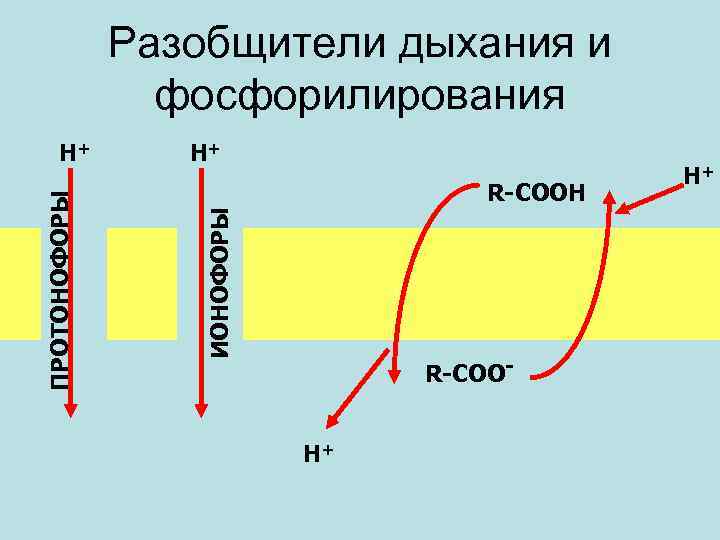
Разобщители дыхания и фосфорилирования Н+ R-СООН ИОНОФОРЫ ПРОТОНОФОРЫ Н+ R-СООН+ Н+

2, 4 -Динитрофенол • 2, 4 -динитрофенол является классическим разобщителем окислительного фосфорилирования. При действии на митохондрии стимулирует их дыхание, но ингибирует сопряженное с ним фосфорилирование, т. е. синтез АТФ из АДФ и фосфата.

Дыхательный контроль - Зависимость интенсивности дыхания митохондрий от концентрации АДФ. В результате дыхательного контроля скорость синтеза АТФ соответствует потребностям клетки в энергии. Общее содержание АТФ в организме 30— 50 г Молекула АТФ «живёт» меньше минуты. В сутки у человека синтезируется 40— 60 кг АТФ и столько же распадается.

Спасибо за внимание!
биологическое окисление1.ppt