Биологическое окисление.pptx
- Количество слайдов: 38

Биологическое окисление: этапы, пути использования кислорода в тканях

История развития учения о биологическом окислении В 1777 г французский химик Антуан Лоран Лавуазье (1743 -1794), впервые правильно истолковал явление горения как процесс соединения веществ с О 2. В 1897 г Алексей Николаевич Бах (1857 -1946) сформулировал «перекисную теорию окисления» , согласно которой молекула О 2 сначала активируется. Активация О 2 происходит в результате разрыва одной его связи (-О-О-) и присоединения к органическим веществам – оксидазам. Активированный О 2 при взаимодействии с окисляемым веществом образует перекись. Теория «перекисного окисления» Баха нашла свое подтверждение, однако главный механизм БО оказался иным.

Важнейшая заслуга в развитии учения о БО принадлежит русскому ученому ботанику и биохимику В. И. Палладину (1859 -1922), который создал теорию дыхания, как совокупности ферментативных процессов. Он предположил, что окисление субстратов может происходить в 2 фазы: 1). Анаэробная фаза. В этой фазе особые вещества хромогены (R) отщепляют Н от субстратов и восстанавливаются (RH 2). Аэробная фаза. Восстановленные хромогены RH 2 передают Н на О 2. В последствии теория В. И. Паладина подтвердилась для процессов митоходриального окисления, а хромогены, принимающие участие в отнятии водорода от субстратов, в настоящее время называются ферментами дегидрогеназами.

Современные представления о биологическом окислении Окисление происходит как в аэробных, так и в анаэробных условиях. В аэробных организмах существует несколько путей использования О 2. Реакции БО необходимы в первую очередь для получения энергии в форме АТФ, а также для синтеза новых веществ, разрушения ксенобиотиков и продуктов метаболизма. БО является сложным, многостадийным процессом, в котором ведущую роль играют ферменты оксидоредуктазы.

В соответствие с путями потребления кислорода и катализируемыми реакциями, все оксидоредуктазы разделены на 5 групп: 1). Оксидазы удаляют Н из субстрата (S), используя в качестве акцептора Н только О 2, продуктом реакции является вода. Все оксидазы содержат медь. Например, цитохромоксидаза, последний фермент дыхательной цепи. SН 2 + ½О 2 → S + Н 2 О

2). Аэробные дегидрогеназы, или ФАД зависимые оксидазы, относятся к металлофлавопротеинам (ФАД, ФМН, Fe, Cu, Mo), находятся в пероксисомах и наружной мембране митоходрий. Они отнимают Н от субстрата, и передают его на О 2 с образованием перекиси. Дегидрогеназа L-аминокислот (оксидаза Lаминокислот) в почках осуществляет окислительное дезаминирование. Ксантиндегидрогеназа (ксантиноксидаза) превращает пурины в мочевую кислоту. Моноаминоксидазы (МАО) окисляют гормон адреналин и некоторые биогенные амины. Диаминоксидазы (ДАО) окисляют гистамин и другие диамины и полиамины. Образующаяся перекись бактерицидное действие. SН 2 + О 2 → S + Н 2 О 2

3). Анаэробные дегидрогеназы многочисленная группа, содержат в качестве коферментов НАДН 2, НАДФН 2, ФАД, ФМН, цитохромы. Они удаляют Н из субстрата, не используя в качестве акцептора протона О 2. Анаэробные дегидрогеназы выполняют две главные функции: перенос Н с одного субстрата на другой в сопряженной ОВР и транспорт электронов в дыхательной цепи. Примеры ферментов: изоцитрат ДГ (НАДН 2), сукцинат ДГ (ФАДН 2), цитохромы в, с1, с, а и а 3. SН 2 + R → S + RН 2

4). Оксигеназы. Включают кислород в молекулу субстрата. Работают в составе мультиферментного комплекса, содержащего ФАД зависимую ДГ, Fe 2 S 2 белок, цитохромы Р 450 или В 5. Этот комплекс встроен в мембрану ЭПР или внутреннюю мембрану митохондрий.

5). Гидроксипероксидазы разрушают перекиси водорода и органические перекиси. Ферменты пероксидаза и каталаза. Пероксидазы, содержат протогем, восстанавливают перекись до воды за счет хинонов, аскорбата или цитохрома с. Глутатионперосидаза, содержит селен, восстанавливает перекись до воды за счет глутатиона. Н 2 О 2 + RH 2 → 2 Н 2 О + R Каталаза, гемопротеин, использует одну Н 2 О 2 как донор е-, а вторую Н 2 О 2 как акцептор е-, в результате образуется вода и молекула кислорода. Каталазы много в крови, костном мозге, слизистых оболочках, почках и печени. 2 Н 2 О 2 → 2 Н 2 О + О 2

Пути использования кислорода в клетке Оксидазный путь - окислительное фосфорилирование. Протекает в митохондриях, является основным источником АТФ в аэробных тканях. Потребляет 90% кислорода. Монооксигеназный путь. Обеспечивает включение 1 атома кислорода в молекулу субстрата. Используется для синтеза новых веществ (стероидные гормоны), обезвреживания ксенобиотиков и токсических продуктов обмена в митохондриях и ЭПР.

Диоксигеназный путь. Обеспечивает включение молекулы кислорода в молекулу субстрата. Используется для деградации АК и синтеза новых веществ.

Пероксидазный и радикальный пути. Кислород участвует в образовании перекисей и активных радикалов, которые необходимы в пероксисомах для внутриклеточного пищеварения, разрушения макрофагами бактерий, вирусов, регуляции метаболизма и т. д. Перекиси и активные кислородные радикалы оказывают также повреждающее воздействие на структуры клеток и тканей, активируя ПОЛ. Разрушение перекисей и инактивация свободных радикалов осуществляется с помощью ферментативной и неферментативной антиокидантной системы.

Основные понятия Окислительно-восстановительные реакции (ОВР) – реакции, в которых меняется степень окисления субстрата за счет присоединения/отщепления: 1) 1 е-; 2) 2 е- и 2 Н+; 3) атомов кислорода. Биологическое окисление (БО) совокупность окислительно-восстановительных реакций, которые протекают во всех живых клетках. Субстрат БО – вещество, способное отдавать электрон. (Любые вещества, способные вступать в реакции окисления).

Тканевое дыхание – окисление органических веществ в клетках, сопровождающееся потреблением О 2 и выделением воды. Субстрат тканевого дыхания – это вещество, которое отдает электрон непосредственно в цепь окислительного фосфорилирования. (Например, НАДН 2, ФАДН 2). Дыхательная цепь – цепь переноса электронов. В переносе электронов от субстратов БО к О 2 принимают участие: 1) НАД и НАДФ зависимые ДГ; 2) ФАД и ФМН зависимые ДГ; 3) цитохромы; 4) коэнзим Q; 5) белки, содержащие негеминовое железо.
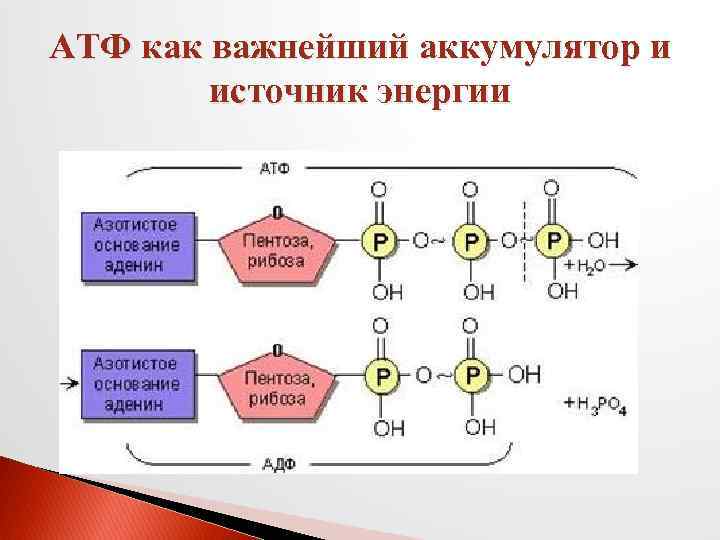
АТФ как важнейший аккумулятор и источник энергии

Энергетический баланс одного оборота ЦТК В 4 окислительно-восстановительных реакциях ЦТК образуются 3 НАДН 2 и 1 ФАДН 2, которые направляются далее в дыхательную цепь окислительного фосфорилирования. В процессе окислительного фосфорилирования ДЦ из 1 НАДН 2 образуется 3 АТФ, из 1 ФАДН 2 - 2 АТФ. Из 1 ГТФ, образующейся в ЦТК за счет субстратного фосфорилирования, синтезируется 1 АТФ. Таким образом, за 1 цикл ЦТК из 3 НАДН 2, 1 ФАДН 2 и 1 ГТФ получается 12 АТФ.
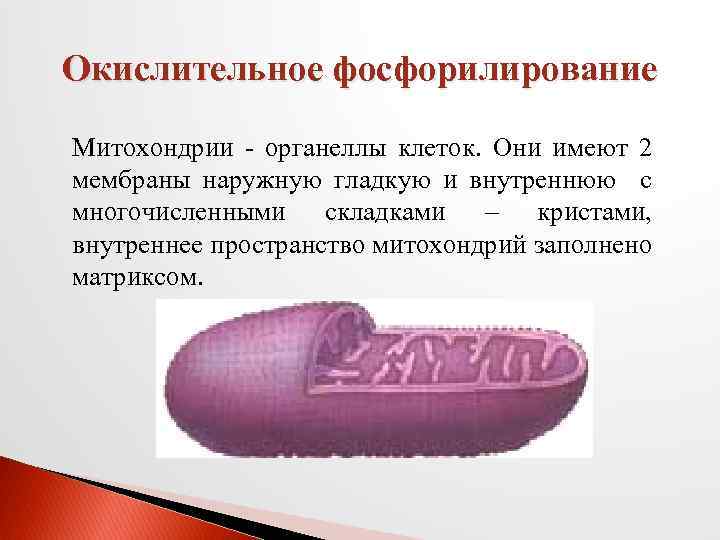
Окислительное фосфорилирование Митохондрии - органеллы клеток. Они имеют 2 мембраны наружную гладкую и внутреннюю с многочисленными складками – кристами, внутреннее пространство митохондрий заполнено матриксом.
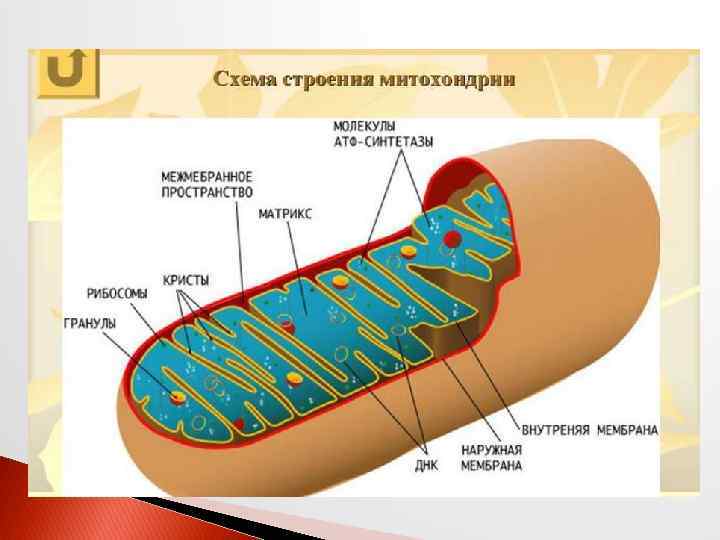

Наружная мембрана содержит много белка порина, образующего гидрофильные каналы, которые пропускаю через мембрану неорганические ионы, метаболиты и даже небольшие белки (меньше 10 к. Да). Также она содержит ферменты: элонгазы (удлиняют молекулы насыщенных жирных кислот), кинуренингидроксилазу, моноаминооксидазу (маркер) и др. Межмембранное пространство митохондрий содержит аденилатциклазу, нуклеозиддифосфаткиназы.

Внутренняя мембрана высокоспецифична, состоит на 70% из белков, которые выполняют каталитическую (окислительное фосфорилирование) и транспортную функцию. Внутренняя мембрана содержит ферменты: а). цепи окислительного фосфорилирования (цитохромоксидаза – маркер) б). СДГ в). βоксибутират ДГ; г). карнитинацилтрансферазу, д). карнитинацилтранслоказу. Внутренняя мембрана на 30% состоит из фосфолипидов, из них 20% приходиться на кардиолипин, который делает мембрану непроницаемой для всех ионов.

Матрикс на 50% состоит из белка и содержит сотни различных ферментов. Это ферменты: а). ЦТК; б). β-окисления жирных кислот; в). аминотрансферазы АСТ, АЛТ; г). глутамат ДГ д). фосфоенолпируваткарбоксилазу е). пируват ДГ. Также матрикс содержит несколько копий митохондриальной ДНК, митохондриальные рибосомы и т. РНК. В клетке содержится от сотни до тысячи митохондрий, их размер 2 -3 мкм в длину и 1 мкм в ширину.

Метаболические и гомеостатические функции митохондрий В митохондриях происходит: синтез АТФ и теплопродукция в реакция окислительного фосфорилирования; β-окисления жирных кислот; реакции ЦТК, через ЦТК протекают некоторые реакции глюконеогенеза, переаминирования, дезаминирования, липогенеза и синтеза гема, осуществляется интеграция белкового, липидного и углеводного обмена.

Причины и последствия повреждений митохондрий Повреждение внутренней мембраны митохондрий химическими и физическими факторами приводит разобщению окислительного фосфорилирования, нарушению синтеза АТФ, торможению анаболических реакций, межмембранного транспорта и всех видов обмена веществ.

Оксидазный путь использования кислорода в клетке Оксидазный путь потребления кислорода протекает в митохондриях, потребляет 90% О 2 и обеспечивает процесс окислительного фосфорилирования. Окислительным фосфорилированием называют синтез АТФ из АДФ и Н 3 РО 4 за счет энергии движении электронов по дыхательной цепи. Окислительное фосфорилирование является основным источником АТФ в аэробных клетках.

Хемиосмотическая теория Митчелла Для объяснения механизма окислительного фосфорилирования в 1961 году Митчеллом была предложена хемиосмотическая теория, которая включала четыре независимых постулата, касавшиеся функции митохондрий: 1. Внутренняя мембрана митохондрий непроницаема для всех ионов. 2. Она содержит ряд белков-переносчиков, осуществляющих транспорт необходимых метаболитов и неорганических ионов. 3. При прохождении электронов по дыхательной цепи внутренней мембраны происходит перемещение Н+ из матрикса в межмембранное пространство. 4. При достаточно большом протонном градиенте протоны начинают «течь» через АТФ-синтетазу, что сопровождается синтезом АТФ.

МЕХАНИЗМ ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ Окислительное фосфорилирование состоит из процессов окисления и фосфорилирования, которые между собой сопряжены. Процесс окисления происходит при движении электронов по дыхательной цепи от субстратов тканевого дыхания на кислород. Дыхательная цепь окислительного фосфорилирования состоит из 4 белковых комплексов, встроенных во внутреннюю мембрану митохондрий и небольших подвижных молекул убихинона и цитохрома С, которые циркулируют в липидном слое мембраны между белковыми комплексами.
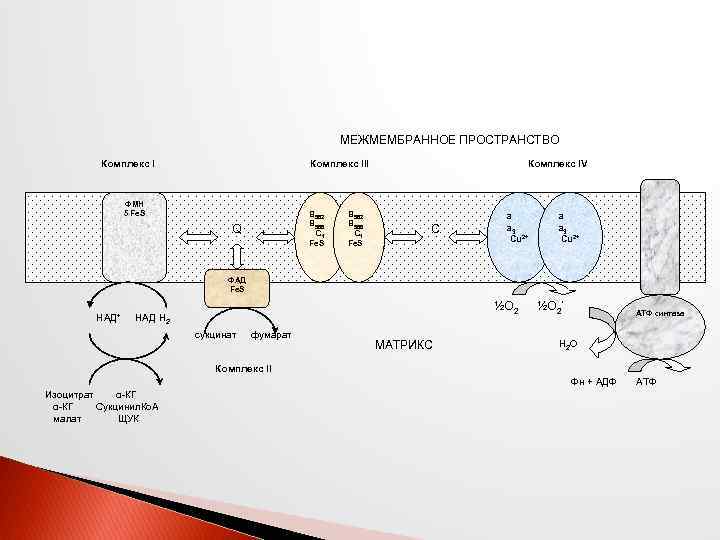
МЕЖМЕМБРАННОЕ ПРОСТРАНСТВО Комплекс III ФМН 5 Fe. S B 562 B 566 C 1 Fe. S Комплекс IV C a a 3 ½О 2 Q a a 3 ½О 2* Cu 2+ ФАД Fe. S НАД+ НАД Н 2 сукцинат фумарат МАТРИКС АТФ синтаза Н 2 О Комплекс II Фн + АДФ Изоцитрат α-КГ Сукцинил. Ко. А малат ЩУК АТФ

Комплекс I – НАДН 2 дегидрогеназный комплекс – самый большой из дыхательных ферментных комплексов – имеет молекулярную массу свыше 800 КДа, состоит из более 22 полипептидных цепей, в качестве коферментов содержит ФМН и 5 железо-серных (Fe 2 S 2 и Fe 4 S 4) белков. Комплекс II – СДГ. В качестве коферментов содержит ФАД и железо-серный белок.

Комплекс III – Комплекс b-c 1 (фермент QH 2 ДГ), имеет молекулярную массу 500 КДа, состоит из 8 полипептидных цепей, и вероятно существует в виде димера. Каждый мономер содержит 3 гема, связанных с цитохромами b 562, b 566, с1, и железосерный белок. Комплекс IV – Цитохромоксидазный комплекс имеет молекулярную массу 300 КДа, состоит из 8 полипептидных цепей, существует в виде димера. Каждый мономер содержит 2 цитохрома (а и а 3) и 2 атома меди. Коэнзим Q (убихинон). Липид, радикал которого у млекопитающих образован 10 изопреноидными единицами (Q 10). Убихинон переносит по 2 Н+ и 2 е-.

Этапы движения е- по дыхательной цепи 2 е- от НАДН 2, проходят через I комплекс (ФМН→Fe. S белок) на Ко. Q, высвобождаемая при этом энергия обеспечивает перекачку Н+ (механизм переноса Н+ неизвестен). Ко. Q с 2 е- забирает у воды 2 Н+ из матрикса и превращается в Ко. QН 2 (восстановление Ко. Q проходит также с участием комплекса II). Ко. QН 2 переносит 2 е- на комплекс III, а 2 Н+ в межмембранное пространство. Цитохром С переносит е- c III комплекса на IV комплекс сбрасывает е- на О 2, высвобождаемая при этом энергия обеспечивает перекачку Н+ (механизм переноса Н+ неизвестен).

При переносе Н+ из матрикса в межмембранное пространство на внутренней мембране создается осмотический градиент протонов ∆р. Н = 60 м. В (при ∆р. Н=1) (в матриксе р. Н выше, чем в цитозоле). Так каждый Н+ несет положительный заряд, на внутренней мембране также появляется разность потенциалов ∆ =160 м. В, внутренняя сторона мембраны заряжается отрицательно, внешняя – положительно. В сумме осмотический градиент протонов и разность потенциалов образуют электрохимический потенциал, который в типичной клетке составляет около 60+160=220 м. В.

Механизм переноса Н+ через мембрану до конца не изучен. Вероятно, у разных компонентов дыхательной цепи существуют разные механизмы сопряжения транспорта е- с перемещением Н+. Образовавшийся на внутренней мембране митохондрий электрохимический потенциал используется для: фосфорилирования АДФ в АТФ; транспорта веществ через мембрану митохондрий; теплопродукцию.
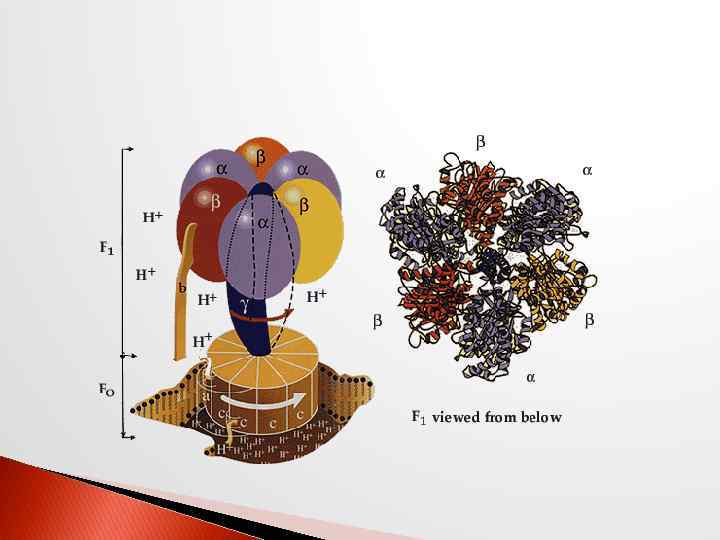

АТФ-синтетаза обеспечивает обратимое взаимопревращение энергии электрохимического потенциала и энергии химических связей. Электрохимический потенциал внутренней мембраны заставляет Н+ двигаться из межмебранного пространства по каналу АТФ-синтазы в матрикс митохондрий. При каждом переносе протонов через канал Fo энергия электрохимического потенциала расходуется на поворот стержня, в результате которого циклически изменяется конформация а- и β-субъединиц и все 3 активных центра, образованных парам α- и βсубъединиц, катализируют очередную фазу цикла: 1) связывание АДФ и Н 3 РО 4 2) образование фосфоангидридной связи АТФ; 3) освобождение конечного продукта АТФ.

Сопряжения и разобщения окислительного фосфорилирования Процесс окисления создает электрохимический потенциал, а процесс фосфорилирования его использует. Таким образом, электрохимический потенциал обеспечивает сопряжение (связывание) процессов окисления и фосфорилирования (окислительного фосфорилирования). Так как необходимый для сопряжения электрохимический потенциал создают I, III и IV комплексы дыхательной цепи, их называют пунктами сопряжения окисления и фосфорилирования.

Разобщение дыхания и фосфорилирования называют явление исчезновения на мембране электрохимического потенциала под действием разобщителей и прекращение синтеза АТФ. Разобщителями являются вещества, которые могут переносить протоны (протонофоры) или другие ионы (ионофоры) через мембрану минуя каналы АТФсинтетазы. В результате разобщения количество АТФ снижается, АДФ увеличивается, возрастает скорость потребления О 2, окисления НАДН 2, ФАДН 2, а образовавшаяся свободная энергия выделяется в виде теплоты. Как правило, разобщители — липофильные вещества, легко проходящие через мембраны. Например, вещество 2, 4 -динитрофенол (переносит Н+), лекарство - дикумарол, метаболит - билирубин, гормон щитовидной железы - тироксин, антибиотики - валиномицин и грамицидин.

Коэффициент окислительного фосфорилирования Коэффициентом окислительного фосфорилирования (Р/О) называют отношение количества фосфорной кислоты (Р), использованной на фосфорилирование АДФ, к атому кислорода (О), поглощённого в процессе дыхания. При окисление молекулы НАДН 2, е- по дыхательной цепи проходят 3 пункта сопряжения, что обеспечивает синтез 3 АТФ при затрате 3 Н 3 РО 4 и 3 АДФ на 1 атом кислорода. Соответственно для НАДН 2 Р/О=3. При окисление молекулы ФАДН 2, е- по дыхательной цепи проходят только 2 пункта сопряжения, что обеспечивает синтез 2 АТФ при затрате 2 Н 3 РО 4 и 2 АДФ на 1 атом кислорода. Соответственно для ФАДН 2 Р/О=2. Эти величины Р/О отражают теоретический максимум синтеза АТФ, фактически эта величина меньше из-за затрат на транспорт.

Дыхательный контроль Зависимость интенсивности дыхания митохондрий от концентрации АДФ называют дыхательным контролем. В результате дыхательного контроля скорость синтеза АТФ соответствует потребностям клетки в энергии. Общее содержание АТФ в организме 30— 50 г, но каждая молекула АТФ в клетке «живёт» меньше минуты. В сутки у человека синтезируется 40— 60 кг АТФ и столько же распадается. В норме субстраты тканевого дыхания и О 2 находятся в достаточном количестве и не лимитируют окислительное фосфорилирование. Активность окислительного фосфорилирования ограничивает только концентрация АДФ, которая обратно пропорциональна концентрации АТФ. При нагрузке концентрация АТФ снижается, а АДФ увеличивается, что ускоряет дыхание и фосфорилирование. В состоянии покоя количество АТФ увеличивается, а АДФ снижается, что тормозит дыхание и фосфорилирование.
Биологическое окисление.pptx