Обмен белков и аминокислот-стомфак, фармфак.ppt
- Количество слайдов: 36

Биологическая химия Обмен белков и аминокислот Лектор: доцент каф. биохимии, к. х. н. Н. Н. Ковганко

Белки в организме постоянно синтезируются и распадаются. Это и называется обмен белков. Азотистый баланс – это общий показатель обмена белка в организме.

Азотистый баланс - разница между азотом, поступившим в организм (в виде белка) и выведенным из него ü положительный (рост, беременность, лактация), ü отрицательный (заболевания, старческий возраст, белковая недостаточность). ü азотистое равновесие Коэффициент изнашивания – количество белка, которые теряются у человека на безбелковой диете (около 20 г/сутки) N = 80 − 100 г белка в сутки

Факторы, определяющие белковую потребность: ü возраст: белковая потребность у детей выше, чем у взрослых; üбеременность: прибавляется приблизительно 950 г нового белка для плода и развития репродуктивных тканей; üлактация: необходимо для обеспечения ребенка белком; üпериод реабилитации после болезни: необходимо для восполнения белков в тканях; üкатаболическое состояние: при хирургических операциях, сепсисе и травмах повышается потребность в белках.

Усвоение белков зависит от: üкачества белков, которое определяется возможностью белка удовлетворить потребность организма в необходимых аминокислотах; üвозможности протеаз переваривать белок (непереваренные белки не усваиваются); üкалорийной ценности пищи. Если калорийность пищи низкая, больше белка используется в качестве источника энергии и поэтому потребность в нем выше.

Биологическая ценность белков Аминокислоты делятся на: Øнезаменимые (вал, лей, иле, тре, мет, фен, три, лиз); Øчастично заменимые (гис, арг); Øусловно заменимые (цис из мет, тир из фен); Øзаменимые (ала, асп, асн, глу, глн, про, гли, сер).

Протеолиз – процесс распада белков 1. Тотальный: üснижение иммуногенности белков; üреутилизация белков; üпополнение аминокислотного фонда клеток и крови. 2. Ограниченный: üделение клеток; üпроцессинг белков; üсистема свертывания и фибринолиза; üобразование активных гормонов; üактивирование ферментов ЖКТ.

Виды протеаз: Ø сериновые (р. Н – 7 -9): трипсин, химотрипсин, эластаза. Ø цистеиновые (р. Н 3 -7); Ø аспарагиновые (р. Н 2 -7): пепсин, Ø металлопротеиназы – Zn, Co, Ni: коллагеназы.

Свойства протеаз: Ø выделяются в неактивном состоянии – в виде предшественников и активируются другими ферментами или веществами; Ø субстратная специфичность: расщепляют пептидные связи, образованные определенными аминокислотами; Ø различаются по месту действия. - Эндопептидазы гидролизуют пептидные связи внутри белковой молекулы, - экзопептидазы отщепляют концевые аминокислоты (аминопептидазы – N-концевые, карбоксипептидазы – С-концевые).

Пищеварительный сок желудочный сок Ферменты Продукты НCl, р. Н=1, 5 -2, 5 пепсиноген → пепсин (асп, глу) белок большие пептиды гастриксин, р. Н = 3, 5; реннин поджелудочная железа свертывание молока химотрипсиноген → химотрипсин (фен, тир, три) трипсиноген → трипсин (арг, лиз) средние пептиды кишечный сок энтерокиназа пептидазы карбоксипептидазы А (нейтральные АК) и В (основные АК) проэластаза → эластаза (гли, ала, сер) аминокислоты

Ингибиторы протеолиза- как лекарственные препараты Примеры использования ингибиторов протеолиза в мед. практике: • Ингитрил, контрикал - получены из ткани легких • Пантрипин, гордокс - получены из ткани поджелудочной железы Используются для лечения воспалительных и некротических процессов (панкреатиты), нарушений свертывания и фибринолиза.
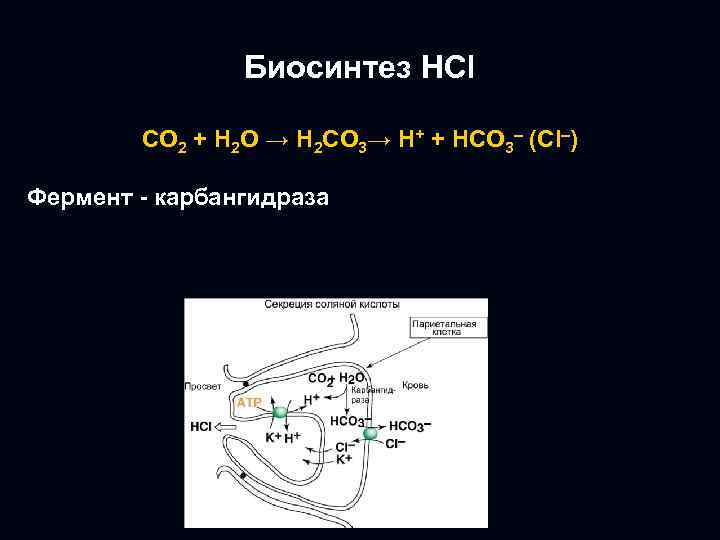
Биосинтез НСl СO 2 + H 2 O → H 2 CO 3→ H+ + HCO 3– (Cl–) Фермент - карбангидраза

Апикальную и базолатеральную мембраны энтероцитов аминокислоты проходят с помощью специальных систем переноса.

. Поступление аминокислот в клетки обеспечивается работой γ-глутамильного цикла. γ-Глутамил. Транс. Пептидаза глутатион (γ-Глу-Цис-Гли) + АК ------------------→ в клетке в крови Цис-Гли + γ-Глу-АК

Гниение белков - это превращения аминокислот под влиянием микроорганизмов в кишечнике. Тир → крезол, фенол; Три → скатол, индол; Орнитин → путресцин; Лиз → кадаверин; Многие из этих продуктов - вазоактивные вещества Конъюгирующие вещества: 1. УДФ-глюкуроновая кислота; 2. ФАФС (фосфоаденозинфосфосульфат).
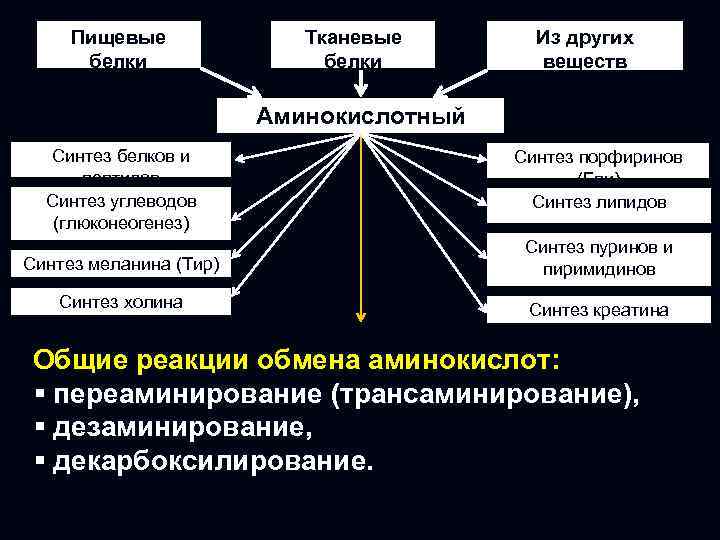
Пищевые белки Синтез белков и пептидов Синтез углеводов (глюконеогенез) Тканевые белки Аминокислотный фонд Из других веществ Синтез порфиринов (Гли) Синтез липидов Синтез меланина (Тир) Синтез пуринов и пиримидинов Синтез холина Синтез креатина Общие реакции обмена аминокислот: § переаминирование (трансаминирование), § дезаминирование, § декарбоксилирование.

Переаминирование – обратимая реакция переноса аминогруппы с аминокислоты на кетокислоту без промежуточного образования NH 3. ------------------------------------------------------------ NH 2 O O NH 2 ׀ ║ ║ ׀ R–CH–COOH + R 1–C–COOH ↔ R–C–COOH + R 1–CН–COOH ------------------------------------------ Ферменты – трансаминазы (аминотрансферазы). Кофермент – пиридоксальфосфат (Vit B 6).
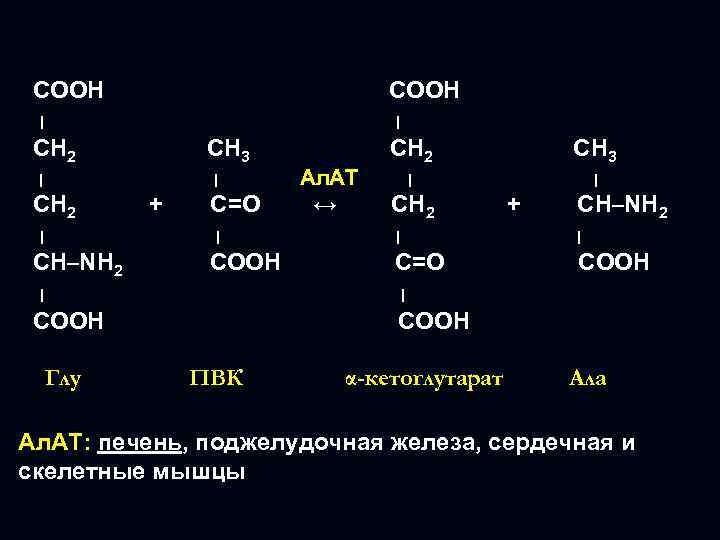
COOH ׀ ׀ CH 2 CH 3 ׀ ׀ CH 2 ׀ CH–NH 2 + C=O ↔ CH 3 ׀ ׀ CH 2 + CH–NH 2 ׀ ׀ ׀ COOH C=O COOH ׀ ׀ COOH Глу Ал. АТ CH 2 COOH ПВК α-кетоглутарат Ала Ал. АТ: печень, поджелудочная железа, сердечная и скелетные мышцы

COOH СOOH COOH ׀ ׀ СH 2 С=О СH 2 СН–NH 2 ׀ ׀ СH 2 ׀ СН–NH 2 + СH 2 ׀ СООН Ас. АТ ׀ ↔ СH 2 ׀ + ׀ С=О ׀ ׀ СООН ׀ COOH СH 2 COOH Глу ЩУК α-кетоглу Асп Ас. АТ: сердечная мышца, печень, скелетные мышцы, почки, поджелудочная железа

Диагностическое значение определения активности в крови: данные ферменты обладают органоспецифичтостью: Ал. АТ преобладает в печени, а Ас. АТ — в миокарде. При инфаркте миокарда, активность Ас. АТ в крови ↑ в 8 -10 раз, а Ал. АТ — в 1, 5 -2 раза, при гепатитах активность Ал. АТ в сыворотке крови ↑ в 8 -10 раз, а Ас. АТ — в 2 -4 раза. В клинической практике используют коэффициент де Ритиса — соотношение Ас. АТ/Ал. АТ, N=0, 91 -1, 75. При ↑ - инфаркт миокарда, при ↓ - гепатит.

Дезаминирование – превращение аминокислот с выделением NH 3. Виды дезаминирования: 1. Восстановительное дезаминирование 2. Гидролитическое дезаминирование 3. Внутримолекулярное дезаминирование 4. Окислительное дезаминирование R–СH– COOH + ½O 2 → R–С–COOH + NH 3 ׀ NH 2 ║ O

Окислительное ферменты – дезаминирование катализируют 1) дегидрогеназы (коферменты НАД+ или НАДФ+) 2) оксидазы (коферменты ФМН и ФАД). COOH ׀ ׀ CH 2 ׀ СООН ׀ CH 2 + НАД+ CH 2 ׀ ׀ ←----→ CH 2 – НАДН∙Н+ ׀ CH–NH 2 ׀ ׀ C=NH ׀ + H 2 O ↔ CH 2 + NH 3 COOH Глу COOH иминоглутарат C=O ׀ COOH α-кетоглутарат

Значение глутаматдегидрогеназной (ГДГ) реакции: Øобразование NH 3, Øфиксирование NH 3 в ходе обратной реакции – прямого (восстановительного) аминирования, Øобразуется α-кетоглутаровая кислота – связь с циклом Кребса, Øучастие ГДГ в реакциях непрямого дезаминирования.
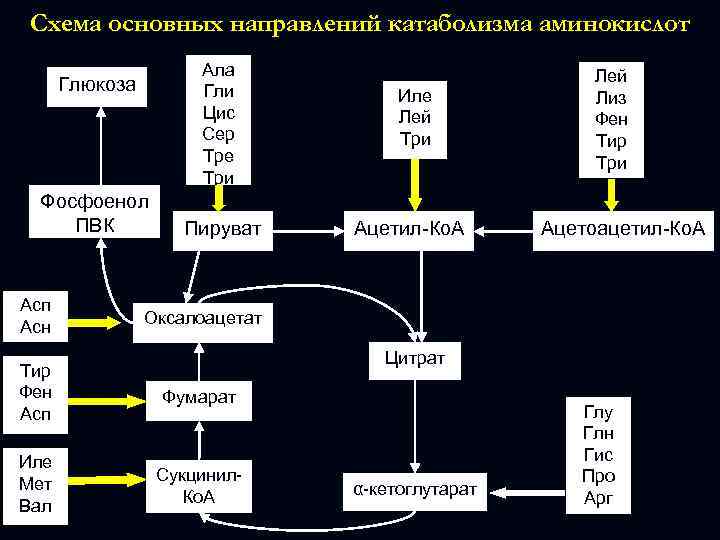
Схема основных направлений катаболизма аминокислот Ала Гли Цис Сер Тре Три Глюкоза Фосфоенол ПВК Асп Асн Пируват Иле Лей Три Ацетил-Ко. А Лей Лиз Фен Тир Три Ацетоацетил-Ко. А Оксалоацетат Цитрат Тир Фен Асп Фумарат Иле Мет Вал Сукцинил. Ко. А α-кетоглутарат Глу Глн Гис Про Арг

Кетогенными являются аминокислоты (АК), углеродные скелеты которых превращаются в ацетил. Ко. А или в ацетоацетил-Ко. А, из которых возможно образование кетоновых тел. Гликогенные АК Ала, Арг, Асп, Асн, Цис, Глу, Глн, Гли, Гис, Мет, Про, Сер, Тре, Вал Кетогенные АК Лей, Лиз Глико- и кетогенные АК Иле, Фен, Тир, Три

Реакции обезвреживания аммиака 1. Реакция прямого (восстановительного) аминирования. 2. Синтез Глн из Глу, Асн из Асп. COOH О=С─NH 2 COOH ׀ ׀ ׀ CH 2 CН 2 + АТФ ׀ CH 2 ׀ CH–NH 2 ׀ COOH Глу + NH 3 → – АДФ, Ф CH 2 ׀ ׀ CH 2 + H 2 O ׀ CН–NH 2 ׀ COOH Глутамин → CH 2 + ׀ C–NH 2 ׀ COOH Глу NH 3

3. Синтез мочевины в печени карбамоилфосфат- O OH синтетаза I (митох. ) ║ ׀ NH 3 + HCO 3 + 2 АТФ + H 2 O → NH 2–C–O~P=O + 2 АДФ + Фн N-ацетилглу ׀ биотин OH карбамоилфосфат
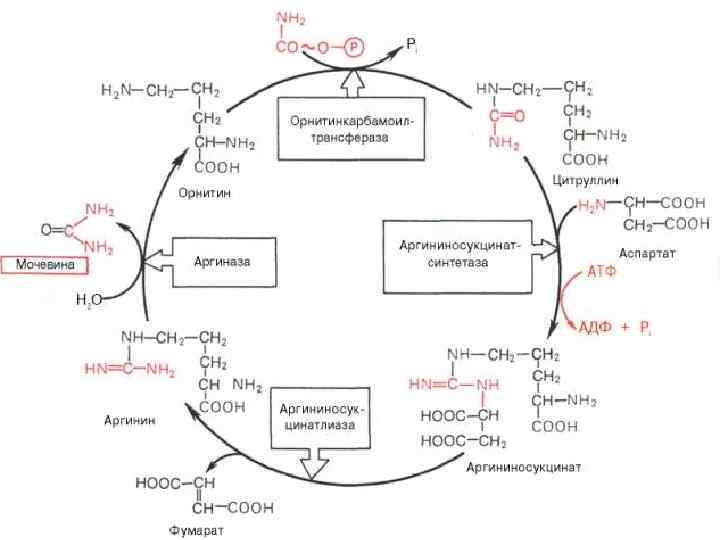

Мочевина в крови – 2, 5 -8, 3 ммоль/л. В сутки выделяется с мочой 25 -30 г. мочевины. Остаточный азот: мочевина – 50%, азот аминокислот – 25%; азот мелких фракций – 25% (креатин – 5%, креатинин – 2, 5%, мочевая кислота – 4% и др. ).

Декарбоксилирование аминокислот – превращение аминокислот с выделением СО 2 и образованием аминов (в случае ароматических аминокислот – биогенных аминов). Ферменты – декарбоксилазы. Кофермент – пиридоксальфосфат. R–СH– COOH → R–СH 2–NH 2 + СО 2 ׀ NH 2 декарбоксилаза – СО 2 5 -гидрокситриптофан серотонин

Серотонин вырабатывается слизистой ЖКТ, тучными клетками, тромбоцитами, ЦНС (медиатор). Индолуксусная кислота в моче – индикатор рака кишечника. Центральное действие серотонина: üрегуляция сна, памяти, научения, настроения, поведения, üрегуляция температуры тела, üрегуляция функций сердечно-сосудистой системы, ü↑ секрецию адреналина → гипергликемия. Периферическое действие серотонина: ü↑ перистальтику кишечника, ü↑ проницаемость мелких сосудов, ü↑ агрегацию тромбоцитов.

Гистамин содержат: легкие, желудок, сердце, тучные клетки, зернистые лейкоциты. Действие: ü↑ тонус гладкой мускулатуры, üрасширяет капилляры, ↓ АД, üстимулирует функцию пищеварительных желез, ü↑ секрецию желудочного сока, ü↑ отделение желчи, üчерез ЦНС контролирует сон и бодрствование, развитие воспаления и явления боли. декарбоксилаза –СО 2 гистидин гистамин

При ↑ концентрации гистамина в головном мозге происходит расширение сосудов, выход крови из них, ↑ внутричерепного давления, возникает головная боль. При ↑ концентрации гистамина в легких происходит ↑ сокращения гладких мышц и возникают приступы удушья.

Образование ГАМК NH 2 ׀ НООС–СH 2–СH–COOH → НООС–СH 2–СH 2 + СО 2 Глутаминовая кислота ГАМК (γ-аминомасляная)
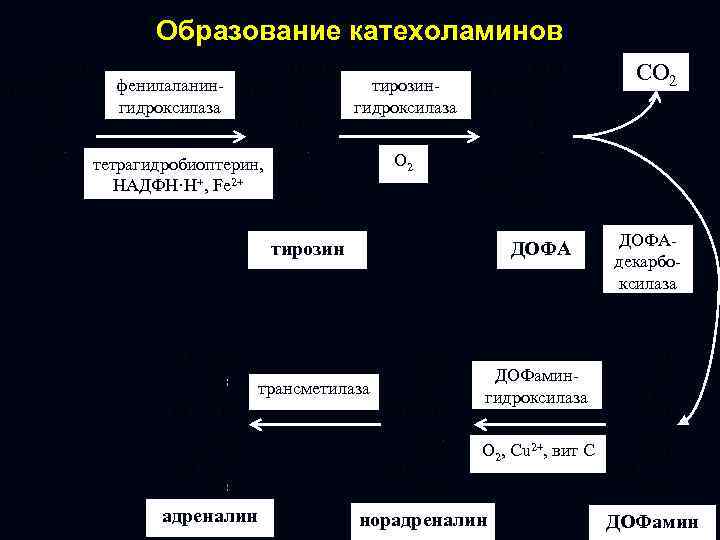
Образование катехоламинов фенилаланингидроксилаза СО 2 тирозингидроксилаза О 2 тетрагидробиоптерин, НАДФН·Н+, Fe 2+ тирозин ДОФА трансметилаза ДОФАдекарбоксилаза ДОФамингидроксилаза O 2, Cu 2+, вит С адреналин норадреналин ДОФамин

Действие катехоламинов: ü↑ потребление О 2 клетками, органами и организмом, ü↑ активность ферментов цикла Кребса, üстимулируют дыхательную цепь и синтез АТФ, ü↑ функцию головного мозга, сердца, легких, ü↑ АД. Это гормоны «трех Б» – борьбы, боязни, бегства. Погоня волка за зайцем. Гнев, ярость, агрессивность → высвобождение норадреналина (НА). Страх, уныние, депрессия → высвобождение адреналина (А). НА – «гормон волка» , А – «гормон зайца» . НА преобладает в надпочечниках у хищников, А – у травоядных.
Обмен белков и аминокислот-стомфак, фармфак.ppt