L5.ppt
- Количество слайдов: 47

БИОЛИГАНДЫ

Аминокислоты • Живые организмы содержат миллионы белков, которые, несмотря на исключительное многообразие свойств и функций, состоят всего из 20 типов строительных блоков аминокислот, и являются их линейными комбинациями. Ткани всегда находятся в состоянии или строительства, или разрушения, поэтому аминокислоты - одновременно строительный материал и обломки постоянно присутствуют в крови. Наиболее распространенными в живом мире аминокислоты показаны в табл. 1. Все они представляют собой α-аминокислоты, причем у подавляющего большинства из них аминогруппа - первичная; исключения составляют лишь пролин и оксипролин. В физиологическом диапазоне значений р. Н аминогруппа обычно бывает протонированная, карбоксигрупа ионизированная: Взаимодействовать с ионами металлов способны и амино- и карбоксильная группа, а также многие другие группы, которые встречаются в боковых цепях, например ОН в серине и тирозине, вторая группа СОО- в аспарагиновой и глутаминовой кислотах, SH в цистеине, -S-S- в цистине, вторая азотсодержащая группа в аргинине или гистидине. • Все аминокислоты, входящие в состав белков, за исключением глицина, не содержащего хиральных центров, оптически активные и имеют L-конфигурацию (т. е. такую же, как в левовращающего изомера L ( ) глицеринового альдегида). Направление и величина угла вращения зависит от строения боковой цепи и р. Н раствора. Интересно, что D аминокислоты также встречаются в природе, но не в белках, а в оболочках бактерий и в структурах многих антибиотиков, например в грамицидине S. Прочность связей в комплексах металлов с оптически активными лигандами не зависит от конфигурации хиральных центров в лигандах, если все лиганды относятся к одному ряду (только D или L ). С другой стороны, ферменты проявляют стереоспецифичнисть, так что обычно фермент, контролирующий превращение субстрата с L конфигурацией, не активен в отношении D формы (и наоборот).
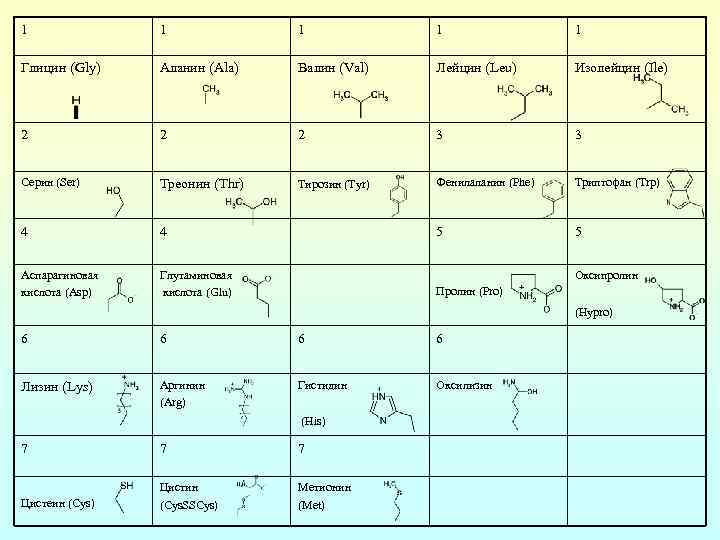
1 1 1 Глицин (Gly) Аланин (Ala) Валин (Val) Лейцин (Leu) Изолейцин (Ile) 2 2 2 3 3 Серин (Ser) Треонин (Thr) Тирозин (Tyr) Фенилаланин (Phe) Триптофан (Trp) 4 4 5 5 Аспарагиновая кислота (Asp) Глутаминовая кислота (Glu) Оксипролин Пролин (Pro) (Hypro) 6 6 Лизин (Lys) Аргинин (Arg) Гистидин Оксилизин (His) 7 7 7 Цистеин (Cys) Цистин (Cys. SSCys) Метионин (Met)

Поскольку в биполярных формах аминокислот заряды разделены, для соединений этого класса характерна хорошая растворимость в воде и очень плохая - в органических растворителях. По этой же причине они имеют высокие температуры плавления. Для всех аминокислот характерны реакции по амино- и карбоксильной группам, а также хелатирования, при котором обе группы образуют связи с одним атомом металла: • Различия в природных аминокислотах обусловлены природой боковой цепи R. Некоторые аминокислоты, имеющие в боковой цепи электроннодонорну группу (как гистидин), способны играть роль тридендатного лиганда по отношению к иону металла. Существенны также размеры и форма боковой цепи, они определяют пространственные эффекты в процессе хелатирования и существенно влияют на форму пептидных цепей (так, пролин в ряде случаев находится в местах изгиба цепей). • Наличие в пище всех вышеперечисленных аминокислот не является обязательным. В результате процессов, протекающих с участием белковых катализаторов, организм человека способен синтезировать одни аминокислоты из других, за исключением десяти незаменимых: аргинина, гистидина, изолейцина, лизина, метионина, фенилаланина, треонина, триптофана и валина. Молоко представляет собой прекрасный сбалансированный источник всех незаменимых аминокислот: все десять входят в состав одного из его белков, лактоальбумина. • В печени происходит распад аминокислот, причем образуется мочевина NH 2 CONH 2, которая переносится кровью в почки и затем выводится из организма.
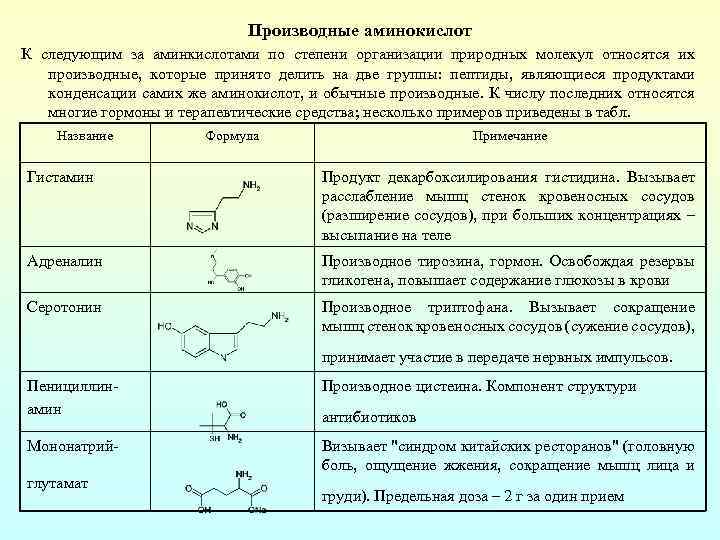
Производные аминокислот К следующим за аминкислотами по степени организации природных молекул относятся их производные, которые принято делить на две группы: пептиды, являющиеся продуктами конденсации самих же аминокислот, и обычные производные. К числу последних относятся многие гормоны и терапевтические средства; несколько примеров приведены в табл. Название Формула Примечание Гистамин Продукт декарбоксилирования гистидина. Вызывает расслабление мышц стенок кровеносных сосудов (разширение сосудов), при больших концентрациях – высыпание на теле Адреналин Производное тирозина, гормон. Освобождая резервы гликогена, повышает содержание глюкозы в крови Серотонин Производное триптофана. Вызывает сокращение мышц стенок кровеносных сосудов (сужение сосудов), принимает участие в передаче нервных импульсов. Пенициллин амин Производное цистеина. Компонент структури Мононатрий Визывает "синдром китайских ресторанов" (головную боль, ощущение жжения, сокращение мышц лица и глутамат антибиотиков груди). Предельная доза – 2 г за один прием
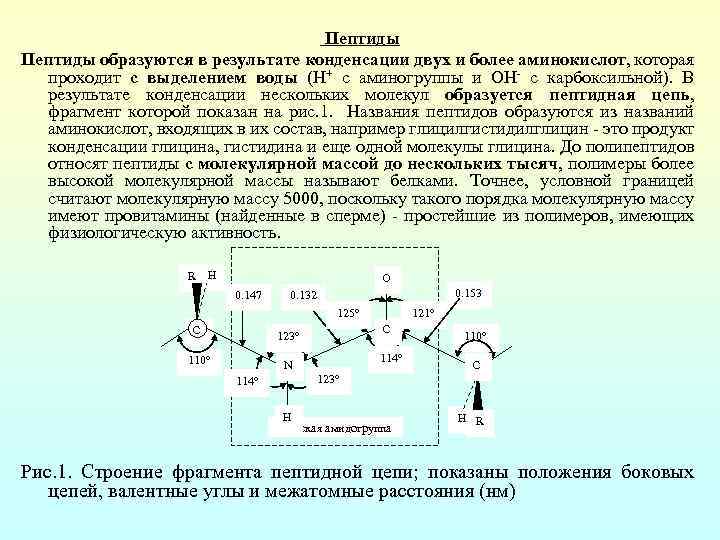
Пептиды образуются в результате конденсации двух и более аминокислот, которая проходит с выделением воды (Н+ с аминогруппы и ОН с карбоксильной). В результате конденсации нескольких молекул образуется пептидная цепь, фрагмент которой показан на рис. 1. Названия пептидов образуются из названий аминокислот, входящих в их состав, например глицилгистидилглицин это продукт конденсации глицина, гистидина и еще одной молекулы глицина. До полипептидов относят пептиды с молекулярной массой до нескольких тысяч, полимеры более высокой молекулярной массы называют белками. Точнее, условной границей считают молекулярную массу 5000, поскольку такого порядка молекулярную массу имеют провитамины (найденные в сперме) простейшие из полимеров, имеющих физиологическую активность. R H О 0. 147 0. 153 0. 132 125° C C 123° 110° N 114° 121° 114° 110° C 123° Н Плоская амидогруппа H R Рис. 1. Строение фрагмента пептидной цепи; показаны положения боковых цепей, валентные углы и межатомные расстояния (нм)
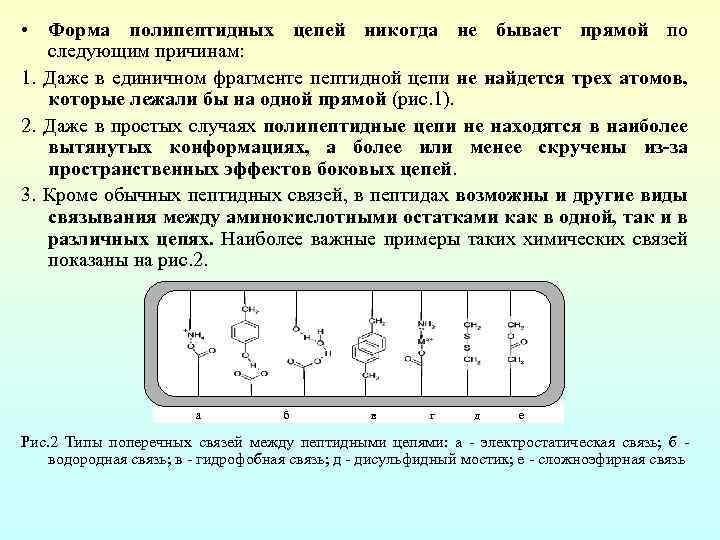
• Форма полипептидных цепей никогда не бывает прямой по следующим причинам: 1. Даже в единичном фрагменте пептидной цепи не найдется трех атомов, которые лежали бы на одной прямой (рис. 1). 2. Даже в простых случаях полипептидные цепи не находятся в наиболее вытянутых конформациях, а более или менее скручены из-за пространственных эффектов боковых цепей. 3. Кроме обычных пептидных связей, в пептидах возможны и другие виды связывания между аминокислотными остатками как в одной, так и в различных цепях. Наиболее важные примеры таких химических связей показаны на рис. 2. а б в г д е Рис. 2 Типы поперечных связей между пептидными цепями: а электростатическая связь; б водородная связь; в гидрофобная связь; д дисульфидный мостик; е сложноэфирная связь

• В пептидах донорами электронной пары по отношению к протону или иону металла могут быть (наряду с группами, упомянутыми в случае аминокислот) атом азота в пептидной (амидной) связи и дисульфидный мостик. Скрученность полипептидных цепей вызывает достаточно большую вероятность ситуаций, когда сразу несколько электронодонорных групп оказываются весьма близкими к иону металла, чтобы образовать с ним комплекс. • Даже небольшие изменения в строении пептидов существенно влияют на их функции. • Так, структура инсулина гормона, необходимого для регулирования обмена глюкозы, у человека и лошади отличаются на одну аминокислоту (серин и глицин, соответственно). • Далее, ошибочная мутация, которая заключается в замене всего лишь одной аминокислоты (глутаминовой кислоты на валин) в гемоглобине А, приводит к тяжелому генетическому заболеванию серповидноклеточной анемии.

Белки по их функциям можно разделить на две большие группы. К первой относятся "рабочие" белки, непосредственно занятые в процессе обмена (переноса, усвоения и т. д. ). Их работу контролируют системы нуклеиновых кислот, передают соответствующую информацию. Во вторую входят ферменты - биокатализаторы, что имеют белковую природу. Их молекулярные массы лежат в широком диапазоне, от 5000 до многих миллионов. В функцию ферментов как катализаторов входит способность регенерировать себя после рабочего цикла. Способностью к автогенерации обладают и многие другие типы белков. Она обусловлена высокой организацией белковых молекул, которая проявляется на четырех уровнях: 1. Первичная структура последовательность аминокислотных остатков в пептидной цепи, которая, конечно, меняется от одного белка к другому. 2. Вторичная структура пространственная конфигурация пептидной цепи. Как мы уже упоминали, наиболее крутые изгибы в таком цепи приходятся на остаток пролина, кроме того, сильное скручивание цепи может фиксироваться образованием дополнительных перекрестных связей между его фрагментами (см. рис. 2).

3. Третичная структура форма, которую принимают несколько взаимодействующих цепей, обвиваясь вокруг друга или образуя складки. Совокупность двух, трех или четырех цепей определяет и форму молекулы в целом, например нитевидную в фибриллярных белков или компактную в глобулярных белков, таких, как гемоглобин. Нужно указать, что не все реакционные группы боковых цепей белков занимают положение, подходящие для образования поперечных связей в середине пептидных цепей или между ними или для координации с ионом металла. Действительно, много таких групп внутри белковой части экранированы соседними цепями. Реакционную способность сохраняют только те аминокислотные остатки, которые образуют внешнюю поверхность молекулы, и, возможно, также те, которые выстилают ее внутренние полости. Тем не менее большинство боковых цепей участвует в создании подходящего электростатического окружения для проявления ферментативной активности. Очевидно, молекулы водорастворимых белков должны иметь обращенными наружу гидрофильные группы, например ОН- и СОО-. 4. Четвертичная структура объединение нескольких крупных молекул, приводящее к характерным, часто видимым образованиям; например, сочетание кератинов дает волос.
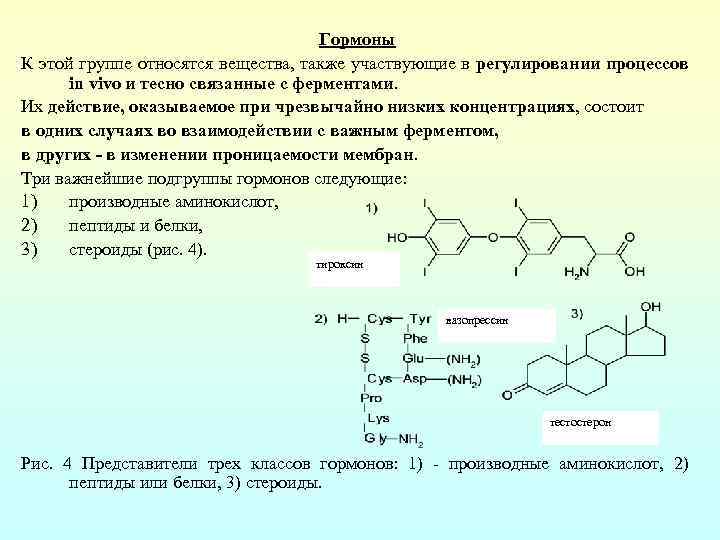
Гормоны К этой группе относятся вещества, также участвующие в регулировании процессов in vivo и тесно связанные с ферментами. Их действие, оказываемое при чрезвычайно низких концентрациях, состоит в одних случаях во взаимодействии с важным ферментом, в других - в изменении проницаемости мембран. Три важнейшие подгруппы гормонов следующие: 1) производные аминокислот, 2) пептиды и белки, 3) стероиды (рис. 4). тироксин вазопрессин тестостерон Рис. 4 Представители трех классов гормонов: 1) производные аминокислот, 2) пептиды или белки, 3) стероиды.

Белки крови Кровь богата белками. Кроме ферментов и гормонов, она содержит альбумины, на которые приходится больше половины белков крови и глобулины. Как уже упоминалось, состав крови достаточно стабилен. Благодаря альбуминам поддерживаются постоянными осмотическое давление и р. Н 7. 4. Функции глобулинов, которые нерастворимые в воде, но растворимы в разбавленных растворах солей, связанные с процессами переноса. α- и -Глобулины, образующиеся в печени, участвуют в переносе веществ и в свертывании крови. -Глобулины играют важную роль в появлении иммунитета: они образуют антитела, связывающие в комплексы вещества, чуждые организму.
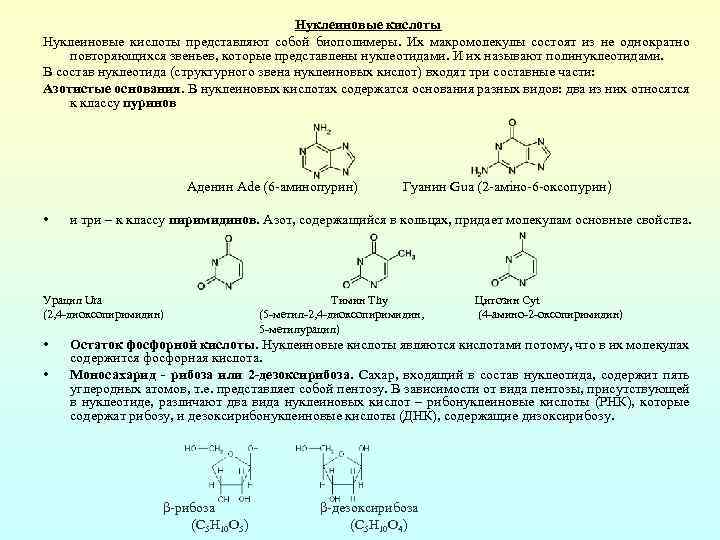
Нуклеиновые кислоты представляют собой биополимеры. Их макромолекулы состоят из не однократно повторяющихся звеньев, которые представлены нуклеотидами. И их называют полинуклеотидами. В состав нуклеотида (структурного звена нуклеиновых кислот) входят три составные части: Азотистые основания. В нуклеиновых кислотах содержатся основания разных видов: два из них относятся к классу пуринов Аденин Ade (6 аминопурин) • и три – к классу пиримидинов. Азот, содержащийся в кольцах, придает молекулам основные свойства. Урацил Ura (2, 4 диоксопиримидин) • • Гуанин Gua (2 аміно 6 оксопурин) Тимин Thy (5 метил 2, 4 диоксопиримидин, 5 метилурацил) Цитозин Cyt (4 амино 2 оксопиримидин) Остаток фосфорной кислоты. Нуклеиновые кислоты являются кислотами потому, что в их молекулах содержится фосфорная кислота. Моносахарид - рибоза или 2 -дезоксирибоза. Сахар, входящий в состав нуклеотида, содержит пять углеродных атомов, т. е. представляет собой пентозу. В зависимости от вида пентозы, присутствующей в нуклеотиде, различают два вида нуклеиновых кислот – рибонуклеиновые кислоты (РНК), которые содержат рибозу, и дезоксирибонуклеиновые кислоты (ДНК), содержащие дизоксирибозу. β рибоза β дезоксирибоза (C 5 H 10 O 5) (C 5 H 10 O 4)
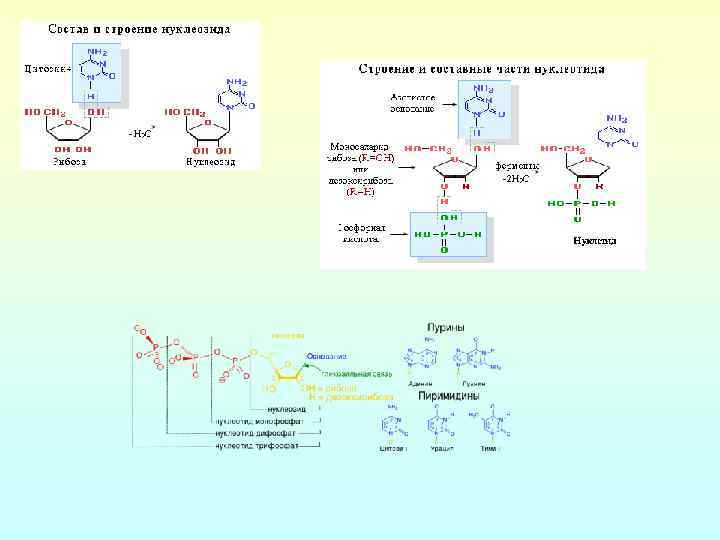
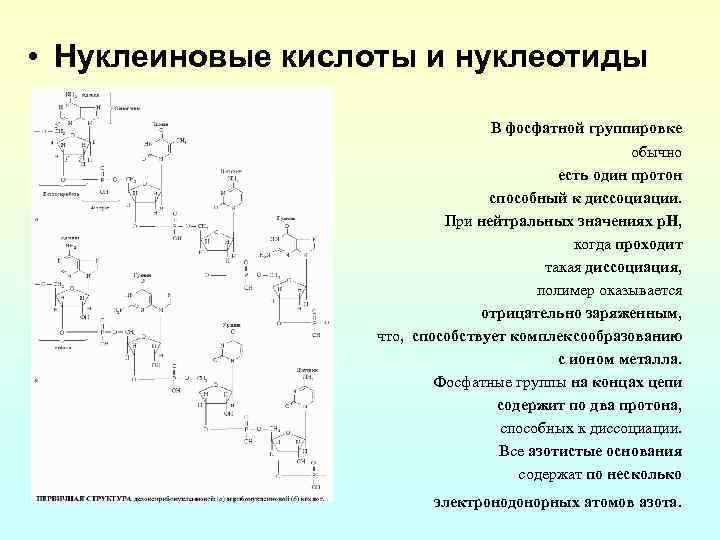
• Нуклеиновые кислоты и нуклеотиды В фосфатной группировке обычно есть один протон способный к диссоциации. При нейтральных значениях р. Н, когда проходит такая диссоциация, полимер оказывается отрицательно заряженным, что, способствует комплексообразованию с ионом металла. Фосфатные группы на концах цепи содержит по два протона, способных к диссоциации. Все азотистые основания содержат по несколько электронодонорных атомов азота.

Нуклеопротеиды (молекулярный вес 108 и выше) представляют собой комплексы белков и нуклеиновых кислот и необходимы для репродуцирования организмов, в том числе передачи наследственных признаков. В зависимости от типа нуклеиновой кислоты (РНК или ДНК), входящей в состав нуклеопротеида, нуклеопротеиды делятся на РНП и ДНП содержатся главным образом в ядрах, а РНП – в цитоплазме клеток. ДНК несет в себе необходимую генетическую информацию, а РНК при встрече с ДНК запоминает ее и на ее основе управляет синтезом пептидов из аминокислот. И в данном случае для нормального течения процесса необходимо полное соответствие между нуклеопротеидом и пептидом. Нуклеиновые кислоты склонны принимать отрицательный заряд, а белки – положительный, таким образование нуклеопротеидов обусловлено в основном электростатическими взаимодействиями.
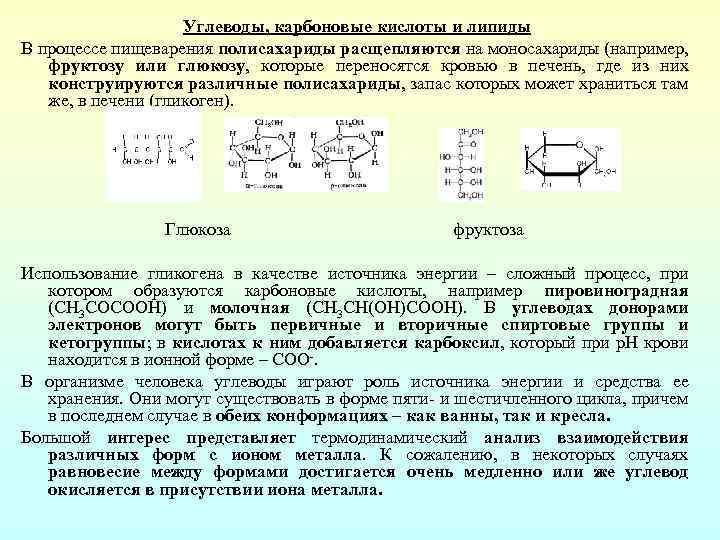
Углеводы, карбоновые кислоты и липиды В процессе пищеварения полисахариды расщепляются на моносахариды (например, фруктозу или глюкозу, которые переносятся кровью в печень, где из них конструируются различные полисахариды, запас которых может храниться там же, в печени (гликоген). Глюкоза фруктоза Использование гликогена в качестве источника энергии – сложный процесс, при котором образуются карбоновые кислоты, например пировиноградная (СН 3 СОСООН) и молочная (СН 3 СН(ОН)СООН). В углеводах донорами электронов могут быть первичные и вторичные спиртовые группы и кетогруппы; в кислотах к ним добавляется карбоксил, который при р. Н крови находится в ионной форме – СОО. В организме человека углеводы играют роль источника энергии и средства ее хранения. Они могут существовать в форме пяти и шестичленного цикла, причем в последнем случае в обеих конформациях – как ванны, так и кресла. Большой интерес представляет термодинамический анализ взаимодействия различных форм с ионом металла. К сожалению, в некоторых случаях равновесие между формами достигается очень медленно или же углевод окисляется в присутствии иона металла.

Липиды Липидами называют различные вещества растительного и животного происхождения, объединяемые всего одним признаком – все они нерастворимы в воде. • Триглицериды (жиры) и жирные кислоты. Жиры – это сложные эфиры глицерина (в зависимости от числа этерифицированных гидроксильных групп различают моно, ди и триглицериды) с монокарбоновыми кислотами, имеющими неразветвленную углеродную цепь, которые называют жирные кислоты. R, R’ и R” – насыщенные или ненасыщенные углеводородные остатки с линейной углеродной цепью и нечетным числом атомов углерода. Растворимость жирных кислот понижается с увеличением длин углеродных цепи и повышается с ростом числа двойных связей в ней. • В организме жиры используют как топливо и как запас питания.
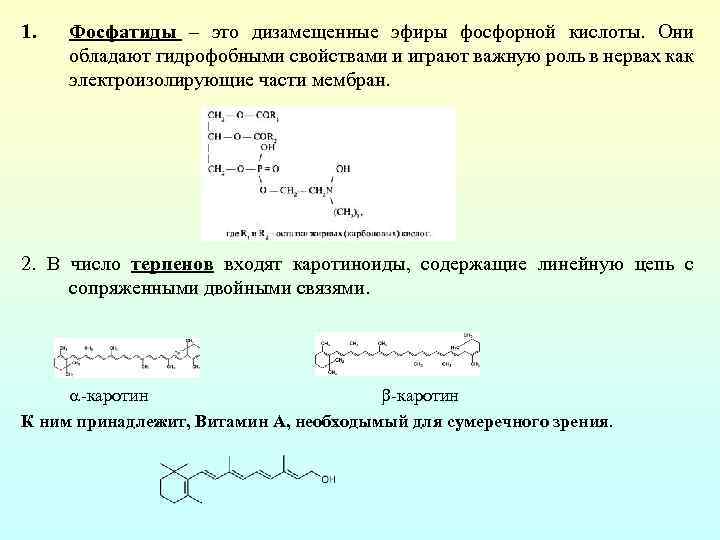
1. Фосфатиды – это дизамещенные эфиры фосфорной кислоты. Они обладают гидрофобными свойствами и играют важную роль в нервах как электроизолирующие части мембран. 2. В число терпенов входят каротиноиды, содержащие линейную цепь с сопряженными двойными связями. каротин К ним принадлежит, Витамин А, необходымый для сумеречного зрения.
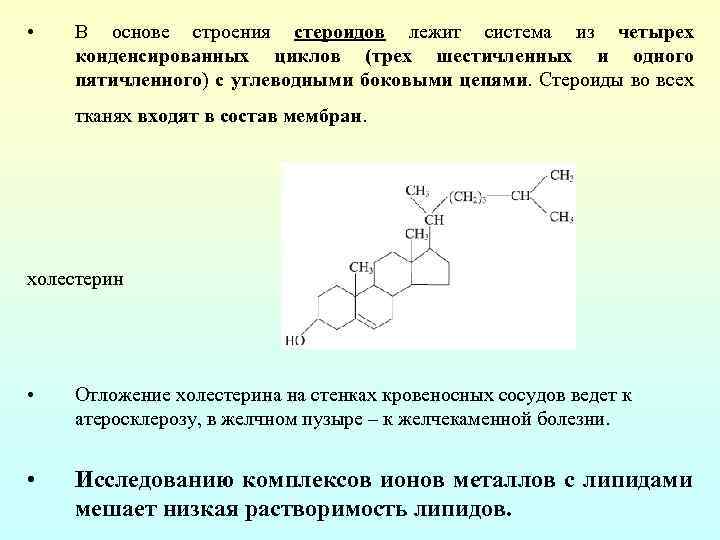
• В основе строения стероидов лежит система из четырех конденсированных циклов (трех шестичленных и одного пятичленного) с углеводными боковыми цепями. Стероиды во всех тканях входят в состав мембран. холестерин • Отложение холестерина на стенках кровеносных сосудов ведет к атеросклерозу, в желчном пузыре – к желчекаменной болезни. • Исследованию комплексов ионов металлов с липидами мешает низкая растворимость липидов.

Ферменты • Каталитические свойства ферментов локализованы в их активных центрах, которые образованы относительно небольшим числом аминокислотных остатков. Роль остальной части молекулы заключается в удерживании этих активных центров в необходимом пространственном расположении и в создании соответствующего электростатического окружения. • В ходе реакций ферменты образуют промежуточные комплексы, часто с участием катионов металлов. Последние могут быть связаны или крепко, образуя неотъемлемую часть активного центра, или слабо, равновесно координируясь в нем. Ферменты очень специфичны по отношению и к субстрату, и к иону металла. • Фермент, подготовленный к выполнению своих каталитических функций, можно рассматривать как резервуар свободной энергии. Очевидно, было бы трудновато сохранять такое состояние активных центров в те периоды, когда фермент не работает. Поэтому во многих случаях фермент бывает заблокирован ингибитором, который обычно представляет собой небольшую полипептидную молекулу, располагающуюся у активного центра. Аддукт ингибитора с ферментом называют предшественником фермента (проферментом или зимогеном); после удаления ингибитора фермент оказывается подготовленным к приему субстрата.

• Некоторые зимогены не работают без активатора; например, в желудке соляная кислота служит активатором для пепсиногена. Но некоторым ферментам (называемым апоферментами) такой подготовки недостаточно для перехода в рабочее состояние, им нужен еще один активатор, что называется коферментом (часто это витамин). Например, пероксидаза, состоит из гематина C 34 H 32 O 4 N 4 Fe(III)OH (низкомолекулярного фермента, содержащего Феррум), и апофермента (белковой частицы составляющей основную часть фермента). • Кроме того, конечно, существуют антиферменты, т. е. вещества, подавляющие активность фермента, если это становится необходимым, их действие заключается в дезактивации активных центров. Например, клетки стенок желудка и кишок содержат антиферменты, защищающие эти стенки от ферментов пищеварения. • Но главное: высокая каталитическая активность фермента обусловлена полным соответствием между субстратами и активными центрами. При измерении р. Н, когда возможна ионизация протонов из активных центров, или нагревании, приводящем к изменению формы последних такое соответствие нарушается и фермент теряет активность. Если потеря необратима, говорят что произошло денатурирование белка.

Простые анионы Вода связанная в комплексе, легко теряет протон в щелочной среде, причем образуется комплекс, содержащий гидроксид ион в качестве лиганда [M(H 2 O)x]2++OH [M(H 2 O)x 1 OH]++H 2 O Чем выше р. Н, тем легче отдает протон связанная в комплексе молекула воды. При низких значениях р. Н действует другой механизм образования гидроксокомплексов – прямое замещение воды на гидроксид ион. • Считают, что при р. Н крови (7. 4) действуют оба механизма. Таблица 2. Произведения растворимости и приблизительные значения р. Н, при которых начинается осаждение гидроксидов метал лов из раствора (с=10 м. М) Ион металла Mg(II) Ca(II) Mn(II) Fe(III) Co(II) Cu(II) Zn(II) ПР 3. 1 10 11 1. 3 10 6 2. 0 10 13 1. 8 10 15 6. 0 10 38 2. 5 10 16 2. 0 10 19 1. 0 10 17 р. Н начала осаждения 10 12 9 2 8 6 6 Если изменить концентрации ионов и состав раствора (например, от воды перейти к крови), порядок осаждения не измениться. Очевидно, для того чтобы ионы Cu(II) и Zn(II) не выпали в виде гидроксидов из крови они должны быть прочно закомплексованы или присутствовать лишь в очень малых концентрациях.

Другие анионные лиганды, найденные in vivo – это • CO 32 ; HCO 3 ; PO 43 ; HPO 42 ; H 2 PO 4 ; SO 42 ; F ; Cl ; Br ; I. • Фосфат и сульфат ионы преобладают среди анионов внутри клеток, тогда как хлорид-ион – в межклетожных жидкостях. Все эти анионы так же необходимы для организма человека, как и катионы. • Хлорид и иодид натрия входят в пищу. Хлорид необходим для образования соляной кислоты в желудке, иодид – для образования тиреоглобулина Недостаток иода в пище приводит к гипотериозу или зобной болезни. • Бромиды натрия, калия и аммония обладают успокаивающим действием. • Фторид необходим для правильного роста костей и зубов; его недостаток в организме ведет к кариесу зубов (чрезмерные дозы вызывают дерматит). Оптимальная концентрация фторида в питьевой воде составляет 10 4 %. Некоторые продукты питания и напитки содержат гораздо больше фторид иона: например, рыбные консервы 12 10 4 %, чай 5 10 4 %. • Карбонат и фосфат ионы используются организмом как буферирующие анионы; их источник – метаболизм углеводов и нуклеиновых кислот. Скорость отложения фосфата в скелете зависит от концентраций Са 2+ и витамина D. Ca 3(PO 4)2 является важной составной частью костей. Фосфаты необходимы также для метаболизма углеводов и для системы хранения гликогена.

Витамины – физиологически активные вещества, которые входят в состав ферментов и играют важную роль в обмене веществ. Они синтезируются в растениях и поступают в организм животных и человека с пищей. • Некоторые витамины склонны к комплексообразованию с металлами, так как содержат донорные атомы азота, серы, кислорода. Примеры витаминов • жирорастворимые витамины • К ним относятся витамины А, D, Е, К и некоторые другие с общими свойствами: 1) имеют несколько аналогов с близкой структурой и аналогичной биологическим действием. Так, у витаминов А и К обнаружено по два аналога; 2) организм способен усваивать их только в присутствии жира и желчи; 3) обладают способностью накапливаться в организме человека при введении их в больших количествах; 4) механизм действия этих витаминов полностью не изучен, известны лишь процессы, на которые они влияют.

Витамин А. распространенной формой является витамин А 1: • • Он легко окисляется под действием кислорода. Термостабильный при отсутствии кислорода. С пальмитиновой кислотой образует эфиры и накапливается в печени. способствует росту и развитию организма, участвует в образовании зрительного пигмента и обеспечивает нормальное зрение, повышает устойчивость организма к инфекциям, некоторым ядам и токсинам, поддерживает функции эпителия кожных покровов и слизистых оболочек. При недостатке количества витамина А развивается болезнь «куриная слепота» , поражается роговица глаза, замедляется рост. В организме человека витамин А не синтезируется. Предшественником витамина А (провитамином А) является растительный пигмент каротин. Потребность в витамине А - 1, 5 мг/сут. Витамином А богаты продукты животного происхождения - сливочное масло, печень морских животных и рыб. Растительные продукты (морковь, перец, томаты) богаты провитамином А (каротин), который в организме легко превращается в витамин А.

Витамин D • образуется в организме под воздействием ультрафиолетовых лучей. • По своей химической природе различные формы витамина D являются производными стеринов: • При отсутствии в пище витамина D у детей развивается рахит, нарушается фосфорно кальциевый обмен, деформируются кости. • Витамин D содержится в рыбьем жире, сливочном масле, желтке яйца, молоке, печени.

• • Витамин Е существует в виде α, и токоферолов, которые отличаются между собой положениями метильных групп в ароматическом ядре. Вместе с витамином А выполняет роль антиоксиданта. Также участвует в окислительном фосфорилировании. Токоферолы принимают участие в обмене белка. Достаточный уровень токоферолов способствует развитию мышц и нормализует мышечную деятельность, предотвращая развитие мышечной слабости и утомления. Эта способность используется в спортивной медицине как средство нормализации мышечной деятельности в период "ударных" тренировок. Способствует нормальному протеканию беременности и развитию плода, а также активно участвует в процессе образовании спермы. Суточная потребность 12 -15 мг. Применяется, главным образом, при некоторых заболеваниях сетчатки глаз, мышечной ди строфии и токсикозах беременных. При отсутствии витамина Е нарушаются функции половых органов, развивается мышечная дистрофия, паралич конечностей. Источниками витамина Е являются растительные жиры, капуста, пророщенное зерно злаков.
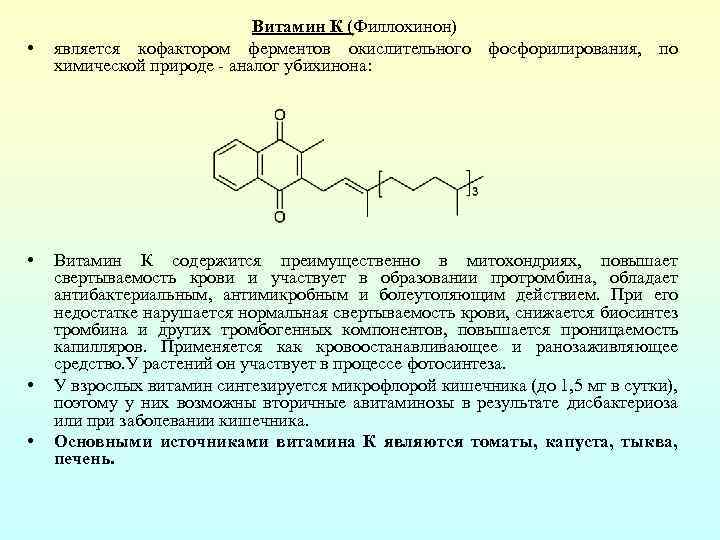
• • Витамин К (Филлохинон) является кофактором ферментов окислительного фосфорилирования, по химической природе аналог убихинона: Витамин К содержится преимущественно в митохондриях, повышает свертываемость крови и участвует в образовании протромбина, обладает антибактериальным, антимикробным и болеутоляющим действием. При его недостатке нарушается нормальная свертываемость крови, снижается биосинтез тромбина и других тромбогенных компонентов, повышается проницаемость капилляров. Применяется как кровоостанавливающее и ранозаживляющее средство. У растений он участвует в процессе фотосинтеза. У взрослых витамин синтезируется микрофлорой кишечника (до 1, 5 мг в сутки), поэтому у них возможны вторичные авитаминозы в результате дисбактериоза или при заболевании кишечника. Основными источниками витамина К являются томаты, капуста, тыква, печень.
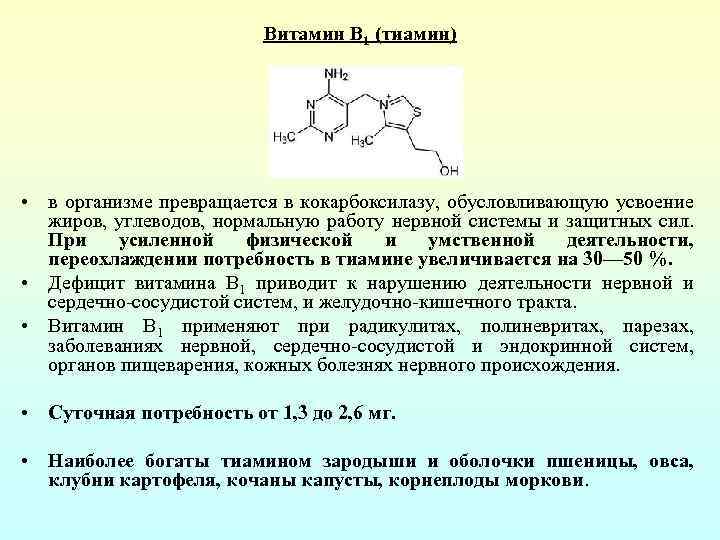
Витамин В 1 (тиамин) • в организме превращается в кокарбоксилазу, обусловливающую усвоение жиров, углеводов, нормальную работу нервной системы и защитных сил. При усиленной физической и умственной деятельности, переохлаждении потребность в тиамине увеличивается на 30— 50 %. • Дефицит витамина B 1 приводит к нарушению деятельности нервной и сердечно сосудистой систем, и желудочно кишечного тракта. • Витамин B 1 применяют при радикулитах, полиневритах, парезах, заболеваниях нервной, сердечно сосудистой и эндокринной систем, органов пищеварения, кожных болезнях нервного происхождения. • Суточная потребность от 1, 3 до 2, 6 мг. • Наиболее богаты тиамином зародыши и оболочки пшеницы, овса, клубни картофеля, кочаны капусты, корнеплоды моркови.
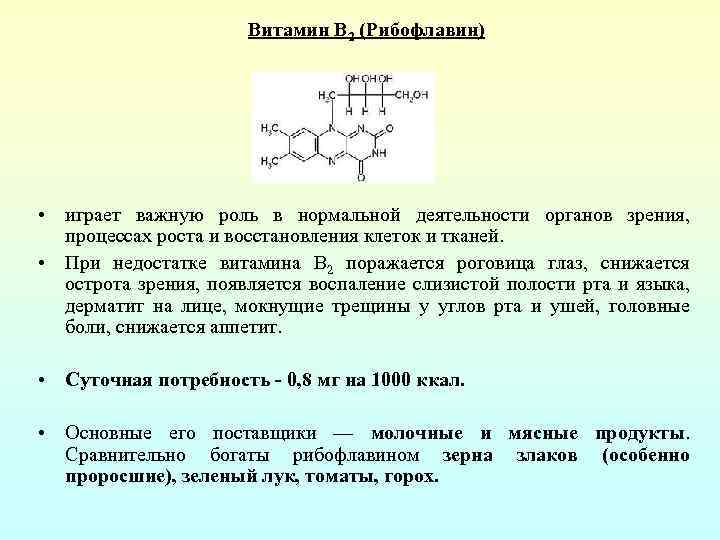
Витамин В 2 (Рибофлавин) • играет важную роль в нормальной деятельности органов зрения, процессах роста и восстановления клеток и тканей. • При недостатке витамина В 2 поражается роговица глаз, снижается острота зрения, появляется воспаление слизистой полости рта и языка, дерматит на лице, мокнущие трещины у углов рта и ушей, головные боли, снижается аппетит. • Суточная потребность - 0, 8 мг на 1000 ккал. • Основные его поставщики — молочные и мясные продукты. Сравнительно богаты рибофлавином зерна злаков (особенно проросшие), зеленый лук, томаты, горох.

Витамин В 3 (пантотеновая кислота) CH 2 OH-C(CH 3)2 -CHOH-CO-NH-CH 2 -COOH усиливает процессы регенерации, участвует в белковом и водном обмене. • Потребность 5 -10 мг в сутки, помимо того, что синтезируется микрофлорой кишечника. • Применяется при ряде нервных заболеваний, местно —при хронических язвах и ожогах. • Относительно много ее в горохе, спарже, ячмене, пшенице, ржи.

Витамин В 6 (Пиридоксин) входит в состав ферментов, влияющих на белковый обмен и участвующих в синтезе и расщеплении аминокислот. Необходим для нормального кроветворения, усвоения жиров, функционирования нервной системы. • Недостаток витамина B 6 ведет к нарушению обмена железа, развитию гипохромной анемии, отеков, дерматозов, дистрофических изменений в клетках различных органов, изменений со стороны нервной системы, нередко сопровождающихся судорогами. • Пиридоксин назначают при бессоннице, хорее, дрожательном параличе, ряде заболеваний периферической нервной системы, гепатитах, пеллагре (в сочетании с никотиновой кислотой), токсикозе беременных и т. д. • Потребность в сутки - 1, 5 -3 мг. Повышенная потребность в нем у беременных, а также у пожилых людей. • Пиридоксин содержат неочищенные зерна злаковых культур, стручки гороха, фасоли, клубни картофеля, овощи.

Витамин РР (Никотиновая кислота) • улучшает углеводный обмен, участвует в тканевом дыхании, оказывает сосудорасширяющее действие, положительно влияет на гемодинамику (циркуляцию крови), нормализует секреторную и моторную функцию желудка (лицам с расстройством желудочной секреции и атонией желудка на заметку), улучшает секрецию и состав сока поджелудочной железы (диабетикам на заметку), нормализует функцию печени, ее антитоксическую функцию. • При ее недостатке поражаются кожные покровы, развивается пеллагра, характеризуемая дерматитом, диареей, деменцией (синдром поражения центральной нервной системы). • Никотиновую кислоту назначают при атеросклерозе, болезнях печени, энтероколитах, отравлении сульфаниламидными препаратами, некоторых формах психоза. • Потребность - 6, 6 мг на 1000 ккал пищи. • Содержится в овощах, фруктах, бобовых, злаках, грибах.
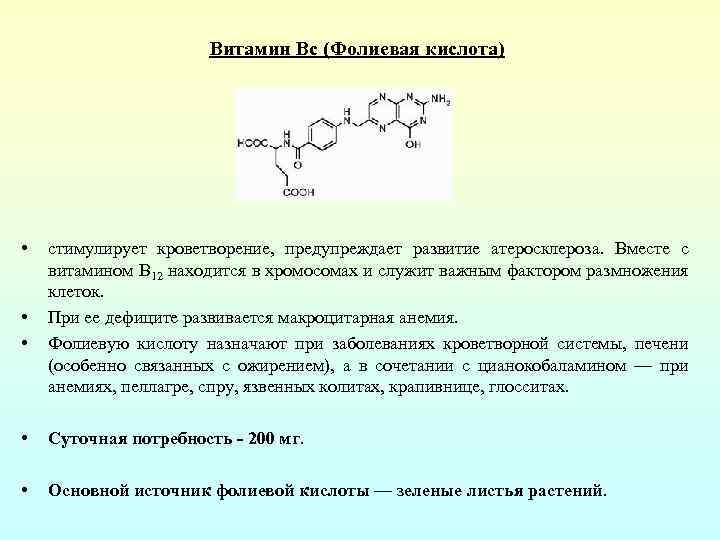
Витамин Вс (Фолиевая кислота) • • • стимулирует кроветворение, предупреждает развитие атеросклероза. Вместе с витамином В 12 находится в хромосомах и служит важным фактором размножения клеток. При ее дефиците развивается макроцитарная анемия. Фолиевую кислоту назначают при заболеваниях кроветворной системы, печени (особенно связанных с ожирением), а в сочетании с цианокобаламином — при анемиях, пеллагре, спру, язвенных колитах, крапивнице, глосситах. • Суточная потребность - 200 мг. • Основной источник фолиевой кислоты — зеленые листья растений.

Витамин Н (Биотин) • нужен для обмена жирных кислот и переноса в организме углекислого газа. • При его недостатке наступает быстрая утомляемость, мышечные боли, исчезает аппетит. • Потребность - 0, 15 - 0, 3 мг. • Обнаружен в сое и горохе, овсяной крупе и яйцах.
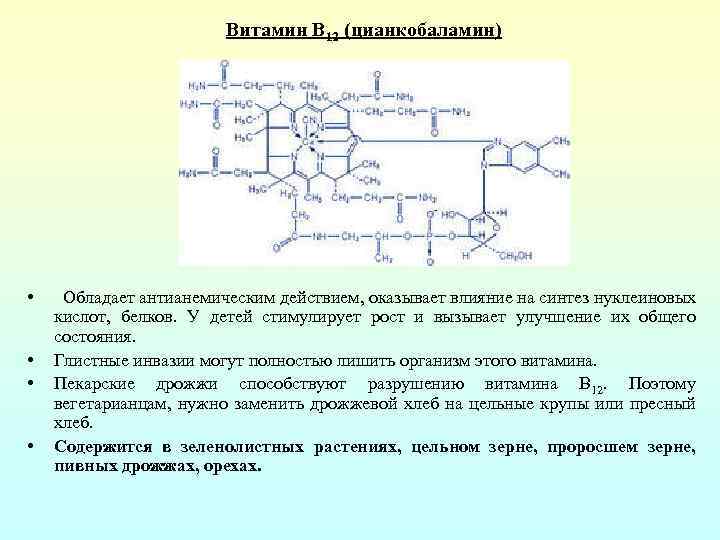
Витамин В 12 (цианкобаламин) • • Обладает антианемическим действием, оказывает влияние на синтез нуклеиновых кислот, белков. У детей стимулирует рост и вызывает улучшение их общего состояния. Глистные инвазии могут полностью лишить организм этого витамина. Пекарские дрожжи способствуют разрушению витамина В 12. Поэтому вегетарианцам, нужно заменить дрожжевой хлеб на цельные крупы или пресный хлеб. Содержится в зеленолистных растениях, цельном зерне, проросшем зерне, пивных дрожжах, орехах.

Витамин С (Аскорбиновая кислота) • • выполняет роль регулятора окислительно восстановительных процессов и обмена веществ, повышает сопротивляемость организма к инфекциям и свертываемость крови, нормализует проницаемость сосудов, оказывает антитоксическое действие при отравлении многими ядами и бактерицидными токсинами, ускоряет заживление ран. При ее недостатке понижается биохимическая активность ряда ферментных систем, повышается проницаемость капилляров, ухудшается заживление ран. При скрытых формах недостаточности витамина С наблюдается быстрая утомляемость, мышечная слабость, снижение аппетита, пониженная сопротивляемость инфекциям. Явная недостаточность витамина С цинга (скорбут) расшатывание зубов, кровоточивость десен, кровоизлияния в кожу, воспаление слизистой оболочки рта. Аскорбиновую кислоту применяют при гипо и авитаминозах, кровотечениях различной природы, интоксикациях и инфекционных заболеваниях, гемморрагических диатезах, болезнях печени, токсикозе беременных и в других случаях. Витамин С обладает некоторыми защитными свойствами в отношении свинца, сероуглерода, анилина, нитрозамина и др. • Суточная потребность - 60 -100 мг. • Содержится во многих растениях, фруктах, ягодах, овощах. Особенно много ее в сушеных плодах шиповника, красном перце, хрене, петрушке, укропе, смородине. • Содержание витамина С значительно снижается при длительной варке продуктов. В целях уменьшения потери витамина овощи следует опускать в кипящую воду.
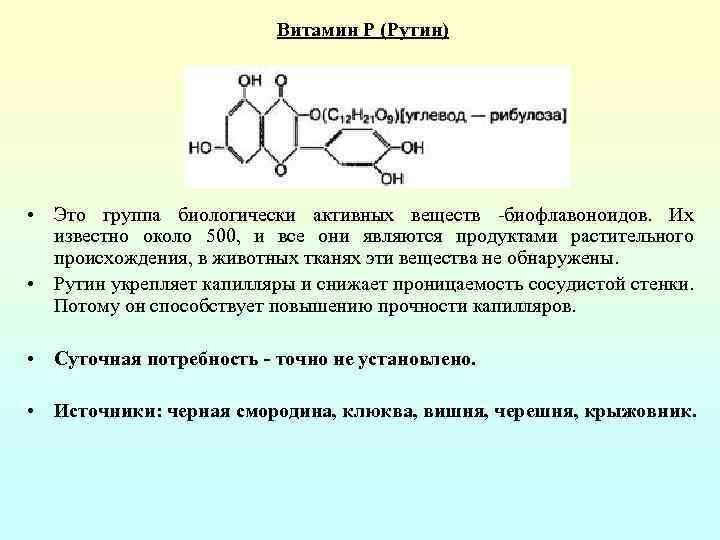
Витамин Р (Рутин) • Это группа биологически активных веществ биофлавоноидов. Их известно около 500, и все они являются продуктами растительного происхождения, в животных тканях эти вещества не обнаружены. • Рутин укрепляет капилляры и снижает проницаемость сосудистой стенки. Потому он способствует повышению прочности капилляров. • Суточная потребность - точно не установлено. • Источники: черная смородина, клюква, вишня, черешня, крыжовник.

Ионофоры • Бывают случаи, когда мембрана наглухо закрывается для определенных ионов: в частности, в митохондриях внутренняя мембрана вообще не пропускает ионов калия. Однако эти ионы попадают внутрь митохондрии, если в окружающей среде имеются антибиотики валиномицин или грамицидин. Валиномицин специализируется, главным образом, на ионах калия (может переносить и ионы рубидия и цезия), а грамицидин переносит, кроме калия, также ионы натрия, лития, рубидия и цезия. • Было выяснено, что молекулы таких проводников имеют форму баранки, радиус отверстия которой таков, что внутри баранки помещается ион калия, натрия или другого щелочного металла. Эти антибиотики назвали ионофорами ("носителями ионов"). грамицидин • Весьма вероятно, что то токсическое действие, которое антибиотики оказывают на различные микроорганизмы, как раз и связано с тем, что в их присутствии мембраны начинают пропускать внутрь те ионы, которым быть там не полагается; это нарушает работу химических систем клетки микроорганизма и ведет к ее гибели или к серьезным расстройствам, прекращающим ее размножение.

Ионофоры – это соединения, способные образовывать ион-дипольные комплексы с катионами металлов, прежде всего с К+ и Na+. • Вещества этой группы связывают ионы металлов в результате согласованного взаимодействия с несколькими карбонильными группами пептидного каркаса; ион при этом удерживается в молекулярной полости комплексона за счет ион дипольных связей. • Ионофоры представляют собой макроциклические структуры, цикл которых состоит из остатков карбоновых и аминокислот. Их молекулярная масса находится в пределах 2000. Важнейшим свойством ионофоров является способность образовывать липидорастворимые катионные комплексы, играющие важную роль в транспорте ионов через мембраны. Одним из распространенных природных ионофоров является валиномицин, который образует достаточно прочные комплексы с ионами калия (р =4. 77) и фактически не образует комплексов с ионами натрия (р =0. 77).

Практически нет природных мембран, в которых бы валиномицин не стимулировал калиевую проводимость. • Схема работы переносчиков ионов ионофоров: а подвижный переносчик (валиномицин); б перенос с помощью канала (грамицидин) • Более простым аналогом валиномицина является энниатин. • Этот ионофор имеет вдвое меньший размер цикла и, кроме того, у него нет групп –NH, образующих в валиномициновых комплексах жесткую систему водородных связей. Комплексы металлов с энниатином уступают валиномициновым комплексам как по устойчивости, так и по специфичности.
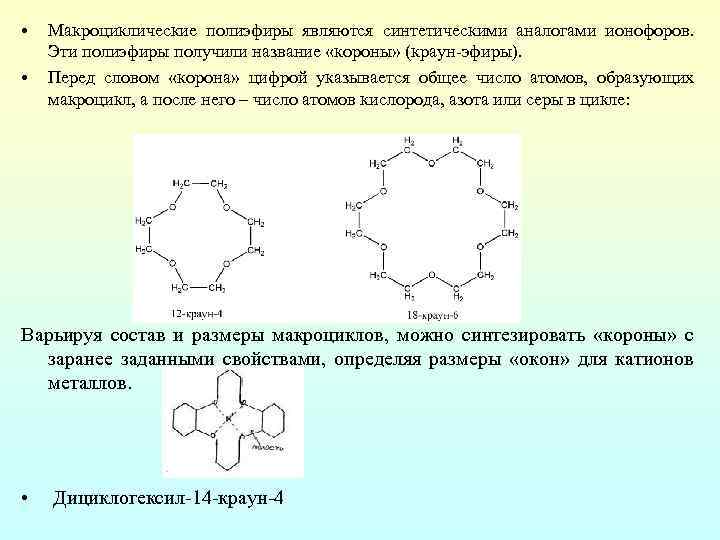
• • Макроциклические полиэфиры являются синтетическими аналогами ионофоров. Эти полиэфиры получили название «короны» (краун эфиры). Перед словом «корона» цифрой указывается общее число атомов, образующих макроцикл, а после него – число атомов кислорода, азота или серы в цикле: Варьируя состав и размеры макроциклов, можно синтезировать «короны» с заранее заданными свойствами, определяя размеры «окон» для катионов металлов. • Дициклогексил 14 краун 4
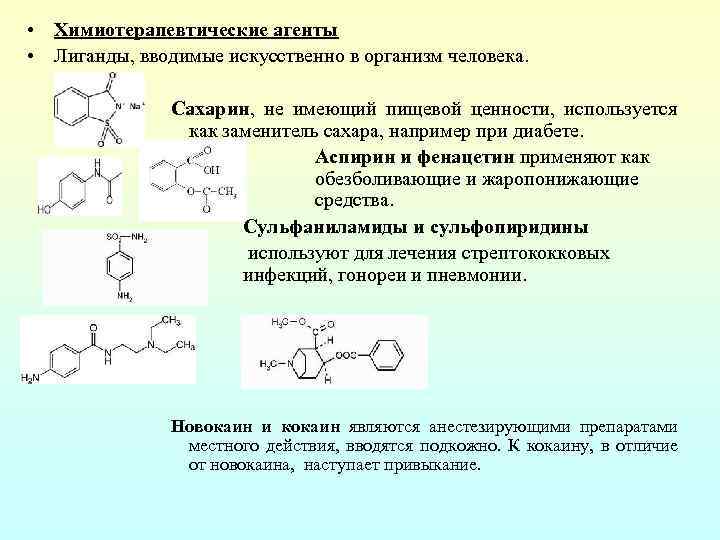
• Химиотерапевтические агенты • Лиганды, вводимые искусственно в организм человека. Сахарин, не имеющий пищевой ценности, используется как заменитель сахара, например при диабете. Аспирин и фенацетин применяют как обезболивающие и жаропонижающие средства. Сульфаниламиды и сульфопиридины используют для лечения стрептококковых инфекций, гонореи и пневмонии. Новокаин и кокаин являются анестезирующими препаратами местного действия, вводятся подкожно. К кокаину, в отличие от новокаина, наступает привыкание.

Все алкалоиды содержат азотисные гетероциклы. К их числу относятся стрихнин, морфин, кодеин, героин, хинин, никотин, диэтиламид лизергиновой кислоты (ЛСД). Стрихнин; Морфин; Кодеин; Героин; Никотин; Хинин; диэтиламид лизергиновой кислоты (ЛСД). Их используют как стимуляторы специфического действия. Взятые в больших количествах они токсичны.
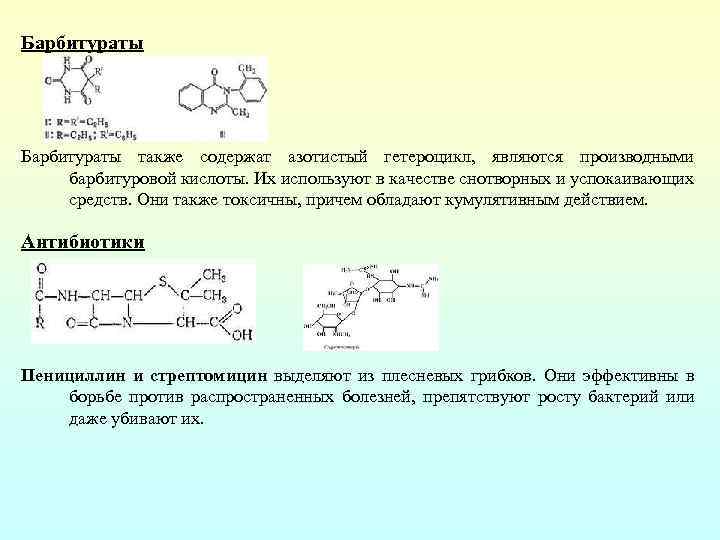
Барбитураты также содержат азотистый гетероцикл, являются производными барбитуровой кислоты. Их используют в качестве снотворных и успокаивающих средств. Они также токсичны, причем обладают кумулятивным действием. Антибиотики Пенициллин и стрептомицин выделяют из плесневых грибков. Они эффективны в борьбе против распространенных болезней, препятствуют росту бактерий или даже убивают их.
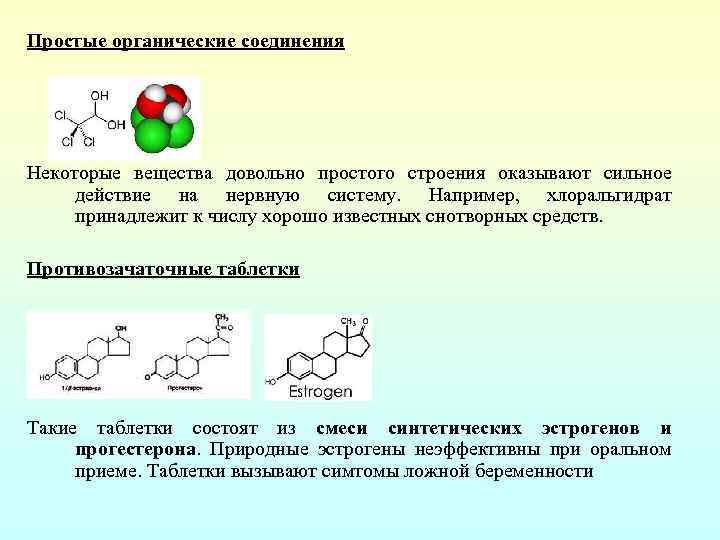
Простые органические соединения Некоторые вещества довольно простого строения оказывают сильное действие на нервную систему. Например, хлоральгидрат принадлежит к числу хорошо известных снотворных средств. Противозачаточные таблетки Такие таблетки состоят из смеси синтетических эстрогенов и прогестерона. Природные эстрогены неэффективны при оральном приеме. Таблетки вызывают симтомы ложной беременности
L5.ppt