Amino acids and proteins.ppt
- Количество слайдов: 75
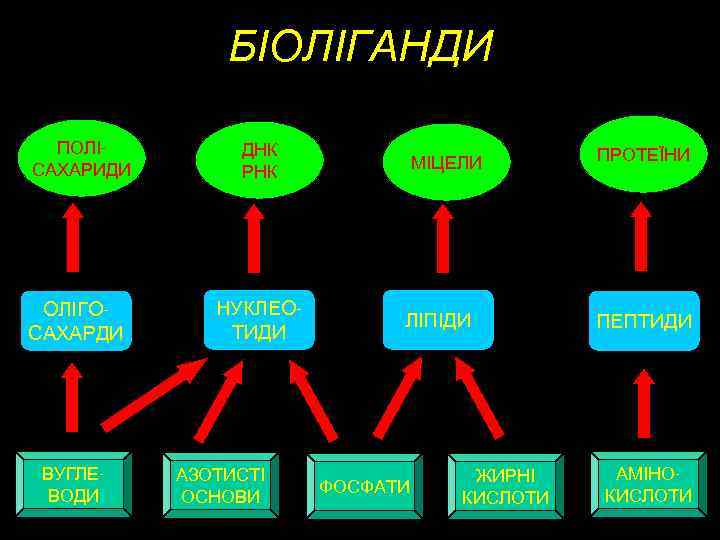
БІОЛІГАНДИ ПОЛІСАХАРИДИ ОЛІГОСАХАРДИ ВУГЛЕВОДИ ДНК РНК НУКЛЕОТИДИ АЗОТИСТІ ОСНОВИ МІЦЕЛИ ЛІПІДИ ФОСФАТИ ЖИРНІ КИСЛОТИ ПРОТЕЇНИ ПЕПТИДИ АМІНОКИСЛОТИ

Протеїни (за самими наближеними оцінками в організмі людини є біля 100 000 білків)
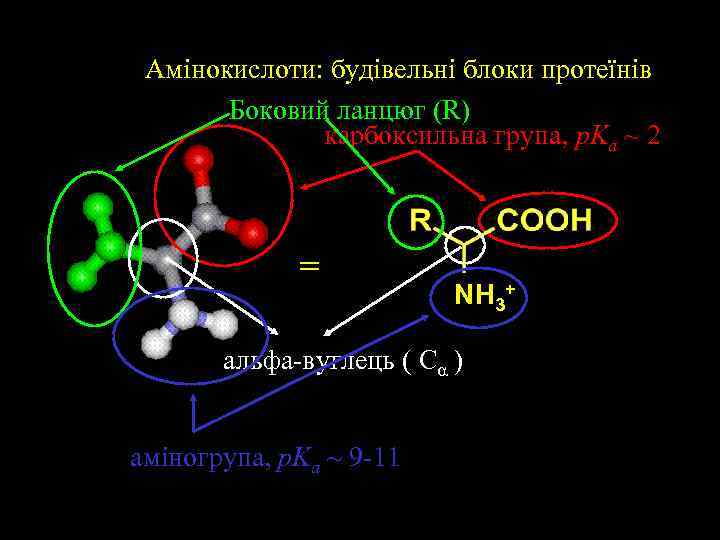
Aмінокислоти: будівельні блоки протеїнів Боковий ланцюг (R) карбоксильна група, p. Ka ~ 2 = NH 3+ альфа-вуглець ( Ca ) аміногрупа, p. Ka ~ 9 -11
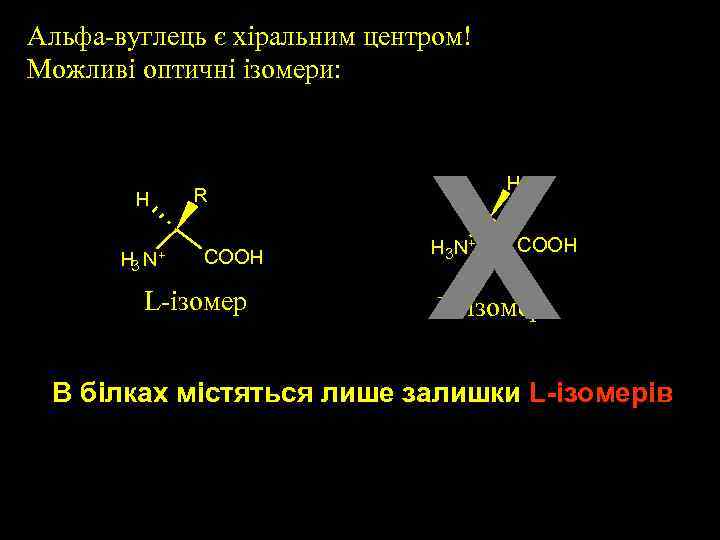
Альфа-вуглець є хіральним центром! Можливі оптичні ізомери: H H 3 N+ R COOH L-iзомер X R H 3 N+ H COOH D-iзомер В білках містяться лише залишки L-iзомерів

L-конфігурація природних амінокислот забезпечує високу cтереоселективність взаємодії із сполуками, що мають строго визначену просторову конфігурацію. У цьому проявляється біохімічний принцип структурної комплементарності. Однак у клітинах багатьох мікроорганізмів знайдені D-амінокислоти (наприклад, у стінках клітин і в складі деяких антибіотиків). Так, до складу білків клітин бактерій сибірської язви входить D-глутамінова кислота, тому проти цього виду бактерій безсилі ферменти, що розщеплюють білки людини та тварин.

Дисоціація амінокислот У складі амінокислот, які не містять здатних до іонізації груп у бокових ланцюгах, тільки карбоксильна та аміногрупа зазнають дисоціації Перший ступінь дисоціації: карбоксильна група R H 3 N+-CH-COOH заряд = +1 p. Ka 1 ~ 2 R H 3 N+-CH-COO- +H+ заряд = 0 цвіттер-іон

Другий ступінь дисоціації: аміногрупа R H 3 N+-CH-COOзаряд = 0 p. Ka 2 ~ 9 R H 2 N-CH-COO- +H+ заряд = -1

Протеїногенні амінокислоти приймають участь у побудові молекул пептидів та білків

Гліцин (Gly, G): найпростіша амінокислота Боковий ланцюг - водень: H H 3 N+-CH-COOH
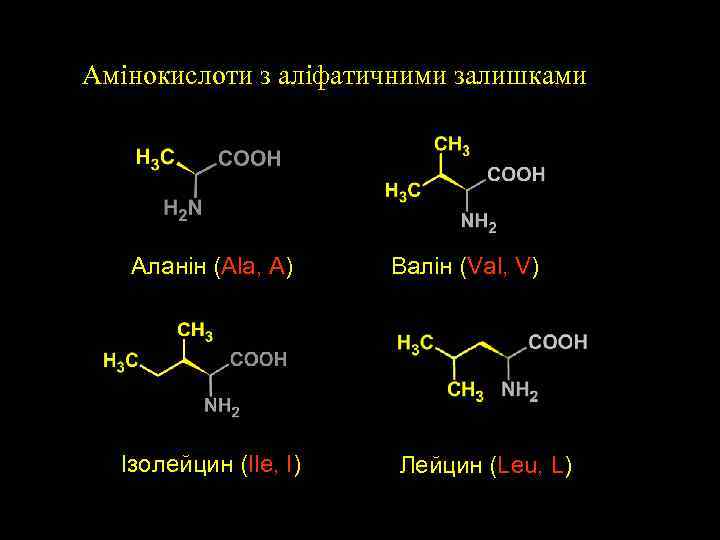
Aмінокислоти з аліфатичними залишками Аланін (Ala, A) Ізолейцин (Ile, I) Валін (Val, V) Лейцин (Leu, L)
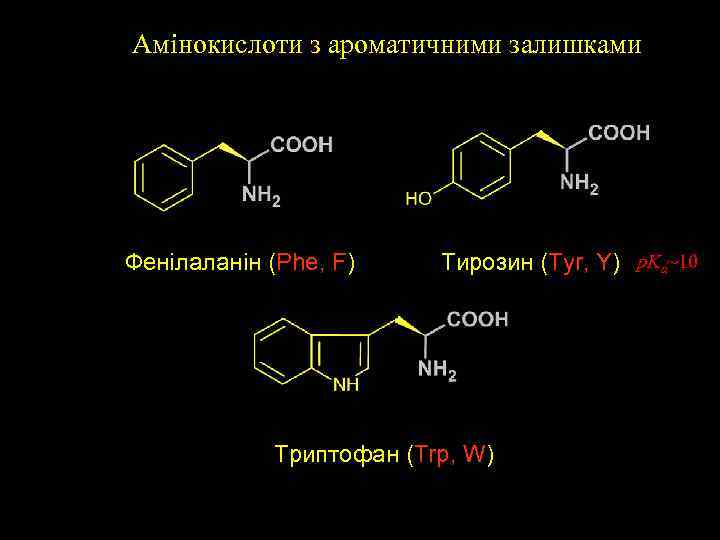
Aмінокислоти з ароматичними залишками Фенілаланін (Phe, F) Тирозин (Tyr, Y) p. Ka~10 Триптофан (Trp, W)
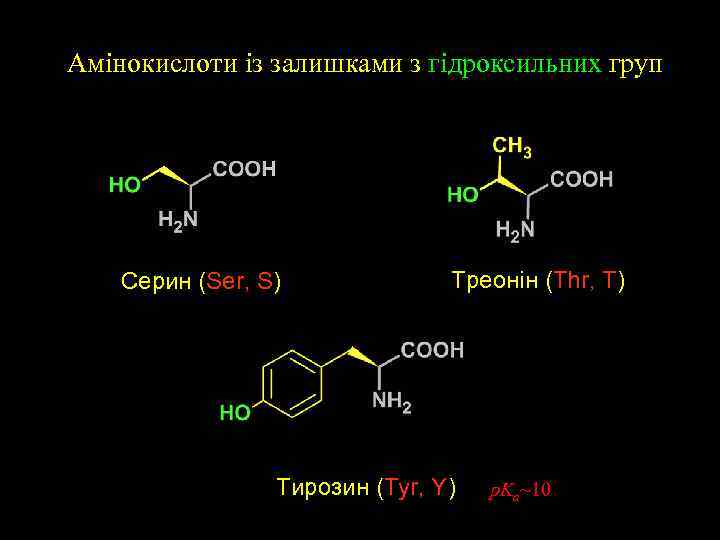
Амінокислоти із залишками з гідроксильних груп Серин (Ser, S) Треонін (Thr, T) Тирозин (Tyr, Y) p. Ka~10
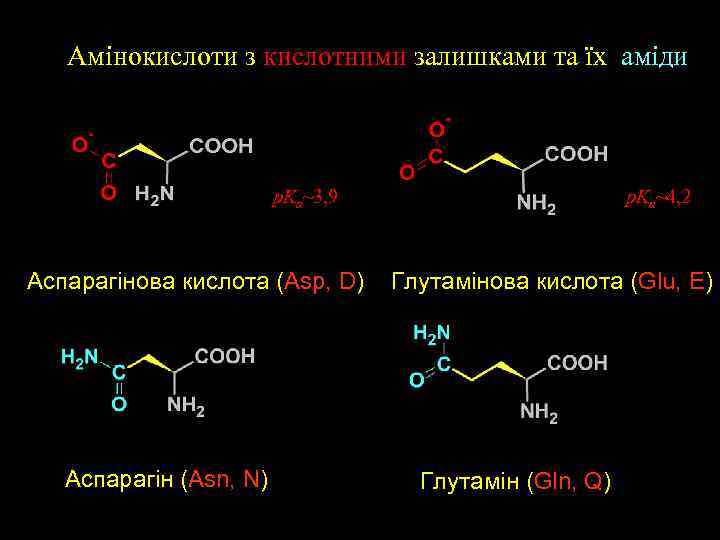
Aмінокислоти з кислотними залишками та їх аміди p. Ka~4, 2 p. Ka~3, 9 Аспарагінова кислота (Asp, D) Аспарагін (Asn, N) Глутамінова кислота (Glu, E) Глутамін (Gln, Q)
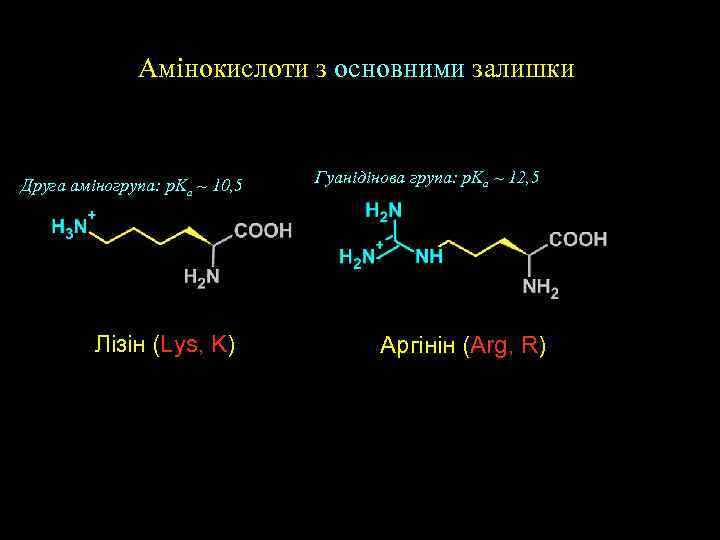
Aмінокислоти з основними залишки Друга аміногрупа: p. Ka ~ 10, 5 Лізін (Lys, K) Гуанідінова група: p. Ka ~ 12, 5 Аргінін (Arg, R)
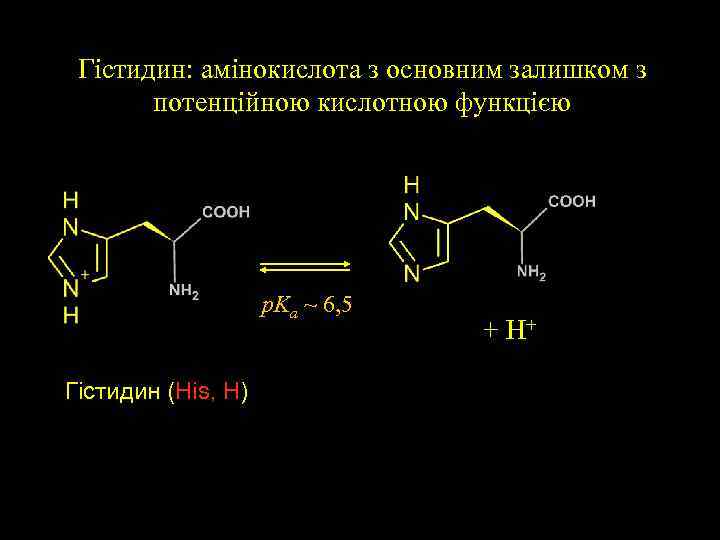
Гістидин: амінокислота з основним залишком з потенційною кислотною функцією p. Ka ~ 6, 5 Гістидин (His, H) + H+
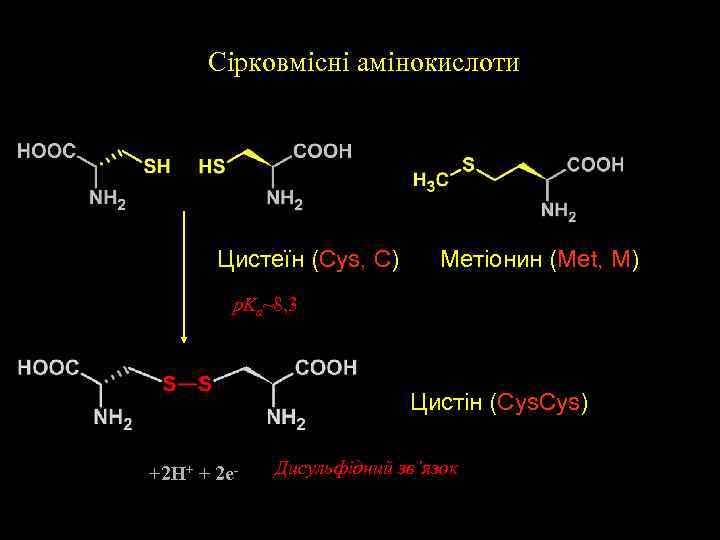
Сірковмісні амінокислоти Цистеїн (Cys, C) Метіонин (Met, M) p. Ka~8, 3 Цистін (Cys. Cys) +2 H+ + 2 e- Дисульфідний зв’язок
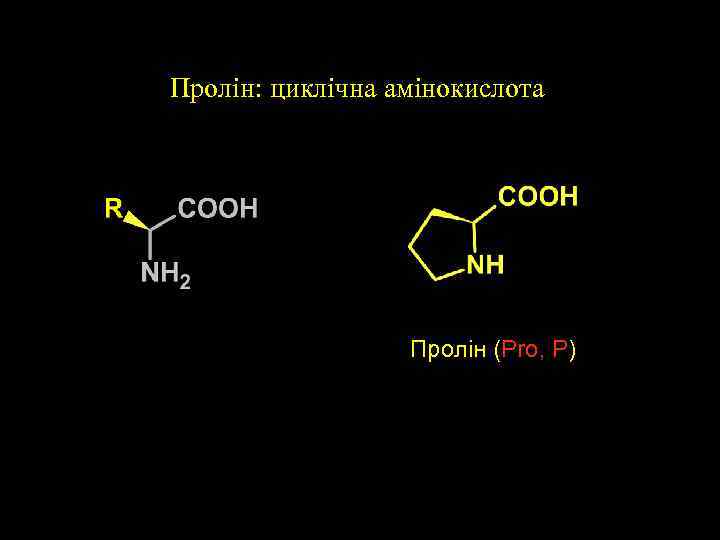
Пролін: циклічна амінокислота Пролін (Pro, P)

Незамінимі амінокислоти (амінокислоти, що не синтезуються в даному організмі із інших сполук) обов’язково повинні надходити в організм ззовні (з їжею)) – валін, лейцин, ізолейцин, треонін, метіонін, фенілаланін, триптофан, лізин. Частково замінимі амінокислоти (синтезуються в організмі, але швидкість їх синтезу недостатня для потреб організму) – гістидин, аргінін Умовно замінимі амінокислоти (можуть синтезуватися в організмі із незамінимих) – цистеїн із метіоніну, тирозин із фенілаланіну. Замінимі амінокислоти (синтезуються у необхідній кількості в організмі) – аланін, аспарагінова кислота, аспарагін, глутамінова кислота, глутамін, пролін, гліцин, серин

Рідкісні протеїногенні амінокислоти (рідко зустрічаються у білках)
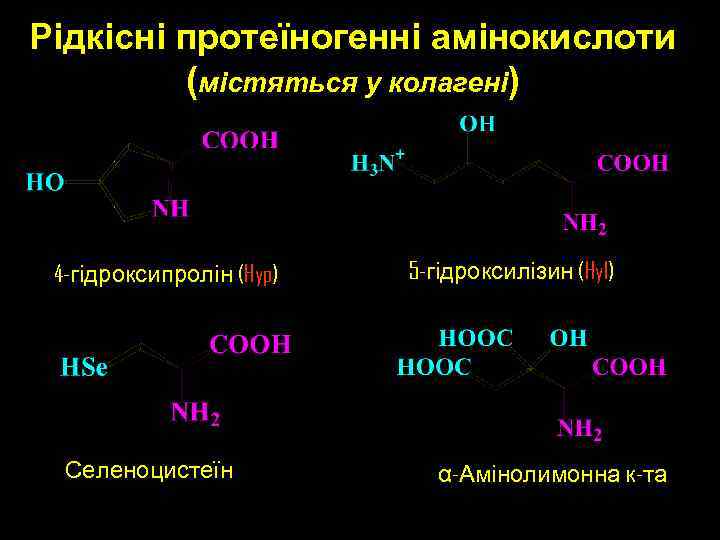
Рідкісні протеїногенні амінокислоти (містяться у колагені) 4 -гідроксипролін (Hyp) Селеноцистеїн 5 -гідроксилізин (Hyl) α-Амінолимонна к-та

Непротеїногенні амінокислоти не входять до складу білкових молекул, але при цьому виконують певні біологічні функції
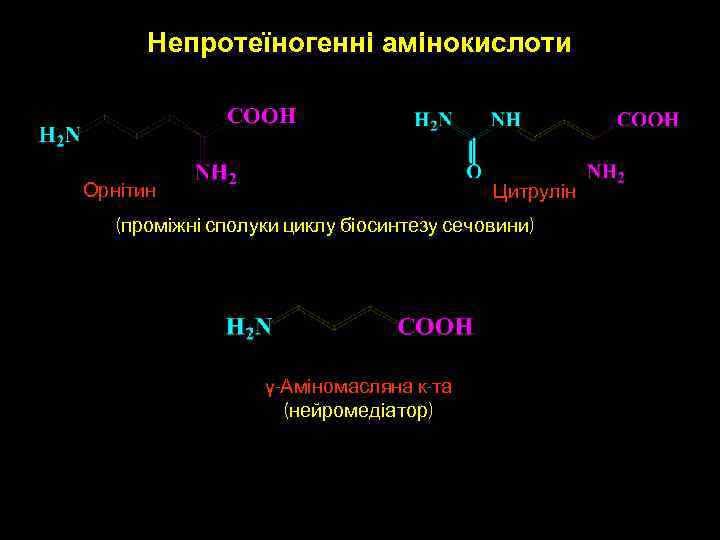
Непротеїногенні амінокислоти Орнітин Цитрулін (проміжні сполуки циклу біосинтезу сечовини) γ-Аміномасляна к-та (нейромедіатор)
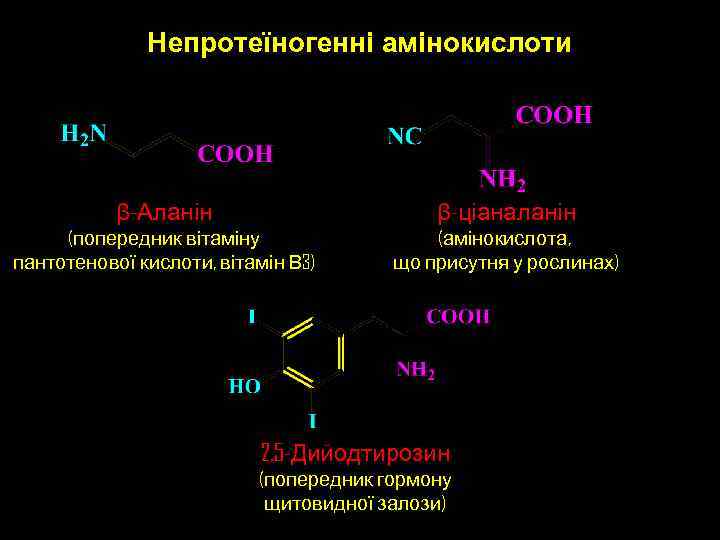
Непротеїногенні амінокислоти β-Аланін β-ціаналанін (попередник вітаміну пантотенової кислоти, вітамін В 3) (амінокислота, що присутня у рослинах) 2, 5 -Дийодтирозин (попередник гормону щитовидної залози)

Пептиди
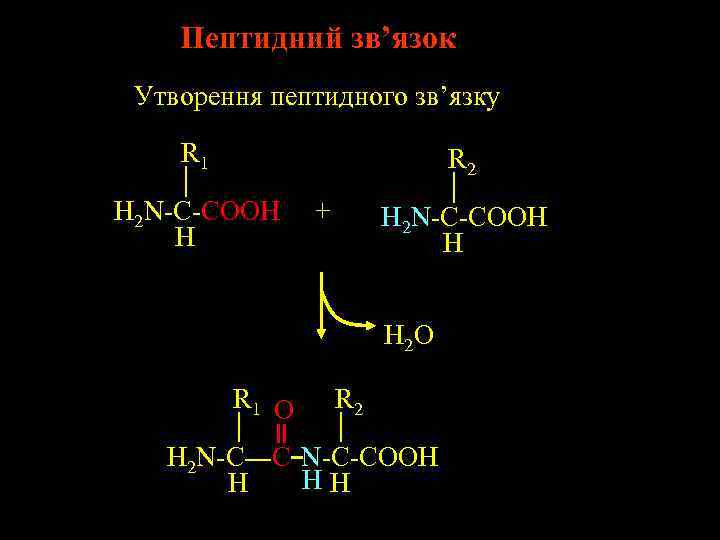
Пептидний зв’язок Утворення пептидного зв’язку R 1 R 2 H 2 N-C-COOH H + H 2 N-C-COOH H H 2 O R 1 O R 2 H 2 N-C---C N-C-COOH HH H
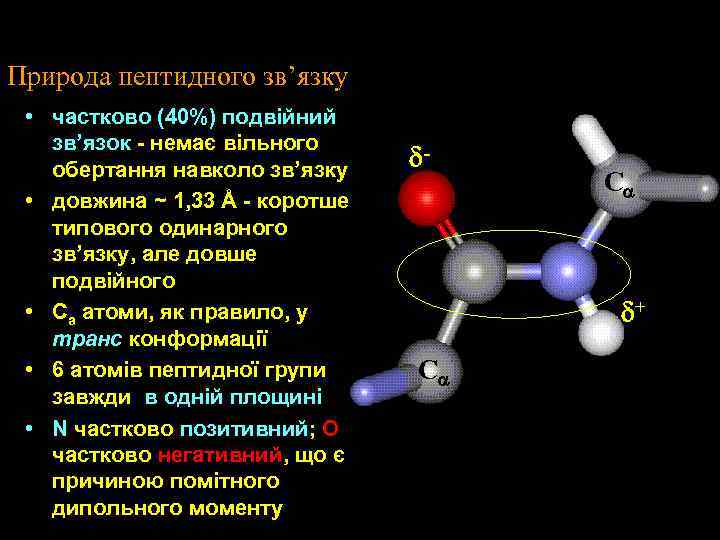
Природа пептидного зв’язку • частково (40%) подвійний зв’язок - немає вільного обертання навколо зв’язку • довжина ~ 1, 33 Å - коротше типового одинарного зв’язку, але довше подвійного • Ca атоми, як правило, у транс конформації • 6 aтомів пептидної групи завжди в одній площині • N частково позитивний; O частково негативний, що є причиною помітного дипольного моменту d- Ca d+ Ca

Пептиди • Короткі полімери амінокислот, з’єднані пептидним зв’язком – – 2 залишки - дипептид 3 залишки - трипептид 12 -20 залишків - oлігопептид багато - поліпептид • пептидні зв’язки утворюють основний ланцюг

Будова протеїнів
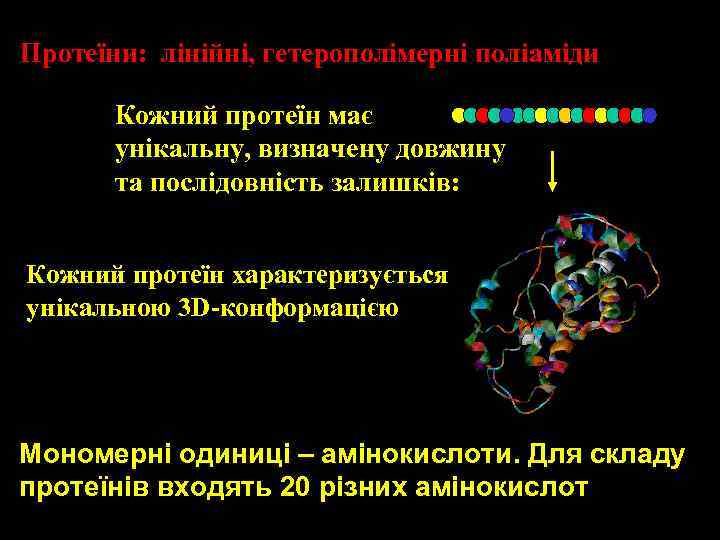
Протеїни: лінійні, гетерополімерні поліаміди Кожний протеїн має унікальну, визначену довжину та послідовність залишків: Кожний протеїн характеризується унікальною 3 D-конформацією Moномерні одиниці – aмінокислоти. Для складу протеїнів входять 20 різних амінокислот

L-конфігурація природних амінокислот забезпечує високу cтереоселективність взаємодії із сполуками, що мають строго визначену просторову конфігурацію. У цьому проявляється біохімічний принцип структурної комплементарності. Однак у клітинах багатьох мікроорганізмів знайдені D-амінокислоти (наприклад, у стінках клітин і в складі деяких антибіотиків). Так, до складу білків клітин бактерій сибірської язви входить D-глутамінова кислота, тому проти цього виду бактерій безсилі ферменти, що розщеплюють білки людини та тварин.

Протеїн: один або декльіка поліпептидних ланцюгів • Moномерний протеїн: один поліпептидний ланцюг • Більше ніж один мультімерний протеїн: – Гомомультімер - більш ніж один ланцюг, усі з однаковою амінокислотною послідовністю – Гетеромультімер - дві або більше різних ланцюгів
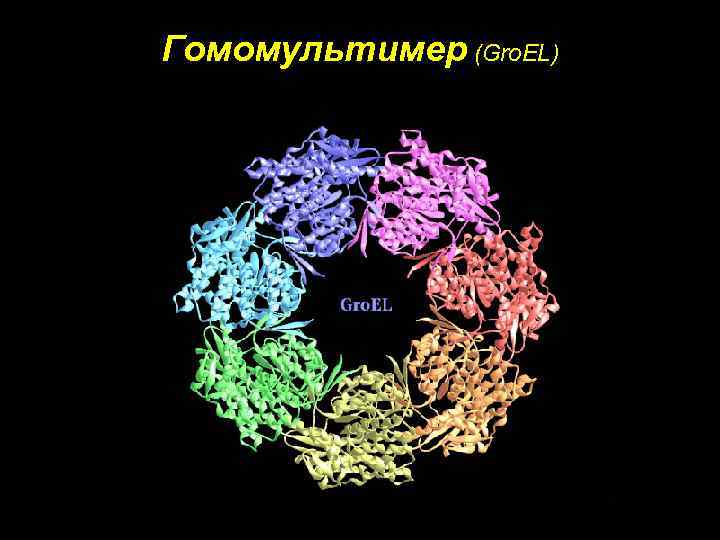
Гомомультимер (Gro. EL)
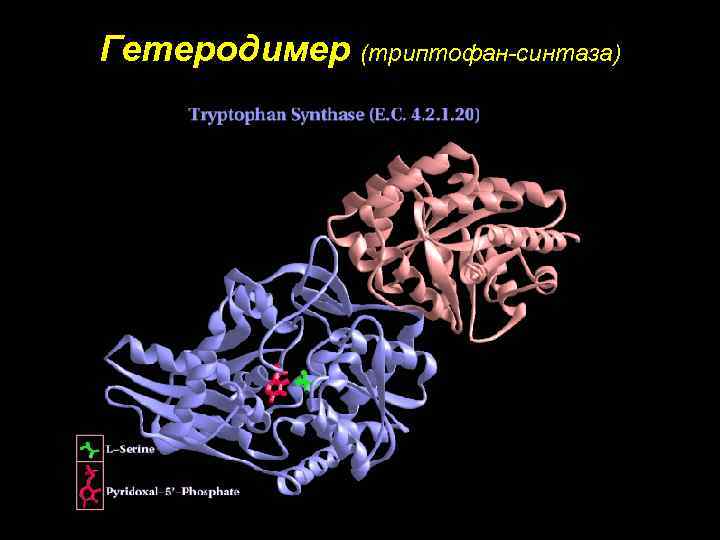
Гетеродимер (триптофан-синтаза)
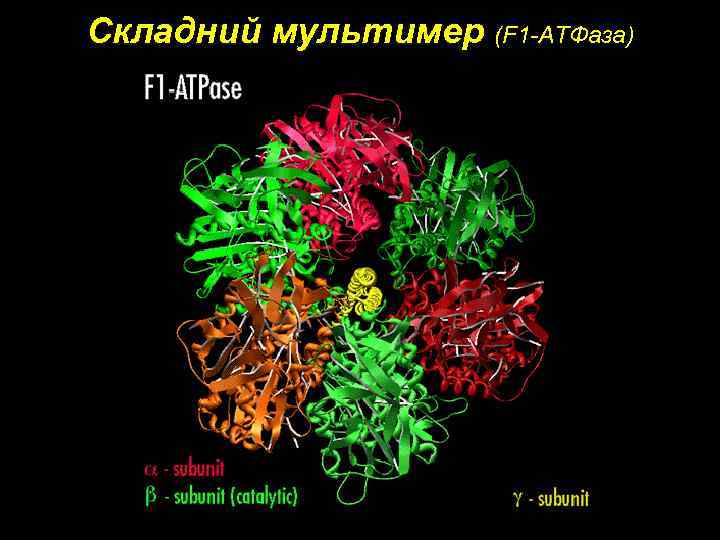
Складний мультимер (F 1 -АТФаза)
Архітектура протеїнів • Рівні структурної організації протеїнів - Первинна - Вторинна - Надвторинна - Доменна - Третинна - Четвертинна (якщо присутня) • Форма - фібрилярні або глобулярні

Які сили визначають структуру протеїнів? • Первинна структура визначається ковалентними зв’язками: послідовність • Вторинна, надвторинна, доменна, третинна, чвертинна структури - всі визначаються слабкими силами: конформація • Слабкі сили - H-зв’язки, йонна взаємодія, сили вандер-Ваальса, гідрофобна взаємодія

Первинна структура - послідовність амінокислот у протеїні • Послідовність амінок-т кодується послідовністю нуклеотидів в ДНК і є, таким чином, однією з форм генетичної інформації • Послідовність амінок-т є унікальною характеристикою кожного протеїну • Послідовність амінок-т читається з амінотермінуса до карбоксильного термінуса, напр. , : Met-Ala-Ser-Arg------Ser-Thr-Leu-Asn MASR----STLN

Первинна структура - яка довжина поліпептидного ланцюга? • Iнсулін: ~ 50 залишків MW ~ 5700 • Gro. EL/Gro. ES: – 14 субодиниць з MW 60 000 – 7 субодиниць з MW 10 000 – загальний MW 910, 000 (~ 8000 залишків)
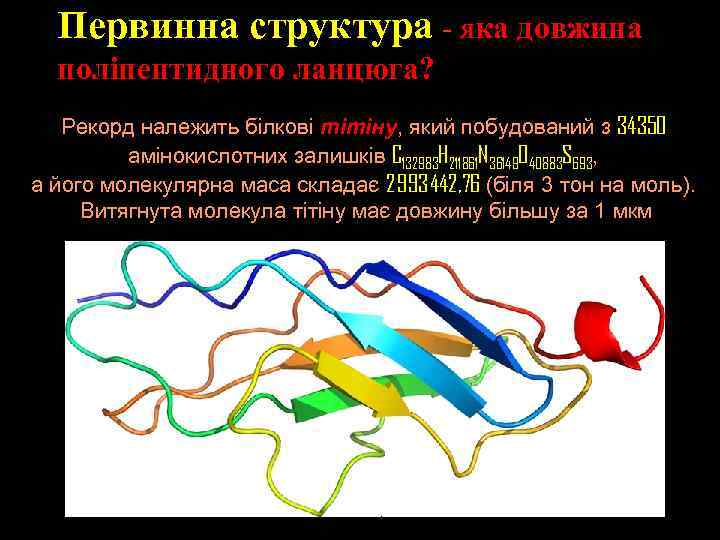
Первинна структура - яка довжина поліпептидного ланцюга? Рекорд належить білкові тітіну, який побудований з 34350 амінокислотних залишків C 132983 H 211861 N 36149 O 40883 S 693, а його молекулярна маса складає 2 993 442, 76 (біля 3 тон на моль). Витягнута молекула тітіну має довжину більшу за 1 мкм

Первинна структура - природа послідовності в протеїнах • Послідовність та склад відображують функцію протеїну, напр. , : -Meмбранні протеїни мають більше гідрофобних залишків -Фібрилярні протеїни можуть мати послідовності, що повторюються • Гомологічні протеїни з різних організмів мають гомологічні послідовності (напр. , гемоглобін людини та бика)

Порівняння послідовності в цитохромі c у різних видів Людський та кіньський цитохром c: 88. 5% iдентичності в 104 залишках ЛЮДИНА 1 GDVEKGKKIFIMKCSQCHTVEKGGKHKTGPNLHGLFGRKTGQAPGYSYTAANKNKGIIWG КІНЬ 1 GDVEKGKKIFVМKCAQCHTVEKGGKHKTGPNLHGLFGRKTGQAPGFTYTDANKNKGITWK ЛЮДИНА КІНЬ 61 61 EDTLMEYLENPKKYIPGTKMIFVGIKKKEERADLIAYLKKATNE EETLMEYLENPKKYIPGTKMIFAGIKKKTEREDLIAYLKKATNE Людський та дріжджовий цитохром c: 64. 4% iдентичності в 101 залишках ЛЮДИНА 1 GDVEKGKKIFIMKCSQCHTVEKGGKHKTGPNLHGLFGRKTGQAPGYSYTAANKNKGIIWG ДРІЖДЖІ 6 GSAKKGATLFKTRCLQCHTVEKGGPHKVGPNLHGIFGRHSGQAEGYSYTDANIKKNVLWD ЛЮДИНА 61 EDTLMEYLENPKKYIPGTKMIFVGIKKKEERADLIAYLKKA ДРІЖДЖІ 66 ENNMSEYLTNPKKYIPGTKMAFGGLKKEKDRNDLITYLKKA Людський та бактеріальний цитохром c: 33. 9% iдентичності в 118 залишках ЛЮДИНА 2 DVEKGKKIFIMKCSQCHTVEKGGKHKTGPNLHGLFGRKTGQAPGYSYTAANKNKG---II RHOPA 2 DAKAGEAVF-KQCMTCHRADK---NMVGPALGGVVGRKAGTAAGFTYSPLNHNSGEAGLV ЛЮДИНА RHOPA 59 WGEDTLMEYLENP----KKYIP--G----TKMIFVGIKKKEERADLIAYLKKAT 58 WTADNIINYLNDPNAFLKKFLTDKGKADQAVGVTKMTFK-LANEQQRKDVVAYL--AT Чорний: Iдентичні залишки Червоний: Різні залишки
Первинна структура - роль послідовності в структурі протеїну Met-Ala-Cys. …. . . Ala-Thr-Arg-Leu Вся інформація, необхідна для згортання протеїнового ланцюга в його “нативну” структуру, міститься в первинній амінокислотній струкутрі пептиду

…. . але здійснюється це згортання за допомогою слабких сил • • ван дер Ваальс: 0. 4 - 4 к. Дж/моль водневі зв’язки: 12 -30 к. Дж/моль іонні зв’язки: 20 к. Дж/моль гідрофобні взаємодії: <40 к. Дж/моль Iндивідуально слабкі, але сумісно міцні взаємодії Ковалентні зв’язки в 10 -100 разів міцніші
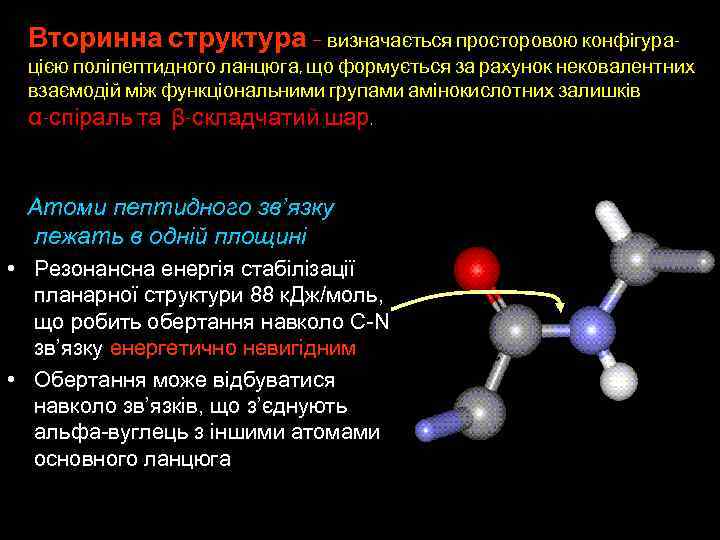
Вторинна структура – визначається просторовою конфігурацією поліпептидного ланцюга, що формується за рахунок нековалентних взаємодій між функціональними групами амінокислотних залишків α-спіраль та β-складчатий шар. Ca Атоми пептидного зв’язку лежать в одній площині • Резонансна енергія стабілізації планарної структури 88 к. Дж/моль, що робить обертання навколо C-N зв’язку енергетично невигідним • Обертання може відбуватися навколо зв’язків, що з’єднують альфа-вуглець з іншими атомами основного ланцюга Ca
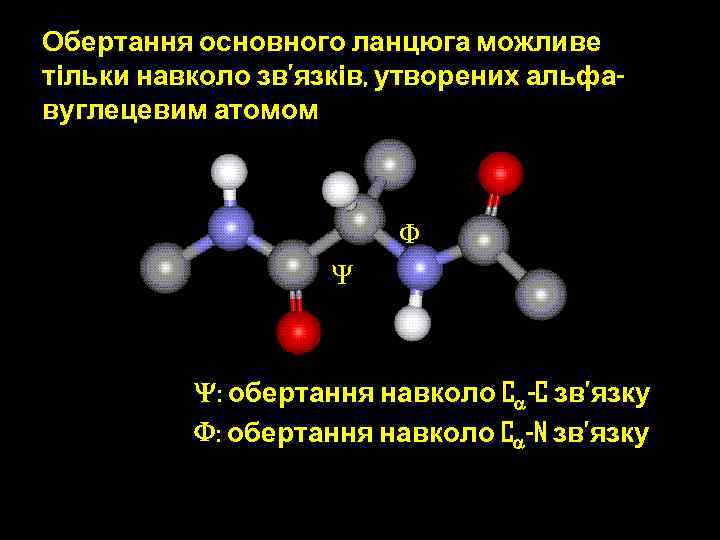
Обертання основного ланцюга можливе тільки навколо зв’язків, утворених альфавуглецевим атомом F Y Y: обертання навколо Ca-C зв’язку F: обертання навколо Ca-N зв’язку

Рис. 2. 36 (Страйер, т. 2, с. 34)

C Вторинна структура - α-спіраль • Правообертаюча спіраль, стабілізована водневими зв’язками • амідний карбоніл залишку i утворює H-зв’язок з амідним азотом залишку i+4 • Залишків на виток: 3. 6 • Зріст ланцюгу на залишок: 1. 5 Å • Зріст ланцюгу на виток (pitch): 3. 6 x 1. 5Å = 5. 4 Å • Помітний дипольний момент • Y = -60 о, F = -45 о N
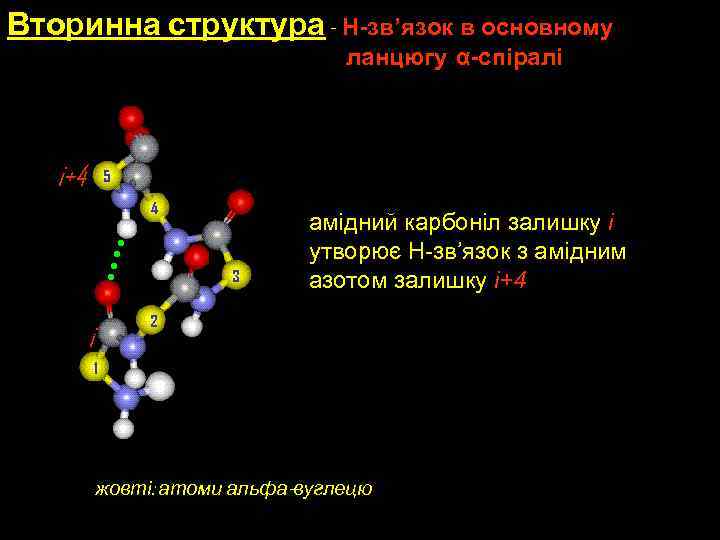
Вторинна структура - H-зв’язок в основному ланцюгу α-спіралі i+4 5 4 3 амідний карбоніл залишку i утворює H-зв’язок з амідним азотом залишку i+4 2 i 1 жовті: атоми альфа-вуглецю

Вторинна структура - способи візуалізації α-спіралі • осн. ланцюг • осн. + бокові ланцюги • заповнення простору • спірально-петельна • циліндр
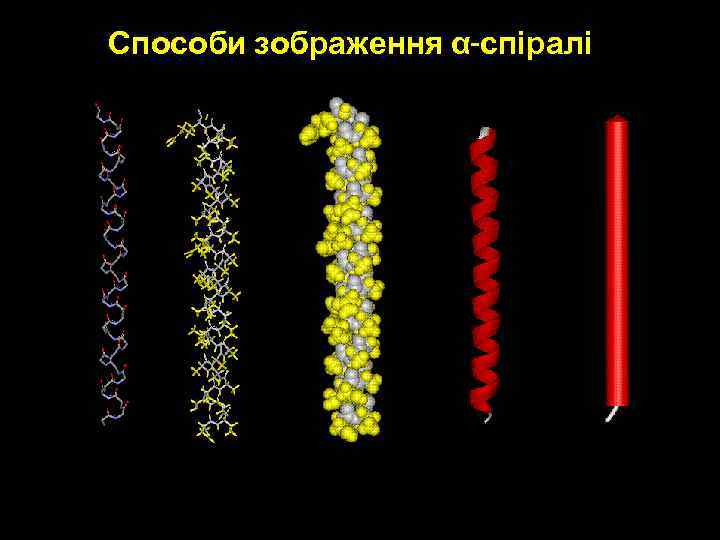
Способи зображення α-спіралі
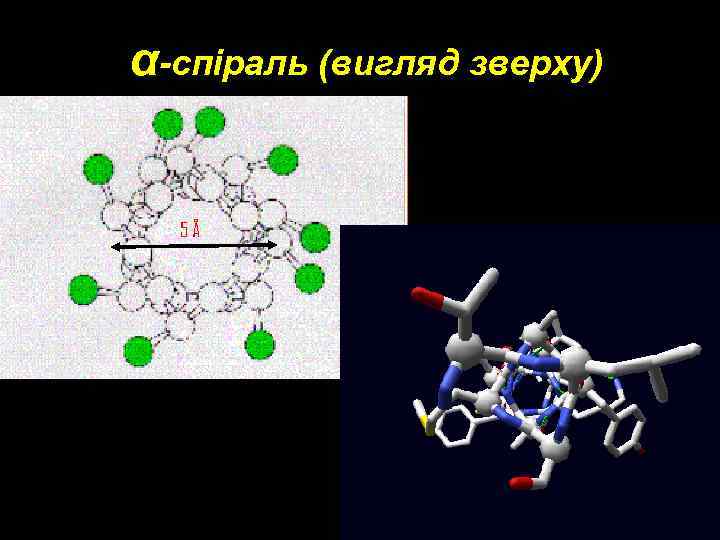
α-спіраль (вигляд зверху) 5Å
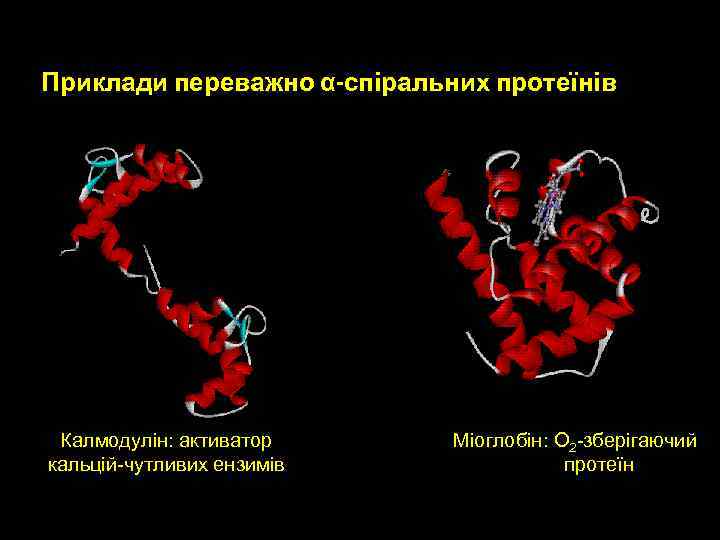
Приклади переважно α-спіральних протеїнів Калмодулін: активатор кальцій-чутливих ензимів Mіоглобін: O 2 -зберігаючий протеїн
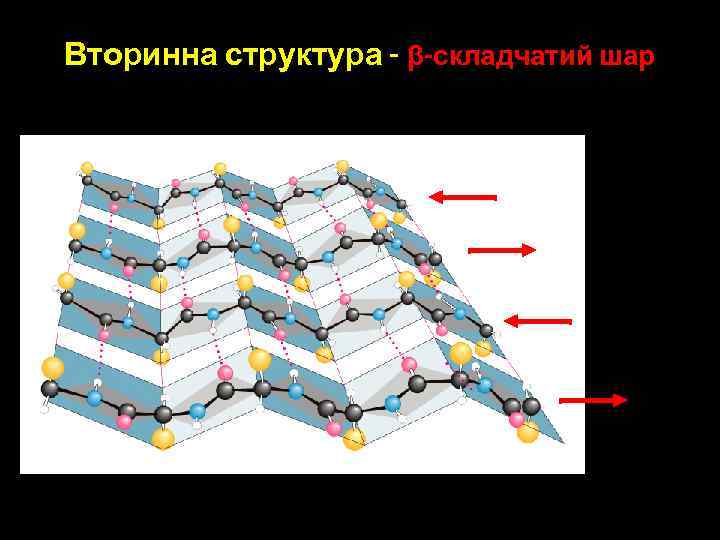
Вторинна структура - β-складчатий шар

Вторинна структура - β-складчатий шар • Пептидні ланцюги розміщені паралельно один до одного, утворюючи фігуру, подібну до аркуша, що складений гармошкою • Шар може бути утворений одним, двома або більшою кількістю поліпептидних ланцюгів • Якщо суміжні ланцюги в шарі орієнтовані N-кінцями в одну сторону, то утворюється паралельна β-структура • Якщо поліпептидний ланцюг робить поворот назад і йде вздовж самого себе у зворотному напрямку, то при цьому формується антипаралельна β-структура
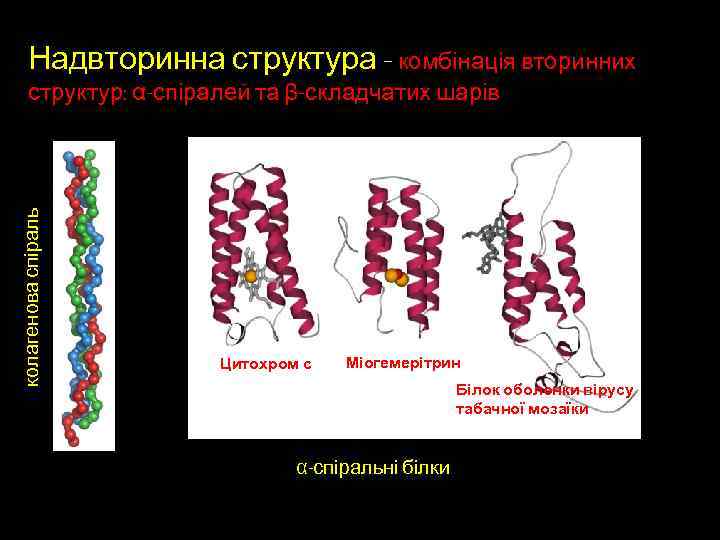
Надвторинна структура – комбінація вторинних колагенова спіраль структур: α-спіралей та β-складчатих шарів Цитохром с Міогемерітрин Білок оболонки вірусу табачної мозаїки α-спіральні білки
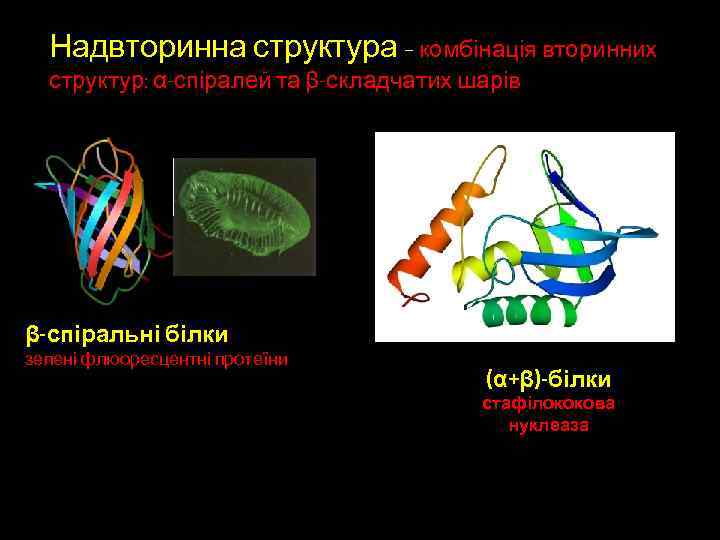
Надвторинна структура – комбінація вторинних структур: α-спіралей та β-складчатих шарів β-спіральні білки зелені флюоресцентні протеїни (α+β)-білки стафілококова нуклеаза
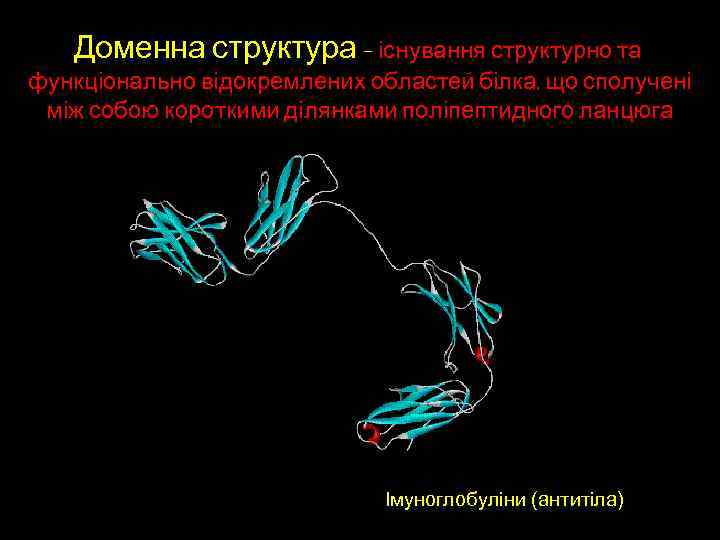
Доменна структура – існування структурно та функціонально відокремлених областей білка, що сполучені між собою короткими ділянками поліпептидного ланцюга Iмуноглобуліни (антитіла)

Третинна структура - фібрилярні або глобулярні
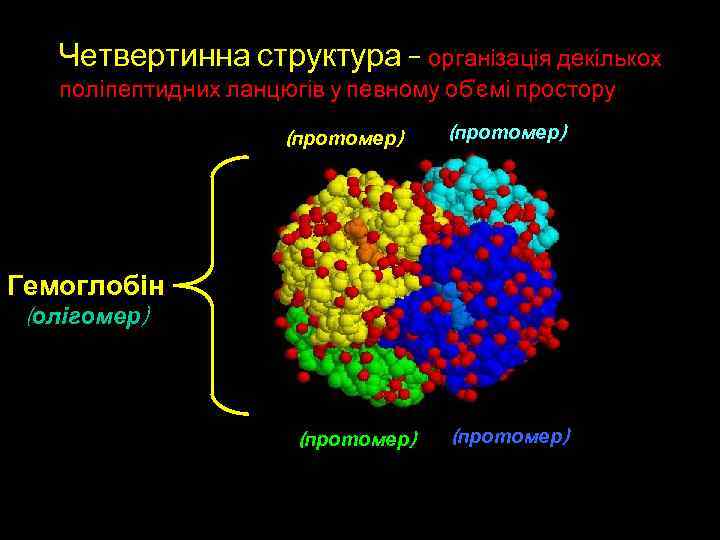
Четвертинна структура – організація декількох поліпептидних ланцюгів у певному об’ємі простору (протомер) Гемоглобін (олігомер) (протомер)

Біологічні функції протеїнів Протеїни - медіатори біологічних функцій • Каталітична - напр. , рибонуклеаза, каталізує гідроліз РНК • Регуляторна – напр. , інсулін, регулює рівень цукру в крові • Tранспортна – напр. , гемоглобін, доставляє O 2 до тканин • Структурна – напр. , коллаген, компонент сполучних тканин • Контрактильна (скорочувальна) – напр. , актин, міозин – опосередковують скорочення м’язів • Захисна – напр, антитіла (імуноглобуліни) впізнають і зв’язують чужорідні для організму об’єкти (віруси, бактерії) • Енергетична – напр. , казеїн молока та ін. слугують джерелом енергії (поживні речовини) • Eкзотична - антифризні протеїни у риб та комах

Функціональні групи небілкової природи у складі протеїнів Протеїни можуть бути ковалентно зв'язаними з іншими хімічними групами • Якщо неамінокислотна частина протеїну є важливою для реалізації його функції, то вона називається простетичною групою. – нуклеопротеїн: протеїн з компонентом нуклеїнової кислоти (напр. , в рибосомах) – глікопротеїн: протеїн, ковалентно зв’язаний з карбогідратом (напр. , поверхневі рецептори клітин) – ліпопротеїн: протеїн, ковалентно зв’язаний з ліпідним компонентом (напр. , деякі мембранно-вбудовані протеїни) – металопротеїн: протеїн, для виконання функції якого потрібний іон (іони) металу, напр. , гемоглобін
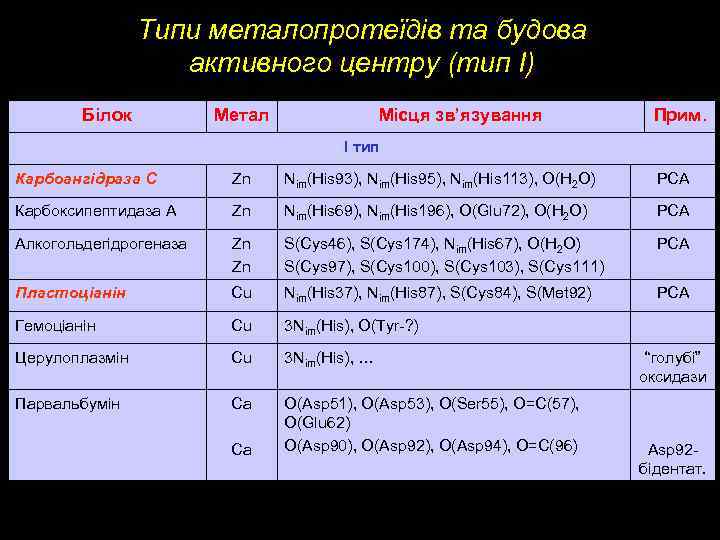
Типи металопротеїдів та будова активного центру (тип І) Білок Метал Місця зв’язування Прим. I тип Карбоангідраза С Zn Nim(His 93), Nim(His 95), Nim(His 113), O(H 2 O) PCA Карбоксипептидаза А Zn Nim(His 69), Nim(His 196), O(Glu 72), O(H 2 O) PCA Алкогольдегідрогеназа Zn Zn S(Cys 46), S(Cys 174), Nim(His 67), O(H 2 O) S(Cys 97), S(Cys 100), S(Cys 103), S(Cys 111) PCA Пластоціанін Cu Nim(His 37), Nim(His 87), S(Cys 84), S(Met 92) PCA Гемоціанін Cu 3 Nim(His), O(Tyr-? ) Церулоплазмін Cu 3 Nim(His), … Парвальбумін Ca O(Asp 51), O(Asp 53), O(Ser 55), O=C(57), O(Glu 62) O(Asp 90), O(Asp 92), O(Asp 94), O=C(96) Ca “голубі” оксидази Asp 92 бідентат.
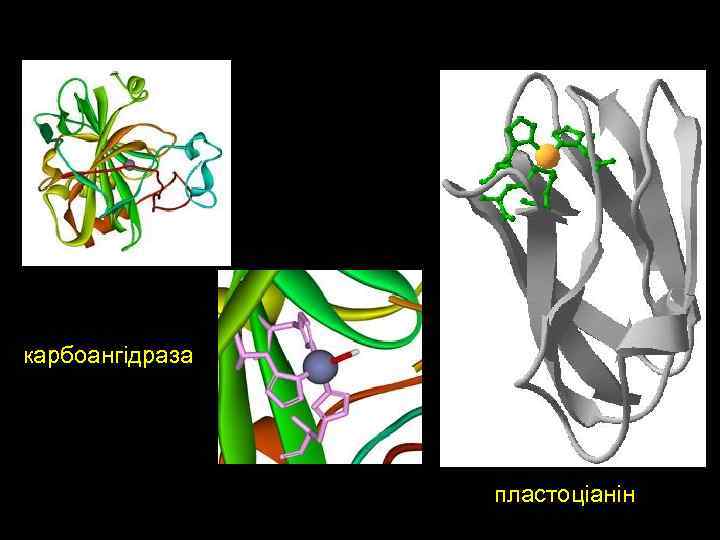
карбоангідраза пластоціанін

Типи металопротеїдів та будова активного центру (тип ІІ) Білок Метал Місця зв’язування Прим. ІI тип Супероксиддисмутаза 1 Cu, Zn Nim(His 44, 46, 118)-Cu-µ-Nim(His 61)-Zn. Nim(His 69, 78), O(Asp 81) PCA Акваметгемерітрин Fe, Fe Nim(His 73, 77, 101)-Fe-µ[O(Glu 58), O(Asp 106), O(H 2 O)]-Fe. Nim(His 25, 54), O(Tyr 109) PCA Оксигемоціанін Cu, Cu Nim(His 173, 177, 204)-Cu-µ-[O(Tyr)? O 2]-Cu. Nim(His 324, 328, 364) Конкавалін А Ca, Mg (Ca) Nim(His 24), O(Asp 8), 2 O(H 2 O)-Ca-µ[O(Asp 10, 19]-Mg(Ca? )-O(Asp 14), 2 O(H 2 O), O=C(12)
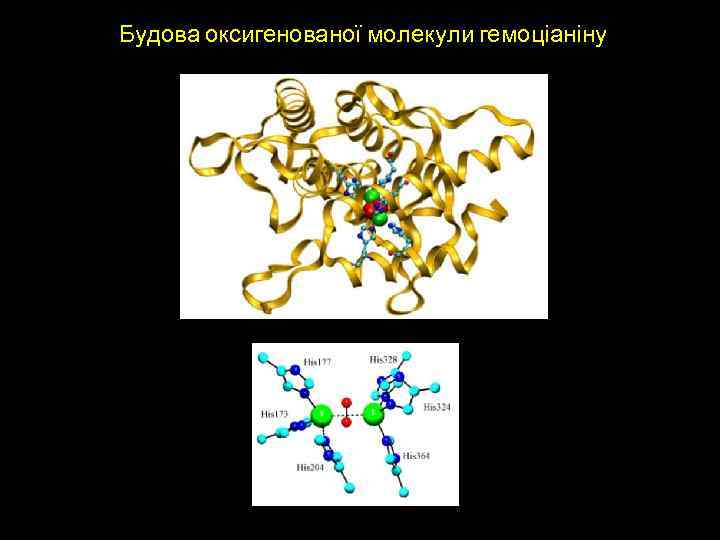
Будова оксигенованої молекули гемоціаніну

Типи металопротеїдів та будова активного центру (тип IIІ) Білок Метал Місця зв’язування Прим. III тип Оксиміоглобін Fe 4 N(порфірин), Nim(His-F 8), O 2 PCA Карбоксиміоглобін Fe 4 N(порфірин), Nim(His-F 8), CO PCA Цитохром с Fe 4 N(порфірин), Nim(His-18), S(Met-80) PCA Каталаза Fe 4 N(порфірин), O(Tyr)? , H 2 O? Nim(His)? Пероксидаза Fe 4 N(порфірин), Nim(His)? Кофермент В 12 Cо 4 N(корин), N(бензымыдазол), С(аденозин) РСА
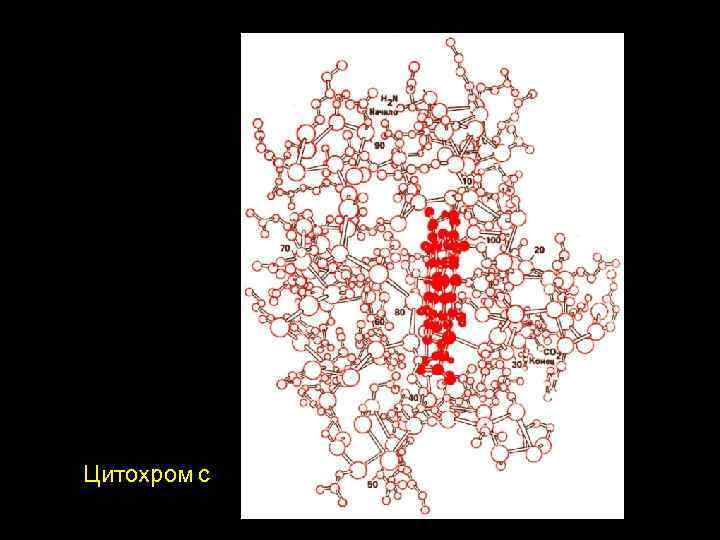
Цитохром с
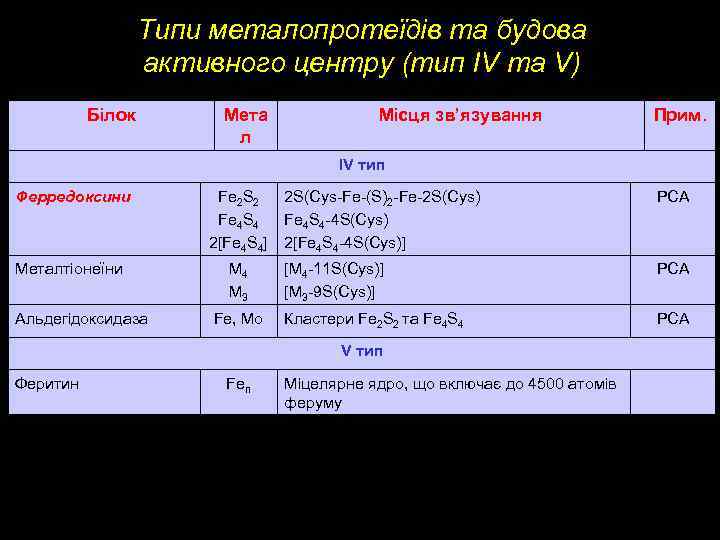
Типи металопротеїдів та будова активного центру (тип ІV та V) Білок Мета л Місця зв’язування Прим. IV тип Ферредоксини Fe 2 S 2 Fe 4 S 4 2[Fe 4 S 4] Металтіонеїни M 4 M 3 Альдегідоксидаза Fe, Mo 2 S(Cys-Fe-(S)2 -Fe-2 S(Cys) Fe 4 S 4 -4 S(Cys) 2[Fe 4 S 4 -4 S(Cys)] PCA [M 4 -11 S(Cys)] [M 3 -9 S(Cys)] PCA Кластери Fe 2 S 2 та Fe 4 S 4 PCA V тип Феритин Fen Міцелярне ядро, що включає до 4500 атомів феруму
![[4 Fe-4 S] ферредоксини - невеликі (6 -12 k. Da) протеїни, що беруть участь [4 Fe-4 S] ферредоксини - невеликі (6 -12 k. Da) протеїни, що беруть участь](https://present5.com/presentation/122040564_46064882/image-69.jpg)
[4 Fe-4 S] ферредоксини - невеликі (6 -12 k. Da) протеїни, що беруть участь у різноманітних окисно-відновних реакцій в живих системах. Вони містять 1 або 2 активних кластери типу Fe 3 S 41+/0 або Fe 4 S 42+/1+, де атоми феруму звязані із залишками протеїну.

Що необхідно знати ? - Природа металу - Число атомів металу в центрі - Ступені окиснення та спіновій стан металу - Геометрія координаційного вузла - Число і типи лігандів - Якомога точні величини довжин зв’язків метал-ліганд - Локалізація металоцентра у білку - Взаємодія між металоцентрами у багатоядерних білках

Існуючі теорії каталітичної активності металоферментів - Концепція ентатичного (напруженого) стану - Теорія індукованої відповідності - Теорія електронно-конформаційних взаємодій -швидка зміна електронного стану активного центру -релаксація макромолекули до рівноважного стану

Роль металу у ферментах Кислота Льюїса (суперкислотний каталізатор) (реакції гідролізу та переносу груп) Переносчик електронів (окисно-відновні реакції)
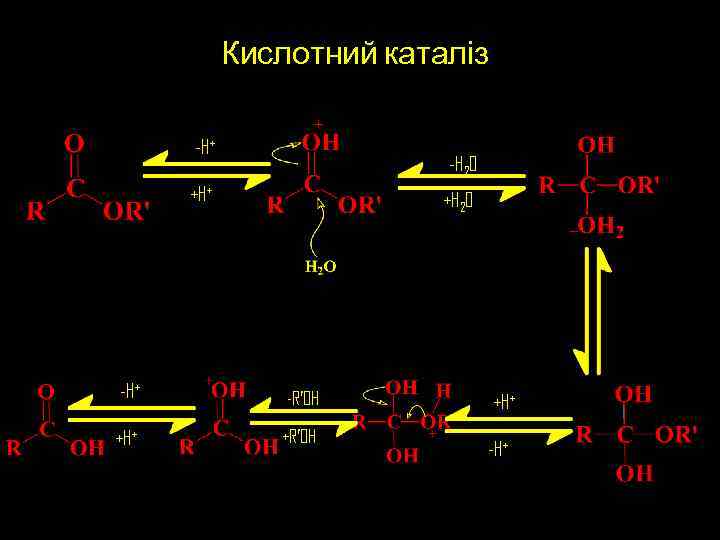
Кислотний каталіз -H+ -H 2 O +H+ +H 2 O -H+ -R’OH +H+ +R’OH +H+ -H+
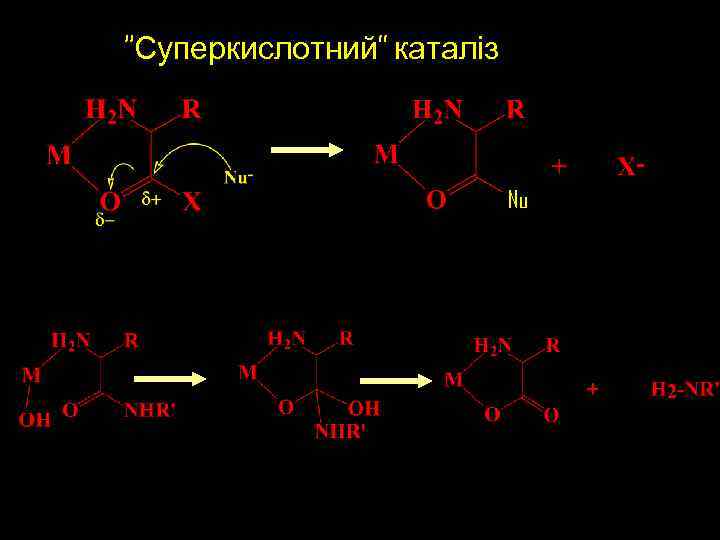
“Суперкислотний” каталіз Nu
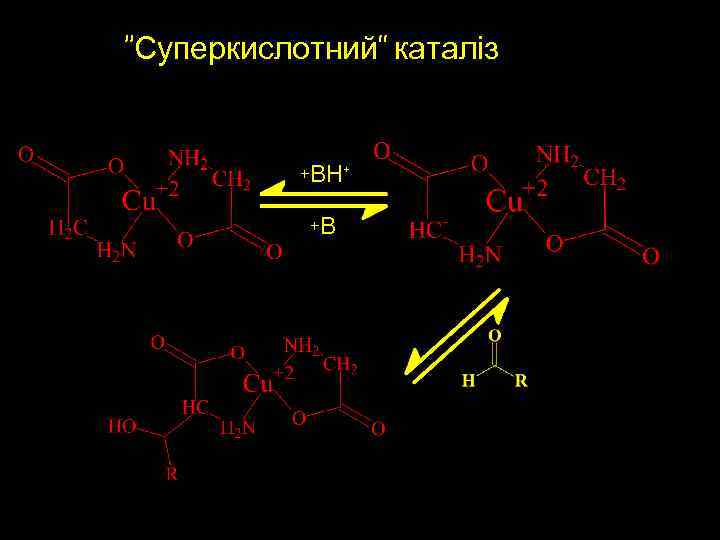
“Суперкислотний” каталіз +ВН+ +В
Amino acids and proteins.ppt