круговороты- N-P-S.ppt
- Количество слайдов: 66

Биогеохимический круговорот азота

Пулы азота: В почве и воде: органический N, NH 4+ (NH 3), NO 2 -, NO 3 В атмосфере: N 2 NH 3 N 2 О NO NO 2 NO 3 -

Энергетические характеристики основных реакций круговорота азота Реакции Выход энергии, ккал ДЕНИТРИФИКАЦИЯ 1. C 6 H 12 O 6+6 KNO 3 6 CO 2+3 H 2 O+6 KOH+3 N 20 545 (на 1 моль глюкозы) 2. 5 C 6 H 12 O 6+24 KNO 3 30 CO 2+18 H 2 O+24 KOH+12 N 2 570 (на 1 моль глюкозы) 3. 5 S+6 KNO 3+2 Ca. CO 3 3 K 2 SO 4+2 Ca. SO 4+ 2 CO 2+3 N 2 132 (на 1 моль серы) ДЫХАНИЕ 4. C 6 H 12 O 6+6 O 2 6 CO 2+6 H 2 O 686 АММОНИФИКАЦИЯ 5. CH 2 NH 2 COOH+1½O 2 2 CO 2+H 2 O+NH 3 глицин 176 НИТРИФИКАЦИЯ 6. NH 3+1½O 2 HNO 2+H 2 O 7. KNO 2+1½O 2 KNO 3 66 17, 5 ФИКСАЦИЯ АЗОТА 8. N 2 2 N «активация азота» 9. 2 N+3 H 2 2 NH 3 -160 12, 8

Распределение азота в различных резервуарах Земли Млн. т Резервуары РАСТИТЕЛЬНАЯ БИОМАССА (наземная) ЖИВОТНАЯ БИОМАССА (наземная) ОПАД (наземный) ПОЧВА -органическое вещество -нерастворимый неорганический -микроорганизмы 1, 1 -1, 4 х104 2 х102 1, 9 -3, 3 х103 3, 0 х105 1, 6 х104 5, 0 х102 ПОРОДЫ ОСАДКИ УГОЛЬНЫЕ ОТЛОЖЕНИЯ 1, 9 х1011 (1) 4, 0 х108 (3) 1, 2 х105 ОКЕАН растительная биомасса животная биомасса мертвое органическое вещество N 2 (растворенный) NO 3 NH 4+ 3, 0 х102 1, 7 х102 5, 3 х105 2, 2 х107 (4) 5, 7 х105 7, 0 х103 АТМОСФЕРА N 2 O NH 3, NOх, NO 3 -, органический N 3, 9 х109 (2) 1, 3 х103 3 -4 (Tamm, 1991)

Активация азота в биосфере: Биологическая фиксация: § фиксация свободноживущими м/о § симбиотическая § ассоциативная Промышленная: § производство удобрений § производство иных продуктов химии § промышленные выбросы § выбросы транспорта Природные поступления (молнии)

Круговорот азота в биосфере (баланс) Приход (Tg N) Фиксация в атмосфере (электрические разряды) Биологическая фиксация Расход (Tg N) 1 -30 Денитрификация 80 -720 45 -330 Речной сток Техногенная фиксация 110130 Сжигание ископаемого топлива 10 -40 15 -45 ВСЕГО: 171535 ВСЕГО: 90 -760
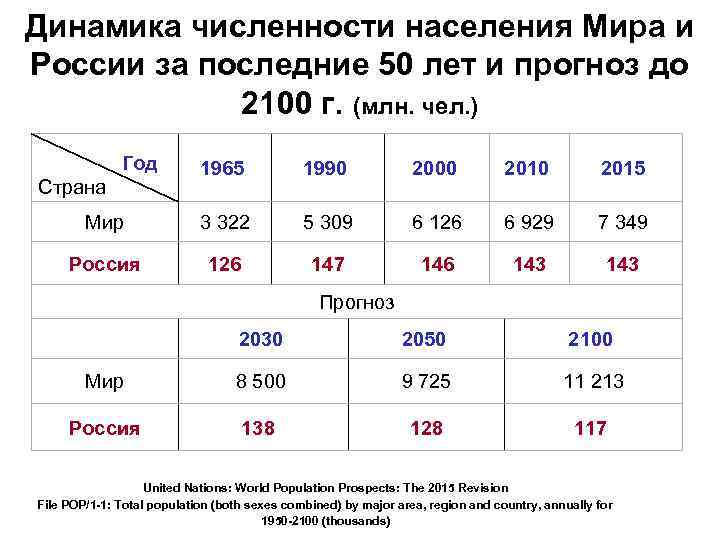
Динамика численности населения Мира и России за последние 50 лет и прогноз до 2100 г. (млн. чел. ) Год Страна 1965 1990 2000 2015 Мир 3 322 5 309 6 126 6 929 7 349 Россия 126 147 146 143 Прогноз 2030 2050 2100 Мир 8 500 9 725 11 213 Россия 138 128 117 United Nations: World Population Prospects: The 2015 Revision File POP/1 -1: Total population (both sexes combined) by major area, region and country, annually for 1950 -2100 (thousands)
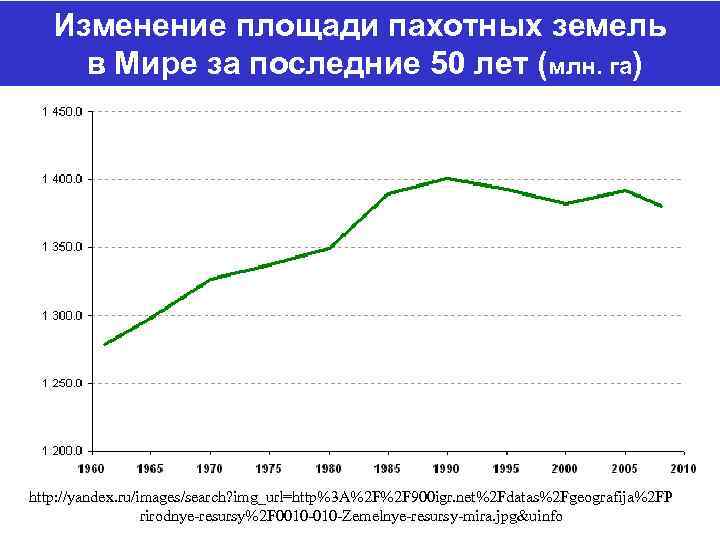
Изменение площади пахотных земель в Мире за последние 50 лет (млн. га) http: //yandex. ru/images/search? img_url=http%3 A%2 F%2 F 900 igr. net%2 Fdatas%2 Fgeografija%2 FP rirodnye-resursy%2 F 0010 -Zemelnye-resursy-mira. jpg&uinfo
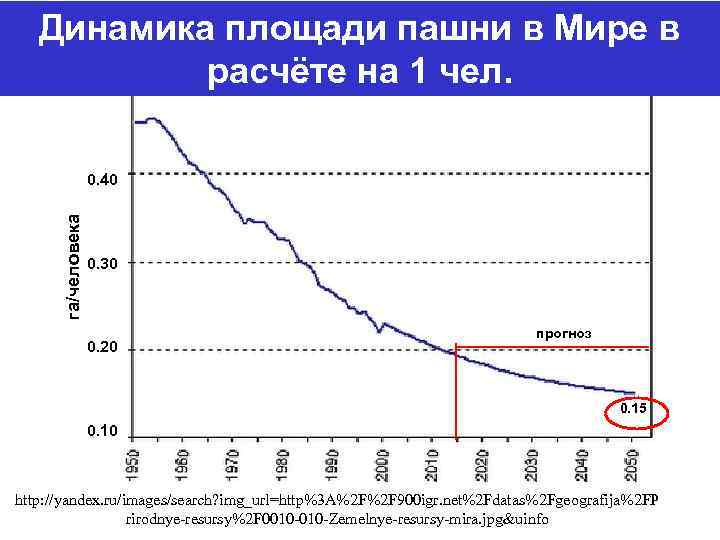
Динамика площади пашни в Мире в расчёте на 1 чел. га/человека 0. 40 0. 30 0. 20 прогноз 0. 15 0. 10 http: //yandex. ru/images/search? img_url=http%3 A%2 F%2 F 900 igr. net%2 Fdatas%2 Fgeografija%2 FP rirodnye-resursy%2 F 0010 -Zemelnye-resursy-mira. jpg&uinfo
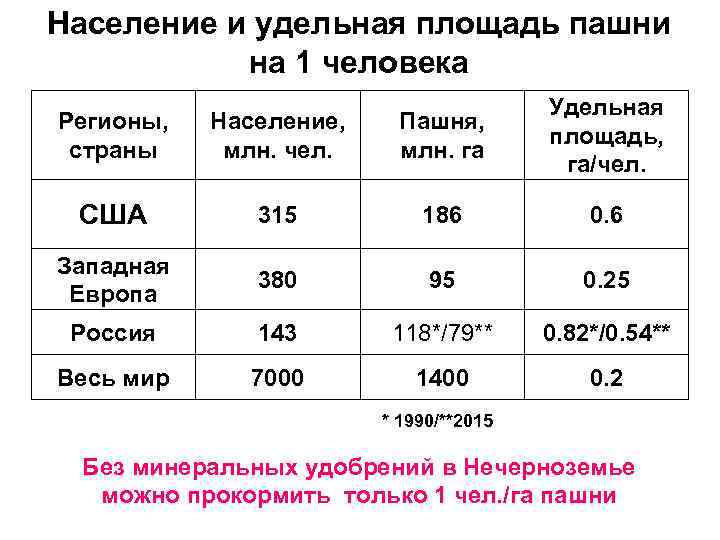
Население и удельная площадь пашни на 1 человека Регионы, страны Население, млн. чел. Пашня, млн. га Удельная площадь, га/чел. США 315 186 0. 6 Западная Европа 380 95 0. 25 Россия 143 118*/79** 0. 82*/0. 54** Весь мир 7000 1400 0. 2 * 1990/**2015 Без минеральных удобрений в Нечерноземье можно прокормить только 1 чел. /га пашни

Потребность в азоте Потребность населения в протеине 60 -70 г/чел. /день или 4 кг N/чел. /год Потребность в Nуд. рассчитывается исходя из равного количества потребляемого протеина (животного и растительного) 50% и 15% - коэффициенты усвоения, соответственно. Nуд. – потребность = 17 кг N/чел. /год Для населения 140 млн. человек – 2, 4 млн. т N уд. Каждый гектар пашни России должен получать не менее 60 кг N/год

Удобрения
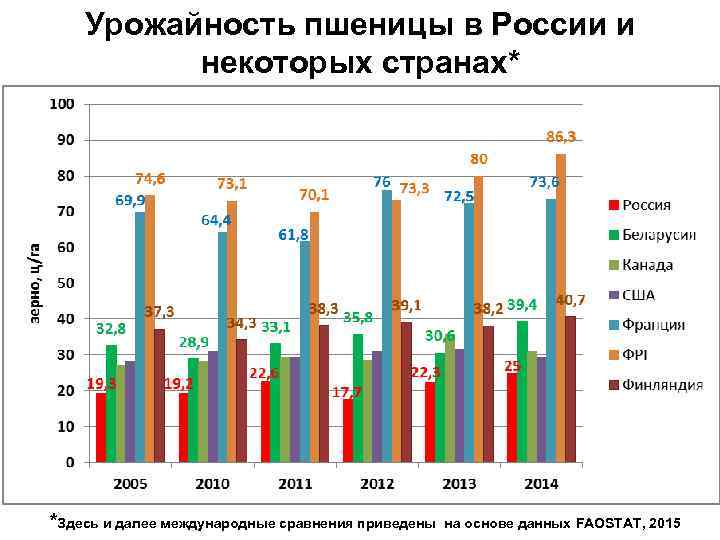
Урожайность пшеницы в России и некоторых странах* *Здесь и далее международные сравнения приведены на основе данных FAOSTAT, 2015
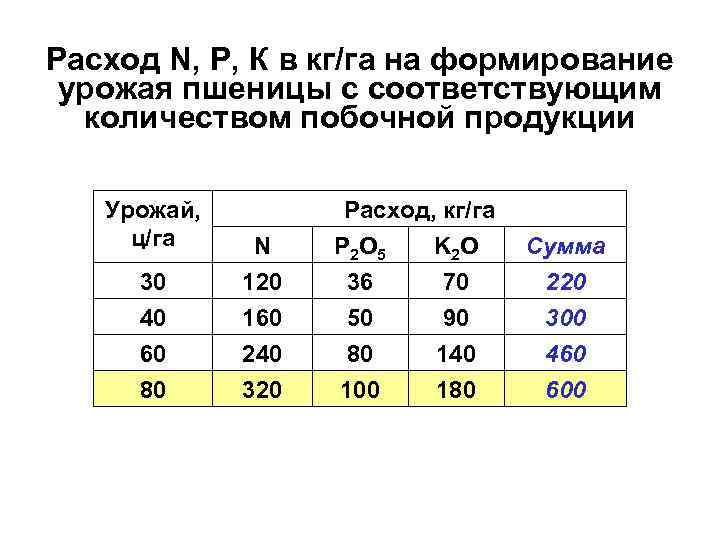
Расход N, Р, К в кг/га на формирование урожая пшеницы с соответствующим количеством побочной продукции Урожай, ц/га 30 40 N 120 160 Расход, кг/га P 2 О 5 K 2 О Сумма 36 70 220 50 90 300 60 80 240 320 80 100 140 180 460 600
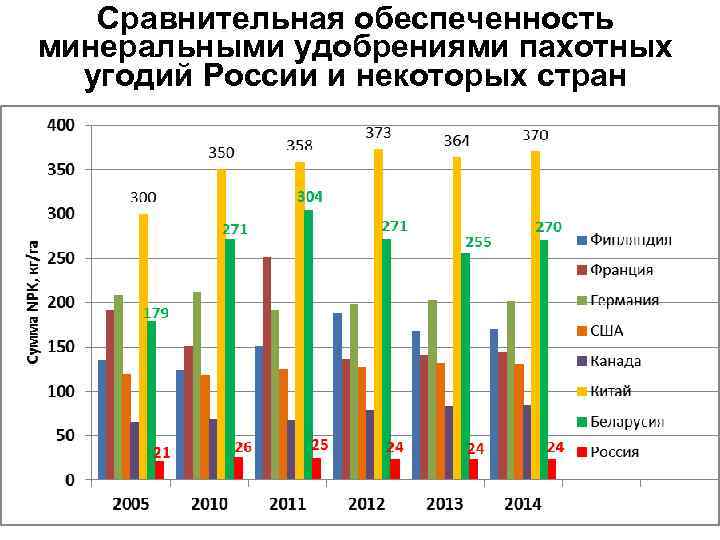
Сравнительная обеспеченность минеральными удобрениями пахотных угодий России и некоторых стран
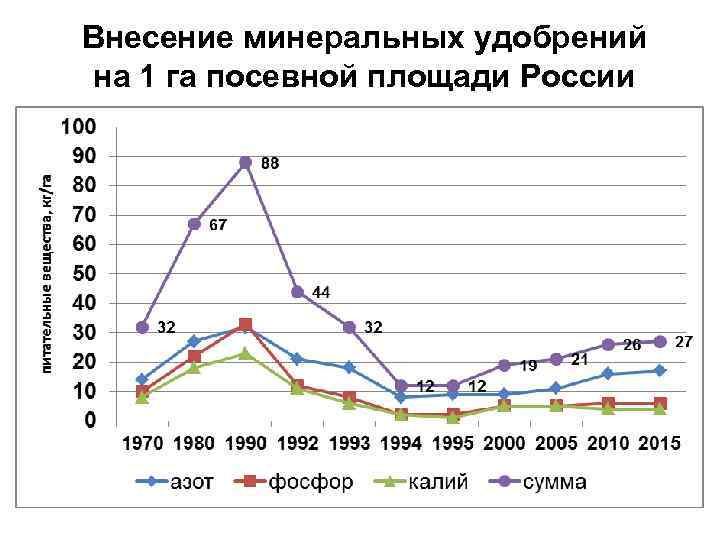
Внесение минеральных удобрений на 1 га посевной площади России
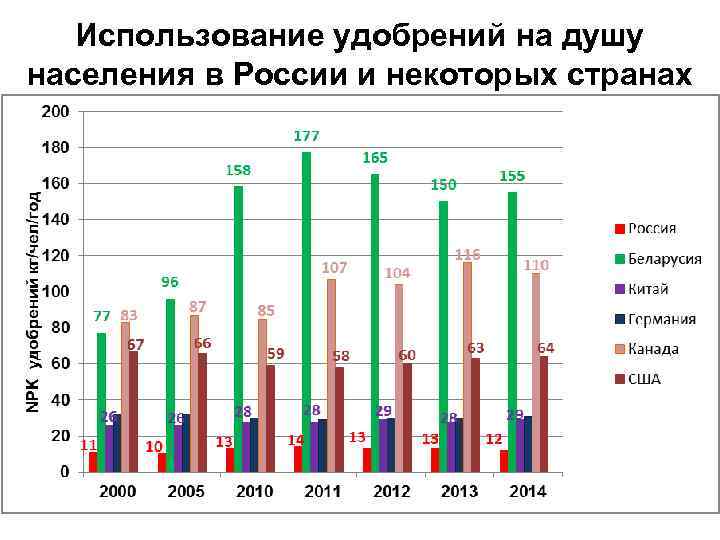
Использование удобрений на душу населения в России и некоторых странах
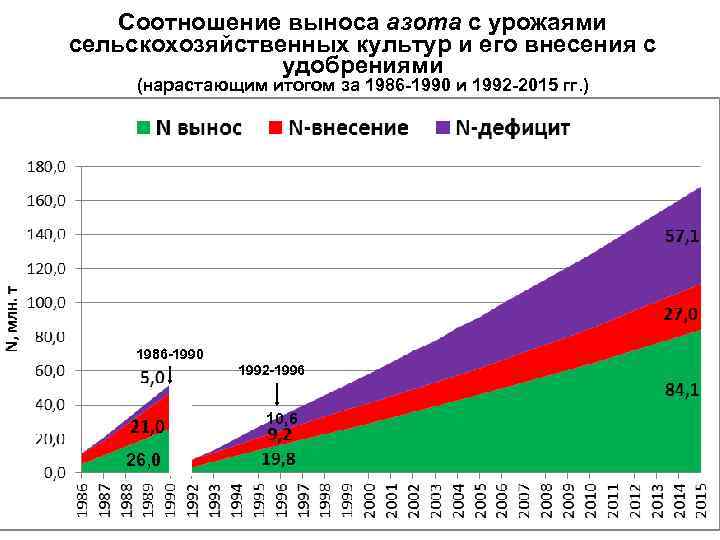
Соотношение выноса азота с урожаями сельскохозяйственных культур и его внесения с удобрениями (нарастающим итогом за 1986 -1990 и 1992 -2015 гг. ) 1986 -1990 1992 -1996 10, 6 26, 0
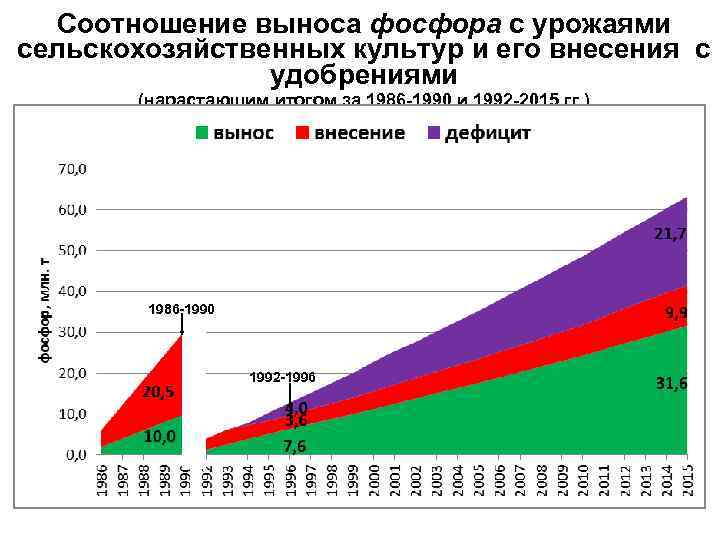
Соотношение выноса фосфора с урожаями сельскохозяйственных культур и его внесения с удобрениями (нарастающим итогом за 1986 -1990 и 1992 -2015 гг. ) 1986 -1990 1992 -1996
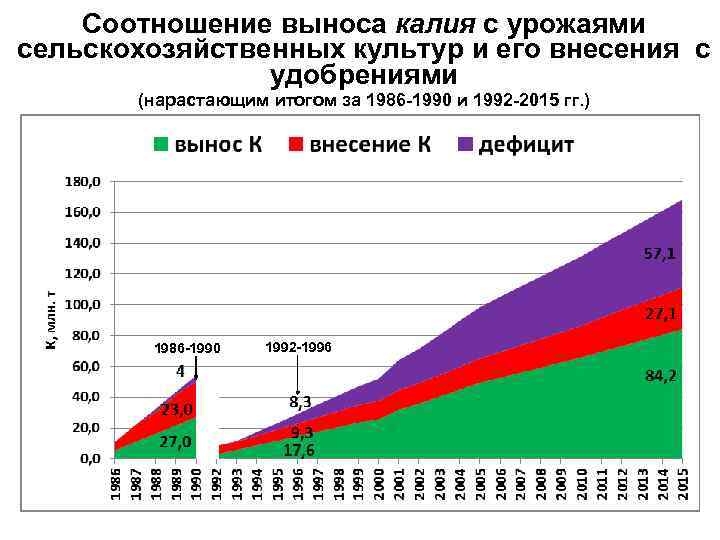
Соотношение выноса калия с урожаями сельскохозяйственных культур и его внесения с удобрениями (нарастающим итогом за 1986 -1990 и 1992 -2015 гг. ) 1986 -1990 1992 -1996
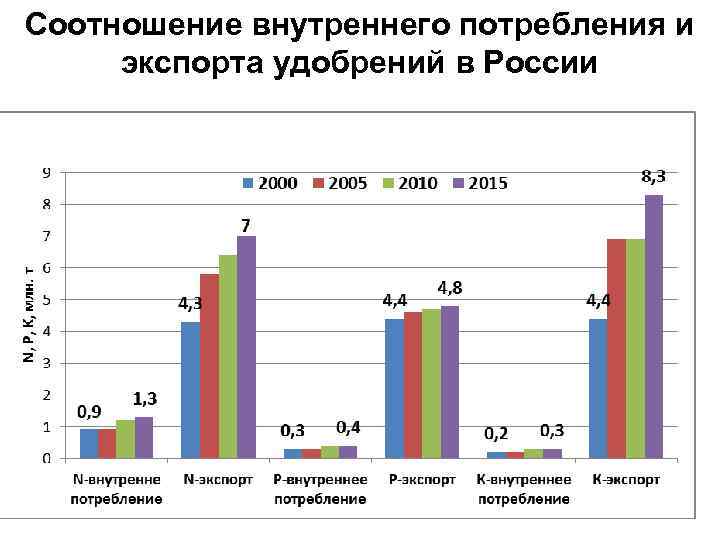
Соотношение внутреннего потребления и экспорта удобрений в России
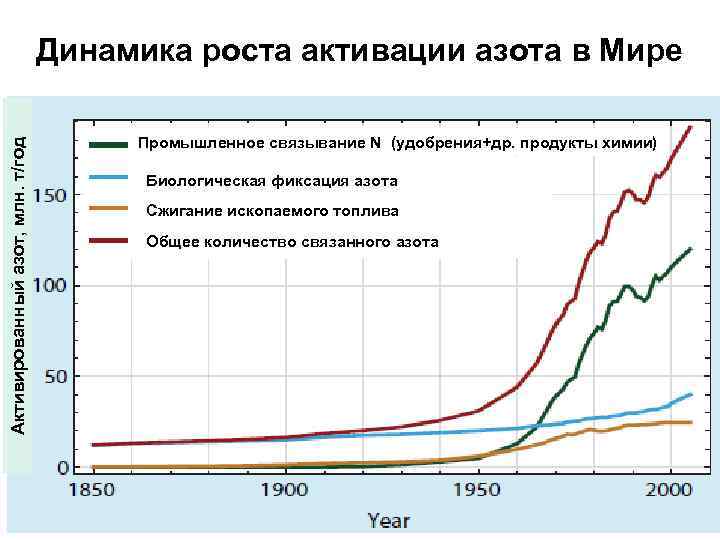
Активированный азот, млн. т/год Динамика роста активации азота в Мире Промышленное связывание N (удобрения+др. продукты химии) Биологическая фиксация азота Сжигание ископаемого топлива Общее количество связанного азота
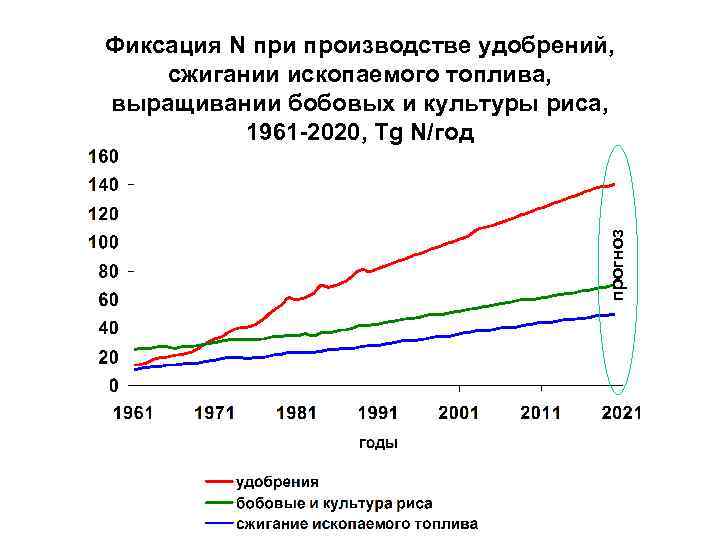
прогноз Фиксация N при производстве удобрений, сжигании ископаемого топлива, выращивании бобовых и культуры риса, 1961 -2020, Tg N/год

Экологические последствия интенсивного вовлечения техногенного азота в круговорот

Потоки азота при сжигании ископаемого топлива Выбросы: NOx, NH 3 Последствия: 1. 2. 3. 4. Фотохимический смог Кислотные атмосферные осадки Разрушение озонового слоя Парниковый эффект

Выбросы NOx Мобильные источники: легковые автомобили тяжелые автомобили и авиация 6 -7 млн. т/год 2 -3 млн. т/год Химическая промышленность (без удобрений) и производство цемента Сжигание древесины и растительных остатков 2 -3 млн. т. /год 5 млн. т/год

Нитраты (NO 3 -) • Нитраты (NO 3 -) - не токсичны! • Нитриты (NO 2 -) консерванты против ботулизма • NO 3 - - используется для лечения мочекаменной болезни, болезней сердца • Растворяет почечные камни фосфатной природы. • Дозировка до 9 г Na. NO 3 или NH 4 NO 3 в сутки - без каких-либо осложнений.

Метгемоглобинемия или синдром «синего ребенка» У детей младше 1 года в желудке NO 3 - NO 2 - Оксигемоглобин, содержит (Fe+++) в окисной форме переходит в метгемоглобин (Fe++) в закисной форме В результате снижается способность переносить О 2
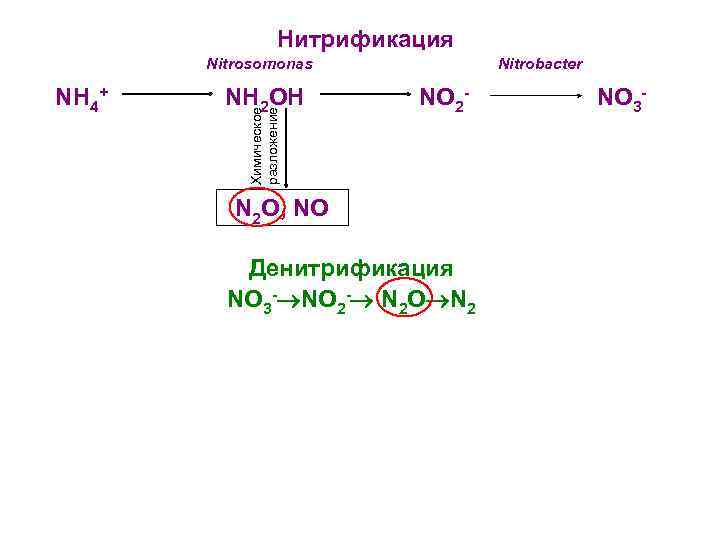
Нитрификация Nitrosomonas Nitrobacter Химическое разложение NH 4+ NH 2 OH NO 2 - NO 3 - N 2 O, NO Денитрификация NO 3 - NO 2 - N 2 O N 2
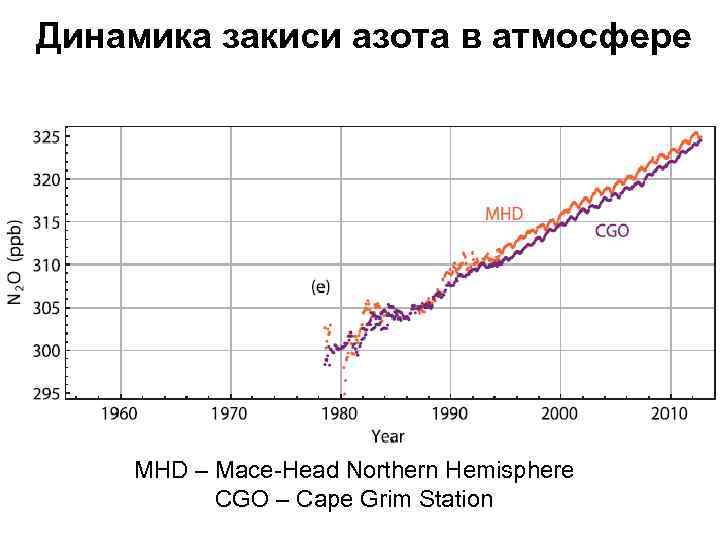
Динамика закиси азота в атмосфере MHD – Mace-Head Northern Hemisphere CGO – Cape Grim Station
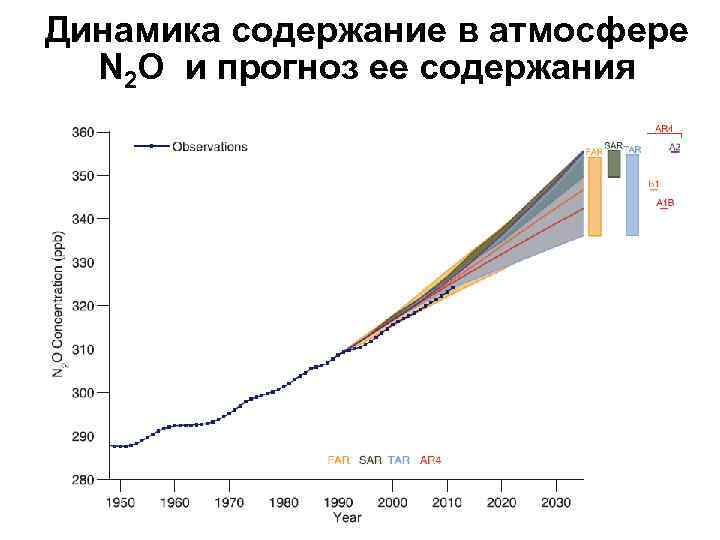
Динамика содержание в атмосфере N 2 O и прогноз ее содержания
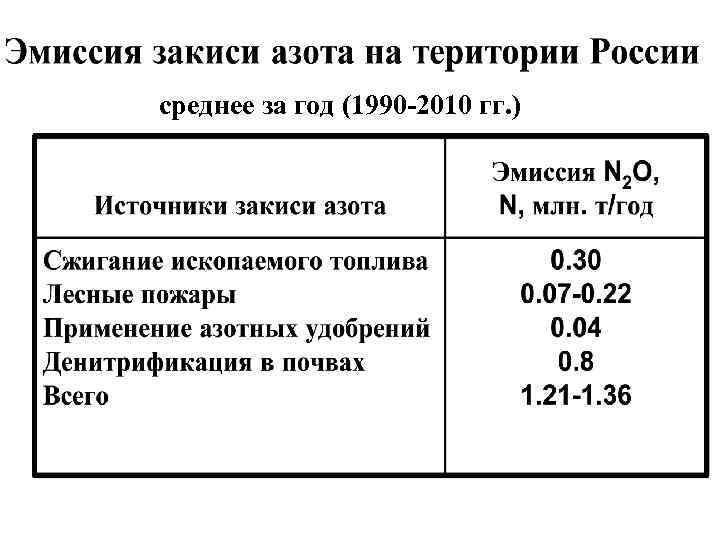
среднее за год (1990 -2010 гг. )
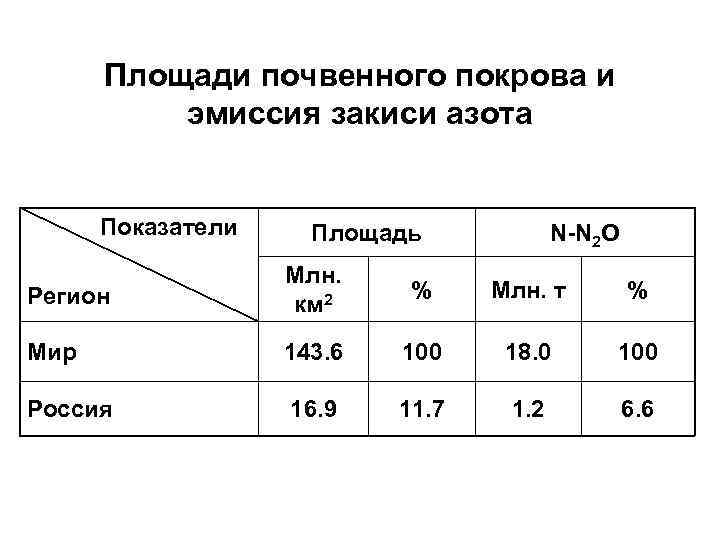
Площади почвенного покрова и эмиссия закиси азота Показатели Площадь N-N 2 O Регион Млн. км 2 % Млн. т % Мир 143. 6 100 18. 0 100 Россия 16. 9 11. 7 1. 2 6. 6

Разрушение озона В стратосфере N 2 O N 2+О (90% фотодиссоциация) N 2 O+O 2 NO и/или N 2+О 2 (∑=10%) NO каталитически разрушает озон: NO+О 3 NO 2+O 2 N 2 O+О NO+O 2 Нетто: O+О 3 2 O 2

Имеются ли в будущем альтернативы применению удобрений? Увеличение использования бобовых или других N- фиксирующих растений (например Azolla в рисовниках) - Ограничено Внедрение N-фиксирующих генов в большинство культур - сложная задача, вероятно не скоро Активация N-фиксации свободноживущих азотфиксаторов - мало надежды для прогресса Усиление ассоциативной азотфиксации большинства культур - может быть определенный эффект, но значительный эффект маловероятен

Биогеохимический круговорот фосфора

Рассмотренные нами круговороты азота и углерода относятся к круговороту газообразных веществ и являются более совершенными, т. е. способные к саморегуляции. В противоположность C, N и S фосфор не улетучивается (хотя РН 3 –фосфин – летучее соединение, но его биосферные потоки не имеют сколько-нибудь значительных атмосферных связей с другими средами). Круговорот фосфора относится к осадочному типу, менее совершенному и менее саморегулируемому

Р – один из важнейших биофильных элементов. Без его участия не могут синтезироваться ни углеводы, ни белки. Р входит в состав АТФ и АДФ, носителей энергии. Фитомассса леса бореального пояса содержит: C – 45 -50%, N – 0. 3 -0. 5% P – 0. 02 -0. 03%.

Позвоночные животные, их мышцы содержат 0. 2% Р, но самое большое содержание Р в скелете. В костях взрослого человека Са 3(РО 4)2 составляет ≈60%, в зубах – 70% Скелет средних размеров взрослого человека содержит 3. 5 кг Са 5(РО 4)3 ОН или 650 г чистого Р. Мы едим каждый день 1. 5 г Р в основном в пище животного происхождения и выбрасываем ≈98% Р в виде Na. NH 4 HPO 4, который удаляется со сточными водами

Путь вовлечения фосфора в круговорот начинается с растворения Р-содержащей горной породы Са 5(РО 4)3 F (фторапатит). В промышленности – кислотная переработка фосфатного сырья – один из самых распространенных способов вовлечения фосфора в современный биогеохимический круговорот.

Фосфорные удобрения – представляют собой конечный продукт переработки фосфатного сырья. Н 3 РО 4 – производные: одно-, ди-, и трехзамещенные соли. Производят также и триполифосфат Na 5 P 3 O 10, используемый в основном для производства детергентов. Внедрение в природный цикл Р синтетических воднорастворимых Р-соединений началось с середины 19 -го века, когда в Англии впервые было начато производство суперфосфата из костей.

В масштабе времени цивилизаций (1000 лет) основной цикл Р представляет собой однонаправленные потоки, с суши в океан. Возврат - очень малый (гуано, рыба). В геологическом масштабе времени первичные неорганические Р-потоки движутся ступенчато, с медленным распространением по морскому дну фосфорсодержащих осадков, имеющих в большей части эрозионное происхождение. Р-содержащие соединения могут возвращаться на сушу только после тектонических подъемов после 107 -109 лет.

Органические соединения фосфора в почве имеют очень короткое время оборота, порядка 0. 1 -1. 0 год. После минерализации Р опять может очень быстро включаться в биологический круговорот. Аналогично короткий биологический круговорот фосфора имеет место и в водной среде. Обмен может осуществляться также между осадками и водной биотой. Человек изменяет скорость и направленность круговорота Р. Добыча полезных ископаемых также как и сведение лесов и лугов, распашка земель усиливает поток Р сторону моря. Возврат Р из моря на сушу в виде гуано птиц До середины 19 века гуано было единственным Рудобрением, которое собирали на птичьих базарах Гуано – уже не имеет практического значения

ПУЛЫ И ПОТОКИ фосфора В СОВРЕМЕННОМ ПРЕДСТАВЛЕНИИ Около 9/10 всех разведанных запасов Р-сырья находится в осадочных породах морского происхождения. Остальное (1/10) – в изверженных породах (апатиты). США и Мароко – являются одними из основных производителей фосфатного сырья. Месторождения в России (Хибинские аппатиты, Егорьевские фосфориты и др. ) Разведанные резервы Р-сырья оцениваются не менее, чем в 20 Рg, общие запасы оцениваются в 90 Pg. Ежегодная добыча фосфатного сырья ≈ 150 Tg или 20 Tg Р, 80% этого сырья идет на удобрение

Потребность в фосфоре Для нормального функционирования организма взрослого человека необходимо каждый день поступление с пищей (в основном животного происхождения) 1. 5 г Р или 550 г Р/год. Из этого количества из организма выбрасывается ≈98% Р в виде Na. NH 4 HPO 4, который необратимо теряется со сточными водами. Для удовлетворения общей годовой потребности населения (143 млн. чел. ) в пищевом фосфоре в продуктах питания должно содержаться не менее 75 тыс. т Р. С учетом коэффициентов усвоения с/х культурами Р удобрений и коэффициентов перевода с/х продукции в продукты питания потребность в фосфатных удобрениях составляет не менее 1. 5 млн. т Р 2 О 5/год или 20 кг Р 2 О 5/га/год/.

ФОСФОР В СЕЛЬСКОМ ХОЗЯЙСТВЕ Средние урожаи зерна выносят 15 -35 кг Р/га. Овощные и плодовые – 5 -15 кг Р/га. Общее содержание Р в сельскохозяйственной продукции мира – 11 12 Тg/год. Единственный источник поступления Р в почвы – удобрения. Мировая потребность в Р-удобрениях – 18 Тg/год при коэффициенте утилизации фосфора не менее 65%. До начала применения Р-удобрений, производимых из фосфатного сырья, внедрение человека в фосфатный цикл было очень ограничено. Рециклирование Р применении местных удобрений (навоз, компосты, зола) возможно не более 20% от общей потребности.
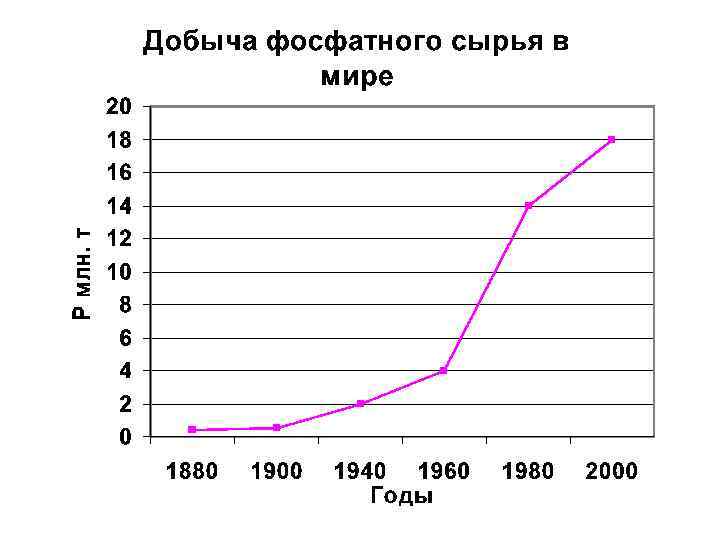
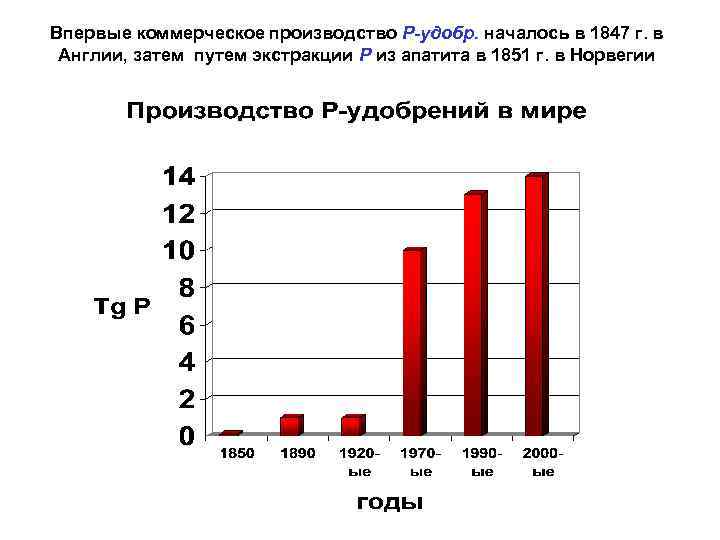
Впервые коммерческое производство Р-удобр. началось в 1847 г. в Англии, затем путем экстракции Р из апатита в 1851 г. в Норвегии
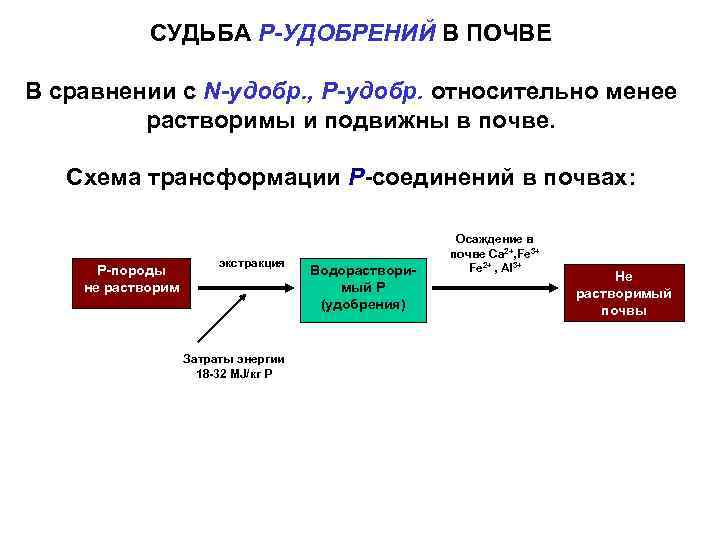
СУДЬБА Р-УДОБРЕНИЙ В ПОЧВЕ В сравнении с N-удобр. , Р-удобр. относительно менее растворимы и подвижны в почве. Схема трансформации Р-соединений в почвах: Р-породы не растворим экстракция Затраты энергии 18 -32 MJ/кг Р Водорастворимый Р (удобрения) Осаждение в почве Ca 2+, Fe 3+ Fe 2+ , Al 3+ Не растворимый почвы
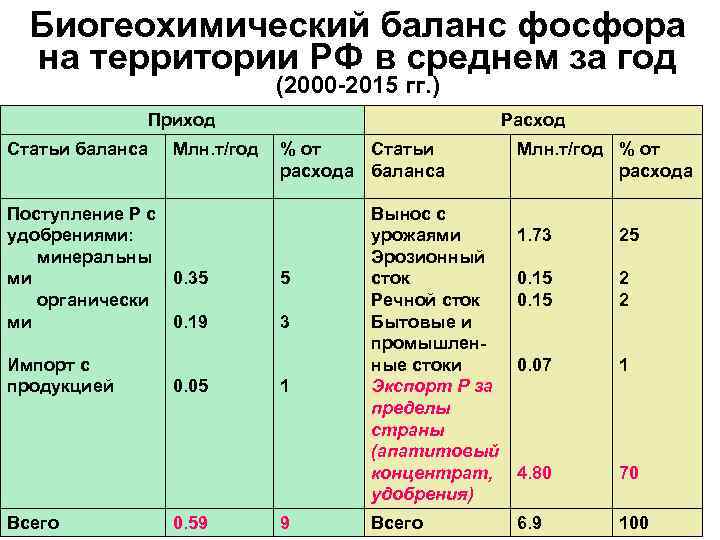
Биогеохимический баланс фосфора на территории РФ в среднем за год (2000 -2015 гг. ) Приход Статьи баланса Млн. т/год Поступление Р с удобрениями: минеральны ми 0. 35 органически ми 0. 19 Импорт с продукцией Всего 0. 05 0. 59 Расход % от Статьи расхода баланса 5 3 1 9 Вынос с урожаями Эрозионный сток Речной сток Бытовые и промышленные стоки Экспорт Р за пределы страны (апатитовый концентрат, удобрения) Всего Млн. т/год % от расхода 1. 73 25 0. 15 2 2 0. 07 1 4. 80 70 6. 9 100

ПРОБЛЕМА ФОСФОРА В ВОДАХ является следствием экстраординарной чувствительности фитопланктона к фосфору. Для поддержания нормальной жизни в водах необходимо благоприятное соотношение C: N: P = 106: 1 Фосфор в большинстве случаев является главным лимитирующим элементом в эвтрофикации водоемов. Повышение концентрации Р в воде неизбежно ведет к сложной перестройке всех взаимоотношений в среде, ведет к мобилизации других питательных элементов.
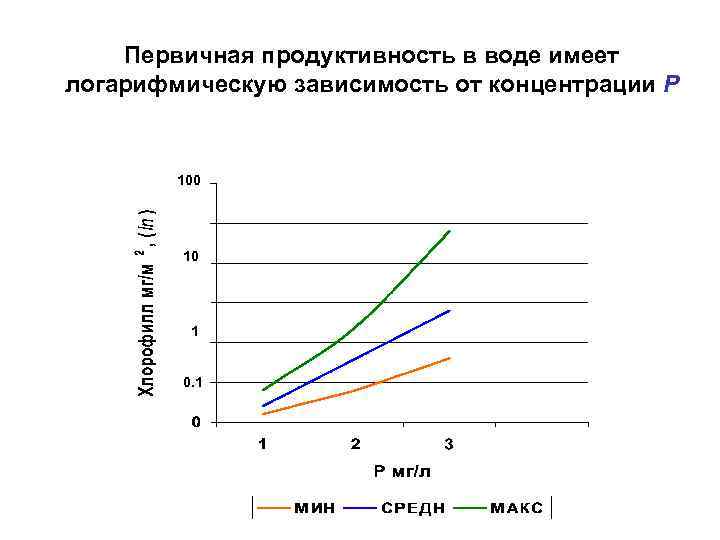
Первичная продуктивность в воде имеет логарифмическую зависимость от концентрации Р 100 10 1 0. 1

Выраженное беспокойство по поводу увеличивающейся эвтрофикации относится к 60 -ым годам прошлого века. • Главным вкладчиком являются фосфорные удобрения. • Полагают, что около 2 -3% от вносимого количества Р с удобрениями подвергается вымыванию. • Такое же количество Р или больше теряется с эрозионным стоком (жидким и твердым). • Применение детергентов на основе полифасфатов

ЭТАПЫ ЭВТРОФИКАЦИИ 1. Медленное увеличение эвтрофикации с момента появления промышленных Р-удобрений и активизации бытовых сбросов, т. е. с 1840 -50 годов в Европе. 2. В Северной Америке это совпало в 1940 -х годах с началом производства фосфатных детергентов и быстрым наращиванием применения Р-удобрений. 3. Связан с экспоненциальным увеличением производства фосфорных удобрений с 1970 -х годов.

ОЧИСТКА СТОКОВ ОТ ФОСФОРА Достигается применением простых химикатов: Fe. Cl 2 , Fe. Cl 3 или Al 2(SO 4)3 или известь, соответственно получают: Fe. PO 4, Al. PO 4, Ca 5(PO 4)3 OH – гидроксилаппатит. СТОИМОСТЬ От 1. 5 до 4. 5 $ /чел.

Биогеохимический круговорот серы

Глобальный биогеохимический цикл серы – целый комплекс химических и биохимических реакций, в которых сера участвует в различных формах с разными физико-химическими свойствами и агрегатными состояниями Газообразные формы серы: H 2 S (сероводород), SO 2 (двуокись серы), SO 3 (триокись серы) Серосодержащие газы образуются как в природе, так и в промышленном производстве

Все серосодержащие газы хорошо растворимы в воде и образуют растворы с ярко выраженными кислотными свойствами В атмосфере H 2 S быстро окисляется до SO 2, который очень реакционен и вступает в реакции окисления, гидратации: SO 2 + 2 H 2 S 2 SO 2 + O 2 3 S + 2 H 2 O 2 SO 3 хорошо растворим в воде с образованием H 2 SO 4, которая ведет себя очень агрессивно, способствуя выветриванию минералов и коррозии металлов.

Большинство сульфатов широко распространено в природе: Ca. SO 4 – ангидрит; Ca. SO 4 H 2 O – гипс Окисленная сера выводится из цикла преимущественно в кальциевых соединениях. Отложения ангидрита и гипса – самые громадные резервуары серы. Сульфиды образуются из водных растворов H 2 S. Большинство сульфидов металлов (за исключением щелочных и щелочеземельных) очень плохо растворимы в воде.

Серосодержащие соединения с металлами меняются в зависимости от окислительно-восстановительных условий: анаэробные аэробные сульфиды сульфаты Окисленные формы, сульфаты металлов, более растворимы и могут вымываться, а сульфиды – плохо растворимы, иммобилизуют металлы. Из всех сульфидов наибольшее распространение имеет сульфид железа – Fe. S 2 или пирит, широко встречаемый в природе. Наряду с элементарной серой пирит используется для производства серной кислоты.

ОБРАЗОВАНИЕ И РАЗЛОЖЕНИЕ S-СОДЕРЖАЩИХ СОЕДИНЕНИЙ В БИОЛОГИЧЕСКИХ ПРОЦЕССАХ Сера входит в состав многих аминокислот и является одним из главных биофильных элементов. Подавляющее большинство растений и микроорганизмов используют реакцию восстановления при ассимиляции сульфатов. Сера затем включается в серосодержащие аминокислоты: цистин, цистеин и метионин.

Другая группа живых организмов (животные и некоторые микроорганизмы) утилизируют серу для своего метаболизма и роста только в виде серосодержащих аминокислот. Некоторые микроорганизмы не ограничиваются только использованием серы из сульфатов, а могут использовать ее из сульфитов и сульфидов. После отмирания биомассы, сера минерализуется с высвобождением либо сульфатов (аэробное разложение) либо сульфидов (анаэробное)

ПОТОК СЕРЫ ЗА СЧЕТ ВЫВЕТРИВАНИЯ ПОРОД, ОБУСЛОВЛЕННОГО ХОЗЯЙСТВЕННОЙ ДЕЯТЕЛЬНОСТЬЮ ЧЕЛОВЕКА Механическое выветривание. Руды и основные породы, которые извлекаются на поверхность Земли с содержанием серы 0. 1% и выше составляют 20 103 Tg/год или 20 Tg S/год. Выветривание, связанное с добычей и сжиганием топлива Во время сжигания органическая и пиритная сера окисляется до SO 2 (94%) или SO 3 (4%)

Содержание S в топливах (%%): Уголь – 1 -14 (уголь из Рура, Донбаса содержит 8 -14% S) Общий пул S в каменном угле оценивается в 20 103 Tg при общих запасах каменного угля 1300 103 Tg. В настоящее время выделение S при сжигании угля 60 -70 Tg/год Нефть Содержит 0. 1 – 3% S Газ Содержит 0. 1 -40% S Эмиссия S при сжигании нефти и газа 20 -25 Tg. S/год

ЭМИССИЯ СЕРЫ В МЕТАЛЛУРГИЧЕСКИХ ПРОИЗВОДСТВАХ Сульфиды присутствуют во всех рудах нежелезных металлов. В некоторых пиритах S 45%. При выплавке меди, цинка, никеля, свинца и др. металлов сульфиды окисляются до SO 2 и выделяются в атмосферу Выделение S в металлургических производствах составляет 10 -29% от количества, выделяемого при сжигании угля, что составляет 10 -20 Tg. S/год

КИСЛОТНЫЕ ДОЖДИ В незагрязненных районах р. Н осадков 5. 7 при 25 о. С В районах с карбонатными почвами, попадание пыли в атмосферу вызывает подщелачивание осадков. В прединдустриальную эпоху р. Н осадков везде был выше 5, 0 В Антарктиде, в снеговом-ледовом профиле пробы имеют р. Н 6. 30 В настоящее время, в индустриальных районах кислотность осадков повысилась в 5 -30 раз по сравнению с незагрязненными районами р. Н осадков в странах Западной и Центральной Европы, а также Восточное побережье США и Ю. В. Канады 4. 0 -4. 5
круговороты- N-P-S.ppt