08 Биохимические процессы.ppt
- Количество слайдов: 17

Биогеохимические процессы Автотроф (литотрофы, Гетеротрофы: продуценты): гелиоавтотрофы (фотосинтез) Биотрофы Редуценты хемоавтотрофы (хемосинтез) (консументы) (бактерии, первичные – травоядные грибы и т. д) вторичные – плотоядные Сапротрофы Трофические цепи - последовательность переноса энергии c пищей от одной группы организмов к другой. Различают пастбищную и детритную Пастбищную трофическая цепь: гелиоавтотрофы → травоядные → хищники 1. Удаляет из окружающей среды и концентрирует в биомассе, т. е. в составе органического вещества C, Si, S, а так же K+, Ca 2+, Mg 2+, и особенно N и P (H 3 PO 4). Азотфиксирующие на 1 г углерода связывают до 20 мг N 2, всего около 10 млн. т в год. 2. Накапливает ежегодно около 4, 67∙ 1011 т O 2. 3. Накапливает и захороняет мертвое органическое вещество: гумус и сапропель. Мертвое органическое вещество + ≈7 мг/л O 2 (Eh 350 -700 м. В, pe 6 - 12).
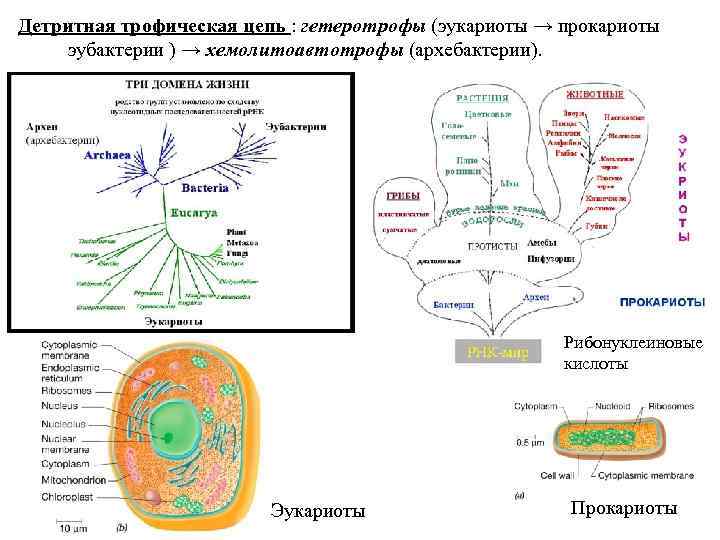
Детритная трофическая цепь : гетеротрофы (эукариоты → прокариоты эубактерии ) → хемолитоавтотрофы (архебактерии). Рибонуклеиновые кислоты Эукариоты Прокариоты
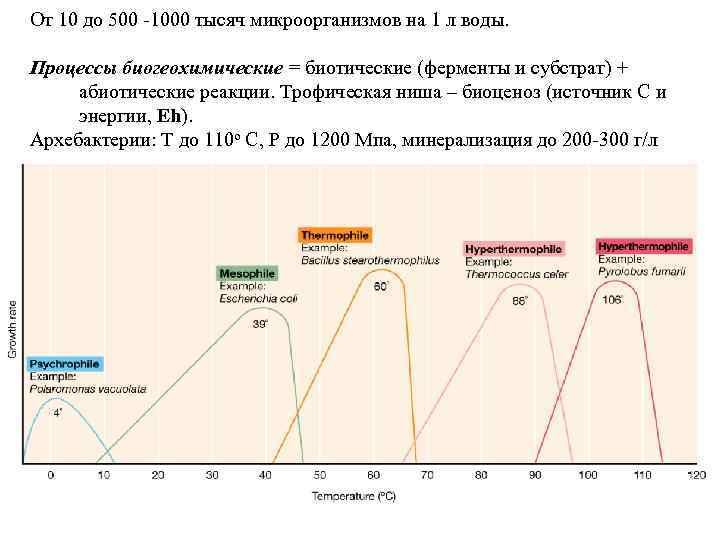
От 10 до 500 -1000 тысяч микроорганизмов на 1 л воды. Процессы биогеохимические = биотические (ферменты и субстрат) + абиотические реакции. Трофическая ниша – биоценоз (источник C и энергии, Eh). Архебактерии: T до 110 o С, P до 1200 Мпа, минерализация до 200 -300 г/л
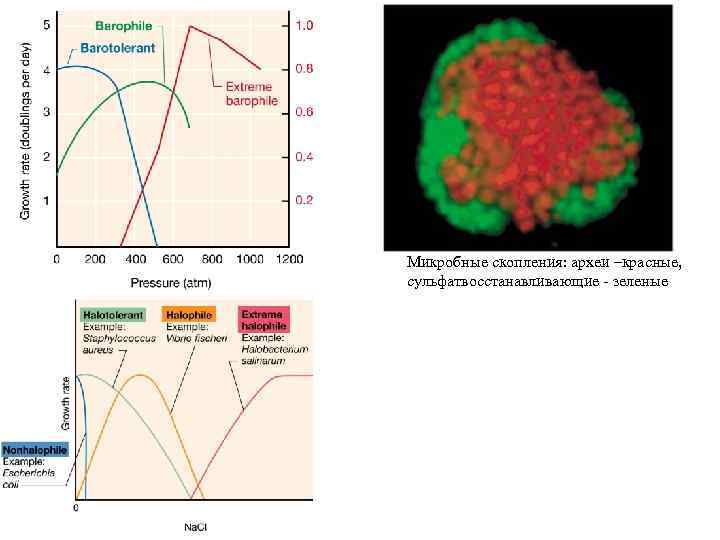
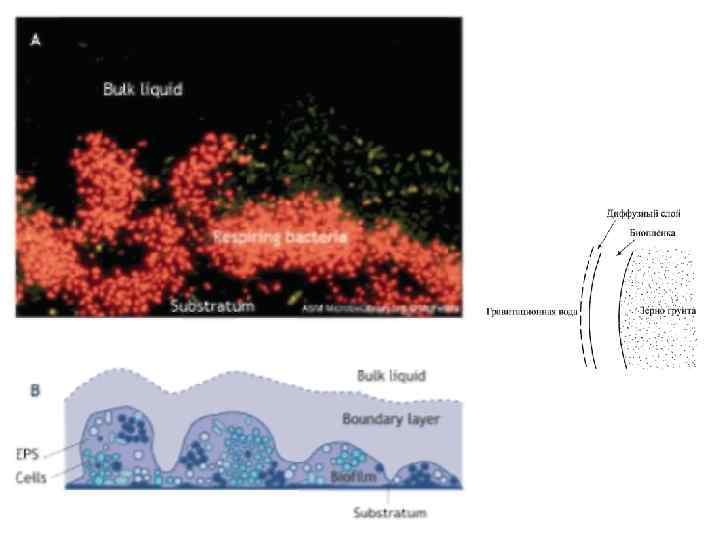
Микробные скопления: археи –красные, сульфатвосстанавливающие - зеленые

Окислительно-восстановительные биогеохимические процессы Действуют коллективно (биоценоз) в разных нишах, т. е. при разных значениях Eh: окислительной, переходной и восстановительной. Окислительная обстановка: Преобладают аэробные гетеротрофы. Расходуется O 2 и накапливаются окисленные формы N, S, Fe и др. (CO 2, HCO 3 -, CO 32 -, NO 3 -, SO 42 -, HPO 42 - и окислы металлов). Переходная окислительно-восстановительная обстановка: Доминируют микроаэрофилы (аэробные, анаэробные). Резкая смена обстановки за счет расхода окисленных форм N, Fe, Mn и др. , S в начале окисляется, в конце восстанавливается. Восстановительная обстановка: Только анаэробы (архибактерии). Расход сульфатов, накопление сульфидов, появление и накопление метана.
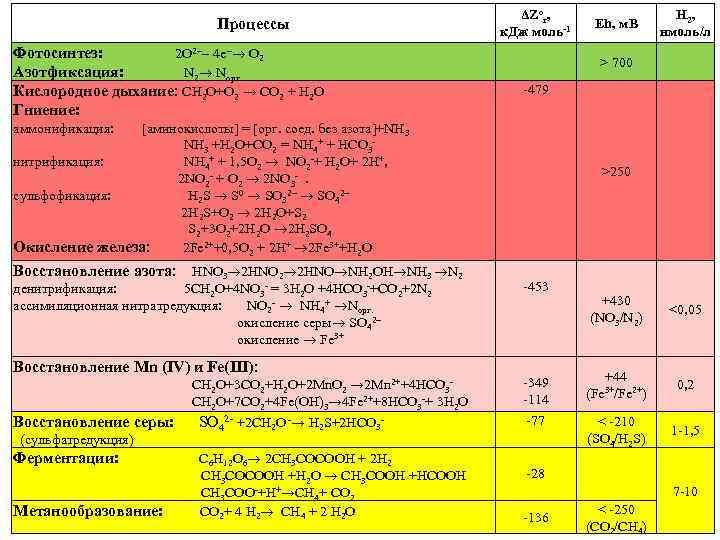
Процессы ΔZor, к. Дж моль-1 Фотосинтез: 2 O 2 4 e O 2 Азотфиксация: N 2 Nорг. Кислородное дыхание: CH 2 O+O 2 → CO 2 + H 2 O Гниение: денитрификация: 5 CH 2 O+4 NO 3 - = 3 H 2 O +4 HCO 3 -+CO 2+2 N 2 ассимиляционная нитратредукция: NO 2 - NH 4+ Nорг. окисление серы SO 42– окисление Fe 3+ Восстановление Mn (IV) и Fe(III): CH 2 O+3 CO 2+H 2 O+2 Mn. O 2 → 2 Mn 2++4 HCO 3 - CH 2 O+7 CO 2+4 Fe(OH)3→ 4 Fe 2++8 HCO 3 -+ 3 H 2 O Восстановление серы: SO 42 - +2 CH 2 O -→ H 2 S+2 HCO 3 (сульфатредукция) Ферментации: C 6 H 12 O 6 2 CH 3 COCOOH + 2 H 2 CH 3 COCOOH +H 2 O CH 3 COOH +HCOOH CH 3 COO-+H+→CH 4+ CO 2 Метанообразование: CO 2+ 4 Н 2 СН 4 + 2 H 2 O H 2, нмоль/л > 700 -479 аммонификация: [аминокислоты] = [орг. соед. без азота]+NH 3 NH 3 +H 2 O+CO 2 = NH 4+ + HCO 3 нитрификация: NH 4+ + 1, 5 O 2 NO 2 -+ H 2 O+ 2 H+, 2 NO 2 - + O 2 2 NO 3 - . сульфофикация: H 2 S S 0 SO 32– SO 42– 2 H 2 S+O 2 2 H 2 O+S 2 S 2+3 O 2+2 H 2 O 2 H 2 SO 4 Окисление железа: 2 Fe 2++0, 5 O 2 + 2 Н+ 2 Fe 3++H 2 O Восстановление азота: HNO 3 2 HNO 2 2 HNO NH 2 OH NH 3 N 2 Eh, м. В >250 -453 -349 -114 -77 +430 (NO 3/N 2) +44 (Fe 3+/Fe 2+) < -210 (SO 4/H 2 S) <0, 05 0, 2 1 -1, 5 -28 7 -10 -136 < -250 (CO 2/CH 4)


Симбиоз Riftia pachyptila и хемолитоавтотрофных серобактерий (CO 2, H 2 S)

Первоначально на поверхности Земли была восстановительная обстановка (избытое e-), в которой процветали анаэробные эубактерии и архебактерии. Они существовали за счет окисления (потери e-) и создали местами окислительную обстановку (дефицит e-). Цианобактерии (цианопрокариоты) способные к фотосинтезу потребляли CO 2 и генерировали O 2. В этих условиях 1, 5— 2 млрд лет назад появились аэробы эукариоты и стали царствовать в симбиозе с фотолитоавтотрофами. Эукариоты в симбиозе с фотолитоавтотрофами создали на поверхности окислительную обстановку. Анаэробные эубактерии и архебактерии спрятались в недрах, где сохранились до наших дней.
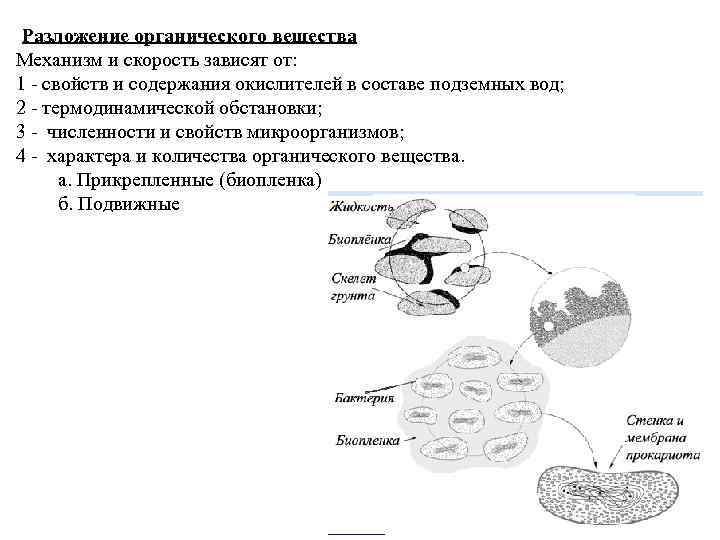
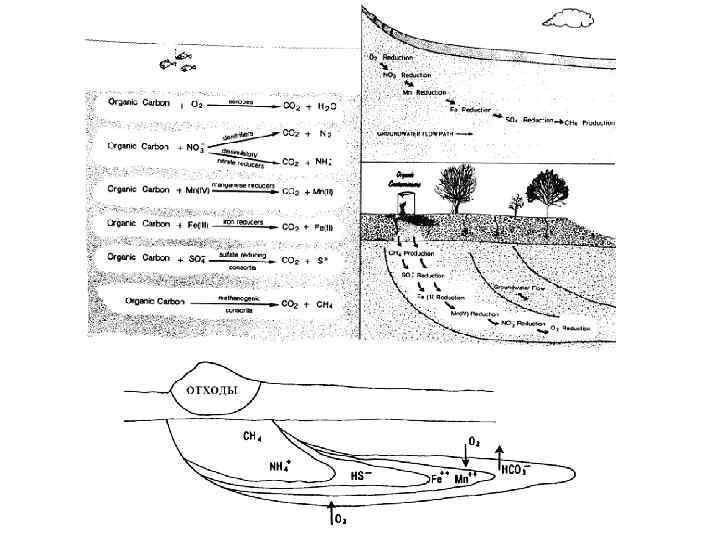
Разложение органического вещества Механизм и скорость зависят от: 1 - свойств и содержания окислителей в составе подземных вод; 2 - термодинамической обстановки; 3 - численности и свойств микроорганизмов; 4 - характера и количества органического вещества. а. Прикрепленные (биопленка) б. Подвижные
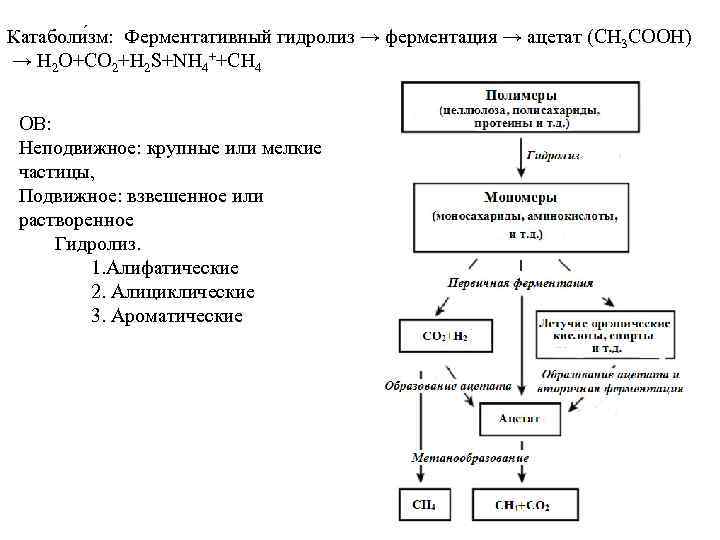
Катаболи зм: Ферментативный гидролиз → ферментация → ацетат (CH 3 COOH) → H 2 O+CO 2+H 2 S+NH 4++CH 4 ОВ: Неподвижное: крупные или мелкие частицы, Подвижное: взвешенное или растворенное Гидролиз. 1. Алифатические 2. Алициклические 3. Ароматические
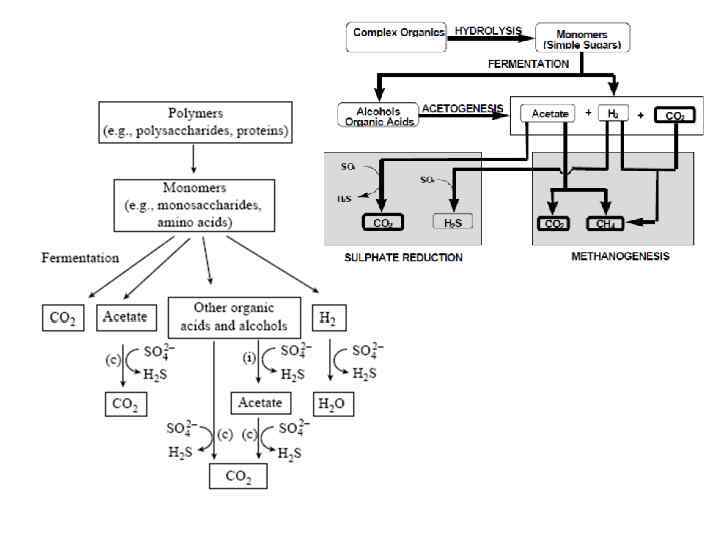

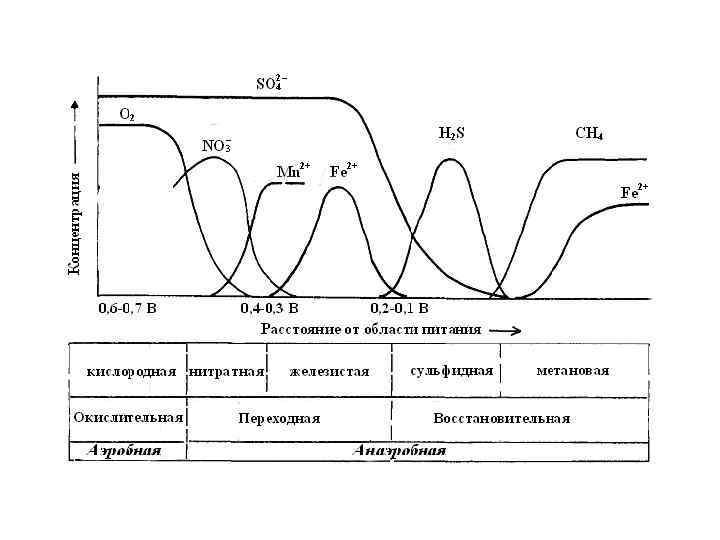
Окислительно-восстановительная зональность 1. Наличие ограниченного содержания O 2 (везде <0, 6 ммоль/л). 2. Наличие ОВ (содержание варьирует в зависимости от климата и растительности) 3. Фильтрация формирует пространственную зональность, которую А. И. Перельман (1916 -1998) в 1972 году назвал окислительно-восстановительной зональностью Концентрации H 2 в осадках в условиях переходной и восстановительной обстановки Образуются более тяжелые вязкие нефти и битумы (мальта, асфальты, асфальтиты, оксикериты, гуминокериты).
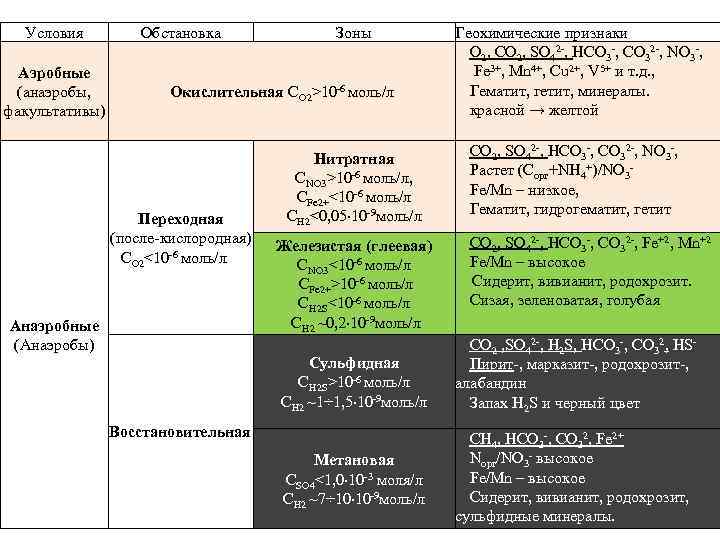
Условия Аэробные (анаэробы, факультативы) Обстановка Зоны Окислительная CO 2>10 -6 моль/л Переходная (после-кислородная) CO 2<10 -6 моль/л Анаэробные (Анаэробы) Нитратная CNO 3>10 -6 моль/л, CFe 2+<10 -6 моль/л CH 2<0, 05 10 -9 моль/л Железистая (глеевая) CNO 3<10 -6 моль/л CFe 2+>10 -6 моль/л CH 2 S<10 -6 моль/л CH 2 ~0, 2 10 -9 моль/л Сульфидная CH 2 S>10 -6 моль/л CH 2 ~1÷ 1, 5 10 -9 моль/л Восстановительная Метановая CSO 4<1, 0 10 -3 моля/л CH 2 ~7÷ 10 10 -9 моль/л Геохимические признаки O 2, CO 2, SO 42 -, HCO 3 -, CO 32 -, NO 3 -, Fe 3+, Mn 4+, Cu 2+, V 5+ и т. д. , Гематит, гетит, минералы. красной → желтой CO 2, SO 42 -, HCO 3 -, CO 32 -, NO 3 -, Растет (Cорг+NH 4+)/NO 3 Fe/Mn – низкое, Гематит, гидрогематит, гетит CO 2, SO 42 -, HCO 3 -, CO 32 -, Fe+2, Mn+2 Fe/Mn – высокое Cидерит, вивианит, родохрозит. Сизая, зеленоватая, голубая CO 2 , SO 42 -, H 2 S, HCO 3 -, CO 32, HS- Пирит-, марказит-, родохрозит-, алабандин Запах H 2 S и черный цвет CH 4, HCO 3 -, CO 32, Fe 2+ Nорг/NO 3 - высокое Fe/Mn – высокое Сидерит, вивианит, родохрозит, сульфидные минералы.
08 Биохимические процессы.ppt