12_Кальций.pptx
- Количество слайдов: 16

Биогеохимические циклы кальция, натрия, калия, фосфора Учение о биосфере Д. Ю. Шишкина Тема 12

Геохимическая характеристика кальция Кальций относится к главным элементам земной коры, его кларк 2, 96%. Содержание элемента уменьшается от глубин к гранитному слою литосферы. В базальтовом слое его концентрация 5, 8%; в гранитном – 2, 7%. Высокое содержание кальция в земной коре обусловливает наличие многочисленных минералов (385), 4 -е место по числу минералов. Из-за своих размеров катион Са+ не может войти в структуру гипергенных силикатов. Поэтому при выветривании и трансформации гипогенных силикатов в глинистые минералы освобождается большое количество этого элемента. Главный металл живого вещества (среднее содержание – 0, 5%). Известны «кальциевые организмы» , содержащие более 10% Ca, строящие свой скелет из Ca. CO 3 (известковые водоросли, многие моллюски, иглокожие, кораллы). В биосфере дифференциация кальция связана с карбонатным равновесием: Ca. CO 3 + H 2 O + CO 2 ↔ Ca 2+ + 2 HCO 3 Поэтому при высоком содержании CO 2 в водах кальций находится в растворе, а при низком – выпадает в осадок в виде кальцита. 2

Кальций в Мировом океане Водорастворимые соединения, гл. обр. , бикарбонат Са(НСО 3)2 поступают в природные воды и мигрируют с ними в океан. Хотя этот процесс развивается на протяжении более 2 млрд. лет, концентрация элемента в океанической воде всего лишь в 30 раз больше по сравнению с водами рек. Это обусловлено ограниченной растворимостью карбоната кальция, а главное – активным поглощением элемента планктонными организмами. Эти процессы способствуют обильному накоплению кальция в составе мощных толщ известняков, доломитов, мергелей, известковых глин и др. Средняя концентрация Са. О в осадочной толще равна 15, 9%. Масса кальция в осадочной оболочке равна 272, 8× 1015 т. Благодаря динамическому равновесию углекислого газа в атмосфере с анионами (НСО 3)- и (СО 3)2 - в океанической воде в океане содержится огромная масса растворенных катионов кальция. Их масса в океане – 5, 6× 1014 т, что на 4 порядка превышает количество элемента, связанного в живом и мертвом органическом веществе планеты. 3

Кальций в живом веществе Кальций играет ответственную роль в физиологии организмов. В растениях он участвует в углеводном и азотном обмене, для животных Са необходим для построения наружного или внутреннего скелета, участвует он также в свертывании крови. Масса кальция, содержащаяся в живом веществе суши, равна (22, 5 -45)× 109 т. Это количество на 3 порядка больше количества кальция, находящегося в биомассе фотосинтетиков океана – 34× 106 т. Масса кальция, содержащаяся в растительных остатках, торфе и гумусе педосферы, равна 15× 109 т, т. е. имеет тот порядок, что и масса элемента во всем живом веществе Мировой суши. Масса кальция в растворимом органическом веществе океана – 20× 109 т. 4

Кальций в биологическом круговороте Для процесса глобального массообмена кальция главное значение имеют биологический круговорот и водная миграция ионов в системе суша-океан. Масса вовлеченного в годовой биологический круговорот кальция составляет 3, 4× 109 т/год. Размеры вовлечения кальция в биологический круговорот сильно различаются в разных природных зонах. Лесостепная растительность (широколиственная и травянистая) ежегодно потребляет 100 кг/га кальция, а тундровая растительность – только 8, 6 кг/га. В наибольшем количестве он требуется растительности степей. Подсчитано, что в доисторический период его потребление с приростом составляло 137 кг/га в год. Весь этот кальций возвращался в почву с растительным опадом, т. е. малый биологический круговорот кальция носил почти замкнутый характер. В настоящее время растительность полей выносит ежегодно только 30 -50 кг/га кальция, но большая его часть отчуждается с урожаем. Нарушение биогеохимического круговорота кальция происходит за счет использования карбонатных пород в строительстве, сельском хозяйстве (известкование почв), металлургической промышленности. 5

Геохимическая характеристика натрия Натрий – один из главных элементов, аккумулированных в земной коре в процессе ее выплавления. Основная масса элемента выпадает на последних стадиях магматической кристаллизации и частично остается в постмагматических растворах. Натрий легко освобождается из структур гипогенных силикатов при выветривании кристаллических пород. Кларк литосферы – 2, 5%. Число минералов – 222. В океанической воде 1, 035% Na, в живом веществе 0, 02%. Натрий выходит из биологического круговорота и в условиях влажного климата с водным стоком уносится за пределы ландшафта. В сухом климате накапливается в ландшафте благодаря испарительной концентрации. Слабая роль биологического круговорота и большое значение водной миграции. 6

Натрий в Мировом океане и почвенном покрове Освобождаясь из кристаллического вещества земной коры, натрий в форме хорошо растворимого аниона переносится с континентальным стоком в океан, в водах которого содержится 14, 7× 1015 т. Главный миграционный поток натрия в биосфере связан с водным стоком с суши, с которым выносится 0, 19× 109 т ионов этого элемента, столько же выносится в составе взвесей. Преобладание растворимого катиона Na+ в биосфере обусловливает присутствие больших масс натрия во всех типах природных вод, в которых он связан эквивалентными соотношениями с анионами Cl-, SO 42 - и отчасти с HCO 31 -. В педосфере натрий играет важную роль в процессах катионного обмена. Высокое содержание натрия в поглощенном комплексе почв способствует образованию солонцов. Натрий принимает активное участие в засолении почв, в которых он образует соли с Cl-, SO 42 -. Масса натрия в педосфере пока не определена количественно. Несмотря на активное участие в континентальном галогенезе, огромная аккумуляция натрия в океане характеризует его как типичный талассофильный (накапливающийся в воде океана) элемент. 7

Натрий в живом веществе В организмах соли натрия имеют важное значение. Хлорид натрия является обязательным компонентом жидких тканей животных (плазмы, крови, лимфы) и клеточного сока растений, играет важную роль в поддержании кислотно-щелочного равновесия, регулирует осмотическое давление и влияет на содержание воды в тканях. В силу важной физиологической роли хлорид натрия в большом количестве поглощается растительными и особенно животными организмами, его недостаток вызывает тяжелые заболевания. В биомассе суши содержится 3× 109 т натрия, в океанической биомассе – на 2 порядка меньше. Из растительных остатков соли натрия легко выщелачиваются, поэтому масса натрия в неживом органическом веществе и гумусе педосферы невелика – около (0, 2 -0, 3)× 109 т. В структуре глобального биологического круговорота натрия ярко проявляется его талассофильность (накопление в воде Мирового океана). На суше в биологический круговорот вовлекается 0, 2× 109 т, а в океане – около 4, 4× 109 т натрия. 8

Геохимическая характеристика калия К входит в состав наиболее распространенных силикатов: полевых шпатов, амфиболов, пироксенов, слюд. Кларк – 2, 5%. Важный биоэлемент, его содержание в живом веществе 0, 3%, в отдельных видах до 1 -2% (гигантские морские водоросли макроцитис). Хотя почти все соли К легкорастворимы, в биосфере мигрирует слабо, чем резко отличается от натрия. При выветривании переходит в воды, но быстро захватывается организмами и поглощается глинами. Поэтому речная вода бедна калием. В океане калий поглощается организмами и донными илами. 9

Калий в живом веществе В гранитном слое масса калия 198× 1015 т, в осадочном – 38, 2× 1015 т. При гипергенной перестройке кристаллохимических структур силикатов большая часть калия остается в составе новообразованных глинистых материалов, поэтому калий прочнее удерживается в пределах Мировой суши, чем кальций и натрий. И все же частичное высвобождение ионов калия происходит и свободные ионы вовлекаются в водную миграцию, а также активно адсорбируются дисперсным минеральным веществом и поглощаются высшими растениями. Калий играет важную роль в жизни растений и животных. Он принимает участие в фотосинтезе, влияет на обмен углеводов, азота, фосфора, усиливает образование сахаров в листьях и передвижение их в другие органы. Кроме того, К улучшает поступление воды в клетки растений и понижает процесс испарения, тем самым увеличивая устойчивость растений к засухе. Поэтому калий активно поглощается растениями и его кларк в живом веществе такой же высокий, как у азота, 0, 3%. В растительности Мировой суши до активного воздействия на нее человека содержалось около 25× 109 т калия, в сухой биомассе фотосинтетиков океана – 0, 176× 109 т. Масса калия, связанная в мертвом органическом веществе биосферы, в несколько раз меньше, чем в живом веществе, и составляет (3 -6)× 109 т. 10

Геохимическая характеристика фосфора Несмотря на низкий кларк в земной коре (около 0, 1%), фосфор играет важную роль в биосфере. Концентрация в базальтах 0, 14%, в гранитах – 0, 07%. В горных породах находится, в основном, в составе апатитов Ca 5(PO 4)3(Cl, F). Образует около 200 минералов. Средняя концентрация в растительности суши 0, 2%, в биомассе океана – 1, 1%. Значительная часть элемента сохраняется в почвенном органическом веществе, в котором концентрация фосфора 0, 15%. Огромное количество фосфора растворено в Мировом океане, где элемент находится в виде анионов [PO 4]3 -, [HPO 4]2 -, а также в составе органических соединений. Концентрация фосфора в речных и морских водах близка – 0, 04 и 0, 088 мг/л. 11

Биологическое значение фосфора Важное значение в биосфере фосфор приобретает не из-за большого содержания, а потому что без него невозможен синтез белков. Экзотермическая реакция аденозинтрифосфата с фотосинтезированными углеводами обеспечивает энергией последующие биохимические реакции. В организмах фосфор входит в состав орто- и пирофосфорных кислот, многочисленных органических соединений. Нуклеиновые кислоты, содержащие фосфор, участвуют в процессах передачи наследственности. Кости человека состоят из гидроксилапатита 3 Са 3(РО 4)3·Ca(OH)2. В состав зубной эмали входит фторапатит. Во всех природных системах фосфора меньше, чем азота, и именно он лимитирует массу живого вещества. Отношение N: P в растительности суши равно 10– 15, но в последнее время хозяйственная деятельность изменила соотношение в пользу фосфора, что привело к негативным экологическим ситуациям. 12

Биогеохимический цикл фосфора (1) Круговорот фосфора в биосфере связан с процессами обмена веществ в растениях и животных. Однако в отличие от других биофильных элементов фосфор в процессе миграции не образует газовой фазы. Кроме того, главная масса фосфора связана с минеральной частью литосферы, небольшая часть мигрирует в составе природных вод и совершенно не участвует в атмосферных процессах. Цикл фосфора состоит из двух частей – морской (континентальный сток) и наземной (биологический круговорот). Из почв и пород фосфор извлекается в растворенном виде наземными растениями и перерабатывается ими в фосфорсодержащие органические вещества. В организм животных фосфор попадает с растительной пищей и подвергается дальнейшим превращениям. В почву химически связанный фосфор попадает с остатками растений и животных, и в дальнейшем происходит повторение цикла. 13

Биогеохимический цикл фосфора (2) Поступление фосфора в океан обеспечивается континентальным стоком. В нем фосфор находится в составе комплексных анионов, дисперсного органического вещества и минеральных взвесей. В морских водах фосфор переходит в состав фитопланктона, с последующим накоплением в тканях морских животных, прежде всего, рыб. Отмершие остатки организмов приводят к накоплению фосфора на различных глубинах. Характерная черта глобального цикла фосфора – отсутствие постоянного геохимического потока, возвращающего крупные массы элемента на сушу. Определенное количество фосфора переносится на сушу морскими птицами и благодаря рыболовству. Птицы отлагают фосфор на отдельных островах и побережьях в виде гуано. Глобальный цикл фосфора является наименее замкнутым по сравнению с ранее рассмотренными элементами. Антропогенные изменения биогеохимического цикла фосфора; 1)внесение в обрабатываемые почвы фосфорных удобрений, значительная часть которых смывается, служит одним из главных факторов эвтрофикации озер и мелководных прибрежных участков морей. 2) загрязнение поверхностных вод бытовыми и промышленными стоками. 14

Общие черты биогеохимических циклов кальция, натрия, калия 1. Все циклы поддерживаются поступлением из одного источника: гранитного слоя земной коры континентального типа. За последние 570 млн лет из гранитного слоя извлечено 16, 5% калия, 19% натрия, 17% фосфора. 2. Биогеохимические циклы складываются из континентального стока и биологического круговорота. Атмосферная миграция более ограничена по сравнению с элементами, поступающими в биосферу в результате дегазации мантии. Поэтому элементы накапливаются преимущественно в осадочных породах (более 99% кальция, 98% калия, 60% натрия). 3. Массы элементов в живом веществе очень малы. 15
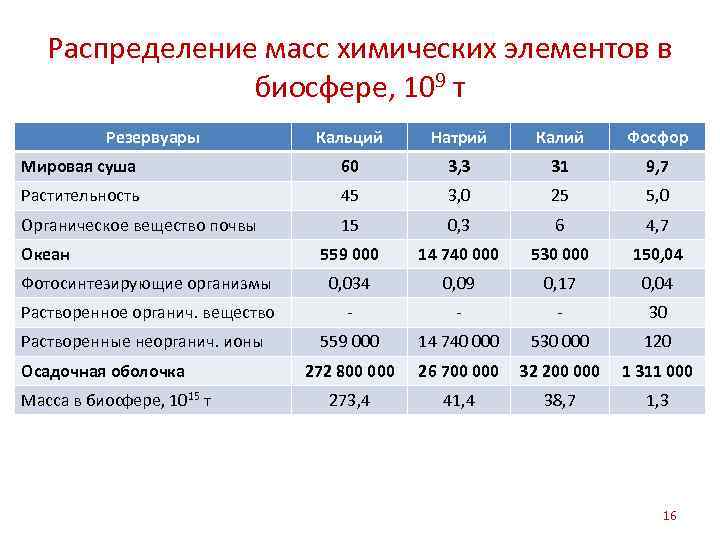
Распределение масс химических элементов в биосфере, 109 т Резервуары Кальций Натрий Калий Фосфор Мировая суша 60 3, 3 31 9, 7 Растительность 45 3, 0 25 5, 0 Органическое вещество почвы 15 0, 3 6 4, 7 559 000 14 740 000 530 000 150, 04 Фотосинтезирующие организмы 0, 034 0, 09 0, 17 0, 04 Растворенное органич. вещество - - - 30 559 000 14 740 000 530 000 120 272 800 000 26 700 000 32 200 000 1 311 000 273, 4 41, 4 38, 7 1, 3 Океан Растворенные неорганич. ионы Осадочная оболочка Масса в биосфере, 1015 т 16
12_Кальций.pptx