Биофизика.ppt
- Количество слайдов: 66

Биофизика — наука о наиболее простых и фундаментальных взаимодействиях, лежащих в основе биологических процессов.

При исследовании биологических систем выделяют два направления: — изучение формы и многообразия живого — этим занимаются анатомия, морфология, гистология и цитология; — изучение процессов, обеспечивающих жизнедеятельность организма, т. е. поступление, распределение и выведение веществ, метаболизм, синтез, а также энергообеспечение этих процессов, — этим занимаются физиология, биохимия и биофизика.

Целью биофизического исследования является первичный механизм функционирования как отдельной клетки, так и ее органелл и молекул при естественных условиях функционирования биосистемы. I этап - с начала XVII до середины XVIII в. ; II этап - с середины XVIII до середины XX в. ; III этап - с середины XX в. до наших дней.

Лайнус Карл Полинг (1954) Джеймс Дьюи Уотсон и Френсис Крик

Сеченов Иван Михайлович Волькенштейн В. М. Николай Евгеньевич Введенский Чаговец Василий Юрьевич

Биофизика - интегративная наука, изучающая структуру, физические свойства и характеристики биологических объектов, фундаментальные взаимодействия молекул и молекулярных комплексов, элементарные физико-химические и физические процессы, лежащие в основе физиологических реакций и биологических явлений, а также влияние на биологические объекты различных физических факторов (света, ионизирующего излучения, температуры и др. ).

Биологическая система - совокупность взаимосвязанных определенным образом элементов, отграниченная от окружающей среды и обладающая рядом специфических особенностей, характерных для живого организма. Цели биофизики: - основываясь на законах и представлениях физики и химии, изучать фундаментальные элементарные процессы, протекающие в биополимерах и надмолекулярных комплексах, лежащие в основе жизнедеятельности клеток и организмов; - исследовать действие ряда физических и химических факторов на биообъекты. Объекты исследования в биофизике: биополимеры и другие биологически важные молекулы, субклеточные комплексы, ткани, органы.

Модель — это всегда некое упрощение объекта исследования и в смысле его структуры, и по сложности внутренних и внешних связей, но обязательно отражающее те основные свойства, которые интересуют исследователя. Моделирование — это метод, при котором производится замена изучения некоторого сложного объекта (процесса, явления) исследованием его модели.
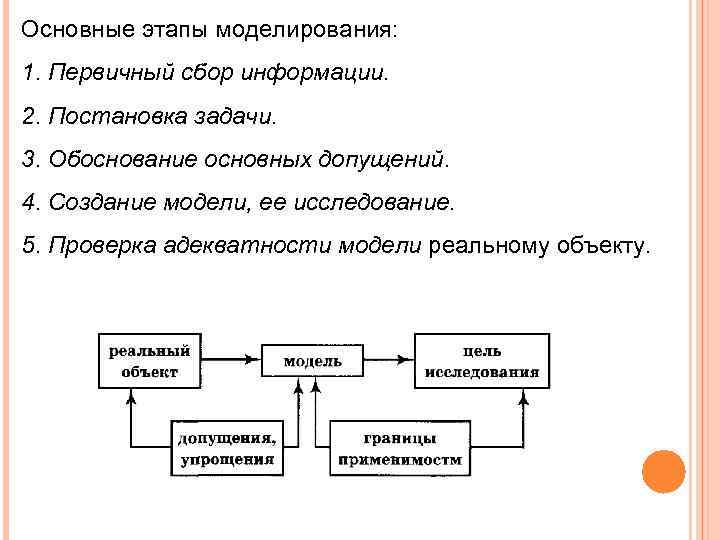
Основные этапы моделирования: 1. Первичный сбор информации. 2. Постановка задачи. 3. Обоснование основных допущений. 4. Создание модели, ее исследование. 5. Проверка адекватности модели реальному объекту.
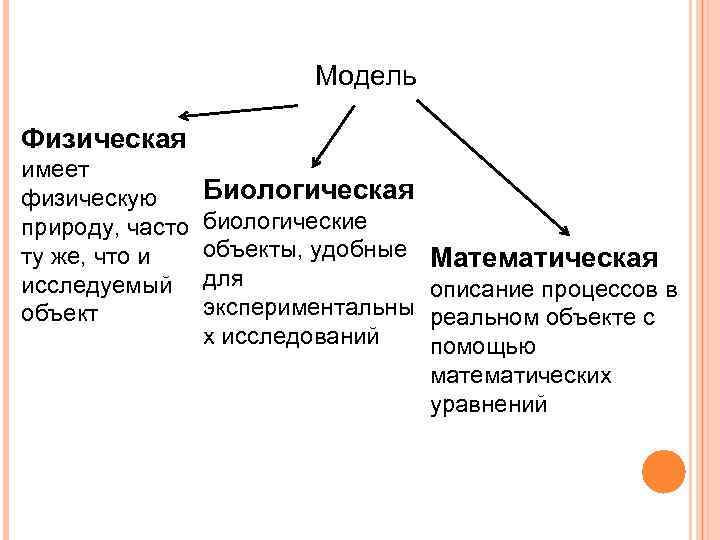
Модель Физическая имеет Биологическая физическую природу, часто биологические объекты, удобные ту же, что и исследуемый для экспериментальны объект х исследований Математическая описание процессов в реальном объекте с помощью математических уравнений

Основные требования, которым должна отвечать модель: 1. Адекватность - соответствие модели объекту, то есть модель должна с заданной степенью точности воспроизводить закономерности изучаемых явлений. 2. Должны быть установлены границы применимости модели, то есть четко заданы условия, при которых выбранная модель адекватна изучаемому объекту, поскольку ни одна модель не дает исчерпывающего описания объекта.

Термодинамика биологических процессов - это раздел биофизики, изучающий общие закономерности превращения энергии. Термодинамика рассматривает также проблемы устойчивости и эволюции биологических систем.

Термодинамическая система - часть пространства с материальным содержимым, ограниченная поверхностью раздела (стенка сосуда, где идет реакция, или мембрана клетки). Примеры: клетка, митохондрия. Область вне оболочки - окружающая среда. Размеры системы всегда больше, чем размеры составляющих ее частиц.
Системы Изолированные Открытые Закрытые
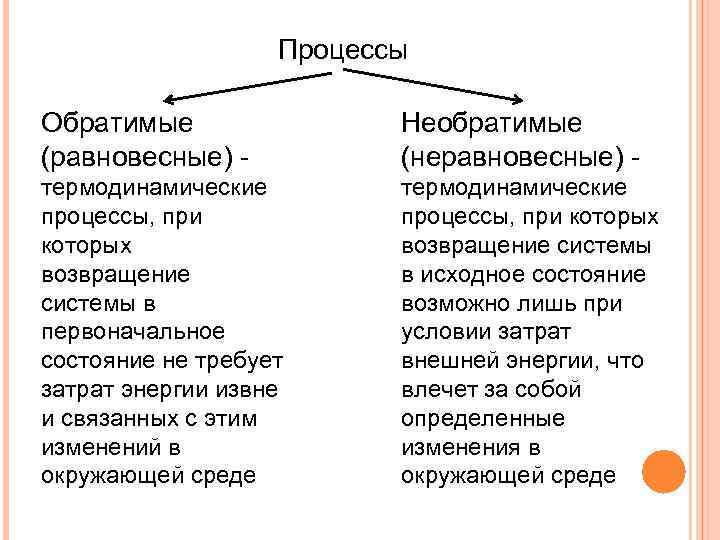
Процессы Обратимые (равновесные) - Необратимые (неравновесные) - термодинамические процессы, при которых возвращение системы в первоначальное состояние не требует затрат энергии извне и связанных с этим изменений в окружающей среде термодинамические процессы, при которых возвращение системы в исходное состояние возможно лишь при условии затрат внешней энергии, что влечет за собой определенные изменения в окружающей среде

Энергия - количественная мера определенного вида движения материи при ее превращениях. Работа - любая макрофизическая форма передачи энергии. Термодинамическое равновесие - это состояние системы, при котором ее параметры не изменяются и она не обменивается с окружающей средой ни веществом, ни энергией.

Первый закон термодинамики 1842 - 1847 гг. Ю. Р. Майер Г. А. Гельмгольц В изолированной термодинамической системе полный запас энергии есть величина постоянная и возможны только превращение одного вида энергии в другой в эквивалентных соотношениях. U=const; ∆U=0 (1)

Формулировка первого начала термодинамики для закрытых систем следующая: теплота, подведенная к системе, расходуете на изменение внутренней энергии системы и на совершение работы против внешних сил. δQ = d. U + δA (2) где Q - теплота, подведенная к системе; U - внутренняя энергия системы; А - работа; δ - обозначает, что теплота и работа не являются функциями состояния системы и не могут быть полными дифференциалами; U - функция системы U = f (m, P, V, Т), зависящая от термодинамических параметров (m, Р, V, Т).

XVIII в. А. Лавуазье П. Лаплас Ледяной калориметр

М. Рубнер (1894) У. Этуотер (1904) VCO 2 δ = ----- (3) VO 2
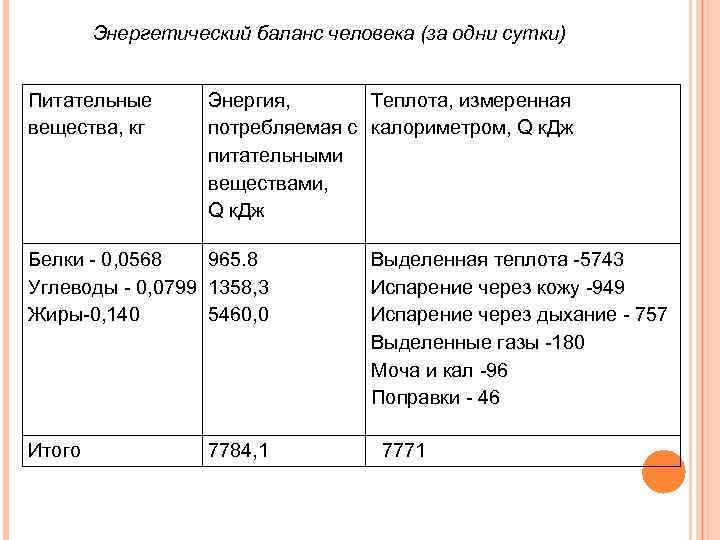
Энергетический баланс человека (за одни сутки) Питательные вещества, кг Энергия, Теплота, измеренная потребляемая с калориметром, Q к. Дж питательными веществами, Q к. Дж Белки - 0, 0568 965. 8 Углеводы - 0, 0799 1358, 3 Жиры-0, 140 5460, 0 Выделенная теплота -5743 Испарение через кожу -949 Испарение через дыхание - 757 Выделенные газы -180 Моча и кал -96 Поправки - 46 Итого 7771 7784, 1

Энтальпия. Закон Гесса У гомойотермных животных в покое 50% всей теплоты образуется в органах брюшной полости, 20% - в скелетных мышцах, 10% - при работе органов дыхания и кровообращения. При напряженной мышечной работе теплопродукция может возрастать в 10 раз по сравнению с состоянием покоя. При понижении температуры окружающей среды теплопродукция организма усиливается.
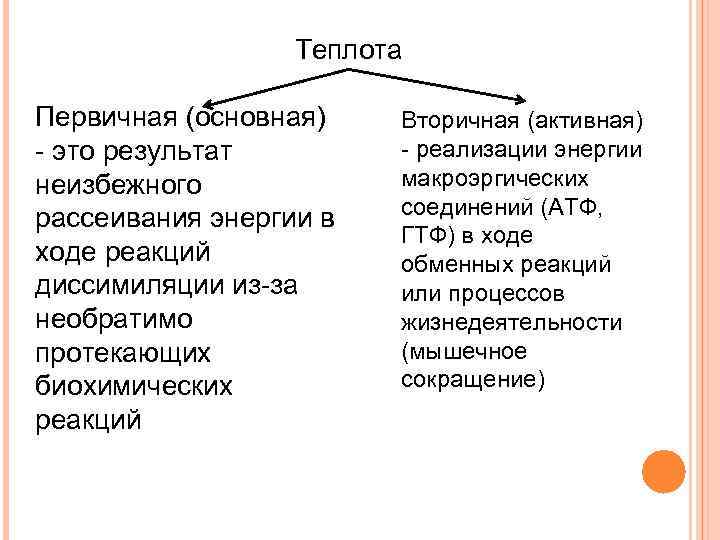
Теплота Первичная (основная) - это результат неизбежного рассеивания энергии в ходе реакций диссимиляции из-за необратимо протекающих биохимических реакций Вторичная (активная) - реализации энергии макроэргических соединений (АТФ, ГТФ) в ходе обменных реакций или процессов жизнедеятельности (мышечное сокращение)

Удельной теплопродукцией называют количество теплоты, выделяемое единицей массы животного в единицу времени: g = QT/μT, (4) где QT - количество теплоты, выделяемое в единицу времени; μT - единица массы; g - удельная теплопродукция. Теплопродукция пропорциональна массе животного: QT = k x M.

Теплопродукция организма может быть определена как сумма Qв + Qc, где Qв - теплота, выделяемая при взаимодействии клеток между собой и пропорциональная массе тела (М); Qc - теплота, выделяемая при взаимодействии организма с окружающей средой, т. е. пропорциональная площади его поверхности (3√ М 2). Таким образом: QT = а х М + в х М 2/3, (5) где а - количество клеток, в - площадь поверхности. Поэтому q = a + в/3√ М. (6)
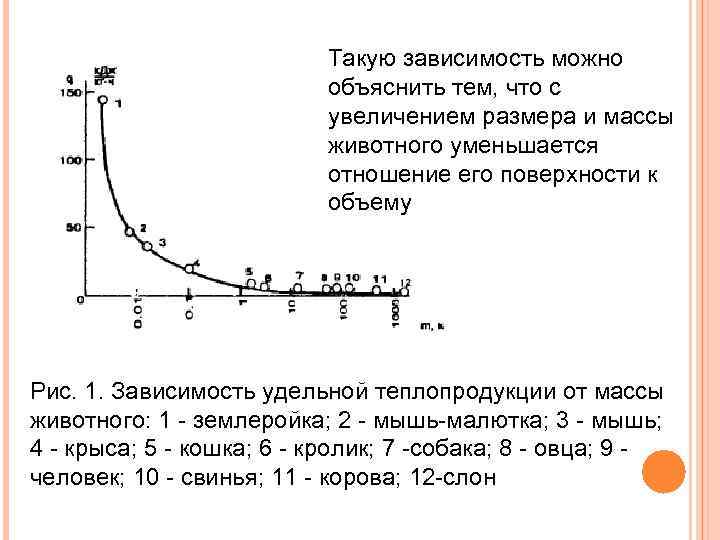
Такую зависимость можно объяснить тем, что с увеличением размера и массы животного уменьшается отношение его поверхности к объему Рис. 1. Зависимость удельной теплопродукции от массы животного: 1 - землеройка; 2 - мышь-малютка; 3 - мышь; 4 - крыса; 5 - кошка; 6 - кролик; 7 -собака; 8 - овца; 9 - человек; 10 - свинья; 11 - корова; 12 -слон

Энтальпия - (от греч. - нагреваю) - это сумма внутренней энергии системы и произведения объема и давления: H = U + P V , (7) где Н - теплосодержание системы.

закон Гесса - основное следствие первого закона термодинамики: тепловой эффект химической реакции, развивающейся через ряд промежуточных стадий, не зависит от пути перехода, а определяется лишь разностью энтальпий конечных и исходных продуктов реакции Q = ∆Н = ƩHп. р – ƩHи. в, (8) где ƩHп. р - сумма энтальпий всех продуктов реакции; ƩHи. в - сумма энтальпий всех исходных веществ; ∆Н - изменение энтальпии химической реакции.

С 6 Н 12 О 6 + 6 О 2 = 6 CO 2 + 6 H 2 O + Q; Q = (6 H CO 2 + 6 H H 2 O) – (H С 6 Н 12 О 6 + 6 H О 2 ) = -2810 к. Дж моль-1 Такое же количество теплоты выделяется при окислении глюкозы в организме животных, когда в процессе анаэробного и аэробного гликолиза образуется ряд промежуточных веществ. Таким образом, потребление 1 л кислорода или выделение 1 л углекислого газа организмом сопровождается выделением 2870 : 134, 4 = 21, 35 к. Дж теплоты. Поэтому тепловыделение любого животного можно подсчитать путем умножения количества потребленного кислорода или выделенного углекислого газа на 21, 35 к. Дж.

Второе начало термодинамики и живые организмы Р. Клаузиус У. Томпсон (1850 -1851) Теплота не может переходить сама собой от более холодного тела к более теплому. Энтропия - это мера неупорядоченности или вероятности состояния системы.

Изменение энтропии d. S системы равно отношению количества теплоты (δQ), сообщенного системе, к термодинамической температуре (Т): d. S = δQ/T. (9) Энтропия изолированной системы возрастает в необратимом процессе и остается неизменной в обратимых термодинамических процессах. d. S ≥ δQ/T. (10)

Сущность второго начала термодинамики для изолированных систем состоит в том, что все необратимые процессы протекают в таком направлении, в котором энтропия системы увеличивается, т. е. d. S>0, d. F ≠ d. U. (F - свободная энергия системы). Это означает, что далеко не вся внутренняя энергия системы переходит в работу, часть ее рассеивается в виде теплоты. При обратимых процессах d. S = 0 и d. F = d. U, т. е. рассеивания энергии в пространстве не происходит.

Второй закон термодинамики показывает, что не все виды энергии эквивалентны. Виды энергии можно разделить на 3 класса (А, В, С) соответственно величине энтропии. Такие виды энергии, как гравитационная, световая и электрическая, наиболее эффективно, т. е. с наименьшей энтропией, могут быть превращены в другие ее виды, и они относятся к классу А. В класс В (среднего качества) попадает химическая энергия. Тепловая энергия относится к классу С (низкое качество) - это энергия с максимальной энтропией.

Живые организмы - системы открытые, и изменение энтропии для них складывается из продукции энтропии внутри организма за счет необратимых биохимических процессов (di. S) и обмена (de. S) энтропии с окружающей средой. d. S = di. S + de. S. (11) Скорость изменения энтропии в организме равна алгебраической сумме производства энтропии внутри организма и скорости поступления энтропии из среды в организм.

Уравнение второго начала термодинамики для открытых систем следующее: d. S/dt = di. S/dt + de. S/dt, (12) где d. S/dt - скорость изменения энтропии в организме; di. S/dt - скорость производства энтропии внутри организма; de. S/dt – скорость обмена энтропией между организмом и окружающей средой.

Л. Больцман установил следующую связь между энтропией и термодинамической вероятностью системы: S = к х ln. W, (13) где к - постоянная Больцмана, равна 1, 38 • 10 -23 Дж/К; W - термодинамическая вероятность, равняется числу всех перегруппировок компонентов в системе и выражается огромными числами. Клетка содержит 109 молекул, W колеблется от 1 до 1015 более.

de. S/dt > 0 показывает увеличение энтропии системы в результате того, что в организм постоянно поступает поток вещества и энергии. de. S/dt < 0 означает, что отток энтропии из организма превышает приток. Величина di. S/dt > 0 (всегда положительна), так как в организме постоянно протекают биофизические и биохимические процессы.

При условии, что di. S/dt > 0, возможны следующие три случая: 1)d. S/dt> 0, если de. S/dt > 0 или если de. S/dt<0, но di. S/dt >de. S/dt, т. е. скорость производства энтропии внутри организма будет превышать скорость обмена энтропией с окружающей средой; 2) d. S/dt < 0, если de. S/dt < 0, скорость обмена энтропией организма с окружающей средой превышает скорость производства энтропии внутри организма de. S/dt > di. S/dt; 3) d. S/dt = 0, если de. S/dt < 0, скорость обмена энтропией с окружающей средой равна скорости производства энтропии за счет внутренних биофизических и биохимических процессов. Последний случай соответствует установлению в системе стационарного состояния.
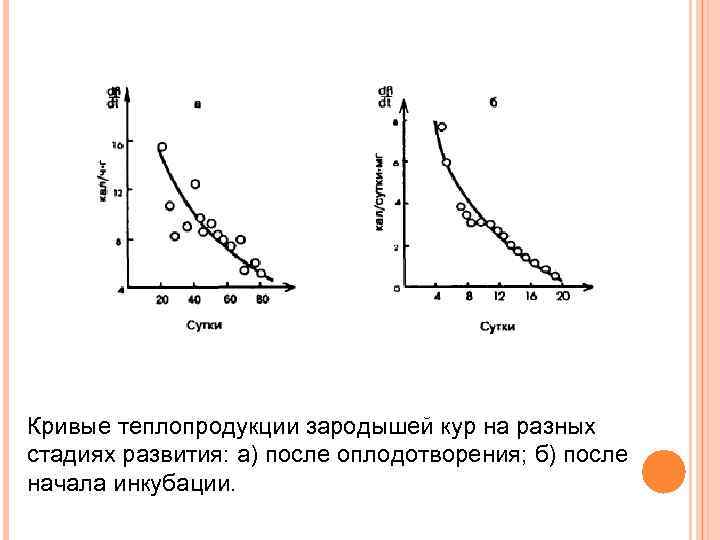
Кривые теплопродукции зародышей кур на разных стадиях развития: а) после оплодотворения; б) после начала инкубации.

di. S/ dt < de. S /dt (15) Скорость накопления энтропии различна у разных видов. Энтропия достигает максимального значения при термодинамическом равновесии. Жизнь - это постоянная борьба против тенденции к возрастанию энтропии. Синтез биомакромолекул, образование клеток со сложной структурой, организация живых существ - мощные антиэнтропийные факторы.

В открытых системах суммарное изменение энтропии в стационарном состоянии равно нулю: d. S=de. S + di. S=0. (17) Стационарное состояние биологической системы поддерживается при условии di. S = de. S, т. е. когда увеличение энтропии системы за счет происходящих в ней необратимых процессов компенсируется оттоком энтропии при взаимодействии с окружающей средой.

Различие между системами, находящимися в термодинамическом равновесии и стационарном состоянии Термодинамическое равновесие Стационарное состояние Отсутствие обмена с окружающей Непрерывный обмен с средой веществом и энергией окружающей средой веществом и энергией Энтропия системы постоянна и Энтропия системы постоянна, но соответствует максимально не равна максимально возможному в данных условиях значению Полное отсутствие в системе Наличие постоянных по величине каких-либо градиентов Не требуется затраты свободной Необходимы постоянные затраты энергии Система нереакционноспособна и В системе совершаются не совершает работу против необратимые реакции, ее внешних сил работоспособность постоянна и не равна нулю

Теорема Пригожина И. Пригожин (1946) на основе изучения открытых систем сформулировал основное свойство стационарного состояния: в стационарном состоянии при фиксированных внешних параметрах скорость продукции энтропии в открытой системе, обусловленная протеканием необратимых процессов, постоянна во времени и минимальна по величине: di. S/dt → min (18)

Градиент (Г) - это отношение разности какой-либо величины ∆Ф (концентрации, давления, температуры) в двух точках к расстоянию между ними (х) ∆Ф Г=----- (19) ∆х Градиент - векторная величина, имеет направления от большего значения к меньшему.

Интенсивность диффузионного потока Ig пропорциональна градиенту концентрации вещества Ig=D dc/dx (20) где D - коэффициент диффузии; dc/dx - концентрационный градиент. По закону Ома Iэл = γ dφ/dx (21) где у - удельная электропроводность, dφ/dx - градиент потенциала. Процесс жизнедеятельности определяют и другие потоки: осмотический, электродиффузионный, которые также характеризуются градиентами соответствующих величин.


Л. Онзагер предположил, что любой необратимый процесс можно в общем виде описать линейной зависимостью: I=Lx (22) где I - термодинамический поток, х - обобщенная сила, L - феноменологический коэффициент. Это уравнение носит название феноменологического

Таким образом, для двух сопряженных потоков сил имеем систему уравнений I 1 = L 11 X 1 + L 12 X 2, I 2 = L 21 X 1 +L 22 X 2 (23) где L 12, 21 - феноменологические коэффициенты, отражающие взаимодействие процессов, коэффициенты взаимности; L 11, 22 - феноменологические коэффициенты, отражающие взаимодействие соответствующих потоков и термодинамических сил. Когда необратимые процессы не взаимодействуют, L 12, 21 равны нулю. Данную систему уравнений называют соотношением взаимности Онзагера.

Кинетика биологических процессов изучает количественные закономерности протекания жизненных явлений во времени. Задачи: -выяснение механизмов, определяющих скорости биологических процессов, и выявление их лимитирующх стадий, - количественное описание протекания процессов жизнедеятельности во времени с использованием молекулярных представлений и законов физической и химической кинетики.

Теория ферментативного катализа развивается по двум направлениям: 1)изучение структуры ферментов и их активных центров; 2)исследование последовательности превращений молекулы субстрата в активном центре фермента, приводящих к образованию продукта.

Модели биологических процессов чаще всего бывают двух категорий: регрессионные и имитационные. Регрессионные модели помогают установить связь между некоторыми переменными в системе, позволяют уточнить характер связи между взаимодействующими компонентами и значение параметров, которые, по существу, определяют протекание биологического процесса. Имитационные модели также представляют собой системы дифференциальных уравнений. Они дают не только качественный, но и количественный прогноз. Имитационные модели включают большое количество переменных и, соответственно, большое число дифференциальных уравнений, в том числе и нелинейных.
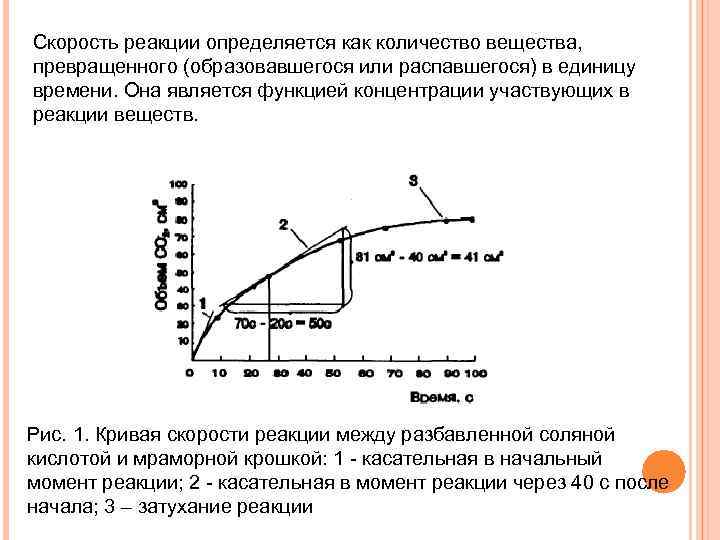
Скорость реакции определяется как количество вещества, превращенного (образовавшегося или распавшегося) в единицу времени. Она является функцией концентрации участвующих в реакции веществ. Рис. 1. Кривая скорости реакции между разбавленной соляной кислотой и мраморной крошкой: 1 - касательная в начальный момент реакции; 2 - касательная в момент реакции через 40 с после начала; 3 – затухание реакции

Средняя скорость реакции за период времени t, которая определяется уравнением: V=∆V/dt. (25) Мгновенную скорость реакции в какой-либо конкретный момент времени можно выразить так: V= d. V/dt. (26) Мгновенная скорость реакции определяется тангенсом угла наклона касательной к кривой скорости в соответствующий момент времени.

фермент А+В C+D, А и В - исходные вещества (субстраты), а С и D - продукты реакции. Скорость такой реакции: А → В A+D →С ЗА → В или 2 А + В → С
![Кинетика мономолекулярных реакций подчиняется следующему уравнению: V=k[A], (27) где к - константа скорости реакции; Кинетика мономолекулярных реакций подчиняется следующему уравнению: V=k[A], (27) где к - константа скорости реакции;](https://present5.com/presentation/62412666_175646418/image-56.jpg)
Кинетика мономолекулярных реакций подчиняется следующему уравнению: V=k[A], (27) где к - константа скорости реакции; [А ] - концентрация вещества А. Скорость бимолекулярной реакции выражается уравнением: V=k[A][B], (28) где [А ] и [В ] - исходные концентрации реагирующих веществ. Если реагируют две одинаковые молекулы (в случае разложения Н 2 О 2), то константа скорости v=k[A]2=k [ B ] 2 (29) бимолекулярной реакции численно равна скорости реакции при условии, что концентрации всех реагентов равны 1, и будет определяться уравнением:

Q 10 = k. Т+10/ k. Т (31) dlnk/dt = ∆H/RT , (32) K = PZe-E a кт / R T (33) Еакт, входящая в уравнение, называется энергией активации реакции; Z - число столкновений молекул; Р – стерический фактор; к - константа скорости реакции. Уравнение показывает, что константа скорости реакции определяется двумя постоянными для данной реакции величинами - числом столкновений молекул и энергией активации реакции Еакт.

Большая скорость реакции в присутствии катализатора может быть обусловлена двумя причинами: 1) катализатор направляет реакцию по пути с более низкой энергией активации; 2) катализатор осуществляет реакцию по цепному механизму, при этом ускорение достигается благодаря образованию богатых энергией частиц в процессе самой реакции.

Ферменты, как и другие катализаторы, ускоряют только реакции, протекание которых термодинамически возможно, т. е. реакции с уменьшением свободной энергии AG < 0. Ферментативный катализ характеризуется выигрышем энергии активации в 16 – 18 ккал, в то время как катализаторы небиологической природы дают снижение энергии активации на 4 - 7 ккал

По современным представлениям, среди механизмов, которые играют главную роль в образовании ферментсубстратного комплекса, можно выделить следующие: 1)образование ковалентных связей; 2)гидрофобное взаимодействие между неполярными углеводородными радикалами молекул субстрата и дегидратированными участками белковой глобулы; 3)электростатическое взаимодействие между заряженной группой субстрата и ионизированными группами фермента; 4)образование водородных связей.

v = Vmax. S 0/Km+S 0, (34) где v - скорость реакции; Vmax - максимальная скорость; Кm - константа Михаэлиса; So - концентрация субстрата.
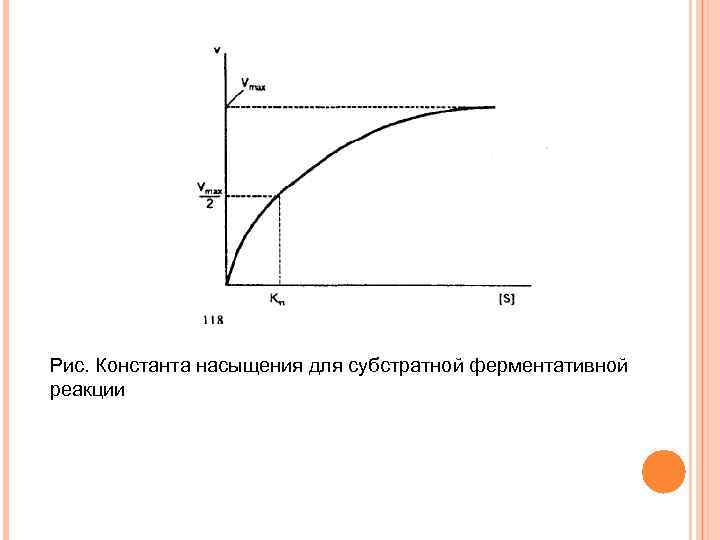
Рис. Константа насыщения для субстратной ферментативной реакции
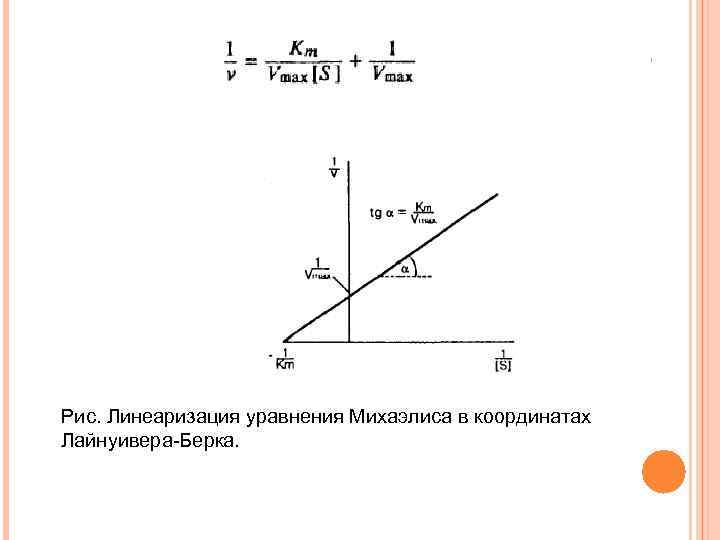
Рис. Линеаризация уравнения Михаэлиса в координатах Лайнуивера-Берка.
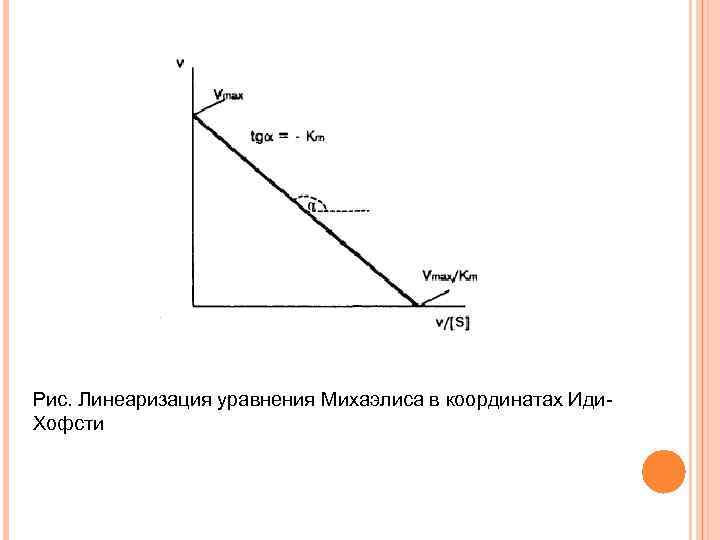
Рис. Линеаризация уравнения Михаэлиса в координатах Иди. Хофсти
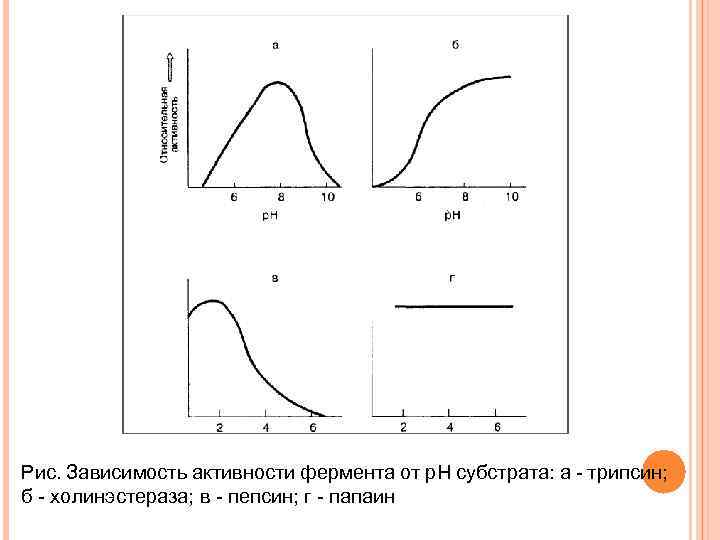
Рис. Зависимость активности фермента от р. Н субстрата: а - трипсин; б - холинэстераза; в - пепсин; г - папаин
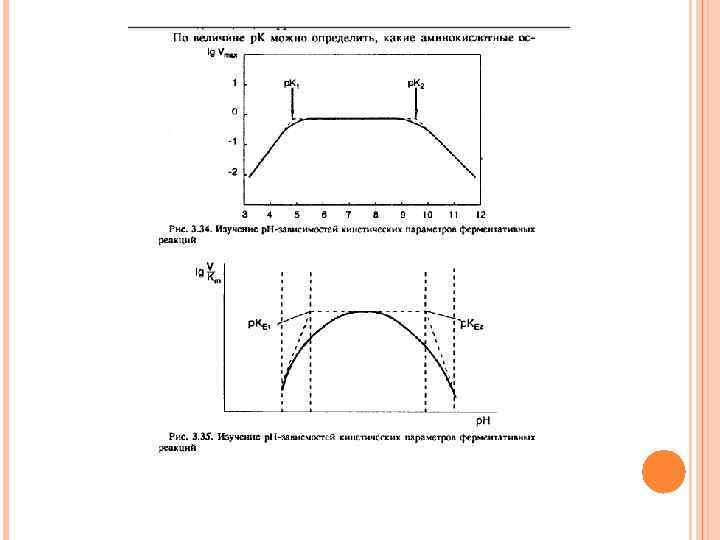
Биофизика.ppt