Биофизика мышцы.ppt
- Количество слайдов: 94

Биофизика мышечного сокращения

Вопросы Структура поперечно-полосатой мышцы Биомеханика мышцы Уравнение Хилла Моделирование мышечного сокращения

Мышечная клетка отличается от других возбудимых клеток таким специфическим сократимость, свойством, как то есть способность генерировать механическое напряжение и укорачиваться.

Мышцы являются генератором тепла. Мышечная активность в процессе жизнедеятельности обеспечивает работы отдельных органов и целых систем: работу опорно -двигательного аппарата, легких, сосудистую активность, желудочно-кишечного тракта, сократительную способность сердца.

Мышечная ткань представляет собой совокупность мышечных клеток (волокон), внеклеточного вещества (коллаген, эластин и др. ) и густой сети нервных волокон и кровеносных сосудов.

гладкие - мышцы кишечника, стенки сосудов, и поперечно-полосатые скелетные, мышцы сердца. Мышцы по строению делятся на:

Мембрана мышечных клеток — сарколемма — также, как и мембрана нервных клеток, электровозбудима и способна проводить потенциал действия. Потенциал покоя (V 0) мышечного волокна составляет -90 м. В, в нервном волокне (-70 м. В.

Поэтому возбудимость мышечного волокна несколько ниже, чем нервного, так клетку требуется деполяризовать на большую величину. где , индексы «м» и «н» относятся соответственно к мышечным и нервным клеткам. Ответом мышечного волокна на возбуждение является сокращение, которое совершает сократительный аппарат клетки — миофибриллы.

миофибриллы представляют собой тяжи, состоящие из двух видов нитей: толстых — миозиновых, и тонких актиновых. Толстые нити (диаметром 15 нм и длиной 1, 5 мкм) имеют в своем составе только один белок — миозин; тонкие (диаметром 7 нм и длиной 1 мкм) содержат три вида белков: актин, тропомиозин и тропонин.
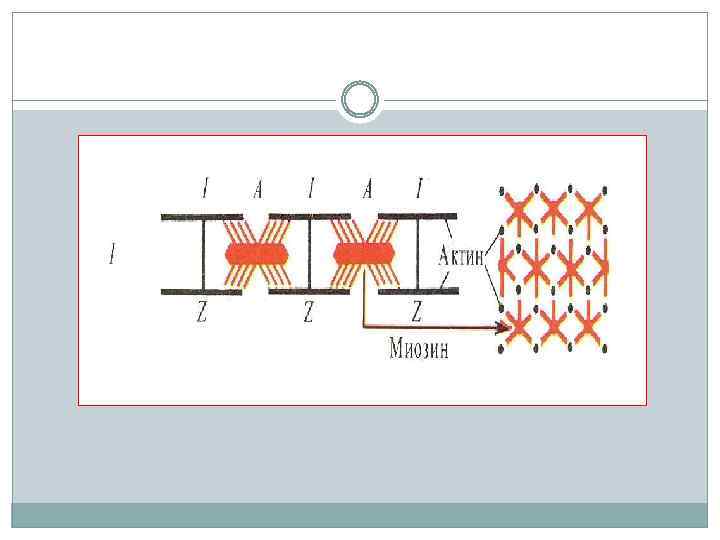

Актин представляет собой длинную белковую нить. Он состоит из отдельных глобулярных белков (G-актина), сцепленных между собой таким образом, что вся структура представляет собой вытянутую цепь. В результате они объединяются, и образуют структуру, которую часто сравнивают с двумя нитками бус, соединенных вместе.
Объединение отдельных глобул G-актина в F-актин.

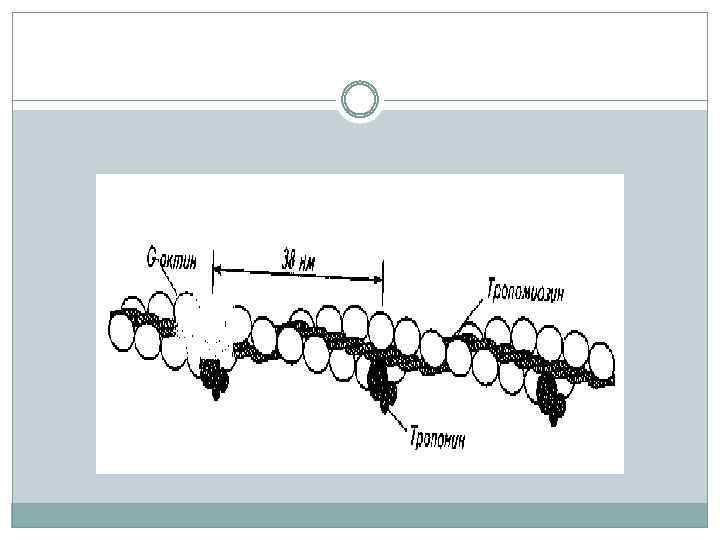
Образованная из молекул G-актина лента закручена в спираль. Такая структура называется фибриллярным актином (Fактином). Шаг спирали (длина витка) составляет 38 нм, на каждый виток спирали приходится 7 пар G-актина.

Вдоль спиральных желобков актиновых филаментов (нитей) располагается белок тропомиозин (греч. trope — поворачивать, mys— мышца). Каждая нить тропомиозина, имеющая длину 41 нм, состоит из двух идентичных цепей, вместе закрученных в спираль с длиной витка 7 нм. Вдоль одного витка F-актина расположены две молекулы тропомиозина
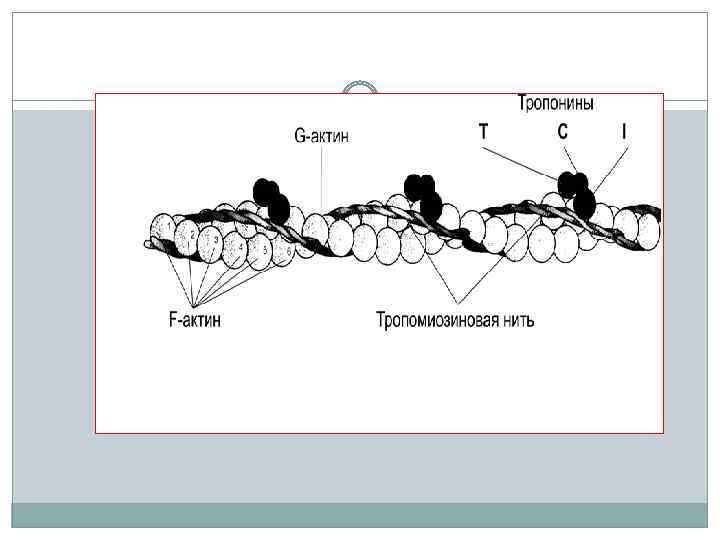

Актиновая нить состоит из двух закрученных один вокруг другого мономеров актина толщиной по 5 нм Эта структура похожа на две нитки бус, скрученные по 14 бусин в витке. В цепях актина регулярно примерно через 40 нм встроены молекулы тропонина, а сама цепь охватывает нить тропомиозина.

Толстая нить состоит из большого числа молекул миозина, собранных в пучок. Каждая молекула миозина длиной около 155 нм и диаметром 2 нм состоит из шести полипептидных нитей: двух длинных и четырех коротких. Длинные цепи вместе закручены в спираль с шагом 7, 5 нм и образуют фибриллярную часть миозиновой молекулы. .

На одном из концов молекулы эти цепи раскручиваются и образуют раздвоенный конец. Каждый из этих концов образует комплекс с двумя короткими цепями, то есть на каждой молекуле имеются две головки. Это глобулярная часть миозиновой молекулы
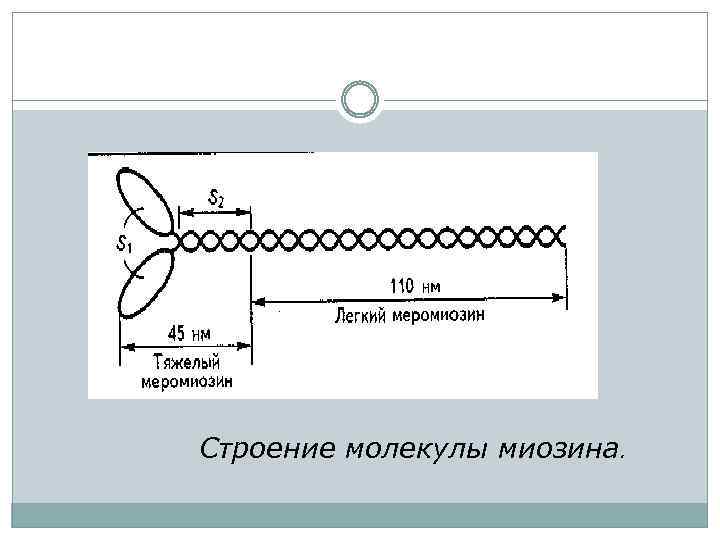
Строение молекулы миозина.

В миозине выделяют два фрагмента: легкий меромиозин (ЛММ) и тяжелый меромиозин (ТММ), между ними находится шарнир. ТММ состоит из двух субфрагментов: S 1, и S 2. , а субфрагмент S 1 выступает над поверхностью. Этот выступающий конец (миозиновая головка) способен связываться с активным центром на актиновой нити и изменять угол наклона к пучку миозиновых нитей
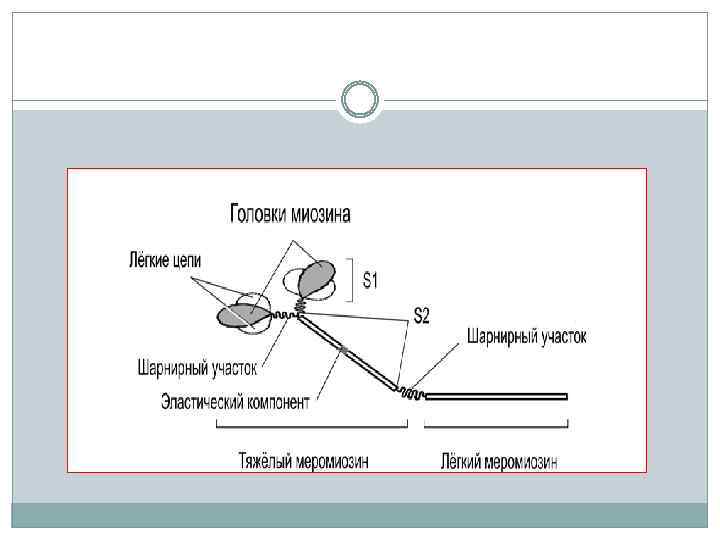
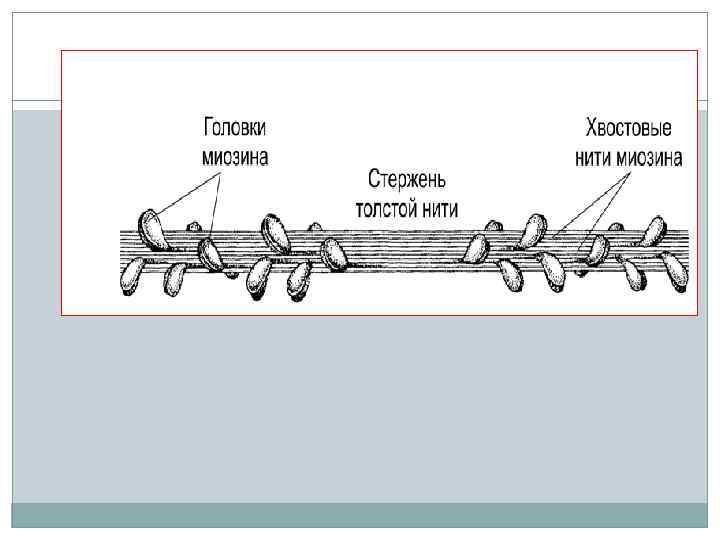

Объединение отдельных молекул миозина в пучок происходит, за счет электростатических взаимодействий

Схема агрегации молекул миозина

В миофибриллах различают: А-зону - темные полосы, которые в поляризованном свете дают двойное лучепреломление, то есть обладают свойством анизотропии (отсюда и название: А-зона), I-зону - светлые полосы, не дающие двойного лучепреломления, то есть изотропные (отсюда название: I-зона).
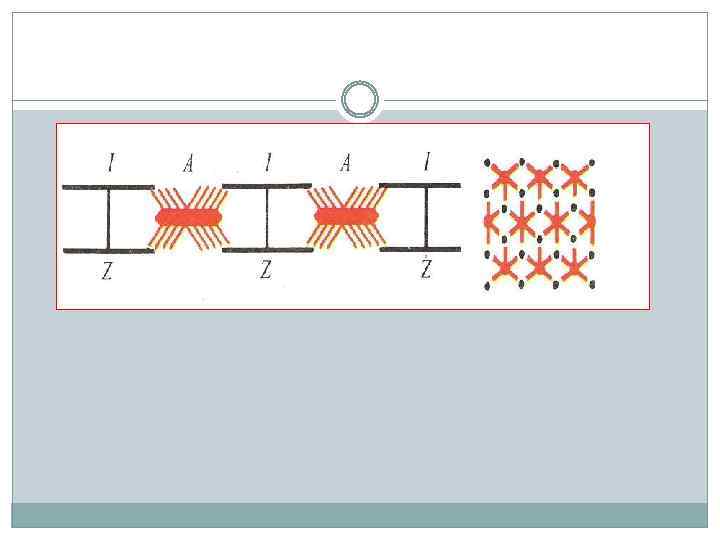

В области I-зоны проходит темная узкая полоса - Zдиск (от нем. zwischenscheibe - промежуточный диск). Промежуток между двумя 2 -дисками называется саркомером и является элементарной сократительной единицей мышечной клетки.
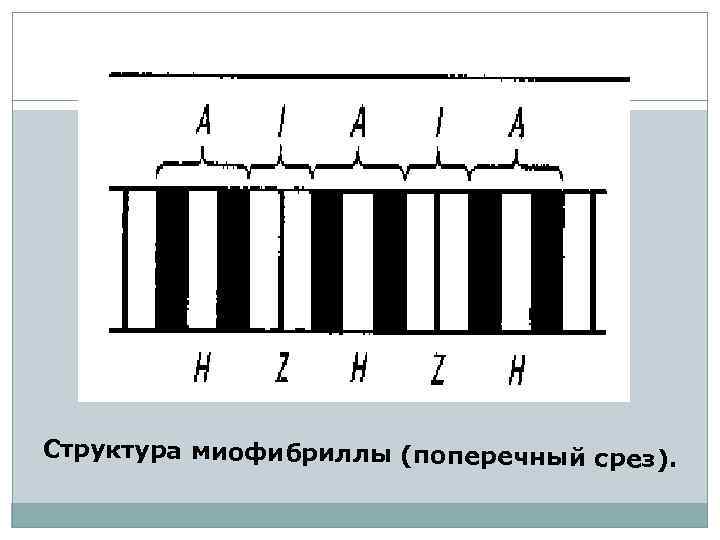
Структура миофибриллы (поперечный срез).

Диск I включает в себя только тонкие нити, диск А — и толстые, и тонкие. В середине диска А видна светлая полоса, называемая Н-зоной. Она не имеет тонких нитей. Диск I разделен тонкой полосой Z, которая представляет собой мембрану, содержащую структурные элементы, скрепляющие между собой концы тонких нитей. Участок между двумя Z-линиями называется саркомером.
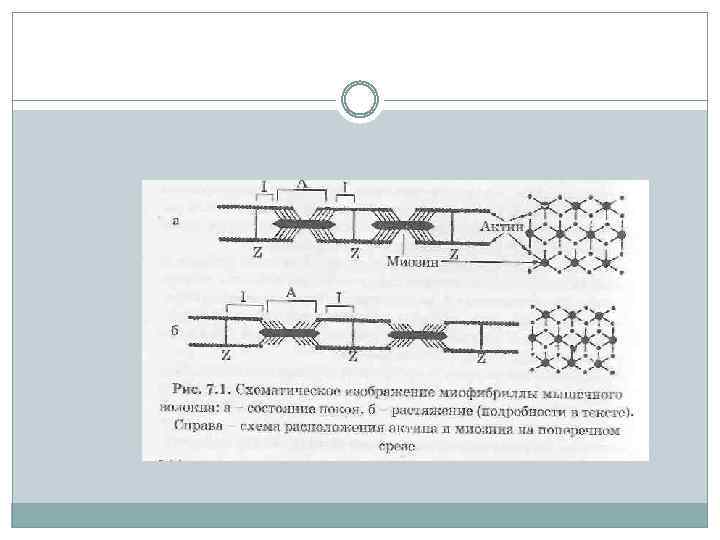
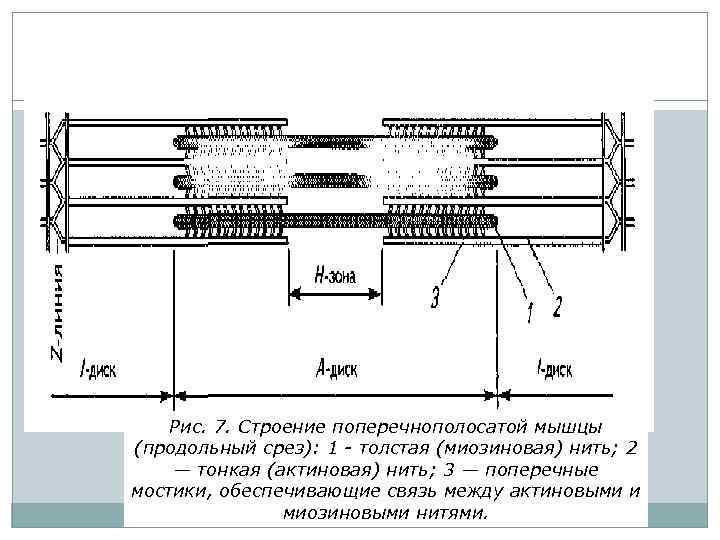
Рис. 7. Строение поперечнополосатой мышцы (продольный срез): 1 - толстая (миозиновая) нить; 2 — тонкая (актиновая) нить; 3 — поперечные мостики, обеспечивающие связь между актиновыми и миозиновыми нитями.

Каждая толстая нить окружена шестью тонкими, а каждая тонкая – тремя толстыми. Таким образом, в поперечном срезе мышечное волокно имеет правильную гексагональную структуру.
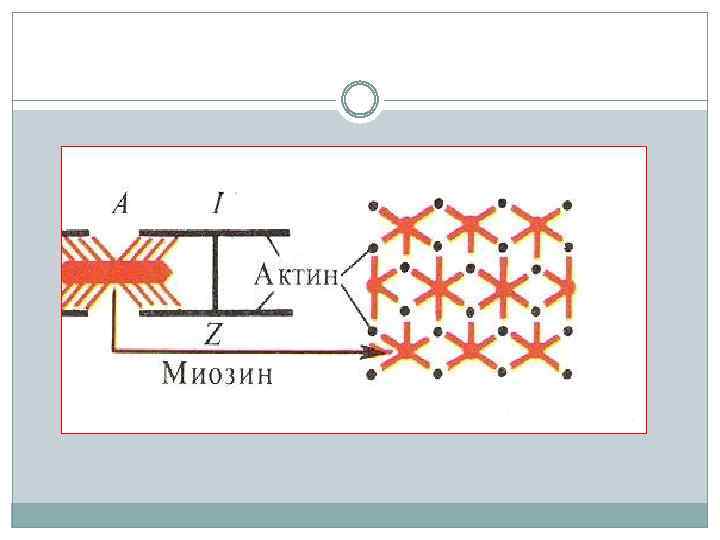
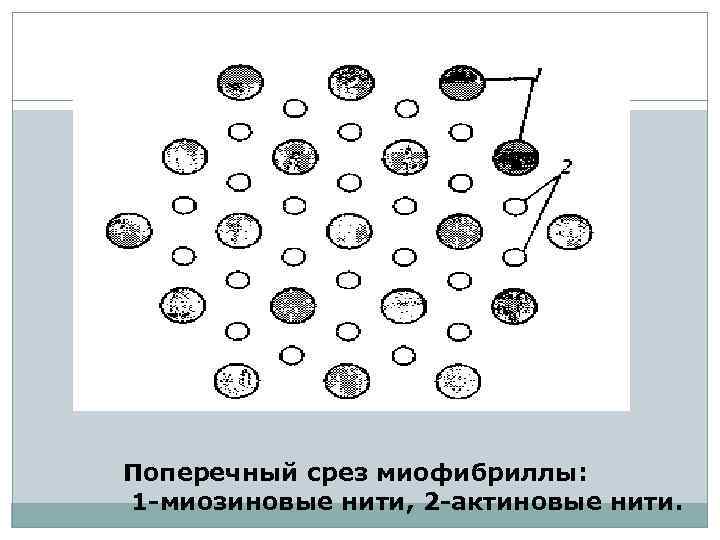
Поперечный срез миофибриллы: 1 -миозиновые нити, 2 -актиновые нити.
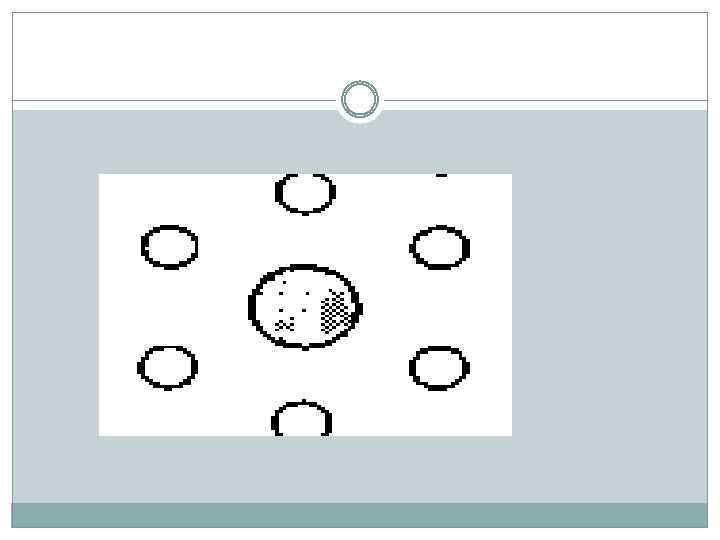
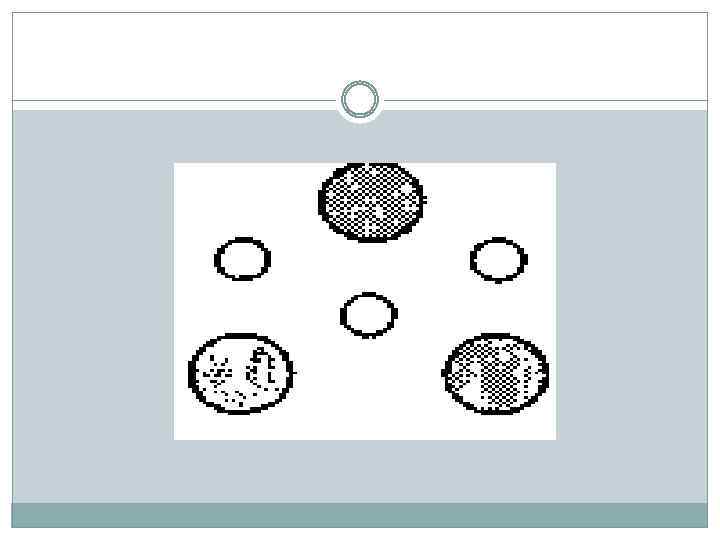

Саркомер — это упорядоченная система толстых и тонких нитей, расположенных гексагонально в поперечном сечении. Толстая нить имеет толщину 12 нм и длину 1, 5 мкм и состоит из белка миозина. Тонкая нить имеет диаметр 8 нм, длину 1 мкм и состоит из белка актина, прикрепленного одним концом к Z-диску.
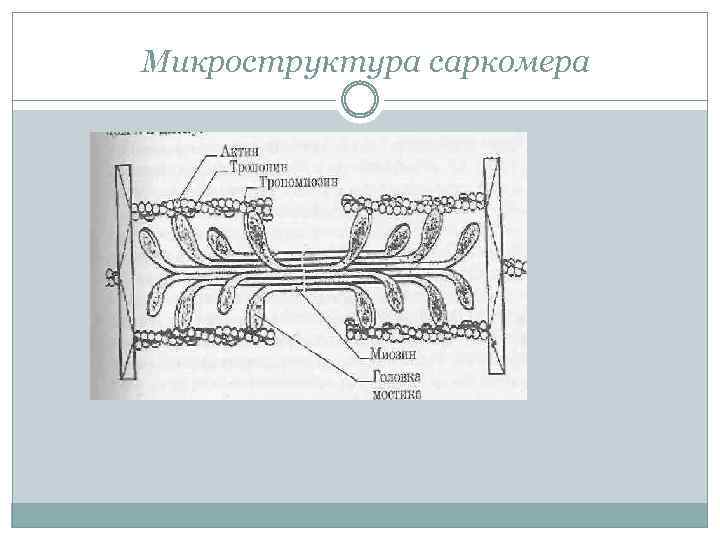
Микроструктура саркомера
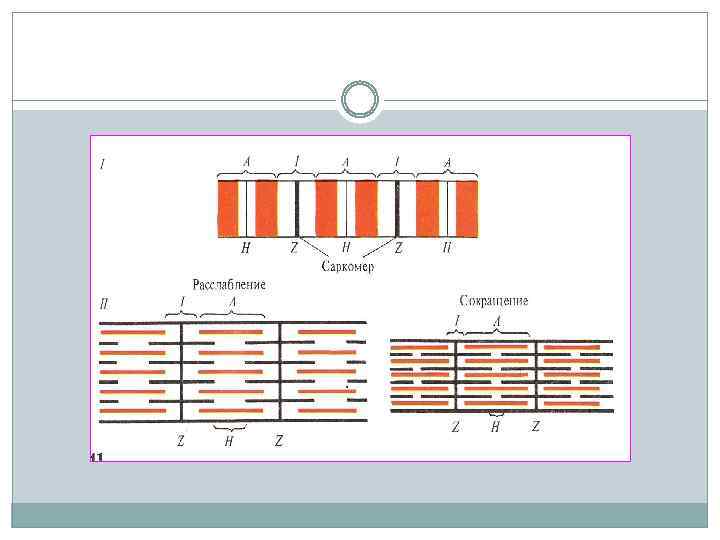

При сокращении мышцы тонкие нити вдвигаются между толстыми. Происходит относительное скольжение нитей без изменения их длины. Этот процесс обусловлен взаимодействием особых выступов миозина — поперечных мостиков с активными Центрами, расположенными на актине. Мостики отходят от толстой нити периодично на расстоянии 14, 5 нм друг от друга

Для того чтобы актин и миозин могли взаимодействовать, необходимо присутствие ионов кальция. В покое они находятся в саркоплазматическом ретикулуме. Распространяющийся по клеточной мембране потенциал действия активирует близко расположенную к поверхности клетки мембрану саркоплазматического ретикулума и вызывает выход Са 2+ в цитоплазму.

Молекула тропонина обладает высоким сродством к кальцию. Под его влиянием она изменяет положение тропомиозиновой нити на актиновой таким образом, что открывается активный центр, ранее прикрытый тропомиозином. К открывшемуся активному центру теперь может присоединиться поперечный мостик. Это приводит к взаимодействию актина с миозином.

Сокращение саркомера: 1 - миозиновая нить; 2 - активный центр; 3 - актиновая нить; 4 - миозиновая головка; 5 – Z -линия;
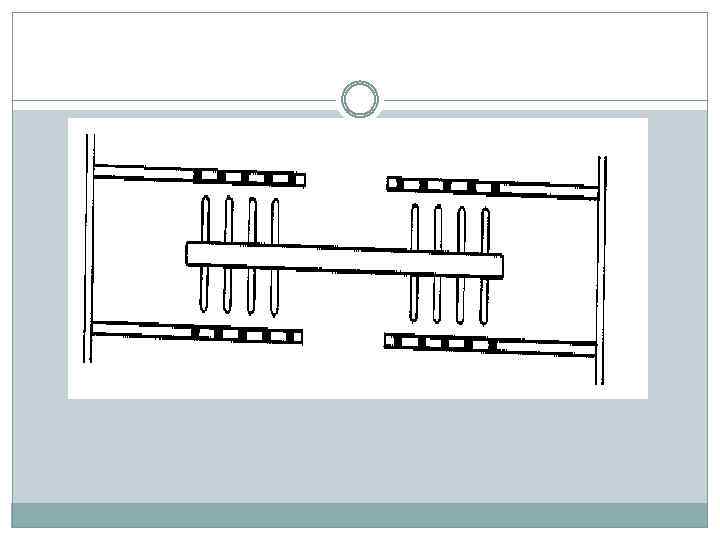

После образования связи миозиновая головка, ранее расположенная почти под прямым углом к нитям, наклоняется и протаскивает актиновую нить относительно миозиновой приблизительно на 10 нм.
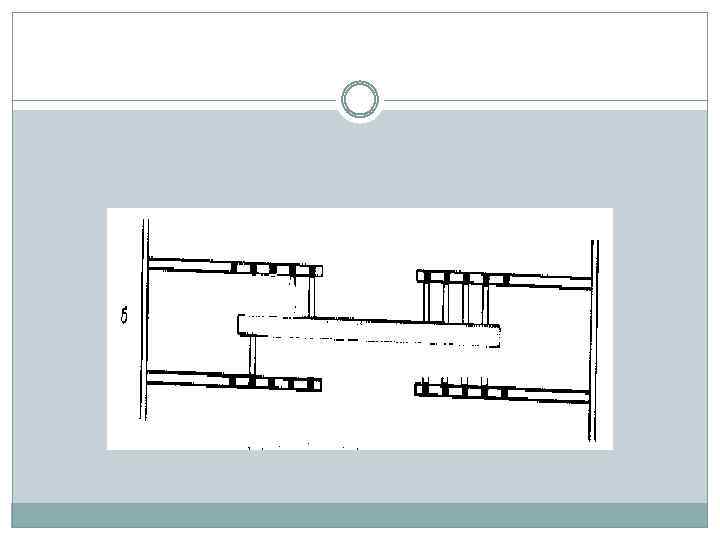

Образовавшийся актин-миозиновый комплекс препятствует дальнейшему скольжению нитей относительно друга, поэтому необходимо его разъединение. Это возможно только за счет энергии АТФ. Миозин обладает АТФ - азной активностью, то есть, способен вызывать гидролиз АТФ.
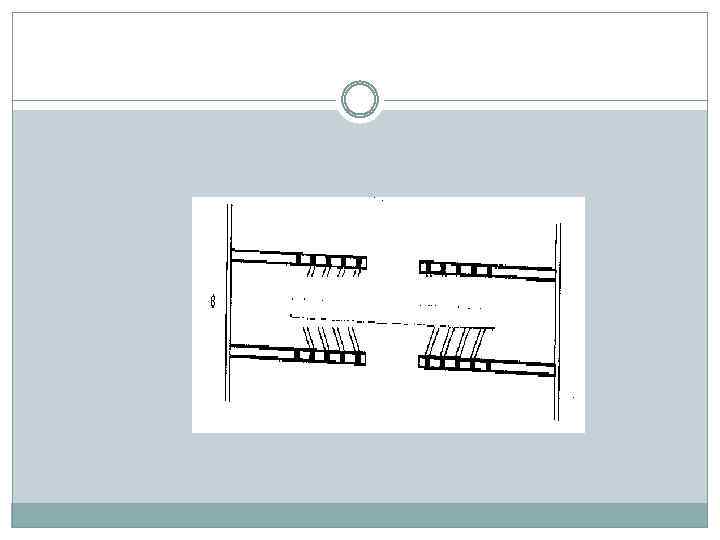

Выделяющаяся при этом и энергия разрывает связь между актином и миозином (Рис. г), и миозиновая головка способна взаимодействовать с новым участком молекулы актина.
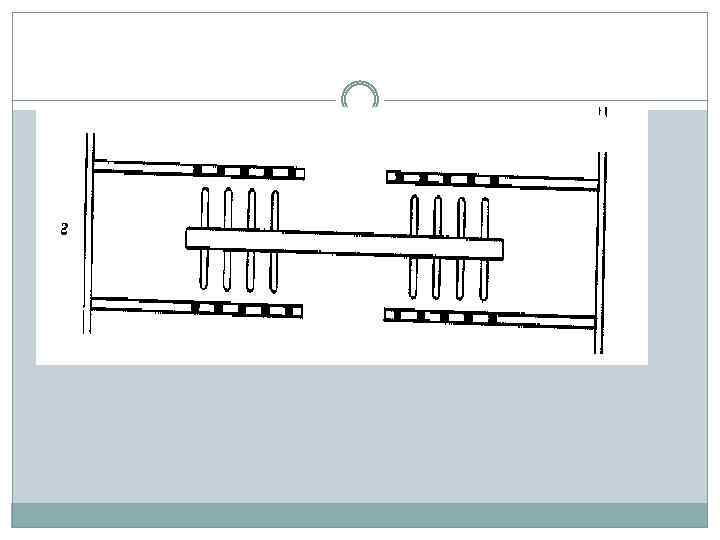

а - взаимодействие между тонкими и толстыми нитями отсутствует; б - в присутствии Са 2+ миозиновая головка связывается с активным центром на актиновой нити; в - поперечные мостики наклоняются и протаскивают тонкую нить относительно толстой, вследствие чего длина саркомера уменьшается; г - связи между ними разрываются за счет энергии АТФ, миозиновые головки готовы взаимодействовать с новыми активными центрами.
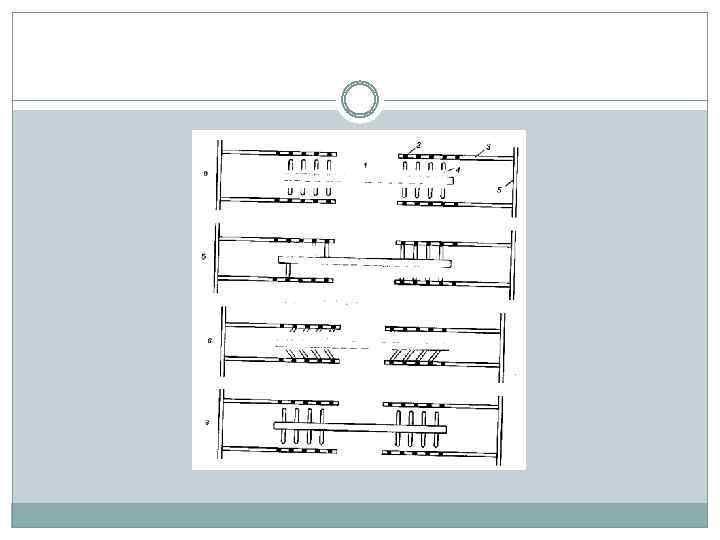

При расслаблении мышцы активизируется работа кальциевого насоса, что понижает концентрацию Са 2+ в цитоплазме; связи между тонкими и толстыми нитями не могут образовываться. В этих условиях при растяжении мышцы нити беспрепятственно скользят относительно друга. Однако такая растяжимость возможна только в присутствии АТФ

Если в клетке отсутствует АТФ, то актин- миозиновый комплекс не может разорваться. Нити остаются жестко сцепленными между собой. Это явление наблюдается при трупном окоченении. Существует два режима сокращения мышцы: изотоническое (изменяется длина волокна, а напряжение остается неизменным) и изометрическое (концы мышцы неподвижно закреплены, вследствие чего изменяется не длина, а напряжение).

Основные положения модели скользящих нитей: 1. Длины нитей актина и миозина в ходе сокращения не меняются. 2. Изменение длины саркомера при сокращении - результат относительного продольного смещения нитей актина и миозина. 3. Поперечные мостики, отходящие от миозина, могут присоединяться к комплементарным центрам актина. 4. Мостики прикрепляются к актину не одновременно.

5. 6. Замкнувшиеся мостики подвергаются структурному переходу, при котором они развивают усилие, после чего происходит их размыкание. Сокращение и расслабление мышцы состоит в нарастании и последующем уменьшении числа мостиков, совершающих цикл замыкание-размыкание.

7. Каждый цикл связан с гидролизом одной молекулы АТФ. 8. Акты замыкания-размыкания мостиков происходят независимо друг от друга.

Мышцы можно представить как сплошную среду, то есть среду, состоящую из большого числа элементов, взаимодействующих между собой без соударений и находящихся в поле внешних сил. Мышца одновременно обладает свойством упругости и вязкости, то есть является вязкоупругой средой. Для такой среды предполагаются справедливыми законы классической механики.

Фундаментальными понятиями механики сплошных сред являются деформация, напряжение, упругость, вязкость, а также энергия и температура.

МОЩНОСТЬ И СКОРОСТЬ СОКРАЩЕНИЯ МЫШЦЫ Важными характеристиками работы мышцы являются сила и скорость сокращения. Уравнения, выражающие эти характеристики, были эмпирически получены А. Хиллом и впоследствии подтверждены кинетической теорией мышечного сокращения (модель Дещеревского).

Уравнение Хилла, связывающее между собой силу и скорость сокращения мышцы, имеет следующий вид: (1)

где v - скорость укорочения мышцы; Р - мышечная сила); vmax - максимальная скорость укорочения мышцы; Р 0—сила, развиваемая мышцей в изометрическом режиме сокращения, при которой не происходит изменение длины мышцы (Р=P 0, при v=0); а и b - константы. Приведенное уравнение имеет вид гиперболы.
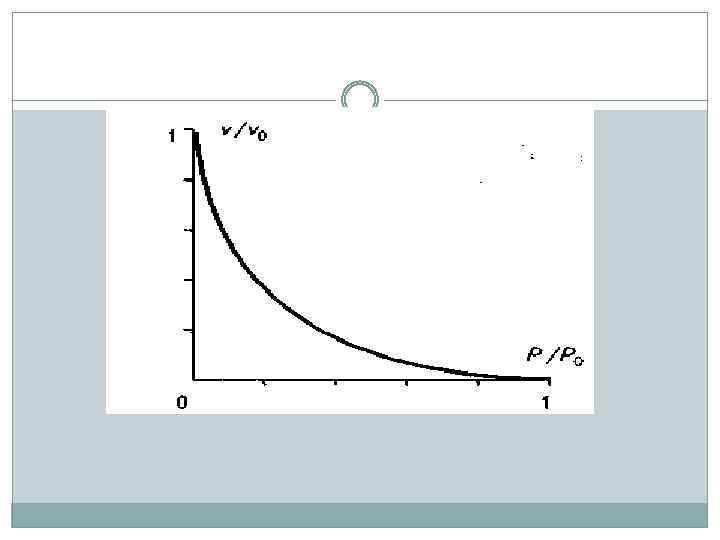

При сокращении за время t мышца совершает работу А: Выразив v из уравнения Хилла, получаем:

В процессе сокращения мышцы выделяется некоторое количество теплоты Q. Эта величина называется теплопродукцией. Как показал Хилл, теплопродукция зависит только от изменения длины х мышцы и не зависит от нагрузки Р: Q = ax.

Общая мощность Nобщ, развиваемая мышцей, определяется скоростями выполнения мышцей работы и выделения теплоты

Подставив выражение (3. 3. 4) в (3. 3. 5), получаем следующее

или, как следует из уравнения Хилла, то есть зависимость мощности Nобщ от нагрузки Р является линейной

Коэффициент полезного действия мышцы записывается в виде: где Ру = Nпоп - полезная мощность. КПД мышцы сохраняет постоянное значение (около 40%) в диапазоне значений силы от 0, 2 Р 0 до 0, 8 Р 0.

Константы а и b имеют постоянные значения для данной мышцы. Константа а имеет размерность силы, а и b - скорости. Константа b в значительной степени зависит от температуры, например, при нагревании на 10°С вблизи 0°С b удваивается. Константа а находится в диапазоне значений от 0, 25 Р 0 до 0, 4 Р 0. По этим данным легко оценить максимальную скорость сокращения для данной мышцы. Так как (следует из последнего равенства уравнения Хилла)

то, следовательно, vmax превышает константу b в 2, 5 -4 раза.

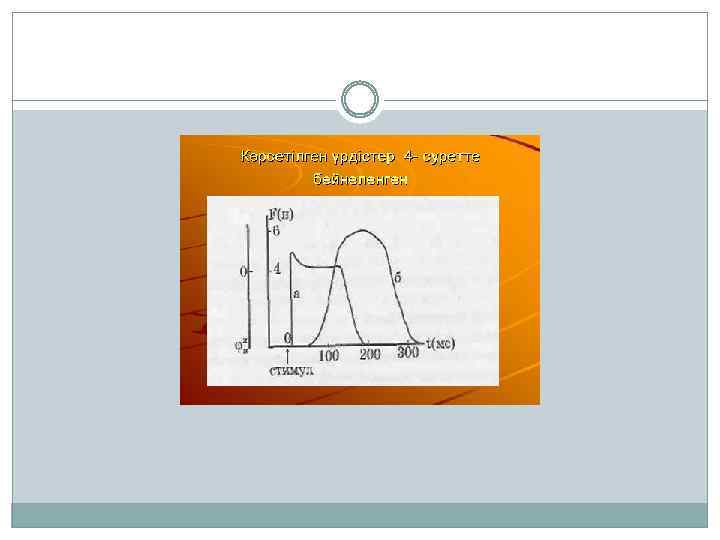
Схема электромеханического сопряжения в кардиомиоците

(М - клеточная мембрана-сарколемма, СР - саркоплазматический ретикулум, МФ миофибрилла, Z -z-диски, Т - Т-система поперечных трубочек); 1 - поступления Nа+ и 2 - поступления Са 2+ в клетку при возбуждении мембраны, 3 - "кальциевый залп", 4 - активный транспорт Са 2+ в СР, 5 - выход из клетки К+, вызывающий реполяризацию мембраны, 6 - активный транспорт Са 2+ из клетки.

Нарушение работы мышц (например, определяющих функционирование легких, сердца) может приводить к патологиям, а ее прекращение - даже к летальному исходу.


Уравнение Хилла. Мощность одиночного сокращения Зависимость скорости укорочения от нагрузки Р является важнейшей при изучении работы мышцы, так как позволяет выявить закономерности мышечного сокращения и его энергетики.
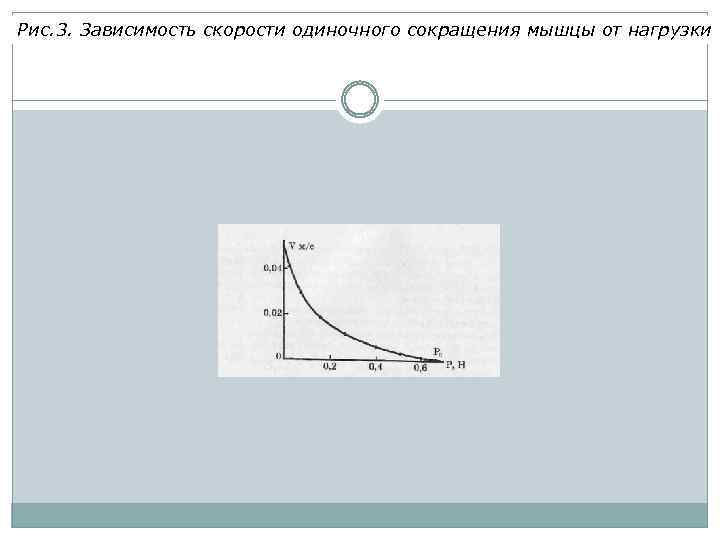
Рис. 3. Зависимость скорости одиночного сокращения мышцы от нагрузки

уравнение Хилла –характеристическа механики мышечного сокращения. Р 0 – максимальное изометрическое напряжение, развиваемое мышцей, или максимальный груз, удерживаемый мышцей без ее удлинения; b - константа, имеющая размерность скорости, а - константа, имеющая размерность силы.

Моделирование мышечного сокращения Математическая модель сокращения мышцы, предложена В. Дещеревским, на модели скользящих нитей

В расслабленном состоянии миофибрилл молекулы тропомиозина блокируют прикрепление поперечных мостиков к актиновым цепям.

Ионы Са 2+ активируют мостики и открывают участки их прикрепления к актину.
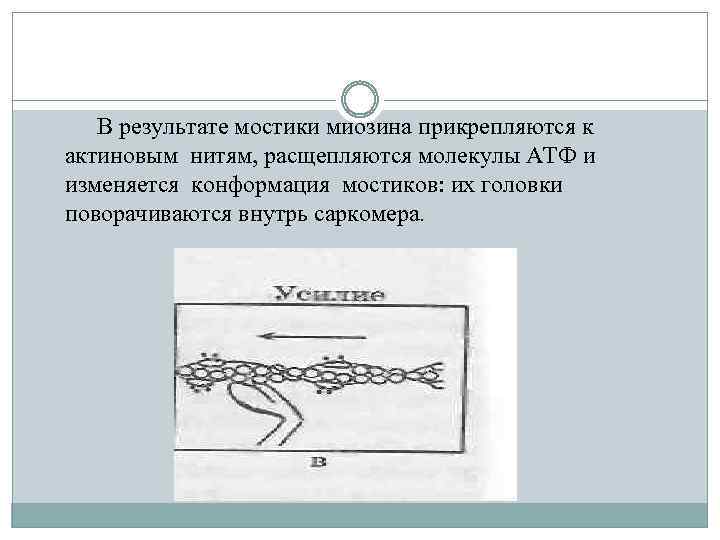
В результате мостики миозина прикрепляются к актиновым нитям, расщепляются молекулы АТФ и изменяется конформация мостиков: их головки поворачиваются внутрь саркомера.

Это приводит к генерации силы, скольжению актина относительно толстой нити миозина к центру саркомера, что вызывает укорочение мышцы. После окончания активации мостик размыкается, и саркомер возвращается в исходное состояние. При укорочении объем саркомера практически не меняется, а, следовательно, он становится толще, что и подтверждается на снимках поперечного сечения мышц с помощью электронной микроскопии.

Каждый цикл замыкание-размыкание сопровождается расщеплением одной молекулы АТФ. Таким образом, актин-миозиновый комплекс является механохимическим преобразователем энергии АТФ. Рассмотренная структура и последовательность процессов называется моделью скользящих нитей.

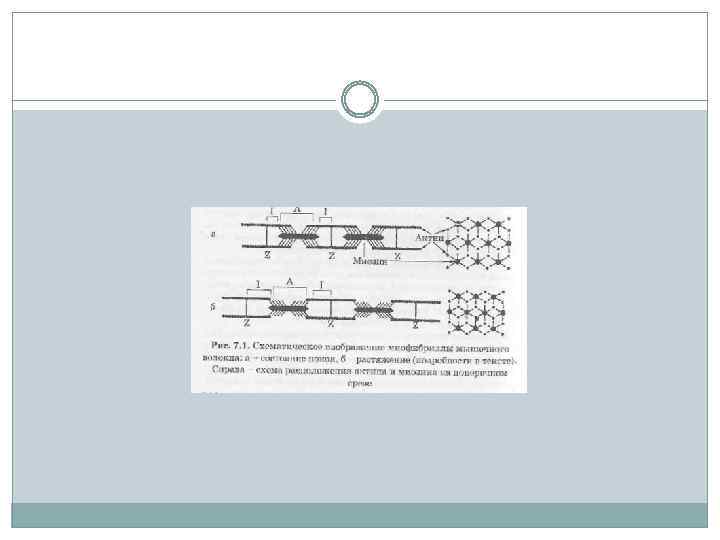

В клетках поперечнополосатых мышц в состав тонких нитей кроме актина и тропомиозина входит еще и белок тропонин. На каждый шаг спирали F-актина приходится две молекулы тропонина.

В области I-зоны проходит темная узкая полоса - Z-диск (от нем. zwischenscheibe промежуточный диск). Промежуток между двумя Z-дисками называется саркомером и является элементарной сократительной единицей мышечной клетки.

Диск I включает в себя только тонкие нити, диск А — и толстые, и тонкие. В середине диска А видна светлая полоса, называемая Н-зоной. Она не имеет тонких нитей. Диск I разделен тонкой полосой Z, которая представляет собой мембрану, содержащую структурные элементы, скрепляющие между собой концы тонких нитей. Участок между двумя Z-линиями называется саркомером.

Каждая толстая нить окружена шестью тонкими, а каждая тонкая – тремя толстыми. Таким образом, в поперечном срезе мышечное волокно имеет правильную гексагональную структуру.
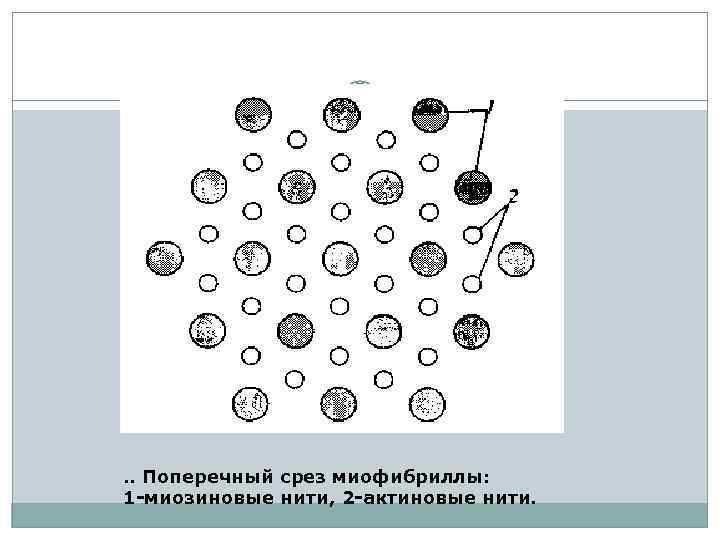
. . Поперечный срез миофибриллы: 1 -миозиновые нити, 2 -актиновые нити.
Биофизика мышцы.ppt