4.Биофизика БМ.pptx
- Количество слайдов: 94

Биофизика мембранных процессов ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 1

Биомембраны – это функциональные высокоорганизованные структуры клеток, ограничивающие цитоплазму и большинство внутриклеточных органелл, а также образующие единую внутриклеточную систему каналов и полостей.

Функции биомембран (БМ) • • • Барьерная – поддержание автономности и компартментализации клетки Матриксная – БМ- матрица для протекания важнейших процессов жизнедеятельности: - Внутренняя мембрана митохондрий содержит ЭТЦ и участвует в синтезе АТФ - Мембраны тилакоидов в хлоропластах участвуют в фотосинтезе - Мембраны ЭПР участвует в: а)синтезе белков, липидов; б)детоксикации ксенобиотиков Транспортная Рецепторная, участие в клеточной сигнализации Межклеточная коммуникация (адгезия, щелевые контакты) Электрическая возбудимость и проведение нервного импульса Определяет гормональный и иммунный ответы Участие в запуске апоптоза (митохондриальная и плазматическая мембраны) Фоторецепторные мембраны участвуют в зрительном восприятии Нарушение стабильности и структуры БМ – основа многих патологий (мембранная патология).
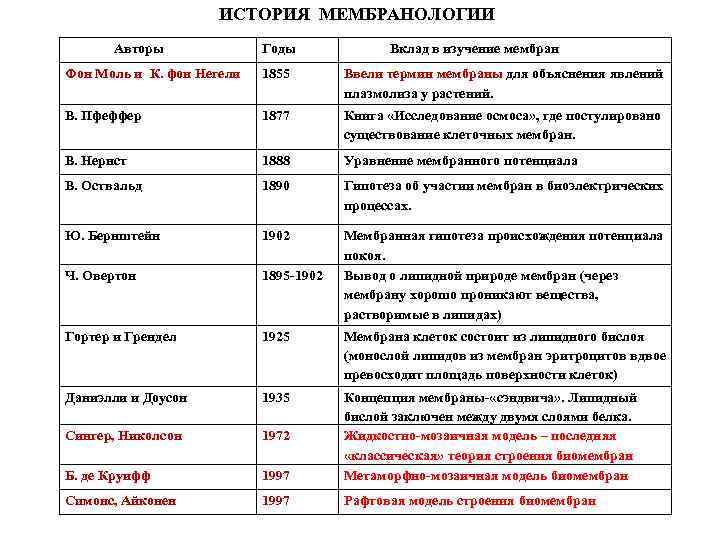
ИСТОРИЯ МЕМБРАНОЛОГИИ Авторы Годы Вклад в изучение мембран Фон Моль и К. фон Негели 1855 Ввели термин мембраны для объяснения явлений плазмолиза у растений. В. Пфеффер 1877 Книга «Исследование осмоса» , где постулировано существование клеточных мембран. В. Нернст 1888 Уравнение мембранного потенциала В. Оствальд 1890 Гипотеза об участии мембран в биоэлектрических процессах. Ю. Бернштейн 1902 Ч. Овертон 1895 -1902 Мембранная гипотеза происхождения потенциала покоя. Вывод о липидной природе мембран (через мембрану хорошо проникают вещества, растворимые в липидах) Гортер и Грендел 1925 Мембрана клеток состоит из липидного бислоя (монослой липидов из мембран эритроцитов вдвое превосходит площадь поверхности клеток) Даниэлли и Доусон 1935 Сингер, Николсон 1972 Б. де Круифф 1997 Концепция мембраны- «сэндвича» . Липидный бислой заключен между двумя слоями белка. Жидкостно-мозаичная модель – последняя «классическая» теория строения биомембран Метаморфно-мозаичная модель биомембран Симонс, Айконен 1997 Рафтовая модель строения биомембран
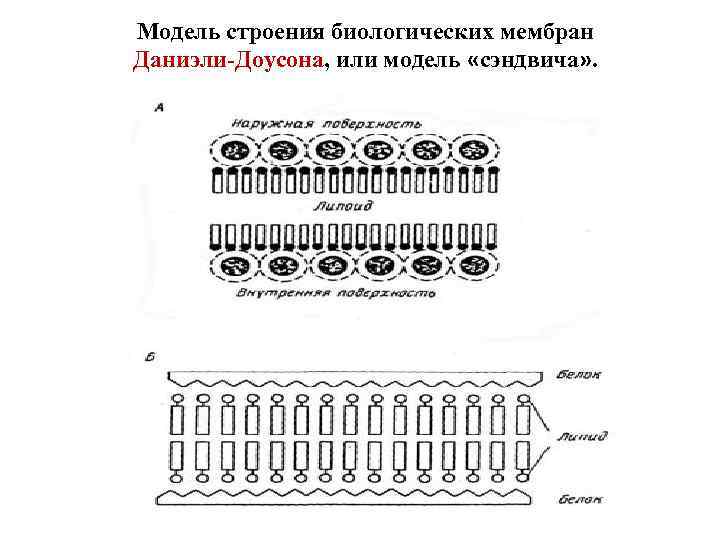
Модель строения биологических мембран Даниэли-Доусона, или модель «сэндвича» .
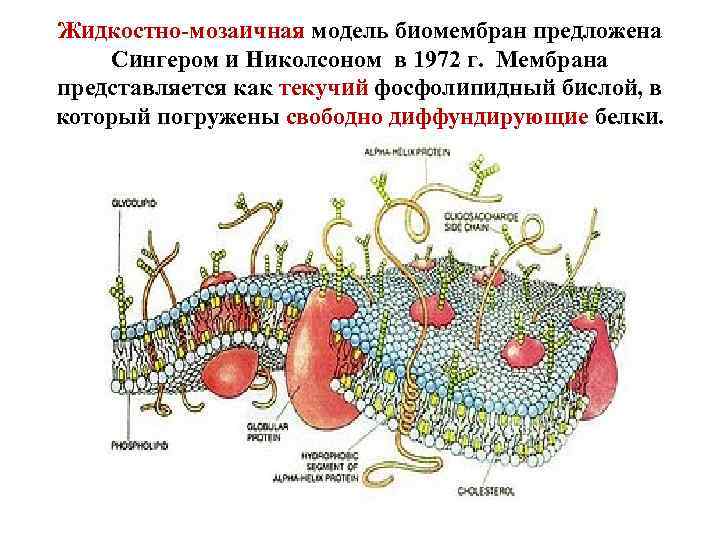
Жидкостно-мозаичная модель биомембран предложена Сингером и Николсоном в 1972 г. Мембрана представляется как текучий фосфолипидный бислой, в который погружены свободно диффундирующие белки.
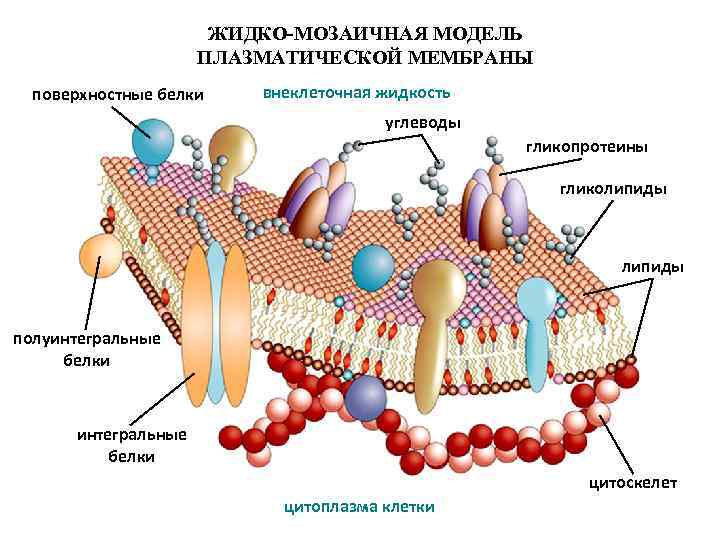
ЖИДКО-МОЗАИЧНАЯ МОДЕЛЬ ПЛАЗМАТИЧЕСКОЙ МЕМБРАНЫ поверхностные белки внеклеточная жидкость углеводы гликопротеины гликолипиды полуинтегральные белки цитоскелет цитоплазма клетки
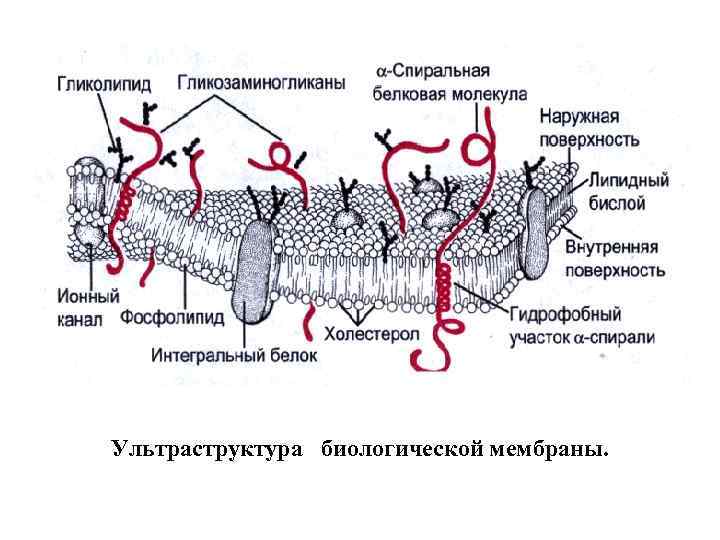
Ультраструктура биологической мембраны.

Жидкостно-мозаичная модель строения биомембран (БМ) 1. БМ различного происхождения имеют общий план строения. 2. БМ - ансамбли липидов и белков, которые удерживаются вместе за счет нековалентных (слабых) взаимодействий, важнейшие из них - гидрофобные взаимодействия. Минорные компоненты мембран - гликолипиды и гликопротеины. Имеется мембранная вода. 3. Липиды образуют двойной липидный слой, который находится в жидко-кристаллическом состоянии. 4. Белки встроены в липидный матрикс подобно элементам мозаики и могут свободно перемещаться в мембране. 5. Липидам отводится пассивная роль, основная роль принадлежит белкам. 6. Наблюдается трансмембранная асимметрия.

• Липидный бислой представлен преимущественно молекулами фосфолипидов состоящими из двух длинных неполярных (гидрофобных) цепей жирных кислот и полярной (гидрофильной) головки. • В мембране гидрофобные цепи обращены внутрь бислоя, а гидрофильные головки – кнаружи.

Недостатки жидкостно-мозаичной модели 1. Не все белки свободно диффундируют в жидком липидном бислое. 2. Имеются отличия от классического липидного бислоя за счет липидного полиморфизма. Наблюдаются вариации толщины и образование небислойных структур. 3. Наблюдается неоднородность мембраны за счет явления латеральной гетерогенности бислоя (рафты). 4. Мембранные липиды имеют не меньшее значение, чем мембранные белки. Разрабатывается метаморфно-мозаичная и рафтовая модели БМ

Жидкостно-мозаичная модель строения мембран названа «последней классической» теорией потому что, с одной стороны, она явно устарела, а с другой – современные представления не достигли еще той лаконичной изящности, чтобы их начала можно было бы легко изложить в школьном учебнике (Bagatolli et al. , 2010).

Метаморфно-мозаичная модель биомембран
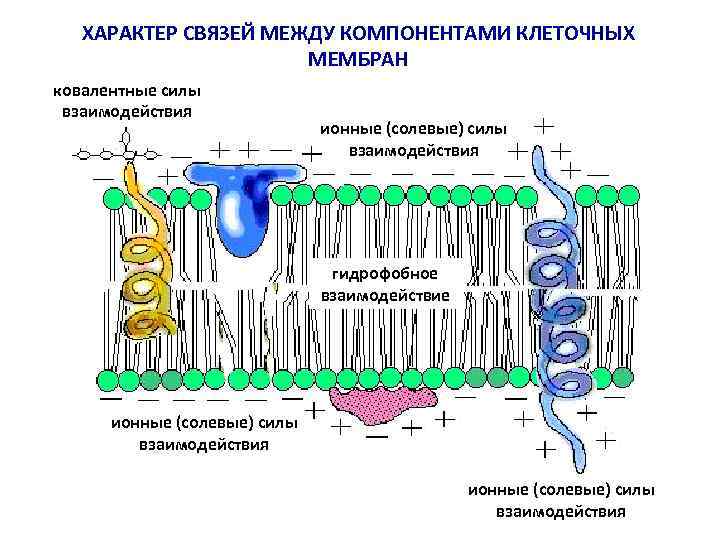
ХАРАКТЕР СВЯЗЕЙ МЕЖДУ КОМПОНЕНТАМИ КЛЕТОЧНЫХ МЕМБРАН ковалентные силы взаимодействия ионные (солевые) силы взаимодействия гидрофобное взаимодействие ионные (солевые) силы взаимодействия

Мембранные липиды

Мембранные липиды представлены 3 классами: фосфолипиды, гликосфинголипиды, стероиды Фосфолипиды делятся на 2 группы: 1. Глицерофосфолипиды – производные фосфатидной кислоты, к гидроксилу фосфорной кислоты которой с помощью простой эфирной связи присоединен радикал Х. (фосфатидилхолин, фосфатидилэтаноламин, фосфатидилсерин, фосфатидилинозитол). 2. Сфингофосфолипиды – производные церамида (жирнокислотного эфира ненасыщенного аминоспирта сфингозина) и монофосфорных эфиров спиртов (сфингомиелин).





Гликосфинголипиды – гликозильные производные церамида, делятся на группы: 1. Цереброзиды – к ОН-группе первого углеродного атома церамида присоединен моно- или олигосахаридный остаток. 2. Ганглиозиды – к ОН-группе церамида присоединен сложный, разветвленный олигосахарид, N-ацетилнейраминовая кислота. 3. Сульфатиды – сульфопроизводные гликолипидов

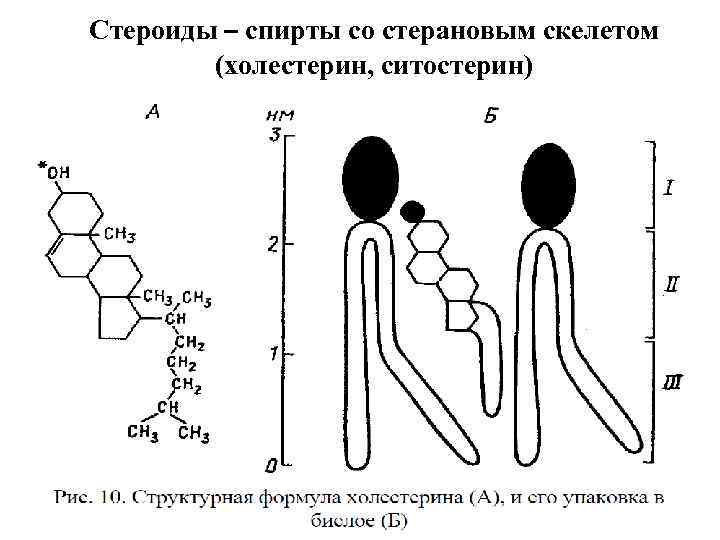
Стероиды – спирты со стерановым скелетом (холестерин, ситостерин)
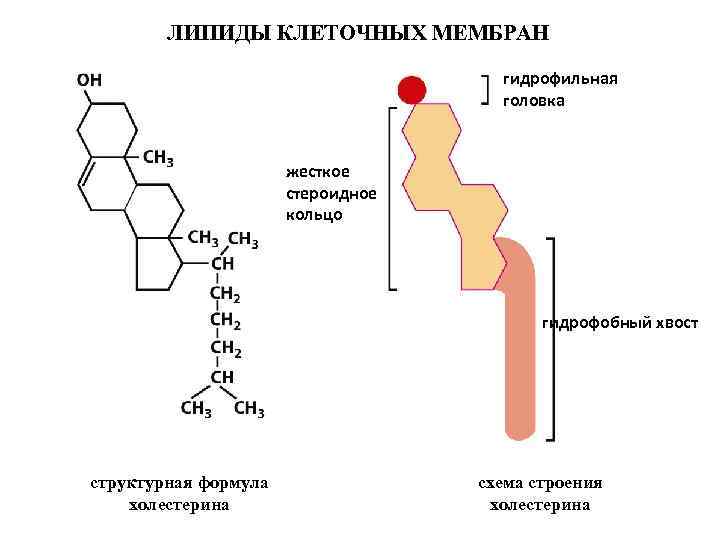
ЛИПИДЫ КЛЕТОЧНЫХ МЕМБРАН гидрофильная головка жесткое стероидное кольцо гидрофобный хвост структурная формула холестерина схема строения холестерина

Роль холестерина в биомембранах 1. Регулирует правильную упаковку мембранных липидов: - если мембрана слишком ригидна, вызывает ее разжижение; -если мембрана слишком «жидкая» (текучая), то вызывает ее уплотнение. 2. Взаимная укладка ФЛ и Хол: неполярные цепи ФЛ вытянуты, а его полярная головка изогнута в виде трости. В образующуюся полость помещается Хол. Другой способ укладки – образование рафтов. 3. Локализован преимущественно в плазматических мембранах.
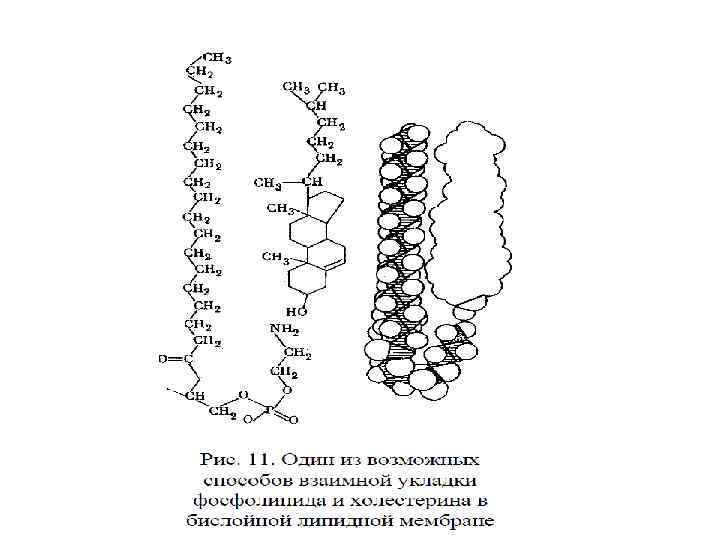

Принципы организации липидного бислоя 1. Амфифильность фосфолипидов. 2. Полиморфизм липидов – способность образовывать агрегаты различных типов, которые могут переходить друг в друга. 3. Фазовые переходы мембранных липидов. 4. Текучесть (микровязкость) биомембран. 5. Латеральная гетерогенность мембранных липидов. 6. Подвижность мембранных липидов. 7. Трансбислойная асимметрия липидов.
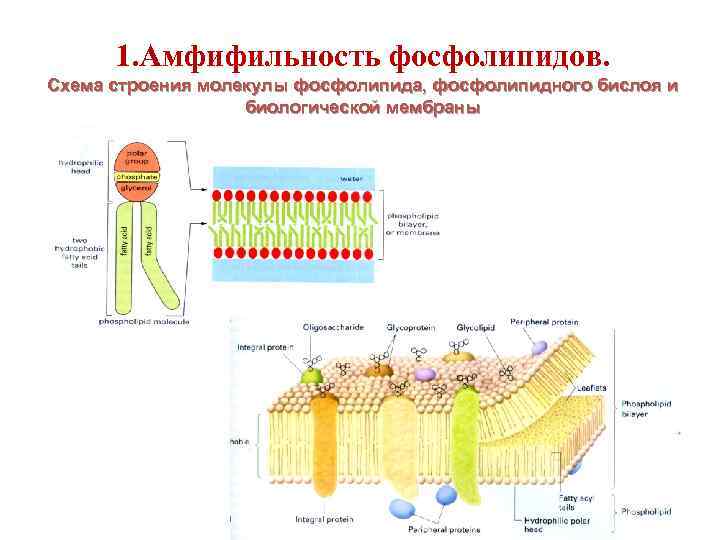
1. Амфифильность фосфолипидов. Схема строения молекулы фосфолипида, фосфолипидного бислоя и биологической мембраны

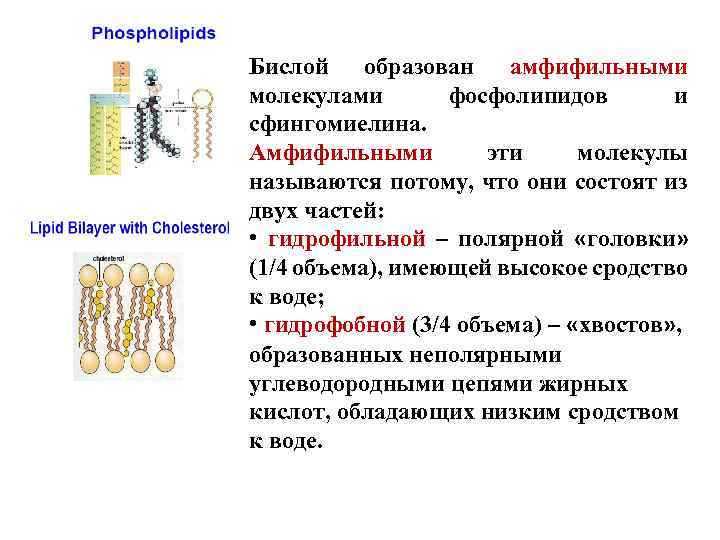
Бислой образован амфифильными молекулами фосфолипидов и сфингомиелина. Амфифильными эти молекулы называются потому, что они состоят из двух частей: • гидрофильной – полярной «головки» (1/4 объема), имеющей высокое сродство к воде; • гидрофобной (3/4 объема) – «хвостов» , образованных неполярными углеводородными цепями жирных кислот, обладающих низким сродством к воде.
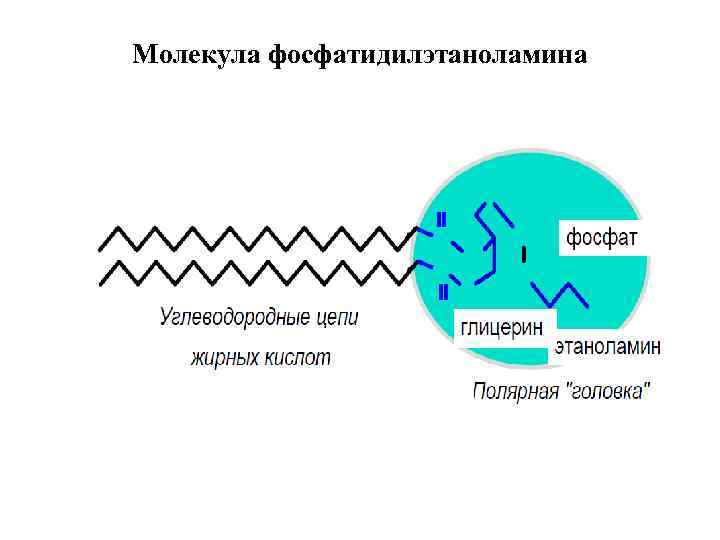
Молекула фосфатидилэтаноламина
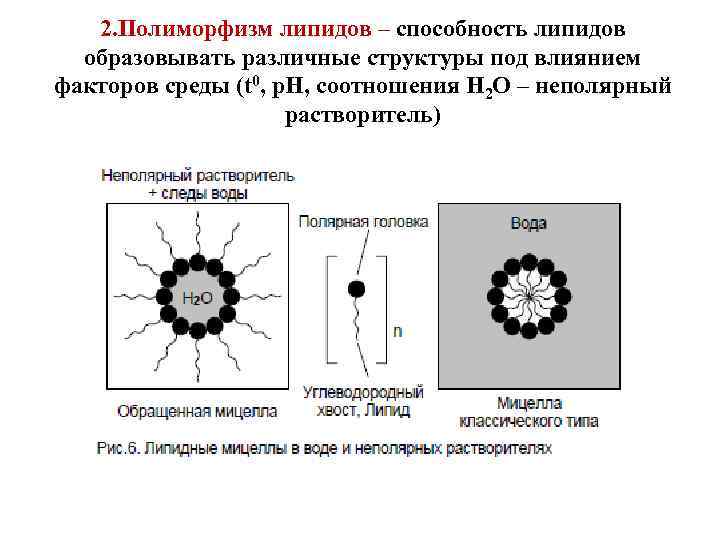
2. Полиморфизм липидов – способность липидов образовывать различные структуры под влиянием факторов среды (t 0, p. H, соотношения H 2 O – неполярный растворитель)
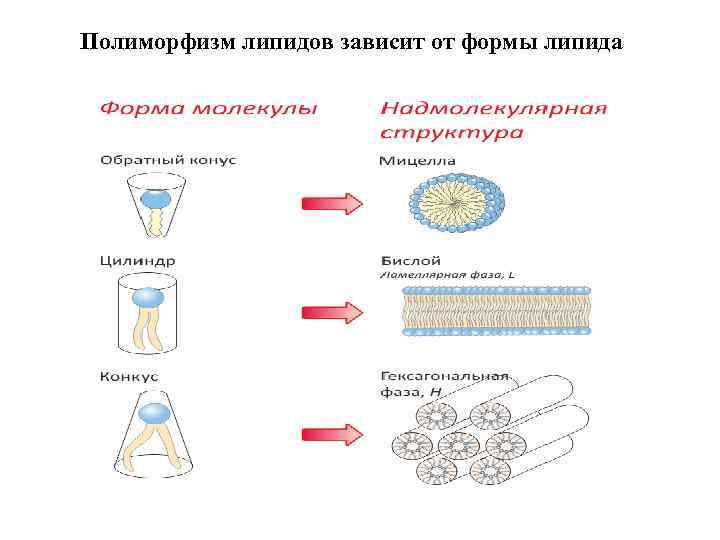
Полиморфизм липидов зависит от формы липида

Основные типы структурной организации водно-липидных систем ламеллярные 1/2 < p < 1 неламеллярные

3. Фазовые переходы мембранных липидов Мембранные липиды в бислое могут находиться в 3 фазах: - твердо-кристаллической So (solid ordered) (гель): толщина бислоя максимальна, площадь на молекулу липида минимальна; - жидко-кристаллической L (liquid), которая делится на 2 фазы (толщина бислоя минимальна, площадь на молекулу липида максимальна): а) жидкая упорядоченная Lo (liquid ordered): высокая упорядоченность жирнокислотных ацилов, но высокая латеральная подвижность липидных доменов (мезофаза); б) жидкая неупорядоченная Ld (liquid disordered): липидные хвосты максимально неупорядочены.

Точка фазового перехода или температура плавления Это такая температура, при которой 50% липидов находятся в жидкокристаллическом состоянии, а 50% липидов – в твердо-кристаллическом состоянии У теплокровных животных и человека точка фазового перехода лежит в области отрицательных температур
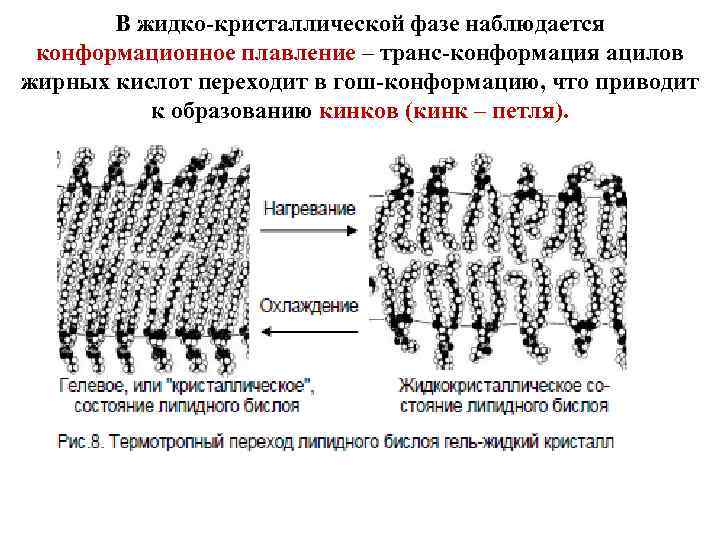
В жидко-кристаллической фазе наблюдается конформационное плавление – транс-конформация ацилов жирных кислот переходит в гош-конформацию, что приводит к образованию кинков (кинк – петля).
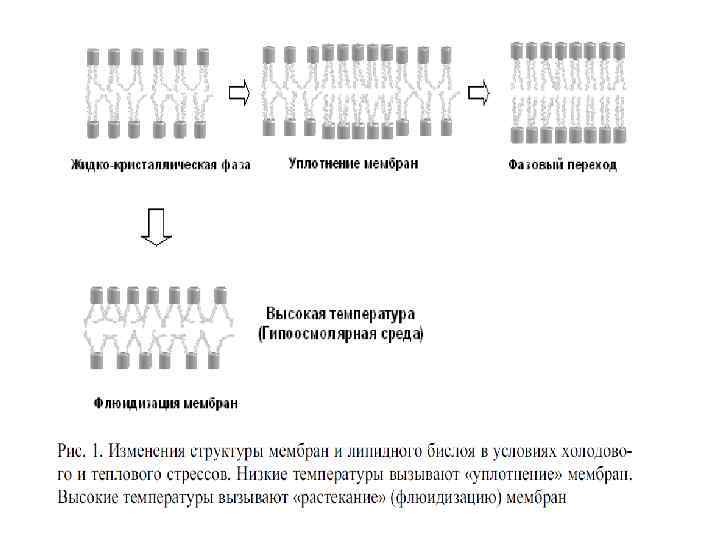

4. Текучесть (микровязкость) липидной фазы биомембран регулирует мембранные процессы. 1. В физиологических условиях липиды мембран имеют жидко-кристаллическую структуру, что необходимо для нормального функционирования. 2. Степень текучести мембран зависит от: - длины жирнокислотных цепей и степени их ненасыщенности; - соотношения фосфолипиды/стерины; - взаимодействия между ФЛ и белками; - физических факторов (to , р, р. Н, потенциала)

Текучесть БМ зависит от: 1. Ненасыщенности мембранных липидов: увеличение количества двойных связей повышает текучесть мембраны. 2. Длины ЖК-цепи: удлинение ацильной цепи уменьшает текучесть мембраны. 3. Температуры среды: увеличение температуры повышает текучесть мембраны

Мембранные липиды – мишень адаптации – повышение ненасыщенности жирнокислотных цепей мембранных липидов по мере продвижения к дистальному отделу конечности полярных животных и птиц

5. Латеральная гетерогенность мембранных липидов. Латеральная гетерогенность мембраны – это свойство бислойной мембраны образовывать неоднородные несмешиваемые микрофазы (рафты).

Мембранные рафты – это маленькие (10 -200 нм), гетерогенные липидные домены, обогащенные холестеролом, сфинголипидами, специфическими белками, более структурированные и упорядоченные, чем окружающая «жидкая» фаза, могут свободно перемещаться и образовывать «платформы» Биологическая роль рафтов 1. Группировка и сортировка белков для выполнения функций. 2. Деление клеток. 3. Везикулярный транспорт. 4. Способствуют проникновению вирусов в клетку и выходу из клетки. 5. Способноствуют проникновению токсинов в клетку.

Рафты наряду с важной биологической ролью в определенных условиях становятся «троянским конем» для клетки Перед тем, как снять осаду, нападающие сообщили троянцам, что построенный ими деревянный «конь» - это символ мира и приношение Афине в знак искупление грехов. И пока он будет стоять, они не нападут. Поздно ночью тридцать бойцов во главе с Одиссеем выбрались из «подарка» и открыли ворота города. В эту ночь Троя пала.
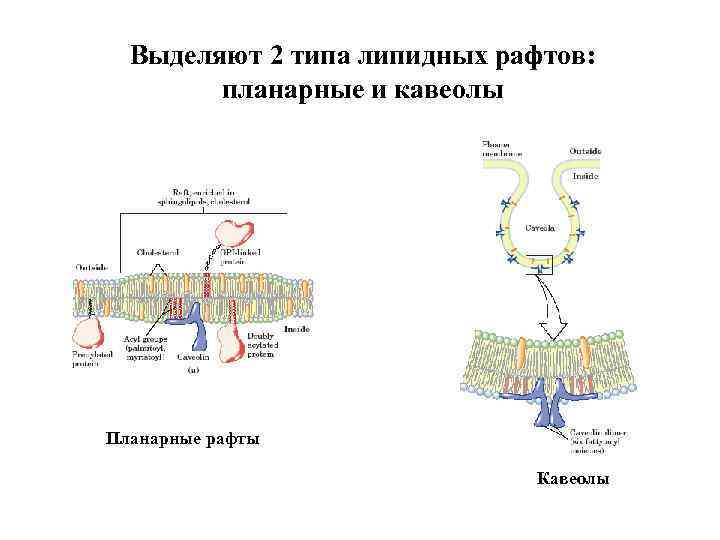
Выделяют 2 типа липидных рафтов: планарные и кавеолы Планарные рафты Кавеолы
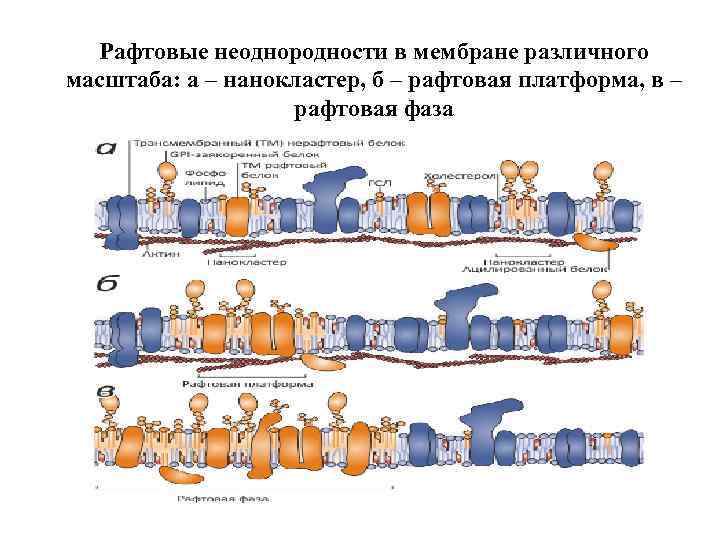
Рафтовые неоднородности в мембране различного масштаба: а – нанокластер, б – рафтовая платформа, в – рафтовая фаза

Взаимодействие лейкоцитов с липидными рафтами

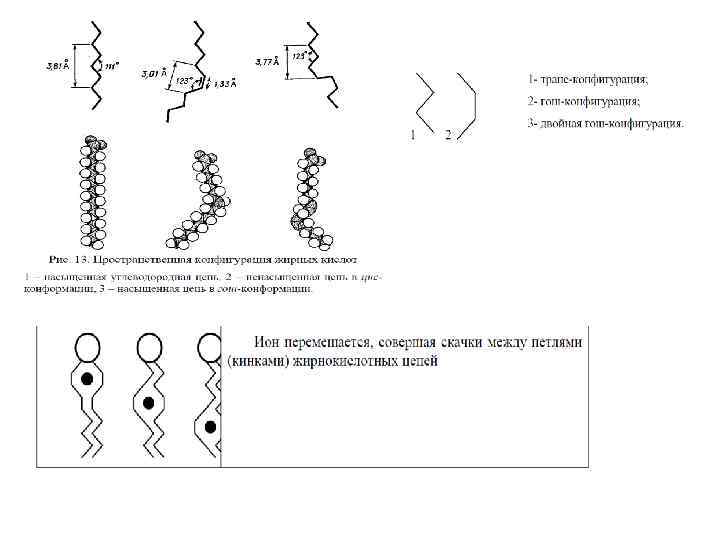
6. Различные виды подвижности мембранных липидов 1. Изменение ориентации полярных голов. 2. Латеральная подвижность. 3. Сегментарная подвижность – колебания ацильных цепей. 4. Образование кинков и их миграция вдоль ацильных цепей. 5. Ротационная подвижность. 6. Флип-флоп переходы. 7. Выход из бислоя.

7. Трансбислойная асимметрия мембранных липидов – это различное распределение липидов между внутренним и наружным монослоями. 1. Во внешнем монослое локализуются холинсодержащие ФЛ – фосфатидилхолин, сфингомиелин, а также стероид холестерол. 2. Во внутреннем монослое локализуются аминосодержащие ФЛ – фосфатидилэтаноламин, фосфатидилсерин. 3. Во внешнем монослое – 1/3 двойных связей, во внутреннем – 2/3 двойных связей. 4. Известны 2 механизма, обеспечивающие асимметрию липидного бислоя: - различия конформационных размеров полярных «головок» липидов; - транслокация с помощью белков-переносчиков.

Трансмембранное перемещение фосфолипидов в двойном липидном слое: • Некатализируемый флип-флоп из одного монослоя в другой; • Катализируемый перенос фосфолипидов в мембране: 1. Флиппазы (АТФ-азы Р-типа) переносят аминофосфолипиды (ФС, ФЭА) от внешнего к внутреннему монослою; 2. Флоппазы (АВС-транспортеры) переносят фосфолипиды от цитозольного монослоя к внешнему монослою (используют АТФ); 3. Скрамблазы выравнивают фосфолипидный состав двух монослоев, нарушают асимметрию (не используют АТФ, активируются Са 2+).
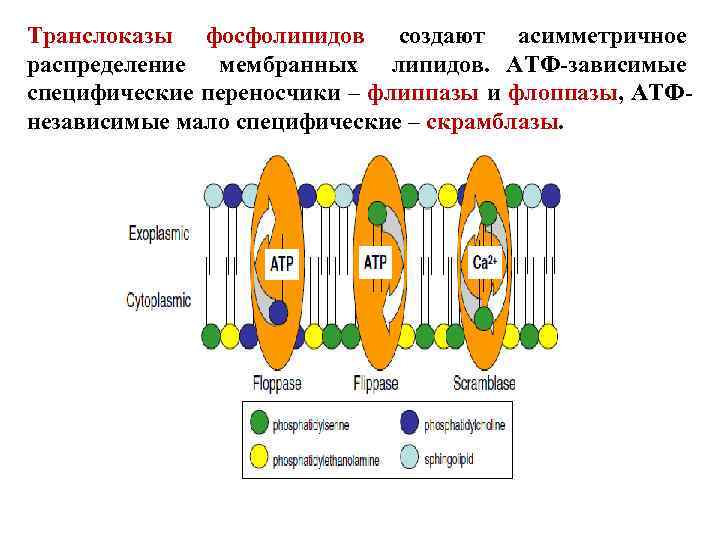
Транслоказы фосфолипидов создают асимметричное распределение мембранных липидов. АТФ-зависимые специфические переносчики – флиппазы и флоппазы, АТФнезависимые мало специфические – скрамблазы.
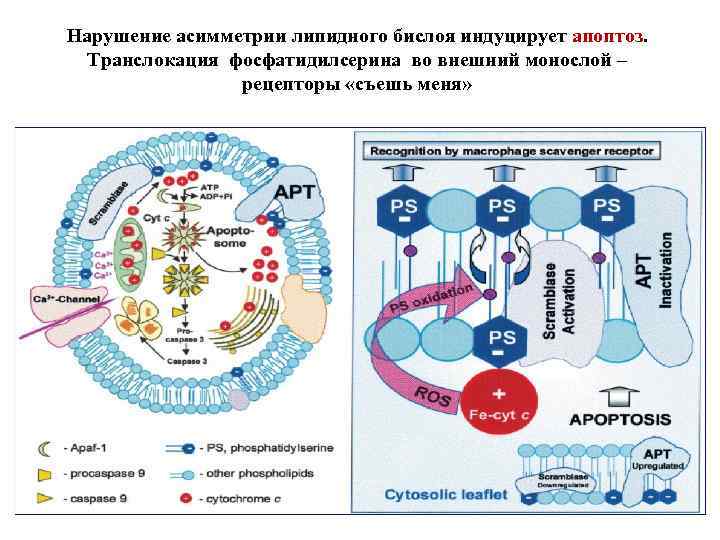
Нарушение асимметрии липидного бислоя индуцирует апоптоз. Транслокация фосфатидилсерина во внешний монослой – рецепторы «съешь меня»

Выделяют 4 вида липидов по типу взаимодействия с белками 1. Аннулярные или иммобилизованные липиды – создают микроокружение мембранных белков 2. «Неаннулярные липиды» - прочно связаны с белком и играют роль кофакторов 3. Липиды общего липидного бислоя или свободного объема (часто находятся в жидко-неупорядоченном состоянии ) 4. Рафтовые липиды – локализованы в рафтах и находятся в жидко-упорядоченном состоянии

Мембранные белки

20 -30% всех белков – мембранные. По своему расположению относительно липидного бислоя мембранные белки разделяются на три типа: 1) Периферические - непрочно связаны с поверхностью мембраны и обычно находятся вне липидного бислоя. очень прочно связаны с мембраной и делятся на: 1. собственно интегральные белки – полностью погружены в липидный бислой; 2. полуинтегральные белки частично погружены в бислой. 3) Амфитропные - белки с переменной гидрофобностью, могут находиться в цитозоле и бислое. 2) Интегральные -
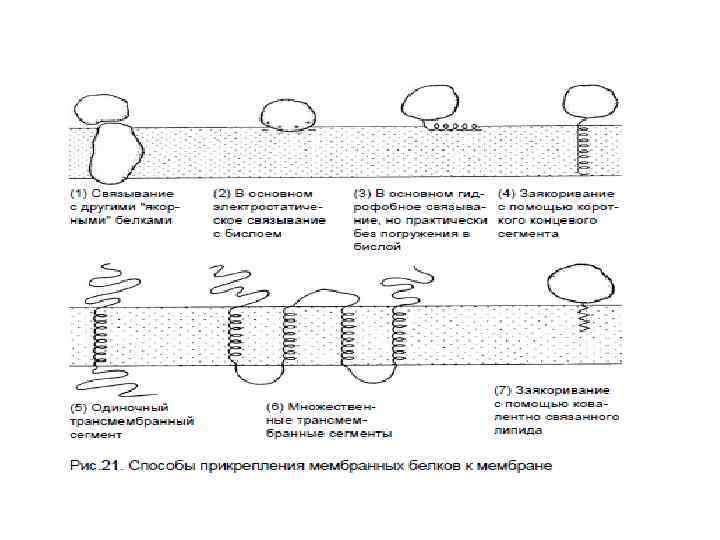

Топологическая классификация мембранных белков: 1. Монотопические – являются периферическими белками и не пронизывают мембрану (цит b 5) 2. Битопические – пронизывают мембрану один раз (гликофорин) 3. Политопические - пронизывают мембрану два и более раз (рецепторы, сопряженные с G-белками; Na, K- АТФ-аза; АТФ-синтаза и др. )
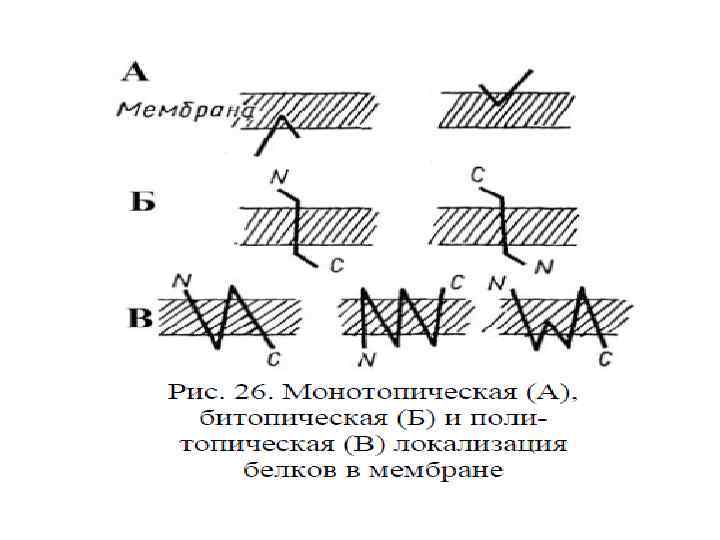

Выделяют 6 типов интегральных белков. I тип – один трансмембранный сегмент, N-конец снаружи II тип – одна трансмембранная спираль, N-конец внутри Ш тип – много трансмембранных спиралей IV тип – трансмембранные домены нескольких полипептидов соединяются с образованием канала через мембрану V тип – белки удерживаются бислоем с помощью ковалентно связанных липидов VI тип – содержат трансмембранные спирали и липидные ГФИ-якори (ГФИ – гликозилфосфатидилинозитол)
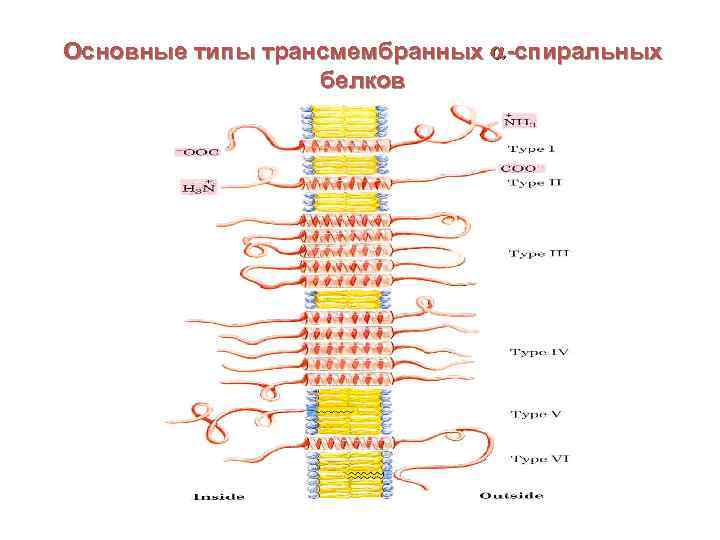
Основные типы трансмембранных -спиральных белков
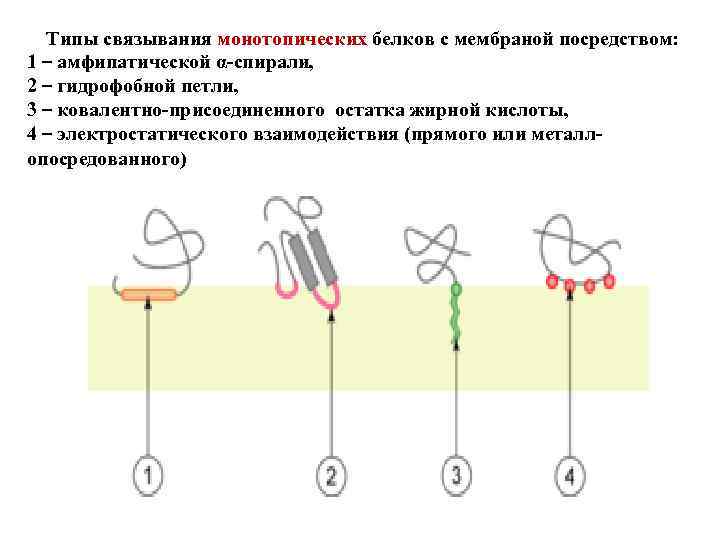
Типы связывания монотопических белков с мембраной посредством: 1 – амфипатической α-спирали, 2 – гидрофобной петли, 3 – ковалентно-присоединенного остатка жирной кислоты, 4 – электростатического взаимодействия (прямого или металлопосредованного)
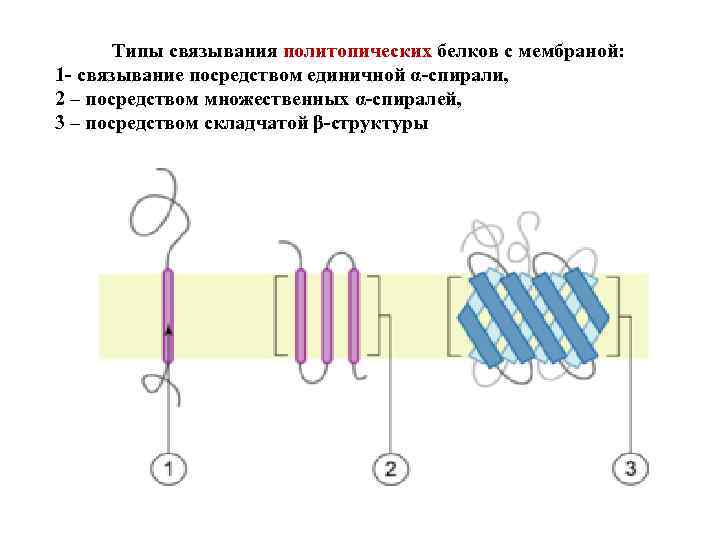
Типы связывания политопических белков с мембраной: 1 - связывание посредством единичной α-спирали, 2 – посредством множественных α-спиралей, 3 – посредством складчатой β-структуры

Функции мембранных белков 1. Ферментативная 2. Рецепторная 3. Транспортная - образуют каналы - белки-подвижные переносчики 4. Межклеточная коммуникация – белки межклеточной адгезии 5. Структурная
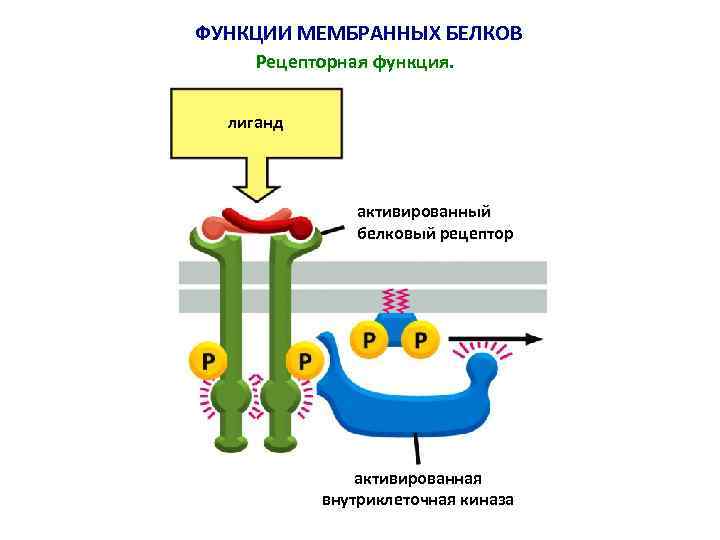
ФУНКЦИИ МЕМБРАННЫХ БЕЛКОВ Рецепторная функция. лиганд активированный белковый рецептор активированная внутриклеточная киназа
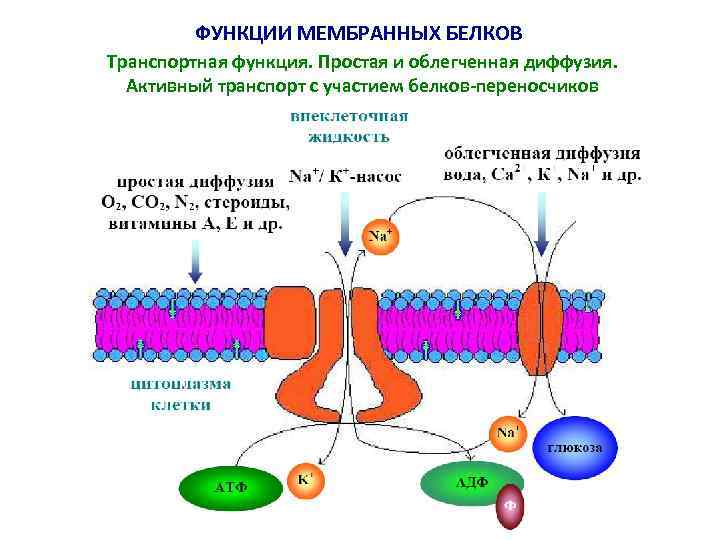
ФУНКЦИИ МЕМБРАННЫХ БЕЛКОВ Транспортная функция. Простая и облегченная диффузия. Активный транспорт с участием белков-переносчиков
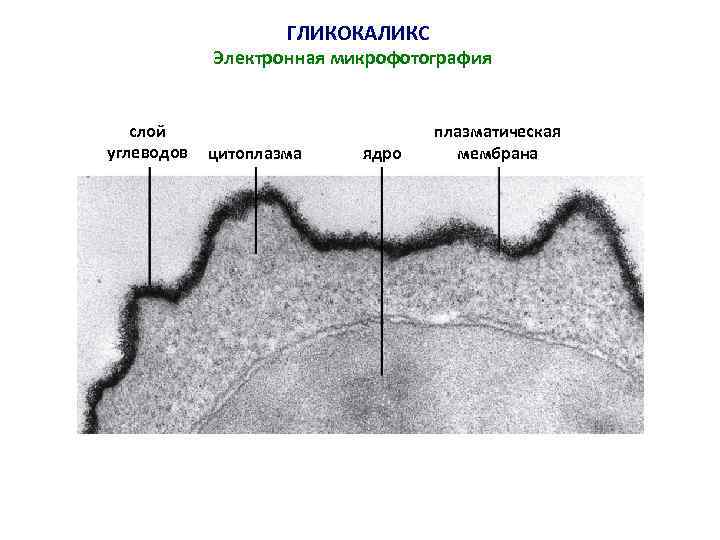
ГЛИКОКАЛИКС Электронная микрофотография слой углеводов цитоплазма ядро плазматическая мембрана
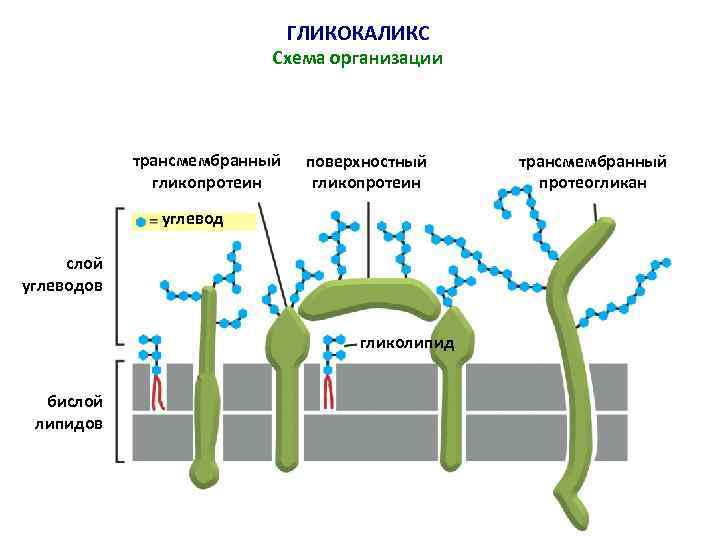
ГЛИКОКАЛИКС Схема организации трансмембранный гликопротеин поверхностный гликопротеин углевод слой углеводов гликолипид бислой липидов трансмембранный протеогликан
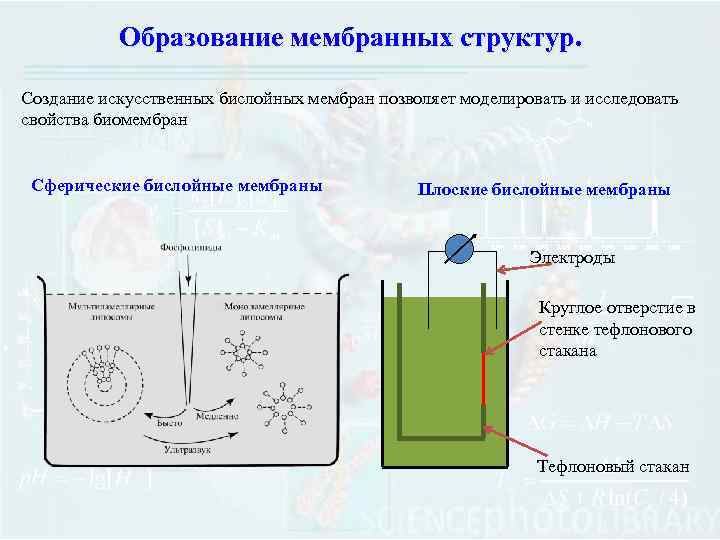
Образование мембранных структур. Создание искусственных бислойных мембран позволяет моделировать и исследовать свойства биомембран Сферические бислойные мембраны Плоские бислойные мембраны Электроды Круглое отверстие в стенке тефлонового стакана Тефлоновый стакан
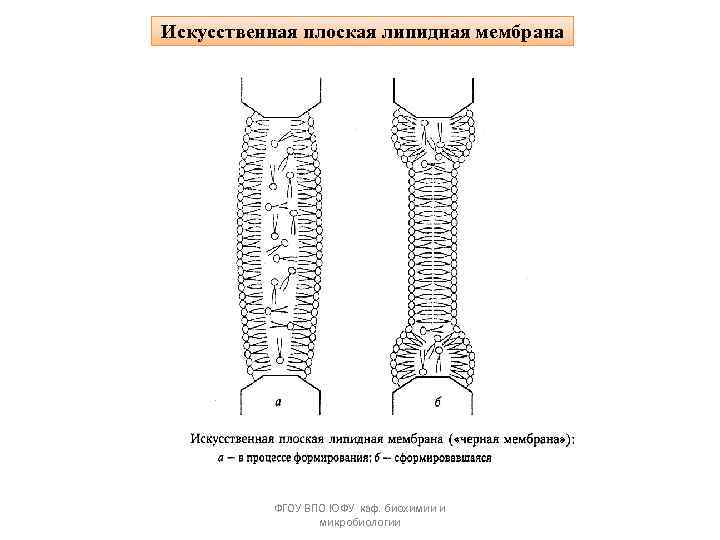
Искусственная плоская липидная мембрана ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
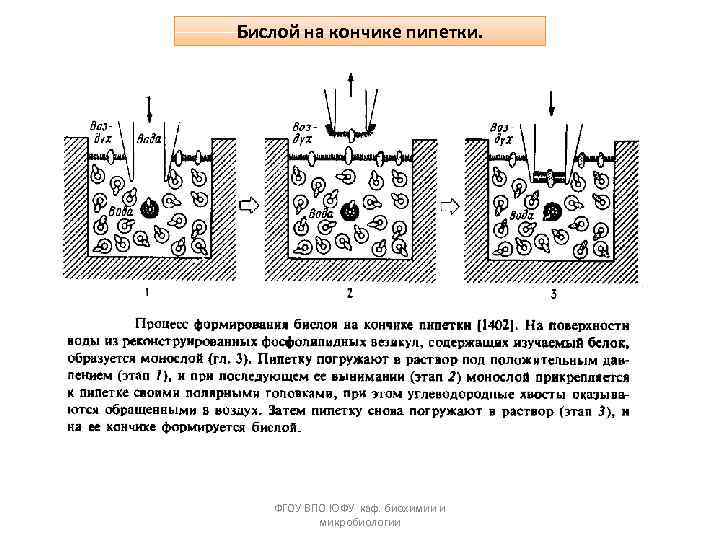
Бислой на кончике пипетки. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
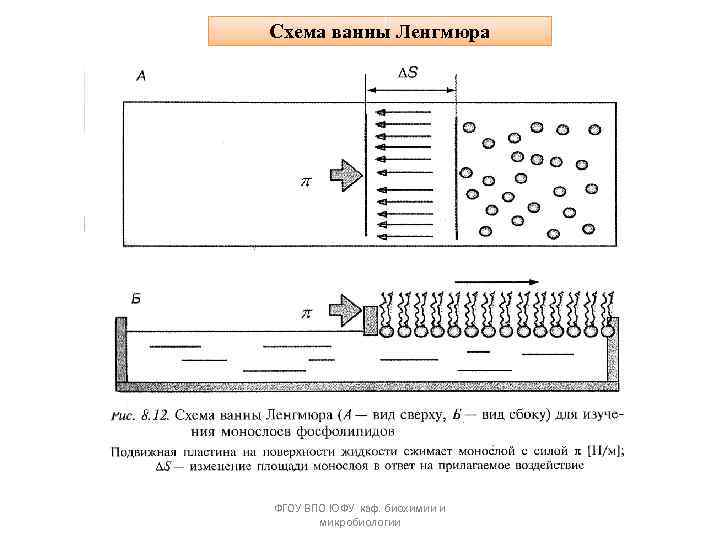
Схема ванны Ленгмюра ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
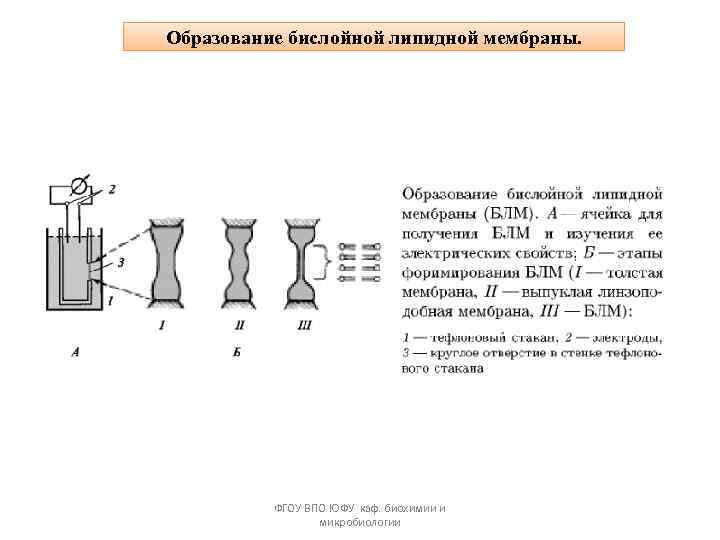
Образование бислойной липидной мембраны. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
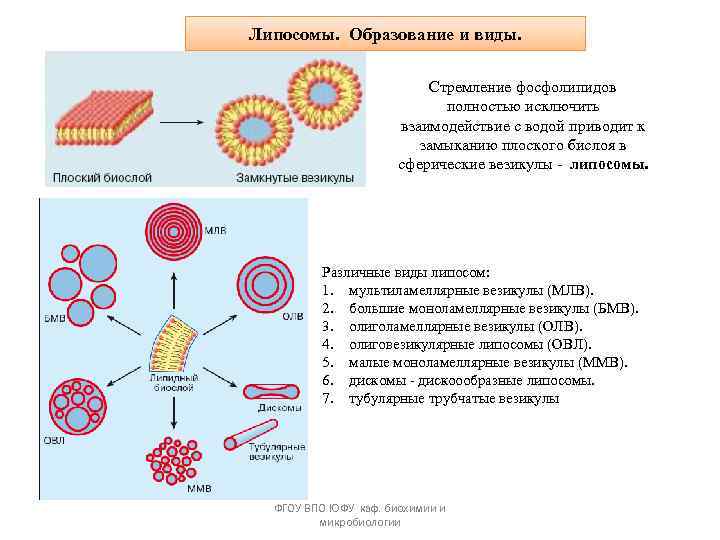
Липосомы. Образование и виды. Стремление фосфолипидов полностью исключить взаимодействие с водой приводит к замыканию плоского бислоя в сферические везикулы - липосомы. Различные виды липосом: 1. мультиламеллярные везикулы (МЛВ). 2. большие моноламеллярные везикулы (БМВ). 3. олиголамеллярные везикулы (ОЛВ). 4. олиговезикулярные липосомы (ОВЛ). 5. малые моноламеллярные везикулы (ММВ). 6. дискомы - дискоообразные липосомы. 7. тубулярные трубчатые везикулы ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
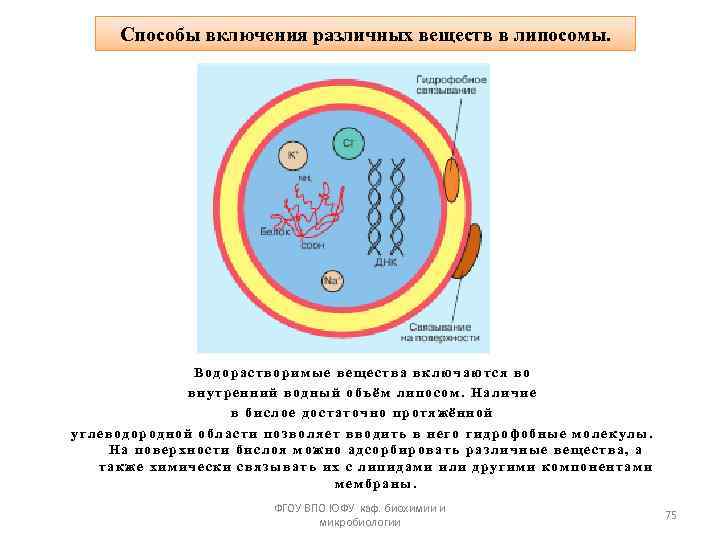
Способы включения различных веществ в липосомы. Водорастворимые вещества включаются во внутренний водный объём липосом. Наличие в бислое достаточно протяжённой углеводородной области позволяет вводить в него гидрофобные молекулы. На поверхности бислоя можно адсорбировать различные вещества, а также химически связывать их с липидами или другими компонентами мембраны. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 75
Применение липосом. Применение липосом и везикул В фундаментальных научных исследованиях В фармакологии и медицине В косметологии ФГОУ ВПО ЮФУ каф. биохимии и микробиологии В пищевой индустрии
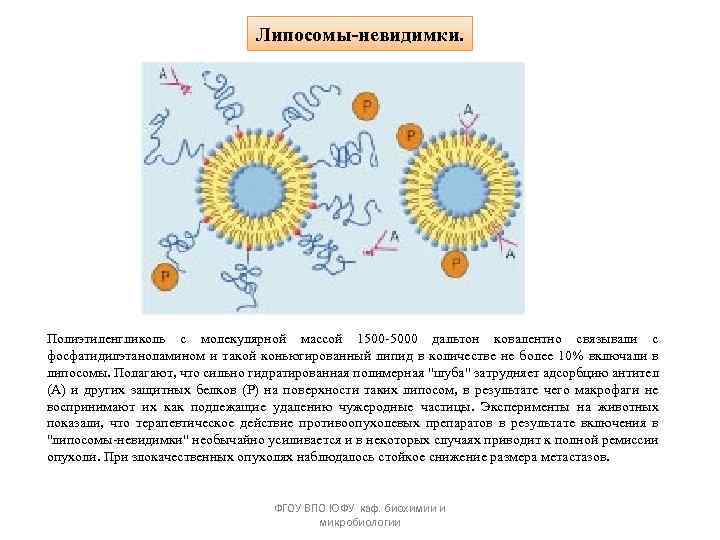
Липосомы-невидимки. Полиэтиленгликоль с молекулярной массой 1500 -5000 дальтон ковалентно связывали с фосфатидилэтаноламином и такой коньюгированный липид в количестве не более 10% включали в липосомы. Полагают, что сильно гидратированная полимерная "шуба" затрудняет адсорбцию антител (А) и других защитных белков (Р) на поверхности таких липосом, в результате чего макрофаги не воспринимают их как подлежащие удалению чужеродные частицы. Эксперименты на животных показали, что терапевтическое действие противоопухолевых препаратов в результате включения в "липосомы-невидимки" необычайно усиливается и в некоторых случаях приводит к полной ремиссии опухоли. При злокачественных опухолях наблюдалось стойкое снижение размера метастазов. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Электрокинетические явления

Электрокинетические явления (ЭКЯ) это движение фаз дисперсной системы под влиянием наложенного на нее постоянного электрического поля, а также образование разности потенциалов в дисперсной системе при механическом движении фаз

Дисперсные системы (ДС) – гетерогенные системы, состоящие из 2 фаз: дисперсионной среды – растворителя, и дисперсной фазы – растворенного вещества. Характерное свойство ДС – наличие межфазной поверхности, свойства которой влияют на ДС. Дисперсионная среда крови – плазма, дисперсные фазы – форменные элементы крови (эритроциты, лейкоциты, тромбоциты)

ЭКЯ характерны для систем, в которых на границе раздела фаз имеется двойной электрический слой (ДЭС). Открыто 4 вида ЭКЯ: электрофорез потенциалы оседания (седиментации) электроосмос потенциалы течения

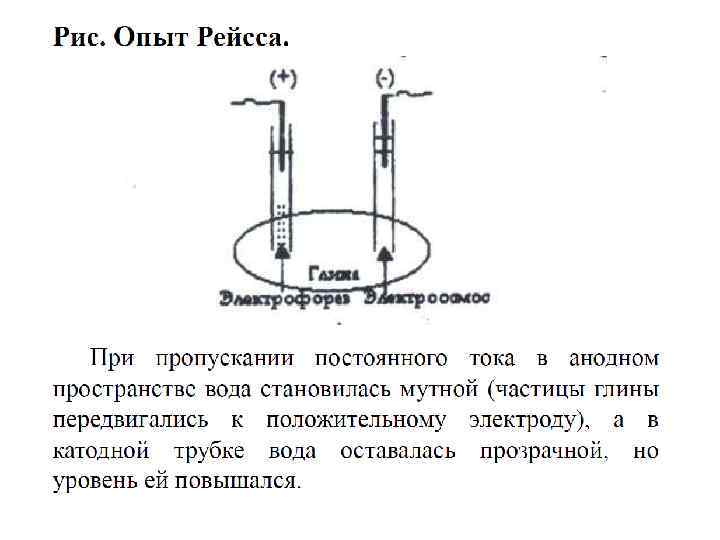
Электрофорез и электроосмос 1. Открыты в 1807 г. проф. Ф. Ф. Рейссом. 2. Электрофорез – направленное движение частиц дисперсной фазы в постоянном электрическом поле к противоположно заряженному электроду. 3. Электроосмос – движение дисперсионной среды в постоянном электрическом поле к противоположно заряженному электроду. 4. Рейсс проводил опыт: в сырую глину помещались 2 трубки, в которые наливалась вода и опускались электроды. При наличии капиллярно-пористой перегородки (в опыте Рейсса – это влажная глина) под действием постоянного электрического поля передвигаются дисперсионная среда (электроосмос) и дисперсная фаза (электрофорез).

Потенциалы течения и седиментации Потенциалы течения (Uf ) (Квинке, 1859) – возникают в результате движения дисперсионной среды (жидкости) через капилляры или поры перегородки в результате разности гидростатического давления (∆р). Величина U пропорциональна ∆р. Это явление противоположно электроосмосу. Потенциалы седиментации (Us) (Дорн, 1878) – возникают в дисперсной системе, когда частицы твердой фазы, несущие заряд, осаждаются под действием силы тяжести. В результате между твердой и жидкой фазами возникнет разность потенциалов. Это явление противоположно электрофорезу.
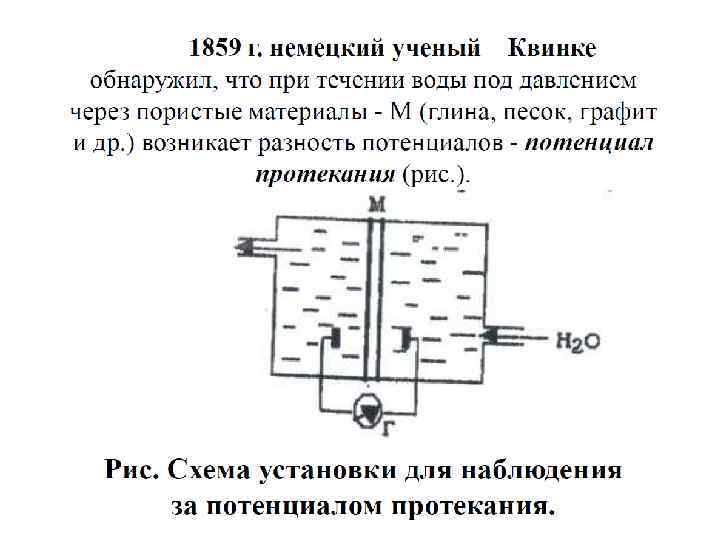


Все ЭКЯ связаны с возникновением разности потенциалов между дисперсной фазой и дисперсионной средой, которая называется электрокинетическим потенциалом или ζпотенциалом. Причина появления ζ- потенциала – возникновение поверхностного заряда на границе раздела двух фаз в результате асимметричного распределения ионов.

Механизм возникновения ζ-потенциала 1. Диссоциация ионогенных групп мембраны, частицы. 2. Адсорбция ионов и полярных молекул на поверхности мембраны, частицы. 3. В итоге ионы одного знака прочно связаны с дисперсной фазой и формируют потенциалообразующий слой, а ионы противоположного знака находятся в дисперсионной среде, образуя адсорбционный слой. 4. Эти два слоя образуют двойной электрический слой (ДЭС), который формируется под действием 2 противоположно действующих сил – электростатического притяжения и теплового движения ионов.

5. В итоге вокруг частицы или клетки образуется ионная атмосфера с избыточным диффузным зарядом. Наиболее высока плотность заряда ДЭС вблизи поверхности клетки, при удалении заряд падает по экспоненциальному закону. φ = φ0 е-рх , где φ0 - полный электрохимический потенциал φ - электрохимический потенциал на расстоянии х р – коэффициент, характеризующий свойства среды Дебаевская длина - расстояние х, на котором φ падает в е раз (φ=0, 37 φ0) 6. Толщина ДЭС находится в обратной зависимости от ионной силы раствора.
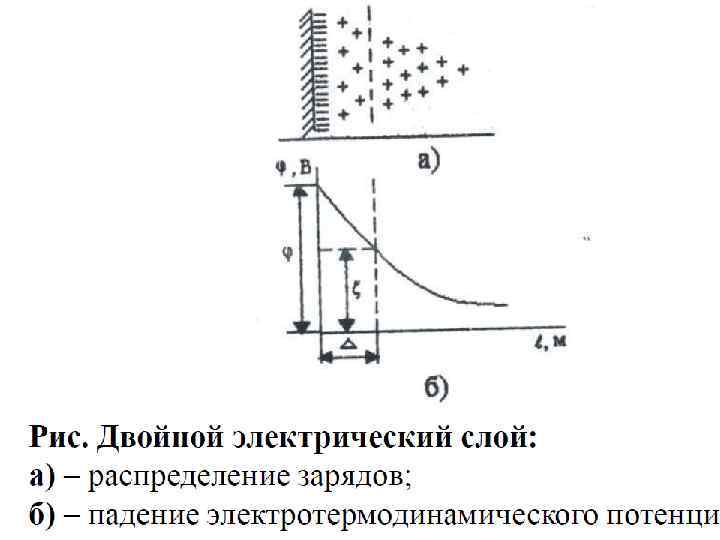

Разность потенциалов, которая возникает на границе между тончайшей пленкой (окружающей частицу или клетку) - адсорбционным слоем и всей остальной массой жидкости (дисперсионной средой), называется электрокинетическим или ζ-потенциалом. Его величина находится в прямой зависимости от толщины ДЭС и в обратной зависимости от ионной силы раствора (дисперсионной среды).

ζ-потенциал измеряется с помощью электрофореза. Формула Смолуховского для определения ζпотенциала: V = Eεζ/4πη, где V - скорость движения частицы в электрическом поле E - напряженность электрического поля ζ - дзета-потенциал ε - диэлектрическая постоянная среды η - вязкость среды ζ = 4πηV/Eε
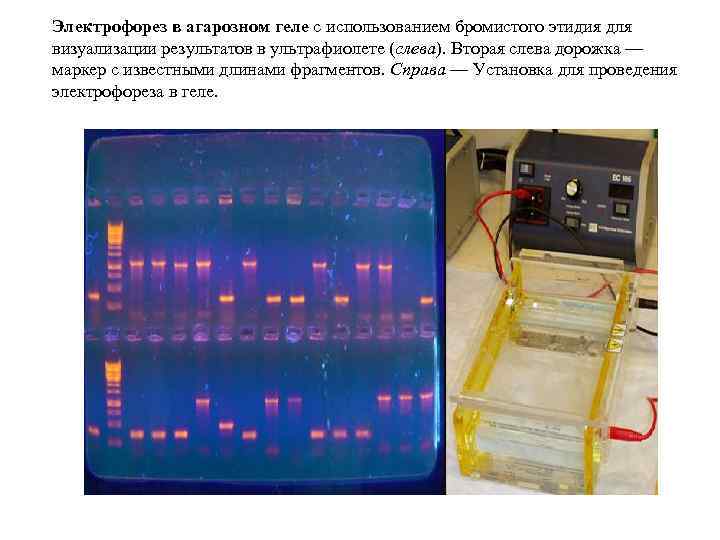
Электрофорез в агарозном геле с использованием бромистого этидия для визуализации результатов в ультрафиолете (слева). Вторая слева дорожка — маркер с известными длинами фрагментов. Справа — Установка для проведения электрофореза в геле.
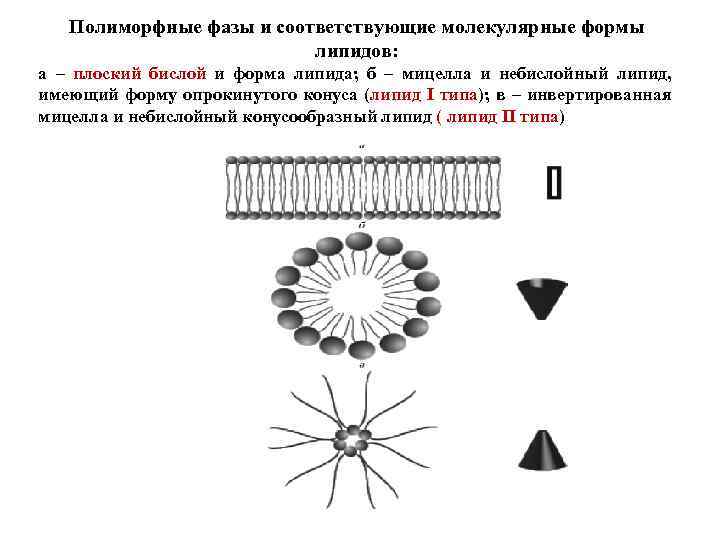
Полиморфные фазы и соответствующие молекулярные формы липидов: а – плоский бислой и форма липида; б – мицелла и небислойный липид, имеющий форму опрокинутого конуса (липид I типа); в – инвертированная мицелла и небислойный конусообразный липид ( липид II типа)
4.Биофизика БМ.pptx