89e25430477daa7b53ec49b96aa47e8e.ppt
- Количество слайдов: 42

Биофизика Биологична физика или Физика на биологичните системи Радостина Георгиева

Литература • Иван Танев Иванов: Медицинска и биологична физика • Roland Glaser – Biophysics • Р. Петрова – Ръководство за упражнения по биофизика
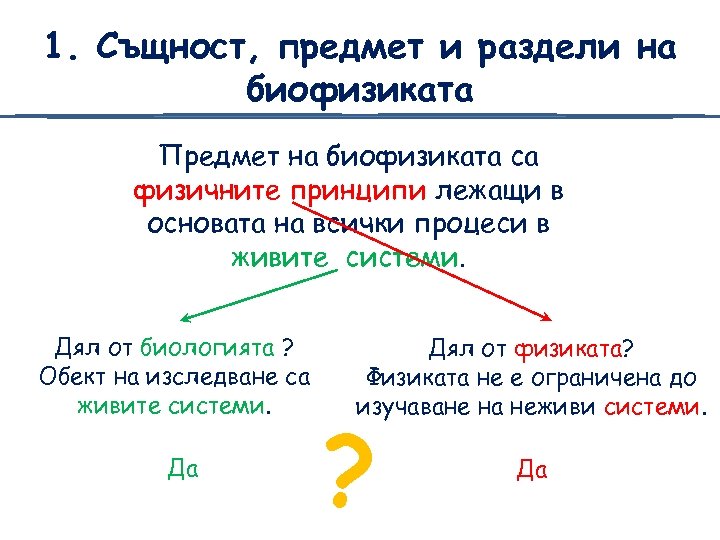
1. Същност, предмет и раздели на биофизиката Предмет на биофизиката са физичните принципи лежащи в основата на всички процеси в живите системи. Дял от биологията ? Обект на изследване са живите системи. Да Дял от физиката? Физиката не е ограничена до изучаване на неживи системи. ? Да

В исторически план Леонардо да Винчи (1452 -1519 г. ) – изследва механичните принципи на птичия полет с цел проектиране на летателен апарат – бионика. Алфонсо Борели (1608 -1679 г. ) – биомеханично описание на движенията на крайниците, полета на птиците, механика на плуването и т. н. Основава училище в Пиза, където човешкото тяло се разглежда като механична машина - първи стъпки на медицинската биофизика.

В исторически план Луиджи Галвани (1737 -1798 г. ) и Алесандро Волта (1745 -1827 г. )– изследват за пръв път феномени на електрофизиологията.

В исторически план Антоан Лорен Лавоазие (1743 -1794 г. ) и Пиер Симон Лаплас (1749 -1827 г. ) – калориметрично доказват еквивалентността между дишане и горене – начални стъпки на биотермодинамиката Юлиус Роберт Майер (1814 -1878 г. ) – стимулиран от наблюденията си като корабен лекар, пръв формулира 1842 г. първия принцип на термодинамиката (по-късно окончателно формулиран 1847 от Херман фон Хелмхолц).

В исторически план Херман фон Хелмхолц (1821 -1894 г. ) – също стартира кариерата си като лекар, но е известен освен като основател на модерната физиология и като един от най-значимите физици на 19 -ти век. Разработва теория на слуха и зрението. Алберт Айнщайн (1879 -1955 г. ) – официално признат 1999 г. за най-великия физик на всички времена, развива теорията за хаотичното движение с цел обяснение на наблюденията на ботаника Роберт Браун. Тази теория играе централна роля в развитието на модерната статистическа физика и за окончателния пробив на атомистичната теория за строежа на материята.

В исторически план 1892 г. - понятието биофизика за пръв път е използвано от Карл Пирсън в „Граматика на науката“ но добива поширока популярност и се утвърждава едва след повече от половин век - в края на 50 те години на 20 -ти век.

Някои исторически обобщения 1. Проблемите на биологията от край време са стимул и предизвикателство за физиците да търсят нови теоретични и експериментални методи за изследване и обяснение на процесите, протичащи в живите системи. От своя страна тези разработки допринасят за развитието на самата физика като наука: - теория на нелинейни отворени системи в термодинамиката; - теория на хаотичното топлинно движение;

Някои исторически обобщения 2. Развитието на модерната биологията е тясно свързано с разработването и въвеждането на нови физични методи, както в теоретичен, така и в експериментален план: - оптичен микроскоп; - електронен микроскоп ; - рентгенов структурен анализ; - спектроскопски методи; - ядреномагнитен резонанс; - и т. н.

Заключение Биофизиката: Øне е дял от биологията, но не е и дял от физиката; Øне е физика за биолози, нито биология за физици; Øне е просто прилагане на оптични, електронни или др. измервателни методи. Øе интердисциплинарна наука, между биология и физика и допирни точки с други дисциплини (напр. математика, физико-химия, биохимия); Øе количествена наука, прилагаща аналитичен подход при решаването на биологични и медицински проблеми.
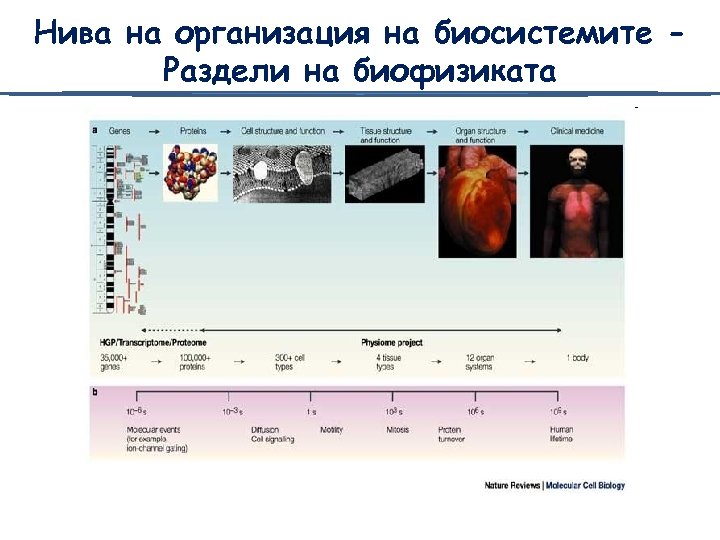
Нива на организация на биосистемите Раздели на биофизиката
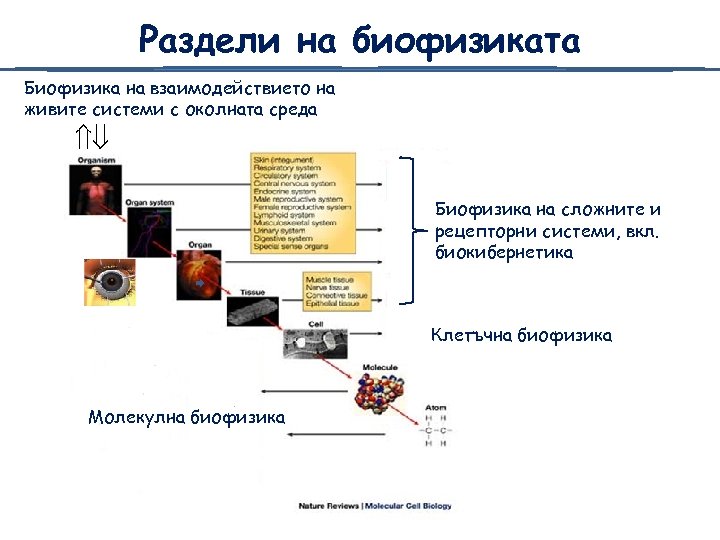
Раздели на биофизиката Биофизика на взаимодействието на живите системи с околната среда Биофизика на сложните и рецепторни системи, вкл. биокибернетика Клетъчна биофизика Молекулна биофизика

2. Биотермодинамика Термодинамика: дял от физиката превръщане на енергията от един вид в друг в материалните системи Биотермодинамика: превръщане на енергията в живите системи
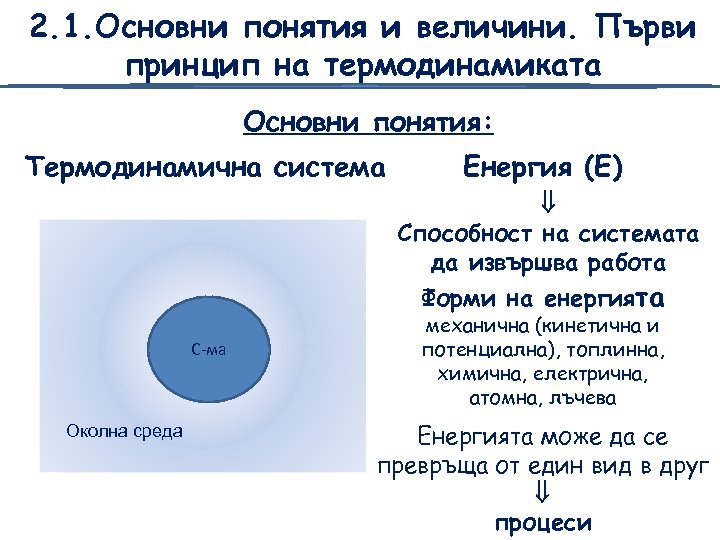
2. 1. Основни понятия и величини. Първи принцип на термодинамиката Основни понятия: Термодинамична система Енергия (Е) Способност на системата да извършва работа Форми на енергията С-ма Околна среда механична (кинетична и потенциална), топлинна, химична, електрична, атомна, лъчева Енергията може да се превръща от един вид в друг процеси
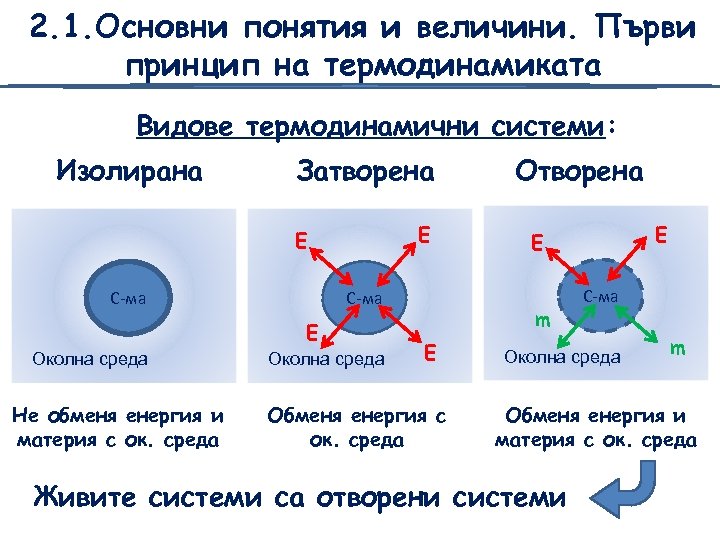
2. 1. Основни понятия и величини. Първи принцип на термодинамиката Видове термодинамични системи: Изолирана Затворена Е Е С-ма Е Околна среда Не обменя енергия и материя с ок. среда Околна среда Отворена m Е Обменя енергия с ок. среда Е Е С-ма Околна среда m Обменя енергия и материя с ок. среда Живите системи са отворени системи

2. 1. Основни понятия и величини. Първи принцип на термодинамиката Състояние на термодинамичната система Определя се: • по отношение на околната среда - равновесно или неравновесно; • от количеството енергия (вътрешна енергия U), т. е. от способността й да извършва работа. вътрешна енергия U = функция на състоянието Параметри на термодинамичните системи: • измеряеми величини - температура (T), налягане (p), обем (V), маса (m), електричен заряд (q) • стойностите им описват изцяло състоянието на системата Tермодинамичен процес: Преход на системата от едно състояние в друго

2. 1. Основни понятия и величини. Първи принцип на термодинамиката Топлина Q – пълната кинетична енергия на хаотичното движение на частиците на веществото: ½mv 2 k. T, k = 1, 38⋅ 10− 23 J / K - константа на Болцман Извършена работа A: A = р. V Термодинамичните системи могат да извършват работа за сметка на вътрешната си енергия: A = р. V = Q - d. U • Машина – система за превръщане на енергия (топлинна, електрична и т. н. ) в работа. • Организъм – извършва работа за сметка на химичната енергия на хранителните вещества.
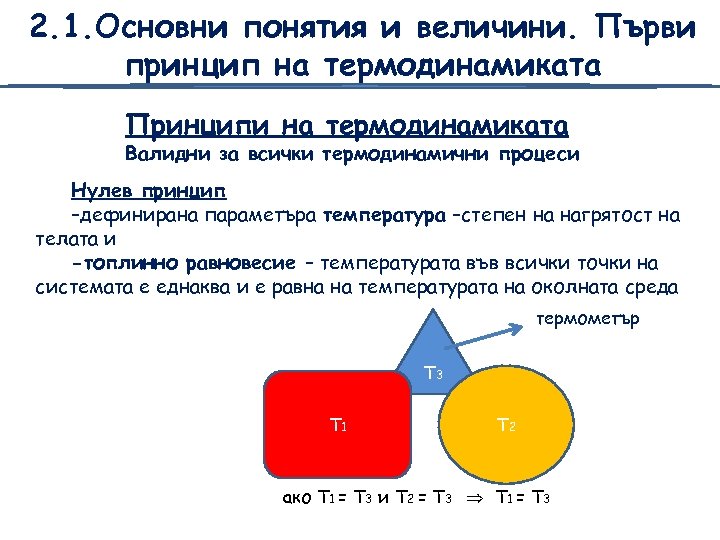
2. 1. Основни понятия и величини. Първи принцип на термодинамиката Принципи на термодинамиката Валидни за всички термодинамични процеси Нулев принцип –дефинирана параметъра температура –степен на нагрятост на телата и -топлинно равновесие – температурата във всички точки на системата е еднаква и е равна на температурата на околната среда термометър T 3 T 1 T 2 ако T 1 = T 3 и T 2 = T 3 T 1 = T 3

2. 1. Основни понятия и величини. Първи принцип на термодинамиката Принципи на термодинамиката Валидни за всички термодинамични процеси Първи принцип – дефинира величините вътрешна енергия и топлина, обяснява промените на вътрешната енергия в съгласие с общия закон за запазване на енергията. Втори принцип - дефинира величината ентропия и посоката на протичане на термодинамичните процеси. Трети принцип - при абсолютната температурна нула, ентропията на тялото е равна на нула (0°К = -273, 15 о. С), всички атоми и молекули се намират в пълен покой. Четвърти принцип - в изолирана термодинамична система, всички процеси завършват с достигане на термодинамично равновесие (всички видове енергия са деградирали до топлина топлинна смърт).

2. 1. Основни понятия и величини. Първи принцип на термодинамиката Вътрешна енергия U – сума от кинетичната и потенциална енергия на всички часици, изграждащи системата • Кинетична енергия – произхожда от движението на частиците (транслационно, ротационно, вибрационно) • Потенциална енергия - произхожда от силите, които действат върху частиците (външни и вътрешни) Първи принцип на термодинамиката състояние на дадена система се характеризира с точно определена стойност на вътрешната енергия U функция на състоянието. За да премине от едно състояние в Всяко друго системата или трябва да обмени енергия (топлина Q) с околната среда, или да извърши работа A. Частен случай на закона за запазване на енергията
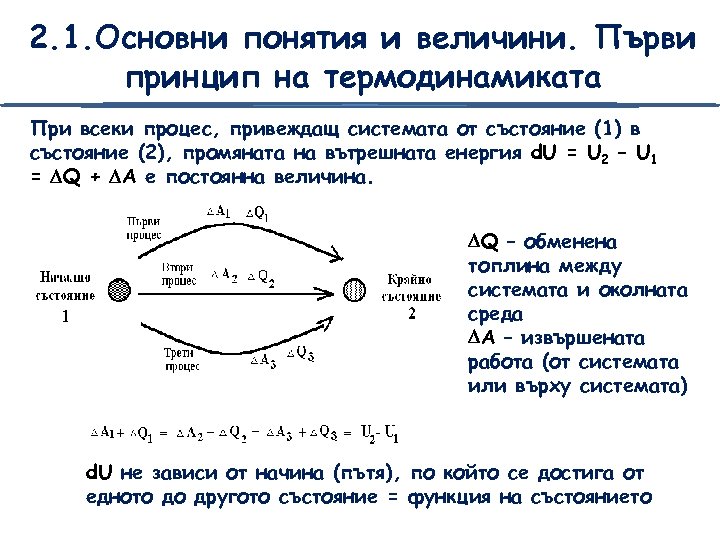
2. 1. Основни понятия и величини. Първи принцип на термодинамиката При всеки процес, привеждащ системата от състояние (1) в състояние (2), промяната на вътрешната енергия d. U = U 2 – U 1 = Q + A е постоянна величина. Q – обменена топлина между системата и околната среда A – извършената работа (от системата или върху системата) d. U не зависи от начина (пътя), по който се достига от едното до другото състояние = функция на състоянието

2. 1. Основни понятия и величини. Първи принцип на термодинамиката Закон на Хес Ако една то химична реакция протича при постоянно налягане Q = d. U, т. е. отделената или погълната топлина не зависи от междинните етапи, а само от началното и крайно състояние. Следствие - живите организми отделят при покой толкова топлина ( Q) в околната среда, колкото е химичната енергия (d. U) на приетите хранителни вещества. Енталпия H (топлосъдържание на материята) – сума от вътрешната енергия и работата необходима да се доведе системата до даден обем V срещу налягането p на окoлната среда H = U + p. V
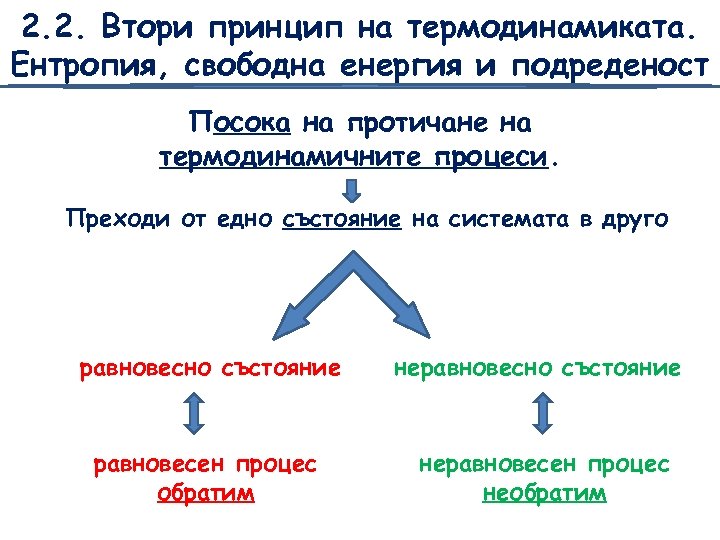
2. 2. Втори принцип на термодинамиката. Ентропия, свободна енергия и подреденост Посока на протичане на термодинамичните процеси. Преходи от едно състояние на системата в друго равновесно състояние неравновесно състояние равновесен процес обратим неравновесен процес необратим
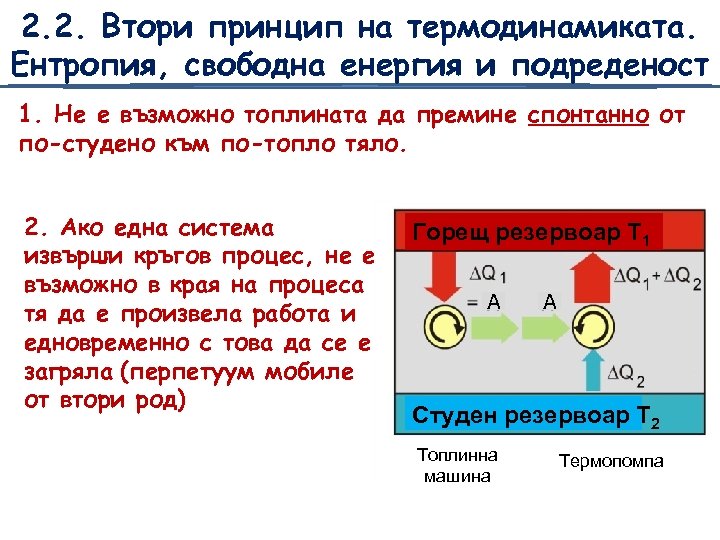
2. 2. Втори принцип на термодинамиката. Ентропия, свободна енергия и подреденост 1. Не е възможно топлината да премине спонтанно от по-студено към по-топло тяло. 2. Ако една система извърши кръгов процес, не е възможно в края на процеса тя да е произвела работа и едновременно с това да се е загряла (перпетуум мобиле от втори род) Горещ резервоар Т 1 А А Студен резервоар Т 2 Топлинна машина Термопомпа
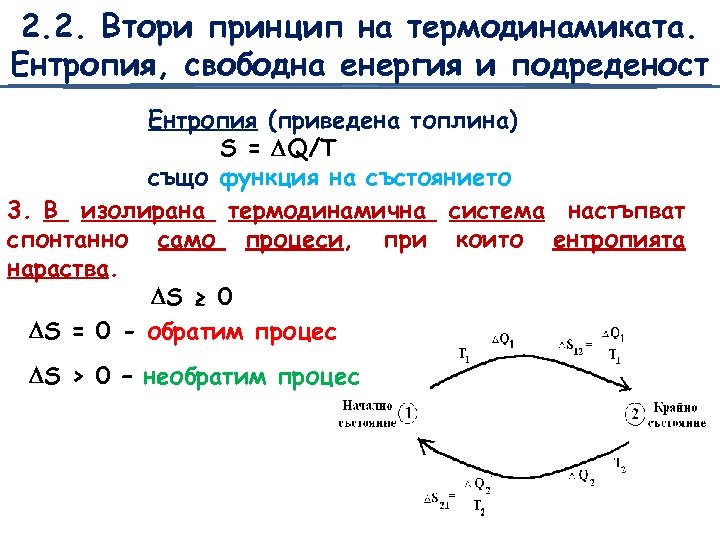
2. 2. Втори принцип на термодинамиката. Ентропия, свободна енергия и подреденост Ентропия (приведена топлина) S = Q/T също функция на състоянието 3. В изолирана термодинамична система настъпват спонтанно само процеси, при които ентропията нараства. S ≥ 0 S = 0 - обратим процес S > 0 – необратим процес
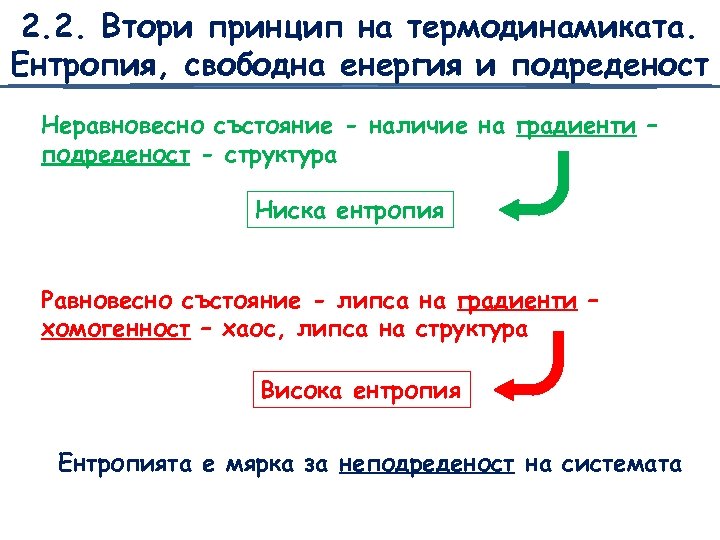
2. 2. Втори принцип на термодинамиката. Ентропия, свободна енергия и подреденост Неравновесно състояние - наличие на градиенти – подреденост - структура Ниска ентропия Равновесно състояние - липса на градиенти – хомогенност – хаос, липса на структура Висока ентропия Ентропията е мярка за неподреденост на системата
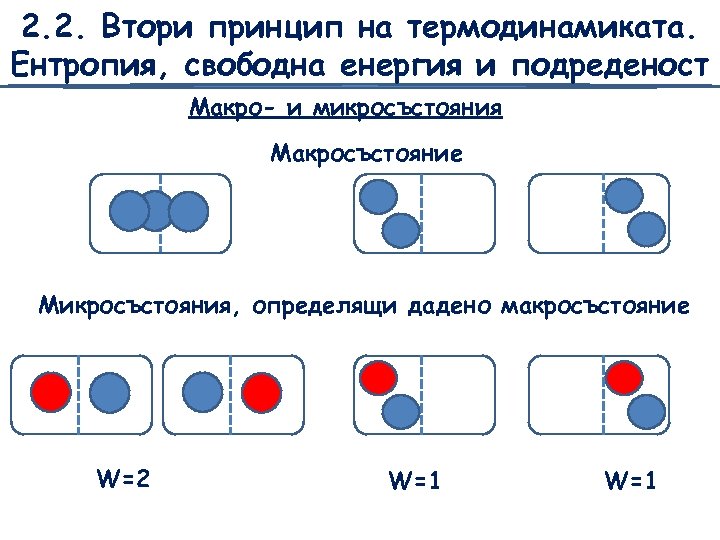
2. 2. Втори принцип на термодинамиката. Ентропия, свободна енергия и подреденост Макро- и микросъстояния Макросъстояниe Микросъстояния, определящи дадено макросъстояние W=2 W=1
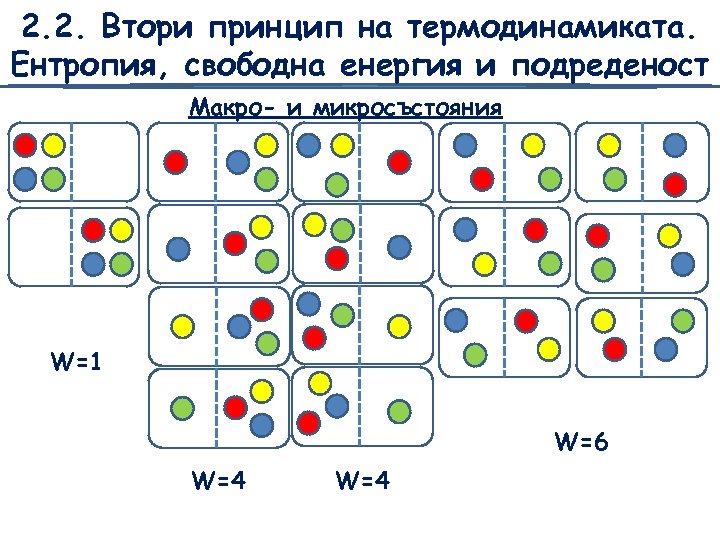
2. 2. Втори принцип на термодинамиката. Ентропия, свободна енергия и подреденост Макро- и микросъстояния W=1 W=6 W=4

2. 2. Втори принцип на термодинамиката. Ентропия, свободна енергия и подреденост Дефиниция на понятието подреденост Термодинамична вероятност на макросъстоянието W: брой на микросъстоянията, определящи едно макросъстояние – неподредената система има голяма ТД вероятност и голяма ентропия S = k. ln. W
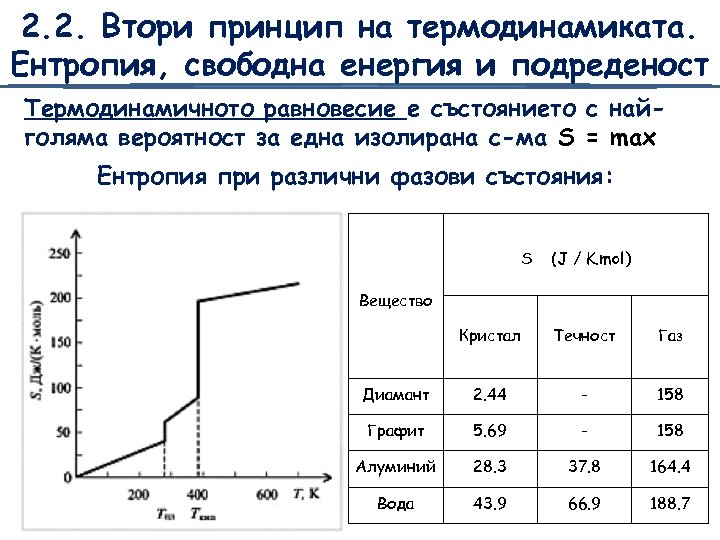
2. 2. Втори принцип на термодинамиката. Ентропия, свободна енергия и подреденост Термодинамичното равновесие е състоянието с найголяма вероятност за една изолирана с-ма S = max Ентропия при различни фазови състояния: S (J / K. mol) Вещество Кристал Течност Газ Диамант 2. 44 - 158 Графит 5. 69 - 158 Алуминий 28. 3 37. 8 164. 4 Вода 43. 9 66. 9 188. 7

2. 2. Втори принцип на термодинамиката. Ентропия, свободна енергия и подреденост Други функции на състоянието Свободна енергия (енергия на Хелмхолц): U= A+ Q – I. принцип Q=T. S – от дефиницията на ентропията A = U - T. S = = (U-T. S) = F F= U - T. S- свободна енергия, т. е. част от U, която може да се превърне в работа T. S - свързана енергия – част от U, която не може да се използва за работа 3. В изолирана термодинамична система настъпват спонтанно само процеси, при които ентропията нараства, а свободната енергия намалява: S ≥ 0 F 0 Свободна енергия на Гибс: G = H - ST Функции на състоянието = термодинамични потенциали
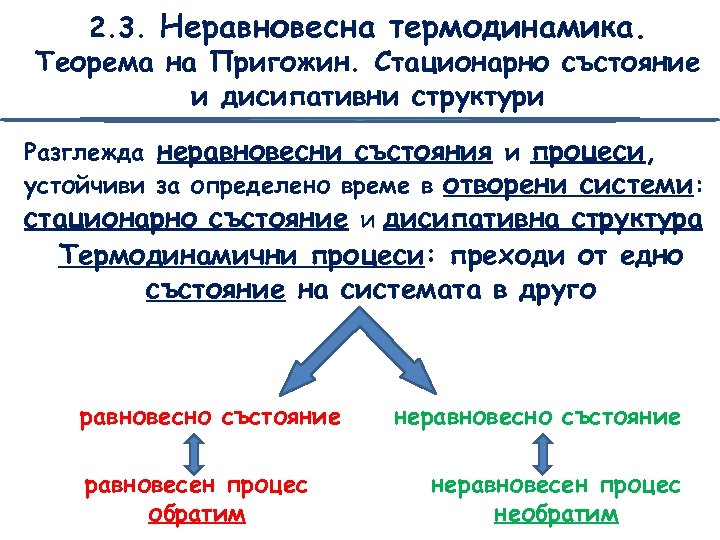
2. 3. Неравновесна термодинамика. Теорема на Пригожин. Стационарно състояние и дисипативни структури Разглежда неравновесни състояния и процеси, устойчиви за определено време в отворени системи: стационарно състояние и дисипативна структура Tермодинамични процеси: преходи от едно състояние на системата в друго равновесно състояние равновесен процес обратим неравновесно състояние неравновесен процес необратим
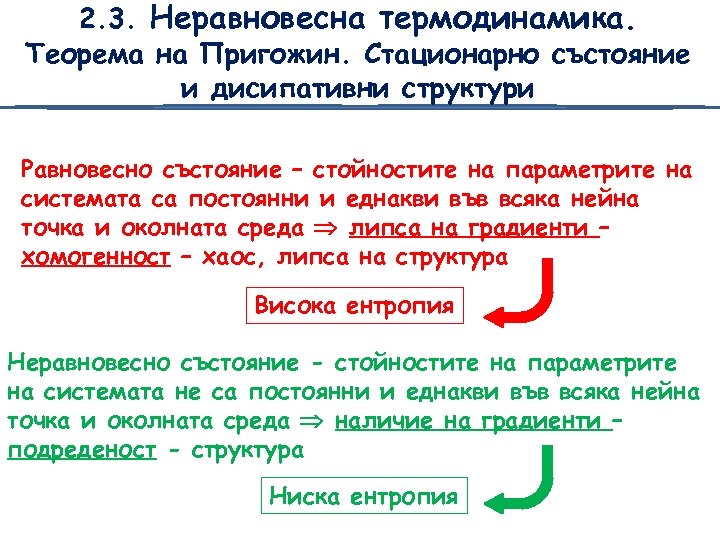
2. 3. Неравновесна термодинамика. Теорема на Пригожин. Стационарно състояние и дисипативни структури Равновесно състояние – стойностите на параметрите на системата са постоянни и еднакви във всяка нейна точка и околната среда липса на градиенти – хомогенност – хаос, липса на структура Висока ентропия Неравновесно състояние - стойностите на параметрите на системата не са постоянни и еднакви във всяка нейна точка и околната среда наличие на градиенти – подреденост - структура Ниска ентропия

2. 3. Неравновесна термодинамика. Теорема на Пригожин. Стационарно състояние и дисипативни структури Равновесен процес –преход от едно равновесно състояние в друго -стойностите на всеки от параметрите на системата са еднакви във всяка нейна точка и околната среда във всеки един момент от прехода Обратим процес Системата може да се върне в изходното си състояние спонтанно Неравновесен процес –поне едното от състоянията е неравновесно -стойностите на параметрите на системата не са постоянни и еднакви във всяка нейна точка и околната среда по време на прехода Необратим процес Системата не може да се върне в изходното си състояние спонтанно

2. 3. Неравновесна термодинамика. Теорема на Пригожин. Стационарно състояние и дисипативни структури Неравновесни състояния и процеси, устойчиви за определено време в отворени системи: стационарно състояние и дисипативна структура Е Е m неравновесно състояние: наличие на градиенти – Т, р, c, , q … С-ма Околна среда m Обменя енергия и материя с ок. среда неравновесни процеси> необратими потоци на вещество, енергия ел. заряди …

2. 3. Неравновесна термодинамика. Теорема на Пригожин. Стационарно състояние и дисипативни структури Градиентите са движещите сили на потоците при неравновесните процеси: J = L 1. X 1 + L 2. X 2 + L 3. X 3 + … J – поток на енергия и/или материя X 1, X 2, Х 3 - движещите сили (градиентите) на различни параметри L 1, L 2, L 3 - феноменологични коефициенти Ако Li f(Xi) – процес с линейна зависимост на потоците от движещите ги градиенти - линейни неравновесни процеси Ако Li = f(Xi) - нелинейни неравновесни процеси

2. 3. Неравновесна термодинамика. Теорема на Пригожин. Стационарно състояние и дисипативни структури Стационарно състояние: не се променя с времето Jin Jex С-ма Jin = Jex постоянни стойности на параметрите на системата Околна среда Ентропия на отворените системи: производство на ентропия в системата Sin ≥ 0, но и обмен на ентропия с околната среда Sex > = < 0 За стационарното състояние – S = Sin + Sex = 0 Sex = - Sin < 0 отрицателна ентропия (негентропия)

2. 3. Неравновесна термодинамика. Теорема на Пригожин. Стационарно състояние и дисипативни структури Теорема на Пригожин (критерий за стабилност на състоянието): В стационарното състояние, скоростта на производство на ентропия вътре в системата ( S/ t)in е винаги положителна, но минимална по стойност величина. разходът на свободна енергия е минимален Валиден за голям брой състояния при живите организми: – биологичната система е отворена система в неравновесно стационарно състояние - процесите протичащи в нея са с минималното възможно производство на ентропия (т. е. минимален разход на свободна енергия) при дадените условия на средата, в която се намира

2. 3. Неравновесна термодинамика. Теорема на Пригожин. Стационарно състояние и дисипативни структури Термодинамично равновесие Стационарно състояние 1. Няма градиенти, няма потоци 1. Има градиенти, има потоци (хомогенност) (структура) 2. S =Smax 3. F = 0 2. Ентропията S << Smax от максимално възможната си стойност 3. F >> 0 системата не може да върши работа системата може да върши работа 4. Съществува за ограничено време 4. Може да съществува вечно като обменя вещество, енергия, ентропия и т. н. с околната среда
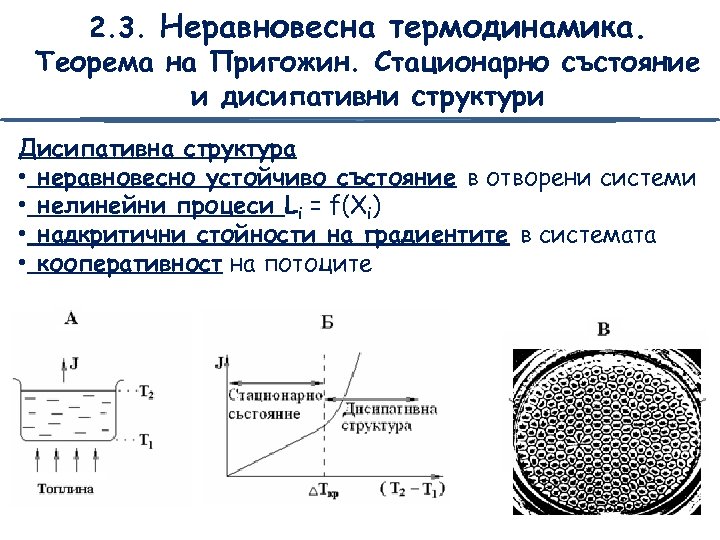
2. 3. Неравновесна термодинамика. Теорема на Пригожин. Стационарно състояние и дисипативни структури Дисипативна структура • неравновесно устойчиво състояние в отворени системи • нелинейни процеси Li = f(Xi) • надкритични стойности на градиентите в системата • кооперативност на потоците Клетка на Бенард

2. 3. Неравновесна термодинамика. Теорема на Пригожин. Стационарно състояние и дисипативни структури Други примери за дисипативни структури:
89e25430477daa7b53ec49b96aa47e8e.ppt