388345059f83cacea913c10a1eeee158.ppt
- Количество слайдов: 178

Биофармация - същност и основни дефиниции проф. Св. Богданова, дфн кат. Технология на лекарствата с биофармация ФФ, МУ - София, уч. 2005/2006 г.

Биофармация - направление във фармацевтичната наука и практика “Biopharmaceutics - this science is our new baby” G. Levy , 1967 г. , Монпелие, Франция, FIP Конгрес
§ John Wagner “Интересна особеност на биофармация-та е, че почти цялата й теория има практическо приложение…тя е в еволюционен стадий. Това, което мислим, че знаем днес може да бъде променено драстично от това, което ще се открие утре. . ”

Любопитни научни наблюдения и постижения историческа ретроспектива 1895 г. - патент на Upjohn за “разтрошаваща се таблетка” с бърза абсорбция 1902 г. - съобщение за липса на очакван ефект от таблетка с определен точен състав 1940/1945 г. - наблюдавана зависимост между размера на частиците на сулфонамиди, серумните нива и силата на ефекта 1948 г. - BP, USP и NF въвеждат тест за разпадаемост на таблетки 1958 г. - G. Levy, Калифорнийски Университет, въвежда понятието “biopharmaceutics”

1961 г. - Levy, G. предлага “тест за разтваряне” и съобщава за терапевтична нееквивалентност на препарати с едно и също ЛВ в една и съща доза 1961 г. - Levy, Nelson “Изборът на вид ЛФ за дадено ЛВ може да се окаже също толкова значим, колкото изборът на самия терапевтичен агент” 1961 г. - 1 -ят научен биофармацевтичен обзор на J. Wagner “Биофармацевтични аспекти на абсорбцията” - дефиниция на т. нар. фармацевтични фактори и влиянието им върху характера на биологичния лекарствен ефект

1963 г. - установена неекиввалентност на таблетки Prednison - времето за разтваряне варира от 4 до 100 минути 1967 г. -проблеми с ефекта на суспензии с хлорамфеникол палмитат - установено е, че само 1 от възможните полиморфи е активен, тъй като само той може да се разгражда хидролитично от ензими - естерази 1967/1968 г. - 27. 5 мил. chloramphenicol caps. и 40 милиона Tetracyclin caps. са иззети от аптеките поради терапевтична неефективност

§ 1970 г. - летални инциденти в Австралия с Phenytoin tabl. при замяна на ПВ калциев сулфат с лактоза Предпоставки за оформяне на биофармацията като ново научно направление във фармацията
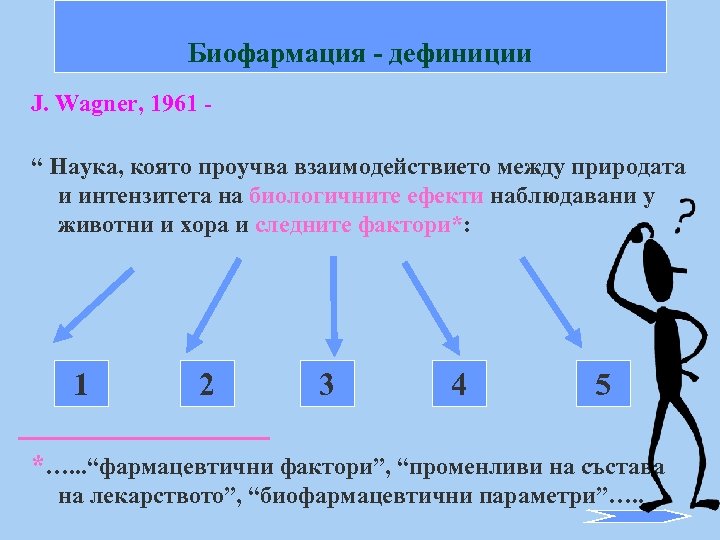
Биофармация - дефиниции J. Wagner, 1961 “ Наука, която проучва взаимодействието между природата и интензитета на биологичните ефекти наблюдавани у животни и хора и следните фактори*: 1 2 3 4 5 *…. . . “фармацевтични фактори”, “променливи на състава на лекарството”, “биофармацевтични параметри”…. .
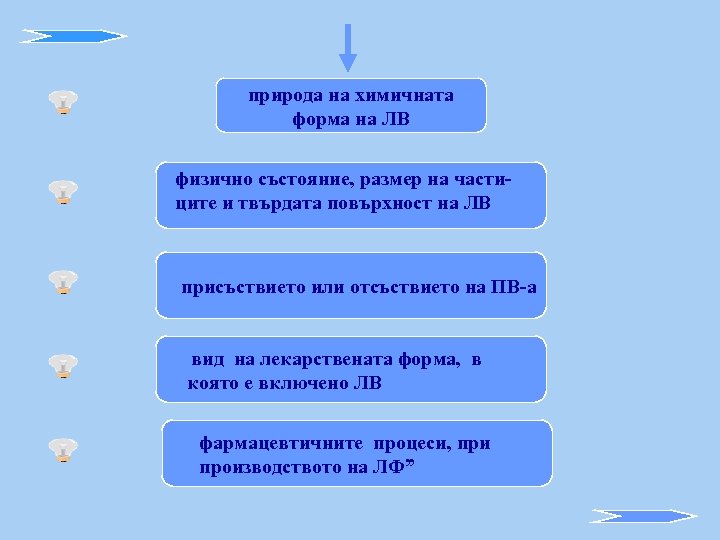
природа на химичната форма на ЛВ физично състояние, размер на частиците и твърдата повърхност на ЛВ присъствието или отсъствието на ПВ-а вид на лекарствената форма, в която е включено ЛВ фармацевтичните процеси, при производството на ЛФ”

Ritschel, 1973 “ Биофармацията изучава зависимостта на ADME - процесите в човешкия или животински организми от физико-химичните свойства на ЛВ (a) и ЛФ-и. Става въпрос за постигане на оптимална или желана наличност на ЛВ след освобождаване от неговата ЛФ както и за влиянието на състава на ЛФ върху биологичната активност на ЛВ(a)…. . ” R. Notari, 1986 “Биофармацията изучава онези фактори, които повлияват бионаличността на едно ЛВ при човека и животните. Получената информация се използва за оптимизиране на фармакологичнта или терапевтична активност на ЛВ при клинично приложение”

т. е. Биофармацията изучава зависимостта между: физикохимичните свойства на ЛВ и неговата ЛФ и появата, интензитета и продължителността на терапевтичния ефект

Биофармацията отхвърля традиционни до около 60 -те години на миналия век схващания за действието на лекарствата и постулира: Необработеното в ЛФ биологично-активно вещество не е терапевтичен агент Дуализмът ЛВ/Доза, не е единствено отговорен за лекарственото действие Изборът на лекарствена форма за едно биологично активно вещество е също толкова важен, колкото и изборът на съответен терапевтичен агент

ЛФ трябва да се разглежда като една физикохимична система, която в организма освобождава ЛВ(a) и го прави фармацевтично налично за взаимодействие с биологичната система Съдбата на лекарството в организма (LADME- фармакокинетични процеси) се определя не само от морфолого-физиологичните и биохимични особености на организма, но в същата степен от физикохимичните и фармацевтично-технологичните свойства на ЛВ и неговата ЛФ “. . . границата между активно ЛВ и ПВ е много неясно очертана. . . ”, няма индеферентни ПВ-а

Системата LADMER L Освобождаване (Liberation) на активното ЛВ от A Абсорбция (Absorption) - лекарствен транспорт през D М Е R съответгната ЛФ или от Лекарство Доставящата Система биологични мембрани Разпределяне (Distribution) -пренос на ЛВ от мястото на абсорбция до други тъкани и течности Метаболизъм (Metabolism) на ЛВ - биотрансформация, след която лекарственото действие може да завърши или да се иницира Екскреция (Excretion) на ЛВ - лекарственото действие завършва Лекарствен отговор (Response) - резултат от взаимодействието ЛВ/рецептор. Осъществява се след абсорбцията на ЛВ и/или разпределението му.
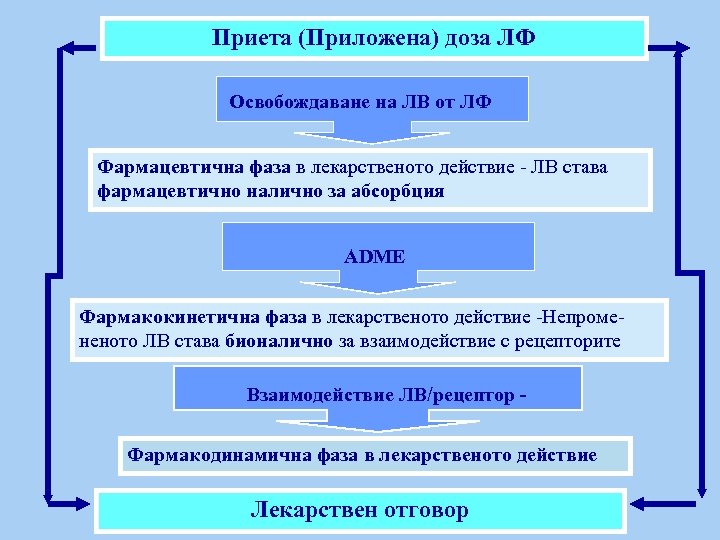
Приета (Приложена) доза ЛФ Освобождаване на ЛВ от ЛФ Фармацевтична фаза в лекарственото действие - ЛВ става фармацевтично налично за абсорбция ADME Фармакокинетична фаза в лекарственото действие -Непромененото ЛВ става бионалично за взаимодействие с рецепторите Взаимодействие ЛВ/рецептор Фармакодинамична фаза в лекарственото действие Лекарствен отговор

Бионаличност (БН) (bioavailability - BA) Oser, 1945 “ Бионаличност е отношението между отделеното за определено време количество активно ЛВ (витамин) от приложена тест доза и отделеното за същото време количество от приложена доза от проба за сравнение ( воден разтвор). FDA, USA - Бионаличност на едно ЛВ е скоростта и степента, с които ЛВ се абсорбира от съответната ЛФ и достига мястото на действие APh. A, USA - Бионаличност на едно ЛВ е скоростта и степента, с които ЛВ се абсорбира от съответната ЛФ и достига системното кръвообращение

APh. A, USA - Бионаличност на едно ЛВ е скоростта и степента, с които ЛВ се абсорбира от съответната ЛФ и достига системното кръвообращение EMEA* - Бионаличност на едно ЛВ е скоростта и степента, с които едно ЛВ или терапевтично ядро се доставя от съответната ЛФ в системното кръвообращение * EMEA - Европейска Агенция за Оценка на Лекарствата

Ritschel, 1973 - Абсолютна БН - скорост и степен на абсорбция на едно ЛВ от една несистемно (екстравазално) прилагана тест ЛФ отнесени към скоростта и степента на абсорбция на това ЛВ от една I. V. приложена референтна ЛФ m(x). 100 (%) m(i. v. ) Относителна БН - скорост и степен на абсорбция на едно ЛВ от една тест ЛФ отнесени към скоростта и степента на абсорбция на това ЛВ от една стандартна ЛФ приложена по същия път в организма m(x) 100 (%) m(s)
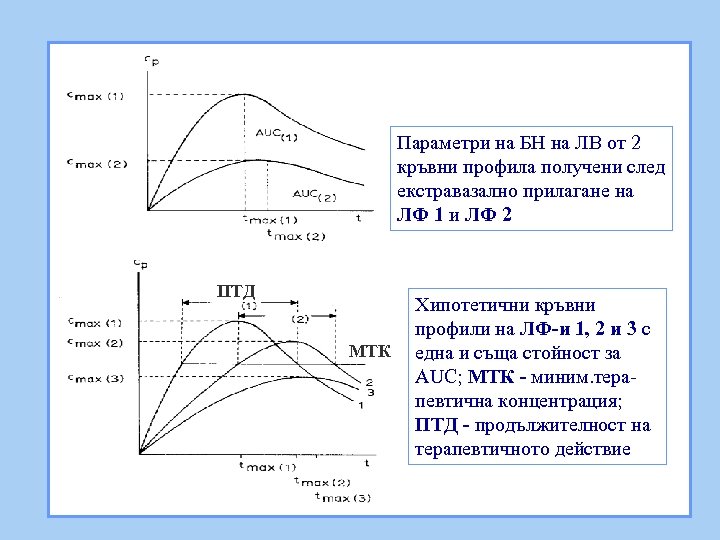
Параметри на БН на ЛВ от 2 кръвни профила получени след екстравазално прилагане на ЛФ 1 и ЛФ 2 ПТД МТК Хипотетични кръвни профили на ЛФ-и 1, 2 и 3 с една и съща стойност за AUC; МТК - миним. терапевтична концентрация; ПТД - продължителност на терапевтичното действие
Определяне на БН Измерване на специфичен фармакологичен или терапевтичен ефект Определяне на концентрацията на ЛВ или метаболити в кръв, плазма, серум или урина AUC - площ под кривата cpmax - максимална концентрация в кръвта tmax - време за достигане на максималната кръвна концентрация
Основни групи фактори на влияние върху БН Физиологичнобиохимичнисвързани са с живия организъм Физикохимични свойства свързани са с ЛВ и ЛФ
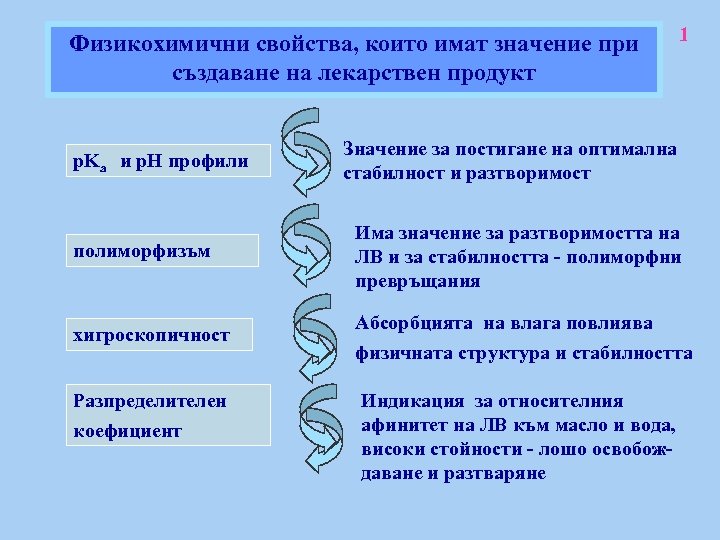
Физикохимични свойства, които имат значение при създаване на лекарствен продукт p. Ka и p. H профили полиморфизъм хигроскопичност Разпределителен коефициент 1 Значение за постигане на оптимална стабилност и разтворимост Има значение за разтворимостта на ЛВ и за стабилността - полиморфни превръщания Абсорбцията на влага повлиява физичната структура и стабилността Индикация за относителния афинитет на ЛВ към масло и вода, високи стойности - лошо освобождаване и разтваряне
2 Взаимодействия с ПВ-а Взаимодействията с ПВ-а или със следи от метали в ПВ-а могат да повлияят стабилността Профил р. Н- стабилност Огромно е значението за предотвратяване или ограничаване разпадането на продукта по време на съхранение и след прилагане в организма
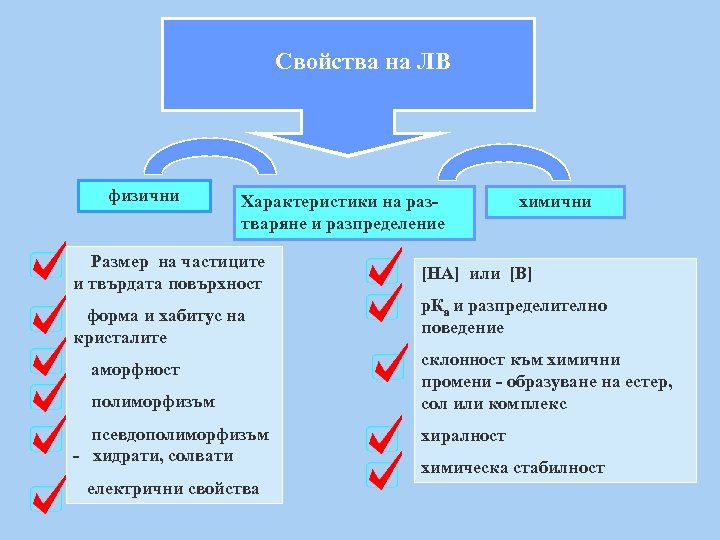
Свойства на ЛВ физични Характеристики на разтваряне и разпределение Размер на частиците и твърдата повърхност форма и хабитус на кристалите аморфност полиморфизъм псевдополиморфизъм - хидрати, солвати електрични свойства химични [HA] или [B] р. Ка и разпределително поведение склонност към химични промени - образуване на естер, сол или комплекс хиралност химическа стабилност
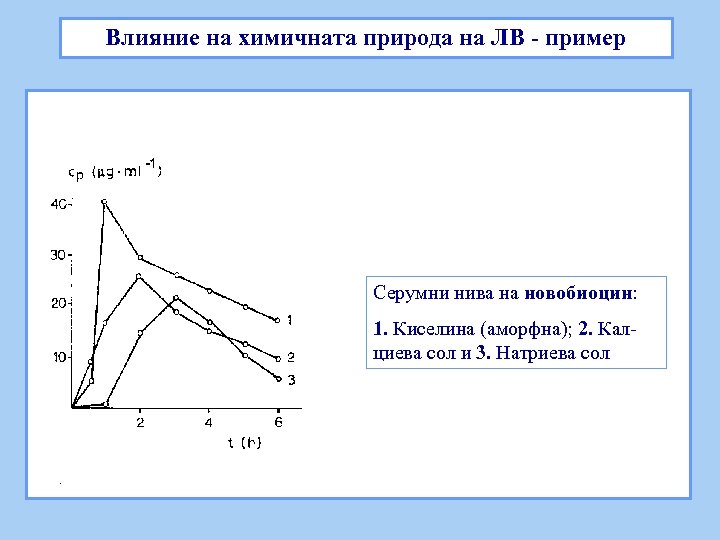
Влияние на химичната природа на ЛВ - пример Серумни нива на новобиоцин: 1. Киселина (аморфна); 2. Калциева сол и 3. Натриева сол
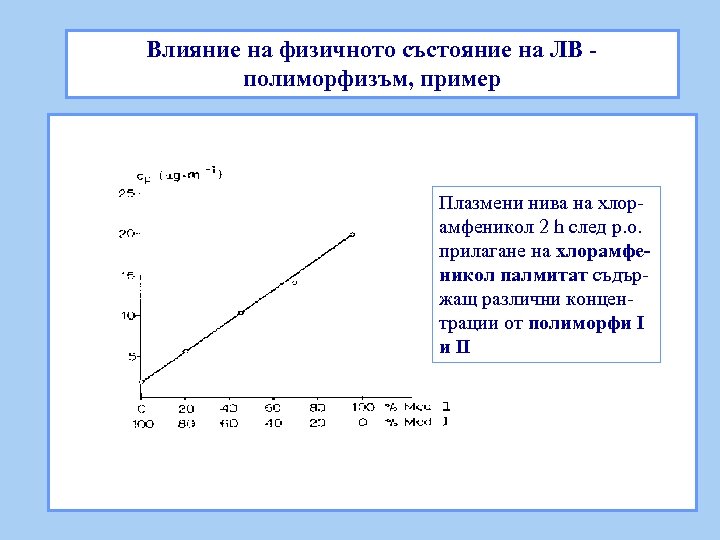
Влияние на физичното състояние на ЛВ полиморфизъм, пример Плазмени нива на хлорамфеникол 2 h след p. o. прилагане на хлорамфеникол палмитат съдържащ различни концентрации от полиморфи I и II
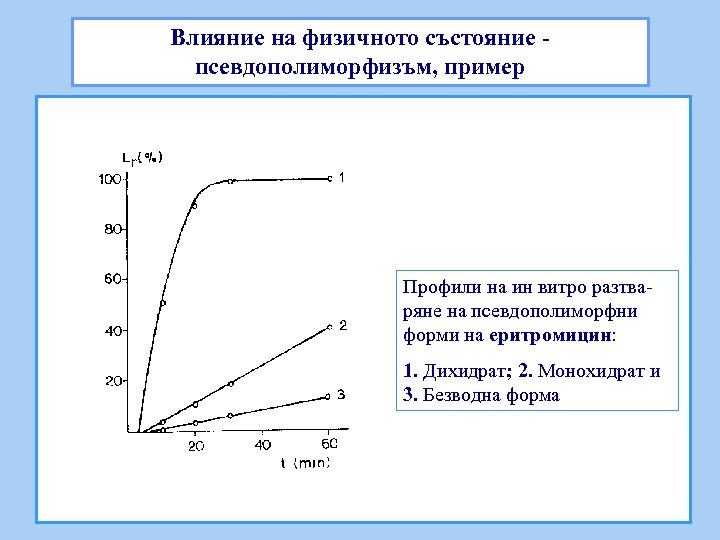
Влияние на физичното състояние псевдополиморфизъм, пример Профили на ин витро разтваряне на псевдополиморфни форми на еритромицин: 1. Дихидрат; 2. Монохидрат и 3. Безводна форма
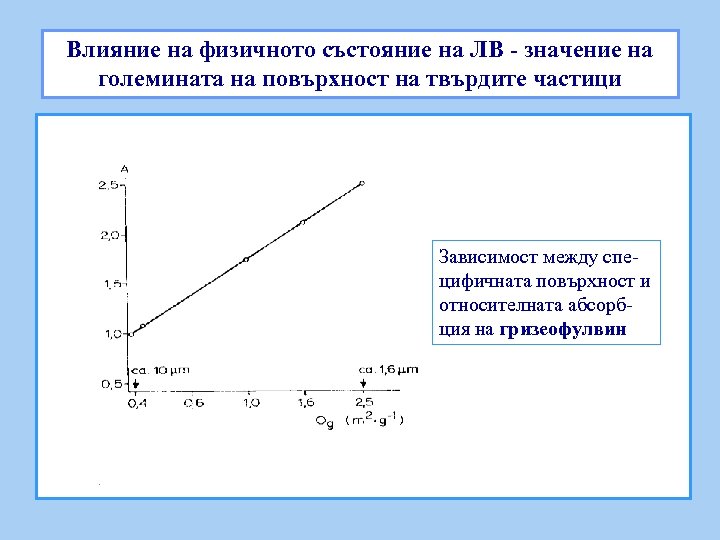
Влияние на физичното състояние на ЛВ - значение на големината на повърхност на твърдите частици Зависимост между специфичната повърхност и относителната абсорбция на гризеофулвин
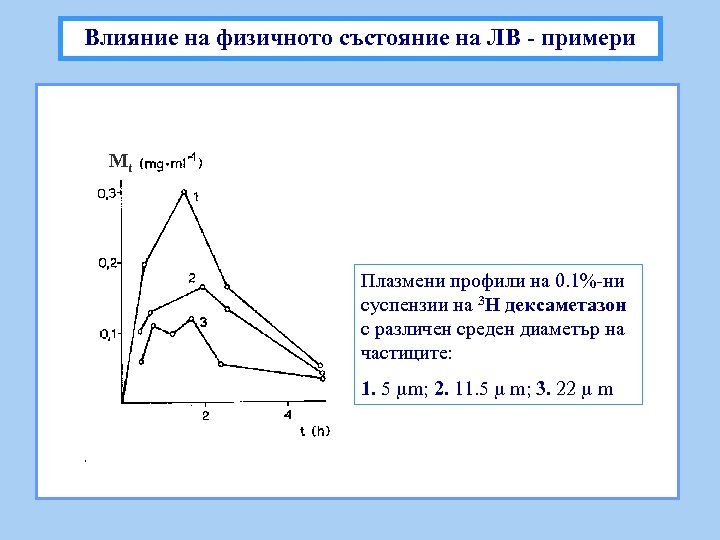
Влияние на физичното състояние на ЛВ - примери Mt Плазмени профили на 0. 1%-ни суспензии на 3 Н дексаметазон с различен среден диаметър на частиците: 1. 5 m; 2. 11. 5 m; 3. 22 m
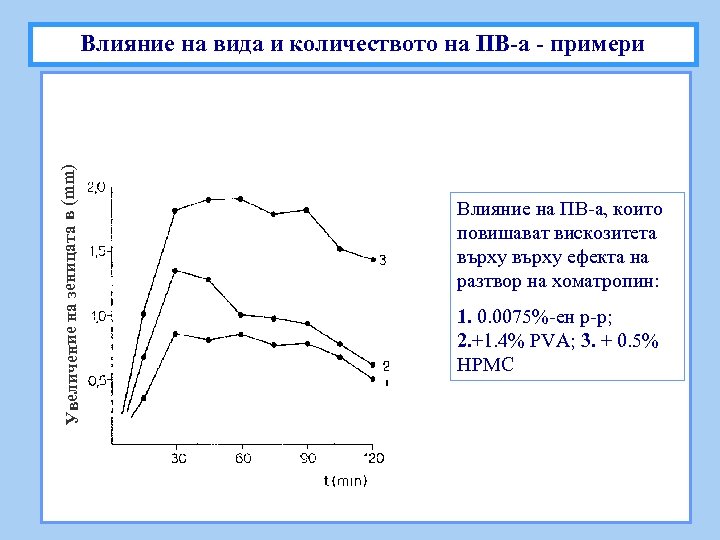
Увеличение на зеницата в (mm) Влияние на вида и количеството на ПВ-а - примери Влияние на ПВ-а, които повишават вискозитета върху ефекта на разтвор на хоматропин: 1. 0. 0075%-ен р-р; 2. +1. 4% PVA; 3. + 0. 5% HPMC
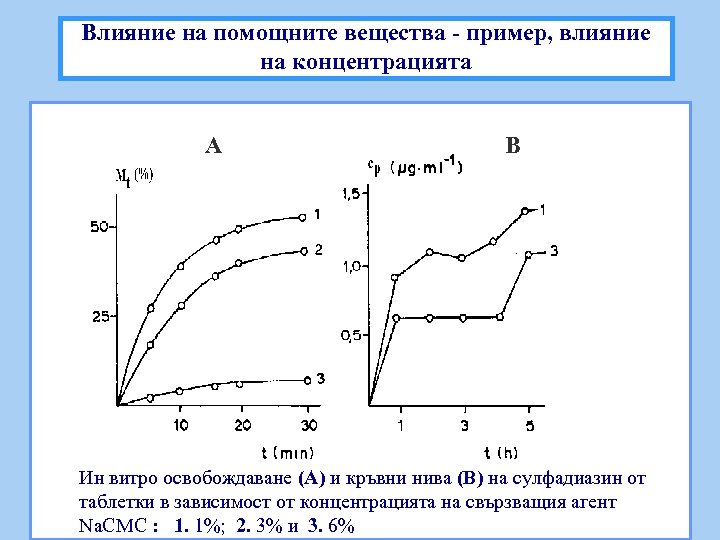
Влияние на помощните вещества - пример, влияние на концентрацията А В Ин витро освобождаване (A) и кръвни нива (B) на сулфадиазин от таблетки в зависимост от концентрацията на свързващия агент Na. CMC : 1. 1%; 2. 3% и 3. 6%

Свойства на ЛФ Вид на ЛФ Път на въвеждане Примери: Разтвор парентерален суспензия перорален прах ректален капсули назален гранули вагинален таблетки терапевтична система Помощни вещества Примери: носители технология Примери: точност при дозиране посредници за разтваряне вид таблетиране емулгатори условия на сушене на гранули суспендиращи агенти стабилизатори вид таблетна машина опаковка
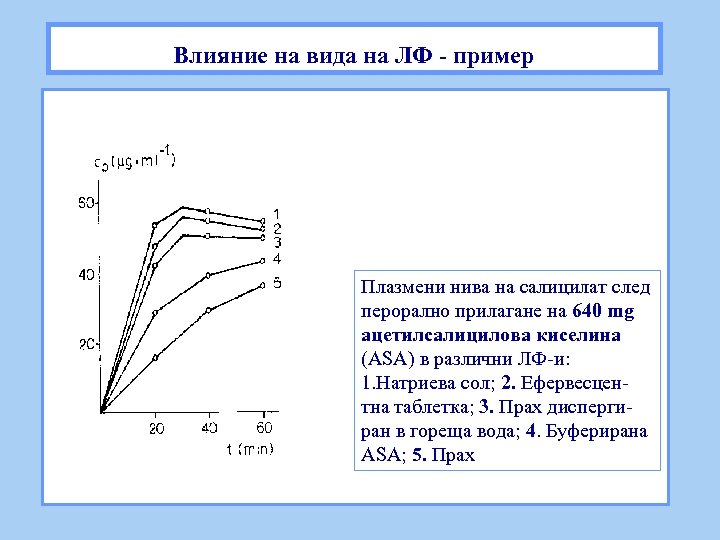
Влияние на вида на ЛФ - пример Плазмени нива на салицилат след перорално прилагане на 640 mg ацетилсалицилова киселина (ASA) в различни ЛФ-и: 1. Натриева сол; 2. Ефервесцентна таблетка; 3. Прах диспергиран в гореща вода; 4. Буферирана ASA; 5. Прах
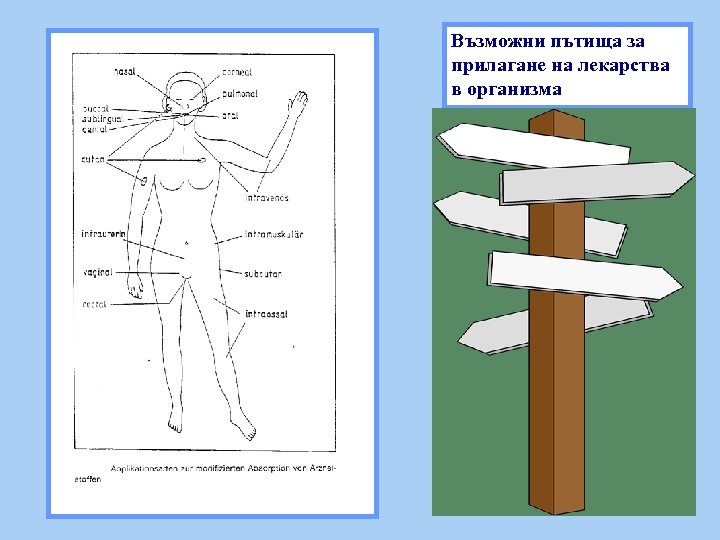
Възможни пътища за прилагане на лекарства в организма
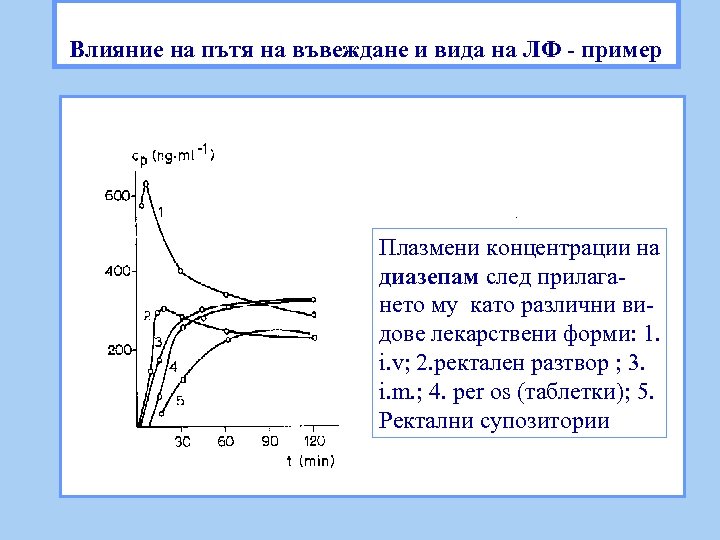
Влияние на пътя на въвеждане и вида на ЛФ - пример Плазмени концентрации на диазепам след прилагането му като различни видове лекарствени форми: 1. i. v; 2. ректален разтвор ; 3. i. m. ; 4. per os (таблетки); 5. Ректални супозитории
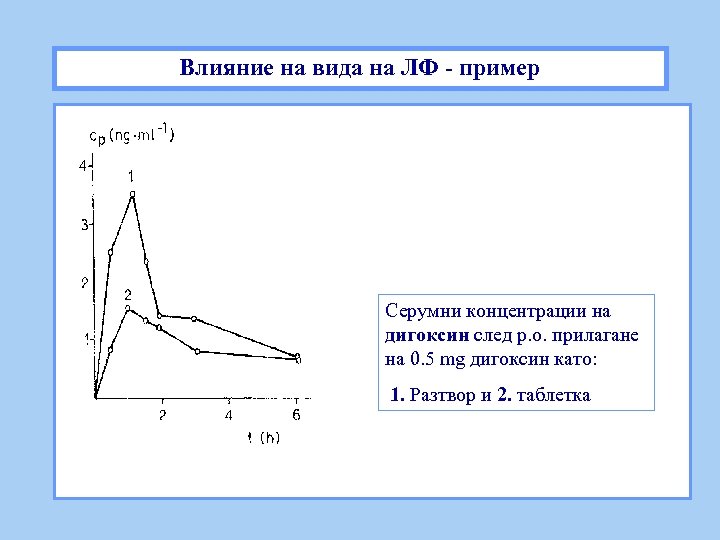
Влияние на вида на ЛФ - пример Серумни концентрации на дигоксин след p. o. прилагане на 0. 5 mg дигоксин като: 1. Разтвор и 2. таблетка
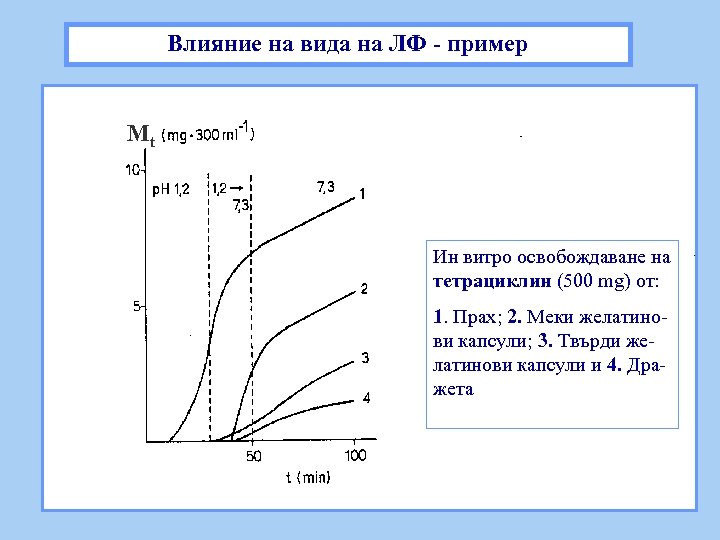
Влияние на вида на ЛФ - пример Mt Ин витро освобождаване на тетрациклин (500 mg) от: 1. Прах; 2. Меки желатинови капсули; 3. Твърди желатинови капсули и 4. Дражета
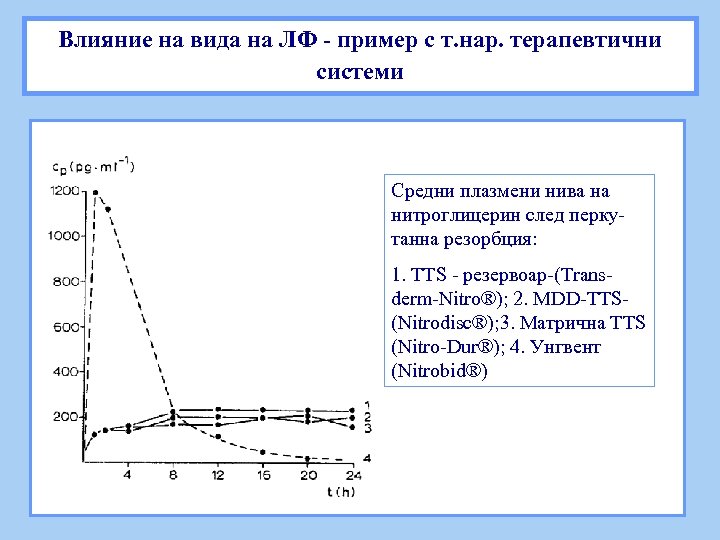
Влияние на вида на ЛФ - пример с т. нар. терапевтични системи Средни плазмени нива на нитроглицерин след перкутанна резорбция: 1. TTS - резервоар-(Transderm-Nitro®); 2. MDD-TTS(Nitrodisc®); 3. Матрична TTS (Nitro-Dur®); 4. Унгвент (Nitrobid®)
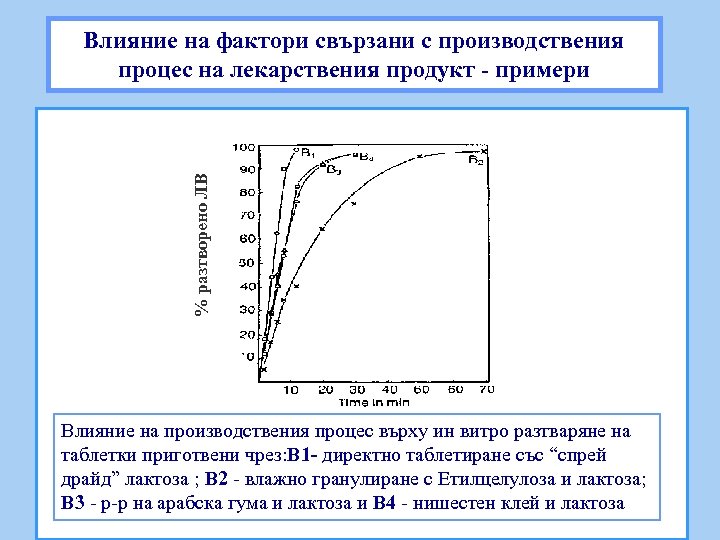
% разтворено ЛВ Влияние на фактори свързани с производствения процес на лекарствения продукт - примери Влияние на производствения процес върху ин витро разтваряне на таблетки приготвени чрез: В 1 - директно таблетиране със “спрей драйд” лактоза ; B 2 - влажно гранулиране с Етилцелулоза и лактоза; В 3 - р-р на арабска гума и лактоза и В 4 - нишестен клей и лактоза

!!! Други биофармацевтични понятия Фармацевтични еквиваленти - два лекарствени продукта, представляващи един и същи вид ЛФ, които съдържат една и съща доза на едно и също ЛВ , които са създадени по най-добрата съществуваща технология и отговарят на съответни фармакопейни и други стандарти. Могат да се различават по вида и количеството на ПВ-а, срок на годност, механизми на освобождаване.

Фармацевтични алтернативи - два лекарствени продукта съдържащи едно и също лекарствено ядро, но ЛВ-а са различни соли, естери или комплекси на това ядро, или са включени в различни ЛФ или има разлика в дозите

Биоеквивалентни продукти - два лекарствени продукта с едно и също ЛВ, които дават една и съща бионаличност, ако се прилагат върху едни и същи доброволци в една и съща моларна доза и еднаква схема на дозиране при подобни експериментални условия Терапевтични еквиваленти - два лекарствени продукта с едно и също ЛВ, които показват една и съща активност и/или токсичност, ако се прилгат на едни и същи доброволци в една и съща доза и схема на дозиране. Терапевтичната еквивалентност може да се определя само в ограничен брой случаи.
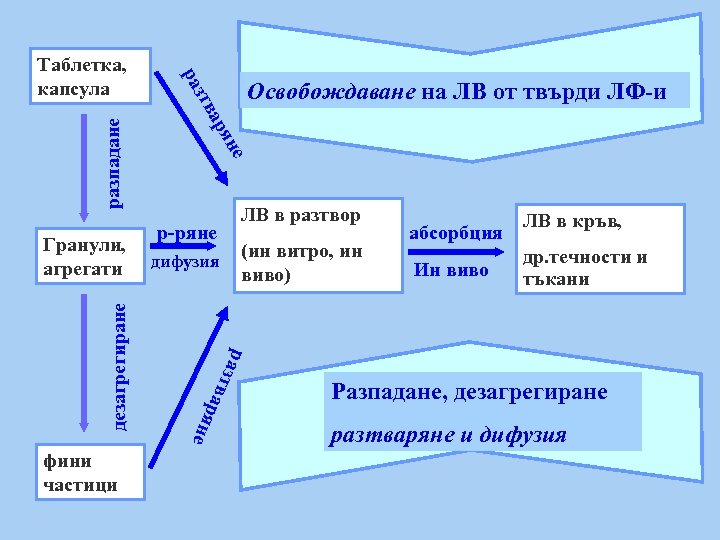
р-ряне дифузия (ин витро, ин виво) в раз т разпадане дезагрегиране не ря ЛВ в разтвор ар яне фини частици Освобождаване на ЛВ от твърди ЛФ-и ва Гранули, агрегати зт ра Таблетка, капсула абсорбция Ин виво ЛВ в кръв, др. течности и тъкани Разпадане, дезагрегиране разтваряне и дифузия
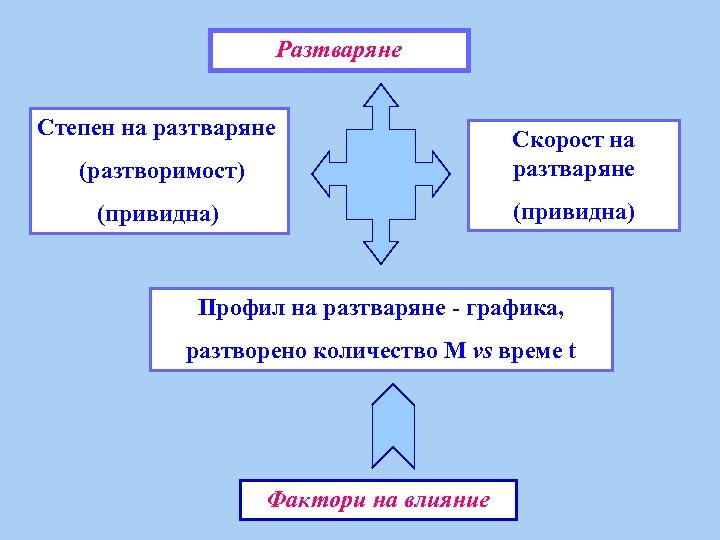
Разтваряне Степен на разтваряне (разтворимост) Скорост на разтваряне (привидна) Профил на разтваряне - графика, разтворено количество М vs време t Фактори на влияние
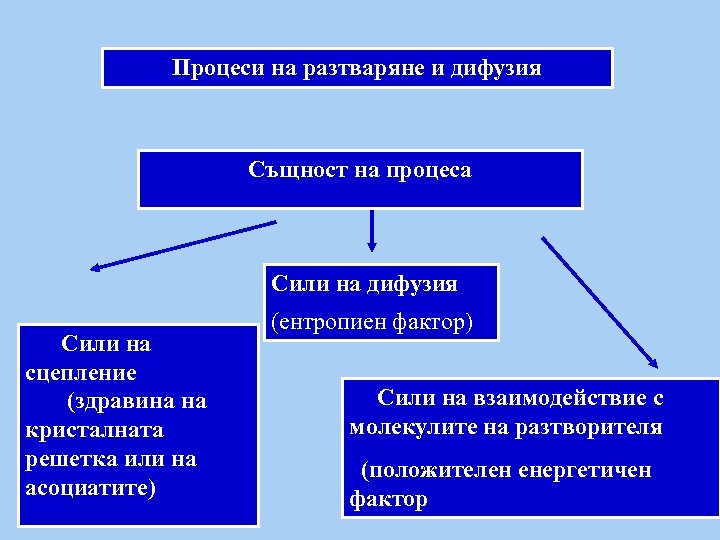
Процеси на разтваряне и дифузия Същност на процеса Сили на дифузия Сили на сцепление (здравина на кристалната решетка или на асоциатите) (ентропиен фактор) Сили на взаимодействие с молекулите на разтворителя (положителен енергетичен фактор

РАЗТВАРЯНЕ Дефиниция Процес, при който при определени условия (t, p) дадено вещество поставено в контакт с течност наречена разтворител, се разпада на молекули, йони или агрегати (частици с размер 1 -100 nm). “Откъсналите се” молекули или йони преминават, дифундират в разтворителя, където се разпределят до получаване на една хомогенна фаза, наречена истински разтвор, а агрегатите съответно до получаване на еднородна ултрамикрохетерогенна колоидна система.
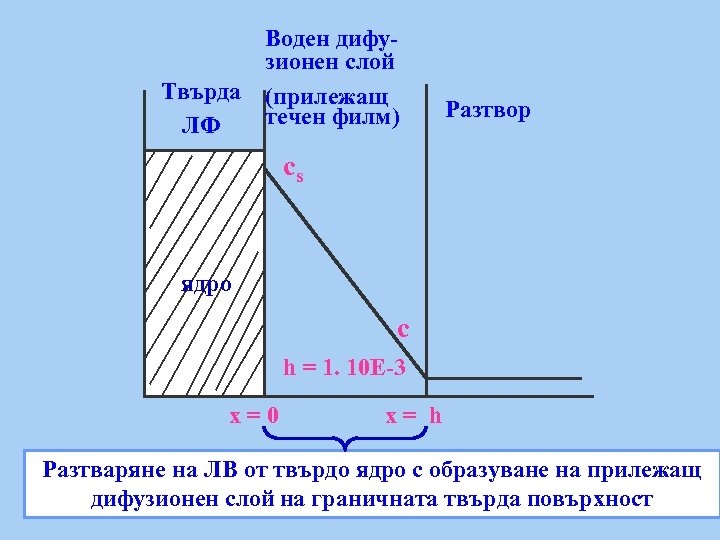
Твърда ЛФ Воден дифузионен слой (прилежащ течен филм) Разтвор cs ядро c h = 1. 10 E-3 x=0 x= h Разтваряне на ЛВ от твърдо ядро с образуване на прилежащ дифузионен слой на граничната твърда повърхност

Процес на разтваряне в организма Ур. Noyes - Whitney (1897 г. ); Nernst, Brunner Dc/dt = (D/h. V). S (cs - ct) (dc/dt) (d. M/dt) скорост на разтваряне S твърда контактна повърхност D дифузионен коефициент на ЛВ h дебелина на дифузионния слой cs разтворимост на ЛВ ct концентрация на ЛВ в даден момент t (D/h. V) = к ( разбъркване, температура и др. ) cs > ct “синк” условия
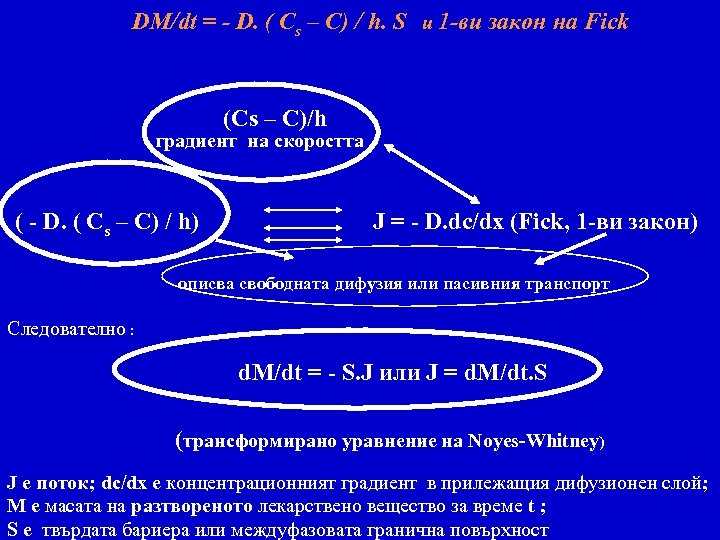
DM/dt = - D. ( Cs – C) / h. S и 1 -ви закон на Fick (Cs – C)/h градиент на скоростта ( - D. ( Cs – C) / h) J = - D. dc/dx (Fick, 1 -ви закон) описва свободната дифузия или пасивния транспорт Следователно : d. M/dt = - S. J или J = d. M/dt. S (трансформирано уравнение на Noyes-Whitney) J е поток; dc/dx е концентрационният градиент в прилежащия дифузионен слой; M е масата на разтвореното лекарствено вещество за време t ; S е твърдата бариера или междуфазовата гранична повърхност
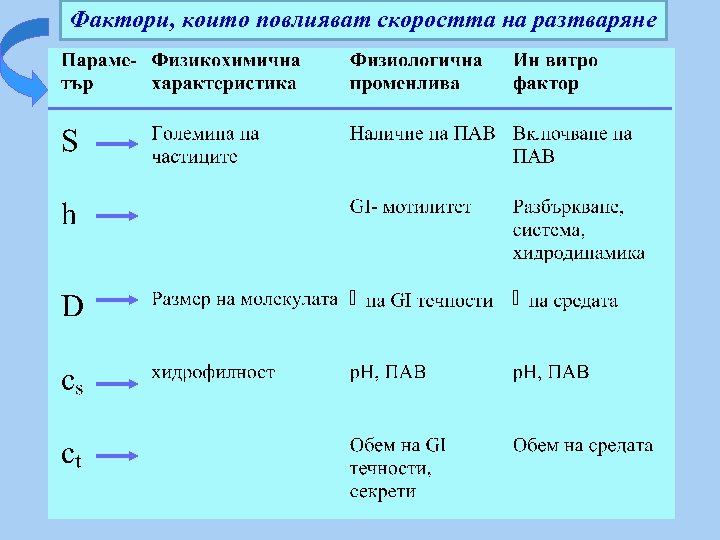
Фактори, които повлияват скоростта на разтваряне
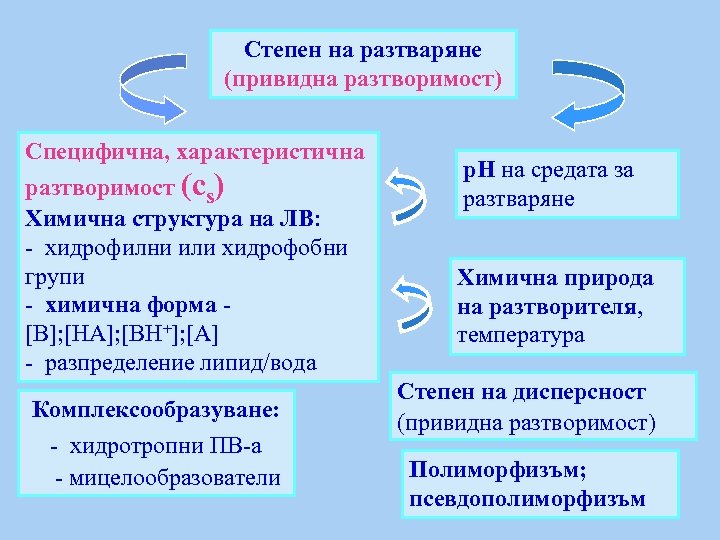
Степен на разтваряне (привидна разтворимост) Специфична, характеристична разтворимост (cs) Химична структура на ЛВ: - хидрофилни или хидрофобни групи - химична форма - [B]; [HA]; [BH+]; [A] - разпределение липид/вода Комплексообразуване: - хидротропни ПВ-а - мицелообразователи р. Н на средата за разтваряне Химична природа на разтворителя, температура Степен на дисперсност (привидна разтворимост) Полиморфизъм; псевдополиморфизъм
![Ур. на Henderson - Hasselbach Разтворимост на ЛВ - слаба киселина [HA] St [HA] Ур. на Henderson - Hasselbach Разтворимост на ЛВ - слаба киселина [HA] St [HA]](https://present5.com/presentation/388345059f83cacea913c10a1eeee158/image-52.jpg)
Ур. на Henderson - Hasselbach Разтворимост на ЛВ - слаба киселина [HA] St [HA] = So ( 1+ 10 p. H - p. Ka ) p. Ka = p. H + log [киселина] [сол] Разтворимост на ЛВ - слаба база - [B] St [B] = So ( 1+ 10 p. Ka - p. H ) p. Ka = p. H - log [база] [сол]

Твърди перорални лекарствени форми - бързо освобождаващи (IR) - с изменено освобождаване (MR) Биофармацевтична класификационна система (BCS)

Сложност на процесите в ГИ тракт – защо? ? ? например, състояние преди приемане на храна и състояние след хранене, цикличния мотилитет след поемане на храна, стомашното изпразване и преминаването през червата, променливото съдържание в лумена, р. Н, ензими, ПАВ и dietary lipids. От друга страна, сложната фармакокинетика на лекарствените вещества – механизъм на абсорбция, проницаемост и промяна на физико-химичните свойства и стабилност на лекарственото вещество по време на ГИ транзит.

Създаването на надеждни модели за предсказване на пероралната лекарствена абсорбция на база на разтварянето на лекарството е все още проблемно. Amidon, G. L. et al. (1995) A Theoretical Basis for a Biopharmaceutic Drug Classification: The Correlation of In Vitro Drug Product Dissolution and In Vivo Bioavailability. Pharm. Res. 12(3) 413 - 420 Corrigan. O. I. (1997)The biopharmaceutic drug classification and drugs administerd in extended release (ER) formulations. Advances in Experimental Medicine and Biology. 423, 111 -128

BCS (Amidon et al. , 1995) е предложена като подход за търсене на зависимости между Ин витро разтварянето на един бързо освобождаващ лекарствен продукт и бионаличността, която той създава Ин виво. BCS: ■ установява база за определяне на условията, при които може да се очаква Ин витро-Ин виво корелация, ■ използва се за установяване на стандарти за БН за IR продукти, ■ използва се за определяне на условията, при които могат да се използват заместители на БЕ- изследвания, ■ включена е в Ръководство на CDER (Center for Drug Evaluation and Research) за Индустрията при оценка на SUPAC промени

Теоретична база на BCS (Amidon G. L. , 1995) 1 -ви закон на Ficк Jw = Pw. Cw където: Jw (x, y, z, t) - (маса/площ/време)е масопреносът през чревната стена Pw (x, y, x, t) - мембранна проницаемост Cw (x, y, z, t) - концентрация на ЛВ върху повърхността на интестиналната мембрана

Скорост на абсорбция = dm / dt = A Pw. Cw. d. A където двойният интеграл обхваща цялата интестинална повърхност гастро- Тоталната маса (М ) на абсорбираното ЛВ за време t се описва с уравнението: M(t) = ot A Pw. Cw. d. A. dt

Проницаемостта Pw се разглежда като зависима от : - мястото, където се осъществява – дуоденум, йейунум, илеум и дебело черво се характеризират с различна морфология и мукозна клетъчна диференциация - времето –зависимост на концентрацията (? ? ? )от други фактори – непряко действие на някои компоненти на лекарството върху мембраната, или на биохимични и физиологични промени вкл. и такива, които засягат мембраната.

Ключови параметри, които контролират абсорбцията на ЛВ 3 безмерни числа Абсорбционно число (Аn) Число на разтваряне (Dn) MRT/AT MRT/MDT (>1) Дозово число (Do) доза/маса р-рена в 250 ml(р. Н 1 - 7. 5) (<1) Легенда: MRT - средно време на престой (стомах, черва и дебело черво); MDT- средно време на разтваряне; AT -време на абсорбция

Число на разтваряне (Dn) Определя се като се допуска, че: • ЛФ е “малтипартикулатна” • скоростта на разтваряне е дифузионно контролирана - модел на Higuchi, Hiestand (водният прилежащ слой е равен или по-голям от радиуса на частицата, която се приема с форма сфера, а промяната на концентрацията на разтворената твърда фаза в разтвора е за пренебрегване във всеки период от време.

D =скоростна константа на дифузия Cs = разтворимост на ЛВ ro = първоначален радиус на частицата = плътност tres = средно време на престой на мястото на абсорбция

Или Числото на разтваряне (Dn) е равно на:

Дозово число (Do)


Абсорбционно число (Аn) или Peff = ефективен коефициент на пропускливост R = радиус на червото (Tes) = средно време на престой в тънкото черво tes = R 2 l/Q (Q = скорост на течене на течността ; l = дължина на червото ) (tabs) = времето на абсорбиране

BCS за IR продукти приема, че • мястото на абсорбция е тънкото черво, • средното време на престой е 180 минути, • Peff стойностите се вземат от проучвания върху хора чрез интубиране и се сравняват с данните за абсолютната бионаличност (вж. Фиг. ) • ЛВ с Peff над 4 х10 -4 cm/sec - с висок пермеабилитет • ЛВ с Peff под 1 х10 -4 cm/sec - с нисък пермеабилитет и следователно, ниска БН
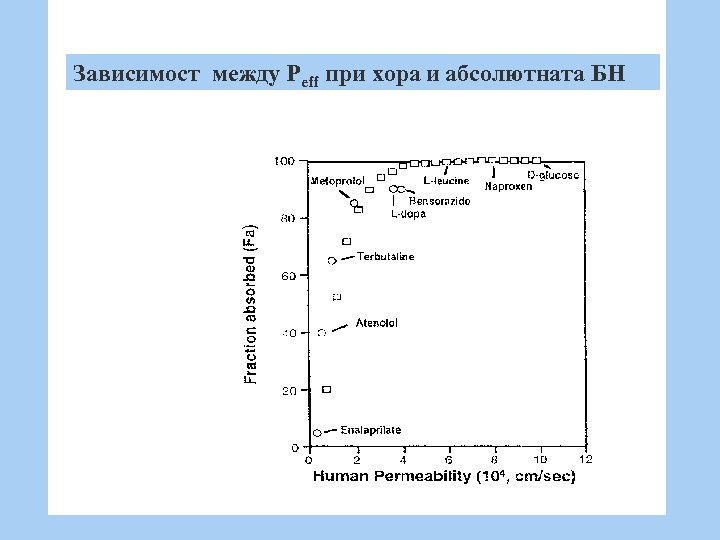
Зависимост между Peff при хора и абсолютната БН
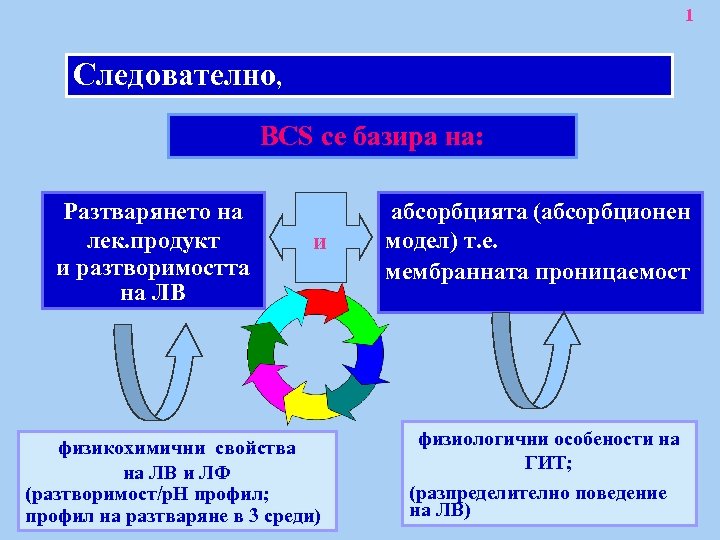
1 Следователно, BCS се базира на: Разтварянето на лек. продукт и разтворимостта на ЛВ и физикохимични свойства на ЛВ и ЛФ (разтворимост/р. Н профил; профил на разтваряне в 3 среди) абсорбцията (абсорбционен модел) т. е. мембранната проницаемост физиологични особености на ГИТ; (разпределително поведение на ЛВ)
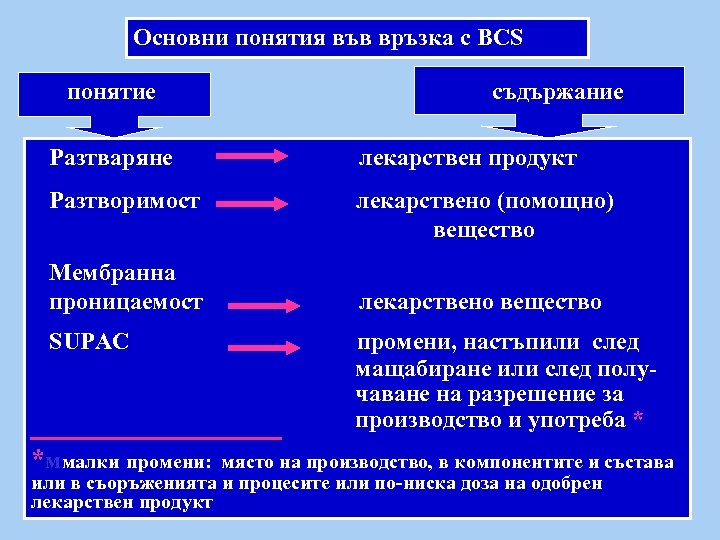
Основни понятия във връзка с BCS понятие съдържание Разтваряне лекарствен продукт Разтворимост Мембранна проницаемост SUPAC *ммалки промени: лекарствено (помощно) вещество лекарствено вещество промени, настъпили след мащабиране или след получаване на разрешение за производство и употреба * място на производство, в компонентите и състава или в съоръженията и процесите или по-ниска доза на одобрен лекарствен продукт

Клас I (например, верапамил, пропранолол метопролол) голяма разтворимост/ висока интестинална проницаемост (скоростоопределящ стадий - изпразването на стомаха или разтварянето на продукта) Клас ІІ (карбамазепин, кетопрофен, напроксен, фенитоин) малка разтворимост/висока интестинална проницаемост (скоростоопределящ стадий - ин виво разтварянето на ЛВ)

Клас ІІІ (симетидин, ранитидин, атенолол) голяма разтворимост/ ниска интестинална проницаемост (скоростоопределящ стадий - проницаемостта на ЛВ; влияние на физиологичните особености) Клас ІV (хидро хлоротиазид, фуросемид) малка разтворимост/ ниска интестинална проницаемост (проблемна абсорбция на ЛВ)
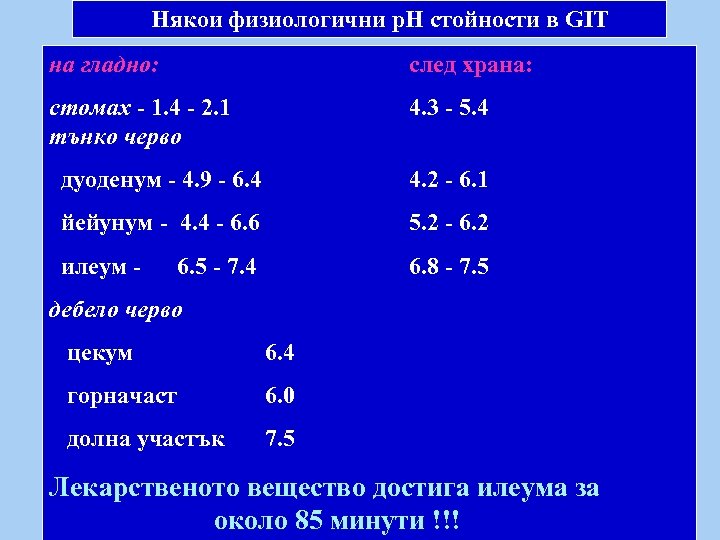
Някои физиологични р. Н стойности в GIT на гладно: след храна: стомах - 1. 4 - 2. 1 тънко черво 4. 3 - 5. 4 дуоденум - 4. 9 - 6. 4 4. 2 - 6. 1 йейунум - 4. 4 - 6. 6 5. 2 - 6. 2 илеум - 6. 8 - 7. 5 6. 5 - 7. 4 дебело черво цекум 6. 4 горначаст 6. 0 долна участък 7. 5 Лекарственото вещество достига илеума за около 85 минути !!!

Време на престой (час) в GIT стомах 0 -3 тънко черво 2 -5 дебело черво 18 физиологичен обем на: тънко черво - 50 -1100 ml (средно 500 ml на гладно) + приблизително 5 m. M жлъчни соли

Голяма разтворимост във вода определя се на базата на най-високата концентрация, доза, на бързо освобождаващ лекарствен продукт, които е обект на съответните изследвания на БЕ. ЛВ се счита като много разтворимо ако неговата най-висока доза е разтворима в 250 ml вода в р. Н областта от 1. 0 до 7. 5 Защо 250 ml ? ? ? протоколи за изследвания на БЕ върху доброволци, които не са поели храна !!!

Бързо разтварящ се лекарствен продукт Лекарствен продукт, от който за 30 минути се разтварят повече от 85% от обозначеното количество ЛВ, в Апарат І (USP) при 100 об. /мин или Апарат ІІ (USP) при 50 об. /мин в 3 вида среда за разтваряне с обем от 900 ml, представляващи съответно: (i) 0. 1 M HCl или изк. стомашен сок без ензими; (ii) буфер с р. Н 4. 5 и (iii) буфер с р. Н 6. 8 или изк. чревен сок без ензими

Висока проинцаемост 1) степента на лекарствената абсорбция при хора е > от 90% (от приложената доза или от от съответна референтна венозна доза), при условие, че ЛВ остава стабилно в GI тракт!!! 2) интестиналната проницаемост е висока, когато се сравнява с избрани референтни продукти прилагане на добре охарактеризирани експериментални методи, както ин виво (например, интестинална перфузия при хора), така и ин ситу (например, интестинална перфузия на животни) или ин витро (например, Caco-2 клетъчни култури) и при условие, че ЛВ остава стабилно в ГИТ.

Възможни източници за непълна абсорбция ЛВ не се освобождава от ЛФ и не се доставя до мястото на абсорбция в ГИ тракт за определен, желан период от време ЛВ се разпада в ГИ тракт или образува не добре абсорбиращ се комплекс ЛВ не се транспортира ефективно през чревната стена в апикална към базална посока ЛВ се метаболизира и/или елиминира по пътя към системното кръвообращение

Лекарствени форми с изменено освобождаване (MR) При ЛФ-и с изменено освобождаване може да участва по-разгънато място на абсорбция. Освобождаването и абсорбцията се влияят главно от 4 физиологични фактора: • времето на престой на всяко място • ефективният коефициент на проницаемост (Peff), • р. Н/буферен капацитет и ефективния обем на интестиналната течност, които могат да се менят с мястото (за йонизиращи се ЛВ-а), • потенциалът на ЛВ да се разгражда на съответно място

ЛФ-и с изменено освобождаване трябва да имат добри характеристики на мембранна проницаемост, затова класовете ІІІ и ІV от класификацията за бързо освобождаващите ЛФ-и са пропуснати.

Биофармацевтична класификационна система на ЛФ-и с изменено освобождаване (Corrigan, 1997)

Клас Іа - голяма разтворимост, очаква се добра IVIVC (ниво А). Използва се 1 среда за разтваряне Клас 1 б - голяма разтворимост , тесен абсорбционен прозорец, абсорбцията в последната част на фазата се контролира от проницаемостта, невъзможна IVIVC ниво А, евентуална възможност за ниво С. Това важи и за ЛВ, които се разграждат в дебелото черво. Клас ІІ - трудно се постигат “синк” условия Клас ІІа - ако се постигнат “синк условия” може да се очаква IVIVC ниво А, не са необходими различни среди Клас ІІб - малко вероятна корелация, в някои отделни случаи абсорбцията може да стане контролирана от разтворимостта

Клас V - ЛВ-а, които се йонизират в ГИТ. Необходимост от ин витро изпитване на разтварянето в среди с променящо се р. Н. IVIVC ниво А може да се очаква при базични ЛВ-а, чието освобождаване не зависи от р. Н. За бази, които са много малко разтворими при р. Н над тяхната р. Ка контролираща абсорбцията става разтворимостта , а не разтварянето. За слабите киселини, които се йонизират значимо в ГИТ, ниво А корелация не се очаква, а се появяват и ефектите на тесния абсорбцио-нен порзорец.
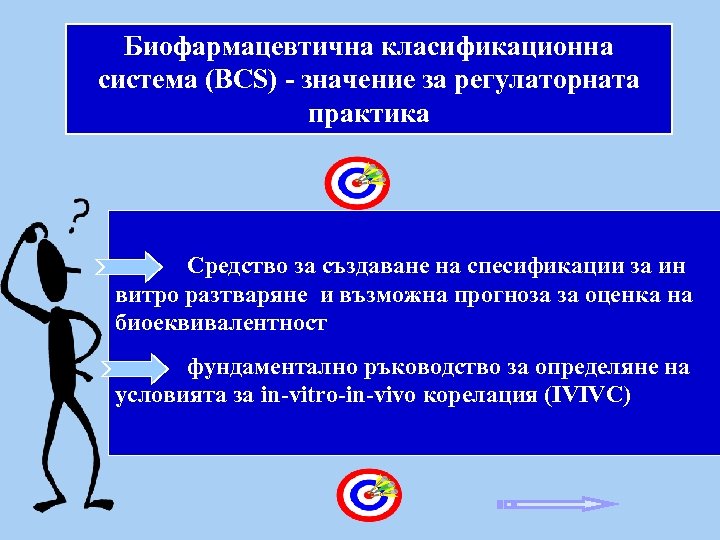
Биофармацевтична класификационна система (BCS) - значение за регулаторната практика Средство за създаване на спесификации за ин витро разтваряне и възможна прогноза за оценка на биоеквивалентност фундаментално ръководство за определяне на условията за in-vitro-in-vivo корелация (IVIVC)

- - може да дава рационална механистична работна рамка за създаване на надеждни тестове за разтваряне, които да служат за оценка на биоеквивалентност, като се разчита минимално на ин виво фармакокинетични данни, - служи за база при определяне на спесификацията (нормите) на параметъра “ин витро разтваряне” - дава указания кога ин виво разтварянето е вероятно или не е вероятно да бъде скоростолимитиращ процес - позволява да се управляват рисковете свързани с надеждността на ин витро теста за разтваряне при оценка на биоеквивалентността и за постигане на успешна ин витро/ин виво корелация

1 (SUPAC) промени ( дефиниции на FDA) 3. Мащабиране и промени след разрешението за употреба Промени в: - компонентите и състава - мащабиране - мястото на производство - производствения процес и апаратурата - опаковка - промяна в дозата на ЛВ

2 3 нива на промени: 1 ниво - промените нямат откриваемо влияние върху качеството и действието на продукта (например, промяна в количеството на някое ПВ) 2 ниво - промените биха имали значимо влияние върху качеството и действието на продукта. Необходими са данни за терапевтичния прозорец на ЛВ, неговата разтворимост и проницаемост 1 ниво и 2 ниво - “Биозаместител” може да се използва !!! - оценка - сравнение на профилите на разтваряне

3 ниво - промените вероятно имат значимо влияние върху качеството и действието на продукта. Например, качествена или количествена промяна в ПВ-а при ЛВ с тесен терапевтичен прозорец Необходимост от ин виво проучвания на БЕ , за да се докаже, че промяната не се отразява на качеството и активността на ЛВ

4 FDA, “Dissolution Testing of Immediate Release Oral Dosage Forms” Guidance for Industry Ръководство за индустрията, съдадено е на базата на BCS Съдържа: - препоръки за провеждане на теста за разтваряне - подходи за определяне на спесификациите за разтваряне въз основа на биофармацевтичните характеристики на ЛВ - статистически методи за сравняване на профилите на разтваряне - как да се установи дали изпитването за разтваряне е достатъчно дасе превърне в биозаместител на изследванията на БЕ.

Пример - някои физиологични особености на ГИ-тракт 1 Стомах Обем - стомашна течност + около 300 ml вода р. Н на стомашна течност - 1 - 3 Време на престой (на гладно) - променливо; t 50% 15 min Пропускливост - ниска, в сравнение с тънкото черво Повърхностно напрежение - по-ниско от водата Хидродинамика

2 Пример - някои физиологични особености на ГИ-тракт Тънко черво Обем (на гладно) - обем от стом. изпразване + собствен обем около 500 ml р. Н - 3 - 8 повърхностно напрежение - ниско Време на престой ( на гладно) - 2 - 4 часа Проницаемост - висока в сравнение с другите части Хидродинамика

10 BCS предполага, че за ЛВ от Клас І и в някои случаи за ЛВ от клас ІІІ, 85% ин витро разтворено количество в 0. 1 М HCl за 15 минути при умерени опитни условия ще означава, че разтварянето на това ЛВ няма да ограничава БН му ин виво. Скоростоопределящият стадий в абсорбционния процес ще бъде стомашното изпразване или разтварянето на лекарствения продукт. Ако разтварянето е по-бавен процес от този на стомашното изпразване, то тогава е необходимо тестът да се проведе в различни среди и да се опише съответния профил на разтваряне. IVIVC не се изисква, но е възможна и е удачна при оценка на SUPAC промени, например.

За ЛВ от Клас ІІ, скоростоопределящият стадий ще бъде разтварянето и може да се очаква IVIVC. Препоръчва се извеждане профилите на разтваряне в различни среди. За ЛВ от клас ІІІ, скоростоопределящият стадий е проницаемостта през клетъчните мембрани и е възможна ограничена IVIVC в зависимост от относителните скорости на разтваряне и интестиналния транзит. ЛВ от клас ІV създават значими проблеми за пероралното доставяне на ЛВ-а.

Кога се използва тестът за разтваряне? ? ? - при създаване на лекарството, избор на състав, определяне на стабилност и срок на годност за проверка качеството на готовия лекарствен продукт при промени след мащабиране или в състава след разрешение за производство и употреба на продукта за предсказване на БН и в някои случаи, за да замести частично клиничните изследвания за биоеквивалентност за оценка и интерпретация на възможни рискове, напр. при ЛФ с изменено осовбождаване - дозов “дъмпинг”, взаимодействия с храна, други ЛВ и т. н.

Ин витро методът трябва: - - да открива влиянието на критични променливи на производството - - да диференцира различни степени на производство на продуктите - - да характеризира биофармацевтичното качество на ЛФ (до известна степен!!!)

Какво се постига с теста за разтваряне ? ? ? биофармацевтична характеристика на лекарствения продукт - възпроизводимост на качеството на производствените партиди т. е. постоянна фармакологична/биологична активност, ефективност и безопасност

Фармакопейни постановки за ин витро разтваряне Затворени системи - основни характеристики Апарат 1 - на принципа на въртяща се кошничка в съд с вместимост 1000 ml Апарат 2 - на принципа на въртяща се бъркалка в съд с вместимост 1000 ml Апарат 3 - на принципа на вертикално движещ се цилиндър, който се потапя в съд с вместимост ………. . ml Апарат 5, 6, 7………….
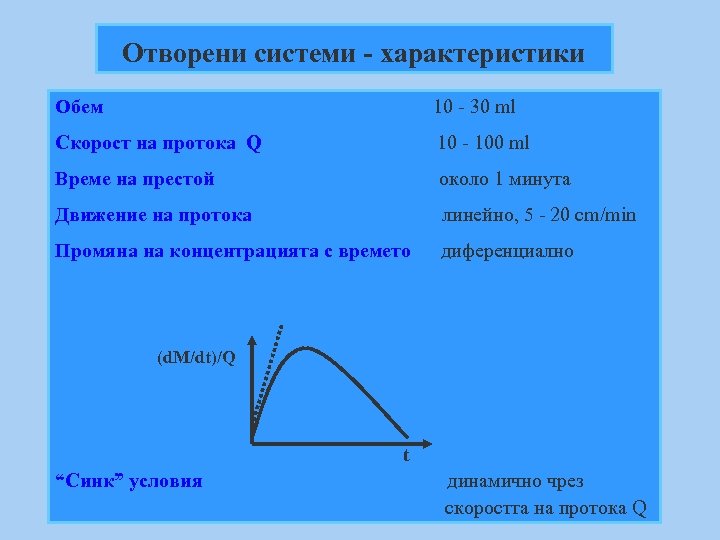
Отворени системи - характеристики Обем 10 - 30 ml Скорост на протока Q 10 - 100 ml Време на престой около 1 минута Движение на протока линейно, 5 - 20 cm/min Промяна на концентрацията с времето диференциално (d. M/dt)/Q t “Синк” условия динамично чрез скоростта на протока Q
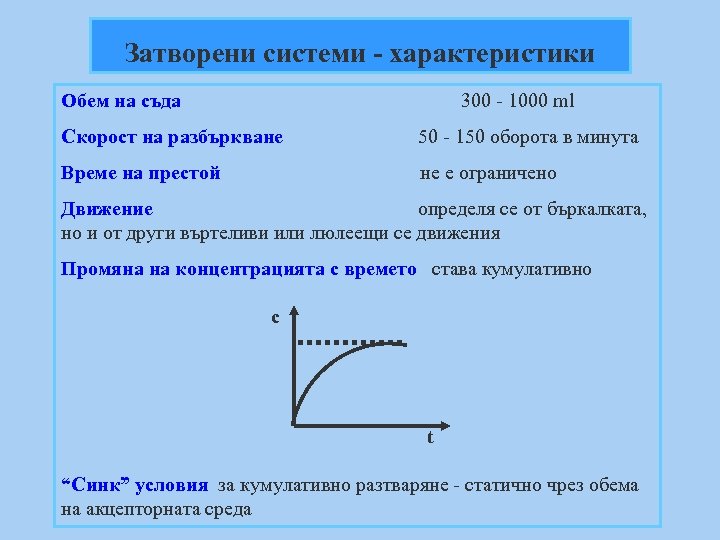
Затворени системи - характеристики Обем на съда 300 - 1000 ml Скорост на разбъркване 50 - 150 оборота в минута Време на престой не е ограничено Движение определя се от бъркалката, но и от други въртеливи или люлеещи се движения Промяна на концентрацията с времето става кумулативно с t “Синк” условия за кумулативно разтваряне - статично чрез обема на акцепторната среда

Избор на опитни условия Изисквания: Извеждане на опитните условия - конкретно за съответен продукт въз основа на съответни данни за БН - да наподобяват физиологичните условия на мястото на прилагане - да отговарят на съответния механизъм на ин виво освобождаване - специфични тестове за даден тип продукт от съответна категория ЛФ

Условия, които се контролират и оптимизират - вид апарат - подход и скорост на разбъркване - р. Н, вид и количество на акцепторната среда - температура - включване на ПАВ - деаериране - време, количество и подход за вземане на проба за анализ - аналитичен метод - спесификацията за разтворено количество за определено време

Среда за освобождаване - вода - препоръчва се за ЛВ-а от Клас І - среда имитираща стомашен сок (p. H 1. 2)* - среда имитираща чревен сок (p. H 6. 8 или 7. 4)* - буфери с р. Н от 4. 5 до 7. 5 Препоръчван обем 500 ml - 1000 ml *с или без ензими

Времетраене на експеримента - 15 - 60 минути (определя се 1 стойност, Клас І, III) - отговаря на t 85%, но се взема проба и на 15 -та мин. (определят се 2 стойности, Клас ІІ ) - сума от 3 времена за разтваряне при ЛФ с изменено освобождаване съответно при : Mt = 20% 30%(обикновено след 1 - 2 h, дозов “дъмпинг”? ? ? ) ; 50% (междинно количество) и съответно 80% (дефинира пълно разтваряне на ЛВ) - 24 часа ако освободеното количество е под 80%,

1 Определяне на спесификации, допустими критерии за теста на разтваряне на бързо освобождаващи ЛФ Въз основа на данни получени с: - основните партиди, изпитвани за БН или БЕ - партидите с успешни клинични изпитвания - основните партиди за изследвания по стабилност на лекарствения продукт в крайната опаковка (3 партиди*, ICH Guideline Stability testing of New Drug substance and Drug Product) Данните трябва да са за продукти с различни дози. З * могат да се използват ако са в биоеквивалентна връзка с партидите с успешна клиника и тези изпитвани за БН и БЕ

2 Категории спесификации: Спесификация за 1 точка не по-малко от (80%) 85% от означеното количество ЛВ да се разтварят за 15 минути в:

Апарат 1 (USP)- 100 об/мин или Апарат 2 (USP) - 50 об/мин, Среда - 900 ml или по-малко 0. 1 М HCl или изкуствен стомашен сок без ензими (USP) ? Буфер с р. Н 4. 5 Буфер с р. Н 6. 8 или изкуствена чревна течност без ензими (USP) Използва се като тест за рутинен качествен контрол при много разтворими ЛВ-а и бързо разтварящи се лекарствени продукти (клас І и клас ІІІ)

Спесификации за 2 точки на: 15 -та минута (прозорец на разтваряне) 30 -та, 45 -та или 60 -та мин. , в зависимост от това кога се достигат 85% разтворено ЛВ Тестът се използва: - за характеризиране качеството на лекарствения продукт - като рутинен тест за качествен контрол при ЛВ-а от клас ІІ , които са с малка разтворимост и бавно разтварящи се (например, карбамазепин)

Описване профил на разтваряне на изпитван и референтен състави във вода, 0. 1 M HCl и буфери съответно с р. Н 4. 5; 6. 5 и 7. 5. Проби се вземат съответно на 15, 30, 45, 60 и 120 -та минути или докато 90% от ЛВ в лекарствения продукт се разтворят или се достигне асимптотата. Където е оправдано може да се използва ПАВ.

Тестът се прилага: - за доказване подобие на лекарствени продукти след SUPAC промени - като заместител на изисквания за БЕ при създаване на лекарствен продукт с по-ниска доза - при създаване на заместители на други изисквания за БЕ - лекарствени вещества от ІІ клас
Валидиране на теста за разтваряне 1. Тест за подходящост (пригодност) на системата за разтваряне при използване на калибратори 2. Деаериране (ако е необходимо, желатинови капсули!) 3. Валидиране между ръчно и автоматично управляване на процесите 4. Валидиране на определящ етап - например, метода за анализ използван за определяне на концентрациите на разтвореното ЛВ. Тук трябва да ес включат всички съответни стъпки и процедури на валидиране на аналитичния метод.
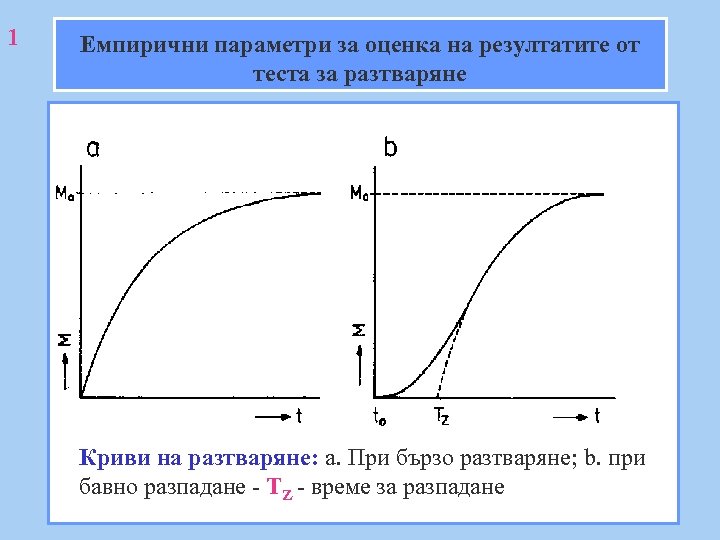
1 Емпирични параметри за оценка на резултатите от теста за разтваряне Криви на разтваряне: а. При бързо разтваряне; b. при бавно разпадане - TZ - време за разпадане
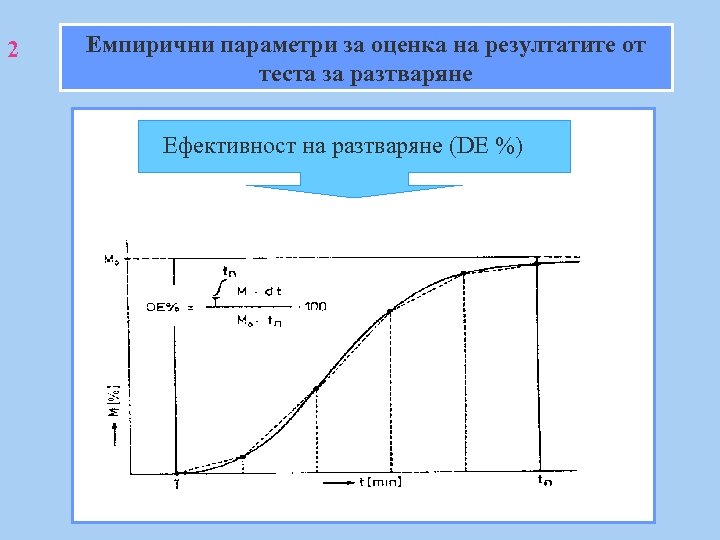
2 Емпирични параметри за оценка на резултатите от теста за разтваряне Ефективност на разтваряне (DE %)
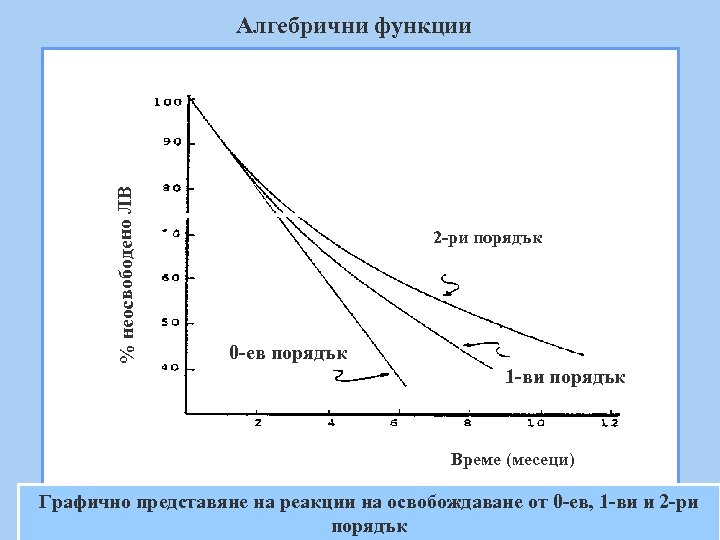
% неосвободено ЛВ Алгебрични функции 2 -ри порядък 0 -ев порядък 1 -ви порядък Време (месеци) Графично представяне на реакции на освобождаване от 0 -ев, 1 -ви и 2 -ри порядък
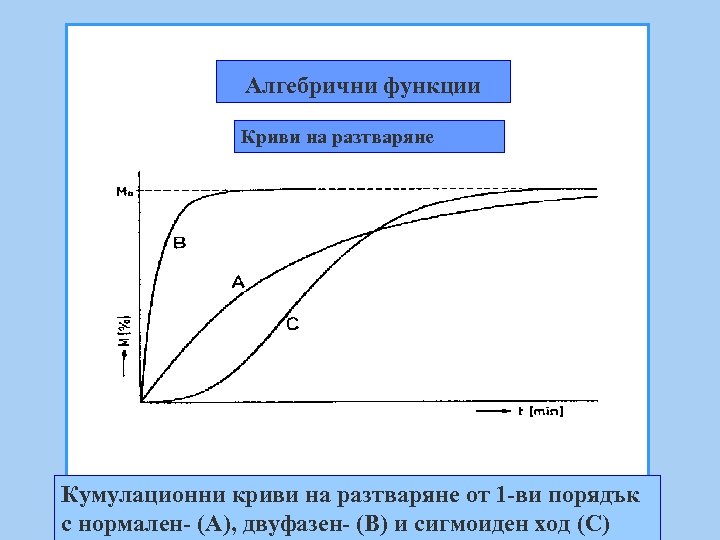
Алгебрични функции Криви на разтваряне Кумулационни криви на разтваряне от 1 -ви порядък с нормален- (A), двуфазен- (B) и сигмоиден ход (C)
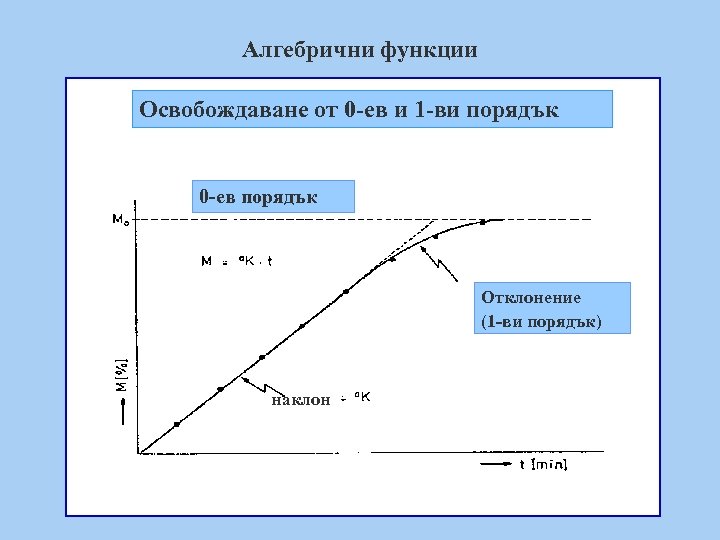
Алгебрични функции Освобождаване от 0 -ев и 1 -ви порядък 0 -ев порядък Отклонение (1 -ви порядък) наклон
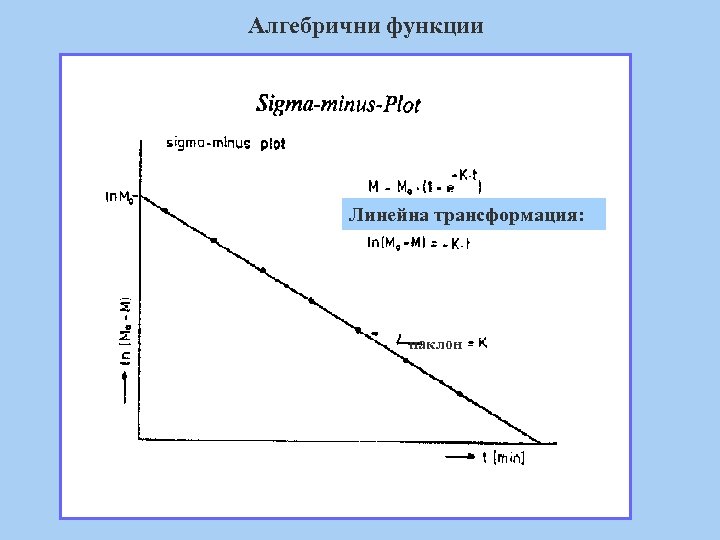
Алгебрични функции Линейна трансформация: наклон
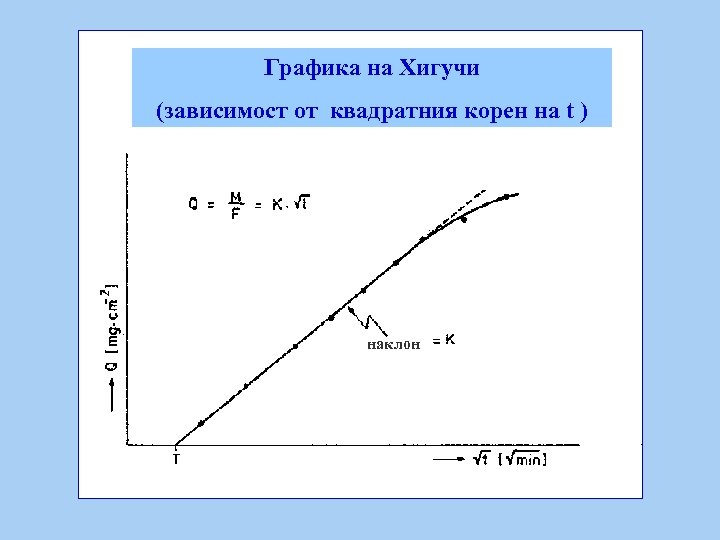
Графика на Хигучи (зависимост от квадратния корен на t ) наклон
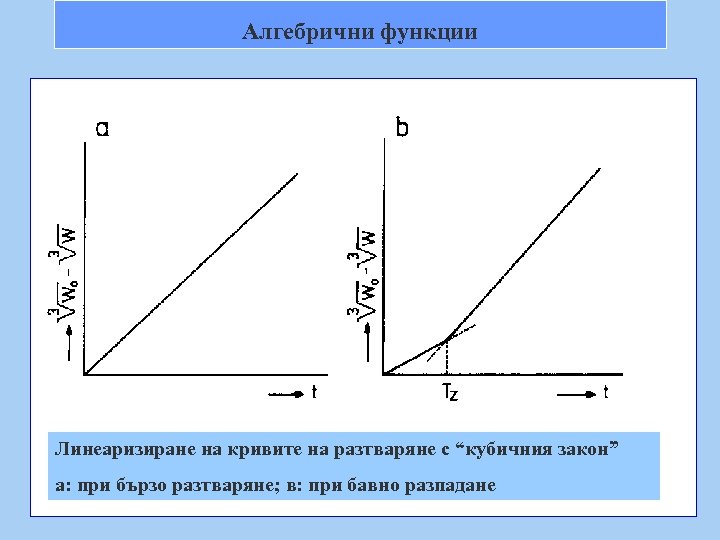
Алгебрични функции Линеаризиране на кривите на разтваряне с “кубичния закон” а: при бързо разтваряне; в: при бавно разпадане
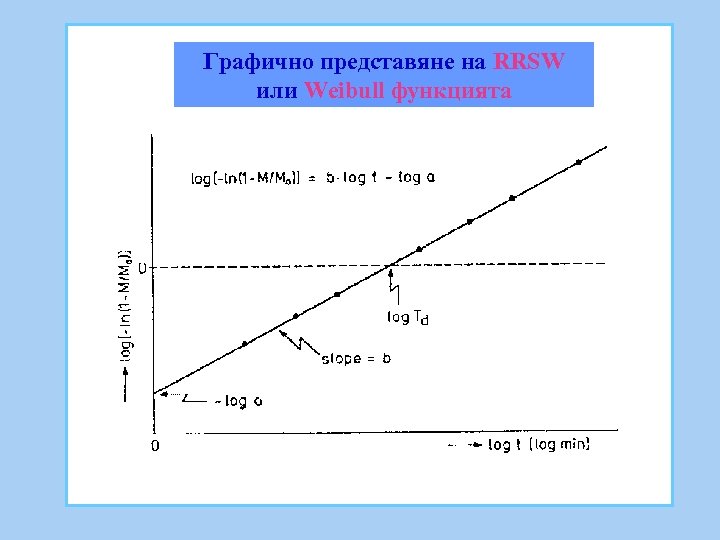
Графично представяне на RRSW или Weibull функцията
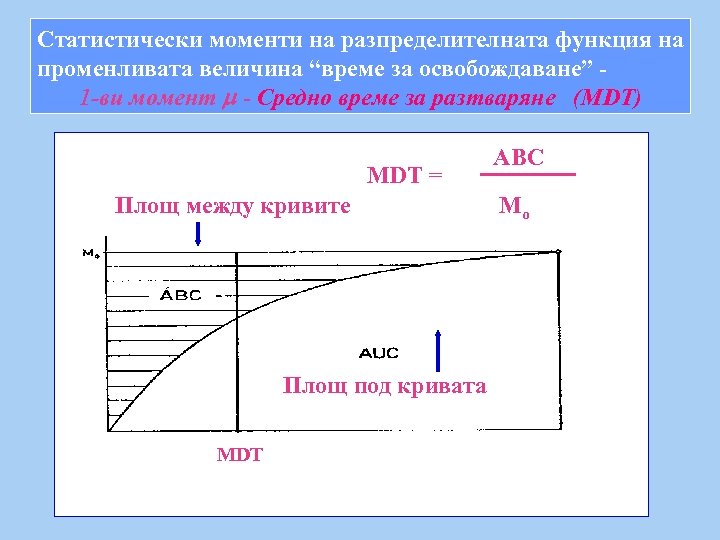
Статистически моменти на разпределителната функция на променливата величина “време за освобождаване” 1 -ви момент - Средно време за разтваряне (MDT) MDT = Площ между кривите Площ под кривата MDT ABC Mo

Еквивалентност на два профила на разтваряне на един и същи лекарствен продукт - Levy Plot Профилите са еквивалентни ако съществува линейна зависимост между времената, за които се разтварят едни и същи количества вещество Важно условие: крайните освободени количества и при двата профила да са над 90%
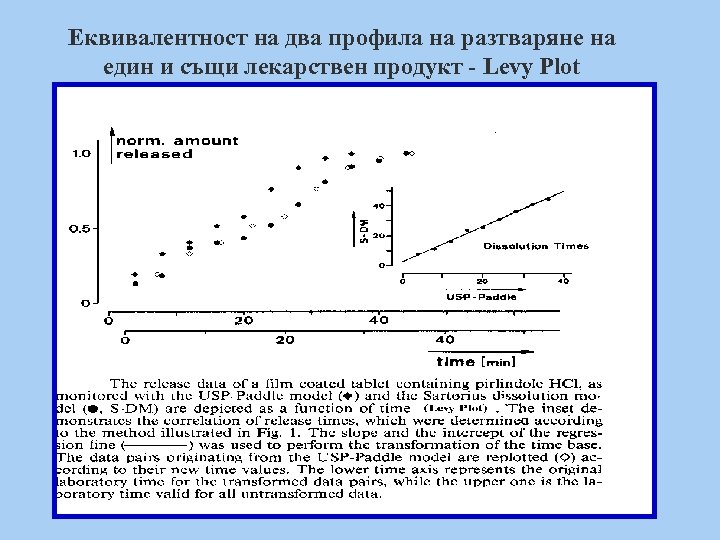
Еквивалентност на два профила на разтваряне на един и същи лекарствен продукт - Levy Plot

Сравняване на профили на разтваряне чрез използване на фактора на подобие f 2 Независими от модела математически подходи: f 1 = {[ t =n ( Rt - Tt )]/[ t = 1 Rt ]}. 100 1 f 2 = 50. Log{[1 + (1/n) t = 1 n(Rt - Tt)2]-0. 5. 100} n Rt и Tt са съответно кумулативния % разтворено ЛВ за всяко от избраните n времена от референтен и изпитван продукти. Факторът f 1 е пропорционален на средната разлика между двата профила, а факторът f 2 е обратно пропорционален на средната разлика между двата профила повдигната на квадрат с подчертаване на по-го-лямата разлика между всичките времена. f 1 - фактор на разликата f 2 - фактор на подобието

Фактор на подобие f 2 Колко голяма може да бъде разликата между 2 профила на разтваряне, без тя да се отрази негативно на ин виво активността на продуктите? ? ? FDA f 2 = 50 - 100

Изисквания: - изследват се 12 единици и се пресмятат средните стойности на параметъра “разтваряне” за всяка точка от времето (вариационен коефициент - 20% за по-ранния интервал от време (напр. 10 -та мин. ) и 10% - за следващите времена) - при голяма вариабилност или ако се търси статистическа оценка се прилагат други подходи за пресмятане на доверителиня интервал - всички изпитвания на двата продукта се провеждат при едни и същи опитни условия, а проби се вземат през еднакви интервали напр. 15, 30, 45 и 60 минути или 1, 2 , 3 , 5 и 8 часа за продукти с изменено освобождаване

Изисквания: - f 2 стойностите са чувствителни към броя времена за вземане на проби, след достигане на 85% разтваряне, се взема само още 1 проба - за лекарствени продукти с бързо разтваряне, т. е. повече от 85% за или по-малко от 15 минути, не е необходимо да се търси фактора на подобие на двата профила - Стойности за f 2 в интервала 50 - 100 осигуряват еднаквост или еквивалентност на двата профила и съответно еднаквост в действието на двата продукта
Създаване на тестове за разтваряне за лекарствени форми с изменено освобождаване - насоки Физико-химични свойства на лекарственото вещество Физиологични условия, които повлияват освобождаването на ЛВ Механизъм на освобождаването на ЛВ и зависимост от р. Н

Апаратура и методики за изследване на ин витро разтварянето на ЛФ с MR Промяна на средата за разтваряне - подход за имитиране на условията в ГИТ- р. Н градиент или условия след храна и на гладно Особено подходящи са : Прибор 3 (потапящ се, вертикално движещ се цилиндър, създават се конвективни сили за разтваряне) и Прибор 4 (проточна клетка с турбулентен или ламинарен проток ) по USP

Тест за разтваряне за предварителна оценка на качеството на лекарствени форми с изменено освобождаване(FDA) Прибор 1 (с кошничка) за капсули ; 100 об/мин Прибор 2 (с лопатка) за таблетки ; 50 и 75 об/мин Температура - 37 о. С Единици за изпитване - 12 Обем на средата за разтваряне - 900 ml с различно р. Н Интервал за вземане на проби - 1, 2, 4 -ти час и след това през 2 часа докато се освободят 80% от ЛВ

Тест за разтваряне за лекарствени форми с изменено освобождаване (FDA) Данните се представят като кумулативно разтворено количество, може да се пресметне и средна скорост на освобождаване за 0 -ев процес. Задължително се определя краен пункт, в който се освобождават не < от 80 (85)% или се достига асимптотата. При отклонения >10% - необходимост от IVIVC или определяне на БЕ.

При това: профилът на разтваряне трябва да включва поне 3 времена за разтваряне съответно при : Mt = 20% - 30% след 1 - 2 h, (отсъствие на дозов “дъмпинг”? ? ? ) ; Mt = 50% (междинно количество) и Mt = 80% (дефинира пълно разтваряне на ЛВ) t = 24 часа ако освободеното количество е под 80%,

Създаване на тест за разтваряне на лекарствени продукти с малко разтворими във вода лекарствени вещества За малко разтворимите във вода ЛВ-а освобождаването е скоростоопределящ стадий в общия абсорбционен процес ин виво. Трудности при създаване на метод и опитни условия за изследване освобождаването респ. разтварянето ин витро.

Подходи за преодоляването им: • използване на водно-алкохолна или водно-органична акцепторна среда • увеличаване на обема на акцепторната среда • увеличаване скоростта на разбъркване Изкуствени, не отговарят на физиологичните условия

Предлаган “алгоритъм” за създаване на ин витро тест за разтваряне на лекарствени продукти с малко разтворими във вода ЛВ-а ( препоръки на FDA ) Базира се на: - естествените за живия организъм различни ПАВ, които улесняват разтварянето и абсорбцията ин виво - р. Н на средата в ГИТ тракт физиологично релевантни подходи Изискват, обаче задължителна корелация с ин виво активността на лекарствения продукт

Схема на “Алгоритъма” 1 -ва стъпка: Оценка на средата за разтваряне ефект на р. Н Апарат 1 - на принципа на въртяща се кошничка с 100 - 120 об. /мин или Апарат 2 - на принципа на въртяща се лопатковидна бъркалка с 50 - 75 об. /мин Обем на средата - 900 - 1000 ml Изпитват се 3 среди: - 0. 1 N HCl; ацетатен буфер с р. Н 4. 5; фосфатен буфер с р. Н 6. 8 брой на пробите - 2 единици

2 -ра стъпка: Определяне вида на ПАВ (Изборът се прави въз основа на химичната природа на ЛВ) Изпитва се по 1 представител от групите съответно на: катионоактивни (напр. СТАВ), анионоактивни (SLS) и нейонни ПАВ (Tween) в конц. 2%. Брой на изпитваните единици - 2

3 -та стъпка: Определяне концентрацията на ПАВ (Водещ принцип: да се установи най-ниската ефективна концентрация, осигуряваща Q = или >85% за t < 120 мин. ) Примерни концентрации за изпитване: 0. 1, 0. 25, 0. 75, 1. 0 и 2. 0%

Примери : Carbamazepine Tablets Ап. 2, 75 rpm, 900 ml вода + 1. 0% SLS Критерий: 30 - 75%/15 мин; Q = 85%/60 мин Cortizone acetate Tablets Ап. 2, 50 rpm, 1000 ml вода + 0. 5% SLS Критерий: Q = 75%/45 мин

Примери: Griseofulvin Capsules Ап. 2, 50 rpm, 1000 ml вода + 0. 54% SLS Критерий: Q = 80%/20 мин Prazosin HCl Capsules Ап. 1, 100 rpm, 900 ml 0. 1 N HCl 0 + 2. 0% SLS Критерий: Q = 80%/60 мин

Проблеми при сравняване на 2 бързо освобождаващи ЛФ-и - разлики в ин витро профилите, но близки ин виво профили - разтварянето ин виво не е скоростоопределящ стадий ? ? ? - 2 продукта отговарят на критерия за Q 80% (85%), но се явяват разлики в плазмените профили - по-лоши показатели на ин витро разтваряне, по-висока плазмена концентрация (много по-рядко!!!)

Възможни причини: - неподходящ критерий за оценка - например, една точка - неподходящи условия на ин витро теста (състав на акцепторната среда, р. Н, обем, хидродинамика) - ПВ, което променя абсорбцията на ЛВ - други причини - статистически грешки и т. н. Следователно, за продукти с бавно разтваряне ин виво е необходимо да се установи ин витро-ин виво корелация и нейното прогнозно действие да бъде потвърдено чрез експеримент.
1 Физиологични условия, които повлияват освобождаването на ЛВ Време на интестинален транзит Изпразване на стомаха - 2 h на гладно Промяна на р. Н - химически взаимодействия с полимерен материал, напр. Пример с неразпадаща се ЛФ - в присъствие на храна, тя остава или отгоре или отдолу (плътност!!!), освобождаването на ЛВ ще се контролира от изпразването на стомаха

2 Биомагнитни измервания с Магнитен Маркер - използват се капсули маркирани с магнит (l = 16. 1 mm, d = 5. 7 mm), за изследване на стомашното изпразване и дуоденалния транзит. Стомашно изпразване на гладно - 14 до 140 минути, теста 2 h в изк. стомашен сок е подходящ Дуоденален транзит - 7 - 245 сек. 3 - 17 сек. (през проксималния дуоденум); 4 - 235 сек. (през дисталния дуоденум) Трудно се имитират тези условия ин витро ако се цели таргетно доставяне на ЛВ в дуоденума - за 7 сек. чревният филм трудно би се разтворил и освободил ЛВ ако филмът е биоразграждащ се при р. Н 6. 5, р. Н в проксималния дуоденум е към 5. 5. Необходи-мост от изследвания при няколко р. Н и съобразяване с потен-циалното време на престой ин виво при всяко едно р. Н

3 Пример с обвити частици, пелети [ предимства пред неразграждащите се лекарство доставящи системи: - диспергират се в ГИТ; - обвити с различни обвивки; показват пропорционалност спрямо дозата ] Стомашното изпрозване е с постоянна скорост, при добра гранулометрия Препоръчвани условия за тест за разтваряне (зависи от дизайна на лекарство доставящата система): - 2 - 3 часа в изкуствен стомашен сок с р. Н 1. 2 - 15 - 30 минути в изкуствена интестинална течност с р. Н 5. 5 - следва разтваряне в изкуствена интестинална течност с р. Н 6. 8 или р. Н 8. 0
4 Ефект на храната върху: Стомашното изпразване- храни с мазнини повишават времето на пребиваване в стомаха Солубилизацията на ЛВ - храни с мазнини влияят, а също и повишават отделеното количество жлъчни соли, а те могат да станат солубилизатори Освобождаването на ЛВ Транспорта на ЛВ през мембраните - липидите повлияват чревните стени и повишават проницаемостта им

1 “Биозаместители” на ин виво проучванията за бионаличност и биоеквивалентност (БЕ) , които се базират на BCS “Биозаместители” - кога могат да се създават ? ? ? - ЛВ трябва: да показва бързо и подобно разтваряне, да принадлежи към Клас І - голяма разтворимост и проницаемост, да има широк терапевтичен прозорец, в ЛФ да са използвани разрешени ПВ-а, които не повлияват скоростта и степента на абсорбция

Необходими данни, доказващи целесъобразността на “биозаместителя” Данни доказващи бързото и подобно разтваряне За заместители на проучването на ин виво ОБН, разтвореното количество за 30 мин. трябва да е > от 85% в препоръчваните 3 среди. За заместители на проучването на ин виво БЕ, изпитваният и референтният продукти трябва да показват подобни профили на разтваряне фактор на подобие f 2 - 50 - 100 във всяка от 3 -те среди.

Данни доказващи висока интестинална проницаемост Фармакокинетични данни от опити върху хора заедно с информация за организацията на проучването и използваните методи Данни от опити по метода на директно определяне на проницаемост, информация за подходящост на метода, критерии за избора на субектите - хора, животни, епителни клетъчни линии, лекарствени концентрации, описание на аналитичния метод, метода за пресмятане на степента на абсорбция или проницаемост, информация за потенциал на изтичане (ако се налага)

Данни за избраните моделни ЛВ-а за доказване на подходящост на метода…. . Данни за проницаемостта на изпитваното ЛВ и използваните методи за определянето й, вътрешните стандарти, информация за стабилността на ЛВ и доказателства за пасивен транспорт (ако е необходимо)
2 “Биозаместители” ин виво проучванията на БЕ , които се базират на BCS лекарственият продукт да е бързо разтварящ се (IR) - количеството на ПВ-а да отговаря на функцията, която ще изпълняват високите концентрации могат да създадат проблеми например, ПАВ или осмотични агенти - всички стойности на другите фармацевтично технологични параметри трябва да отговарят на съответната спесификация

3 “Биозаместители” на ин виво проучванията на БЕ на базата на BCS “Биозаместители” на базата на BCS !!! не могат да се използват !!! при лекарствени вещества с тясна терапевтична ширина ЛВ-а, които се абсорбират в устната кухина при ЛФ-и с изменено освобождаване има допълнителни изисквания

Биозаместители без IVIVC - Примери Бързо освобождаващи ЛФ-и 1. По-ниска/по-висока концентрация на ЛВ Когато няколко концентрации от една и съща ЛФ са “пропор-ционално подобни” по отношение на ЛВ и ПВ-а, може да се използва: “биозаместител” за ниска концентрации ако: - има сравнимост на профилите - успешни ин виво проучвания на високата концентрация “биозаместител” за по-висока концентрация ако: - е потвърдена клиничната безопасност и ефективност на тази доза -ЛВ проявява линейни фармакокинетични характеристики в терапевтичната дозова зона - профилите на различните концентрации са сравними

Биозаместители без IVIVC-Бързо освобождаващи ЛФ-и 2. Клиничен състав спрямо vs. състав разрешен за употреба В някои случаи разликата в състава за клинични изпитвания и този, който е в употреба е, например, че за клинични изпитвания се използват капсули със съдържанието на 1 таблетка с цел провеждане на слепи опити. Употреба на “биозаместител” на проучванията на БЕ възможно е !!! ако: - в капсулата не са включени допълнително други ПВ-а - профилите на разтваряне са снети в 3 среди - 0. 1 M HCl, фосфатен буфер с р. Н 4. 5 и съответно 6. 8.

Биозаместители без IVIVC - ЛФ-и с изменено освобождаване Примери: 1. Капсули с пелети - по- ниска концентрация “Биозаместител” за по-ниската доза - може да се използва !!! ако: - има данни за БЕ на продукта с по-високата концентрация (прилагане на единична доза , на гладно) - се снемат ин витро профилите на разтваряне за всяка концентрация - сравняването на профилите се извършва с фактора на подобие f 2 и ако f 2 > 50

Биозаместители без IVIVC - ЛФ-и с изменено освобождаване 2. Таблетки - модел с по-ниска концентрация Възможно е използване на “биозаместител” !!! ако: - има ин виво данни за лекарствения продукт с по-високата доза - сравняваните продукти са една и съща ЛФ, но с различна концентрация ЛВ - продуктите са пропорционално подобни по отношение на активно ЛВ и ПВ-а - освобождават ЛВ по един и същи механизъм - профилите на разтваряне за по-високата и съответно пониска концентрация се снемат в 3 среди (р. Н 1. 2, 4. 5 и 6. 8) - сравняването на профилите е с фактора на подобие f 2

Биозаместители без IVIVC - ЛФ-и с изменено освобождаване 3. Мащабиране и промени след разрешение за употреба Използването на “биозаместител”е възможно само ако промените са ниво 1 и ниво 2. За ниво 2 промени се провеждат допълнителни изпитвания, различни от тези в досието или съответната фармакопейна статия и в зависимост от типа ЛФ с изменено освобождаване Например, за ЛФ със забавено освобождаване, (delayed release) - в 0. 1 M HCl - 2 h и след това при р. Н 4. 5 - 7. 5 при стандартни условия + при 2 различни скорости на разбъркване За ЛФ с изменено освобождаване (extended release) - допълнително в 3 среди - вода, 0. 1 M HCl и буфер с р. Н 4. 5 - 7. 5

Биозаместители въз основа на IVIVC за ЛФ с изменено освобождаване БЕ проучвания могат да бъдат заместени ако е установена IVIV корелация (например, най-често ниво А) и е оценена нейната предсказуемост. Може да се използва “биозаместител” !!! за продукт с по-ниска концентрация ако: - разликата в предсказания среден пик на плазмената концентрация (Cmax) и площта под кривата плазмена концен-трация/време AUC на продукта за изпитване и референтния продукт е не повече от 20%

- ако продуктите с ниската и висока доза са пропорцио-нално подобни или количествено еднакви - профилите на ин витро разтваряне са подобни - всички концентрации освобождават по еднакъв механи-зъм, а дозите са безопасни и ефективни
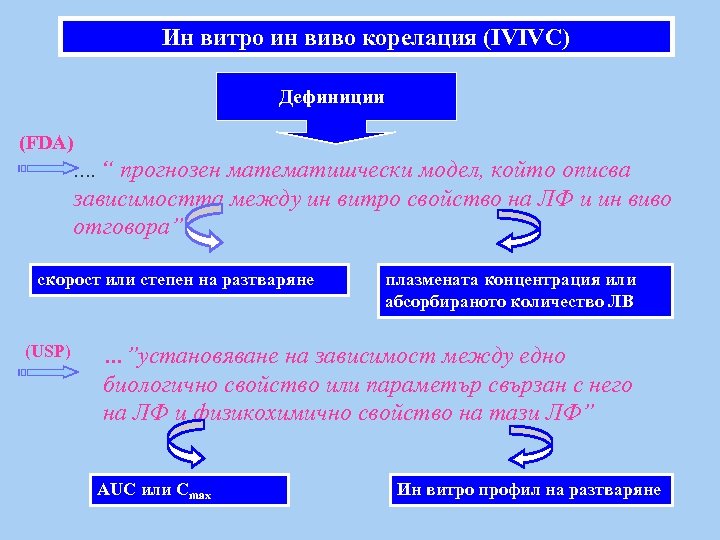
Ин витро ин виво корелация (IVIVC) Дефиниции (FDA) …. “ прогнозен математишчески модел, който описва зависимостта между ин витро свойство на ЛФ и ин виво отговора” скорост или степен на разтваряне (USP) плазмената концентрация или абсорбираното количество ЛВ …”установяване на зависимост между едно биологично свойство или параметър свързан с него на ЛФ и физикохимично свойство на тази ЛФ” AUC или Cmax Ин витро профил на разтваряне

Валидираната IVIVC* играе важна роля в създаването на един лекарствен продукт Защо? ? ? - служи за създаване на “биозаместители” на ин виво проучванията на БЕ върху хора. - за създаване и/или валидиране на тест за разтваряне и съответните спесификации - за избор на състав в процеса на създаване на лекарството - доказване на качеството, възпроизводимостта на партидите и стабилността в процеса на производство * само за продукти с еднакъв механизъм на освобождаване

1 Категории на IVIVC Ниво А най-общ тип корелация; ин витро данните трябва да предсказват целия ин виво процес Използват се 2 или 3 състава с различна скорост на освобождаване (бързо, умерено и бавно освобождаване) Принцип: IVIVC ниво А се определя чрез трансформиране на ин виво плазмените данни във фракция абсорбирано ЛВ

2 Стадии : 1. Пресмятане фракцията абсорбирано ЛВ 2. Графично представяне на фракцията абсорбирано ЛВ vs. фракцията разтворено ЛВ за съответен интервал от време; пресмятане на линейната регресия Корелацията е линейна и изразява зависимост във всяка точка между ин витро разтварянето и ин виво скоростта на освобождаване на ЛВ. При линейна зависимост кривите на ин витро разтваряне и ин виво “инпут” на ЛВ се припокриват (възможно е и използване на скалиращ фактор)

Определяне на ин виво абсорбцията 1. Методи зависими от модела: Метод на Wagner - Nelson - за еднокомпартиментен модел Метод на Loo-Riegelman - за многокомпартиментна система, изисква данни от венозно въвеждане

Определяне на ин виво абсорбцията 2. Независими от модела методи деконволуция - числен метод, който се използва да се определи (“input”) концентрацията на ЛВ с времето и който използва математически модел с конволуционен интеграл. Алтернативен подход - конволуционна техника, която моделира зависимост между ин витро разтваряне и плазмена концентрация в една стъпка. Предсказаните чрез съответен математичен модел концентра-ции и тези, които се наблюдават се сравняват директно.

2 Категории на IVIVC Ниво В използва се статистически моментен анализ Принцип: Сравнява се ин витро средното време за разтваряне със средното време на престой (MRT) или средното време на разтваряне (MDT) в организма. Корелация В не е корелация във всеки момент. Много често не отразява еднозначно действителната плазмена крива, тъй като много криви могат да покажат близки, подобни MRT.

3 Категории на IVIVC Ниво С много рядко се установява Принцип Установява се в една точка от време зависимост между даден параметър на разтваряне, например, t 50%- 4 h, и един фармакокинетичен параметър, например, AUC, Cmax, Tmax. Този тип коерлация не отразява профила плазмена концентрация/време!!!

Категории на IVIVC Многопараметрово Ниво С Принцип свързват се един или няколко фармакокинетични параметри с количеството разтворено ЛВ в няколко точки от време от профила на разтваряне

Ниво В и ниво С корелация се търси в процеса на избор на състав за лекарствения продукт - ПВ-а, технологична схема и др. Ниво А е най-високото ниво на корелация - взема се предвид целия плазмен профил; препоръчва се за ЛФ-и с изменено освобождаване Установена и валидирана IVIVC ниво А означава: създаване на “биозаместители” създаване на спесификации за ин витро тест за разтваряне
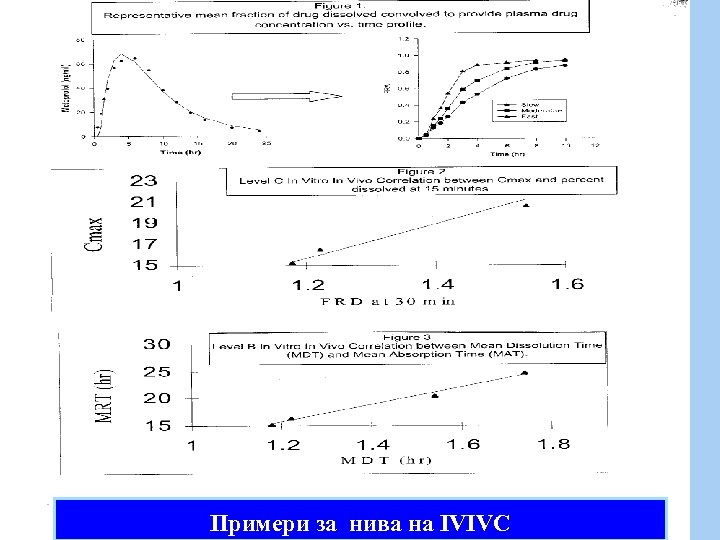
Примери за нива на IVIVC

Подходи за постигане на IVIVC 1. Намиране на съответен математически модел, който да описва зависимостта между ин витро - ин виво разтварянето 2. Избор на различни условия за изследване на разтварянето, за да се постигне действителния ин виво профил на разтваряне

Стратегии за създаване на ин витро тест за разтваряне Скъпи, но подходящи за установяване на IVIVC при доказване на промени вследствие на мащабиране или след получен лиценз за производство и употреба (SUPAC) - Среда за разтваряне съдържаща смесени мицели - натриев таурохолат и яйчен лецитин (4: 1) - Среда за разтваряне - М/В емулсии трудно за работа, особено при 37 о. С - среда с по-високо съдържание на липиди - особено ако е необходимо да се извежда IVIVC - имитиране на гастро-интестиналния метаболизъм, особено ако ще се търси IVIVC

Биорелевантни среди за разтваряне Симулирани стомашни течности на гладно HCl М 0. 01 - 0. 05 Натриев лаурилсулфат 2. 5 g Натриев хлорид 2. 0 g Дестилирана вода q. s. 1 liter
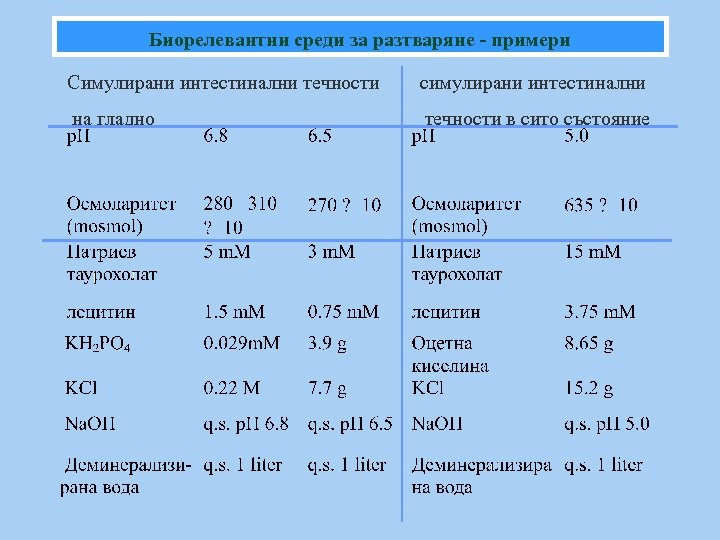
Биорелевантни среди за разтваряне - примери Симулирани интестинални течности симулирани интестинални на гладно течности в сито състояние
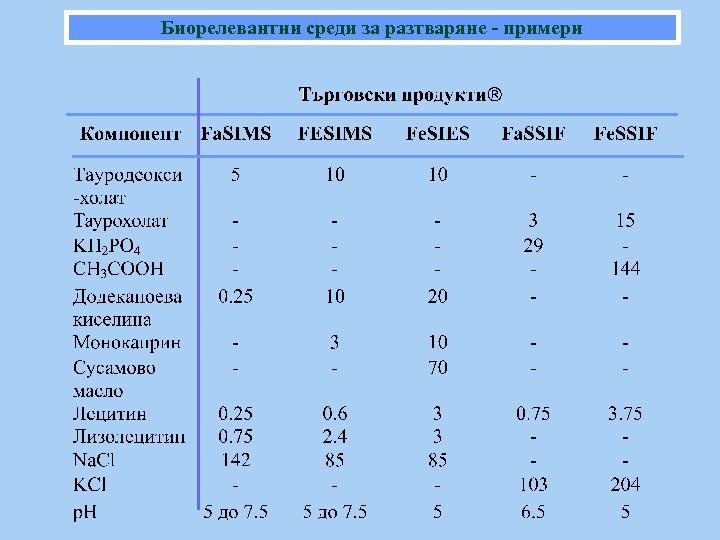
Биорелевантни среди за разтваряне - примери

Очаквана IVIVC за бързо освобождаващи ЛФ-и на базата на BCS на Amidon et al. (1995)

Очаквана IVIVC за лекарствени продукти с изменено освобождаване на базата на BCS на Corrigan (1997)

Какво означава: ? ? ? - Осигуряване на качеството изпитване постоянство в качеството на партидите дава информация за партиди изследвани за IVIVC и основни клинични изпитвания дава индикации за разлики в БН доказва качеството след мащабиране на производствения процес или промени след лиценз за производство и употреба дава информация за референтния продукт, използван в IVIVC и клиничните изследвания

2 ? ? ? Ин витро тестовете за разтваряне могат да намалят броя на необходимите ин виво опити ако дават надеждна: - оценка на възпроизводимостта на качеството на производствените партиди и основания за освобождаване на партидата - служат за контрол на процесите и за осигуряване на качеството - за оценка необходимостта от следващи изследвания на БЕ, ако са въведени малки промени след лицензиране на продукта.
388345059f83cacea913c10a1eeee158.ppt