Биофармацевтика, занятие 2 Фармацевтическая разработка биотехнологических субстанций и


Биофармацевтика, занятие 2 Фармацевтическая разработка биотехнологических субстанций и лекарственных форм МГУ, ФФМ 26.03.13 Иван И. Воробьев, к.х.н. [email protected]
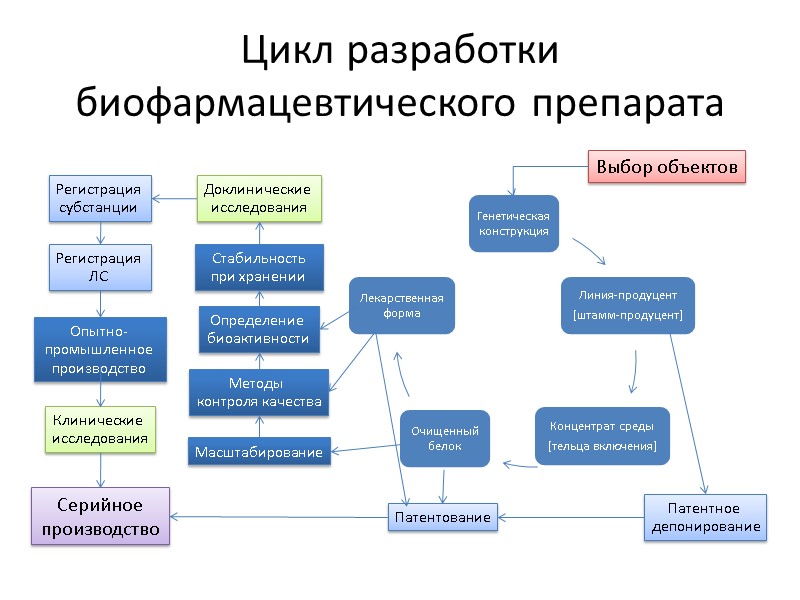
Цикл разработки биофармацевтического препарата Выбор объектов Патентное депонирование Патентование Масштабирование Определение биоактивности Методы контроля качества Стабильность при хранении Доклинические исследования Регистрация субстанции Регистрация ЛС Опытно-промышленное производство Клинические исследования Серийное производство

Оригинальные и воспроизведенные лекарственные средства «Оригинальное (инновационное) лекарственное средство – это ЛС, которое было впервые зарегистрировано на основе полной документации в отношении его качества, безопасности и эффективности, защищенное патентом на срок до 20 лет» Directive 2004/27/EC of the European Parliament and of the Council, Art. 10.1. – 2004. «воспроизведенное лекарственное средство - лекарственное средство, содержащее такую же фармацевтическую субстанцию или комбинацию таких же фармацевтических субстанций в такой же лекарственной форме, что и оригинальное лекарственное средство, и поступившее в обращение после поступления в обращение оригинального лекарственного средства» Федеральный закон РФ «Об обращении лекарственных средств» №61-ФЗ от 2010 г.

Воспроизведенные биофармацевтические препараты Синонимы: Biogenerics, Biosimilars, Bio-betters, Follow-on biopharmaceuticals etc. В большинстве случаев точное копирование структуры молекул оригинального биофармацевтического препарата невозможно Оценка биодженериков может быть проведена на основе принципа взаимозаменяемости (interchangeability) – оригинальное и воспроизведенное лекарственные средства взаимозаменяемы, если они эквивалентны терапевтически, фармацевтически, биологически и in vitro WHO Technical Report Series 937, annex 7 « Multisource (generic) pharmaceutical products: guidelines on registration requirements to establish interchangeability». WHO Expert Committee on Specifications for Pharmaceutical Preparations. – WHO, 2006.

Поиск фармацевтически перспективных биополимеров Заболевания, вызванные дефектом единственного гена или потерей функции единственной ткани – продукт гена или секретируемый тканью гормон (инсулин, гормон роста, фактор VIII) Если продукт поврежденного гена не секретируется клетками, заболевание может сдерживаться ферментами, разлагающими патологические продукты ( ДНКаза I при муковисцидозе) Избыточно секретируемые при патологии сигнальные белки могут быть нейтрализованы антагонистами, внеклеточными фрагментами рецепторов и антителами (анти-ФНО антитела, ФНОР-Fc, ИЛ-1ар) Специфические белковые маркеры раковых клеток – опсонизация моноклональными антителами (анти-CD20, анти-HER2/Neu и т.д.) Нейтрализация патогенов путем активной и пассивной иммунизации – поиск специфических токсинов и антигенов Активация или подавление активности клеток иммунной системы – интерфероны, анти-ФНО антитела

Геномика для поиска лекарств Геномика – систематическое изучение полных геномов видов Персональная геномика – полное описание геномов различных особей Основные приложения геномики в фармакологии: 1. Предсказание специфических антигенов и токсинов при сравнении геномных данных патогенных и родственных им непатогенных микроорганизмов 2. Поиск связей между вариантами генов и частотой возникновения заболеваний 3. Поиск новых фармацевтически активных белков

Предсказание функций неизвестных белков - 1

Предсказание функций неизвестных белков - 2
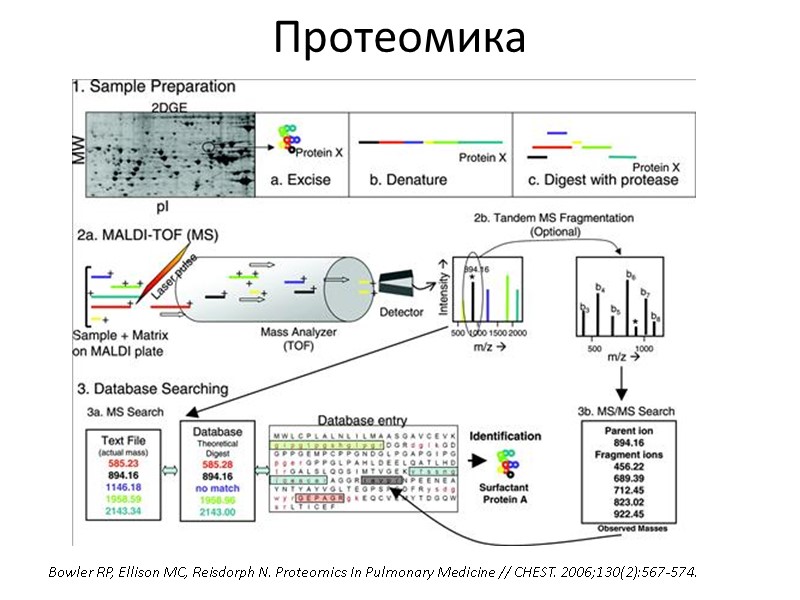
Протеомика Bowler RP, Ellison MC, Reisdorph N. Proteomics In Pulmonary Medicine // CHEST. 2006;130(2):567-574.

Метаболомика Weckwerth W. Anal Bioanal Chem. 2011 Jun;400(7):1967-78.
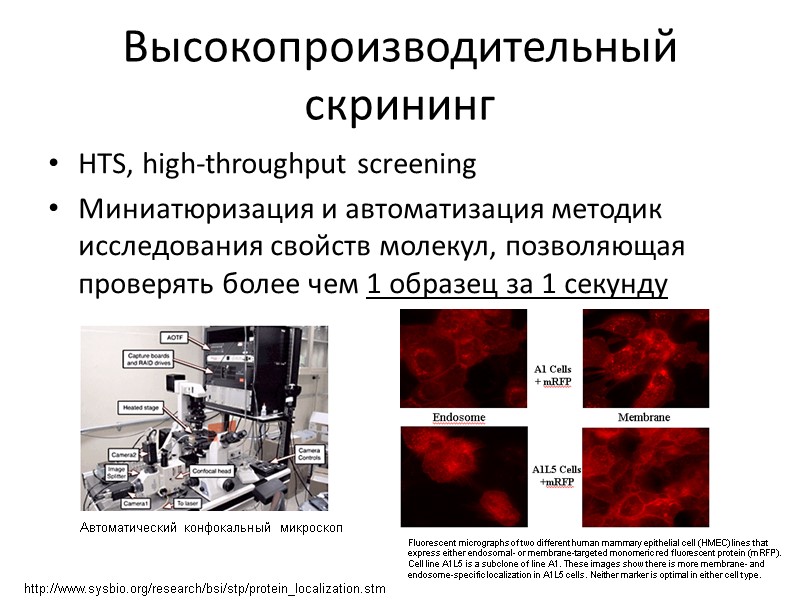
Высокопроизводительный скрининг HTS, high-throughput screening Миниатюризация и автоматизация методик исследования свойств молекул, позволяющая проверять более чем 1 образец за 1 секунду Fluorescent micrographs of two different human mammary epithelial cell (HMEC) lines that express either endosomal- or membrane-targeted monomeric red fluorescent protein (mRFP). Cell line A1L5 is a subclone of line A1. These images show there is more membrane- and endosome-specific localization in A1L5 cells. Neither marker is optimal in either cell type. http://www.sysbio.org/research/bsi/stp/protein_localization.stm Автоматический конфокальный микроскоп
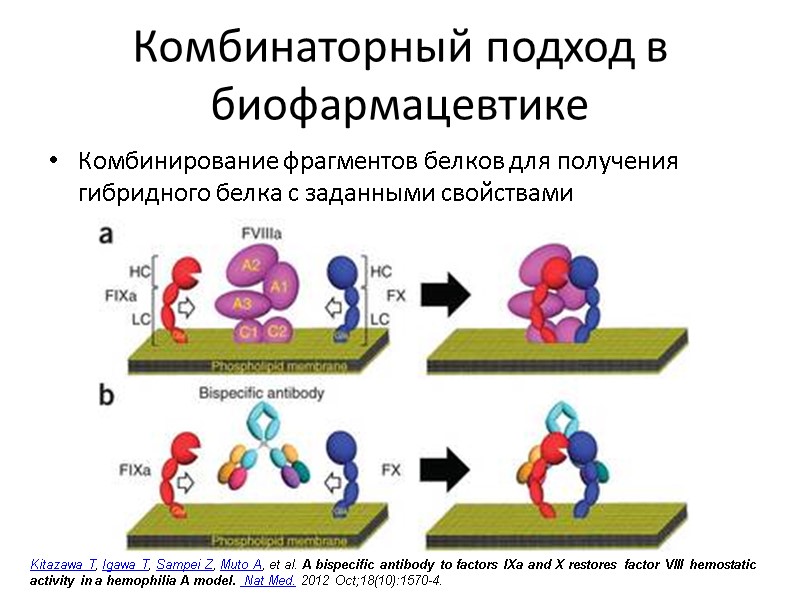
Комбинаторный подход в биофармацевтике Комбинирование фрагментов белков для получения гибридного белка с заданными свойствами Kitazawa T, Igawa T, Sampei Z, Muto A, et al. A bispecific antibody to factors IXa and X restores factor VIII hemostatic activity in a hemophilia A model. Nat Med. 2012 Oct;18(10):1570-4.

Интеллектуальная собственность Раскрытие информации – патенты Сокрытие информации – ноу-хау и коммерческая тайна Что может быть запатентовано (три “П”): Продукт Процесс Применение

Разработка лекарственных форм Традиционные парентеральные формы – лиофилизат и стерильный раствор для инъекций Перспективные способы доставки: Оральный – инкапсуляция, мукозоадгезивные системы доставки Ингаляционный – пыль инсулина Exubera®, отозван из-за низкого спроса Интраназальный, трансдермальный и т.д. Подкожное введение без иглы Biojector 2000 http://www.bioject.com/products/b2000-info

Доклинические исследования Основная цель проведения доклинических исследований – демонстрация безопасности лекарственного средства на животных моделях. 90% новых лекарственных средств не преодолевают доклиничиские испытания Выполняются в контролируемых условиях и должны отвечать требованиям надлежащей лабораторной практики (GLP)

Доклинические исследования - структура Фармакокинетика (ADME) и фармакодинамика Биоэквивалентность и биодоступность Острая, суб-хроническая, хроническая токсичность Репротоксичность и тератогенность Мутагенность, тератогенность Иммунотоксичность, переносимость в месте инъекции

Клинические исследования 1.18 клиническое испытание/исследование (clinical trial/study): Любое исследование, проводимое с участием человека в качестве субъекта для выявления или подтверждения клинических и/или фармакологических эффектов исследуемых продуктов и/или выявления нежелательных реакций на исследуемые продукты, и/или изучения их всасывания, распределения, метаболизма и выведения с целью оценить их безопасность и/или эффективность. Термины "клиническое испытание" и "клиническое исследование" являются синонимами. Надлежащая клиническая практика. ГОСТ Р 52379-2005 Клинические испытания успешно проходят 10-20% новых лекарственных средств
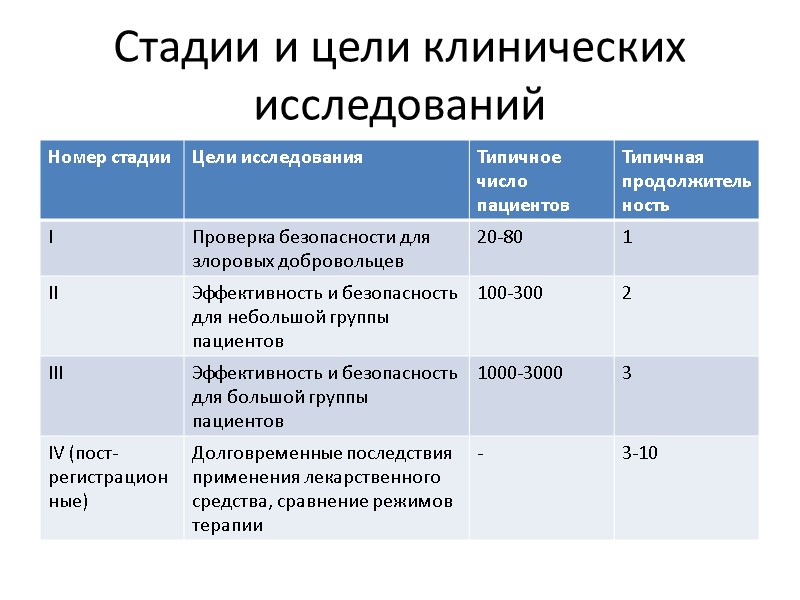
Стадии и цели клинических исследований

Регистрационное досье 1. Административные документы 2. Описание фармацевтических свойств Cостав и описание лекарственного средства, содержание основных действующих веществ, физико-химические, биологические, микробиологические свойства. 3. Данные о производстве лекарственного средства Схема производственного процесса, контроль этапов производства и промежуточных продуктов, валидация или квалификация процесса. 4. Данные по контролю качества лекарственного средства Методы контроля качества лекарственного средства, аналитические процедуры, валидация аналитических процедур, посерийный анализ, результаты исследований стабильности. 5. Доклинические исследования лекарственного средства 6. Сведения о результатах клинических исследований лекарственного средства

Иван И. Воробьев, лаборатория биоинженерии клеток млекопитающих Центра «Биоинженерия» РАН, лаборатория биокатализа Института биоорганической химии РАН, [email protected]
40716-ffm_2013_lec_2.ppt
- Количество слайдов: 20

