a52057c528d4bd151a99957902d59de6.ppt
- Количество слайдов: 15

Bioequivalencia en Chile Dra. María Teresa Valenzuela B. Directora Instituto de Salud Pública de Chile
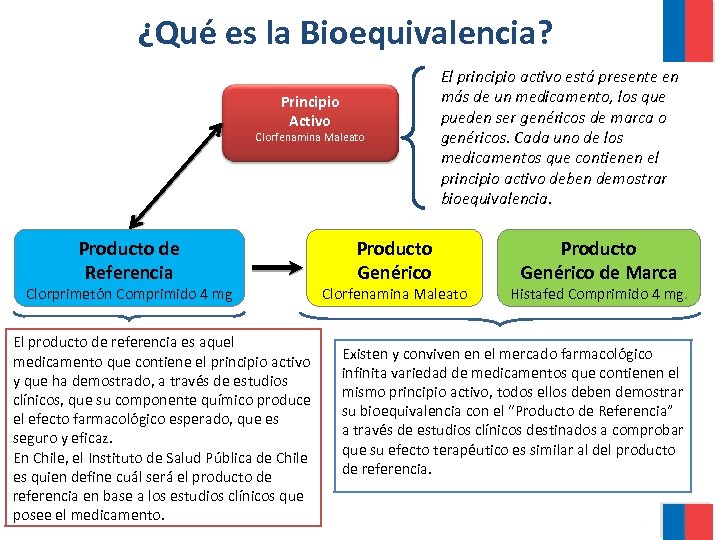
¿Qué es la Bioequivalencia? Principio Activo Clorfenamina Maleato Producto de Referencia Clorprimetón Comprimido 4 mg El producto de referencia es aquel medicamento que contiene el principio activo y que ha demostrado, a través de estudios clínicos, que su componente químico produce el efecto farmacológico esperado, que es seguro y eficaz. En Chile, el Instituto de Salud Pública de Chile es quien define cuál será el producto de referencia en base a los estudios clínicos que posee el medicamento. Producto Genérico El principio activo está presente en más de un medicamento, los que pueden ser genéricos de marca o genéricos. Cada uno de los medicamentos que contienen el principio activo deben demostrar bioequivalencia. Clorfenamina Maleato Producto Genérico de Marca Histafed Comprimido 4 mg. Existen y conviven en el mercado farmacológico infinita variedad de medicamentos que contienen el mismo principio activo, todos ellos deben demostrar su bioequivalencia con el “Producto de Referencia” a través de estudios clínicos destinados a comprobar que su efecto terapéutico es similar al del producto de referencia.
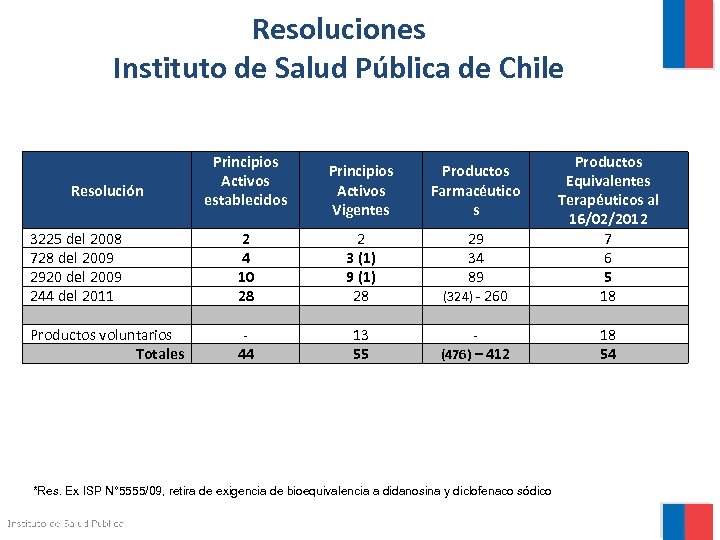
Resoluciones Instituto de Salud Pública de Chile 3225 del 2008 728 del 2009 2920 del 2009 244 del 2011 2 4 10 28 2 3 (1) 9 (1) 28 29 34 89 (324) - 260 Productos Equivalentes Terapéuticos al 16/02/2012 7 6 5 18 Productos voluntarios Totales 44 13 55 (476) – 412 18 54 Resolución Principios Activos establecidos Principios Activos Vigentes Productos Farmacéutico s *Res. Ex ISP N° 5555/09, retira de exigencia de bioequivalencia a didanosina y diclofenaco sódico
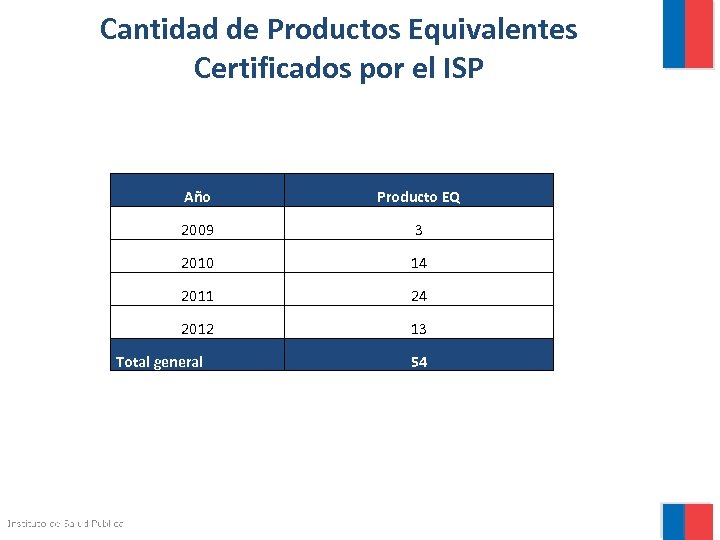
Cantidad de Productos Equivalentes Certificados por el ISP Año Producto EQ 2009 3 2010 14 2011 24 2012 13 Total general 54
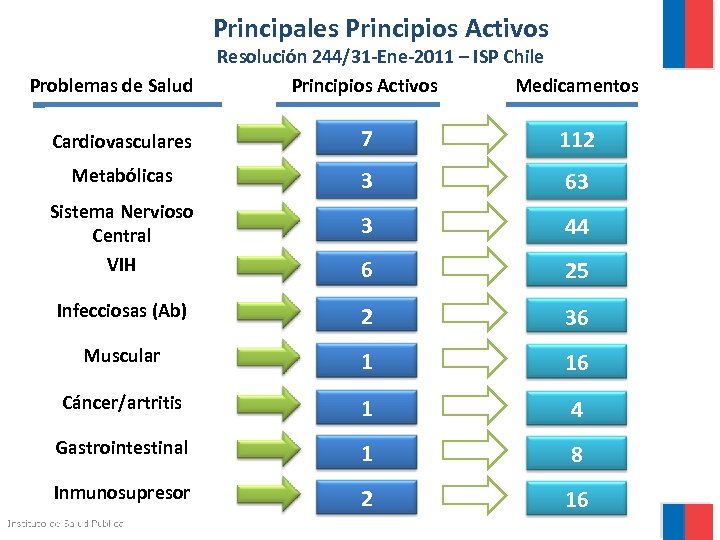
Principales Principios Activos Problemas de Salud Resolución 244/31 -Ene-2011 – ISP Chile Principios Activos Medicamentos Cardiovasculares 7 112 Metabólicas 3 63 3 44 6 25 Infecciosas (Ab) 2 36 Muscular 1 16 Cáncer/artritis 1 4 Gastrointestinal 1 8 Inmunosupresor 2 16 Sistema Nervioso Central VIH
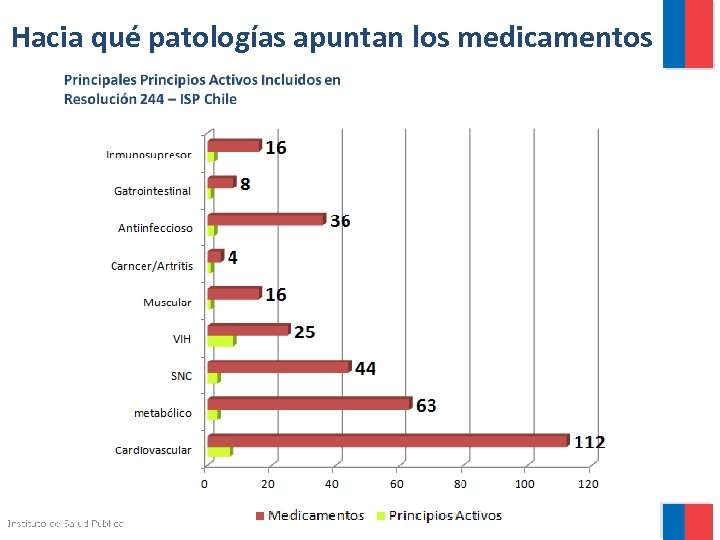
Hacia qué patologías apuntan los medicamentos
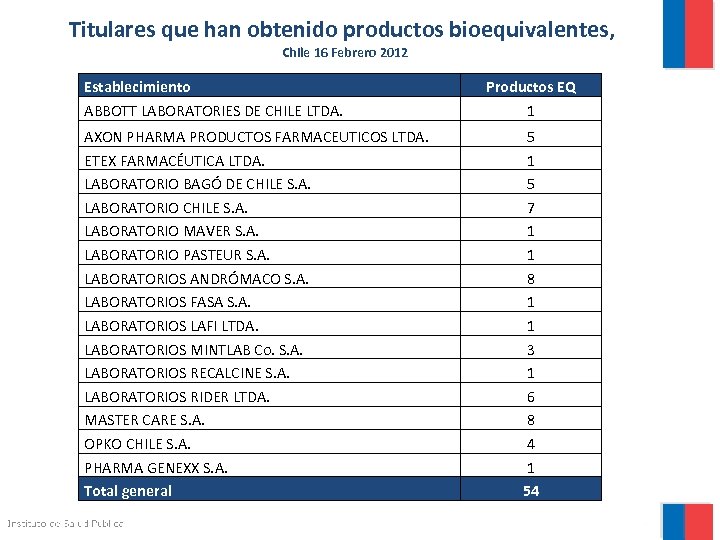
Titulares que han obtenido productos bioequivalentes, Chile 16 Febrero 2012 Establecimiento ABBOTT LABORATORIES DE CHILE LTDA. AXON PHARMA PRODUCTOS FARMACEUTICOS LTDA. ETEX FARMACÉUTICA LTDA. LABORATORIO BAGÓ DE CHILE S. A. LABORATORIO MAVER S. A. LABORATORIO PASTEUR S. A. LABORATORIOS ANDRÓMACO S. A. LABORATORIOS FASA S. A. LABORATORIOS LAFI LTDA. LABORATORIOS MINTLAB Co. S. A. LABORATORIOS RECALCINE S. A. LABORATORIOS RIDER LTDA. MASTER CARE S. A. OPKO CHILE S. A. PHARMA GENEXX S. A. Total general Productos EQ 1 5 7 1 1 8 1 1 3 1 6 8 4 1 54

Proyecciones de Trámites de Bioequivalencia 2012 por Resolución: Resolución Res: 244 Res: 2920 Res: 3225 Res: 728 Sin Exigencia Total general Estado de Tramite – Proyecciones 2012 Resultados Protocolos Aprobados, en Revisión de aprobados espera. protocolos resultados 47 7 64 15 9 2 3 1 1 2 1 6 2 8 62 12 66 28 Total general 133 14 2 3 16 168

Centros de Bioequivalencia certificados por El Instituto de Salud Pública de Chile

Bioequivalencia y su exigencia en las Américas Países Exigencia EE. UU. y Canadá Exige demostrar EQT (in vivo/ in vitro) para el registro de medicamentos no innovadores México y Brasil Normal para el registro de genéricos y de productos similares no intercambiables Otros países • Sin normas para genéricos • Exigencia de bioequivalencia o declaración de intercambiabilidad (in vivo/ in vitro) • Empleo del concepto de país de referencia (registro como similar)

Situación de Países Latinoamericanos (Publicación de Normas de Equivalencia Terapéutica) 1998 1999 Argentina Brasil 2001 C. Rica México 2000 2005 2006 Colombia Chile 2007 Uruguay Venezuela Cuba BOLIVIA, PARAGUAY, PERÚ, ECUADOR, carecen de normas definidas o se encuentran en etapa de propuestas técnicas En países como Argentina, el número de productos EQT en el mercado en la actualidad sólo llega a alrededor de 40 productos farmacéuticos, a pesar de haber publicado normas de bioequivalencia hace más de 10 años.
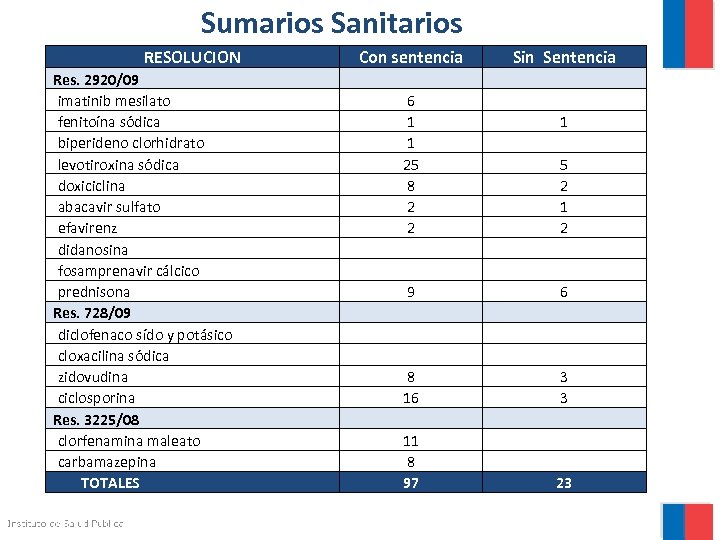
Sumarios Sanitarios RESOLUCION Res. 2920/09 imatinib mesilato fenitoína sódica biperideno clorhidrato levotiroxina sódica doxiciclina abacavir sulfato efavirenz didanosina fosamprenavir cálcico prednisona Res. 728/09 diclofenaco sído y potásico cloxacilina sódica zidovudina ciclosporina Res. 3225/08 clorfenamina maleato carbamazepina TOTALES Con sentencia Sin Sentencia 6 1 1 25 8 2 2 9 8 16 11 8 97 1 5 2 1 2 6 3 3 23
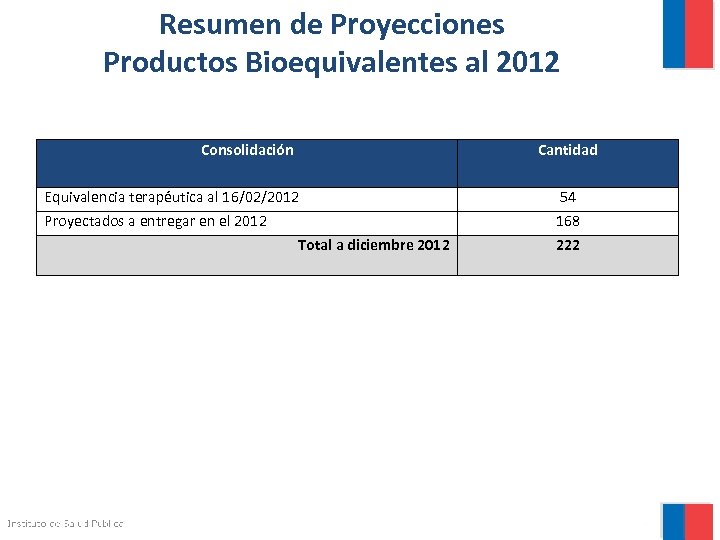
Resumen de Proyecciones Productos Bioequivalentes al 2012 Consolidación Cantidad Equivalencia terapéutica al 16/02/2012 Proyectados a entregar en el 2012 Total a diciembre 2012 54 168 222

Conclusiones ü Chile cumple con la Política de Gobierno: Mayor accesibilidad a medicamentos de calidad a meno precio. ü Los habitantes de Chile podrán acceder a medicamentos con Bioequivalencia comprobada a menor precio. ü Nos posiciona como país en un nivel de desarrollo que nos permite aspirar a relacionarnos con Agencias de nivel mundial. ü Cumplimos con el principio de equidad: toda la población puede acceder a medicamentos de calidad.

“Reconocemos el esfuerzo de la Industria Farmacéutica en colaborar con la Política de Gobierno”.
a52057c528d4bd151a99957902d59de6.ppt