л10 биоэнергетика 2.ppt
- Количество слайдов: 42

Биоэнергетика изучает механизмы преобразования энергии в клетке

1. Пути преобразования энергии в клетке Энергетические превращения, протекающие в живой клетке, можно разделить на 2 группы: 1) процессы, локализованные в мембранах – источником энергии служат H+ или a+; 2) процессы, протекающие в немембранных отделах протоплазмы – источником энергии служит энергия химических связей АТФ или других высокоэнергетических веществ. Мембраны, способные превращать называются энергопреобразующими. одну форму энергии в другую, Преобразование энергии в таких мембранах осуществляется встроенными в них белковыми комплексами.

Пути преобразования энергии в клетке В подавляющем большинстве случаев биомембранах описывается схемой: преобразование энергии в АТФ - трансмембранная разность электрохимического потенциала иона Согласно данной схеме, внешняя энергия, потребляемая мембраной (свет или энергия субстратов дыхания), используется сначала на транспорт ионов через мембрану против сил электрического поля и в направлении большей концентрации иона (т. е. против градиента электрохимического потенциала). Этот процесс называется энергизация мембраны. Далее энергия, накопленная в виде градиента электрохимического потенциала иона, используется в качестве движущей силы для совершения работы, либо обратимо превращается в энергию АТФ.

Пути преобразования энергии в клетке Биоэнергетическая классификация мембран

Пути преобразования энергии в клетке Биоэнергетическая классификация мембран

Пути преобразования энергии в клетке Биоэнергетическая классификация мембран
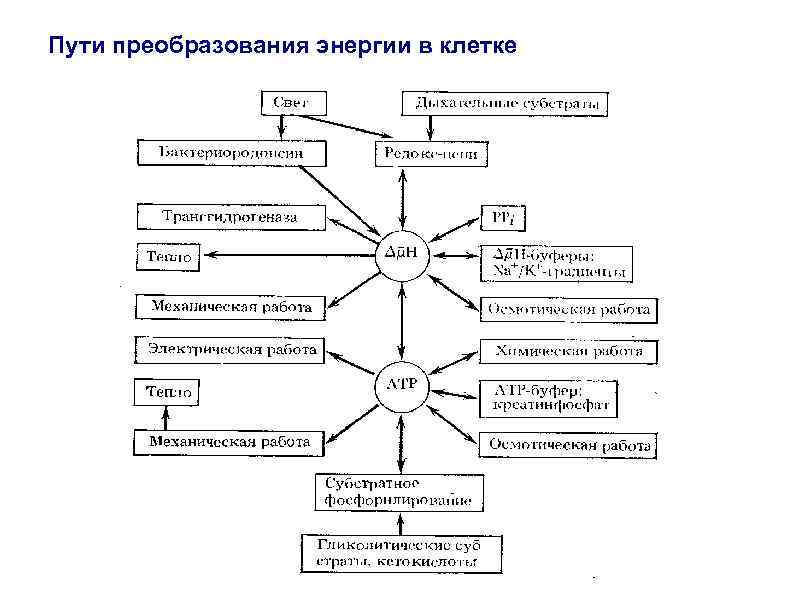
Пути преобразования энергии в клетке
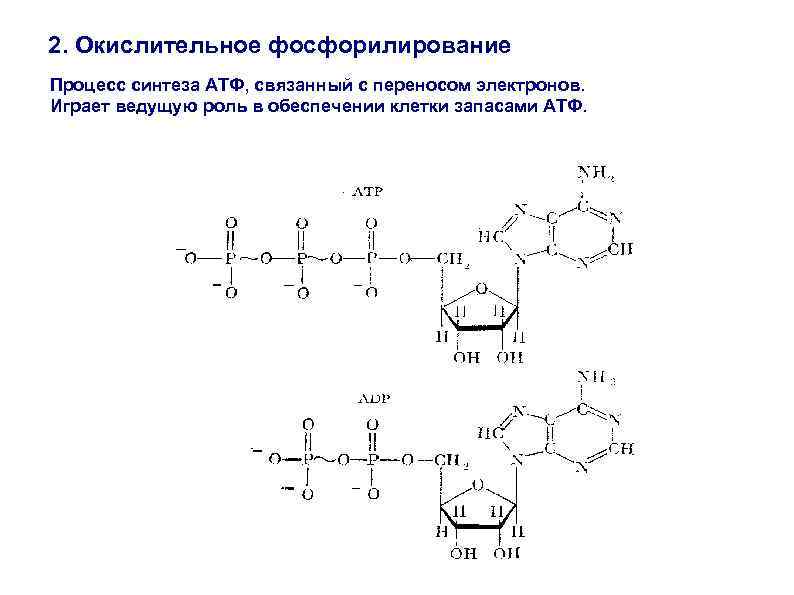
2. Окислительное фосфорилирование Процесс синтеза АТФ, связанный с переносом электронов. Играет ведущую роль в обеспечении клетки запасами АТФ.

Окислительное фосфорилирование 1930 -1932 гг. - В. А. Энгельгардт открыл окислительное фосфорилирование. Обнаружил синтез АТФ, сопряженный с внутриклеточным дыханием. 1939 г. - В. А. Бельцер показал, что синтез АТФ происходит при переносе электронов в дыхательной цепи. 1949 г. - А. Ленинджер установил, что окислительное фосфорилирование происходит в митохондриях. 1961 г. - П. Митчел разработал хемиосмотическую теорию, согласно которой транспорт электронов в дыхательной цепи и синтез АТФ связаны через трансмембранный перенос протонов. 1976 г. - П. Митчел получил Нобелевскую премию. 1975 г. - В. П. Скулачев экспериментально подтвердил хемиосмотическую теорию П. Митчела

2. 1 Дыхательная электрон-транспортная цепь

2. 1 Дыхательная электрон-транспортная цепь В матриксе митохондрий содержатся: - ферменты цикла Кребса; - ферменты окисления жирных кислот; - аденилаткиназа АМФ-АДФ-АТФ; - геном митохондрий, молекулы РНК; - рибосомы. Внешняя мембрана митохондрий содержит: - порины (обеспечивают проницаемость внешней мембраны митохондрий для веществ с молекулярной массой до 10 к. Да); - АТФ-зависимую ацетил-Ко. А-синтетазу; - НАДН-дегидрогеназу. Во внутренней мембране митохондрий находятся: - переносчики электронов, формирующие дыхательную электрон-транспортную цепь; - Н+-АТФ-синтетаза; - АТФ-АДФ-транслоказа; - переносчики Н 2 РО 4 - - ОН-; - Са 2+-каналы
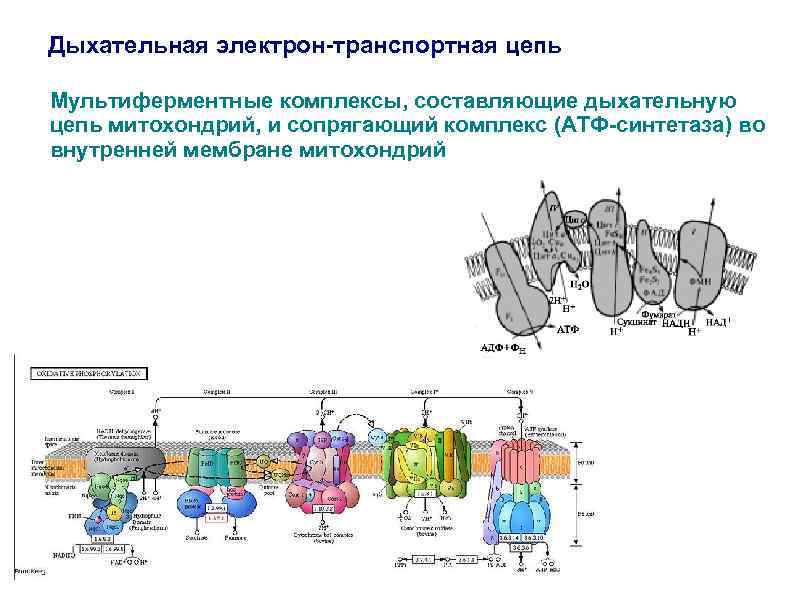
Дыхательная электрон-транспортная цепь Мультиферментные комплексы, составляющие дыхательную цепь митохондрий, и сопрягающий комплекс (АТФ-синтетаза) во внутренней мембране митохондрий
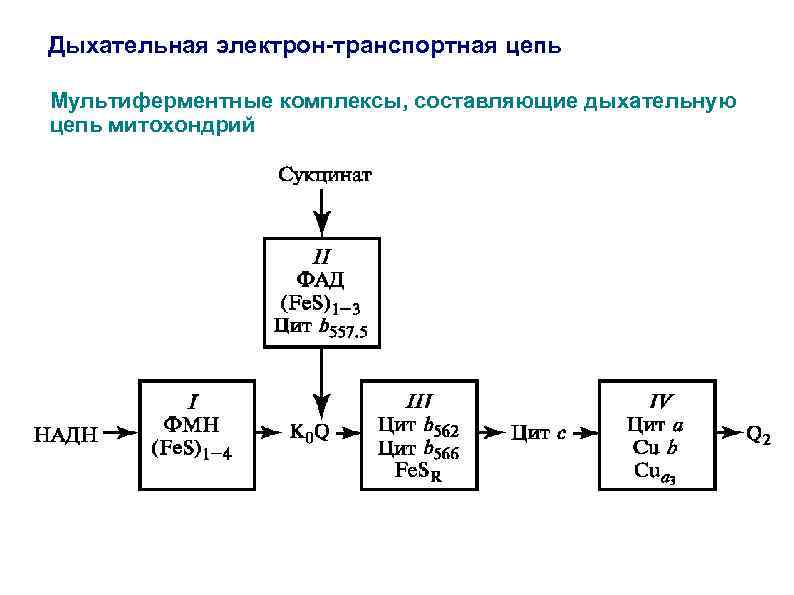
Дыхательная электрон-транспортная цепь Мультиферментные комплексы, составляющие дыхательную цепь митохондрий
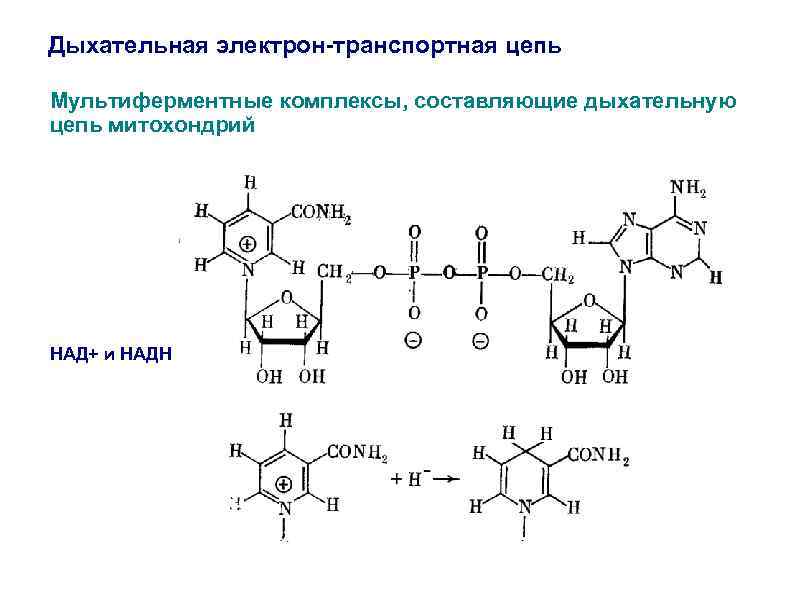
Дыхательная электрон-транспортная цепь Мультиферментные комплексы, составляющие дыхательную цепь митохондрий НАД+ и НАДН
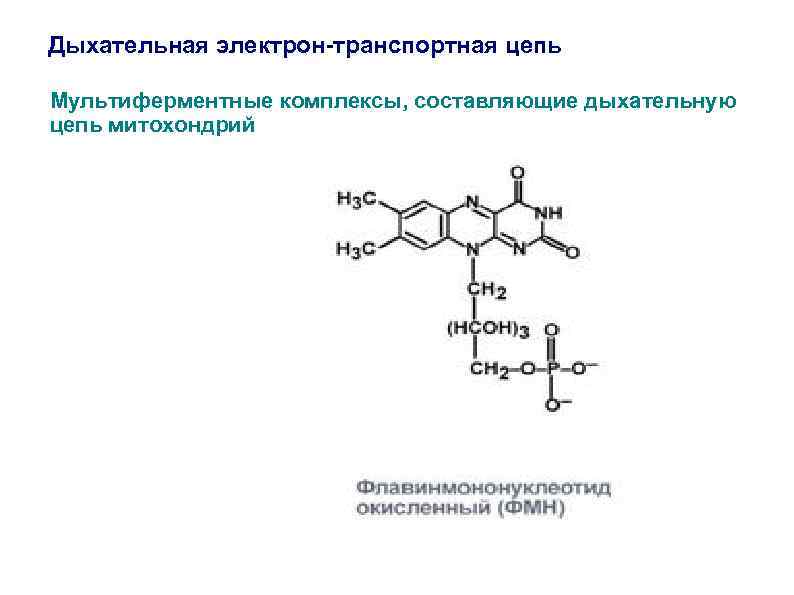
Дыхательная электрон-транспортная цепь Мультиферментные комплексы, составляющие дыхательную цепь митохондрий
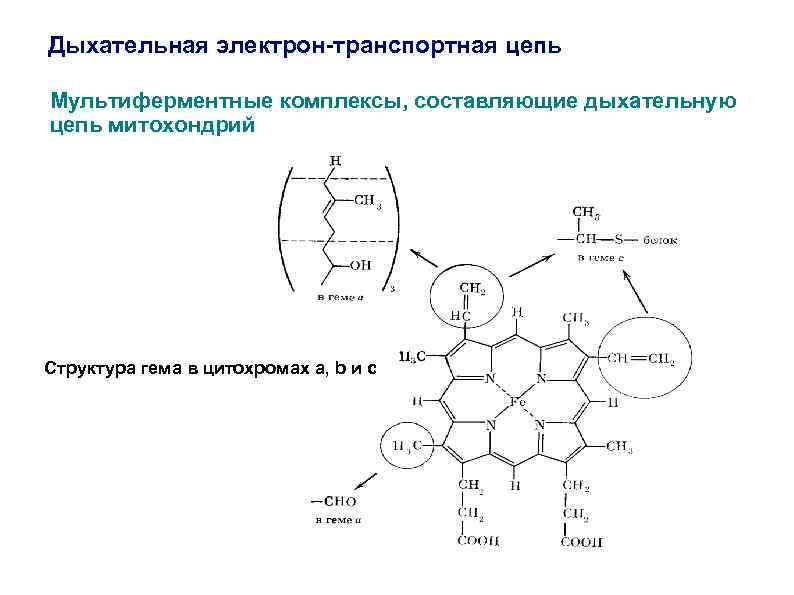
Дыхательная электрон-транспортная цепь Мультиферментные комплексы, составляющие дыхательную цепь митохондрий Структура гема в цитохромах a, b и c
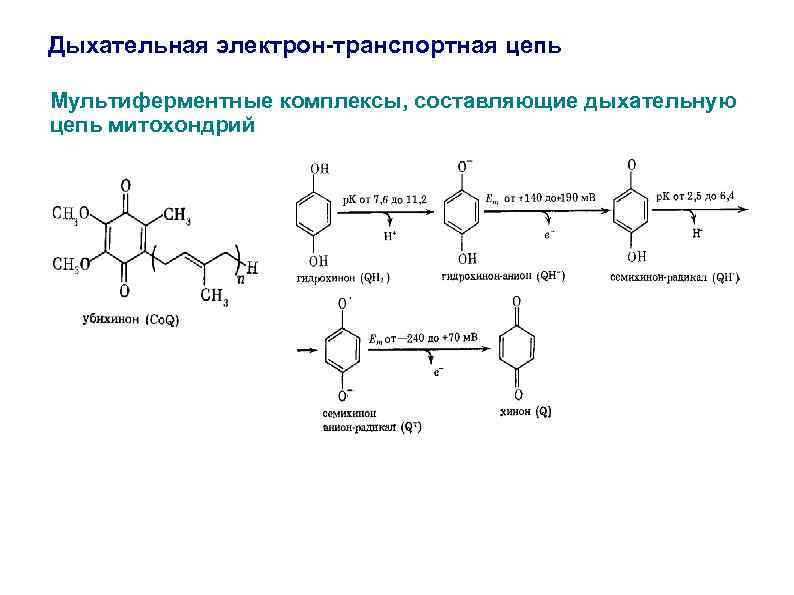
Дыхательная электрон-транспортная цепь Мультиферментные комплексы, составляющие дыхательную цепь митохондрий
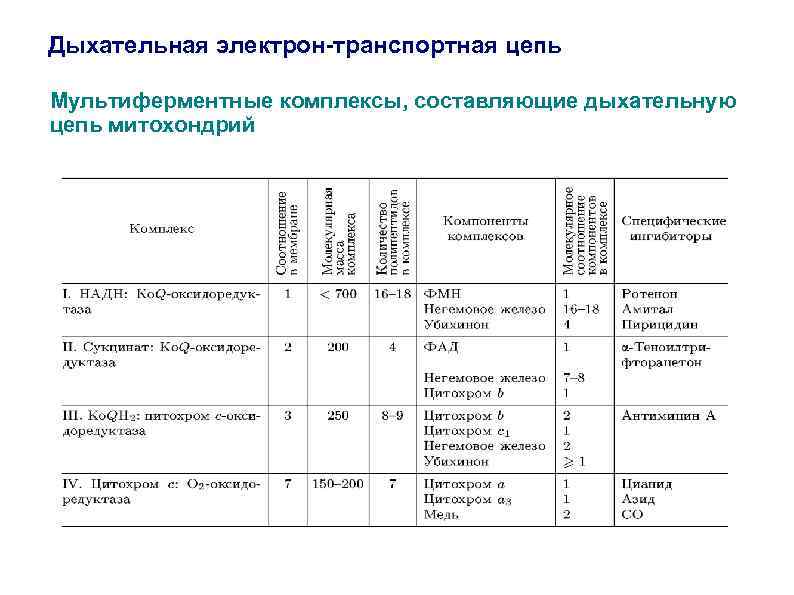
Дыхательная электрон-транспортная цепь Мультиферментные комплексы, составляющие дыхательную цепь митохондрий

2. 2 Перенос электронов в мембранах митохондрий Механизмы сопряжения транспорта электронов и синтеза АТФ
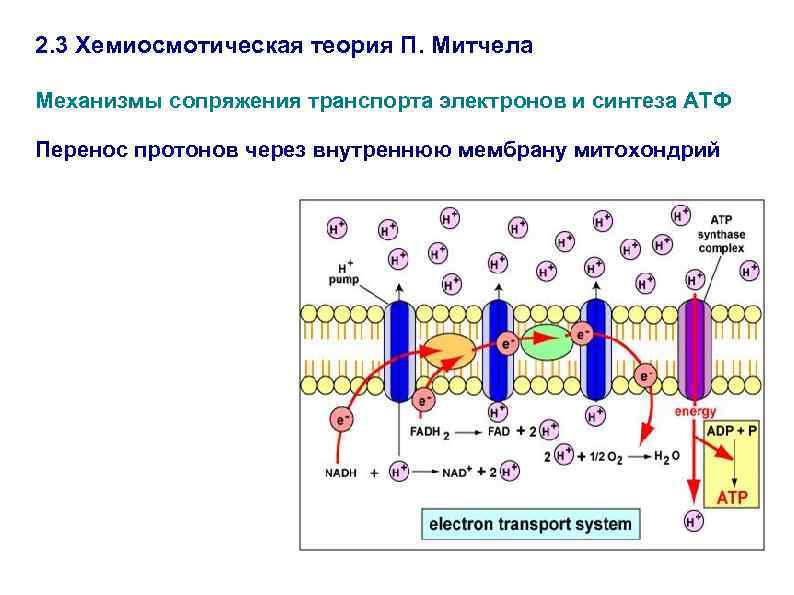
2. 3 Хемиосмотическая теория П. Митчела Механизмы сопряжения транспорта электронов и синтеза АТФ Перенос протонов через внутреннюю мембрану митохондрий
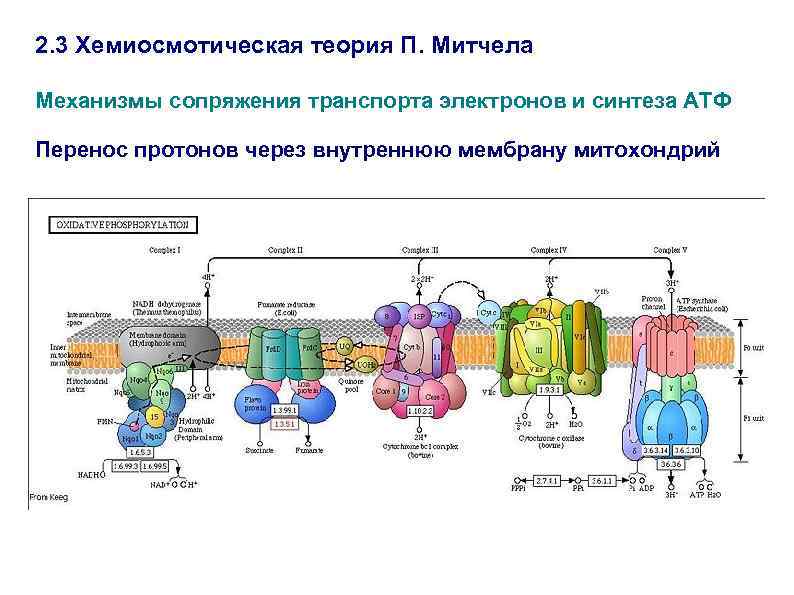
2. 3 Хемиосмотическая теория П. Митчела Механизмы сопряжения транспорта электронов и синтеза АТФ Перенос протонов через внутреннюю мембрану митохондрий
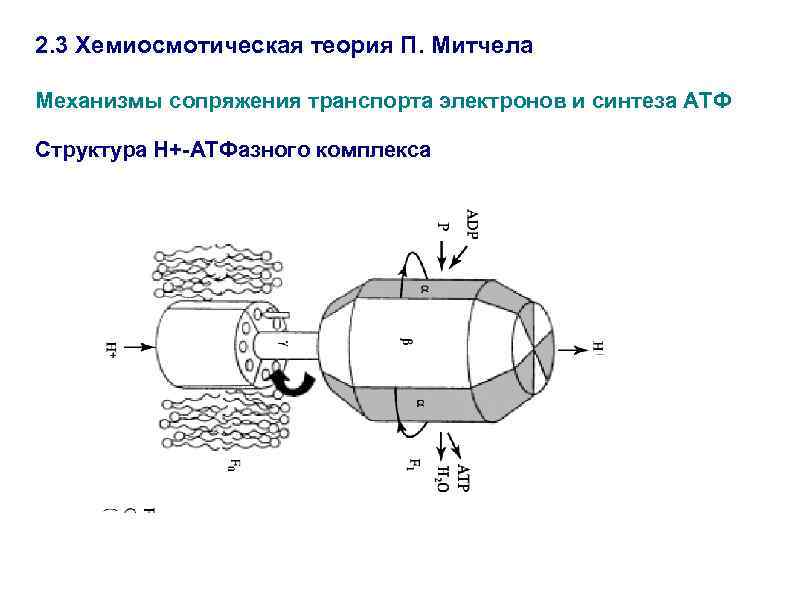
2. 3 Хемиосмотическая теория П. Митчела Механизмы сопряжения транспорта электронов и синтеза АТФ Структура Н+-АТФазного комплекса
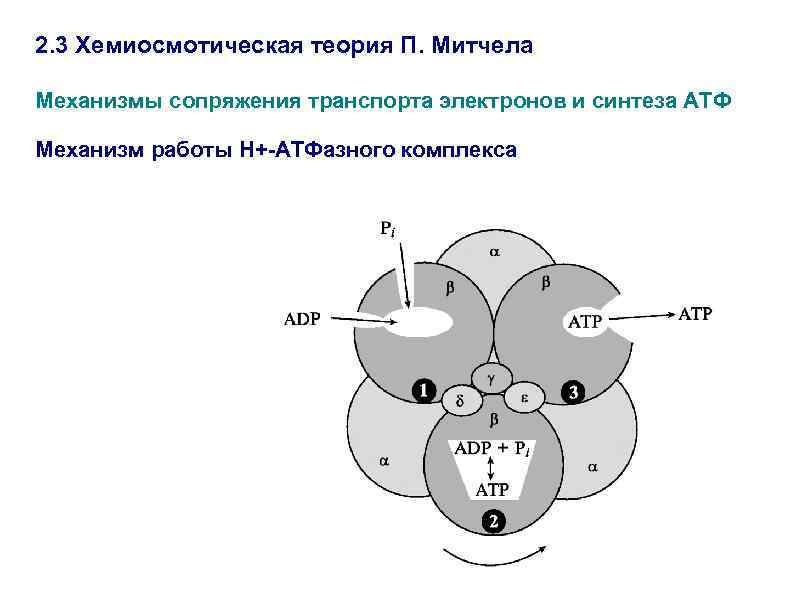
2. 3 Хемиосмотическая теория П. Митчела Механизмы сопряжения транспорта электронов и синтеза АТФ Механизм работы Н+-АТФазного комплекса
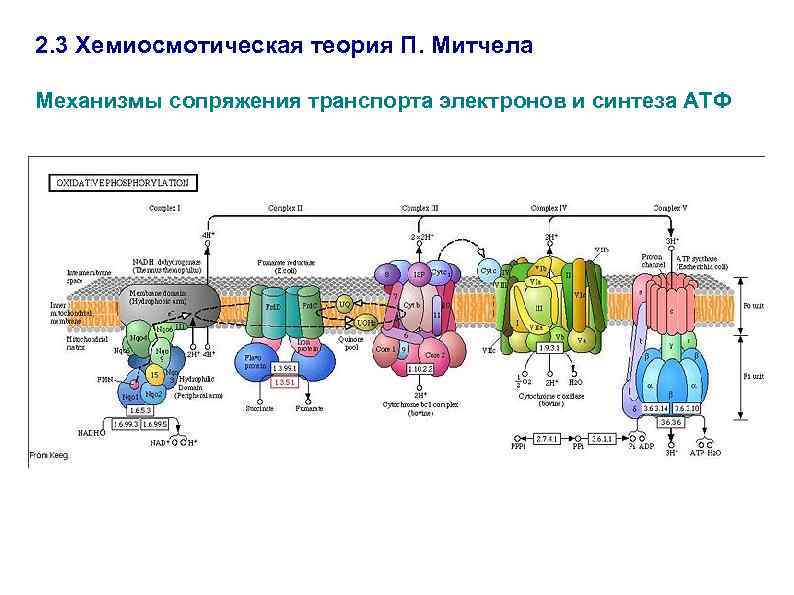
2. 3 Хемиосмотическая теория П. Митчела Механизмы сопряжения транспорта электронов и синтеза АТФ

3. Роль молекулярного кислорода в дыхании и метаболизме клетки Кислород снимает электроны с переносчиков дыхательной электрон-транспортной цепи, обеспечивая - поток электронов по дыхательной электрон-транспортной цепи; - перенос ионов Н+ через внутреннюю мембрану митохондрий из матрикса в межмембранной пространство; - создание и поддержание H+ и ; - синтез АТФ

3. Роль молекулярного кислорода в дыхании и метаболизме клетки Последовательность событий при тканевой гипоксии При недостатке и отсутствии кислорода нет транспорта электронов по дыхательной цепи нет переноса ионов Н+ через внутреннюю мембрану митохондий 0 -5 минут прекращается синтез АТФ, концентрация АТФ в клетке снижается перестают работать ионные насосы на внешней (цитоплазматической) мембране клеток нарушение распределения ионов между клеткой и окружающей средой поступление воды в клетку отек клеток и тканей не поддерживается на внутренней мембране митохондрий и на внешней цитоплазматической мембране клеток 5 -15 минут поступление кальция (Ca 2+) в цитоплазму клеток и матрикс митохондрий активация фосфолипаз 15 -30 минут формирование пор в мембране гибель клетки 90 -120 минут

4. Перекисное окисление липидов наблюдается при нормальном функционировании мембран, сильно возрастает при патологических состояниях организма. Б. Н. Тарусов исследовал повреждающее действие на клетку цепного свободнорадикального окисления липидов. Процесс начинается с образования свободных радикалов за счет разрыва в углеводородных остатках жирных кислот липидов связей С-Н или С-С. Разрыв связей легче протекает в углеводородных остатках, содержащих ненасыщенные двойные связи. Наименьшей энергией разрыва обладает связь С-Н, находящаяся рядом с двойной связью в -положении.

4. Перекисное окисление липидов Радикал взаимодействует с кислородом, образуя перекисный радикал L + O 2 LOO Далее перекисный радикал взаимодействует молекулой фосфолипида LH, формируя перекись с другой LOO + LH LOOH + L Реакции, в ходе которых исходный углеводородный радикал L регенерируется вновь из другой молекулы фосфолипида, называются цепными. Число циклов, которое успевает совершить радикал до момента исчезновения, определяет длину цепи реакции.

4. Перекисное окисление липидов OH + LH HOH + L (1) L + O 2 LOO (2) LOO + LH LOOH + L (3) зарождение цепи продолжение цепи LOOH + Fe 2+ Fe 3+ + LO + OH LO + LH LOH + L (6) L + LOOL (7) L + In. H LH + In (8) разветвление цепи (5) L + L LL (4) обрыв цепи LOO + In. H LOOH + In (9) In + In In-In (10) защита
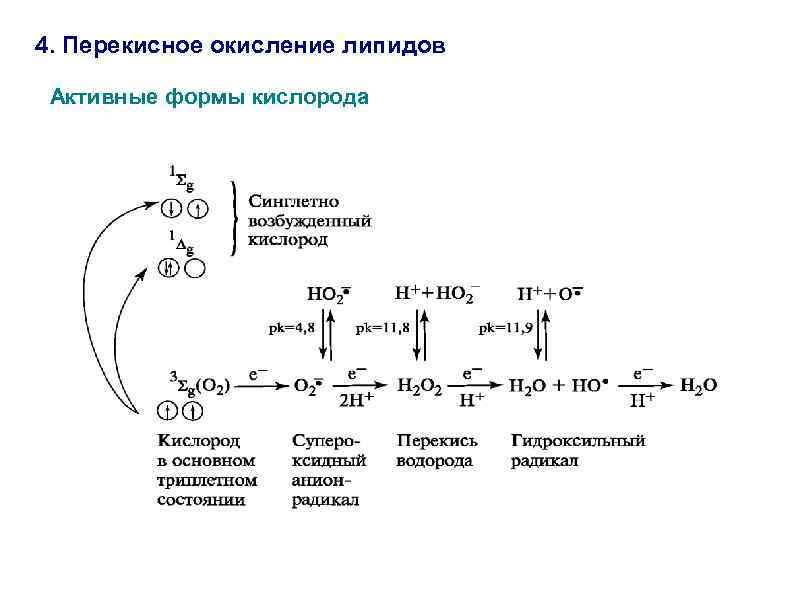
4. Перекисное окисление липидов Активные формы кислорода
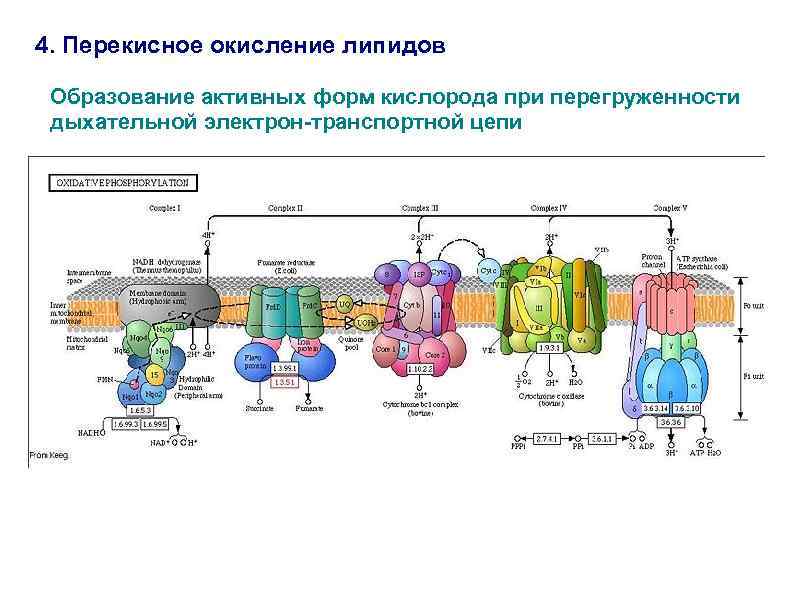
4. Перекисное окисление липидов Образование активных форм кислорода при перегруженности дыхательной электрон-транспортной цепи

4. Перекисное окисление липидов Активные формы кислорода
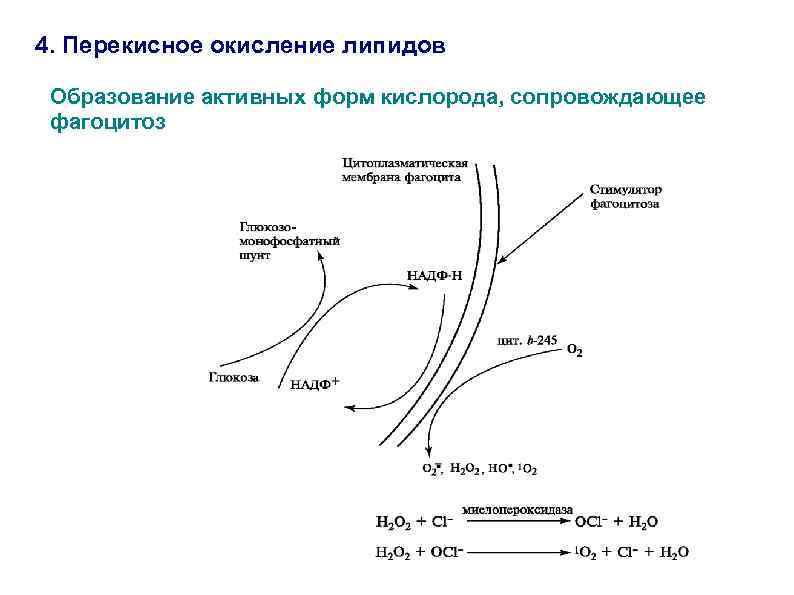
4. Перекисное окисление липидов Образование активных форм кислорода, сопровождающее фагоцитоз

4. Перекисное окисление липидов Образование активных форм кислорода Активные формы кислорода появляются в клетках как побочный продукт ряда биохимических реакций, а также в связи с целенаправленной активацией кислорода в целях защиты от инфекций, удаления ксенобиотиков, самоликвидации поврежденных клеток. Активные формы кислорода обладают мощным токсичным и бактерицидным действием. Главной мишенью их действия являются полиненасыщенные липиды мембран.

4. Перекисное окисление липидов Защита от токсичного действия активных форм кислорода Живые организмы адаптированы к обитанию в аэробных условиях. Они защищены от токсичного и повреждающего действия активных форм кислорода 1) ферментами – каталазы, пероксидазы, глутатионпероксидаза. 2) антиоксидантами – веществами, защищающими биологические системы от окисления за счет взаимодействия со свободными радикалами. Наиболее типичными антиоксидантами являютя соединения фенольного типа (токоферолы – витамин Е) 3) тушители синглетного кислорода – витамин Е, аскорбиновая кислота (витамин С), каротины.

4. Перекисное окисление липидов OH + LH HOH + L (1) L + O 2 LOO (2) LOO + LH LOOH + L (3) зарождение цепи продолжение цепи LOOH + Fe 2+ Fe 3+ + LO + OH LO + LH LOH + L (6) L + LOOL (7) L + In. H LH + In (8) разветвление цепи (5) L + L LL (4) обрыв цепи LOO + In. H LOOH + In (9) In + In In-In (10) защита
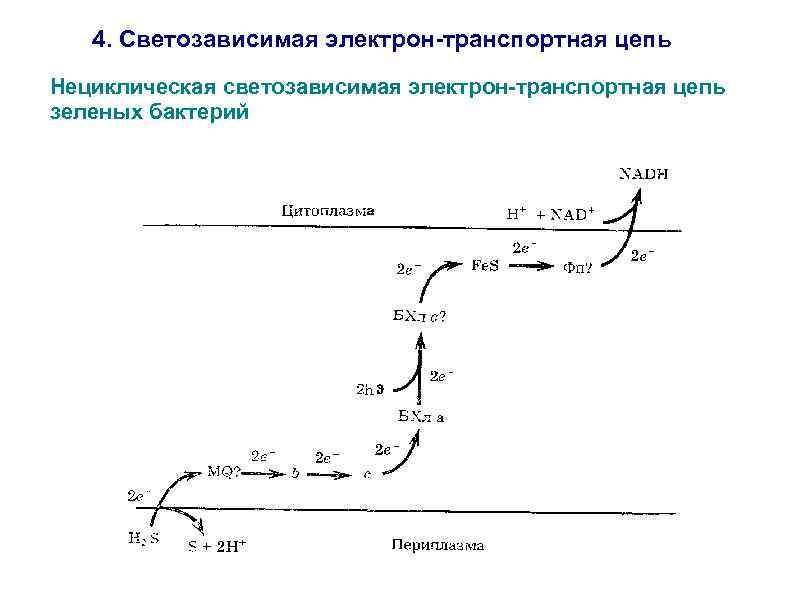
4. Светозависимая электрон-транспортная цепь Нециклическая светозависимая электрон-транспортная цепь зеленых бактерий
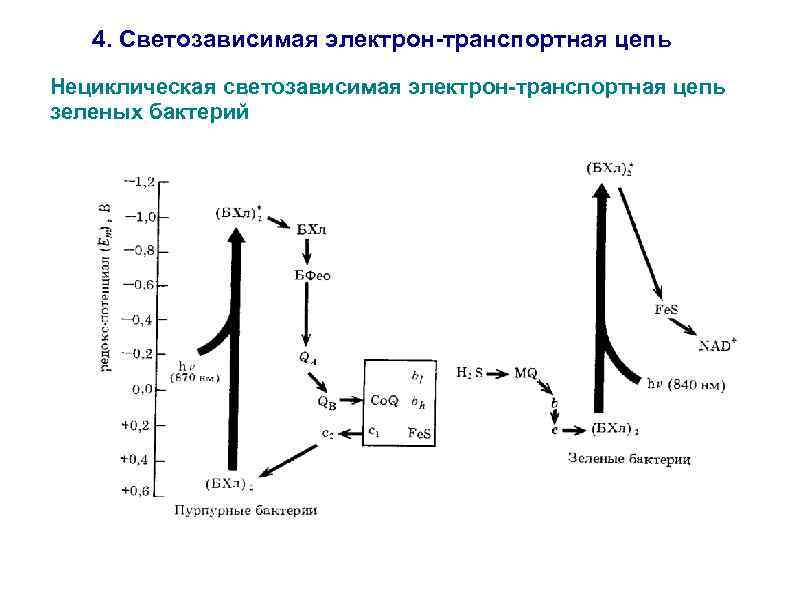
4. Светозависимая электрон-транспортная цепь Нециклическая светозависимая электрон-транспортная цепь зеленых бактерий

4. Светозависимая электрон-транспортная цепь Циклическая светозависимая электрон-транспортная цепь пурпурных бактерий
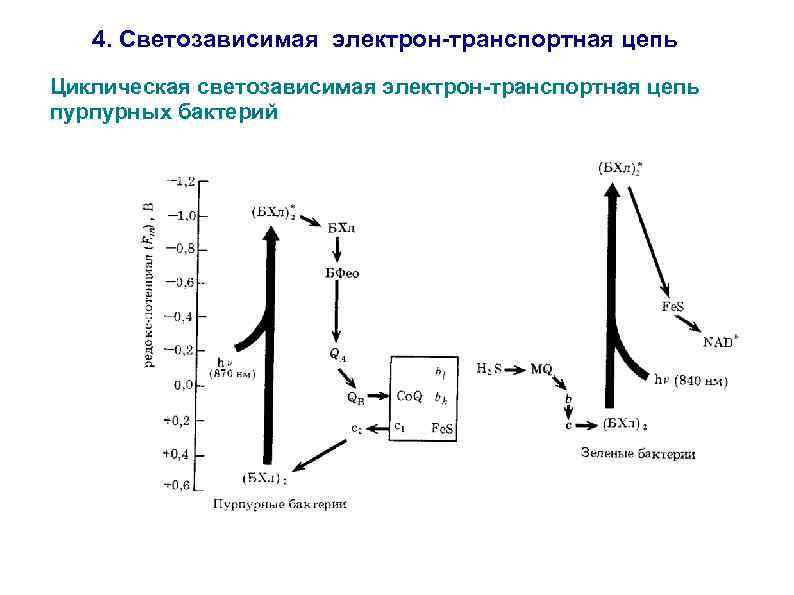
4. Светозависимая электрон-транспортная цепь Циклическая светозависимая электрон-транспортная цепь пурпурных бактерий
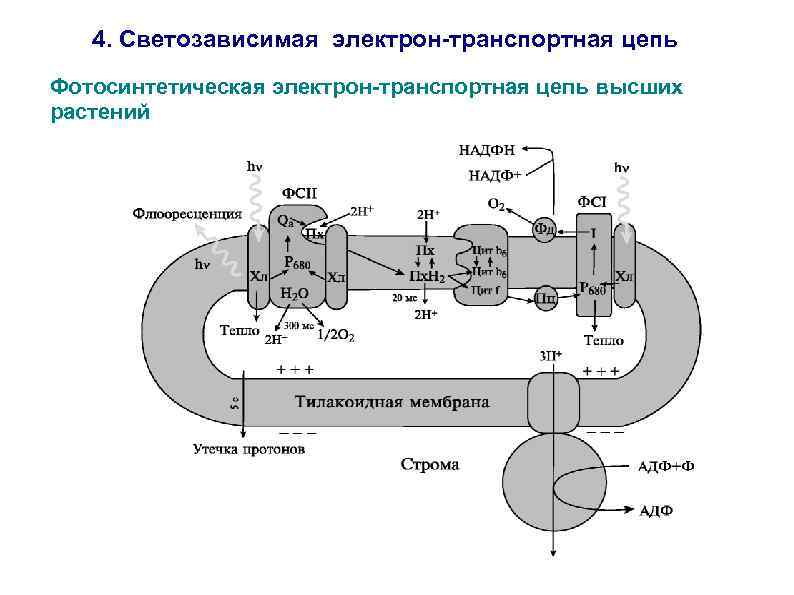
4. Светозависимая электрон-транспортная цепь Фотосинтетическая электрон-транспортная цепь высших растений
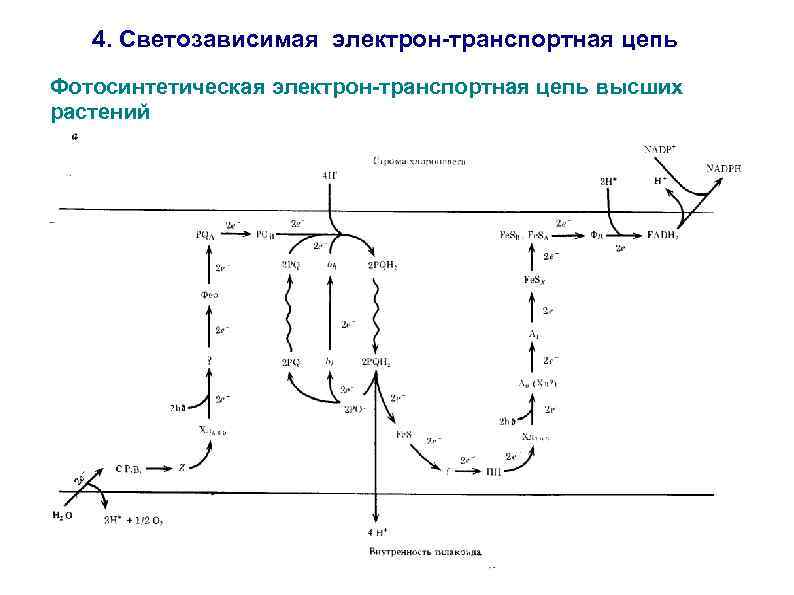
4. Светозависимая электрон-транспортная цепь Фотосинтетическая электрон-транспортная цепь высших растений
л10 биоэнергетика 2.ppt