Биоэнергетика стомат 1 лекц.ppt
- Количество слайдов: 83

Биоэнергетика Е. В. Бондаренко

Обмен веществ включает 3 этапа: n поступление веществ в организм, n метаболизм, n выделение конечных продуктов из организма.

Метаболизм. Катаболизм. Анаболизм. Метаболизм — совокупность химических реакций, происходящих в организме. n Метаболический путь — последовательность реакций, приводящих к образованию определенного продукта. n Соединения, образующиеся в ходе превращений — метаболиты. n В метаболизме можно выделить пути катаболизма, ведущие к расщеплению сложных молекул и пути анаболизма, предназначенные для биосинтезов. n
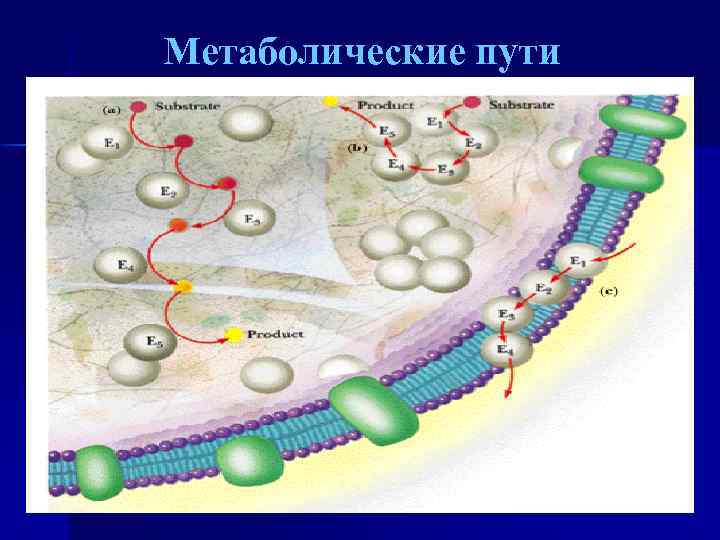
Метаболические пути

Эндергонические и экзергонические реакции n В результате катаболизма образуются конечные продукты обмена — СО 2, Н 2 О и мочевина. Реакции катаболизма сопровождаются выделением энергии – - экзергонические реакции. n n n Анаболизм объединяет биосинтетические процессы, в которых простые строительные блоки соединяются в сложные макромолекулы. Анаболические реакции - эндергонические реакции, используют энергию, освобождающуюся при катаболизме. Катаболические и анаболические пути во многом различаются, но в тоже время они тесно связаны друг с другом. Катаболизм и анаболизм — это сопряженные взаимодополняющие процессы.
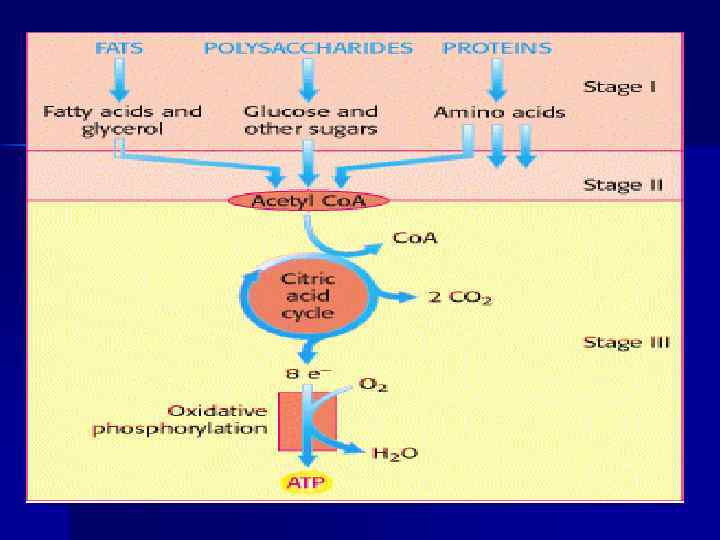
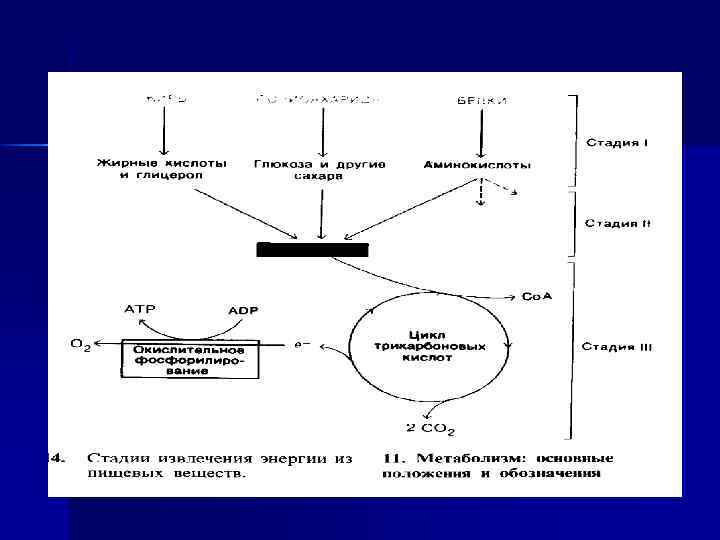

Эндергонические и экзергонические реакции n Каждое органическое вещество, входящее в состав живой материи, обладает определенным запасом внутренней энергии Е. Часть этой внутренней энергии может быть использована для совершения полезной работы, это свободная энергия — G.

Эндергонические и экзергонические реакции n Направление химической реакции определяется значением G. Если G - , то реакция протекает самопроизвольно и сопровождается уменьшением G. n Реакции, сопровождающиеся уменьшением G — экзергонические. n Если G +, то реакция будет протекать только при поступлении свободной энергии извне, такие реакции называют эндергоническими.

Сопряжение эндергонических и экзергонических процессов В биологических системах термодинамически невыгодные (эндергонические) реакции могут протекать лишь за счет энергии экзергонических реакций. Процессы, протекающие с потреблением и выделением энергии, связаны между собой. Эти реакции происходят при участии АТФ, АТФ — сопрягающий фактор, форма запасания энергии.
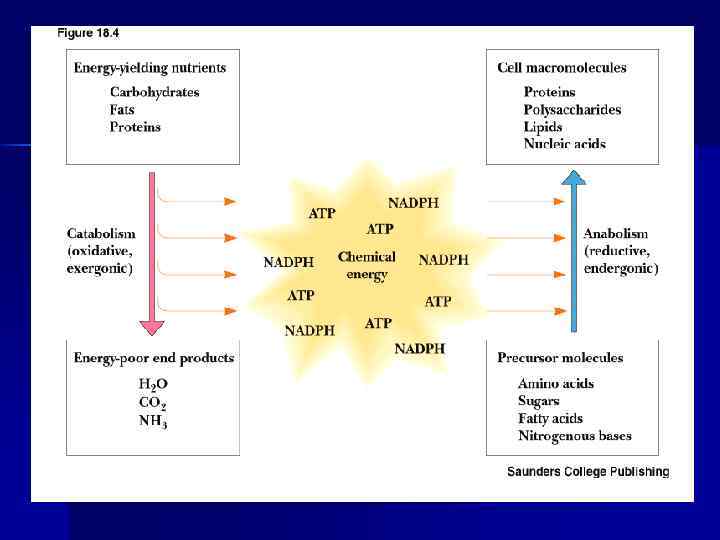

Роль АТФ в клеточной энергетике Химическая энергия, освобождаемая в процессе катаболизма, запасается путем фосфорилирования АДФ с образованием АТФ; n энергия АТФ затем используется после расщепления химических связей АТФ в ходе эндергонических реакций (процессы биосинтеза, активный транспорт, сокращение мышц и т. д. ) n Основные источники энергии: углеводы, жиры, белки. n
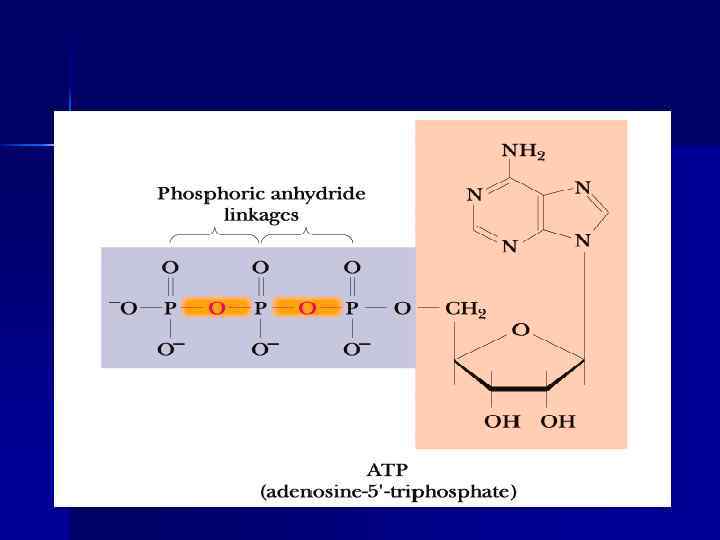
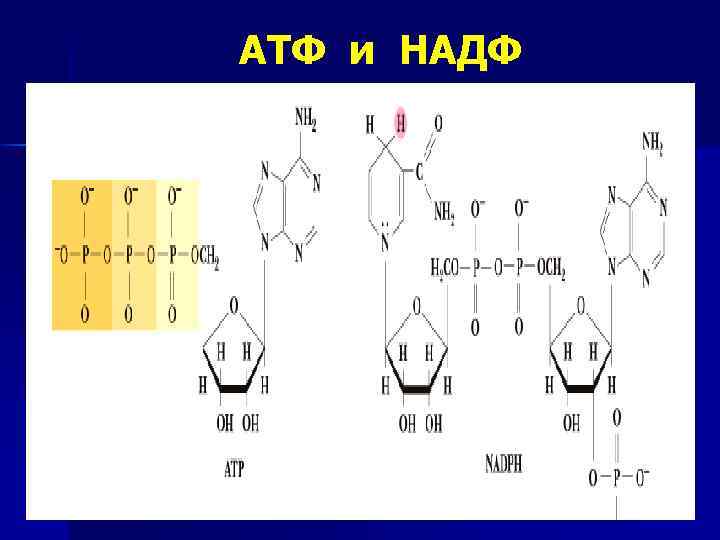
АТФ и НАДФ
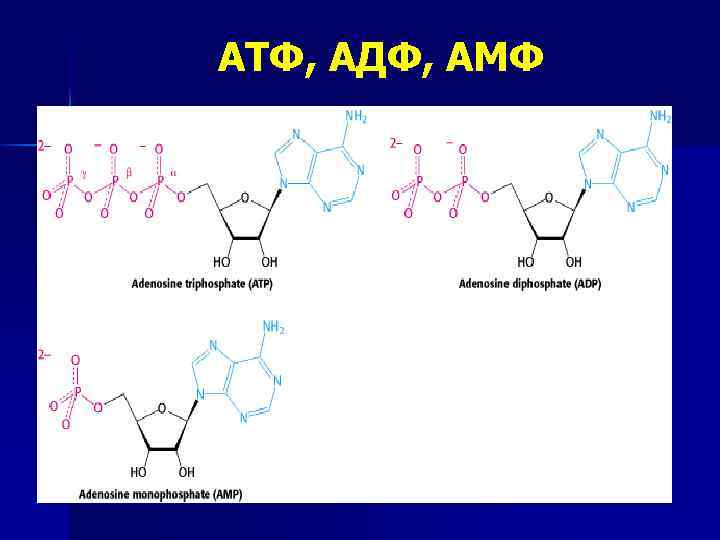
АТФ, АДФ, АМФ
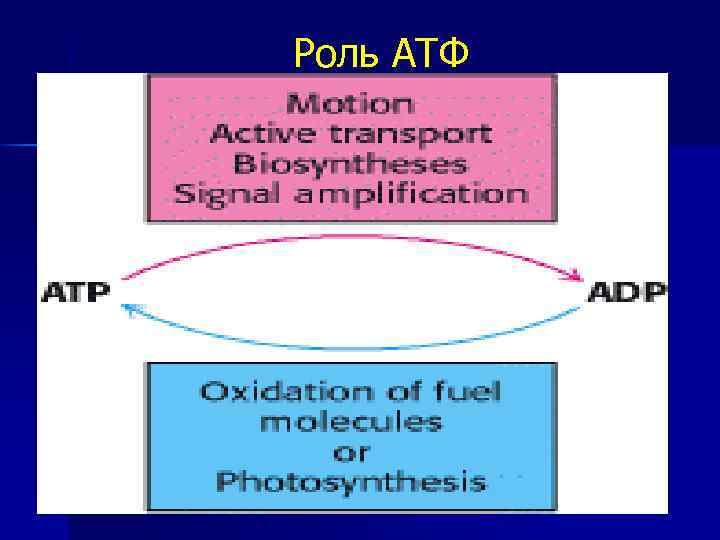
Роль АТФ

n Макроэргические соединения Если энергия, освобождающаяся при гидролизе веществ, превышает 30 к. Дж/моль (7, 3 ккал/моль), то гидролизуемая связь – высокоэнергетическая, n (макроэргическая, ~ ). Макроэргические соединения — вещества, содержащие в своем составе высокоэнергетические (макроэргические ) связи, при гидролизе которых высвобождается более 30 к. Дж энергии на 1 моль связей.

Макроэргические соединения n n n n n К ним относят: нуклеозидтрифосфаты (АТФ, ГТФ, УТФ, ЦТФ), нуклеозиддифосфаты, фосфоэнолпируват, 1, 3 дифосфоглицерат, карбамоилфосфат, сукцинил-Ко. А, ацетил-Ко. А, креатинфосфат, пирофосфат

Виды фосфорилирования как реакции образования АТФ: окислительное, субстратное, фотофосфорилирование АДФ + Фн АТФ + Н 2 О Окислительное фосфорилирование — главный путь синтеза АТФ из АДФ и Рнеорг. n n n Реакция энергетически сопряжена с переносом Н с восстановленных коферментов на О 2. При этом освобождается основная часть энергии окисляемых веществ. Энергия образуется в ходе окислительновосстановительных реакций и на промежуточном этапе запасается в виде электрохимического потенциала. Энергетическое сопряжение реакций переноса Н (е- и Н+) и синтеза АТФ происходит при участии МТХ мембраны и Н+-АТФ-синтетазы.

Субстратное фосфорилирование n n — энергия, необходимая для образования АТФ (ГТФ) высвобождается при гидролизе связей других макроэргических соединений. Синтез АТФ происходит за счет энергии макроэргических связей S. Механизм сопряжения не требует участие мембраны.

Субстратное фосфорилирование, фотофосфорилирование Гликолиз: ФЭП +АДФ АТФ + ПВК; 1, 3 дифосфогицерат + АДФ АТФ + 3 -фосфоглицерат; ЦТК: сукцинил-Ко. А сукцинат. Мышцы: n креатинфосфат + АДФ креатин + АТФ фотофосфорилирование — для синтеза АТФ используется энергия электромагнитного излучения (видимого света), которая запасается в виде электрохимического потенциала (у зеленых растений).
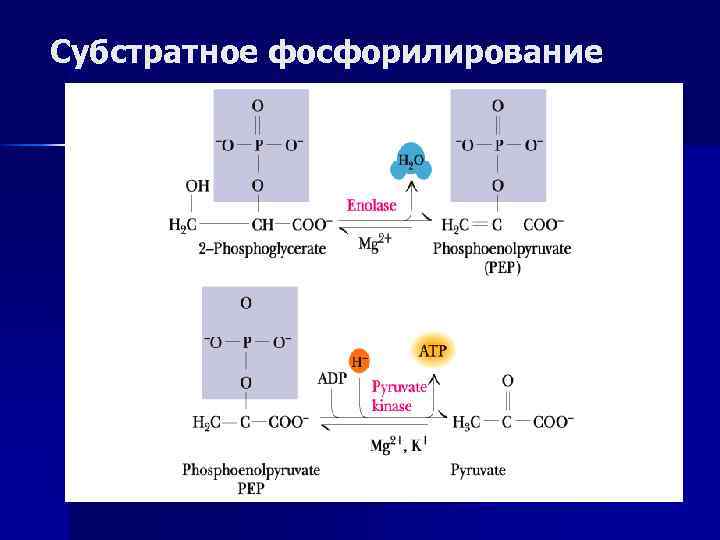
Субстратное фосфорилирование

Тканевое дыхание. Дыхательная цепь n Окисление орг. веществ в клетках, сопровождающееся потреблением О 2, образованием Н 2 О и освобождением энергии— тканевое дыхание. n Тканевое дыхание включает: а) отнятие Н (е- и Н+) от S (дегидрирование); б) многоэтапный процесс переноса е- на О 2. n Тканевое дыхание и синтез АТФ энергетически сопряжены.

Тканевое дыхание. Дыхательная цепь n О 2 в процессе биоокисления используется как акцептор Н окисляемых (дегидрирумых) S, в результате чего синтезируется Н 2 О (400 мл в сутки) -2 Н+ SH 2 + ½ О 2 S + Н 2 О+220 к. Дж/моль. -2 е

Тканевое дыхание. Дыхательная цепь n Энергия, освобождающаяся в ходе реакции окисления, либо рассеивается в виде тепла, либо частично (40%) тратится на фосфорилирование AДФ с образованием АТФ. Реакции дегидрирования и способ превращения выделившейся энергии путем синтеза АТФ— это энергетически сопряженные реакции. Целиком весь сопряженный процесс называется окислительным фосфорилированием.

Дыхательная цепь n Дыхательная цепь (ЦПЭ) — путь переноса Н+ и е- от органических веществ на О 2 воздуха. Это система переносчиков, структурно закрепленная на мембране МТХ и расположенная в соответствии со своими редокспотенциалами. n Последовательность расположения компонентов дыхательной цепи определяется окислит. -восстановит. потенциалами их окисленных и восстановленных форм.
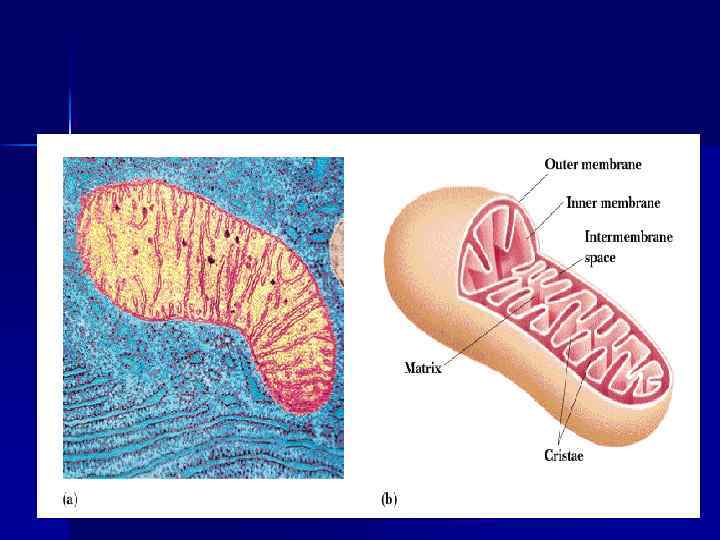
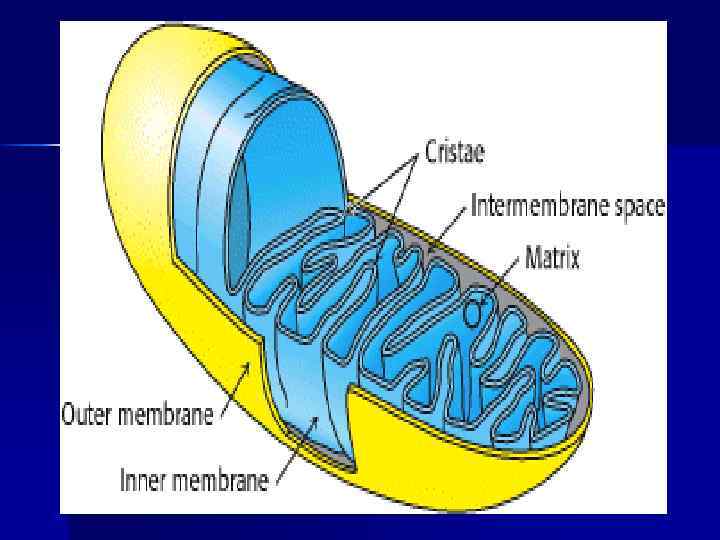
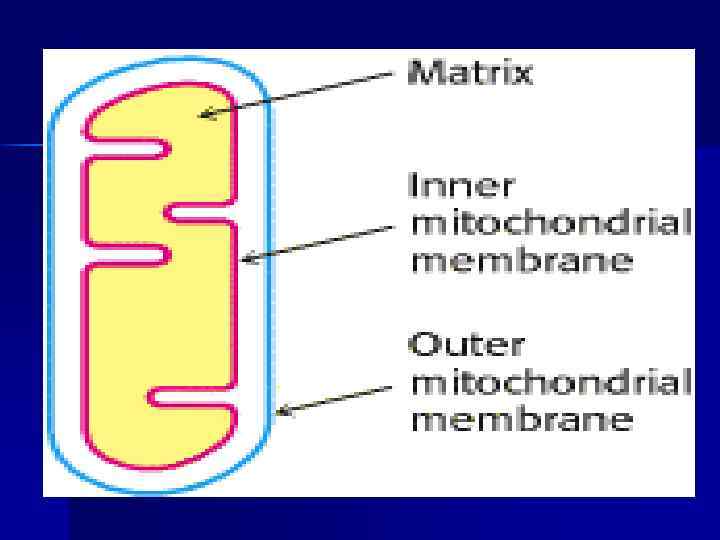

Строение дыхательной цепи n Четыре белковых комплекса расположены во внутренней митохондриальной мембране. n n Жирорастворимый кофермент коэнзим Q и водорастворимый цитохром C перемещаются между белковыми комплексами. Перемещение электронов в дыхательной цепи происходит по градиенту окислитвосстановит. потенциала.
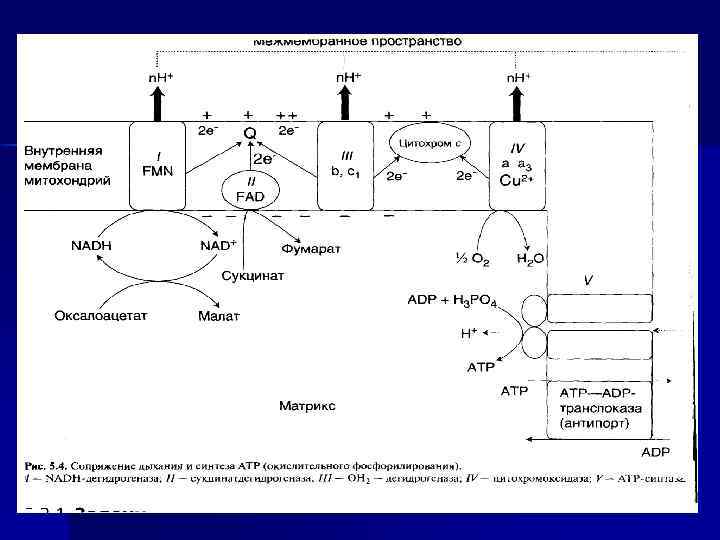
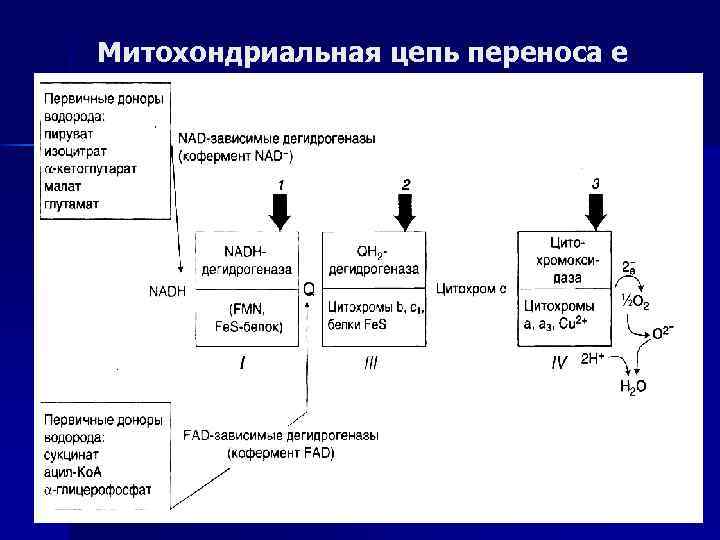
Митохондриальная цепь переноса е

I, III, IV, V комплексы n НАДН-дегидрогеназа (НАДН – Ко. Q- редуктаза, комплекс I) - FMN содержащий Е. n Сукцинат-дегидрогеназа (СДГ)— комплекс II (кофермент ФАД). n Ко. Q 2 -дегидрогеназа (коэнзим. Q – цит. С-редуктаза) — комплекс III. n Цитохромоксидаза — комплекс IV. n Н+-АТФ-синтетаза — комплекс V.

n n Е и коферменты дыхательной цепи За исключением Ко. Q — все компоненты — белки. Субстраты НАД и НАДФ-зависимых дегидрогеназ — в матриксе МТХ и в цитозоле. Первичные доноры Н для НАДзависимых дегидрогеназ: пируват, изоцитрат, α-кетоглутарат, малат, глутамат. У аэробных организмов конечным акцептором е-, получаемых от молекул, является О 2. е- передаются от метаболитов к специальным переносчикам е-, от которых к О 2 передаются по ЦПЭ.

Дыхательная цепь n Последовательность расположения компонентов дыхательной цепи определяется окислительно -восстановительными потенциалами их окисленных и восстановленных пар.
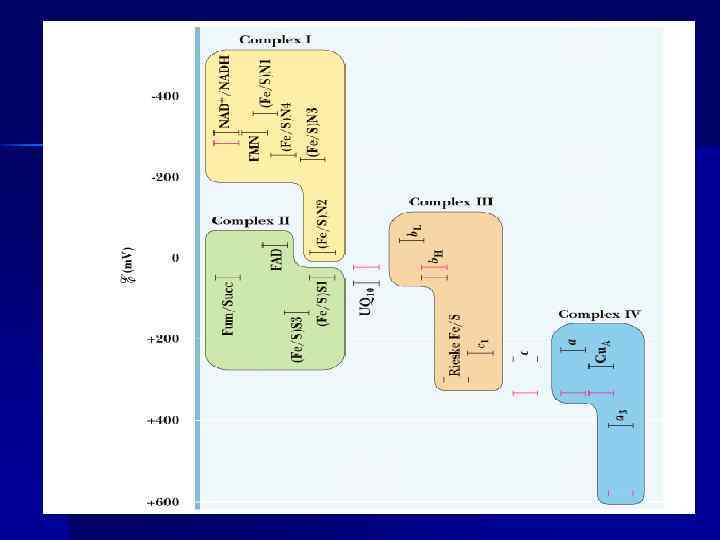

Комплекс I НАДН-дегидрогеназы (FMN содержащий Е) + железо-серные белки Fe. S. n НАДН-дегидрогеназа (НАДН – Ко. Qредуктаза, комплекс I) – Переносит электроны от НАДН к коферменту Q n
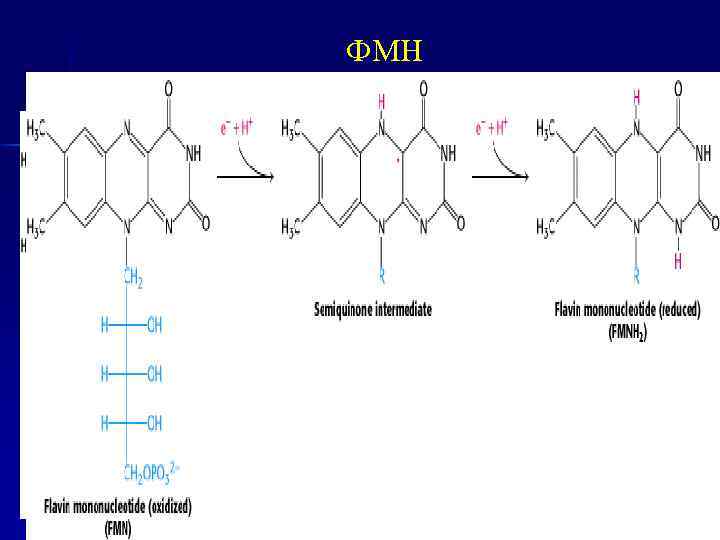
ФМН
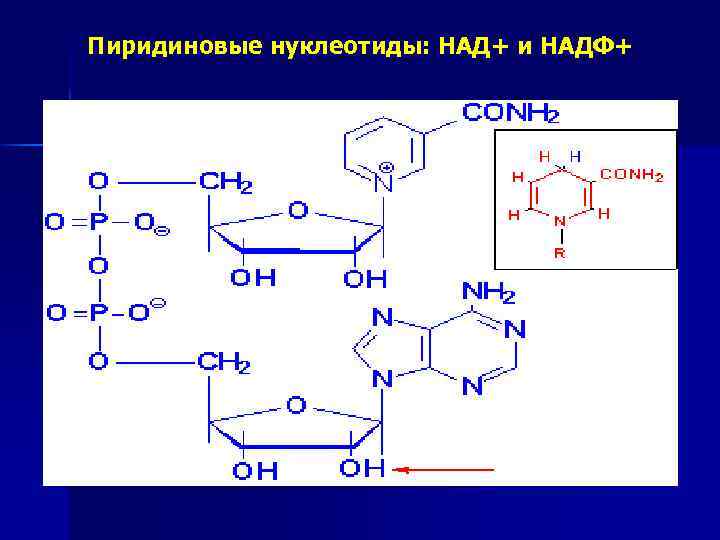
Пиридиновые нуклеотиды: НАД+ и НАДФ+
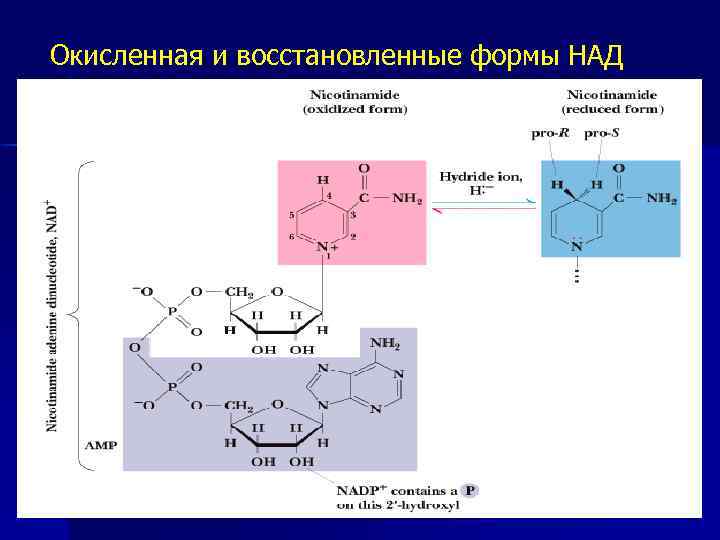
Окисленная и восстановленные формы НАД
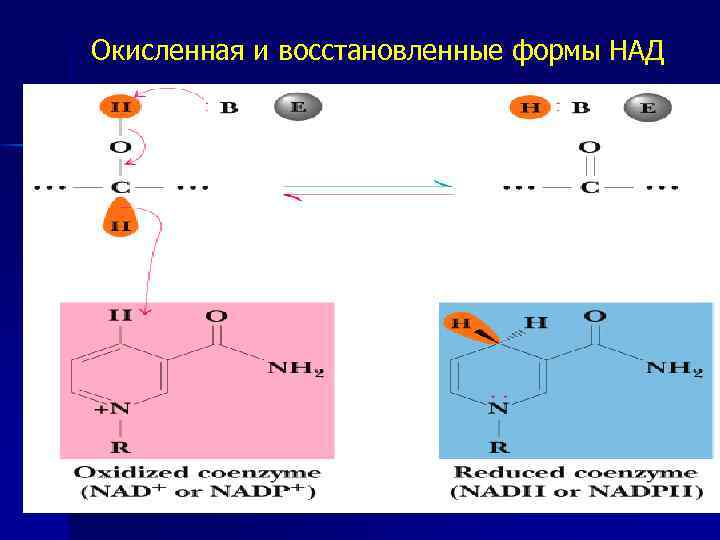
Окисленная и восстановленные формы НАД

n Комплекс II. Fe S центры СДГ — комлекс II. ФАД-зависимыедегидрогеназы (СДГ, дегидрогеназа ЖК) переносят Н на убихинон. Суммарная реакция: Сукцинат + коэнзим Q фумарат + коэнзим QH 2 – Первичные доноры Н для ФАД-зависимых дегидрогеназ: сукцинат, ацил-Ко. А, αглицерофосфат. n Большинство ФАД-зависимых дегидрогеназ — локализовано в матриксе МТХ, за исключением СДГ (во внутренней мембране МТХ).
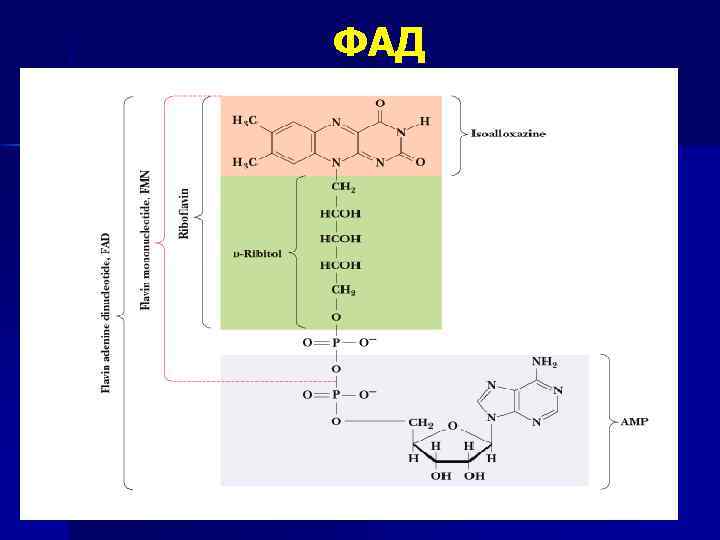
ФАД
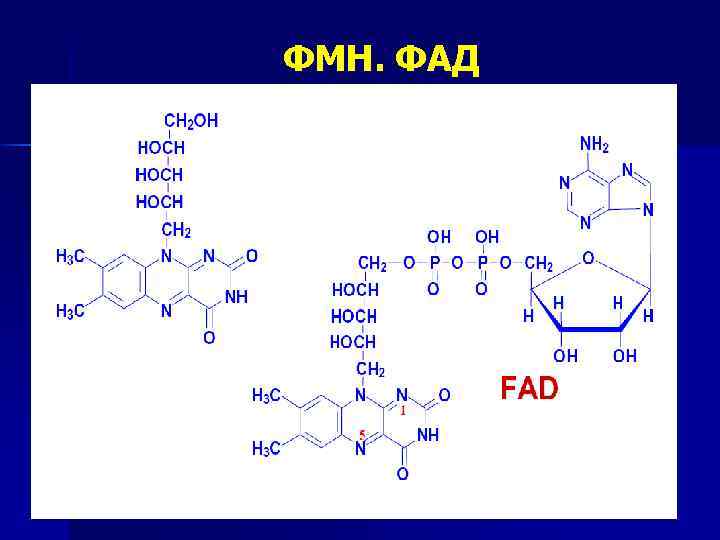
ФМН. ФАД
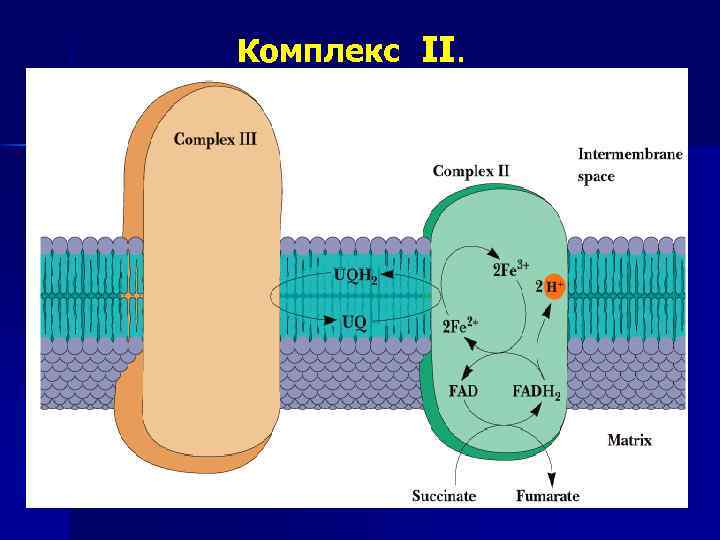
Комплекс II.

Fe S центры n n Fe S центры входят в состав ферментных комплексов I, II и III (во флавопротеидах, ЦТХ). содержат негемовое Fe. 3 х типов (Fe. S, Fe 2 S 2, Fe 4 S 4), атом Fe связан с атомом S остатков цис или неорг. S. Атомы Fе могут отдавать и принимать е - поочередно, переходя в ферро (Fe 2+) и ферри (Fe 3+) состояния.
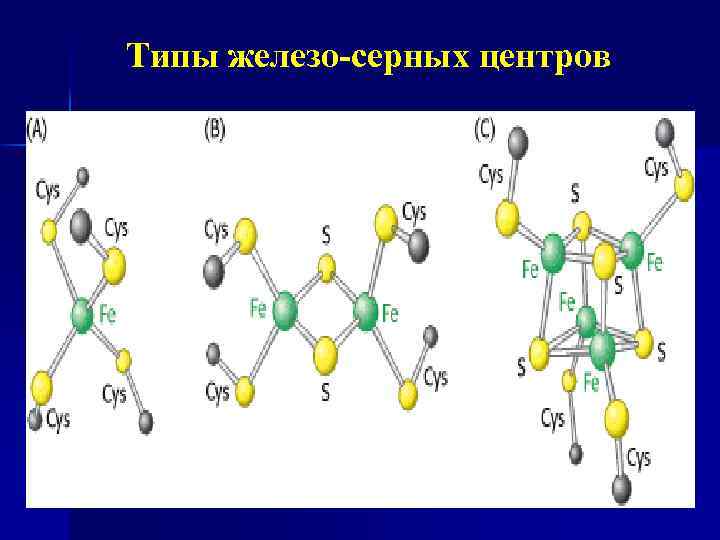
Типы железо-серных центров

Комплекс III n n n Ко. Q — коллекторная функция, присоединяет Н от НАДНдегидрогеназы и др. флавинзависимых дегидрогеназ (СДГ). Ко. Q-дегидрогеназа (коэнзим Q – цит. С-редуктаза) — комплекс III. Ко Q передаёт е- на цитохром С и выкачивает протоны (Н+) в межмембранное пространство (Q цикл);
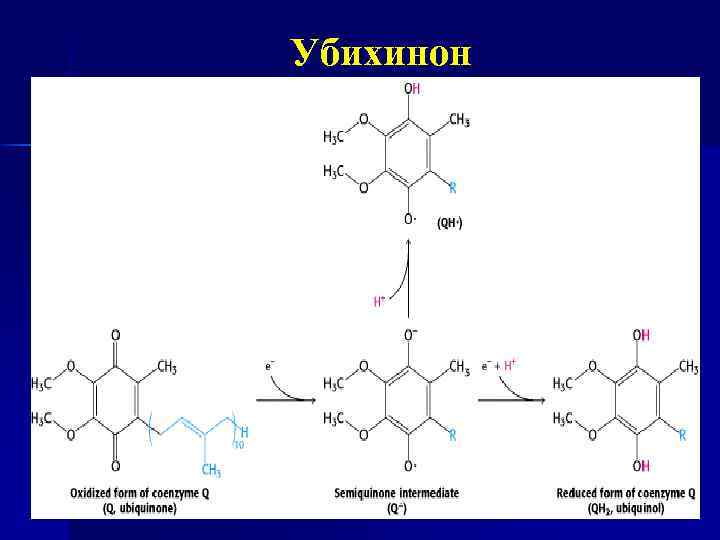
Убихинон

Комплекс III n n n Ко. Q-дегидрогеназа переносит е- от убихинола (Ко. QН 2) на цит. С. В состав входят две формы цитохрома b, один Fe. S-белок и цитохром с1. Цит. С - периферический водорастворимый мембранный белок, сод. 1 полипептидную цепь и молекулу гема.

Цитохромы n n Цитохромы (ЦТХ) ЦПЭ обозначают буквами b, с1, с, а и а 3, расположены в ЦПЭ в порядке увеличения редокс-потенциала. ЦТХ - гемопротеины. Атом Fe в геме ЦТХ меняет валентность, присоединяя и отдавая е-. Fe 2+ ↔ Fe 3+ + е. Комплекс III, включающий ЦТХ b и с1, функционирует как Ko. QН 2 -дегидрогеназа, осуществляет перенос е- с QH 2 на цит. С. епоследовательно проходят через атомы Fe ЦТХ b и с1, а затем поступают на цит. С. С Ko. QН 2 передаются 2 е-, т. к. ЦТХ переносят за 1 цикл по 1 е-, то перед символом ЦТХ ставится коэффициент 2.
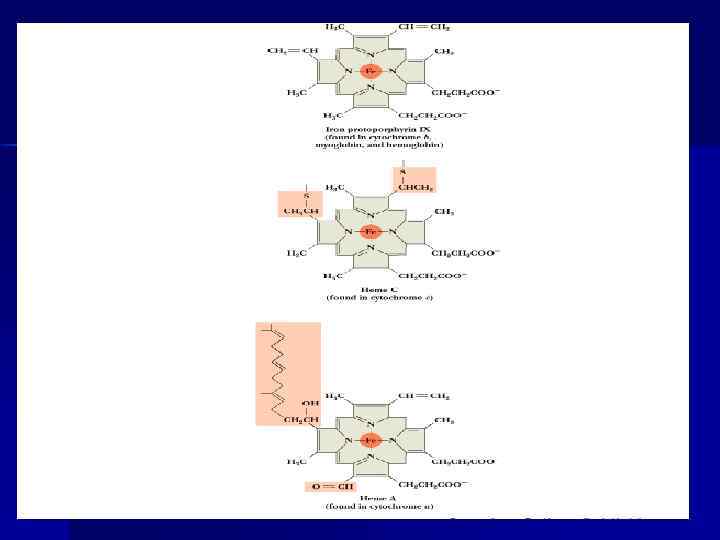

IV-комплекс Цитохромоксидаза (цтх с-оксидаза, IV комплекс), включает 2 ЦТХ (а-а 3), содержит ионы меди. n n Перенос е-комплексом а-а 3 включает р-ции : Си+ ↔ Си 2+ + е. Fe 2+ ↔ Fe 3+ + е- n Переносит е- с цит. С на О 2. Каждый из атомов О 2 последовательно присоединяет по 2 е- и 2 Н+, превращаясь в Н 2 О. О 2 + 4 е- + 4 Н+ 2 Н 2 О
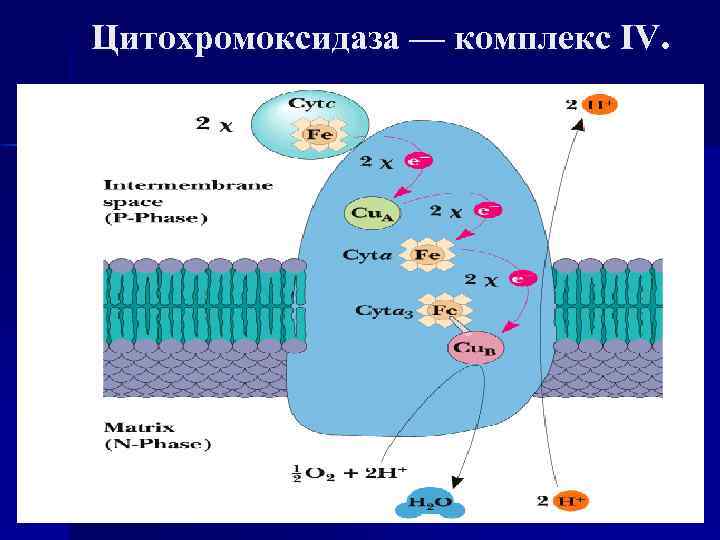
Цитохромоксидаза — комплекс IV.
Комплекс IV Cytochrome c Oxidase
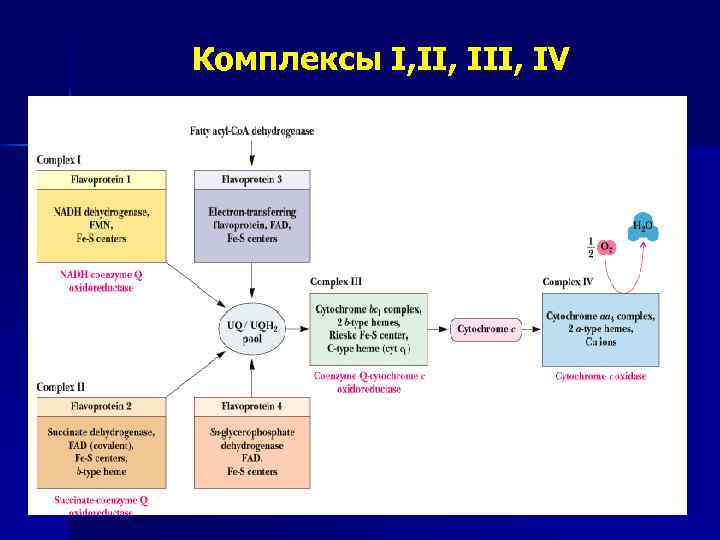
Комплексы I, III, IV
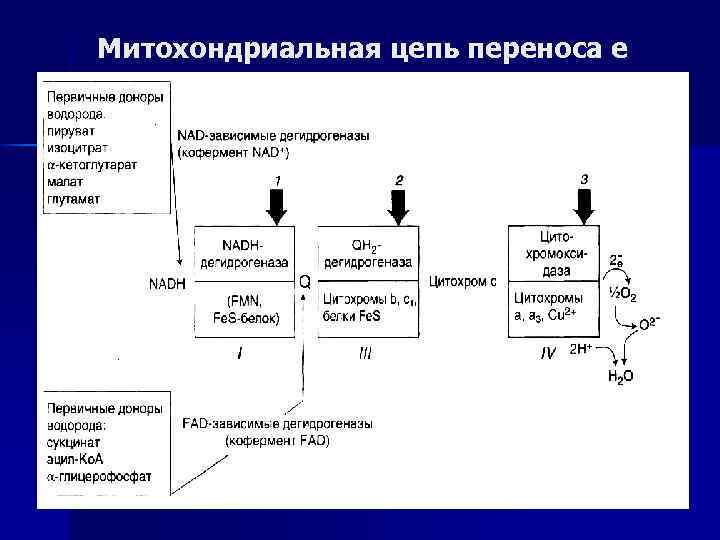
Митохондриальная цепь переноса е
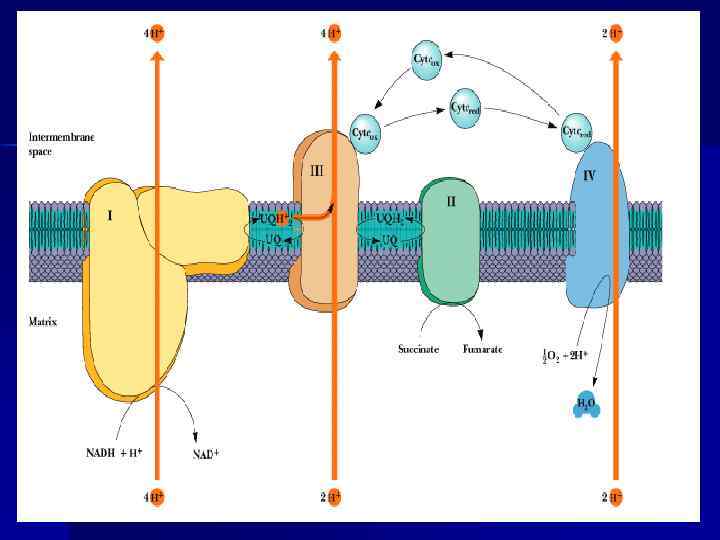

Ингибиторы дыхательной цепи n n Ингибиторы NADH-дегидрогеназы: ротенон, амитал (из группы барбитуратов). Ингибитор QH 2 -дегидрогеназы – антимицин А (антибиотик). n Ингибиторы ЦТХ-оксидазы – цианид, СО, Н 2 S. Цианид присоединяется к Fе ЦТХ-оксидазы. n Переносчики цепи, стоящие в цепи непосредственно перед блокированным этапом, становятся более восстановленными, а стоящие после – более окисленными
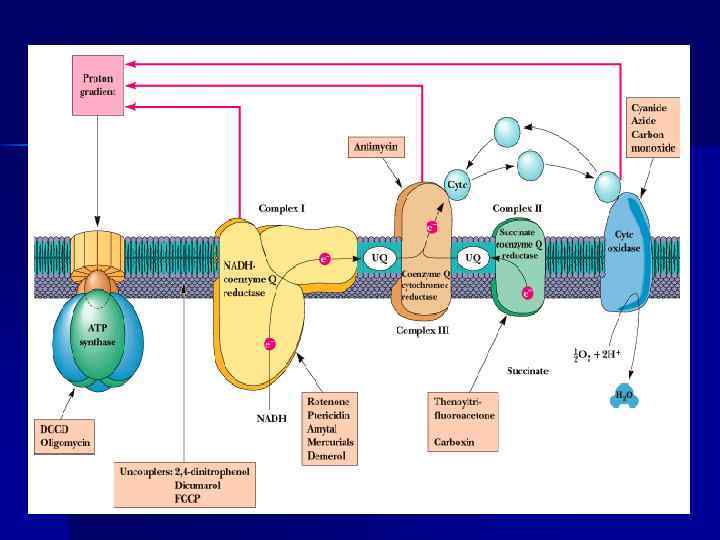

В митохондриях процессы: n Перенос е- с окисляемых S на О 2 (дыхание). n Перенос Н+ из матрикса МТХ в межмембранное пространство и образование трансмембранного электрохимического потенциала. n Синтез АТФ за счет потока Н+ из мембранного пространства в матрикс.


Векторное действие Е ЦПЭ n Е ЦПЭ фиксированы в МТХ мембране так, что их действие векторно, т. е. характеризуется не только величиной скорости реакции, но и пространственной направленностью. Основным проявлением векторности в ЦПЭ является перенос Н+ с внутренней стороны мембраны (со стороны матрикса) на наружную (в межмембранное пространство).

Сопряженное окислительное фосфорилирование вдыхаемый О 2 - SH 2 ----2 Н+-- 2 е- + ½ О 2 S + Н 2 О S восст (окисление, экзергонический процесс) S окислен ↓ энергия---- тепловая энергия ↓(40%) АДФ + Фн АТФ + Н 2 О (фосфорилирование, эндергонический процесс)

Окислительное фосфорилирование n n n NADH+H++1/2 О 2 NAD++ Н 2 О+ 52, 6 ккал/моль (220 к. Дж/моль)— экзергонический процесс. АДФ + Н 3 РО 4 + 7, 3 ккал/моль (30, 5 к. Дж/моль) АТФ + Н 2 О — эндергонический процесс. Синтез АТФ из АДФ и Н 3 РО 4 за счет энергии переноса е- по ЦПЭ — окислительное фосфорилирование.

Н+-АТФ-синтетаза n Электрохимический потенциал вынуждает Н+ двигаться в обратном направлении — с наружной поверхности внутрь. Однако мембрана непроницаема для них, за исключением участков, где располагается Е Н+-АТФсинтетаза, катализирующую р-цию: АДФ + Н 3 РО 4 АТФ + Н 2 О.

ΔμН n На работу, совершаемую при выкачивании Н+, расходуется часть свободной энергии, которая освобождается при переносе е- по градиенту редокс-потенциала. n Энергия электрохимического потенциала (ΔμН+) используется для синтеза АТФ, если Н+ возвращается в матрикс через ионные каналы АТФ-синтетазы.
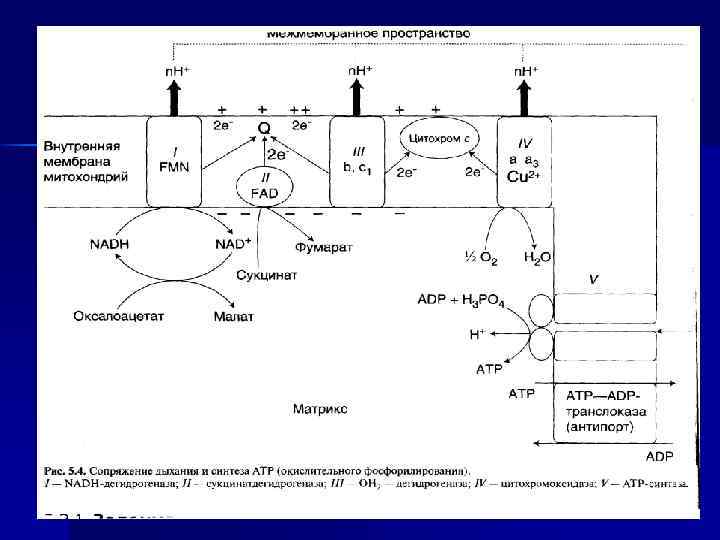

Хемиосмотическая теория П. Митчела (Нобелевская премия). n n n Перенос электронов по дыхательной цепи от НАД. Н+Н+ к кислороду сопровождается выкачиванием Н+ из матрикса митохондрий через внутреннюю мембрану в межмембранное пространство. Протоны, перенесенные из матрикса в межмембранное пространство, не могут вернуться обратно в матрикс, так как внутренняя мембрана непроницаема для протонов. Создается протонный градиент, при котором концентрация протонов в межмембранном пространстве больше, а р. Н меньше, чем в матриксе.

Хемиосмотическая теория П. Митчела Каждый протон несет положительный заряд, и вследствие этого появляется разность потенциалов по обе стороны мембраны: отрицательный заряд на внутренней стороне и положительный на внешней. n В совокупности электрический и концентрационный градиенты составляют электрохимический потенциал Н+– источник энергии для синтеза АТФ n
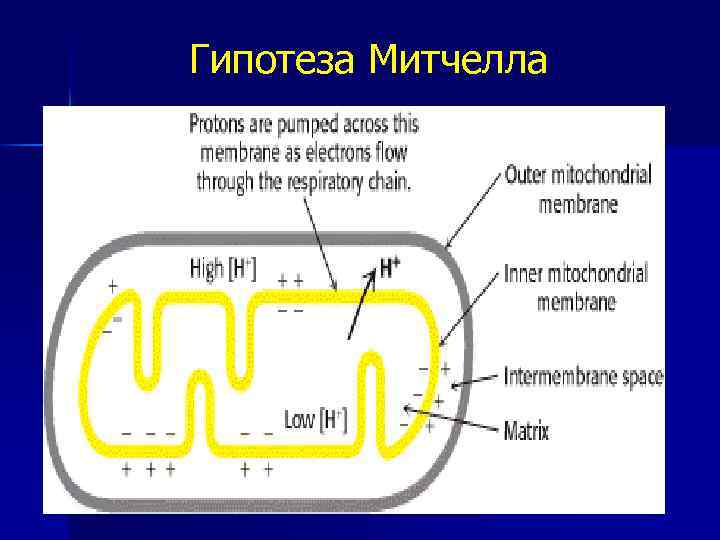
Гипотеза Митчелла
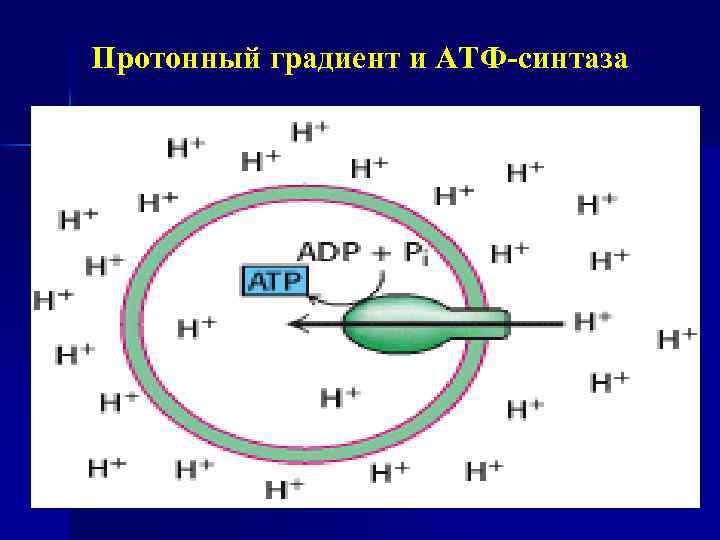
Протонный градиент и АТФ-синтаза

Н+-АТФ-синтетаза n n n Н+-АТФ-синтетаза — интегральный белок внутренней мембраны МТХ, Олигомерный белок, состоит из 2 х комплексов — F 0 и F 1. Гидрофобный комплекс F 0 (трансмембранная часть) погружен в мембрану, состоит из нескольких субъединиц, образующих гидрофильный канал, по которому Н+ переносятся в матрикс. F 1 -субъединица (9 субъединиц) содержит активные центры Е Н+-АТФ-синтетазы, синтезирующей АТФ. ΔμН+ заставляет Н+ двигаться по каналу АТФсинтетазы в матрикс. Под действием ΔμН+происходят конформационные изменения в субъединицах и активация АТФсинтетазы, в результате чего синтезируется АТФ.
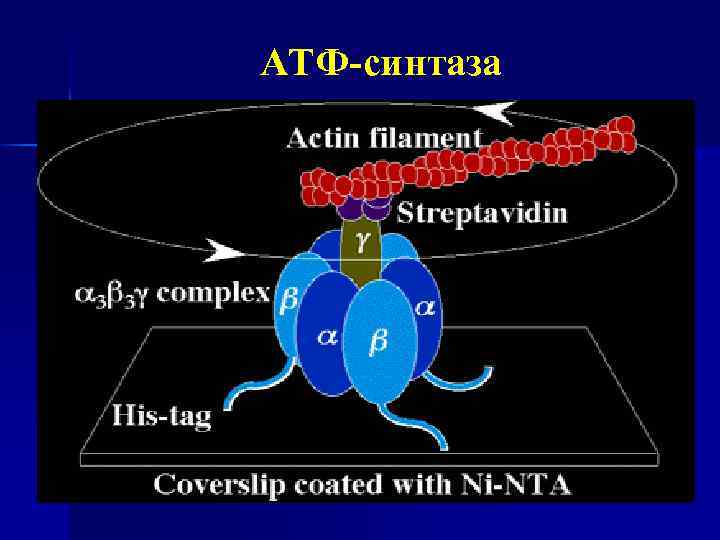
АТФ-синтаза
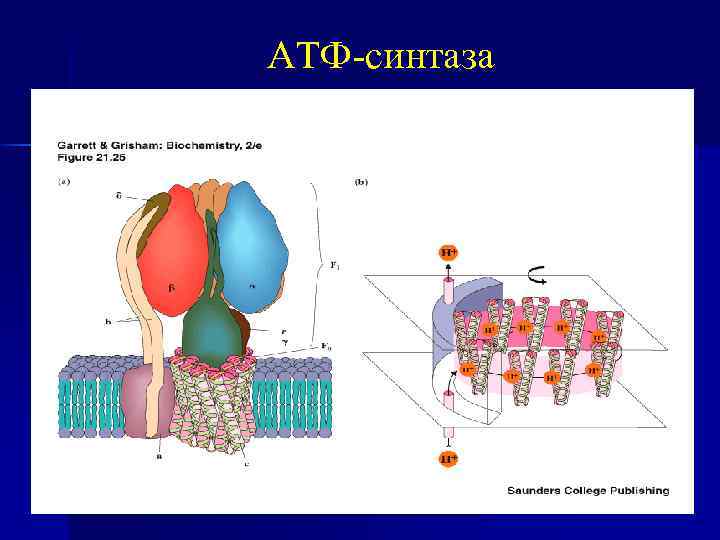
АТФ-синтаза

АТФ-синтаза n n Переносчики е- организованы в 3 комплекса (I, III, IV) во внутренней мембране МТХ. Эти комплексы, используя энергию е-, обеспечивают перенос Н+ из матрикса в межмембранное пространство (векторное действие). В результате возникает протонный электрохимический потенциал (μН+). При достижении определенного значения ΔμН+ происходит активация АТФ-синтазы (комплекс V), в ней открывается канал, через который Н+ возвращаются в матрикс из межмембранного пространства, а энергия ΔμН+ используется для синтеза АТФ. Каждый из 3 комплексов ЦПЭ (I, III, IV) обеспечивает необходимый градиент Н+ для активации АТФ-синтазы и синтеза 1 молекулы АТФ. Образующаяся АТФ при участии АДФ/АТФтранслоказы из матрикса ЦП. Та же транслоказа переносит АДФ из ЦП в матрикс МТХ.

АТФ-АДФ-транслоказа n В большинстве клеток синтез АТФ происходит в митохондриях, а основные потребители АТФ расположены вне её; n В мембране есть белок АТФ/АДФ-антипортер (транслоказа), осуществляющий перенос этих метаболитов через мембрану; n Молекула АДФ поступает в митохондриальный матрикс только при условии выхода молекулы АДФ из матрикса; Движущая сила такого обмена - мембранный потенциал переноса электронов по ЦПЭ; На транспорт АТФ и АДФ расходуется около четверти свободной энергии протонного потенциала. n n n Т. О. образующаяся АТФ при участии АДФ/АТФтранслоказы из матрикса ЦП. Та же транслоказа переносит АДФ из ЦП в матрикс МТХ.
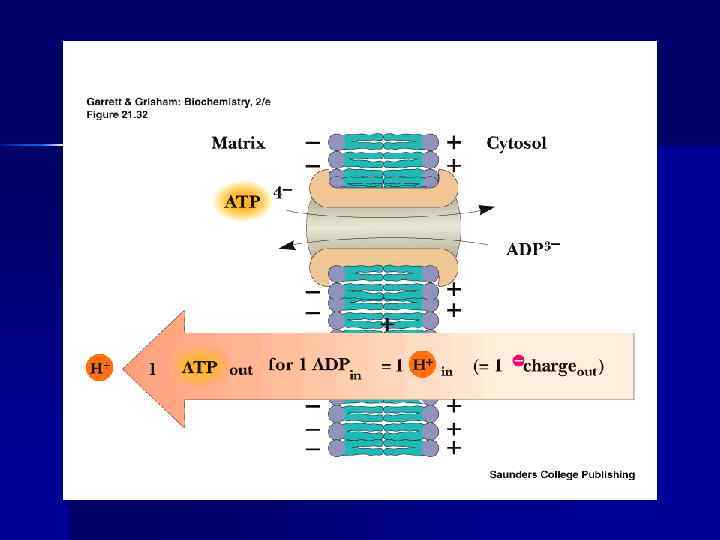

Р/О n В расчете на каждый атом поглощенного О 2 МТХ образуют 3 молекулы АТФ, т. е. 3 молекулы Н 3 РО 4 связываются с АДФ. n Отношение количества связанной Н 3 РО 4 к количеству поглощенного О называют коэффициентом фосфорилирования, обозначают Р/О = 3. ФАД-зависимые-дегидрогеназы не являются протонными насосами: в этом случае в ЦПЭ действуют только два пункта перекачки протонов — комплексы III и IV и коэффициент Р/О не может быть >2. Т. о. , Р/О = 3 или<3.

Дыхательный контроль n Результат окисления НАДН и фосфорилирования АДФ в ЦПЭ можно представить так: НАДН+Н++ ½ О 2 НАД + Н 2 О 3 АДФ + 3 Н 3 РО 4 3 АТФ + 3 Н 2 О n Зависимость дыхания МТХ от концентрации АДФ — дыхательный контроль. n Скорость синтеза АТФ определяется потребностью клетки в энергии. При увеличении расходования АТФ, увеличивается концентрация АДФ, а это ведет к ускорению дыхания и фосфорилирования.

Разобщение дыхания и фофорилирования n Разобщение потока электронов и окислительного фосфорилирования происходит при нарушении протонного градиента; Разобщители являются гидрофобными (липофильными) молекулами, способными диссоциировать и проходить через липофильный слой мембраны. n Они перемещаются через мембрану, перенося протоны из межмембранного пространства обратно в матрикс, нарушая протонный градиент. n

Разобщение дыхания и фофорилирования n n n 2, 4 динитрофенол (липофильное вешество) диффундирует через МТХ мембрану как в ионизированной, так и в неионизированной форме и поэтому может переносить Н+ через мембрану в сторону их меньшей концентрации в обход протонных каналов. 2, 4 динитрофенол уничтожает ΔμН+ МТХ мембраны и энергия рассеивается в виде тепла (разобщители обладают пирогенным действием. ). Потребление О 2 и окисление S при этом происходят, но синтез АТФ не возможен. Разобщители: дикумарол, билирубин, тироксин в высоких концентрациях, ВЖК.

Терморегуляторная функция – Разобщающий белок – термогенин способен переносить анионы ЖК, служащие разобщителями.
Биоэнергетика стомат 1 лекц.ppt