5 Гидриды, фториды, оксиды.ppt
- Количество слайдов: 36

Бинарные соединения Водородные соединения

Классификация • Солеобразные гидриды: ▪ гидриды щелочных и щелочно-земельных металлов (Li. H, Na. H, …, Ca. H 2) • Полимерные и димерные гидриды: ▪ водородные соединения легких элементов IIA и IIIA -групп ((Be. H 2)x, (Mg. H 2)x, (Al. H 3)x, B 2 H 6, Ga 2 H 6) • Металлоподобные гидриды: ▪ Фазы внедрения на основе переходных металлов с дефектной d-оболочкой (Me. H 1–x, Me. H 2–x, Me. H 3–x) • Летучие водородные соединения (характеристические соединения): ▪ Молекулярные водородные соединения элементов (IVA–VIIA-групп) 2 • • ЭIVH 4 (CH 4, Si. H 4, …) ЭVH 3 (NH 3, PH 3, …) ЭVIH 2 (H 2 O, H 2 S, …) ЭVIIH (HF, HCl, …)

Особенности номенклатуры • ОЭО(H) = 2, 1 • Гидрид – бинарное соединение водорода с менее электроотрицатльным элементом (H – анионообразователь, ст. ок. = – 1) ▪ Солеобразные и полимерные гидриды элементов IA-IIIA-групп ▪ H– (из гидрида) + H+ (из воды) H 2 (гидрид-ион – сильный восстановитель) ▪ Металлоподобные фазы внедрения – гидриды условно (H – не анионообразователь, говорить о ст. ок. бессмысленно) 3

Особенности номенклатуры • IV-группа • CH 4 H 4 C – карбид водорода (ОЭО(С) = 2, 6) • НО ▪ ▪ Si. H 4 – гидрид кремния (ОЭО(Si) = 1, 9) Ge. H 4 – гидрид германия (ОЭО(Ge) = 2, 0) Sn. H 4 – гидрид олова (ОЭО(Sn) = 1, 8) Используется единообразная тривиальная номенклатура и формально ст. ок. (Эл-та) = – 4 ▪ C(– 4)H(+1)4 – метан; Si(– 4)H(+1)4 – силан; Ge(– 4)H(+1)4 – герман; Sn(– 4)H(+1)4 – станнан; 4

Особенности номенклатуры • V-группа • NH 3 H 3 N – нитрид водорода (ОЭО(N) = 3, 0) • НО ▪ PH 3 – гидрид фосфора, фосфид водорода (ОЭО(P) = 2, 1) ▪ As. H 3 – гидрид мышьяка ▪ Sb. H 3 – гидрид сурьмы ▪ Bi. H 3 – гидрид висмута ▪ N(– 3)H(+1)3 – аммиак (аммин); P(– 3)H(+1)3 – фосфин; As(– 3)H(+1)3 – арсин; Sb(– 3)H(+1)3 – стибин; Bi(– 3)H(+1)3 – висмутин; 5
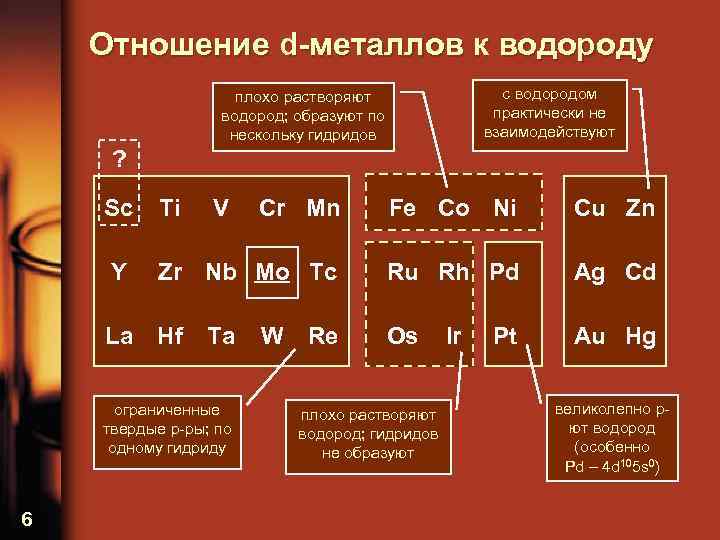
Отношение d-металлов к водороду с водородом практически не взаимодействуют плохо растворяют водород; образуют по нескольку гидридов ? Sc Ti V Cr Mn Fe Co Ni Cu Zn Y Zr Nb Mo Tc Ru Rh Pd Ag Cd La Hf Os Au Hg Ta ограниченные твердые р-ры; по одному гидриду 6 W Re плохо растворяют водород; гидридов не образуют Ir Pt великолепно рют водород (особенно Pd – 4 d 105 s 0)

Изменение температур плавления в изо-рядах характеристических водородных соединений
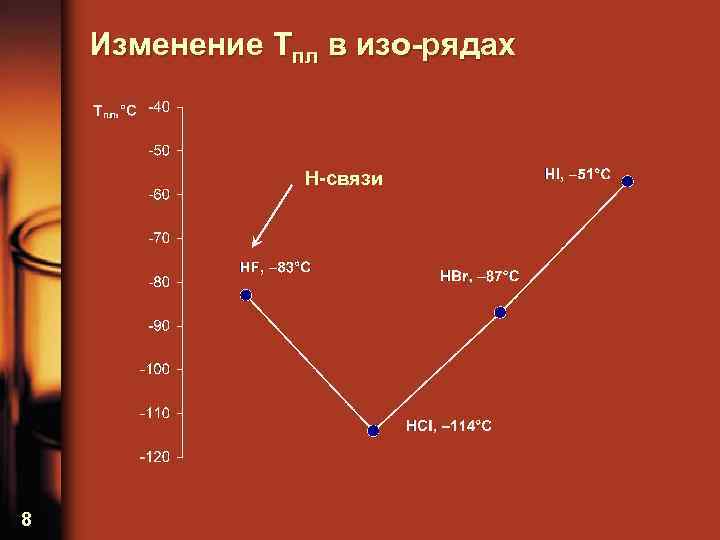
Изменение Tпл в изо-рядах H-связи 8
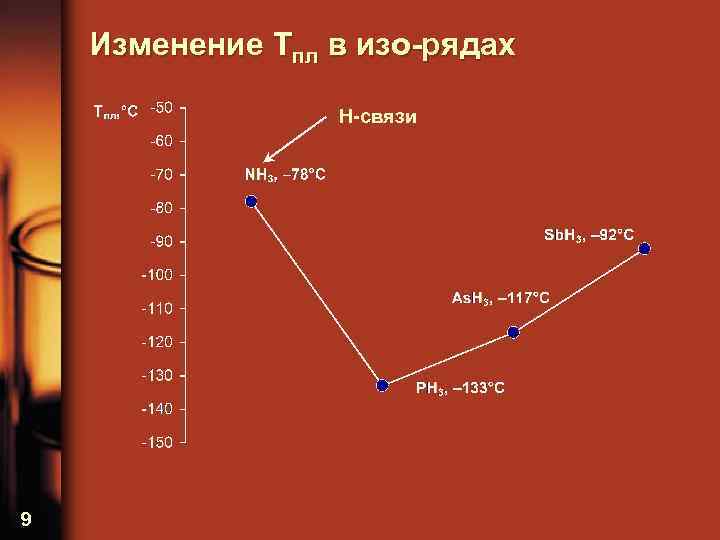
Изменение Tпл в изо-рядах H-связи 9

Изменение Tпл в изо-рядах H-связи 10
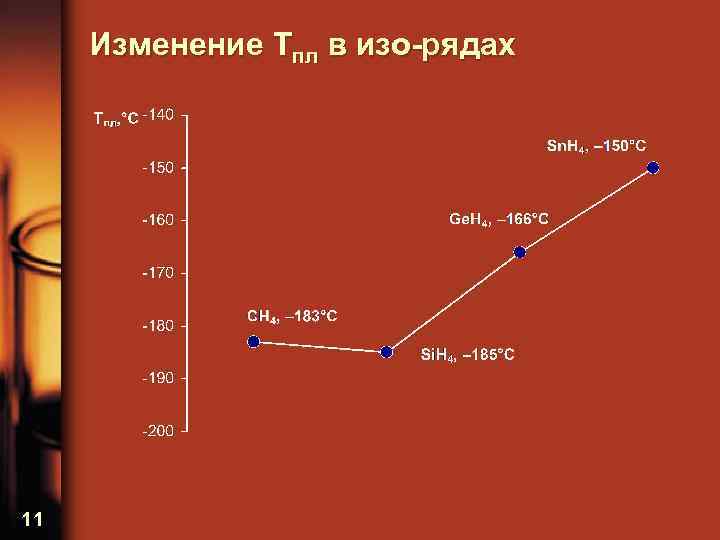
Изменение Tпл в изо-рядах 11

Характер диссоциации в H 2 O растворах (Трансформация межмолекулярных водородных связей в донорно-акцепторные)
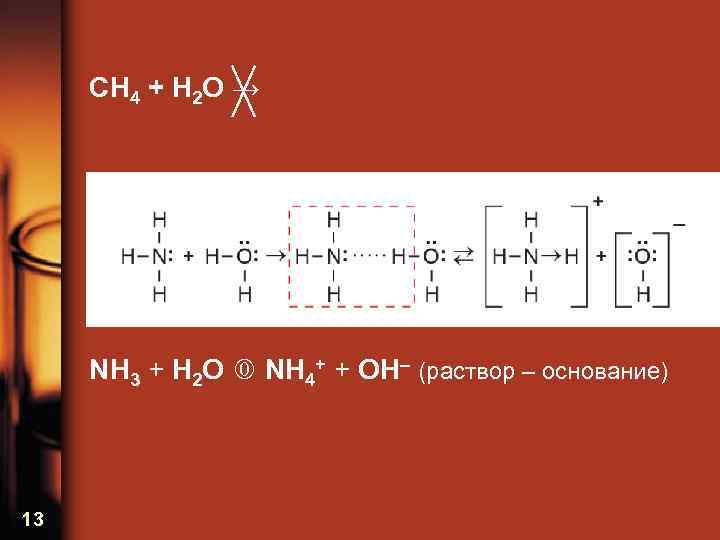
CH 4 + H 2 O → NH 3 + H 2 O NH 4+ + OH– (раствор – основание) 13
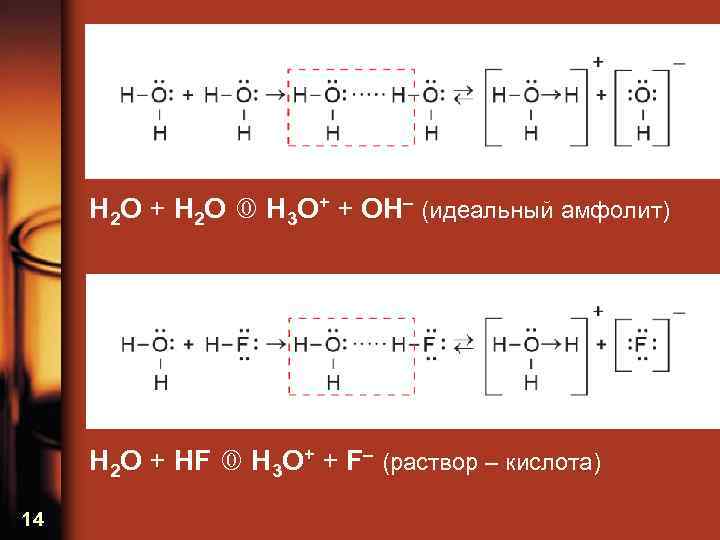
H 2 O + H 2 O H 3 O+ + OH– (идеальный амфолит) H 2 O + HF H 3 O+ + F– (раствор – кислота) 14
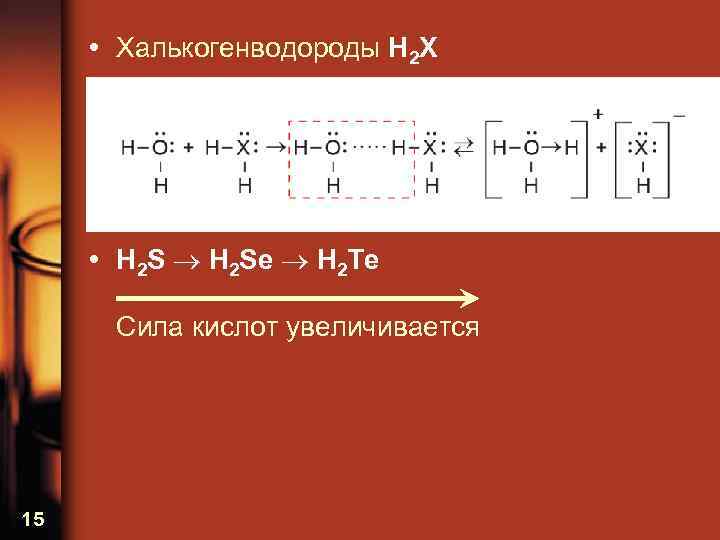
• Халькогенводороды H 2 X • H 2 Se H 2 Te Сила кислот увеличивается 15
![• Галогенводороды HГ • HCl HBr HI Сила кислот увеличивается H–F [H–F→H]+ + • Галогенводороды HГ • HCl HBr HI Сила кислот увеличивается H–F [H–F→H]+ +](https://present5.com/presentation/3/14884915_68581649.pdf-img/14884915_68581649.pdf-16.jpg)
• Галогенводороды HГ • HCl HBr HI Сила кислот увеличивается H–F [H–F→H]+ + [H–F→H]– (H 2 F+ + HF 2–) • HF – слабая кислота! 16

Бинарные соединения Галогениды как характеристические соединения
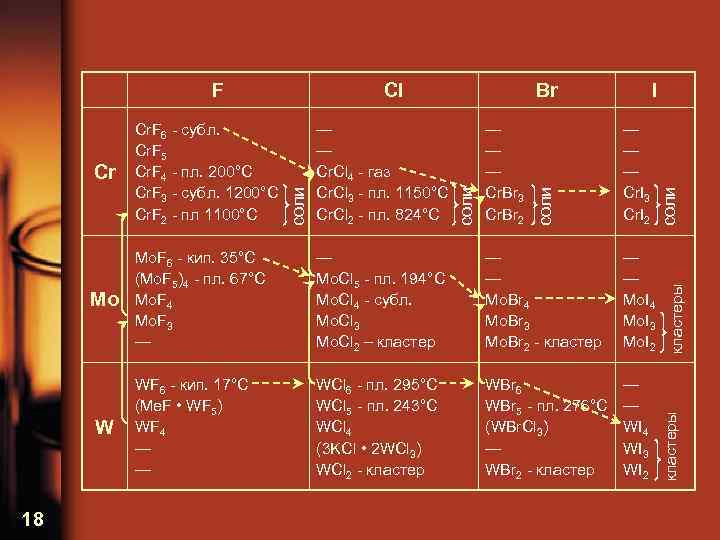
— — Mo. Br 4 Mo. Br 3 Mo. Br 2 - кластер — — Mo. I 4 Mo. I 3 Mo. I 2 WF 6 - кип. 17°С (Me. F • WF 5) WF 4 — — WCl 6 - пл. 295°С WCl 5 - пл. 243°С WCl 4 (3 KCl • 2 WCl 3) WCl 2 - кластер WBr 6 WBr 5 - пл. 276°С (WBr. Cl 3) — WBr 2 - кластер — — WI 4 WI 3 WI 2 соли — Mo. Cl 5 - пл. 194°С Mo. Cl 4 - субл. Mo. Cl 3 Mo. Cl 2 – кластеры Mo Mo. F 6 - кип. 35°С (Mo. F 5)4 - пл. 67°С Mo. F 4 Mo. F 3 — соли — — — Cr. I 3 Cr. I 2 соли Cr 18 — — — Cr. Br 3 Cr. Br 2 I Cr. F 6 - субл. Cr. F 5 Cr. F 4 - пл. 200°С Cr. F 3 - субл. 1200°С Cr. F 2 - пл 1100°С W — — Cr. Cl 4 - газ Cr. Cl 3 - пл. 1150°С Cr. Cl 2 - пл. 824°С Br кластеры Cl соли F
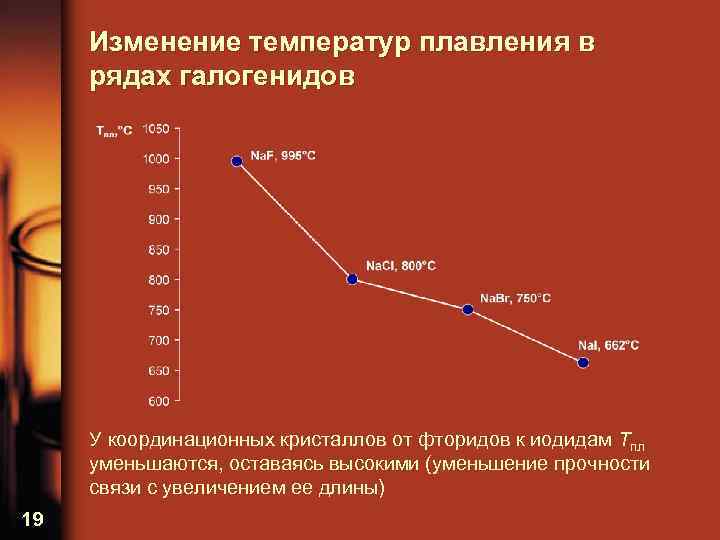
Изменение температур плавления в рядах галогенидов У координационных кристаллов от фторидов к иодидам Tпл уменьшаются, оставаясь высокими (уменьшение прочности связи с увеличением ее длины) 19
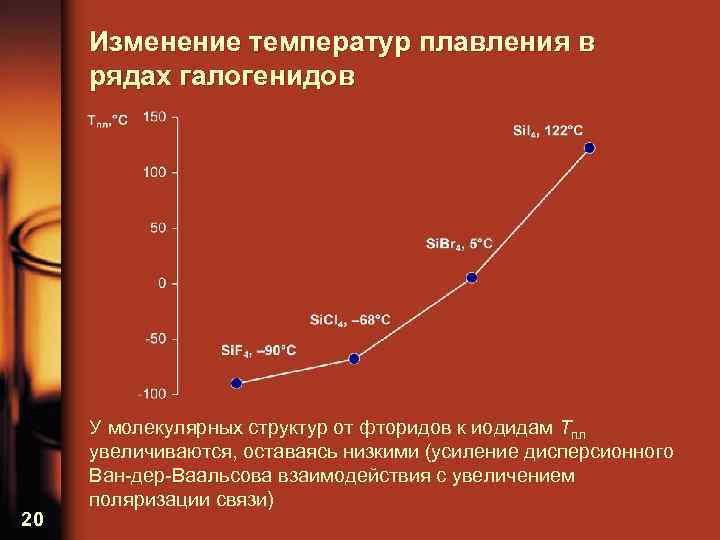
Изменение температур плавления в рядах галогенидов 20 У молекулярных структур от фторидов к иодидам Tпл увеличиваются, оставаясь низкими (усиление дисперсионного Ван-дер-Ваальсова взаимодействия с увеличением поляризации связи)

Эволюция степеней окисления катионообразователя при нагревании 370°C 435°C 581°C 583°C Pt. Cl 4 Pt. Cl 3 Pt. Cl 2 Pt. Cl Pt 263°C 272°C 355°C Ptl 4 Ptl 3 Ptl 2 Pt 21

Полный гидролиз «по катиону» • BBr 3 + 3 H 2 O 3 HBr + H 3 BO 3 • Si. Cl 4 + 2 H 2 O 4 HCl + Si. O 2 • CCl 4, SF 6, NI 3 в воде нерастворимы (нет гидролиза) 22

Изменение восстановительных свойств в ряду галогенид-ионов • Na. F(к) + H 2 SO 4(конц) Na. HSO 4 + HF • Na. Cl(к) + H 2 SO 4(конц) Na. HSO 4 + HCl • 2 Na. Br(к) + 2 H 2 SO 4(конц) Na 2 SO 4 + Br + SO 2 + 2 H 2 O ▪ Br– восстанавливает H 2 SO 4 до SO 2 • 8 Na. I(к) + 5 H 2 SO 4(конц) 4 Na 2 SO 4 + 4 I + H 2 S + 4 H 2 O ▪ I– восстанавливает H 2 SO 4 до H 2 S 23
![Галогенидные ацидокомплексы • Типичное к. ч. 4: K 2[Hg. I 4], H[Au. Cl 4] Галогенидные ацидокомплексы • Типичное к. ч. 4: K 2[Hg. I 4], H[Au. Cl 4]](https://present5.com/presentation/3/14884915_68581649.pdf-img/14884915_68581649.pdf-24.jpg)
Галогенидные ацидокомплексы • Типичное к. ч. 4: K 2[Hg. I 4], H[Au. Cl 4] • Для фторидов помимо к. ч. 4 есть к. ч. 6: Me. I 2[Be. F 4], Me. I 3[Al. F 6], Me. I 2[Si. F 6], 24

Бинарные соединения Кислородсодержащие соединения

Классификация • Соединения не подчиняющиеся правилу формальной валентности ▪ анионоизбыточные соединения • пероксиды (Na 2 O 2, Ca. O 2, …) ст. окисления кислорода – 1) • супероксиды (надпероксиды) (KO 2, …) ст. окисления – 1/2) • озониды (KO 3, …) ст. окисления – 1/3 ▪ катионоизбыточные соединения – металлидные фазы типа соединений Курнакова (Ti 6 O, Ti 3 O, …) 26

Классификация • Характеристические соединения – подчиняющиеся правилу формальной валентности, оксиды с ионно-ковалентным типом связи ▪ солеообразующие • основные (оксиды металлов в невысоких степенях окисления) • кислотные (оксиды неметаллов в любых степенях окисления и металлов в высоких степенях окисления) • амфотерные (оксиды металлов в промежуточных степенях окисления +2…+4 при ОЭО 1, 4… 1, 8) ▪ несолеообразующие (CO, N 2 O, NO) – им не соответствуют гидроксиды и от них не происходят соли 27

Характерные структурные типы оксидов в зависимости от природы химической связи

Оксиды ЭО • Структурный тип Na. Cl ▪ Mg. O, Pb. O, Ti. O, … ▪ к. ч. = 6; 6 • Вюрцит ▪ Zn. O, Be. O… ▪ к. ч. = 4; 4 29
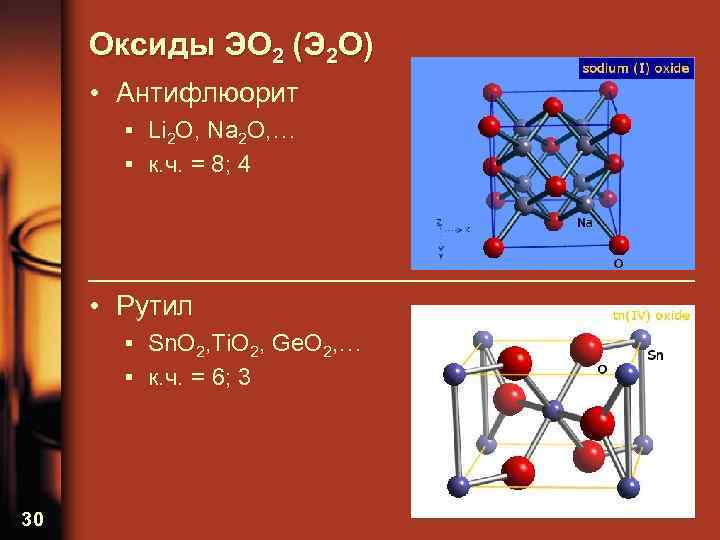
Оксиды ЭО 2 (Э 2 О) • Антифлюорит ▪ Li 2 O, Na 2 O, … ▪ к. ч. = 8; 4 • Рутил ▪ Sn. O 2, Ti. O 2, Ge. O 2, … ▪ к. ч. = 6; 3 30
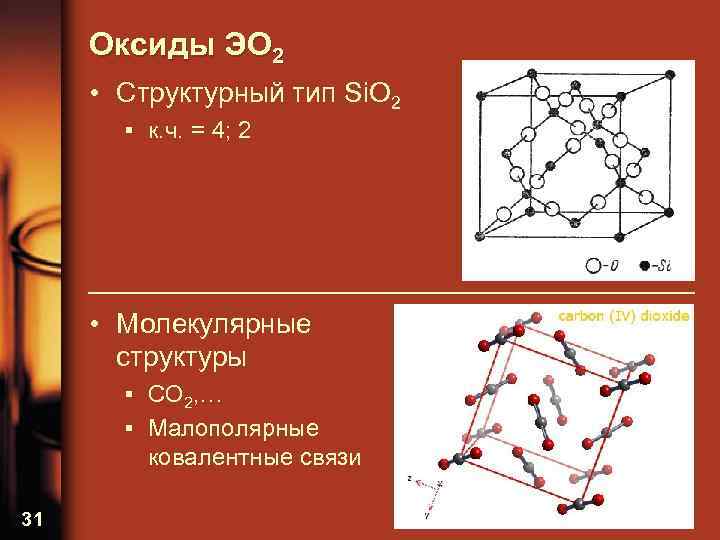
Оксиды ЭО 2 • Структурный тип Si. O 2 ▪ к. ч. = 4; 2 • Молекулярные структуры ▪ CO 2, … ▪ Малополярные ковалентные связи 31

основные ↓ • Антифлюорит • Рутил амфотерные ↓ кислотные 32 • Si. O 2 • Молекулярные структуры уменьшение ионного и нарастание ковалентного вклада

Структуры характеристических оксидов элементов IVA-VIIA-групп

IVA-группа CO 2 – молекуляр. Si. O 2 – (кварц, кристобалит, тридимит) Ge. O 2 Sn. O 2 Pb. O 2 рутил VA-группа VIIA-группа все оксиды Nи. P– молекулярны SO 2 SO 3 оксиды As и Sb – псевдомолекулярны Se. O 2 – Bi 2 O 3 – молекулярен координационная (к. ч. 6 и 3) молекуляр. псевдомолекулярен Se. O 3 – Te. O 2 – рутил Te. O 3 – молекулярен 34 все оксиды Cl, Br , I – молекулярны со фтором OF 2 – фторид (молекулярен)
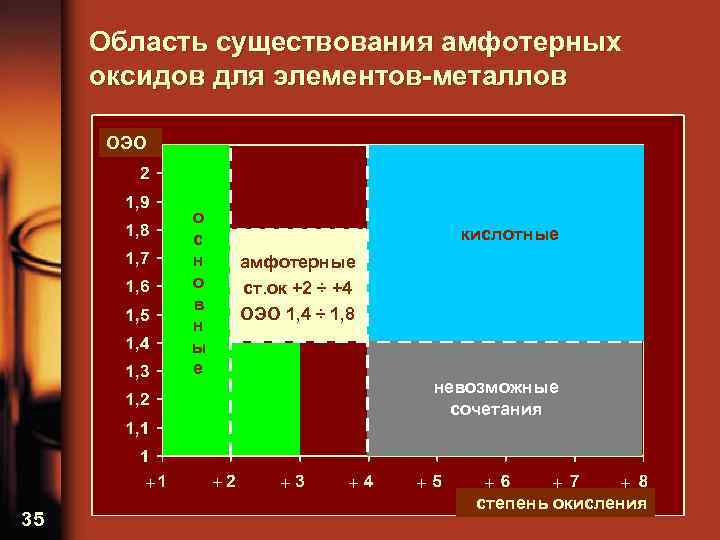
Область существования амфотерных оксидов для элементов-металлов ОЭО о с н о в н ы е + 35 кислотные амфотерные ст. ок +2 ÷ +4 ОЭО 1, 4 ÷ 1, 8 невозможные сочетания + + + + степень окисления

Амфотерные свойства оксидов ▪ В отличие от гидроксидов многие амфотерные оксиды (Zn. O, Al 2 O 3, Cr 2 O 3, …), особенно прокаленные, обладают малой реакционной способностью – проявляют амфотерность только в жестких условиях, при сплавлении t, сплав. • Al 2 O 3 + 2 Na. OH(безвод. ) 2 Na. Al. O 2 + H 2 O t, сплав. • Al 2 O 3 + 3 K 2 S 2 O 7(безв. ) Al 2(SO 4)3 + 3 K 2 SO 4 36
5 Гидриды, фториды, оксиды.ppt