Tema_2_A_bioorgan_khimija.ppt
- Количество слайдов: 27

БІЛКИ Білки, протеїни (від грец. protos – перший, найважливіший) – природні органічні високомолекулярні сполуки, які у вигляді мономерних ланок містять залишки протеїногенних амінокислот, сполучених пептидним зв'язком. Білки є досить важливими у біологічному відношенні та досить складними за структурою сполуками. Вони зустрічаються в усіх живих організмах і є основою їх життєдіяльності. Кожний білок характеризується специфічною амінокислотною послідовністю й індивідуальною просторовою структурою (конформацією). На частку білків доводиться не менш 50% сухої маси органічних сполук тваринної клітини, і в організмі людини налічується до 5 млн. різних видів білків. Функціонування білка лежить в основі найважливіших процесів життєдіяльності організму.

АМІНОКИСЛОТНИЙ СКЛАД БІЛКІВ Більшість білків отримані в чистому кристалічному вигляді: Кристали цитохрому С Кристали трипсину бика Амінокислота Аланін Аргінін Аспарагінова кислота Цистеїн Глутамінова кислота Гліцин Гистидин Ізолейцин Лізин Метіонін Фенилаланін Пролін Серин Треонін Триптофан Тирозин Валін Цитохром С людини Хімотрипсиноген бика 6 2 5 3 2 2 8 13 3 8 6 18 3 3 4 2 7 1 5 3 104 22 4 15 8 10 10 5 23 2 10 19 14 2 6 9 28 23 8 4 23 245

БІОЛОГІЧНІ ФУНКЦІЇ БІЛКІВ Ферментативна. Обмін речовин (травлення, подих та ін. ), м'язове скорочення, нервова провідність і життя клітини в цілому нерозривно пов'язані з активністю ферментів – високоспецифічних каталізаторів біохімічних реакцій, які є білками. Будівельна. Основою кісткової й сполучної тканин, вовни, рогових утворень є структурні білки. Вони ж формують кістяк клітинних органел (мітохондрій, мембран та ін. ). Скорочувальна. Розходження хромосом при розподілі клітини, рух джгутиків, робота м'язів тварин і людини здійснюються за єдиним механізмом за допомогою білків скорочувальної системи (актину й міозину). Регуляторна. Важливою групою є регуляторні білки, які контролюють біосинтез білка й нуклеїнових кислот. До регуляторних білків належать також пептидно-білкові гормони, які секретуються ендокринними залозами. Рецепторна. Інформація про стан зовнішнього середовища, різні регуляторні сигнали (у т. ч. гормональні) сприймаються клітиною за допомогою спеціальних рецепторних білків, що розташовуються на зовнішній поверхні плазматичної мембрани. Ці білки відіграють важливу роль у передачі нервового збудження й в орієнтованому русі клітини (хемотаксисі).

БІОЛОГІЧНІ ФУНКЦІЇ БІЛКІВ Транспортна. В активному транспорті іонів, ліпідів, цукрів і амінокислот через біологічні мембрани беруть участь транспортні білки, або білкипереносники. До них відносяться також гемоглобін і міоглобін, що здійснюють перенос кисню. Захисна. Захисні системи вищих організмів формуються захисними білками, до яких відносяться імуноглобуліни (відповідальні за імунітет), білки комплемента (відповідальні за лізис чужорідних клітин і активацію імунологічної функції), білки системи згортання крові (наприклад, тромбін, фібрин) і противірусний білок інтерферон. Спеціальна. Перетворення й утилізація енергії, що надходить в організм із харчуванням, а також енергії сонячного випромінювання відбуваються при участі білків біоенергетичної системи (наприклад, родопсин, цитохроми). Живильна. Велике значення мають харчові й запасні білки (наприклад, казеїн, проламіни), які відіграють важливу роль у розвитку й функціонуванні організмів.
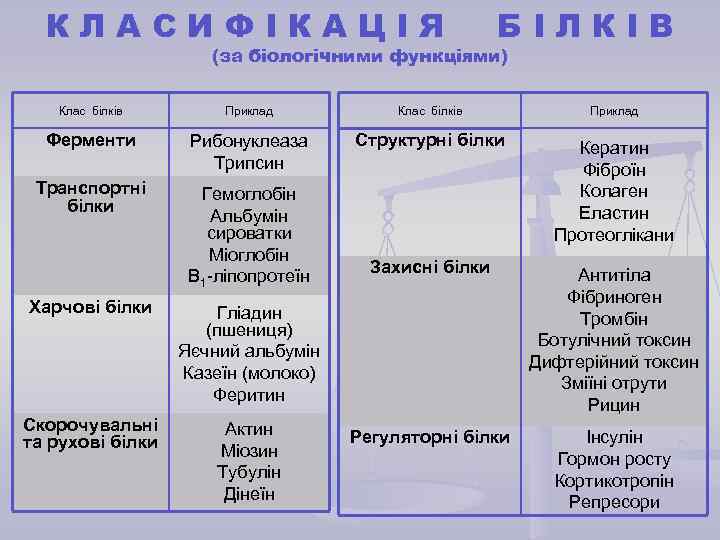
КЛАСИФІКАЦІЯ БІЛКІВ (за біологічними функціями) Клас білків Приклад Клас білків Ферменти Рибонуклеаза Трипсин Структурні білки Транспортні білки Гемоглобін Альбумін сироватки Міоглобін В 1 -ліпопротеїн Кератин Фіброїн Колаген Еластин Протеоглікани Захисні білки Антитіла Фібриноген Тромбін Ботулічний токсин Дифтерійний токсин Зміїні отрути Рицин Регуляторні білки Інсулін Гормон росту Кортикотропін Репресори Харчові білки Гліадин (пшениця) Яєчний альбумін Казеїн (молоко) Феритин Скорочувальні та рухові білки Актин Міозин Тубулін Дінеїн Приклад

КЛАСИФІКАЦІЯ БІЛКІВ За складом білки ділять на прості, що складаються тільки з амінокислотних залишків і складні. Складні можуть включати іони металу (металопротеїди) або пігмент (хромопротеїди), утворювати міцні комплекси з ліпідами (ліпопротеїди), нуклеїновими кислотами (нуклеопротеїди), а також ковалентно зв'язувати залишок фосфорної кислоти (фосфопротеїди), вуглеводу (глікопротеїди) або нуклеїнової кислоти (геноми деяких вірусів).
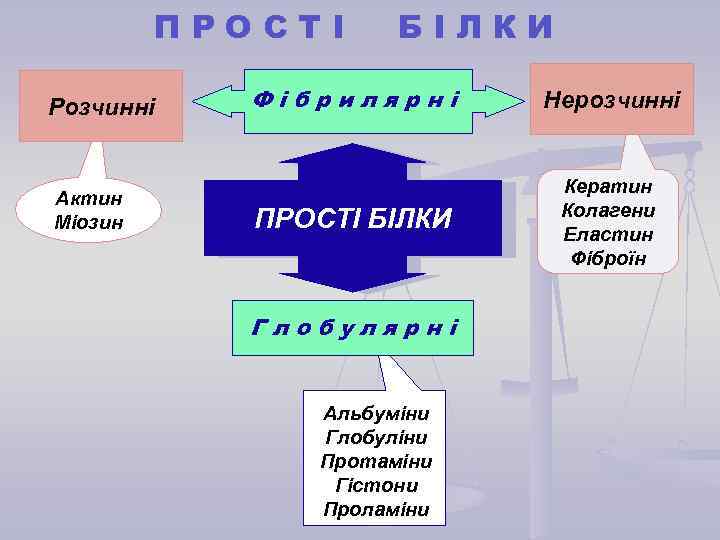
ПРОСТІ Розчинні Актин Міозин БІЛКИ Фібрилярні Нерозчинні ПРОСТІ БІЛКИ Кератин Колагени Еластин Фіброїн Глобулярні Альбуміни Глобуліни Протаміни Гістони Проламіни

ПРОСТІ Глобулярні білки У глобулярних білків поліпептидний ланцюг згорнутий так, що утворюється компактна структура. БІЛКИ Фібрилярні білки – довгі нитковидні молекули, поліпептидні ланцюги яких витягнуті вздовж однієї осі. На рисунку показані три молекули кератину, навиті одна на одну на зразок канату.
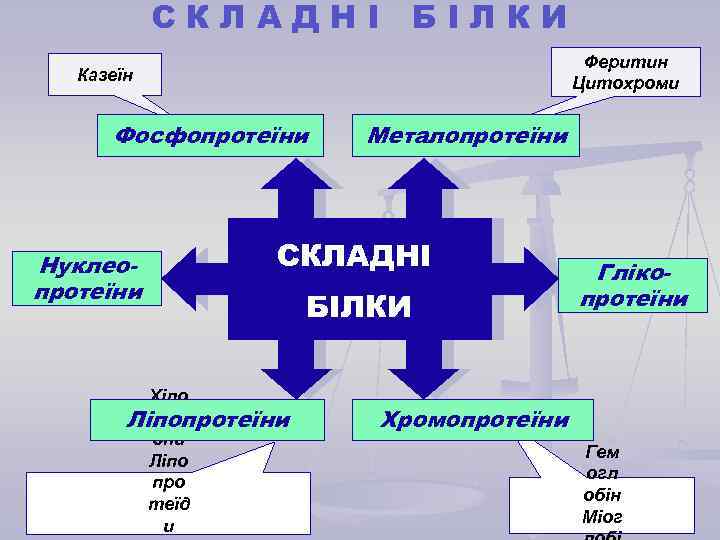
СКЛАДНІ БІЛКИ Феритин Цитохроми Казеїн Фосфопротеїни Нуклеопротеїни Металопротеїни СКЛАДНІ Хіло мікр Ліпопротеїни они Ліпо про теїд и БІЛКИ Глікопротеїни Хромопротеїни Гем огл обін Міог

СКЛАДНІ БІЛКИ Клас Простетична група Приклад Ліпопротеїни Ліпіди 1 -ліпопротеїн крові Глікопротеїни Вуглеводи -глобулін крові Фосфопротеїни Фосфатні групи казеїн молока Гемопротеїни Гем гемоглобін Флавопротеїни Металопротеїни Флавінові нуклеотиди Залізо Цинк сукцинатдегідрогеназа феритин алкогольдегідрогеназа
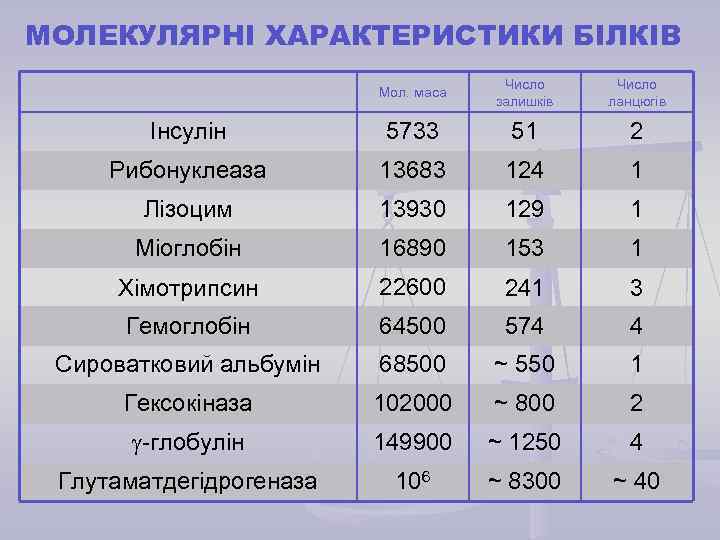
МОЛЕКУЛЯРНІ ХАРАКТЕРИСТИКИ БІЛКІВ Мол. маса Число залишків Число ланцюгів Інсулін 5733 51 2 Рибонуклеаза 13683 124 1 Лізоцим 13930 129 1 Міоглобін 16890 153 1 Хімотрипсин 22600 241 3 Гемоглобін 64500 574 4 Сироватковий альбумін 68500 ~ 550 1 Гексокіназа 102000 ~ 800 2 -глобулін 149900 ~ 1250 4 Глутаматдегідрогеназа 106 ~ 8300 ~ 40
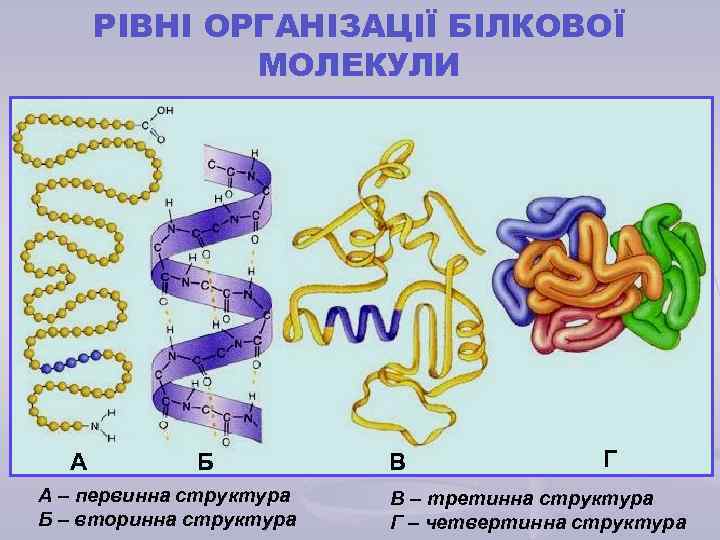
РІВНІ ОРГАНІЗАЦІЇ БІЛКОВОЇ МОЛЕКУЛИ А Б А – первинна структура Б – вторинна структура В Г В – третинна структура Г – четвертинна структура
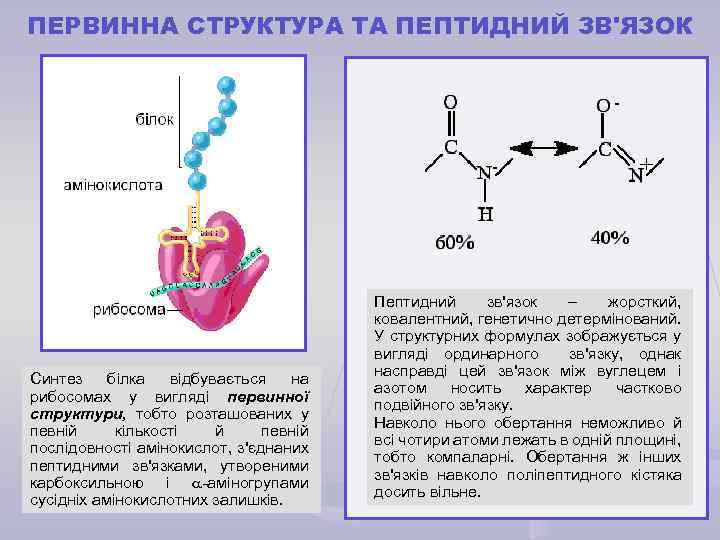
ПЕРВИННА СТРУКТУРА ТА ПЕПТИДНИЙ ЗВ'ЯЗОК Синтез білка відбувається на рибосомах у вигляді первинної структури, тобто розташованих у певній кількості й певній послідовності амінокислот, з'єднаних пептидними зв'язками, утвореними карбоксильною і -аміногрупами сусідніх амінокислотних залишків. Пептидний зв'язок – жорсткий, ковалентний, генетично детермінований. У структурних формулах зображується у вигляді ординарного зв'язку, однак насправді цей зв'язок між вуглецем і азотом носить характер частково подвійного зв'язку. Навколо нього обертання неможливо й всі чотири атоми лежать в одній площині, тобто компаларні. Обертання ж інших зв'язків навколо поліпептидного кістяка досить вільне.
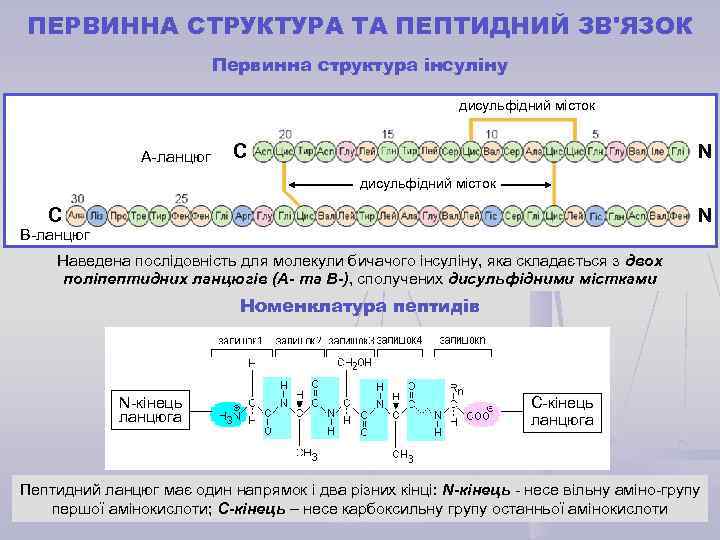
ПЕРВИННА СТРУКТУРА ТА ПЕПТИДНИЙ ЗВ'ЯЗОК Первинна структура інсуліну дисульфідний місток А-ланцюг С N дисульфідний місток С N В-ланцюг Наведена послідовність для молекули бичачого інсуліну, яка складається з двох поліпептидних ланцюгів (А- та В-), сполучених дисульфідними містками Номенклатура пептидів N-кінець ланцюга С-кінець ланцюга Пептидний ланцюг має один напрямок і два різних кінці: N-кінець - несе вільну аміно-групу першої амінокислоти; С-кінець – несе карбоксильну групу останньої амінокислоти
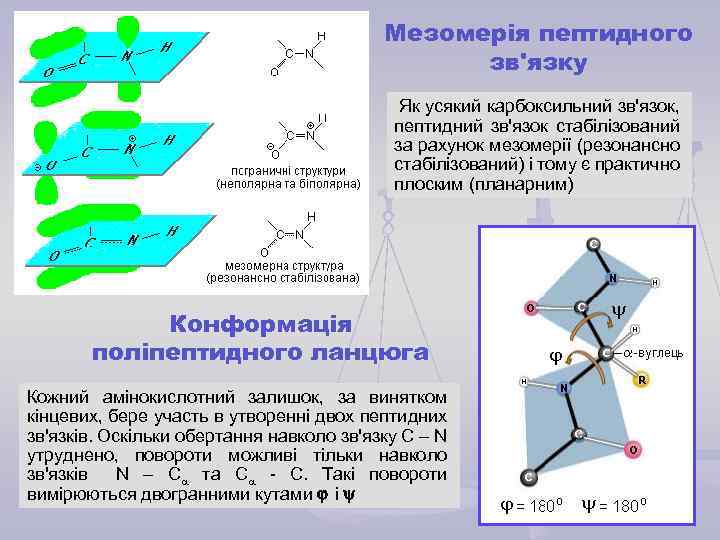
Мезомерія пептидного зв'язку Як усякий карбоксильний зв'язок, пептидний зв'язок стабілізований за рахунок мезомерії (резонансно стабілізований) і тому є практично плоским (планарним) Конформація поліпептидного ланцюга Кожний амінокислотний залишок, за винятком кінцевих, бере участь в утворенні двох пептидних зв'язків. Оскільки обертання навколо зв'язку С – N утруднено, повороти можливі тільки навколо зв'язків N – С та С - С. Такі повороти вимірюються двогранними кутами і
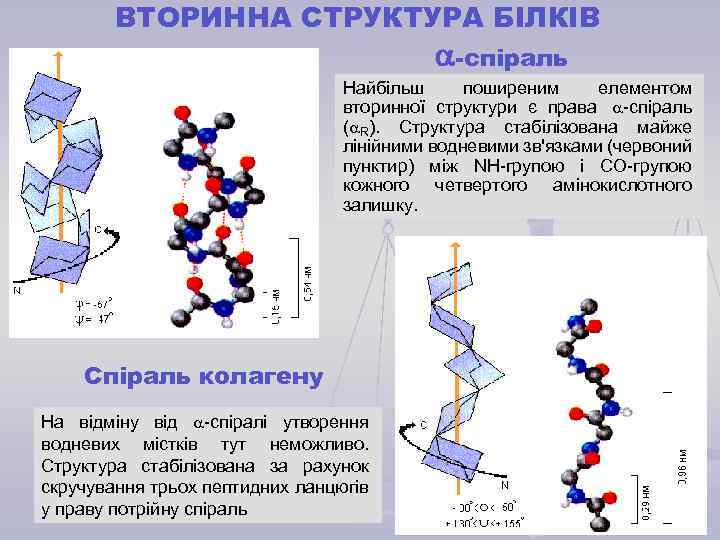
ВТОРИННА СТРУКТУРА БІЛКІВ -спіраль Найбільш поширеним елементом вторинної структури є права -спіраль ( R). Структура стабілізована майже лінійними водневими зв'язками (червоний пунктир) між NН-групою і СО-групою кожного четвертого амінокислотного залишку. Спіраль колагену На відміну від -спіралі утворення водневих містків тут неможливо. Структура стабілізована за рахунок скручування трьох пептидних ланцюгів у праву потрійну спіраль
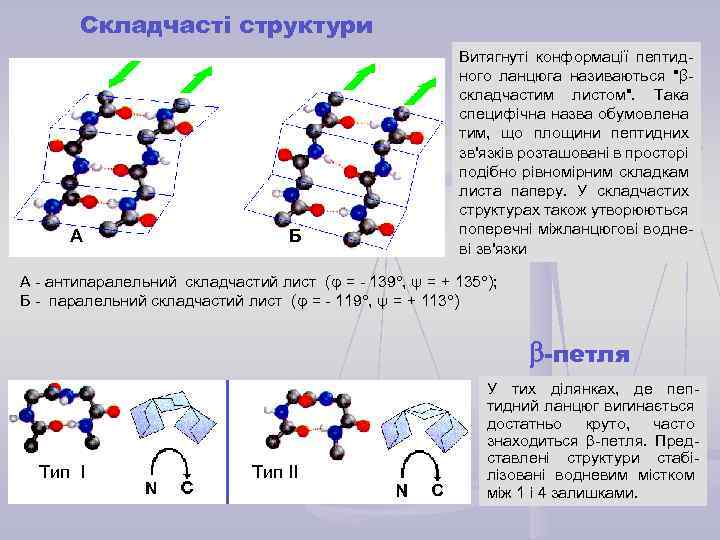
Складчасті структури А Б Витягнуті конформації пептидного ланцюга називаються "βскладчастим листом". Така специфічна назва обумовлена тим, що площини пептидних зв'язків розташовані в просторі подібно рівномірним складкам листа паперу. У складчастих структурах також утворюються поперечні міжланцюгові водневі зв'язки А - антипаралельний складчастий лист (φ = - 139 , ψ = + 135 ); Б - паралельний складчастий лист (φ = - 119 , ψ = + 113 ) -петля Тип ІІ У тих ділянках, де пептидний ланцюг вигинається достатньо круто, часто знаходиться -петля. Представлені структури стабілізовані водневим містком між 1 і 4 залишками.
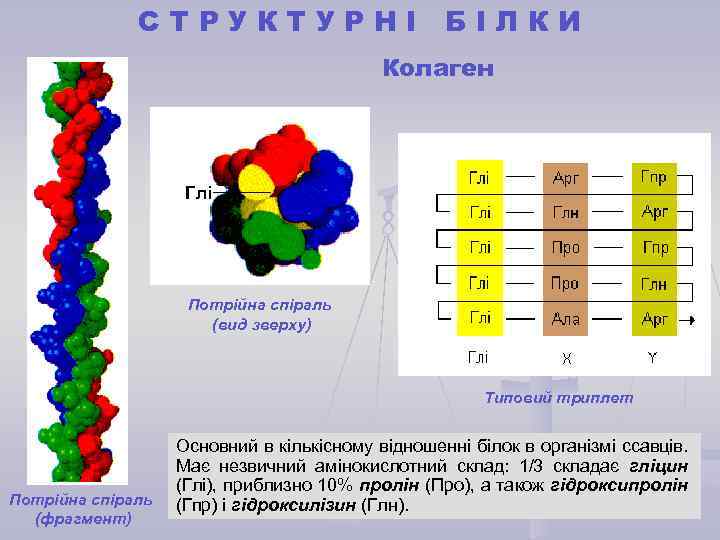
СТРУКТУРНІ БІЛКИ Колаген Глі Потрійна спіраль (вид зверху) Типовий триплет Потрійна спіраль (фрагмент) Основний в кількісному відношенні білок в організмі ссавців. Має незвичний амінокислотний склад: 1/3 складає гліцин (Глі), приблизно 10% пролін (Про), а також гідроксипролін (Гпр) і гідроксилізин (Глн).
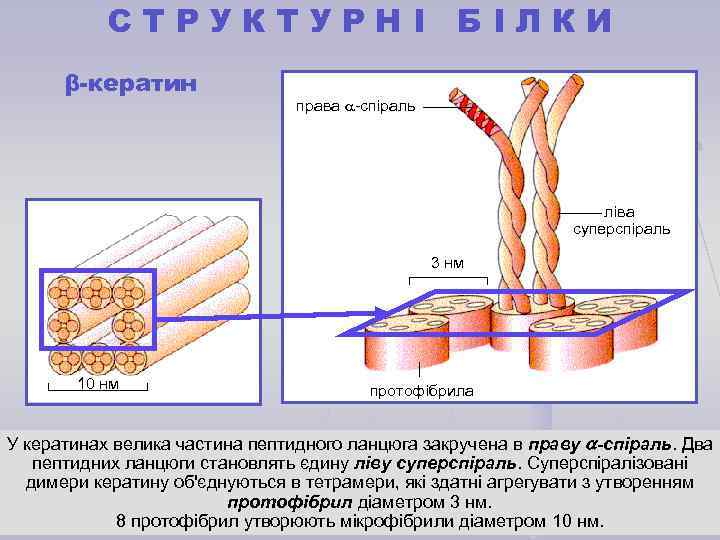
СТРУКТУРНІ БІЛКИ β-кератин права -спіраль ліва суперспіраль 3 нм 10 нм протофібрила У кератинах велика частина пептидного ланцюга закручена в праву -спіраль. Два пептидних ланцюги становлять єдину ліву суперспіраль. Суперспіралізовані димери кератину об'єднуються в тетрамери, які здатні агрегувати з утворенням протофібрил діаметром 3 нм. 8 протофібрил утворюють мікрофібрили діаметром 10 нм.
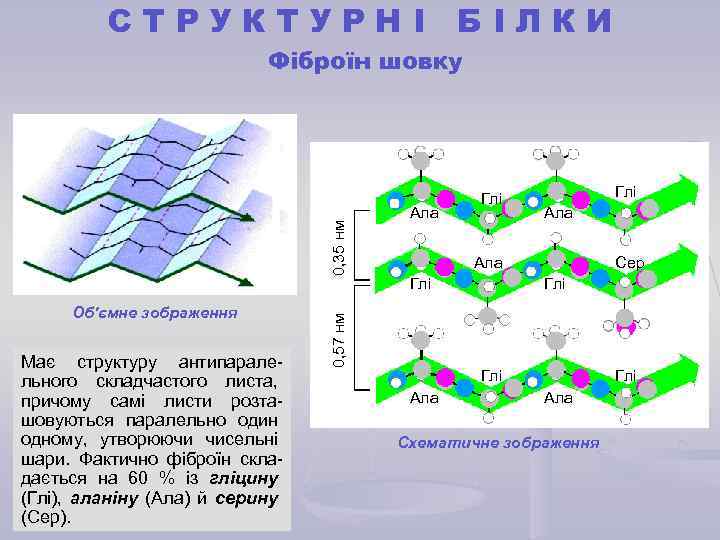
СТРУКТУРНІ БІЛКИ Об'ємне зображення Має структуру антипаралельного складчастого листа, причому самі листи розташовуються паралельно один одному, утворюючи чисельні шари. Фактично фіброїн складається на 60 % із гліцину (Глі), аланіну (Ала) й серину (Сер). Ала Глі 0, 57 нм 0, 35 нм Фіброїн шовку Сер Глі Ала Схематичне зображення
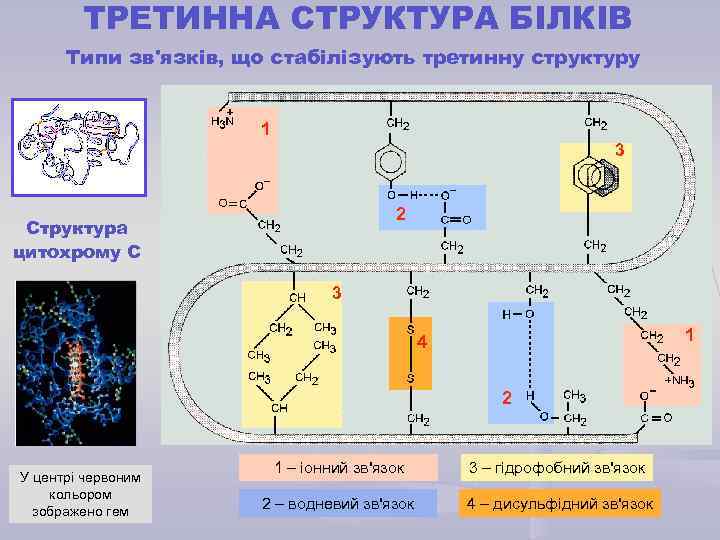
ТРЕТИННА СТРУКТУРА БІЛКІВ Типи зв'язків, що стабілізують третинну структуру 1 3 2 Структура цитохрому С 3 1 4 2 У центрі червоним кольором зображено гем 1 – іонний зв'язок 3 – гідрофобний зв'язок 2 – водневий зв'язок 4 – дисульфідний зв'язок
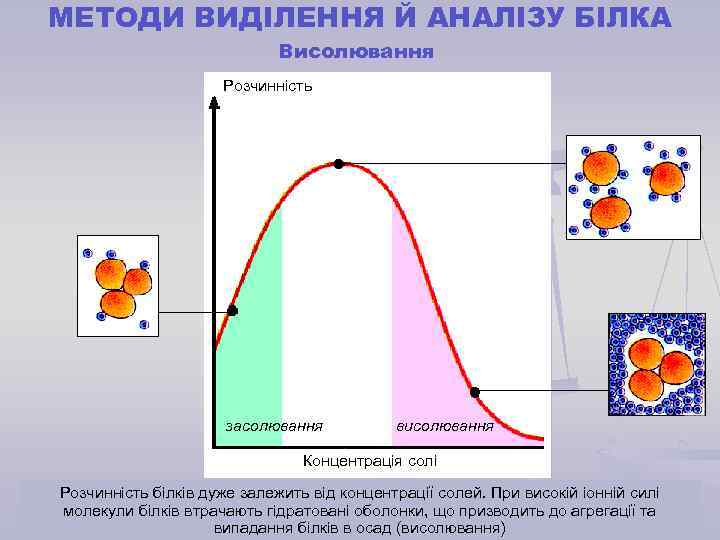
МЕТОДИ ВИДІЛЕННЯ Й АНАЛІЗУ БІЛКА Висолювання Розчинність засолювання висолювання Концентрація солі Розчинність білків дуже залежить від концентрації солей. При високій іонній силі молекули білків втрачають гідратовані оболонки, що призводить до агрегації та випадання білків в осад (висолювання)
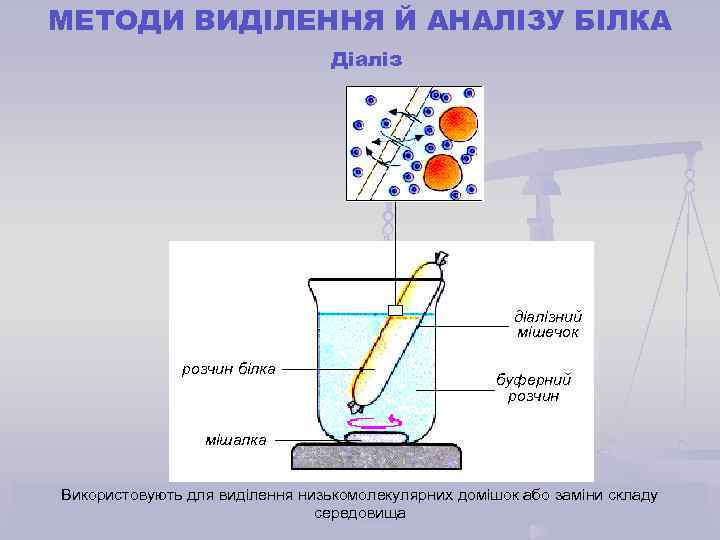
МЕТОДИ ВИДІЛЕННЯ Й АНАЛІЗУ БІЛКА Діаліз діалізний мішечок розчин білка буферний розчин мішалка Використовують для виділення низькомолекулярних домішок або заміни складу середовища
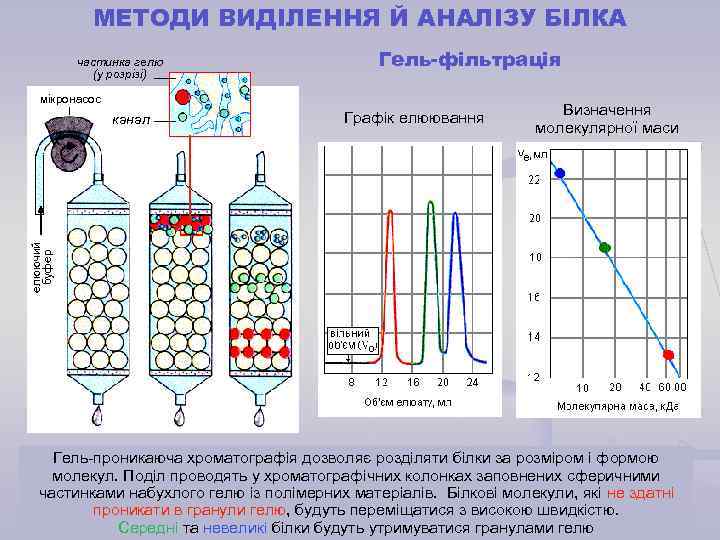
МЕТОДИ ВИДІЛЕННЯ Й АНАЛІЗУ БІЛКА частинка гелю (у розрізі) Гель-фільтрація мікронасос Графік елюювання Визначення молекулярної маси елюючий буфер канал Гель-проникаюча хроматографія дозволяє розділяти білки за розміром і формою молекул. Поділ проводять у хроматографічних колонках заповнених сферичними частинками набухлого гелю із полімерних матеріалів. Білкові молекули, які не здатні проникати в гранули гелю, будуть переміщатися з високою швидкістю. Середні та невеликі білки будуть утримуватися гранулами гелю
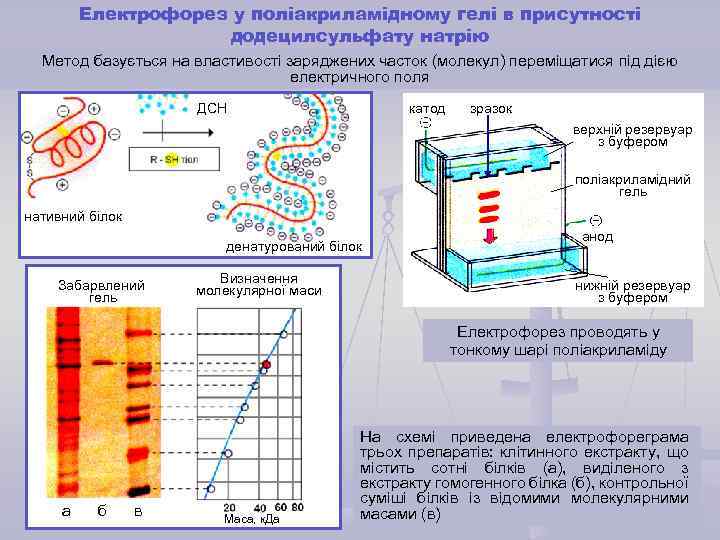
Електрофорез у поліакриламідному гелі в присутності додецилсульфату натрію Метод базується на властивості заряджених часток (молекул) переміщатися під дією електричного поля ДСН катод зразок верхній резервуар з буфером поліакриламідний гель нативний білок денатурований білок Забарвлений гель Визначення молекулярної маси анод нижній резервуар з буфером Електрофорез проводять у тонкому шарі поліакриламіду а б в Маса, к. Да На схемі приведена електрофореграма трьох препаратів: клітинного екстракту, що містить сотні білків (а), виділеного з екстракту гомогенного білка (б), контрольної суміші білків із відомими молекулярними масами (в)
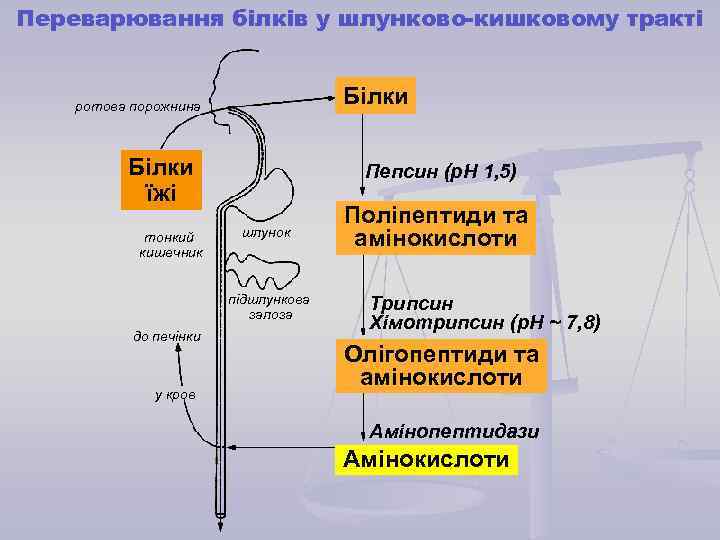
Переварювання білків у шлунково-кишковому тракті Білки ротова порожнина Білки їжі тонкий кишечник Пепсин (р. Н 1, 5) шлунок підшлункова залоза до печінки у кров Поліпептиди та амінокислоти Трипсин Хімотрипсин (р. Н ~ 7, 8) Олігопептиди та амінокислоти Амінопептидази Амінокислоти

БІЛКОВЕ ХАРЧУВАННЯ Білки (амінокислоти) – найважливіший компонент їжі. Середньодобова потреба в білку становить 80 – 100 г. Чим ближче амінокислотний склад білків їжі до складу білка нашого організму, тим він цінніше. М'ясо. Цінний харчовий продукт, високе джерело повноцінних тваринних білків, що містять всі незамінні амінокислоти в значних кількостях і найбільш сприятливих співвідношеннях. Про біологічну цінність м'яса судять в основному по кількості й якості білків, що містяться в ньому. Найбільш багаті білками (до 20 %) яловичина, свинина, а також м'ясо кролика й птахів. Риба. Поряд з м'ясом є одним із кращих джерел високоякісного білка. Білки риби містять всі необхідні організму незамінні амінокислоти. На відміну від м'яса, у білку риби міститься у великій кількості така важлива незамінна амінокислота, як метіонін. Перевагою білків риб також є низький вміст сполучнотканинних утворень. Білки риби засвоюються на 93 – 98 %, у той час як білки м'яса - на 87 - 89%. Куряче яйце. У порівнянні з іншими тваринними продуктами, самий повноцінний білок, що практично повністю засвоюється організмом і містить в оптимальних співвідношеннях всі незамінні амінокислоти. Продукти рослинного походження. Із продуктів рослинного походження повноцінні білки містять соя, квасоля, рис, горох, кукурудза, хліб.
Tema_2_A_bioorgan_khimija.ppt