конференция МС.pptx
- Количество слайдов: 53

БФУ им. И. Канта Медицинский факультет Конференция по патологической физиологии на тему : «Метаболический синдром» Подготовили: студенты 3 курса ЛД ВПО 1 А группы Преподаватель: к. м. н. Кириенкова Елена Витальевна


Что такое метаболический синдром? Синонимы: Синдром Reaven; метаболический синдром Х Определение: увеличение массы висцерального жира, снижение чувствительности периферических тканей к инсулину и гипеинсулинемия, которые вызывают развитие нарушений углеводного, липидного, пуринового обмена и артериальную гипертензию.

Введение Проблема метаболического синдрома Х - одна из важнейших в современной клинике внутренних болезней. Ряд отечественных авторов, уже ставят вопрос о выделении его в самостоятельную нозологическую форму. Широкое внедрение концепции синдрома в практическую деятельность сегодня, безусловно, может привести к снижению заболеваемости и смертности от сердечно-сосудистой патологии в будущем.


Согласно данным ВОЗ: Распространенность МС в индустриальных странах – 10 -20% Распространенность Мс в США – 25% С 1994 по 2000 год частота встречаемости метаболического синдрома среди молодежи возросла с 4, 2 до 6, 4% В общенациональных масштабах количество молодежи с МС = более чем 2 млн. человек

Метаболический синдром Подготовили: Данилов Василий Викторович Степанян Ира Андраниковна

История. Термин «метаболический синдром» стал наиболее употребляемым в медицинской литературе в связи с тем, что использовался авторитетными экспертными группами при публикации клинических рекомендаций и других рабочих документов, в том числе и российскими учеными. История развития представлений о МС: • 1960 -е гг. – Е. Camus выделил метаболический трисиндром (СД, гипертриглицеридемия, подагра). • 1980 г. – M. Henefeld, W. Leonhardt ввели термин «метаболический синдром» • 1988 г. – G. M. Reaven предложил термин «метаболический синдром Х» (ИР, ГИ, нарушение толерантности к глюкозе, дислипопротеинемия, гипертриглицеридемия и АГ) • 1989 г. – N. M. Kaplan охарактеризовал сочетание абдоминального ожирения, нарушение толерантности к глюкозе, АГ и гипертриглицеридемию как смертельный квартет. • 1992 г. – S. M. Haffner предложил термин «синдром инсулинорезистентности» . • 1998 г. – синдром Z- смертельный квартет +синдром апноэ во сне.

Совокупность факторов риска сердечно-сосудистых заболеваний оказался тесно ассоциирован с сахарным диабетом 2 типа (СД 2) и инсулинорезистентностью (ИР), что позволило выдвинуть предположение о существовании единого патофизиологического состояния, которое впоследствии получило название «метаболический синдром» , или «синдрома инсулинорезистентности» .

Впервые данную концепцию сформулировал M. Reaven в 1988 г. Обобщив данные многочисленных исследований, он сделал вывод, что гиперинсулинемия, нарушение толерантности к глюкозе, повышение уровня триглицеридов и понижение уровня липопротеинов высокой плотности (ЛПВП) в плазме крови, а также артериальная гипертония, могут развиваться в результате снижения чувствительности клеток тканей к инсулину. Для обозначения упомянутого симптомокомплекса автор предложил термин "синдром X".

в 1989 г. J. Kaplan, описав смертельный квартет, определил абдоминальное ожирение, наряду с НТГ, АГ и гипертриглицеридемией, в качестве существенной составляющей синдрома, подчеркнув этим, что наличие подобного сочетания существенно повышает смертность населения от сердечнососудистых заболеваний.

1992 г. S. M. Haffner предложил термин "синдром инсулинорезистентности", так как, по его мнению, он хорошо отражает этиологию синдрома. Тем не менее, термин «синдром Х» оказался наиболее удачным для определения данного симптомокомплекса, поскольку до сих пор не известны точные причинно-следственные связи между составляющими его компонентами

Комплекс метаболических, гормональных и клинических нарушений, являющихся факторами риска развития сердечно-сосудистых заболеваний, в основе которых лежит инсулинорезистентность и компенсаторная гиперинсулинемия, в литературе известен под названиями: метаболический трисиндром (Camus J. , 1966) полиметаболический синдром (Avogaro P. , 1965) синдром изобилия (Mehnert A. , 1968) метаболический синдром (Hanefeld М. , 1991) синдром Х (Reaven G. , 1988) смертельный квартет (Kaplan J. , 1989) гормональный метаболический синдром (Bjorntorp Р. , 1991) синдром инсулинорезистентности (Haffner S. , 1992) смертельный секстет (Enzi G. , 1994) метаболический сосудистый синдром (Hanefeld M. , 1997). Чаще других употребляются названия метаболический синдром инсулинорезистентности. В индустриальных странах среди населения старше 30 лет распространенность метаболического синдрома составляет, по данным различных авторов, 10 -20% [12, 13]. Это заболевание чаще встречается у мужчин, у женщин его частота возрастает в менопаузальном периоде.
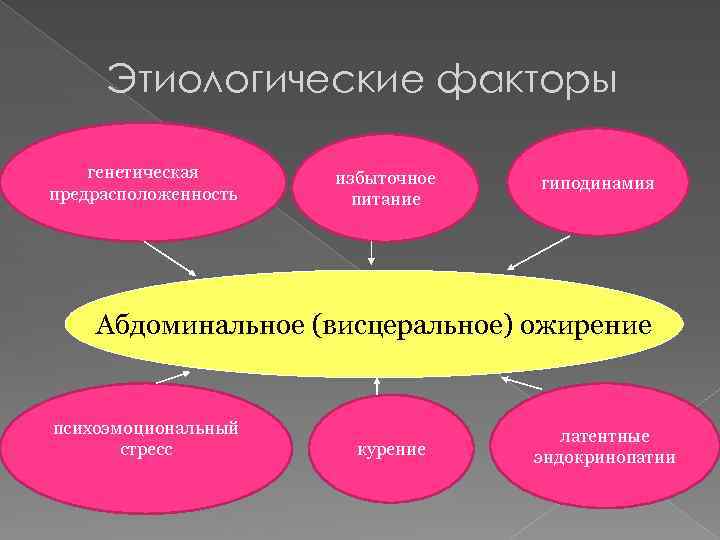
Этиологические факторы генетическая предрасположенность избыточное питание гиподинамия Абдоминальное (висцеральное) ожирение психоэмоциональный стресс курение латентные эндокринопатии
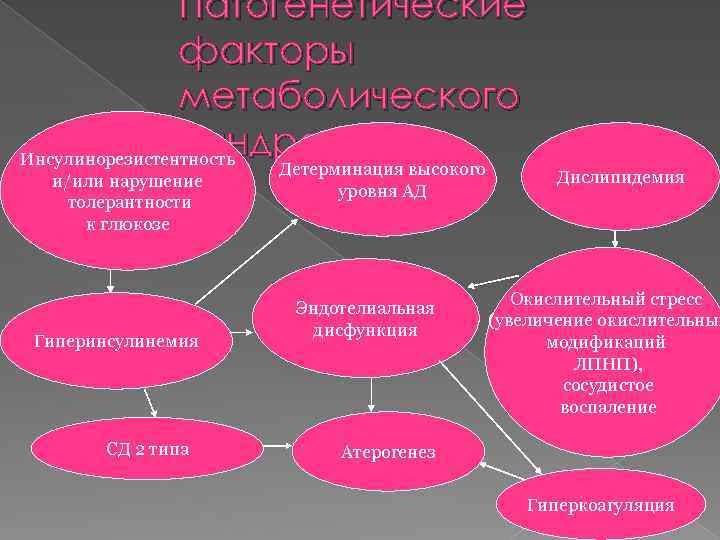
Патогенетические факторы метаболического синдрома Инсулинорезистентность и/или нарушение толерантности к глюкозе Гиперинсулинемия СД 2 типа Детерминация высокого уровня АД Эндотелиальная дисфункция Дислипидемия Окислительный стресс (увеличение окислительных модификаций ЛПНП), сосудистое воспаление Атерогенез Гиперкоагуляция

Представленные сложные взаимосвязи патогенетических факторов, участвующих в механизме нарушений регуляции углеводного и жирового обмена при СД 2 типа, позволили Г. Ревену в 1988 г. Сформулировать концепцию метаболического синдрома, основными компонентами которого является ИР тканей и гиперинсулинемия, нарушение толерантности к глюкозе и развитие СД 2 типа, абдоминальное ожирение, дислипидемия, артериальная гипертензия атеросклероз.

Исследования последних лет расширили компоненты метаболического синдрома, добавив к ним гиперурикемию, гомоцистеинемию, гиперандрогению у женщин, нарушения гомеостаза ( увеличение содержания в крови ингибитора активатора плазминогена, гиперфибриногенемия). Наиболее часто в литературе используется термин «метаболический синдром» , хотя прилагательное «дисметаболический» более точно отражает сущность патогенеза этого синдрома.
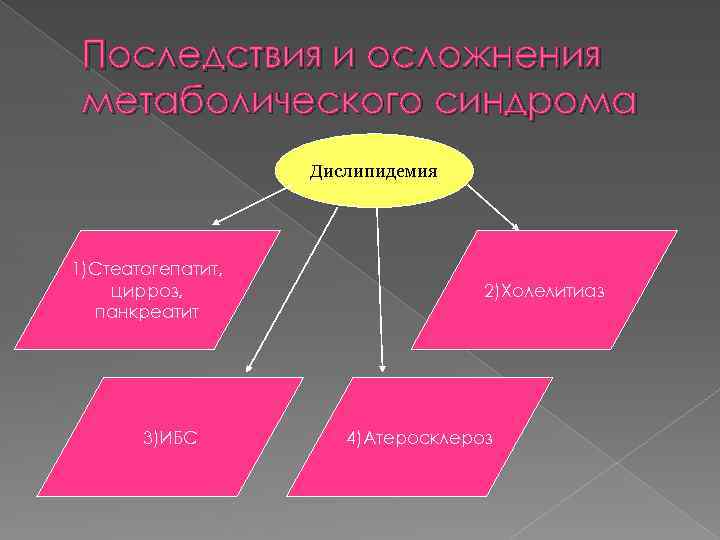
Последствия и осложнения метаболического синдрома Дислипидемия 1)Стеатогепатит, цирроз, панкреатит 3)ИБС 2)Холелитиаз 4)Атеросклероз

Нарушения углеводного обмена при МС Подготовили: Шарохина Таисия Андреевна Ментуз Алина Александровна

В основе нарушений: Инсулинорезистентность Гиперинсулинемия Нарушение толерантности к глюкозе

Инсулинорезистентность может быть обусловлена генетическими нарушениями влиянием внешних факторов (ожирение, стрессы) понижение объемного кровотока в капиллярах скелетной мускулатуры

3 уровня инсулинорезистентности § 1. 2. 3. 4. § § ИР (рецепторная) на уровне печени и в результате: ↓ транспорт глюкозы в гепатоциты из-за нарушения глюкокиназного механизма, что приводит к гипергликемии, снижается экстракция инсулина гепатоцитами (инсулин становится недоступным для действия инсулиназы гепатоцитов), и развивается системная гиперинсулинемия. СЖК подавляют тормозящее действие инсулина на глюконеогенез и гликогенолиз, увеличивая продукцию глюкозы печенью – к гипергликемии. Далее гипергликемия усиливает ГИ, активируется метаболизм Хм и ЛПОНП в крови и ↑ СЖК, а они → ИР (рецепторная) на уровне мышечной ткани, так как СЖК в мышечной ткани конкурируют с глюкозой и обусловливают ИР, усугубляя гипергликемию. Длительная гипергликемия и гиперинсулинемия, хроническое повышение СЖК приводит к нарушению механизма узнавания глюкозы -клетками поджелудочной железы и возникает ИР (пострецепторная) на уровне -клеток. При наличии инсулинорезистентности B-клетки островкового аппарата поджелудочной железы увеличивают синтез и секрецию инсулина, чтобы компенсировать нарушение чувствительности к нему и сохранить нормальную толерантность к глюкозе, что приводит к развитию. гиперинcvлинемии
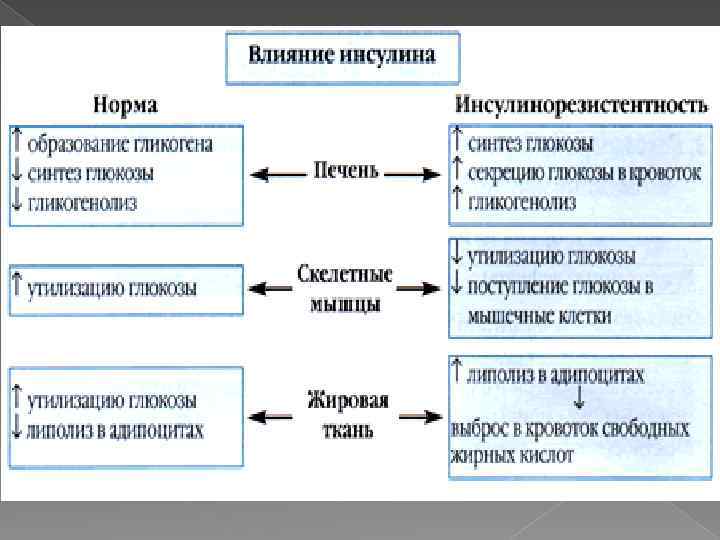

Гиперинсулинемия вызывает: парадоксальную вазоконстрикцию ↑ ОЦК АГ элиминация ЛПОНП замедляется, ↓ ЛПВП, ↑ катаболизм ЛПВП = атерогенная дислипидемия ↑ развитие атеросклероза ↑ активность рецепторов ЛПНП и синтез эндогенного холестерина в клетках сосудистой стенки. гиперфибриногенемию и ↑ активности ингибитора тканевого активатора плазминогена I типа = развитие гиперкоагуляции. Таким образом, гиперинсулинемия, являясь компенсаторной ответной реакцией, поддерживающей нормальный транспорт глюкозы в клетки одновременно является патологической, т. к. приводит к развитию дислипидемии, артериальной гипертонии, атеросклероза и его осложнений –ИБС и инфаркта миокарда.
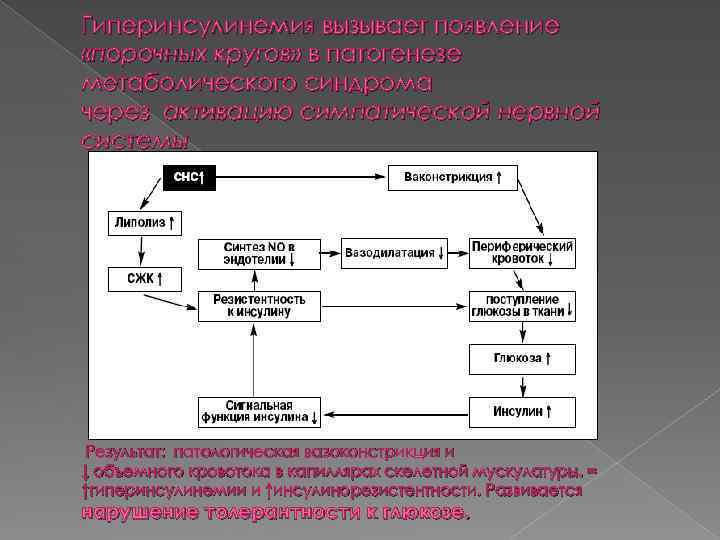
Гиперинсулинемия вызывает появление «порочных кругов» в патогенезе метаболического синдрома через активацию симпатической нервной системы Результат: патологическая вазоконстрикция и ↓ объемного кровотока в капиллярах скелетной мускулатуры. = ↑гиперинсулинемии и ↑инсулинорезистентности. Развивается нарушение толерантности к глюкозе.

Критерии нарушения углеводного обмена Гипергликемия (норма 3, 3 -5, 5 ммоль/л) Глюкозурия (почечный порог – 8, 89, 9 ммоль/л) Кетонурия Гликированный гемоглобин ( норма – 3 -6% всего гемоглобина) С-пептид (норма - соотношение С-пептид/инсулин составляет 3: 1)
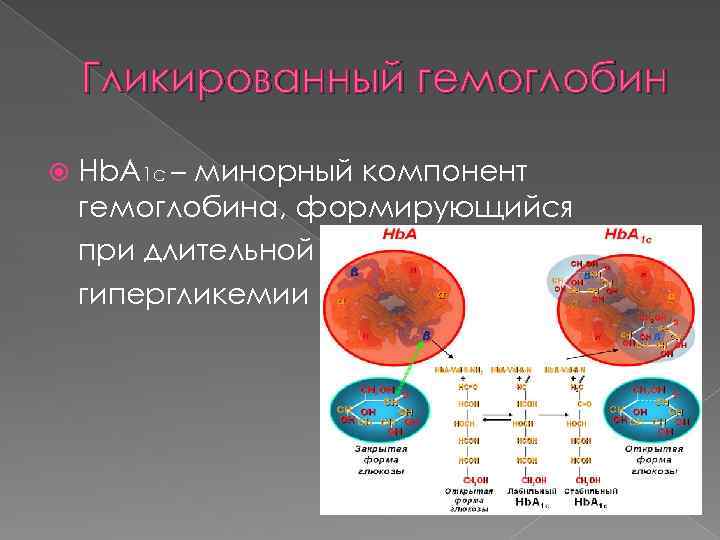
Гликированный гемоглобин Hb. A 1 c – минорный компонент гемоглобина, формирующийся при длительной гипергликемии
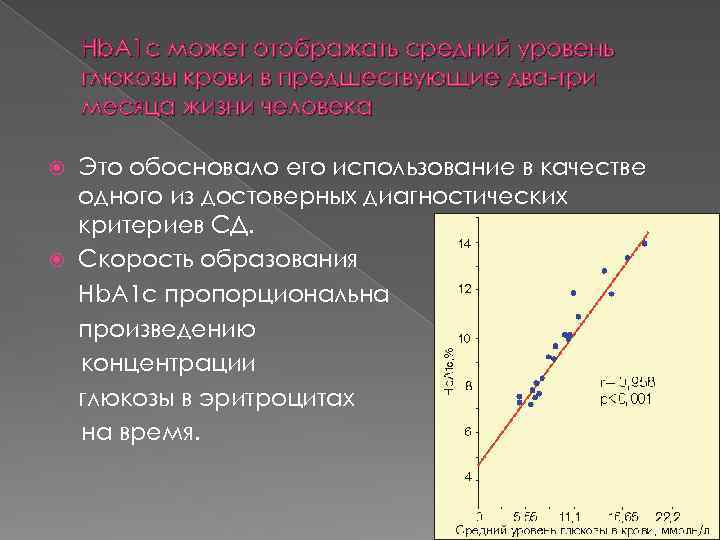
Hb. A 1 с может отображать средний уровень глюкозы крови в предшествующие два-три месяца жизни человека Это обосновало его использование в качестве одного из достоверных диагностических критериев СД. Скорость образования Hb. A 1 с пропорциональна произведению концентрации глюкозы в эритроцитах на время.
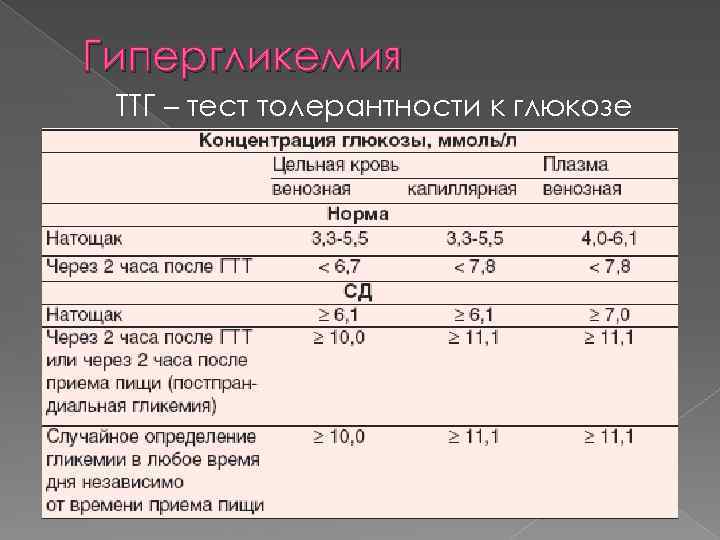
Гипергликемия ТТГ – тест толерантности к глюкозе

Нарушения липидного обмена при метаболическом синдроме Выполнили: Синёва Надежда Сергеевна Бординовская Ольга Игоревна
Виды ожирения Алиментарное ожирение Ожирение, вследствие психических расстройств, неправильного подхода к питанию и малоподвижному образу жизни. Симптоматическое ожирение Этот вид ожирения является сопутствующей иным физиологическим расстройствам, болезнью. Это может быть диабет, гормональные нарушения, заболевания желез внутренней секреции или же нарушения обмена веществ.

Обратите внимание на фигуру вашего пациента В зависимости от мест преимущественного избыточного накопления жировой ткани выделяют: Андроидное ожирение чаще встречается у мужчин и хар-ся накоплением жира в области туловища (живот, подмышечные области), а также в сальнике (анатомическая структура, располагающаяся в брюшной полости) в виде так называемого внутреннего жира. Гиноидное ожирение присуще преимущественно женщинам и проявляется избыточным накоплением жира под кожей нижней части живота и бедер. Смешанный тип ожирения, или промежуточный тип ожирения характеризуется равномерным распределением жира по всему телу.

Предрасполагающие факторы ожирения Малоподвижный образ жизни Генетические факторы, в частности: › ↑ активность ферментов липогенеза › ↓ активности ферментов липолиза Повышенное потребление легкоусваиваемых УВ: › питьё сладких напитков › диета, богатая сахарами Некоторые болезни, в частности эндокринные заболевания (гипогонадизм, гипотиреоз, инсулинома) Нарушения питания (например, binge eating disorder), в русской литературе называемое нарушения пищевого поведения — психологическое нарушение, приводящее к расстройству приёма пищи Склонность к стрессам Недосыпание Психотропные препараты
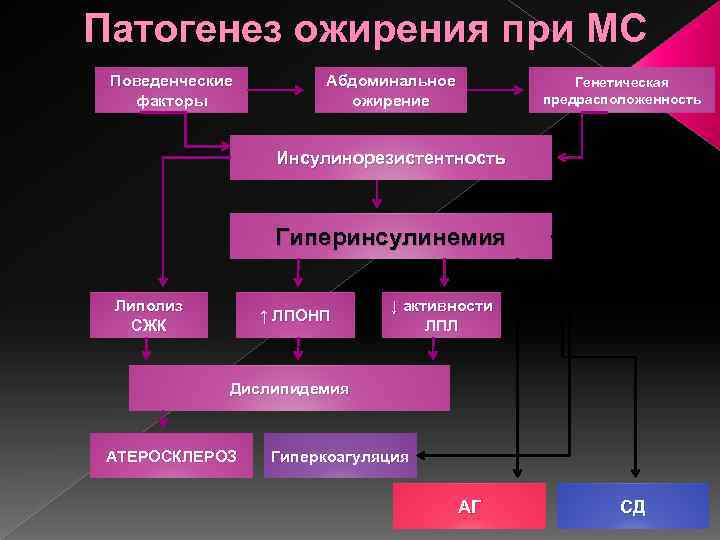
Патогенез ожирения при МС Поведенческие факторы Абдоминальное ожирение Генетическая предрасположенность Инсулинорезистентность Гиперинсулинемия Липолиз СЖК ↑ ЛПОНП ↓ активности ЛПЛ Дислипидемия АТЕРОСКЛЕРОЗ Гиперкоагуляция АГ СД

Некоторые данные, указывают на то, что сновополагающим в развитии МС яв-ся нергетический дисбаланс, когда энергия отребления › энергии расхода. Из внешних акторов к такому дисбалансу приводит алоподвижный образ жизни, ерациональное питание и алообразованность пациентов. Пищевое поведение контр-ся Пищ. Ц ентролат и медиальными ядрами гипоталамуса. Поэтому нарушение ейргуморальной регуляции, проявяющейся в развитии дисбаланса адипокинов и ейротрансмиттеров или в нарушении чув-ти ПЦ к сигналам ищевого насыщения, приводят к нарушению жирового обмена. ажная роль в регуляции ЖО - серотонин. Показано, что при ↑ его ровня в гипоталамусе возникает чувство сытости и потребление ищи ↓, а при ↓ – наоборот ↑. Часто депрессия сопровождается ↓ мозгового серотонина и ↑ чувства голода. Существует гипотеза, то переедание, ведущее к развитию ожирения, может быть ледствием скрытой депрессии. Благодаря питанию, уровень мозгового серотонина ↑ и настроение улучшается.

Клиника и диагностика ожирения при МС Критерий Объём талии Мужчины > 102 см Женщины > 88 см Сахар крови Уровень ТАГов > 6, 1 ммоль/л > 1. 7 ммоль/л >1, 0 ммоль/л > 6, 1 ммоль/л > 1. 7 ммоль/л >1. 3 ммоль/л > 3, 1 ммоль/л Уровень ЛПВП Уровень ЛПНП
Лечение ожирения при МС Медикаментозное Немедикаментозное

Немедикаментозное лечение Немедикаментозные методы лечения - диетотерапия и физнагрузки (↑ физ. акт-ти) имеют самостоятельное значение на 1 этапе лечения МС и являются обязательным фоном приеме ЛС на 2 этапе лечения. Т. к. это комплекс нарушений обмена веществ и заболеваний, то немедикаментозное лечение основано на объединении тех подходов, которые применяются при лечении СД 2 -го типа, ожирения, АГ и т. д. Это важно! ↓ массы тела должно быть постепенным. Быстрый и резкий «сброс» массы тела на 10 -20 кг приводит к ↓ содержания в организме гормона лептина вследствие резкого похудения (лептин образуется в жировой ткани). Это, в свою очередь, приводит к компенсаторному, трудно преодолимому чувству голода и ↑ потребления пищи, и, в результате, - к возврату лишних килограммов, иногда даже в > количестве, чем до диеты.

Лекарственное лечение МС Если с помощью немедикаментозного лечения не удалось достичь успеха, надо дополнить диету и физические нагрузки ЛС, которые способны ↑ чув-ть тканей к инсулину (↓ резистентность к инсулину), ↓ его содержание в крови при гиперинсулинемии, улучшить углеводный и липидный обмен. Безусловно, необходима лекарственная терапия АГ на фоне МС. Целесообразен также прием ЛС, которые способствуют ↓ массы тела при ожирении, если немедикаментозные методы его лечения оказались малоэффективными.

Артериальная гипертензия и метаболический синдром Подготовил: Студент 3 курса Лангольф С. С.

Введение Артериальная гипертония и резистентность тканей к инсулину – наиболее важные компоненты метаболического синдрома. АГ часто является одним из первых клинических проявлений МС. В основе патогенеза АГ при МС лежит ИР и вызванная ею компенсаторная ГИ в сочетании с сопутствующими метаболическими нарушениями. В клинической практике сочетание артериальной гипертонии и инсулинорезистентности встречается гораздо чаще, чем это могло бы наблюдаться, исходя из распространенности каждого из факторов в отдельности. Так, артериальная гипертония выявляется у больных сахарным диабетом 2 типа в два раза чаще, чем у лиц без сахарного диабета. По данным литературы, среди больных с метаболическим синдромом смертность от ИБС в 23 выше, чем в общей популяции. Анализ распространенности этих заболеваний показывает, что взаимосвязь сахарного диабета и артериальной гипертонии не зависит от возраста или массы тела больного. Инсулиновая резистентность способствует повышению артериального давления, влияя на ряд патогенетических механизмов артериальной гипертензии.
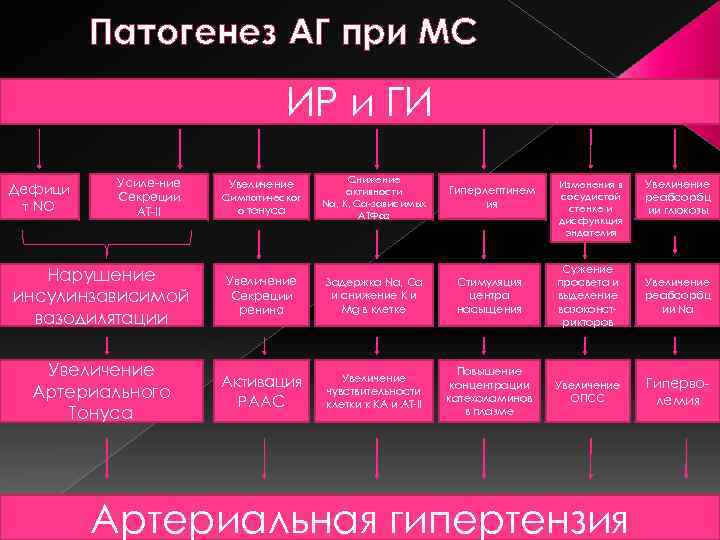
Патогенез АГ при МС ИР и ГИ Симпатическог о тонуса Снижение активности Na, K, Ca-зависимых АТФаз Гиперлептинем ия Нарушение инсулинзависимой вазодилятации Увеличение Секреции ренина Задержка Na, Ca и снижение K и Mg в клетке Стимуляция центра насыщения Сужение просвета и выделение вазоконстрикторов Увеличение реабсорбц ии Na Увеличение Артериального Тонуса Активация РААС Увеличение чувствительности клетки к КА и АТ-II Повышение концентрации катехоламинов в плазме Увеличение ОПСС Гиперволемия Дефици т NO Усиле-ние Секреции АТ-II Увеличение Изменения в сосудистой стенке и дисфункция эндотелия Артериальная гипертензия Увеличение реабсорбц ии глюкозы

1) 2) 3) Нарушенная инсулинзависимая вазодилятация Инсулин является прямым вазодилатирующим агентом, поэтому ИР сама по себе способствует повышению ОПСС. Инсулининдуцируемая вазодилатация является полностью NO– зависимой. Определенный вклад в генез и становление АГ при МС вносит дисфункция эндотелия сосудов. Одним из основных биохимических маркеров дисфункции эндотелия является дефицит оксида азота – NO (либо недостаточная его продукция, либо его инактивация). При АГ к дефициту NO может привести образование избыточного количества свободных радикалов и деградация брадикинина. Поскольку биохимические изменения, лежащие в основе дефицита NO и дисфункции эндотелия, ведут к атеротромбозу, их также можно отнести к метаболическим нарушениям. Синтез NO в сосудистой стенке также оказывает сдерживающее влияние на пролиферацию гладкомышечных клеток, тормозит адгезию моноцитов к эндотелию сосудистой стенки, снижает перекисное окисление липидов, т. е. предохраняет стенки сосудов от повреждения. Поэтому развивающаяся дисфункция эндотелия способствовует ускорению развития атеросклеротических повреждений сосудов, что и подтверждено многочисленными исследованиями.

4) В норме инсулин подавляет стимулирующий эффект гипергликемии на экспрессию гена ангиотензиногена (AT) в клетках проксимальных канальцев почек и препятствует увеличению секреции AT. При ИР подавление инсулином глюкозостимулируемой экспрессии гена AT в клетках проксимальных канальцев почек не происходит, экспрессия гена растормаживается и секреция AT усиливается. По– видимому, именно этот механизм лежит в основе обнаруженного увеличения продукции AT–II в клубочковых и канальцевых клетках почечной ткани под влиянием гипергликемии.

Увеличенный симпатический тонус 1) 2) Ренальная гиперсимпатикотония, являясь характерной особенностью инсулининдуцированной артериальной гипертензии, возникает, как последствие ГИ стимуляции центральных механизмов СНС и как результат увеличения выделения НА в симпатических синапсах почек вследствие активизации почечной тканевой ренин–ангиотензинальдостероновой системы (РААС) в условиях ИР. Гиперсимпатикотония усиливает секрецию ренина в почках. Повышение ренина активизирует РААС. Увеличение концентрации AT–II воздействует на рецепторы резистивных сосудов и на AT–I рецепторы в нейромышечных синапсах скелетной мускулатуры. В результате возникает подъем АД, что приводит к ухудшению кровотока скелетных мышц и понижению транспорта глюкозы в мышцах, к дальнейшему нарастанию показателей ИР и компенсаторной ГИ.

Блокирование трансмембранных ионообменных механизмов Снижается активность трансмембранного фермента Na+, K+ и Са 2+ – зависимой АТФазы), тем самым повышается содержание Na + и Са 2+ и уменьшается содержание К+, Mg 2+, снижается р. Н внутри клетки, в том числе и в гладких миоцитах. Это приводит к увеличению чувствительности сосудистой стенки к прессорным воздействиям катехоламинов, AT–II и , следовательно, повышению АД, в результате увеличения ОПСС.

Влияние гиперлептинемии АГ при ожирении и ИР может быть связана с гиперлептинемией. Лептин – гормон, синтезируемый адипоцитами висцеральной жировой ткани. Концентрация лептина в плазме прямо пропорциональна степени ожирения. Уровень лептина тесно коррелирует с индексом массы тела (ИМТ), артериальным давлением (АД), концентрацией АТ–II и норадреналина. Установлено также, что лептин стимулирует NO-опосредованную вазодилатацию. В эксперименте установлено, что инфузия данного пептида обусловливает увеличение содержания NO в плазме крови, а последующее блокирование синтеза NO на фоне введения лептина приводит к значительному повышению АД. Следовательно, увеличение синтеза оксида азота может противодействовать гипертензивному эффекту лептининдуцированной симпатической стимуляции. Инсулин и лептин регулируют чувство насыщения на уровне дугообразного и паравентрикулярного ядер гипоталамуса, стимуляция которых приводит к активации ряда симпатических нервов (почечных, надпочечниковых и висцеральных) и повышению концентрации катехоламинов в плазме.

Изменения сосудистой стенки при МС 1) 2) 3) Отложение липидов в сосудистой стенке приводит к дисфункции эндотелия. На фоне гиперинсулинемии повышается продукция эндотелием вазоконстрикторных веществ, в частности, эндотелина-1, тромбоксана А 2, снижается образование оксида азота и простациклина, оказывающих вазодилатирующие эффекты. В менопаузальном периоде, вне зависимости от наличия инсулиновой резистентности, наблюдается увеличение уровня в крови эндотелина-1. Это объясняется тем, что в менопаузу снижается образования эстрадиола, который блокирует синтез эндотелина. Эндотелин является сильным вазоконстриктором и при длительном повышении уровня в крови увеличивает реабсорбцию натрия в почках. Дополнительно к этому, эндотелин усиливает оксидативный стресс, что также способствует повышению АД. Инсулин стимулирует пролиферацию гладкомышечных клеток сосудистой стенки, влекущее за собой сужение артериол и увеличение сосудистого сопротивления.
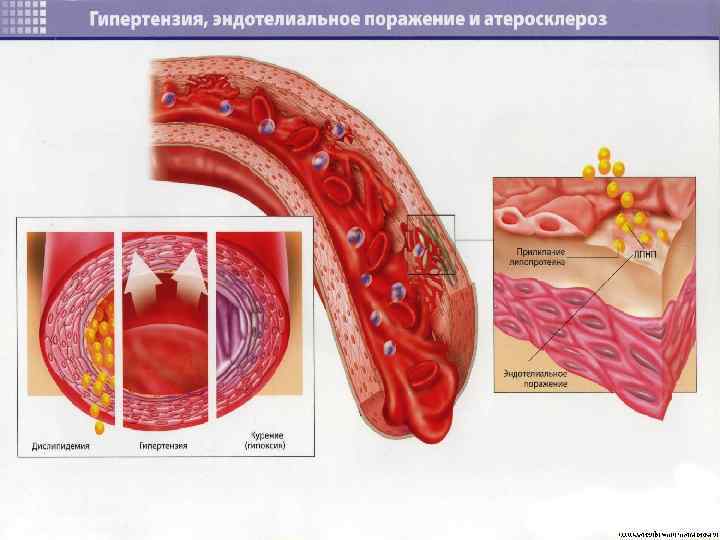

Гиперволемия при МС Увеличение фильтрации глюкозы клубочками почек приводит к усилению обратного всасывания глюкозы вместе с натрием в проксимальных и дистальных канальцах нефрона. Это, в свою очередь, приводит к увеличению ОЦК, и следовательно к увеличению артериального давления. Это приводит к гиперволемии и повышению содержания натрия и кальция в стенках сосудов, вызывая спазм последних и повышение общего периферического сосудистого сопротивления (ОПСС).
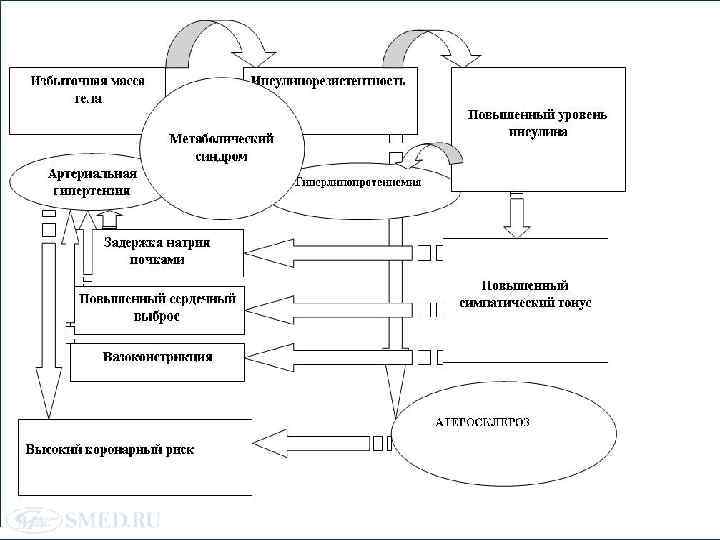

ВЫВОД Согласно приведенной схеме основная триггерная роль в развитии синдрома АГ отводится ГИ и ИР. Допускается, что у разных больных ГИ и ИР, являясь первичными метаболическими эффектами, могут вызвать развитие АГ разными путями или их сочетанием. В одних случаях может преобладать задержка натрия и воды, а в других – усиление сердечного выброса и повышение ОПСС. Один и тот же механизм развития АГ может быть обусловлен разными причинами. Так, например, задержка натрия может быть вызвана как прямым действием инсулина, так и опосредовано, через активацию симпатоадреналовой системы и РААС. И, если в последнем случае активность ренина плазмы будет повышена, то в других, где ведущим является механизм непосредственной задержки натрия под действием инсулина, активность ренина плазмы может быть компенсаторно снижена. Это может служить основой для объяснения противоречивости полученных ранее данных о роли того или иного фактора (катехоламины, РААС, альдостерон) в повышении АД при ГИ. С точки зрения гипотезы о первичной роли ГИ и ИР в развитии АГ популяция больных АГ гетерогенна, но эта гетерогенность заключается не в причине АГ, а в путях реализации этой причины.

Благодарим Вас за внимание!
конференция МС.pptx