06_Lecture_Proteins in acton_2011.ppt
- Количество слайдов: 44
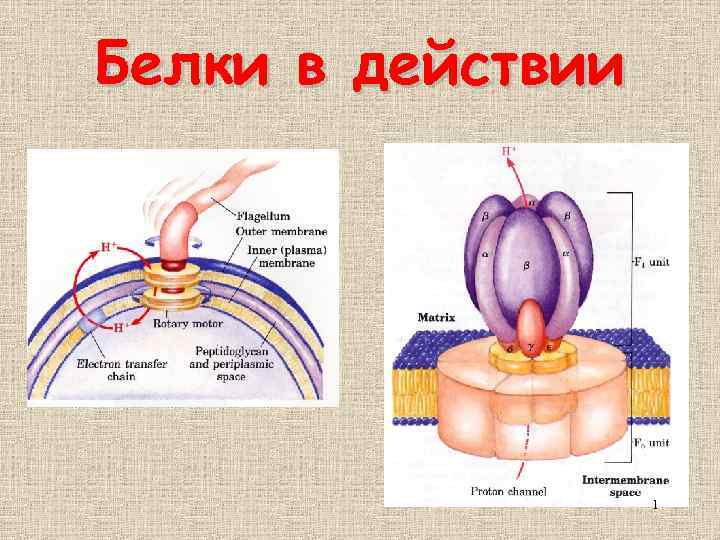
Белки в действии 1
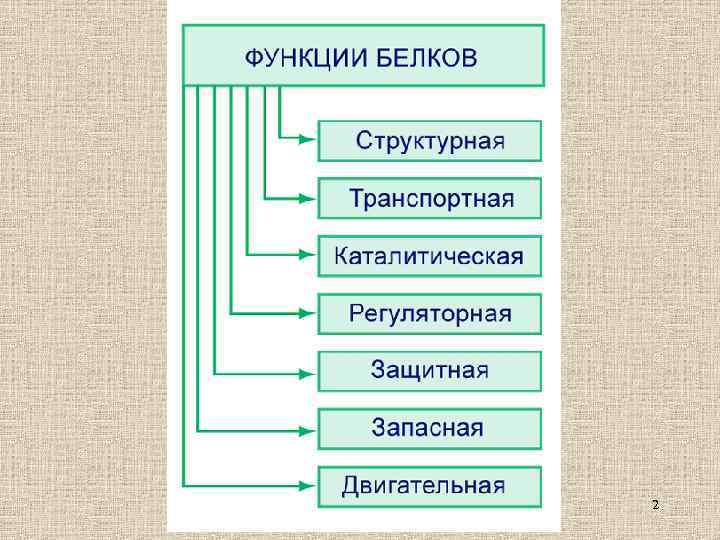
2

Структурная (строительная) Белки входят в состав всех клеточных органелл, цитоплазмы, мембран и межклеточного вещества: коллаген, белки плазмы крови 3
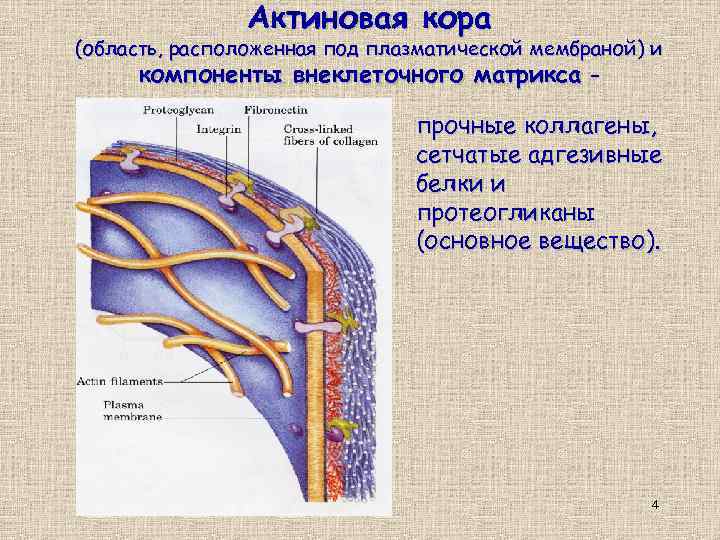
Актиновая кора (область, расположенная под плазматической мембраной) и компоненты внеклеточного матрикса – прочные коллагены, сетчатые адгезивные белки и протеогликаны (основное вещество). 4
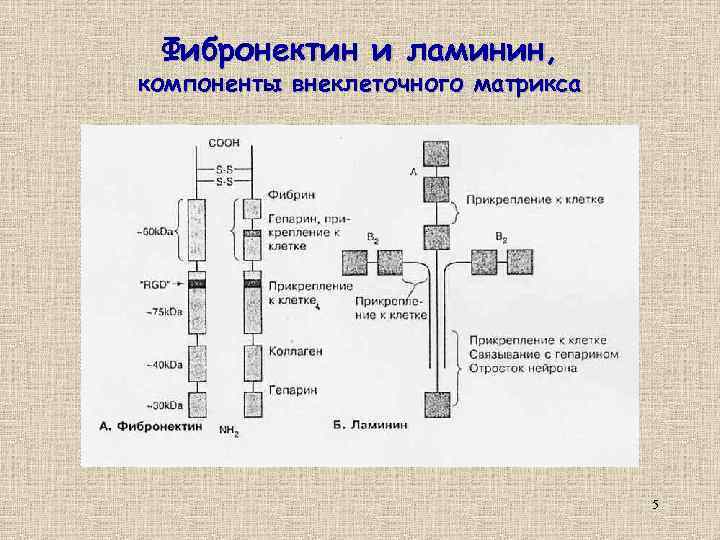
Фибронектин и ламинин, компоненты внеклеточного матрикса 5
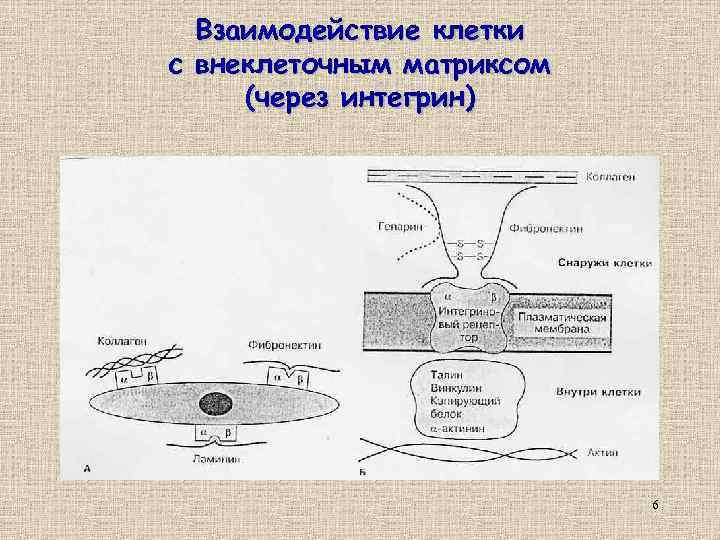
Взаимодействие клетки с внеклеточным матриксом (через интегрин) 6
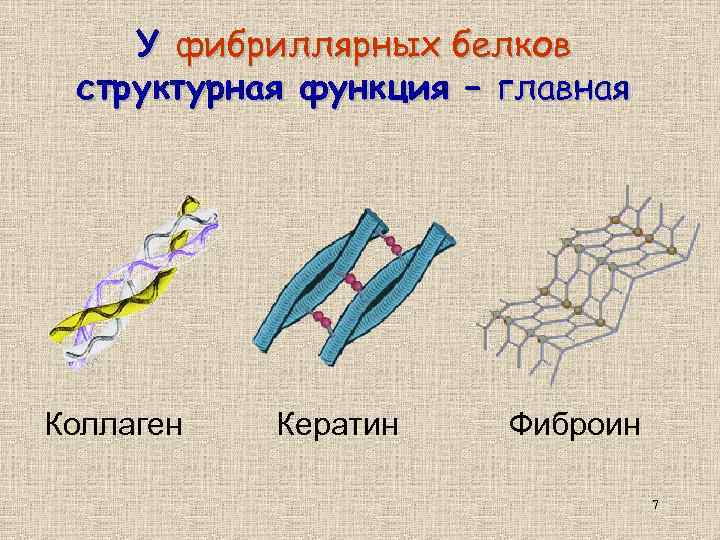
У фибриллярных белков структурная функция – главная Коллаген Кератин Фиброин 7
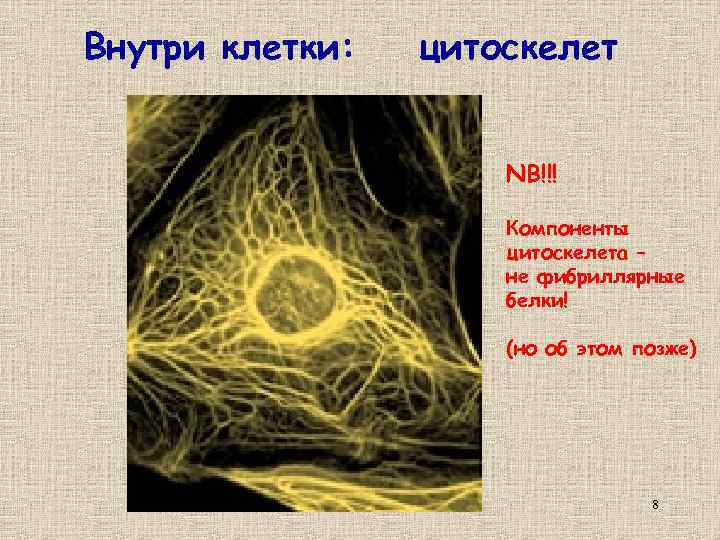
Внутри клетки: цитоскелет NB!!! Компоненты цитоскелета – не фибриллярные белки! (но об этом позже) 8

Вне клетки: кератин Прямой волос Курчавый 9

Фиброин – белок шелка и паутины 10
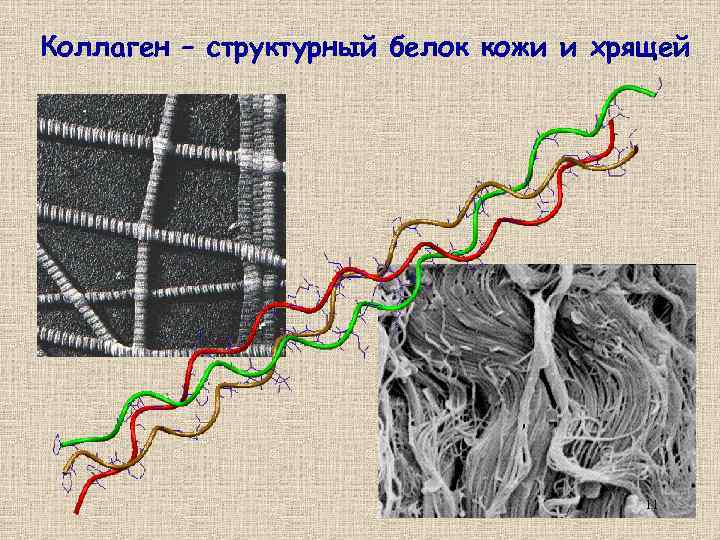
Коллаген – структурный белок кожи и хрящей 11
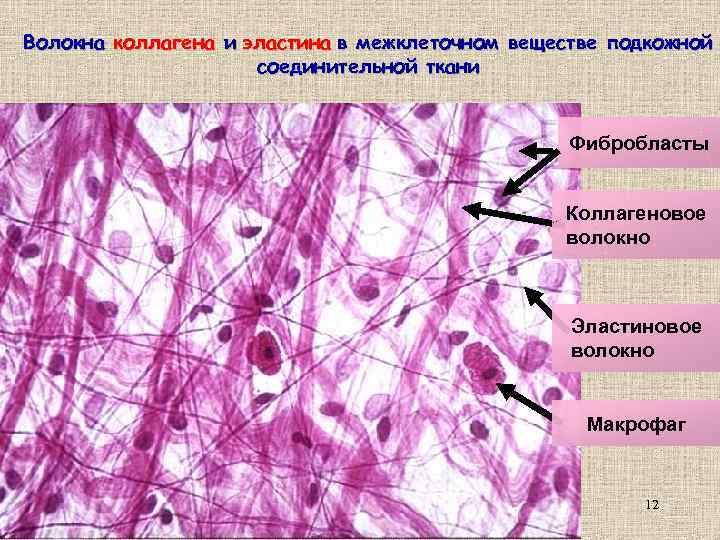
Волокна коллагена и эластина в межклеточном веществе подкожной соединительной ткани Фибробласты Коллагеновое волокно Эластиновое волокно Макрофаг 12
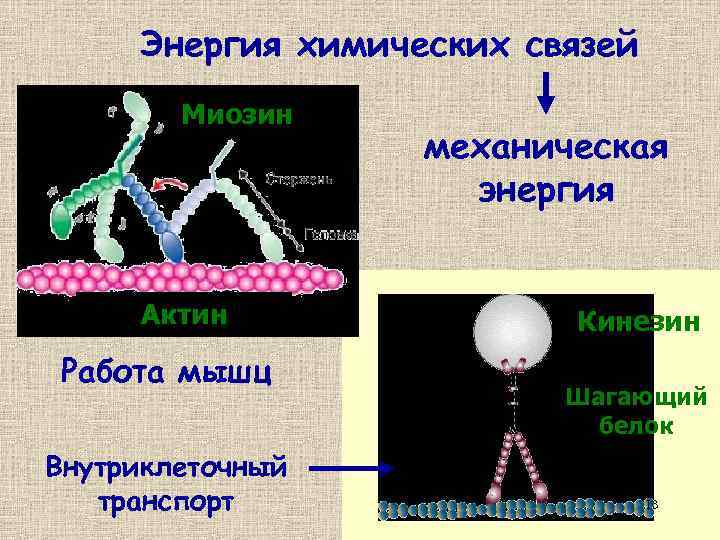
Энергия химических связей Миозин Актин Работа мышц Внутриклеточный транспорт механическая энергия Кинезин Шагающий белок 13

Двигательные белки • Актино-миозиновая система подвижности (мышечное сокращение и др. ) • Динеино-тубулиновая система подвижности (в микротрубочках) • Белковое обеспечение бактериальной подвижности (жгутики) • Двигательная система бактериофагов 14

Строение миофибрилл 15
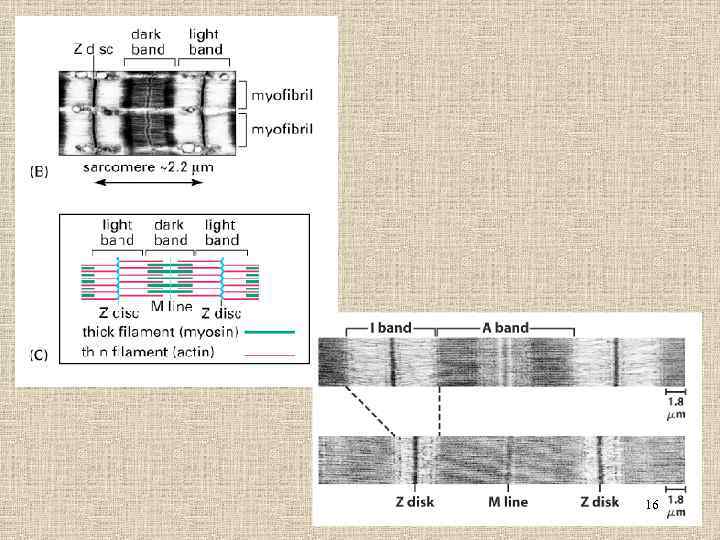
16
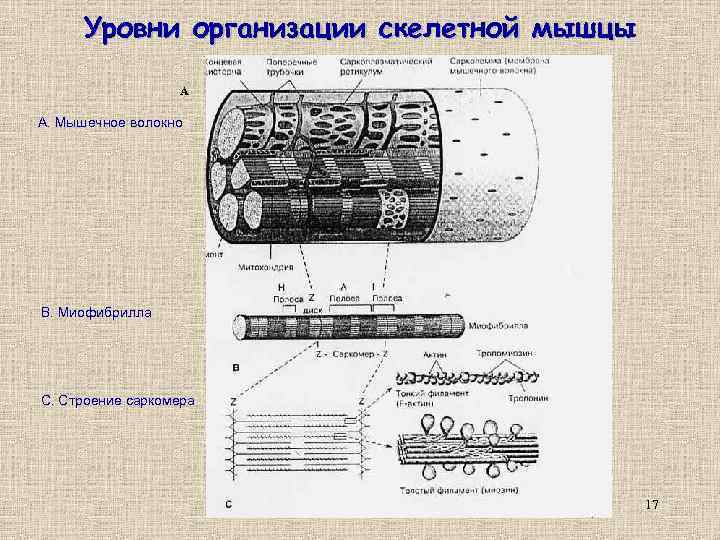
Уровни организации скелетной мышцы А А. Мышечное волокно B. Миофибрилла С. Строение саркомера 17
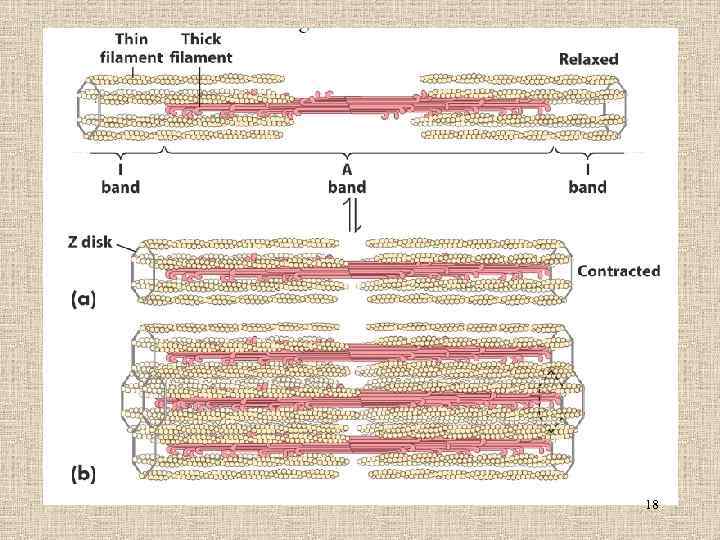
18
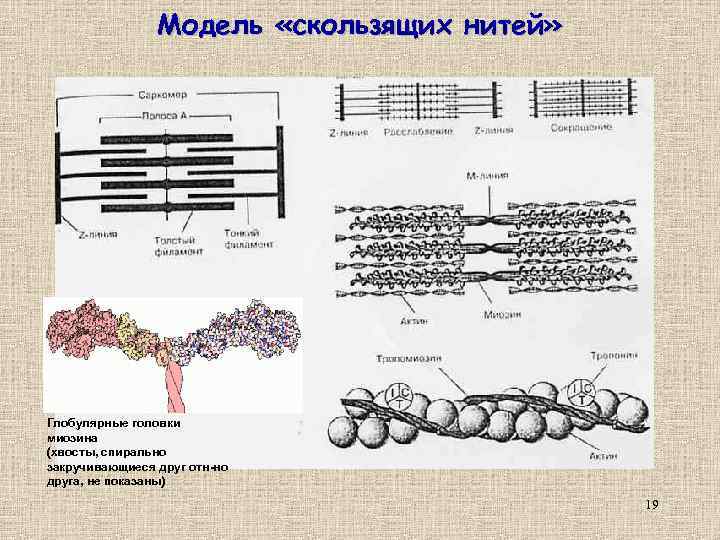
Модель «скользящих нитей» Глобулярные головки миозина (хвосты, спирально закручивающиеся друг отн-но друга, не показаны) 19
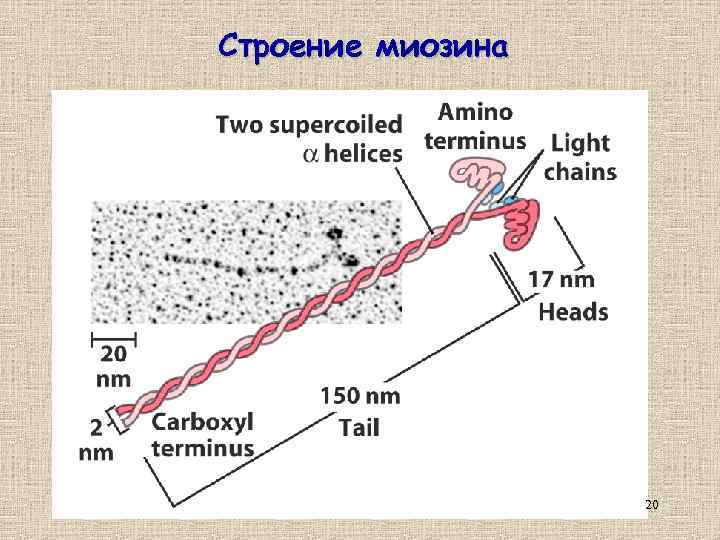
Строение миозина 20

21
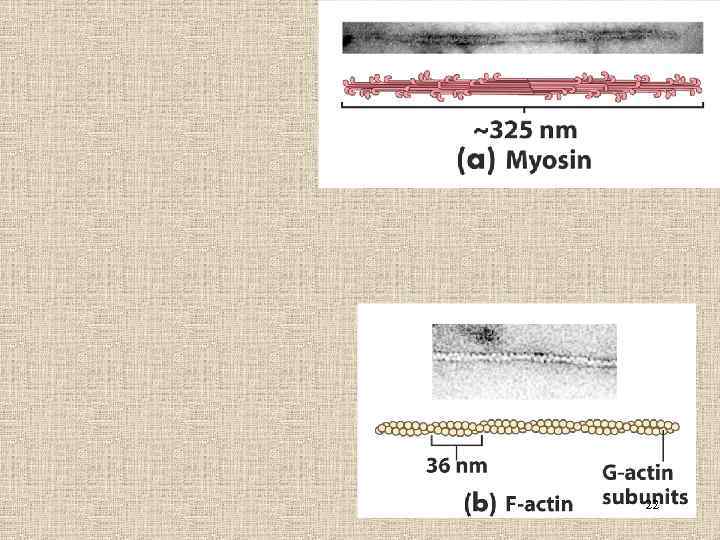
22
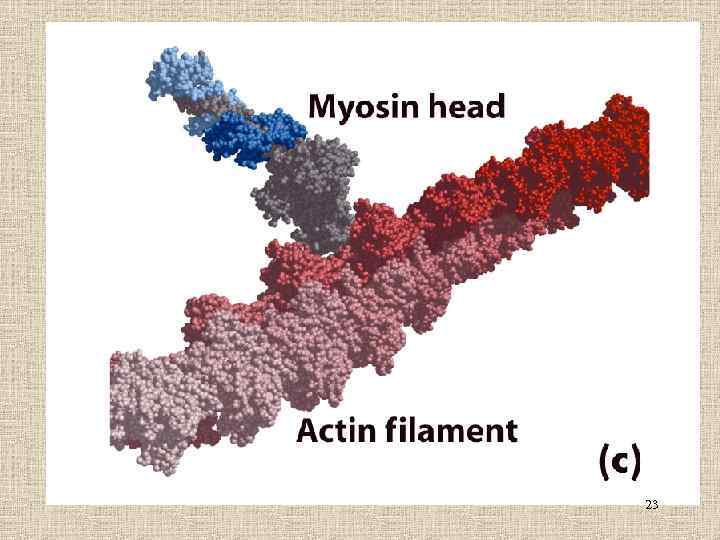
23
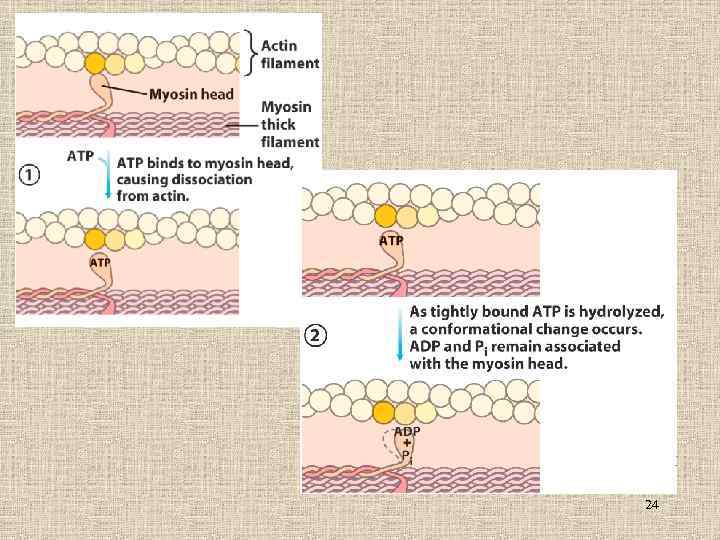
24
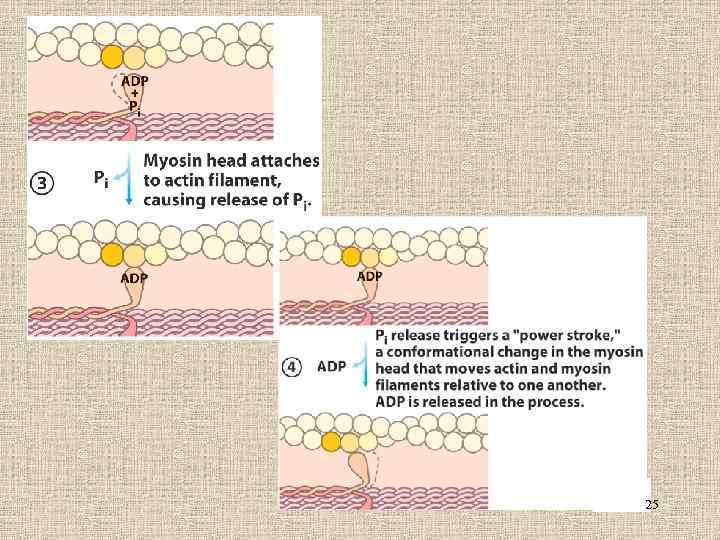
25
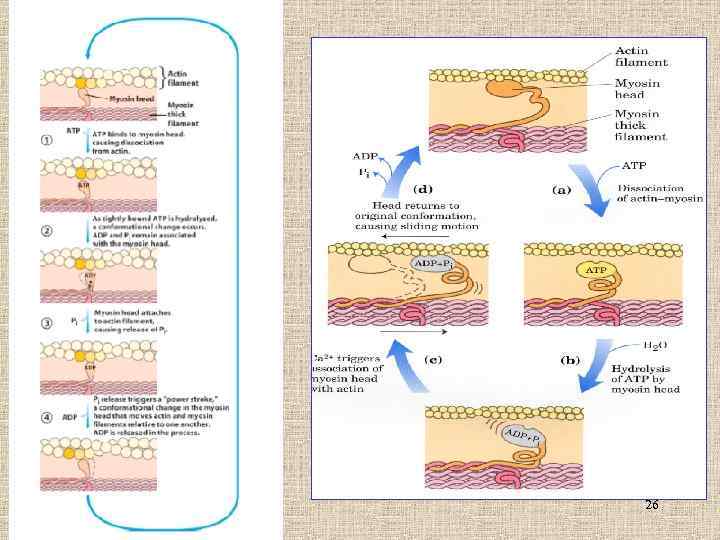
26
Белки цитоскелета 27
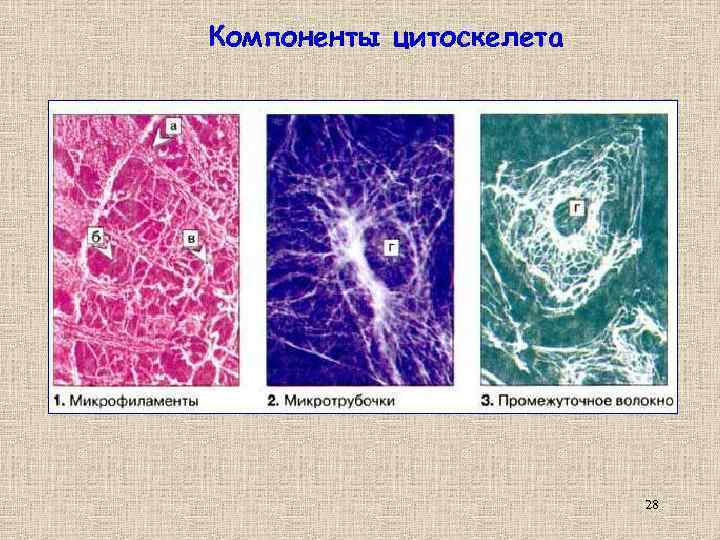
Компоненты цитоскелета 28
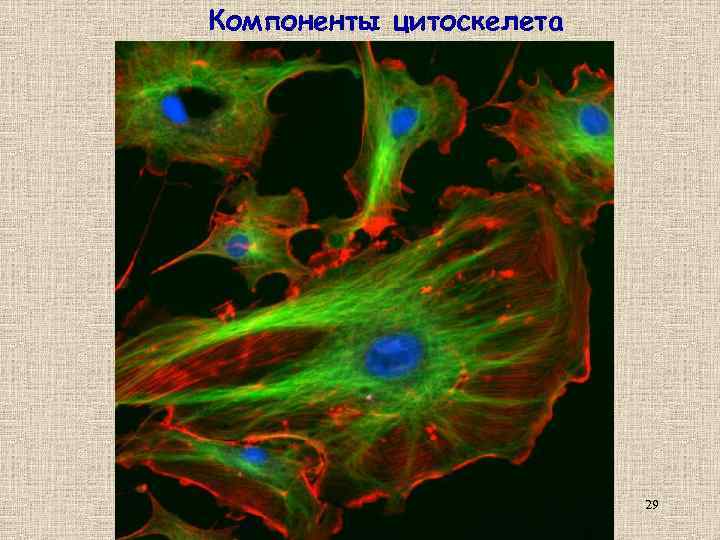
Компоненты цитоскелета 29
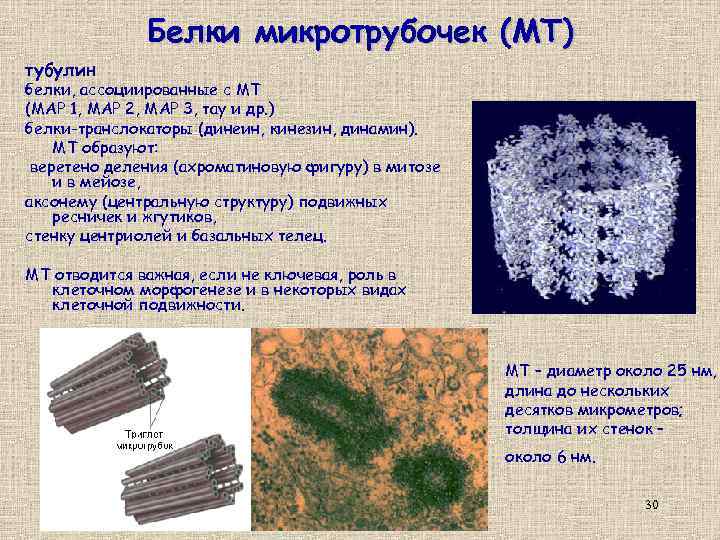
Белки микротрубочек (МТ) тубулин белки, ассоциированные с МТ (МАР 1, МАР 2, МАР 3, тау и др. ) белки-транслокаторы (динеин, кинезин, динамин). МТ образуют: веретено деления (ахроматиновую фигуру) в митозе и в мейозе, аксонему (центральную структуру) подвижных ресничек и жгутиков, стенку центриолей и базальных телец. МТ отводится важная, если не ключевая, роль в клеточном морфогенезе и в некоторых видах клеточной подвижности. МТ – диаметр около 25 нм, длина до нескольких десятков микрометров; толщина их стенок – около 6 нм. 30
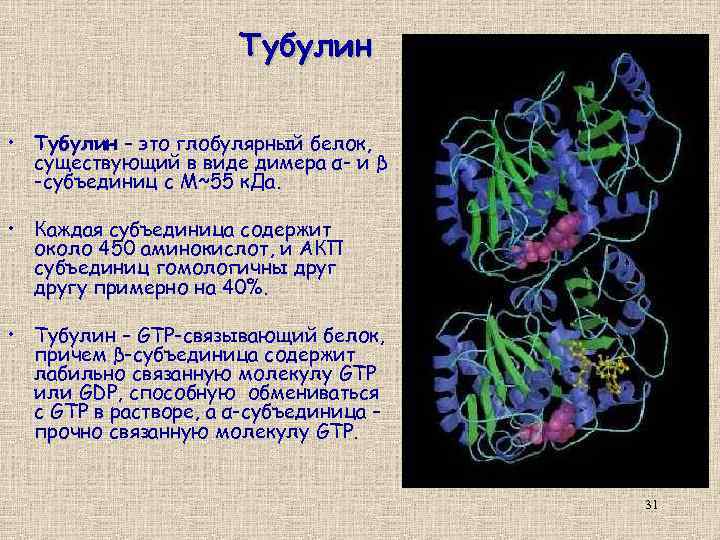
Тубулин • Тубулин – это глобулярный белок, существующий в виде димера α- и β -субъединиц с М~55 к. Да. • Каждая субъединица содержит около 450 аминокислот, и АКП субъединиц гомологичны другу примерно на 40%. • Тубулин – GTP-связывающий белок, причем β-субъединица содержит лабильно связанную молекулу GTP или GDP, способную обмениваться с GTP в растворе, а α-субъединица – прочно связанную молекулу GTP. 31
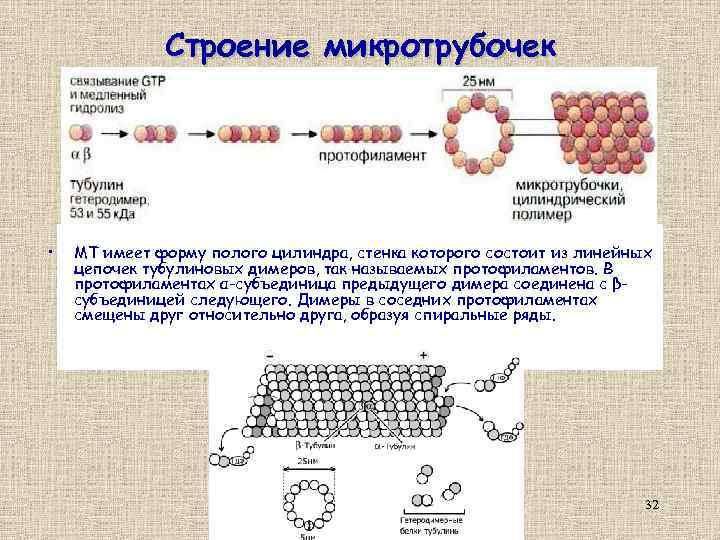
Строение микротрубочек • МТ имеет форму полого цилиндра, стенка которого состоит из линейных цепочек тубулиновых димеров, так называемых протофиламентов. В протофиламентах α-субъединица предыдущего димера соединена с βсубъединицей следующего. Димеры в соседних протофиламентах смещены друг относительно друга, образуя спиральные ряды. 32
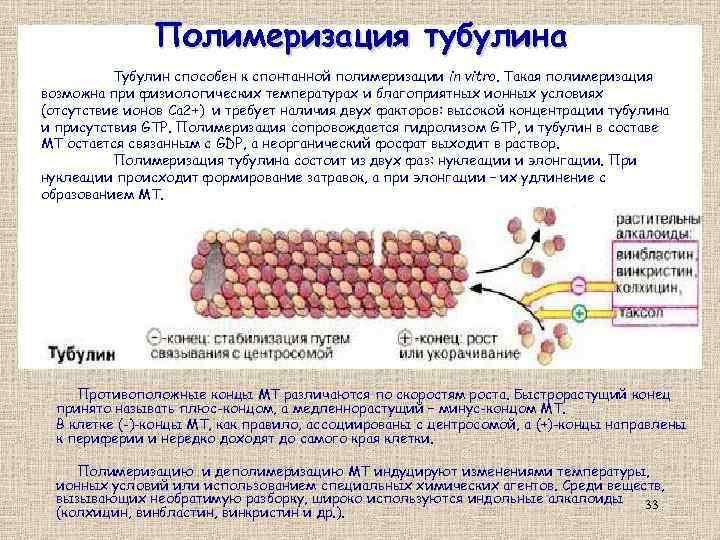
Полимеризация тубулина Тубулин способен к спонтанной полимеризации in vitro. Такая полимеризация возможна при физиологических температурах и благоприятных ионных условиях (отсутствие ионов Ca 2+) и требует наличия двух факторов: высокой концентрации тубулина и присутствия GTP. Полимеризация сопровождается гидролизом GTP, и тубулин в составе МТ остается связанным с GDP, а неорганический фосфат выходит в раствор. Полимеризация тубулина состоит из двух фаз: нуклеации и элонгации. При нуклеации происходит формирование затравок, а при элонгации – их удлинение с образованием МТ. Противоположные концы МТ различаются по скоростям роста. Быстрорастущий конец принято называть плюс-концом, а медленнорастущий – минус-концом МТ. В клетке (-)-концы МТ, как правило, ассоциированы с центросомой, а (+)-концы направлены к периферии и нередко доходят до самого края клетки. Полимеризацию и деполимеризацию МТ индуцируют изменениями температуры, ионных условий или использованием специальных химических агентов. Среди веществ, вызывающих необратимую разборку, широко используются индольные алкалоиды 33 (колхицин, винбластин, винкристин и др. ).
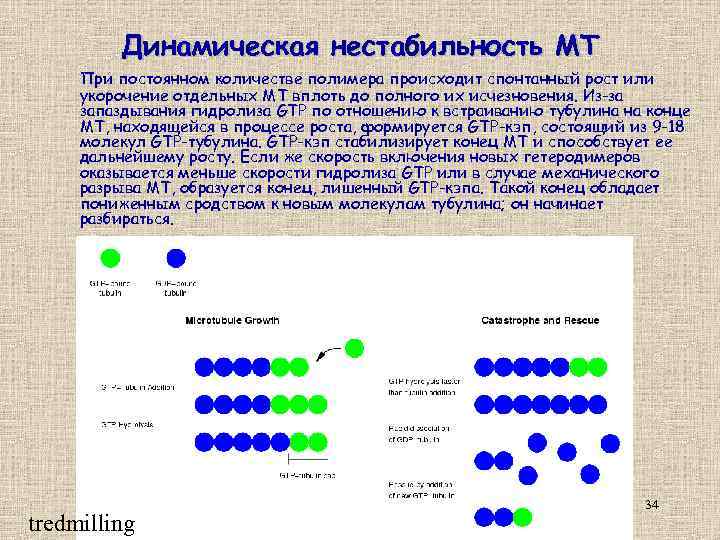
Динамическая нестабильность МТ При постоянном количестве полимера происходит спонтанный рост или укорочение отдельных МТ вплоть до полного их исчезновения. Из-за запаздывания гидролиза GTP по отношению к встраиванию тубулина на конце МТ, находящейся в процессе роста, формируется GTP-кэп, состоящий из 9 -18 молекул GTP-тубулина. GTP-кэп стабилизирует конец МТ и способствует ее дальнейшему росту. Если же скорость включения новых гетеродимеров оказывается меньше скорости гидролиза GTP или в случае механического разрыва МТ, образуется конец, лишенный GTP-кэпа. Такой конец обладает пониженным сродством к новым молекулам тубулина; он начинает разбираться. tredmilling 34

БЕЛКИ, АССОЦИИРОВАННЫЕ С МИКРОТРУБОЧКАМИ (МАР) • • Структурные МАР. Общее свойство – перманентная ассоциация с МТ; связываются с С-концевой частью тубулина. МАР 1, МАР 2, Тау, МАР U и др. МАР способны стимулировать инициацию и элонгацию и стабилизировать готовые МТ; сшивать МТ в пучки. Три основные функции структурных МАР: регуляция динамики МТ, клеточный морфогенез и участие во взаимодействии МТ с другими внутриклеточными структурами. Белки-транслокаторы. Отличительная особенность – свойство преобразовывать энергию АТР в механическое усилие, способное перемещать частицы вдоль МТ или МТ вдоль субстрата. Соответственно транслокаторы являются механохимическими АТР-азами и их АТР-азная активность стимулируется МТ. В отличие от структурных МАР, транслокаторы ассоциированы в МТ только в момент АТРзависимого перемещения. 35

Молекулярные двигатели • Миозин Кинезины – движутся по микротрубочкам в направлении (+)-конца (т. е от центросомы к клеточной периферии) Динеины – перемещаются к (-)-концу микротрубочек 36
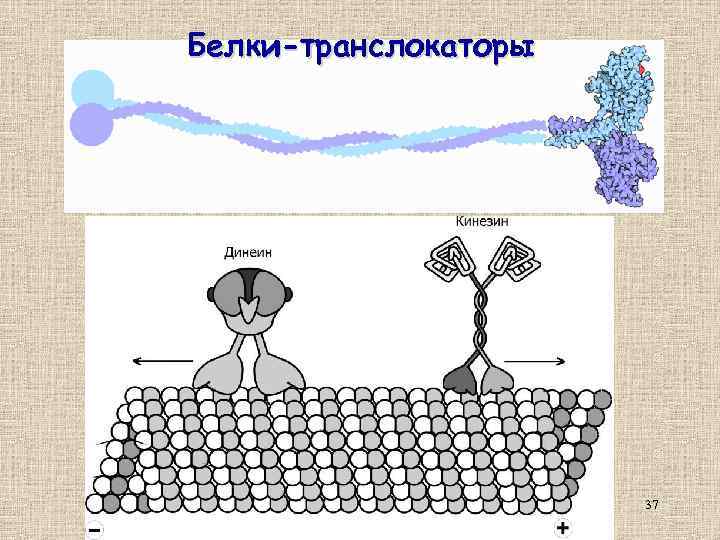
Белки-транслокаторы 37

Белки-транслокаторы 38
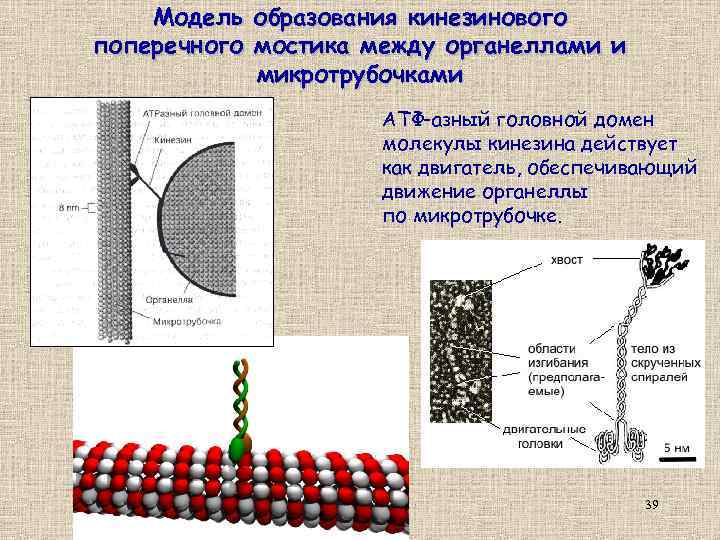
Модель образования кинезинового поперечного мостика между органеллами и микротрубочками АТФ-азный головной домен молекулы кинезина действует как двигатель, обеспечивающий движение органеллы по микротрубочке. 39
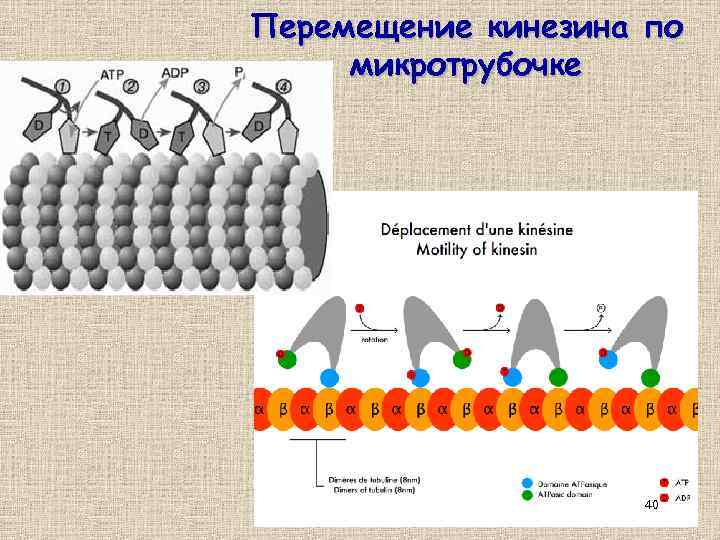
Перемещение кинезина по микротрубочке 40
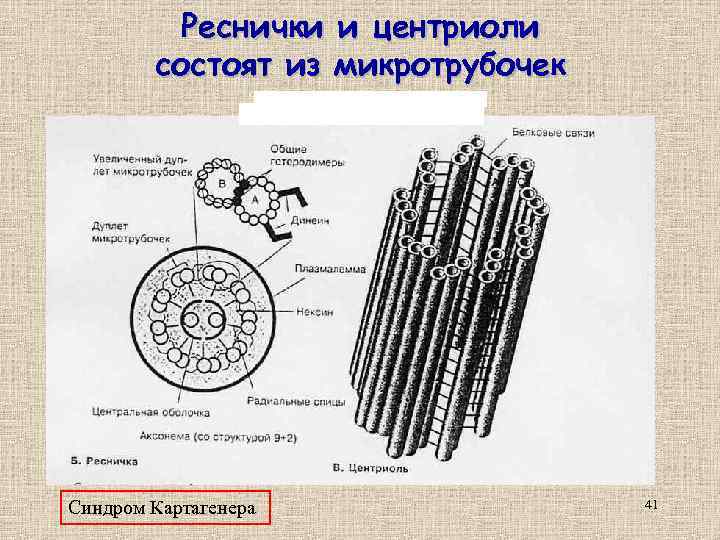
Реснички и центриоли состоят из микротрубочек • • • Кинезин из мозга крупного рогатого скота имеет М~380 к. Да и представляет собой тетрамер двух легких (62 к. Да) и двух тяжелых (120 к. Да) полипептидных цепей. Молекула кинезина имеет форму стеpжня диаметром 2 -4 нм и длиной 80 -100 нм с двумя глобулярными головками на одном конце и веерообразным расширением на другом. В середине стержня находится шарнирный участок. N-Концевой фрагмент тяжелой цепи размером около 50 к. Да, обладающий механохимической активностью, называется моторным доменом кинезина. Динеин – высокомолекулярный белок, состоящий из различных комбинаций α-, β- и γ-тяжелых цепей с молекулярной массой более 400 к. Да и набора промежуточных и легких цепей с М от 10 до 80 к. Да. В зависимости от количества тяжелых цепей на молекулу динеина различают одно-, двух- и трехголовые динеины. Динамин – М 100 к. Да, обладает GTP-азной активность, которая стимулируется при добавлении МТ. При добавлении динамина к МТ происходит образование гексагонально упакованных пучков. Синдром Картагенера 41
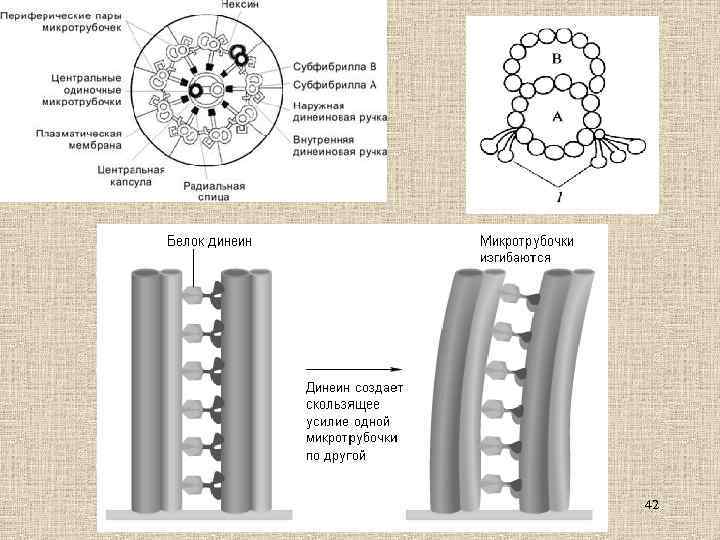
42
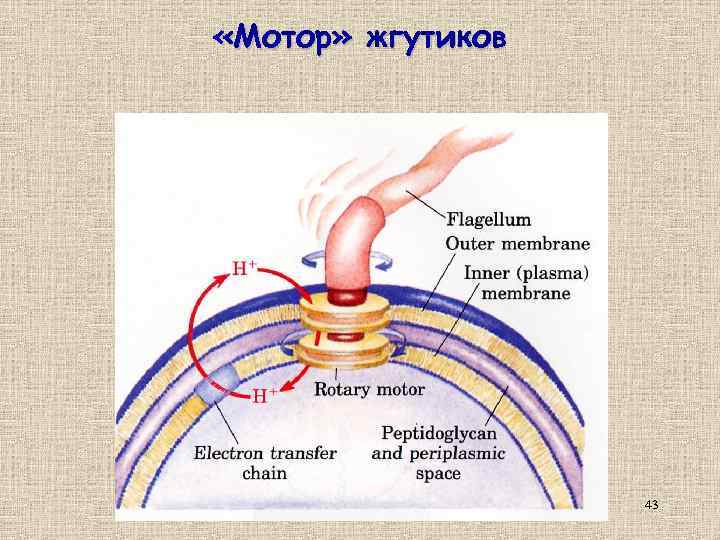
«Мотор» жгутиков 43
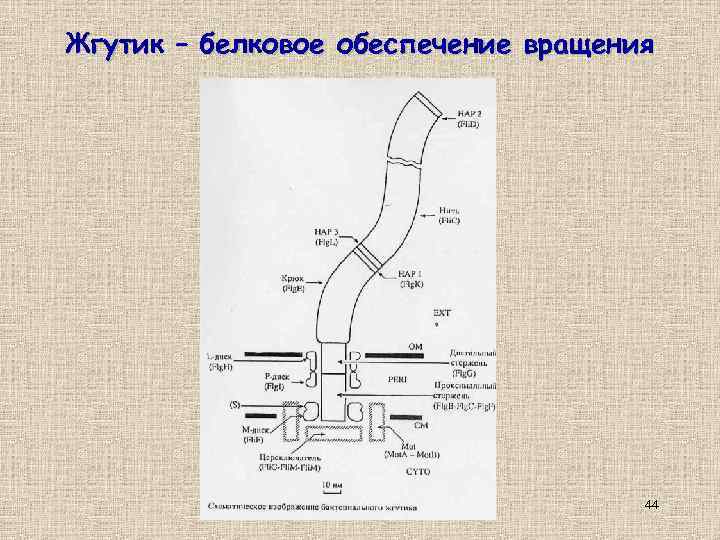
Жгутик – белковое обеспечение вращения 44
06_Lecture_Proteins in acton_2011.ppt