лекция белки.ppt
- Количество слайдов: 45
Белки Строение и функции

n n Аминокислоты В клетках и тканях встречается свыше 170 различных аминокислот. Обычными компонентами белка можно считать 20 аминокислот.

n Аминокислотами называются карбоновые кислоты, в углеводородном радикале которых один или несколько атомов водорода замещены аминогруппами. В зависимости от взаимного расположения карбоксильной и аминогрупп различают α, β, γ и т. д. аминокислоты. Например,

n Чаще всего термин "аминокислота" применяют для обозначения карбоновых кислот, аминогруппа которых находится в a- положении, т. е. для a- аминокислот. Общую формулу aаминокислот можно представить следующим образом:

n n n Свойства аминокислот Аминокислоты – бесцветные кристаллические твердые вещества, растворимы в воде и нерастворимы в органических растворителях. Являются амфотерными соединениями (проявляются свойства кислот и оснований). В растворах действуют как буферы: препятствуют изменениям р. Н, являясь донорами и акцепторами Н+.

n n Растения синтезируют все необходимые им аминокислоты из более простых веществ. Основным источником α - аминокислот для живого организма служат пищевые белки, которые в результате ферментативного гидролиза в желудочнокишечном тракте дают α - аминокислоты. Животные синтезируют не все аминокислоты, многие α- аминокислоты синтезируются в организме, а некоторые необходимые для синтеза белков α аминокислоты не синтезируются в организме и должны поступать извне, в готовом виде, т. е. с пищей. Такие аминокислоты называются незаменимыми. Эти аминокислоты не важнее других, «незаменимы» они лишь в том смысле, что организм животного не способен их синтезировать.
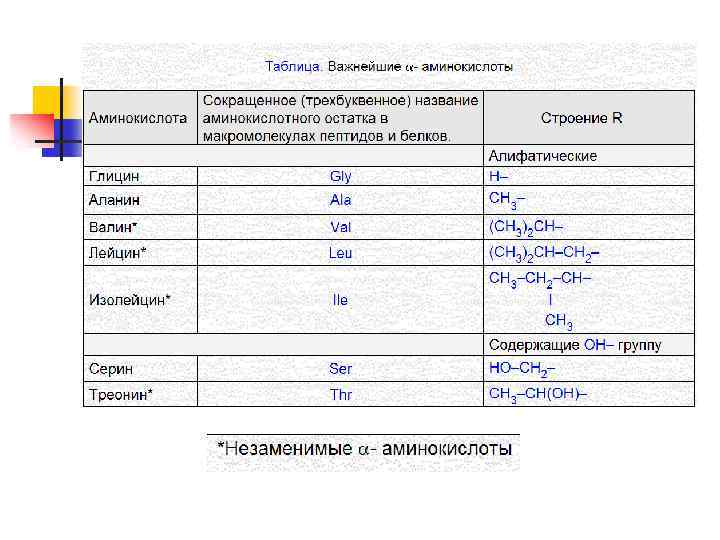
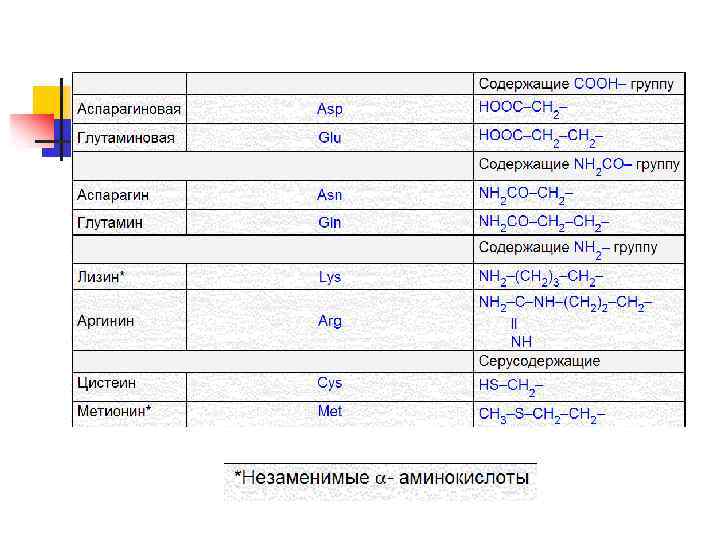
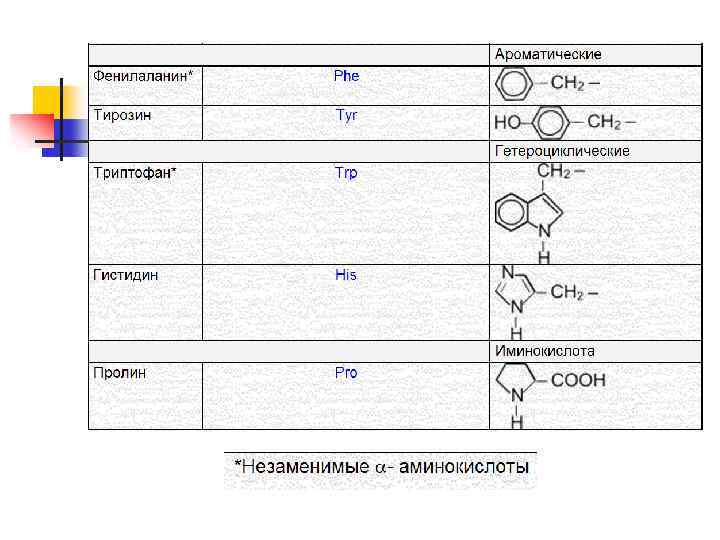
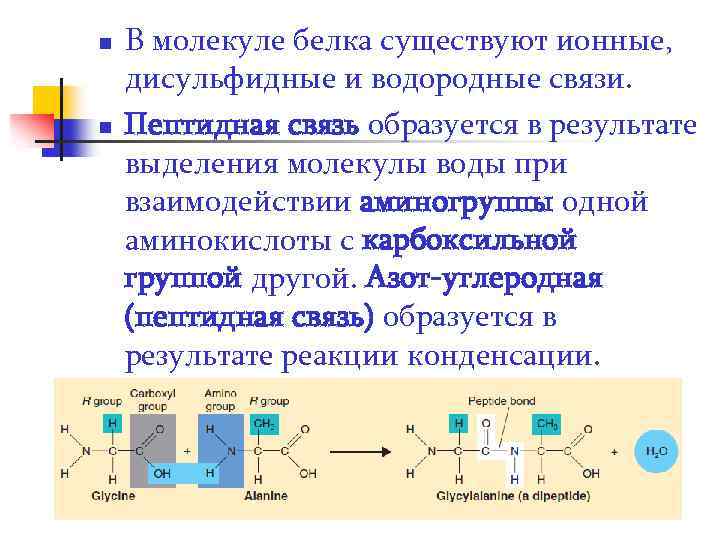
n n В молекуле белка существуют ионные, дисульфидные и водородные связи. Пептидная связь образуется в результате выделения молекулы воды при взаимодействии аминогруппы одной аминокислоты с карбоксильной группой другой. Азот-углеродная (пептидная связь) образуется в результате реакции конденсации.
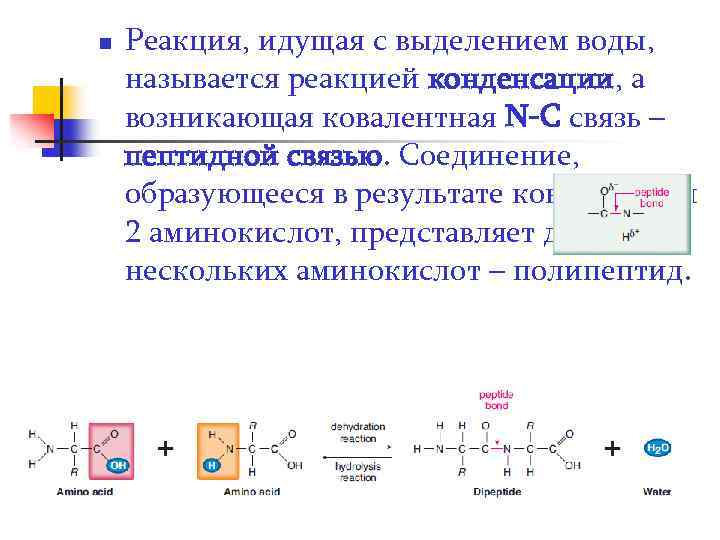
n Реакция, идущая с выделением воды, называется реакцией конденсации, а возникающая ковалентная N-C связь – пептидной связью. Соединение, образующееся в результате конденсации 2 аминокислот, представляет дипептид, нескольких аминокислот – полипептид.
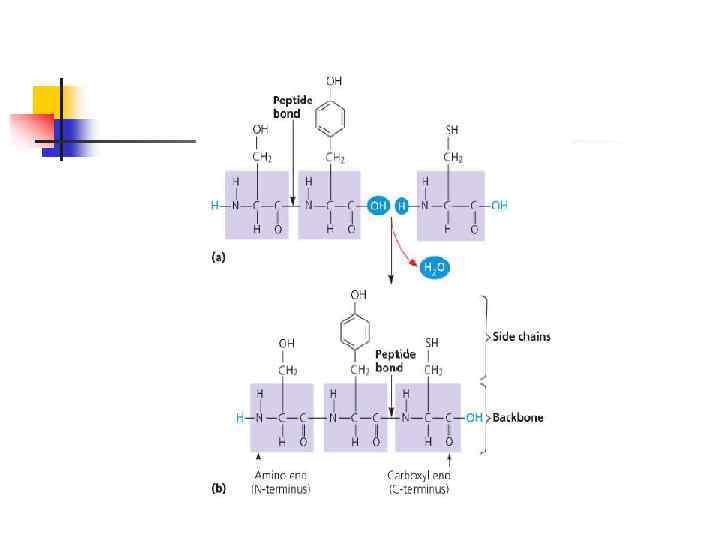
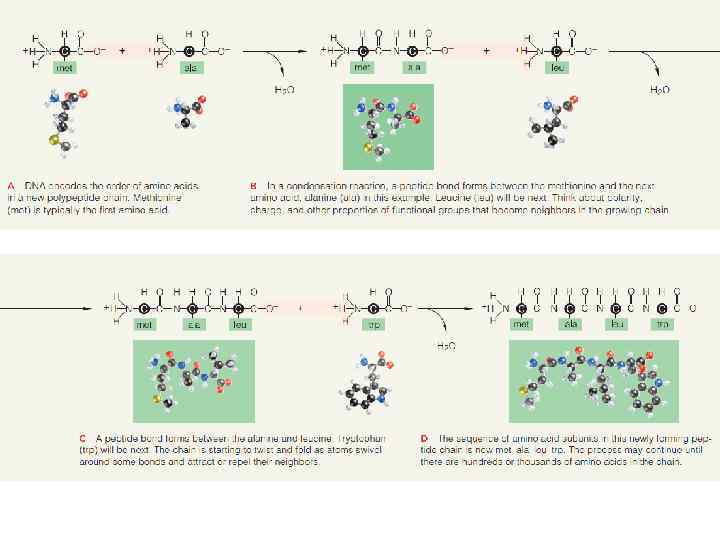

n n n Белки – сложные органические соединения, состоящие из C, H, O, N, в некоторых есть еще и S. Часть белков образует комплексы с молекулами, содержащими P, Fe, Zn, Cu. Пептиды и белки различают в зависимости от величины молекулярной массы. Условно считают, что пептиды содержат в молекуле до 100 (соответствует молекулярной массе до 10000), а белки - свыше 100 аминокислотных остатков (молекулярная масса от 10000 до нескольких миллионов). При этом в пептидах различают олигопептиды, содержащие в цепи не более 10 аминокислотных остатков, и полипептиды, содержащие до 100 аминокислотных остатков. На долю белков приходится более 50% общей сухой

n n n Структура белков Каждому белку свойственна особая геометрическая форма, или конформация. Для полипептидов и белков характерны четыре уровня пространственной организации, которые принято называть первичной, вторичной, третичной и четвертичной структурами.

n Первичная структура – число и последовательность аминокислот, соединенных друг с другом пептидными связями в полипептидной цепи (специфическая аминокислотная последовательность, т. е. порядок чередования a- аминокислотных остатков в полипептидной цепи). Первый белок, для которого была выяснена аминокислотная последовательность – инсулин (1944 – 1954 г. г. Сэнгер Ф. , Кембридж), 51 аминокислота.

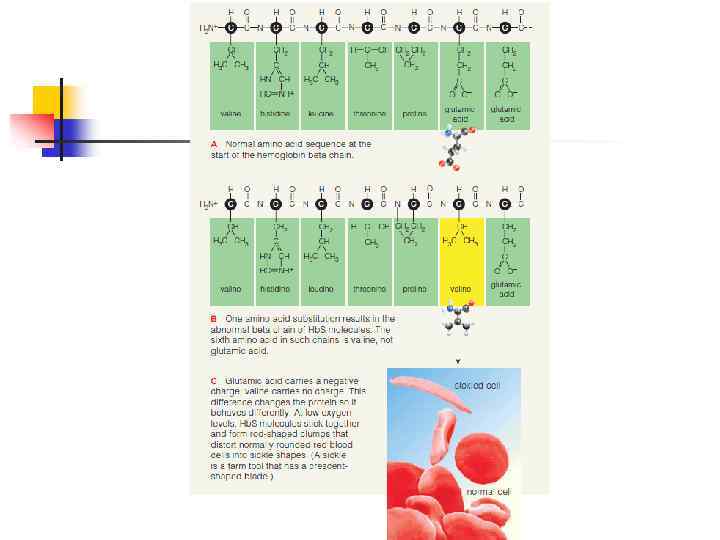
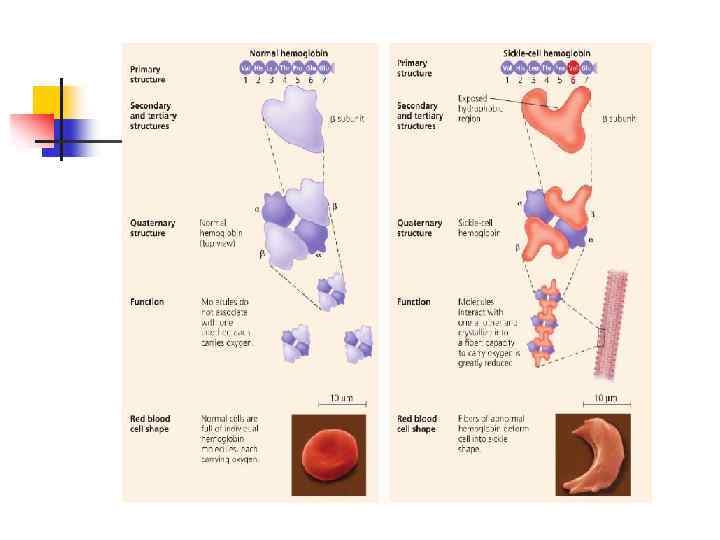
n n Аминокислотная последовательность белка определяет его биологическую функцию. Каждому белку свойственна своя особая аминокислотная последовательность, генетически контролируемая, т. е. закодированная в ДНК, вырабатывающей данный белок. Аминокислотная последовательность определяется нуклеотидной последовательностью ДНК. Замена 1 аминокислоты может резко изменить его функцию (серповидноклеточная анемия).

n n Вторичная структура - конформация полипептидной цепи, т. е. способ скручивания цепи в пространстве за счет водородных связей между группами NH и CO. Например: Белковая молекула может иметь структуру α – спирали, стабилизируемой множеством водородных связей (кератин, белок волос, шерсти, ногтей, клюва, перьев, рогов, кожа позвоночных). Устойчивая и распространенная конформация. β слой, или складчатый слой, белок шелка фиброин (гусеницы)
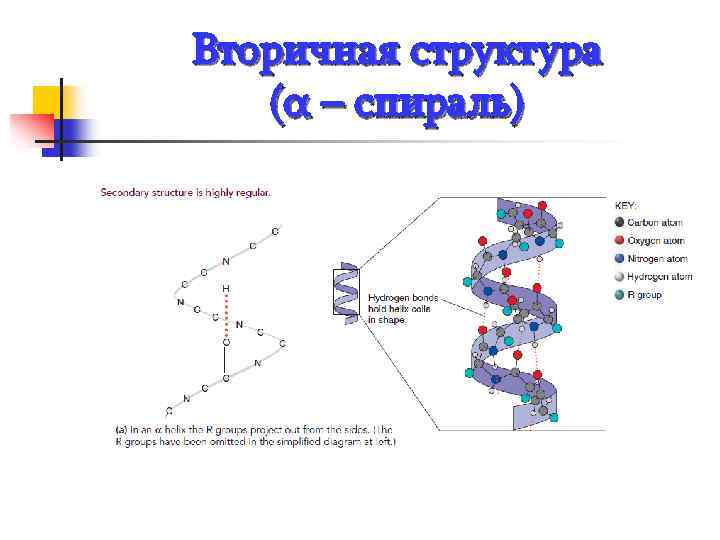
Вторичная структура (α – спираль)
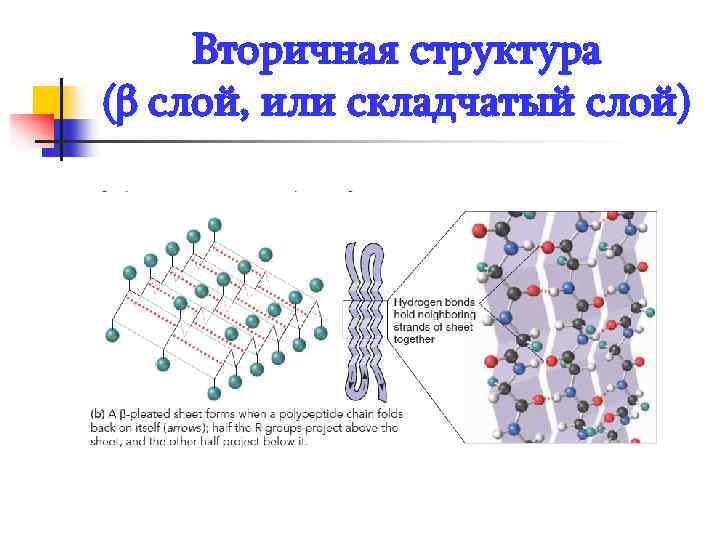
Вторичная структура (β слой, или складчатый слой)

Вторичная структура (β слой, или складчатый слой)

n n Третичная структура Способ свертывания полипетидных цепей глобулярных белков, поддерживается ионными, водородными, дисульфидными связями (S-S), а также гидрофобными взаимодействиями. Белок свертывается таким образом, чтобы гидрофобные цепи были внутри молекулы защищены от соприкосновения с водой, гидрофильные боковые цепи направлены наружу.
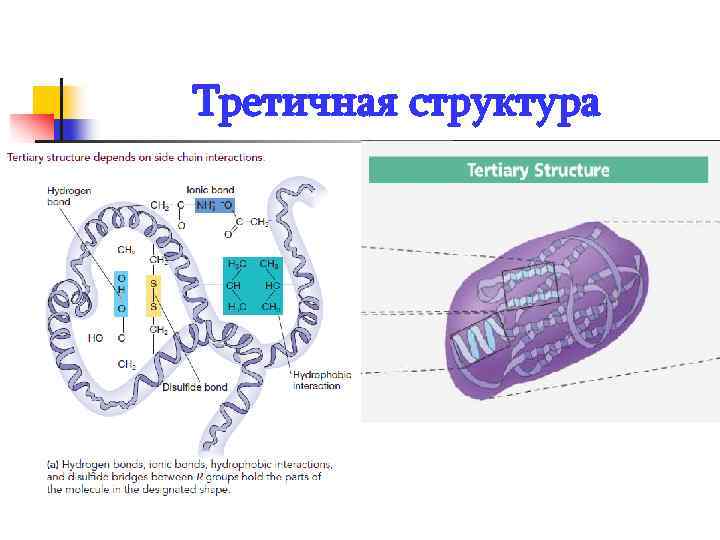
Третичная структура
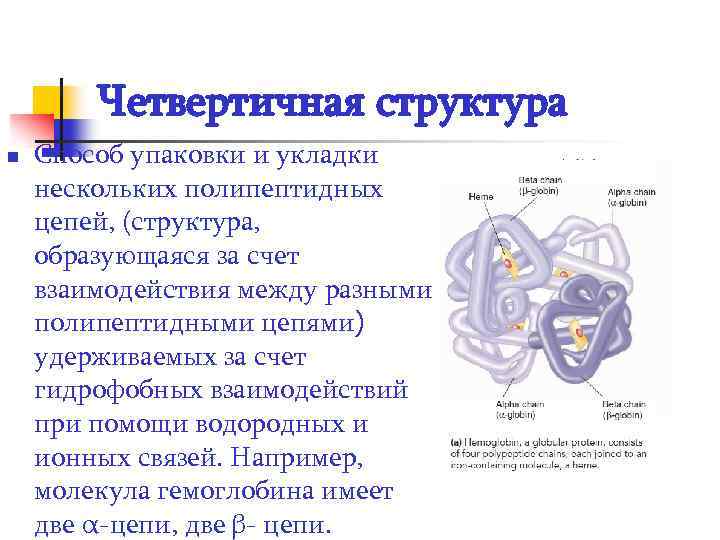
Четвертичная структура n Способ упаковки и укладки нескольких полипептидных цепей, (структура, образующаяся за счет взаимодействия между разными полипептидными цепями) удерживаемых за счет гидрофобных взаимодействий при помощи водородных и ионных связей. Например, молекула гемоглобина имеет две α-цепи, две β- цепи.

n Денатурация – утрата трехмерной конформации, присущей данной белковой молекуле, носит временный или постоянный характер, аминокислотная последовательность остается неизменной. Молекула развертывается и теряет способность выполнять обычную функцию.

n Денатурация - утрата белком природной (нативной) конформации, сопровождающаяся обычно потерей его биологической функции. С точки зрения структуры белка – это разрушение вторичной и третичной структур белка, обусловленное воздействием кислот, щелочей, нагревания, радиации и т. д. Первичная структура белка при денатурации сохраняется. Денатурация может быть обратимой (так называемая, ренатурация) и необратимой. Пример необратимой денатурации при тепловом воздействии – свертывание яичного альбумина при варке яиц

n n n Факторы, вызывающие денатурацию: нагревание, воздействие инфрактрасного, ультрафиолетового излучения )разрываются слабые ионные и водородные связи) сильные кислоты, сильные щелочи, концентрированные растворы солей (разрушаются ионные, пептидные связи) тяжелые металлы (разрушаются ионные связи, снижается растворимость, выпадают в осадок) органические растворители (например, спирт вызывает денатурацию белка бактерий)

n Гидролиз белков – разрушение первичной структуры белка под действием кислот, щелочей или ферментов, приводящее к образованию α- аминокислот, из которых он был составлен.

Классификация белков по их функциям

n n n I. Структурные белки Коллаген – компонент соединительной ткани, костей, сухожилий, хряща Склеротин – наружный скелет насекомых α-кератин – кожа, перья, ногти, волосы, рога мукопротеины – синовинальная жидкость, слизистые секреты белки оболочки вирусов – «обертка» нуклеиновой кислоты вируса

n n II. Ферменты Трипсин – катализатор гидролиза белков Рибулозобисфосфаткарбоксилаза – катализирует карбоксилирование (присоединение СО 2 ) рибулозобисфосфата при фотосинтезе Глутаматсинтетаза – катализирует образование аминокислоты глутамина из глутаминовой кислоты и аммиака

n n n III. Гормоны инсулин, глюкагон – регулируют обмен глюкозы АКТГ – стимулирует рост и активность коры надпочечников

n n n IV. Транспортные белки Гемоглобин – переносит О 2 в крови позвоночных Гемоцианин - переносит О 2 в крови беспозвоночных Миоглобин - переносит О 2 в мышцах Сывороточный альбумин – служит для транспорта жирных кислот
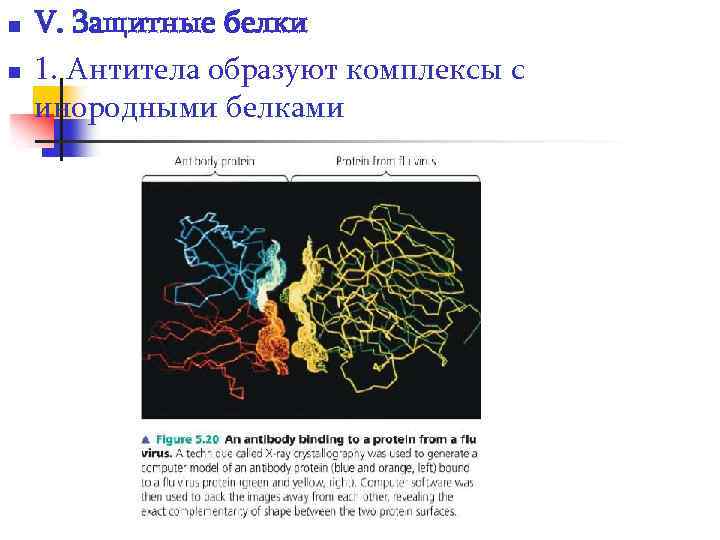
n n V. Защитные белки 1. Антитела образуют комплексы с инородными белками

V. Защитные белки n n 2. Фибриноген - предшественник фибрина при свертывании крови 3. Тромбин – участвует в процессе свертывания крови

n n n YI. Сократительные белки Миозин – подвижные нити миофибрилл саркомера Актин – неподвижные нити миофибрилл саркомера

n n n YII. Запасные белки Яичный альбумин – белок яйца Дифтерийный токсин – токсин, вырабатываемый дифтерийной палочкой

n n Классификация белков по составу По составу белки подразделяются на простые и сложные. Простые белки состоят только из аминокислот. Сложные белки состоят из глобулярных белков и небелкового материала. Небелковую часть сложного белка называют простетической группой.

Простые белки n n n n Альбумины Нейтральные Растворимы в воде Растворимы в разбавленных солевых растворах Примеры: Яичный альбумин Сывороточный альбумин крови

n n n n Глобулины Нейтральные Нерастворимы в воде Растворимы в разбавленных растворах Примеры: Содержащиеся в крови антитела Фибрин

n n n Гистоны Основные Растворимы в воде Нерастворимы в разбавленном водном растворе аммиака Примеры: Связаны с нуклеиновыми кислотами в нуклеопротеидах клетки

n n Склеропротеины Нерастворимы в воде и в большей части в других растворителях Примеры: Кератин волос, кожи, перьев, коллаген сухожилий и межклеточного вещества костной ткани, эластин связок

лекция белки.ppt