
Белки. Состав и строение Белки = Протеины «Протос» - первый (греч. ) % сухой массы животной клетки - ? % сухой массы растительной клетки - ? C, H, O, N, S - элементы, входящие в состав белков Мономер белка – аминокислота.

Аминокислоты. Строение и классификация 170 аминокислот. 20 аминокислот входит в состав белков. Незаменимые – аминокислоты, которые не могут быть синтезированы в организме животного. Общая формула аминокислот • Амфотерность аминокислот Нейтральные, кислые, основные аминокислоты • •

Связи, встречающиеся в молекулах белков 1. Пептидная связь - связь между остатками аминокислот 2. Водородная связь - связь между СО- и NHгруппами; между R-группами аминокислот 3. Дисульфидная связь – дисульфидный мостик между остатками цистеина 4. Ионная связь - связь между заряженными Rгруппами 5. Гидрофобные взаимодействия – объединения неполярных молекул или R-групп

Уровни организации белковой молекулы 1. 2. 3. 4. Первичная структура – последовательность аминокислот в полипептидной цепи, соединенных пептидными связями; Вторичная структура – α-спираль (Н-связи между СО- и NHгруппами одной полипептидной цепи), β-конформация (Н-связи между СО- и NH-группами соседних цепей), тройная спираль (кератин, фиброин, коллаген) Третичная структура – глобула, поддерживаемая ионными, водородными, дисульфидными связями, а также гидрофобными взаимодействиями (миозин, инсулин). Четвертичная структура - способ совместной упаковки нескольких полипептидных цепей (гемоглобин)

Денатурация и ренатурация белков Денатурация – утрата трехмерной структуры. Факторы, вызывающие денатурацию: • Нагревания или излучения; • Сильные кислоты, щелочи, концентрированные растворы солей; • Тяжелые металлы; • Органические растворители. Ренатурация – способность белка спонтанно приобретать третичную структуру.

Классификация белков по структуре • Фибриллярные – наиболее важна вторичная структура. Нерастворимы в воде, механически прочные (например, колллаген, фиброин, миозин). • Глобулярные - наиболее важна третичная структура. Растворимы - легко образуют коллоидные суспензии (например, ферменты, антитела). • Промежуточные – фибриллярной природы, но растворимы в воде (фибриноген, превращающийся в фибрин).

Классификация белков по составу • Простые – состоят только из аминокислот (например, альбумин, фибрин); • Сложные – состоят из белков и небелковой части: 1. 2. 3. 4. Фосфопротеиды – казеин молока; Гликопротеиды – муцин (компонент слюны); Липопротеиды – компонгенты мембран; Хромопротеиды – гемоглобин (пигмент крови). Функции белков – самостоятельно по учебнику

Свойства ферментов • Ферменты – глобулярные белки; • Ферменты действуют как катализаторы; • Их присутствие не влияет ни на свойства, ни на природу конечного продукта; • Ферменты действуют чрезвычайно эффективно; • Один фермент – одна реакция; • Фермент снижает энергию активации катализируемой реакции; • В мол-ле фермента есть активный центр, который вступает в контакт с субстратом.

Классы ферментов 1. Оксидоредуктазы – катализ окислительновосстановительных реакций; 2. Трансферазы – переносят ту или иную функциональную группу от одного субстрата на другой; 3. Гидролазы – катализ реакций расщепления, идущих с участием воды; 4. Лиазы – катализируют расщепление или соединение, при этом исчезают или образуются двойные связи; 5. Изомеразы – перемещают группы в пределах молекулы без изменения общей формулы субстрата; 6. Лигазы – катализируют энергозависимые реакции присоединения.
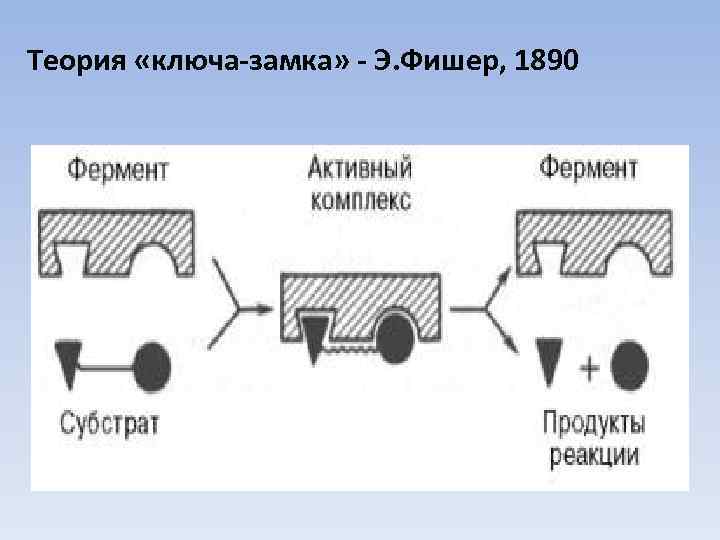
Теория «ключа-замка» - Э. Фишер, 1890
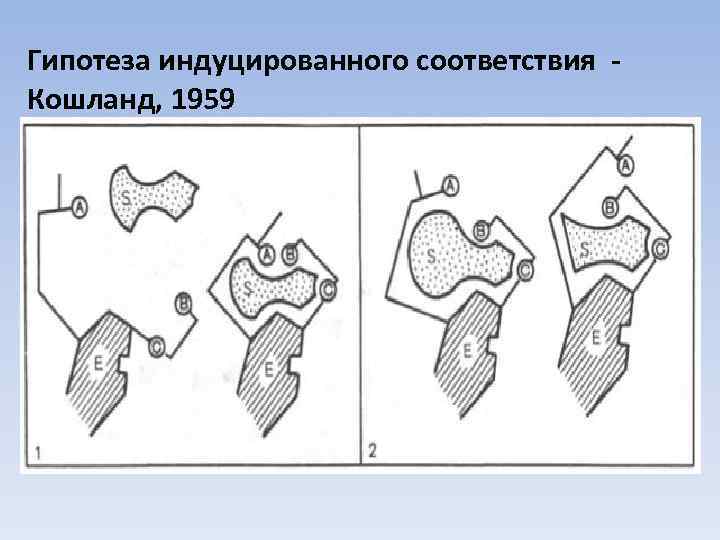
Гипотеза индуцированного соответствия Кошланд, 1959

Кофакторы ферментов – небелковые компоненты ферментов • Неорганические ионы заставляют фермент или субстрат принять форму, способствующую образованию фермент-субстратного комплекса; • Простетические группы – органические молекулы не аминокислотной природы, прочно связанные с ферментом (ФАД, гем); • Коферменты - органические молекулы не аминокислотной природы, сохраняющие связь с ферментом только в ходе реакции (производные витаминов).