Тема 1. Общие сведения о белках.ppt
- Количество слайдов: 20

Белки. Общие сведения. Вопрос 1. Элементарный состав белков. Вопрос 2. Полипептидная теория химического строения белков. Вопрос 3. Пространственное строение белков. Типы химических связей в белках. Вопрос 4. Классификация белков. Вопрос 5. . Биосинтез белков и его регуляция.

Белки, или протеины (от греч. protos – первый, важнейший), являются важнейшим классом органических соединений, играющим основополагающую роль в жизнедеятельности любой живой клетки. На долю белков приходится не менее 50 % сухой массы органических веществ клетки. Учитывая разнообразие живых организмов можно судить о существовании нескольких миллиардов химически индивидуальных белков, отличающихся как структурой, так и функциями. Например, клетка кишечной палочки содержит 3000 различных белков, а человеческий организм ~1 млн. Средний элементарный состав большинства белков (%): углерод – 50 -54; кислород – 20 -23; азот – 15 -18; водород – 6 -8; сера 0, 3 -2, 5. Однако в мире белков существуют исключения, например в белках – протаминах содержание азота достигает 30 %. Роль структурных элементов в белках выполняют L-изомеры αаминокислот, отличающиеся друг от друга боковыми радикалами. Именно их специфические особенности придают каждому белку индивидуальность и влияют на его биологические и физико-химические свойства.
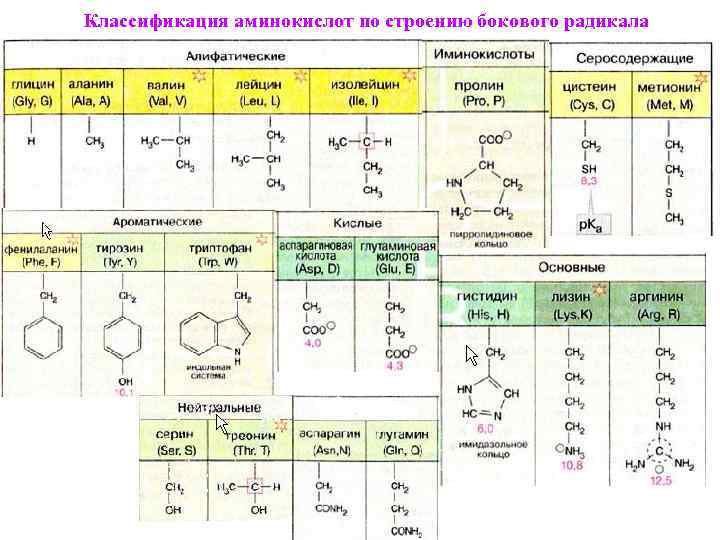
Классификация аминокислот по строению бокового радикала

Оптическая изомерия аминокислот. Все протеиногенные аминокислоты кроме глицина — оптически активны и имеют как минимум один хиральный центр и принадлежат, как уже упоминалось к L-ряду. Принадлежность аминокислот к L- или D-ряду определяется по расположению функциональных групп у хирального атома углерода, несущего аминогруппу, в сравнении с глицериновым альдегидом. Однако ряд протеиногенных аминокислот имеет несколько хиральных центров и несколько оптических изомеров может принадлежать к L-ряду. Так, например, треонин имеет два хиральных центра (n = 2) и соответственно 2 n = 22 = 4 оптических изомера. Из этих двух оптических изомеров именно Lтреонин входит в состав природных белков: Еще два оптических изомера треонина относятся к D-ряду и в составе белков не обнаруживаются.

Физические свойства. α-Аминокислоты — кристаллические вещества. Они имеют высокую температуру плавления (более 200 °С), нелетучи, нерастворимы в неполярных органических растворителях, хорошо растворимы в воде (важный фактор, обеспечивающий полноценную всасываемость и транспорт аминокислот в организме). Интересно отметить, что L-аминокислоты имеют сладкий вкус, a Dизомеры безвкусны или горькие.
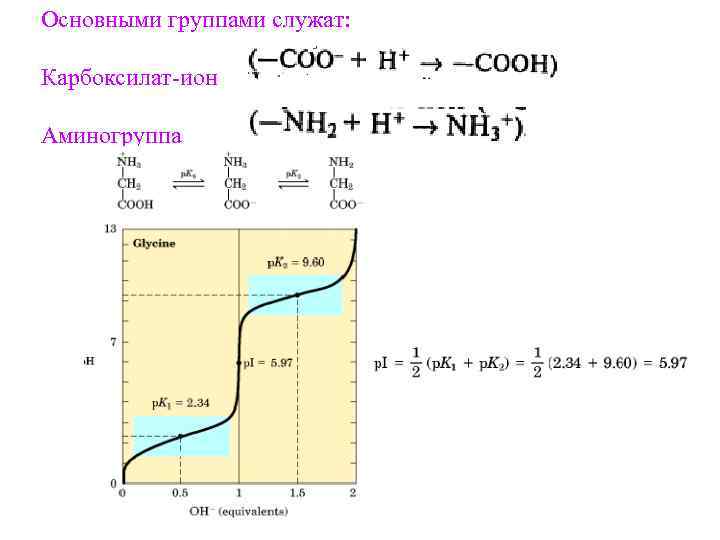
Основными группами служат: Карбоксилат-ион Аминогруппа
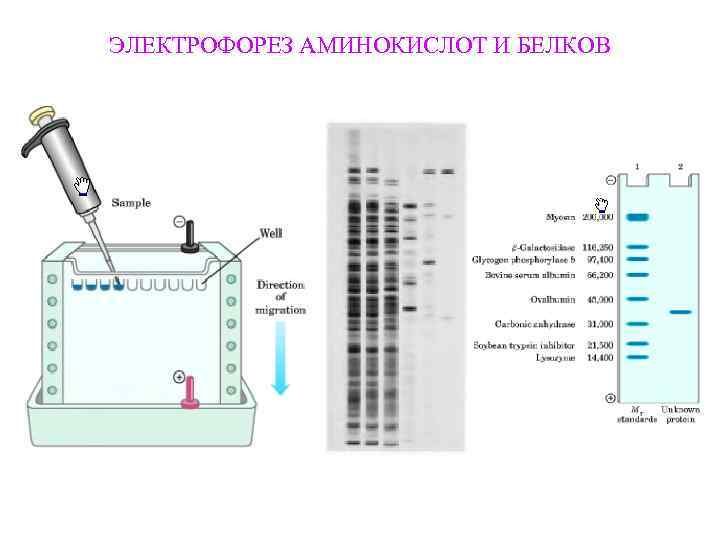
ЭЛЕКТРОФОРЕЗ АМИНОКИСЛОТ И БЕЛКОВ
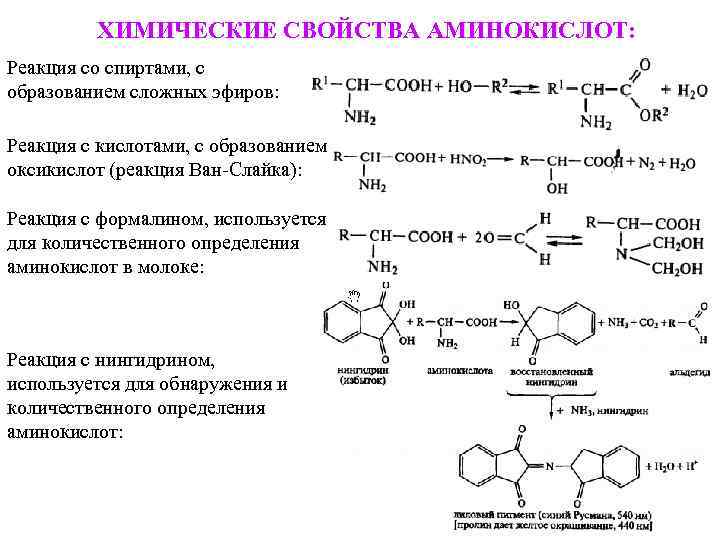
ХИМИЧЕСКИЕ СВОЙСТВА АМИНОКИСЛОТ: Реакция со спиртами, с образованием сложных эфиров: Реакция с кислотами, с образованием оксикислот (реакция Ван-Слайка): Реакция с формалином, используется для количественного определения аминокислот в молоке: Реакция с нингидрином, используется для обнаружения и количественного определения аминокислот:

Непротеиногенные аминокислоты. К настоящему времени в различных объектах живого мира найдено около 200 различных аминокислот. В организме человека содержится около 60 различных аминокислот и их производных, но, как уже отмечалось, не все они участвуют в построении белковых молекул. Аминокислоты, не участвующие в построении полипептидных цепей, получили название непротеиногенных. Они либо находятся в клетке в свободном виде (как продукты обмена), либо входят в состав других небелковых соединений. Ниже представлены некоторые из непротеиногенных аминокислот, имеющие важное био-логическое значение:
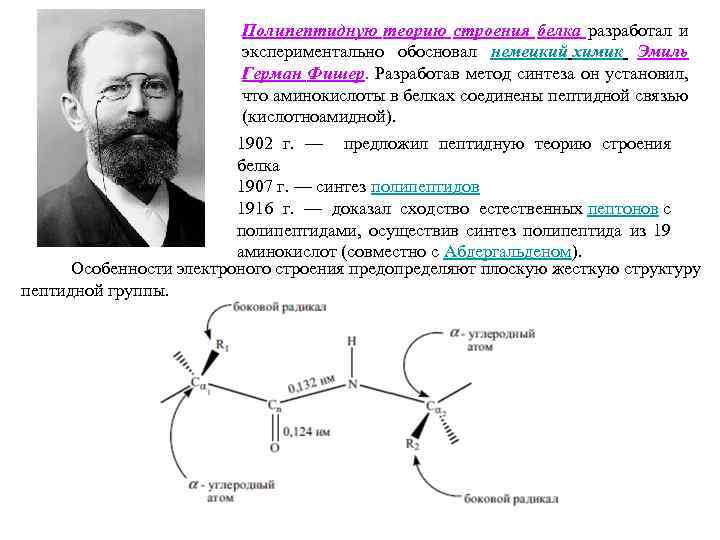
Полипептидную теорию строения белка разработал и экспериментально обосновал немецкий химик Эмиль Герман Фишер. Разработав метод синтеза он установил, что аминокислоты в белках соединены пептидной связью (кислотноамидной). 1902 г. — предложил пептидную теорию строения белка 1907 г. — синтез полипептидов 1916 г. — доказал сходство естественных пептонов с полипептидами, осуществив синтез полипептида из 19 аминокислот (совместно с Абдергальденом). Особенности электроного строения предопределяют плоскую жесткую структуру пептидной группы.
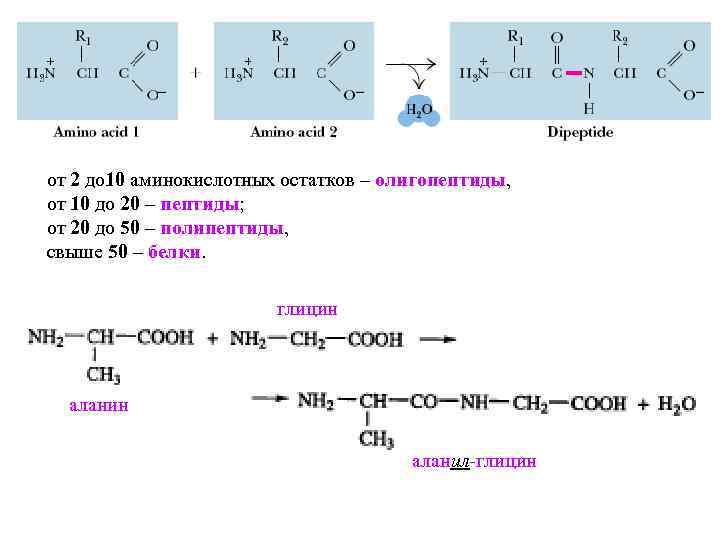
от 2 до 10 аминокислотных остатков – олигопептиды, от 10 до 20 – пептиды; от 20 до 50 – полипептиды, свыше 50 – белки. глицин аланил-глицин
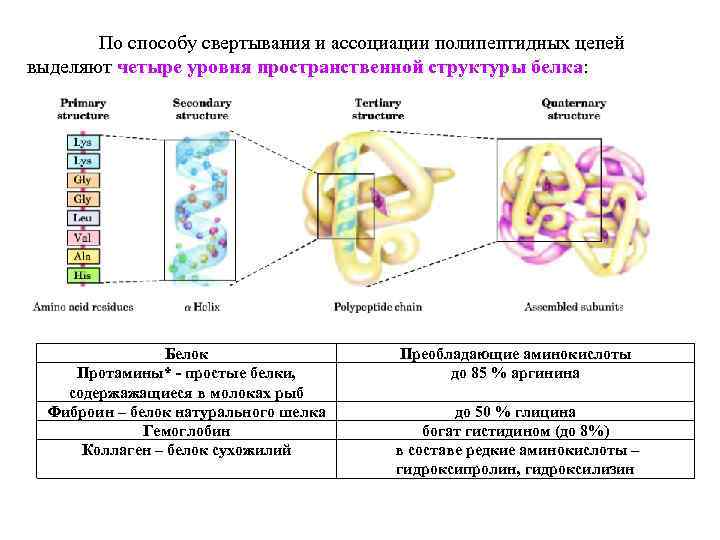
По способу свертывания и ассоциации полипептидных цепей выделяют четыре уровня пространственной структуры белка: Белок Протамины* - простые белки, содержажащиеся в молоках рыб Фиброин – белок натурального шелка Гемоглобин Коллаген – белок сухожилий Преобладающие аминокислоты до 85 % аргинина до 50 % глицина богат гистидином (до 8%) в составе редкие аминокислоты – гидроксипролин, гидроксилизин

Вторичные структуры белка: α-спираль На один виток α-спирали в среднем приходится 3, 7 аминокислотных остатка. Шаг спирали составляет 0, 54 нм, диаметр — 0, 5 нм. Плоскости двух соседних пептидных групп располагаются при этом под углом 108˚. Боковые радикалы α– аминокислот находятся на наружной стороне спирали и направлены от поверхности цилиндра. Основную роль в закреплении такой конформации цепи играют водородные связи, которые в α-спирали образуются между атомом кислорода карбонильного фрагмента пептидной группы каждого первого аминокислотного остатка и атомом водорода - NH-фрагмента пептидной группы каждого пятого аминокислотного остатка. Некоторые α-аминокислоты в силу строения бокового радикала препятствуют спирализации цепи: - пролин не содержит атома водорода в составе пептидной группы и, следовательно, не может образовывать водородную связь. Поэтому в тех участках, где имеются звенья пролина, белковая цепь теряет способность к спирализации (деспирализуются) и изгибается; - остатки глутаминовой и аспарагиновой кислот, ---групп, расположенные рядом, за счет взаимного отталкивания –СОО несущих отрицательный заряд при физиологических значениях р. Н; - остатки лизина и аргинина, расположенные рядом, за счет отталкивания положительных зарядов диссоциированных аминогрупп. - аминокислоты с объемными радикалами, расположенные рядом.
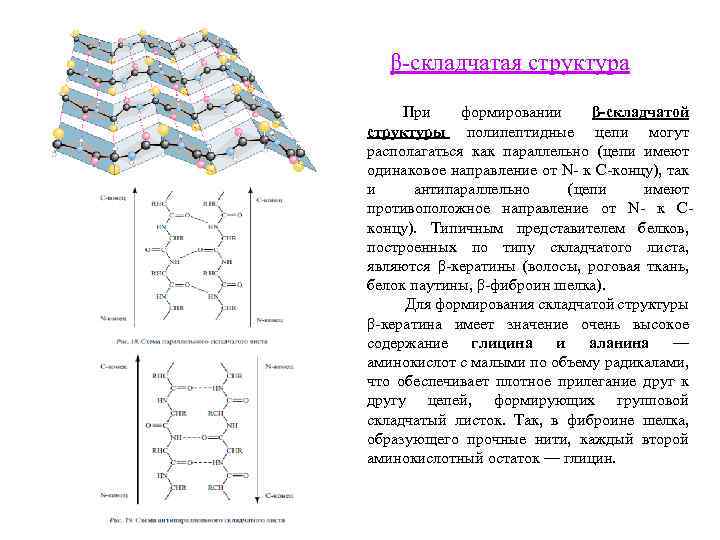
β-складчатая структура При формировании β-складчатой структуры полипептидные цепи могут располагаться как параллельно (цепи имеют одинаковое направление от N- к С-концу), так и антипараллельно (цепи имеют противоположное направление от N- к Сконцу). Типичным представителем белков, построенных по типу складчатого листа, являются β-кератины (волосы, роговая ткань, белок паутины, β-фиброин шелка). Для формирования складчатой структуры β-кератина имеет значение очень высокое содержание глицина и аланина — аминокислот с малыми по объему радикалами, что обеспечивает плотное прилегание друг к другу цепей, формирующих групповой складчатый листок. Так, в фиброине шелка, образующего прочные нити, каждый второй аминокислотный остаток — глицин.
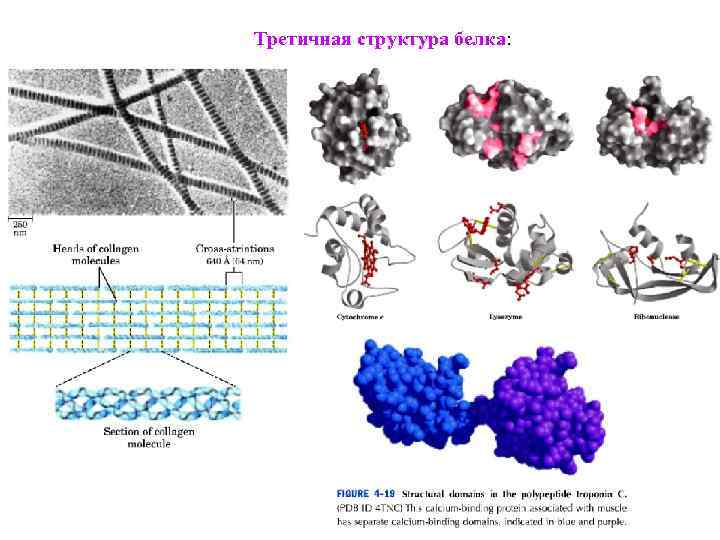
Третичная структура белка:

Четвертичная структура белка:
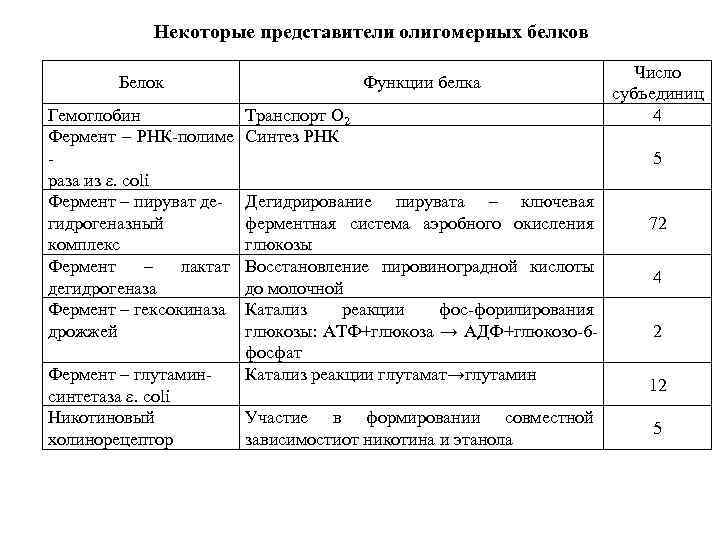
Некоторые представители олигомерных белков Белок Гемоглобин Фермент – РНК-полиме раза из ε. сoli Фермент – пируват дегидрогеназный комплекс Фермент – лактат дегидрогеназа Фермент – гексокиназа дрожжей Фермент – глутаминсинтетаза ε. сoli Никотиновый холинорецептор Функции белка Транспорт О 2 Синтез РНК Число субъединиц 4 5 Дегидрирование пирувата – ключевая ферментная система аэробного окисления глюкозы Восстановление пировиноградной кислоты до молочной Катализ реакции фос-форилирования глюкозы: АТФ+глюкоза → АДФ+глюкозо-6 фосфат Катализ реакции глутамат→глутамин Участие в формировании совместной зависимостиот никотина и этанола 72 4 2 12 5
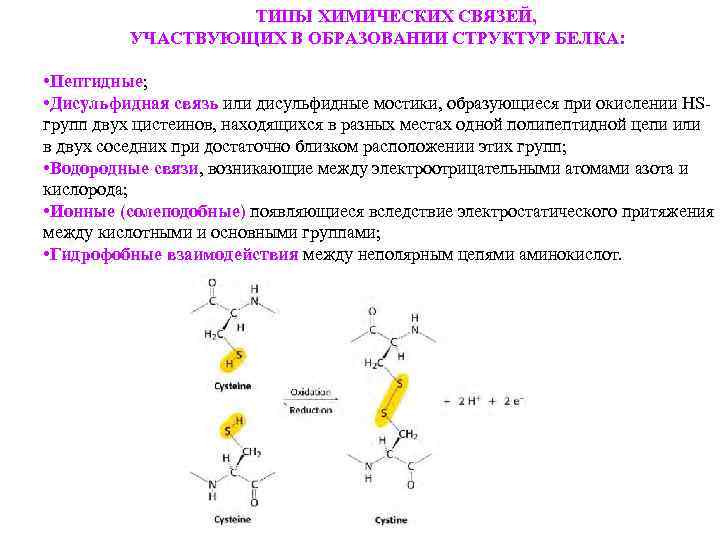
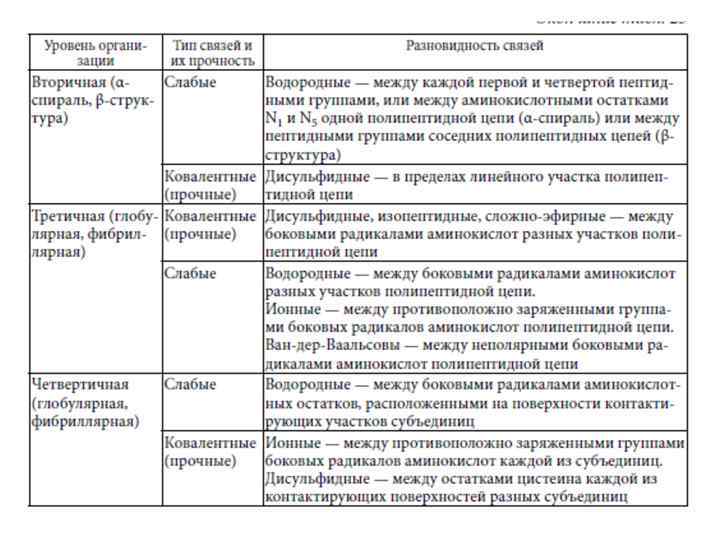
ТИПЫ ХИМИЧЕСКИХ СВЯЗЕЙ, УЧАСТВУЮЩИХ В ОБРАЗОВАНИИ СТРУКТУР БЕЛКА: • Пептидные; • Дисульфидная связь или дисульфидные мостики, образующиеся при окислении НSгрупп двух цистеинов, находящихся в разных местах одной полипептидной цепи или в двух соседних при достаточно близком расположении этих групп; • Водородные связи, возникающие между электроотрицательными атомами азота и кислорода; • Ионные (солеподобные) появляющиеся вследствие электростатического притяжения между кислотными и основными группами; • Гидрофобные взаимодействия между неполярным цепями аминокислот.
Тема 1. Общие сведения о белках.ppt