10 урок 3 белки.ppt
- Количество слайдов: 29
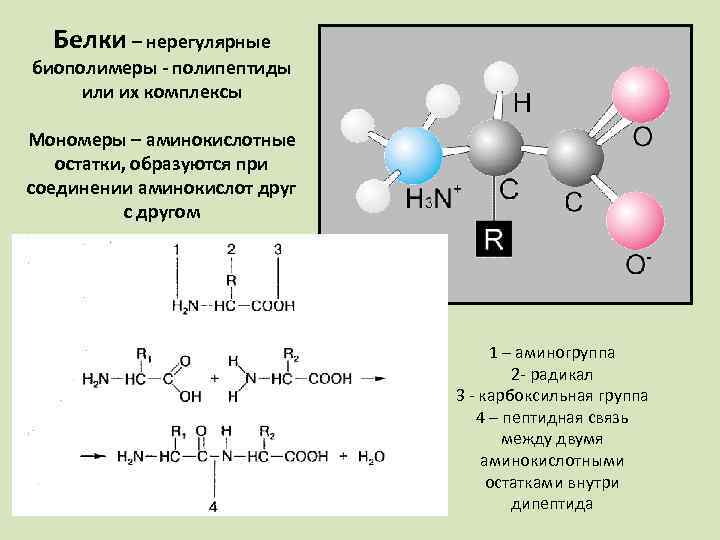
Белки – нерегулярные биополимеры - полипептиды или их комплексы Мономеры – аминокислотные остатки, образуются при соединении аминокислот друг с другом 1 – аминогруппа 2 - радикал 3 - карбоксильная группа 4 – пептидная связь между двумя аминокислотными остатками внутри дипептида
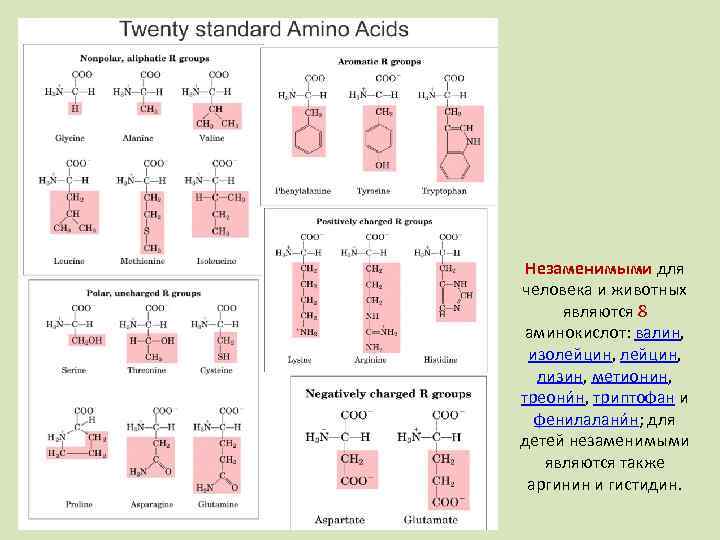
Незаменимыми для человека и животных являются 8 аминокислот: валин, изолейцин, лизин, метионин, треони н, триптофан и фенилалани н; для детей незаменимыми являются также аргинин и гистидин.
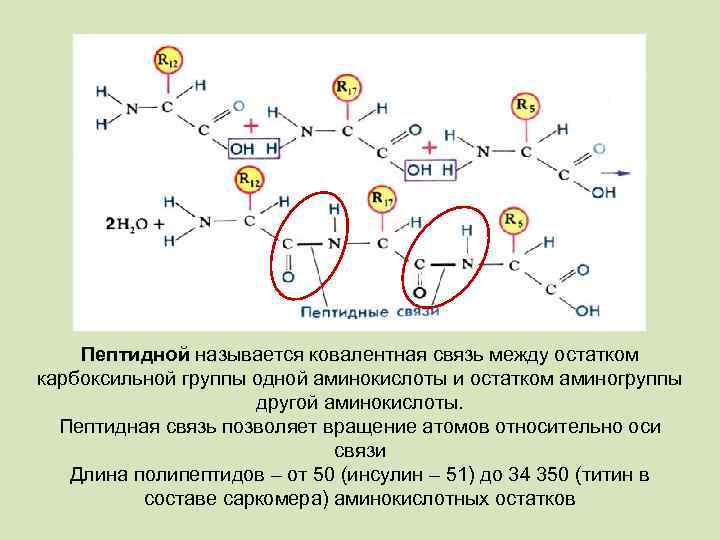
Пептидной называется ковалентная связь между остатком карбоксильной группы одной аминокислоты и остатком аминогруппы другой аминокислоты. Пептидная связь позволяет вращение атомов относительно оси связи Длина полипептидов – от 50 (инсулин – 51) до 34 350 (титин в составе саркомера) аминокислотных остатков
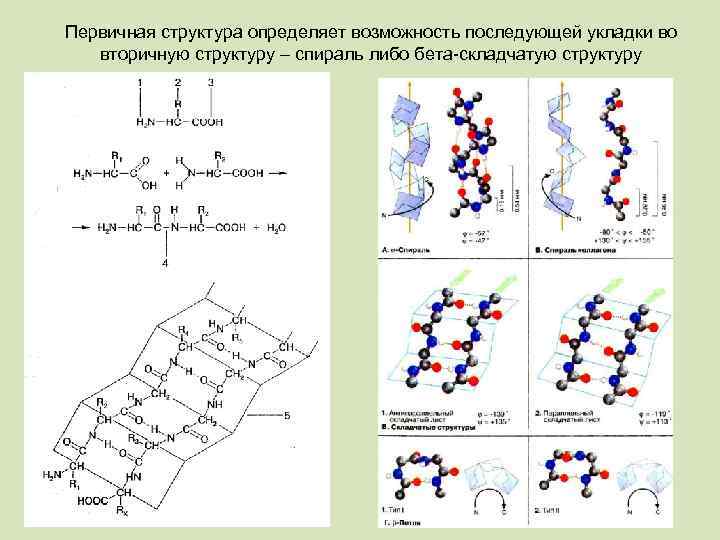
Первичная структура определяет возможность последующей укладки во вторичную структуру – спираль либо бета-складчатую структуру
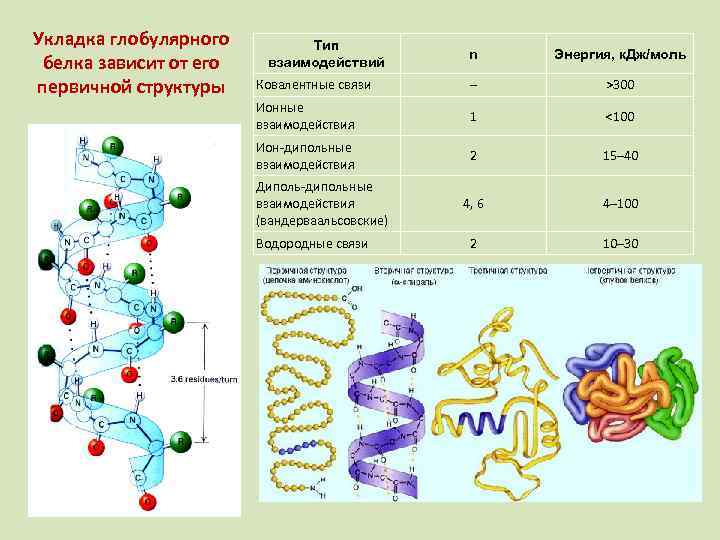
Укладка глобулярного белка зависит от его первичной структуры Тип взаимодействий n Энергия, к. Дж/моль Ковалентные связи – >300 Ионные взаимодействия 1 <100 Ион-дипольные взаимодействия 2 15– 40 4, 6 4– 100 2 10– 30 Диполь-дипольные взаимодействия (вандерваальсовские) Водородные связи
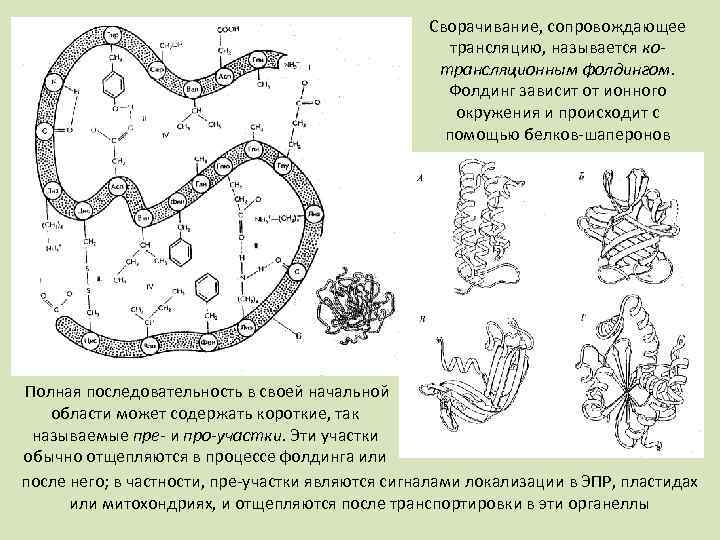
Сворачивание, сопровождающее трансляцию, называется котрансляционным фолдингом. Фолдинг зависит от ионного окружения и происходит с помощью белков-шаперонов Полная последовательность в своей начальной области может содержать короткие, так называемые пре- и про-участки. Эти участки обычно отщепляются в процессе фолдинга или после него; в частности, пре-участки являются сигналами локализации в ЭПР, пластидах или митохондриях, и отщепляются после транспортировки в эти органеллы
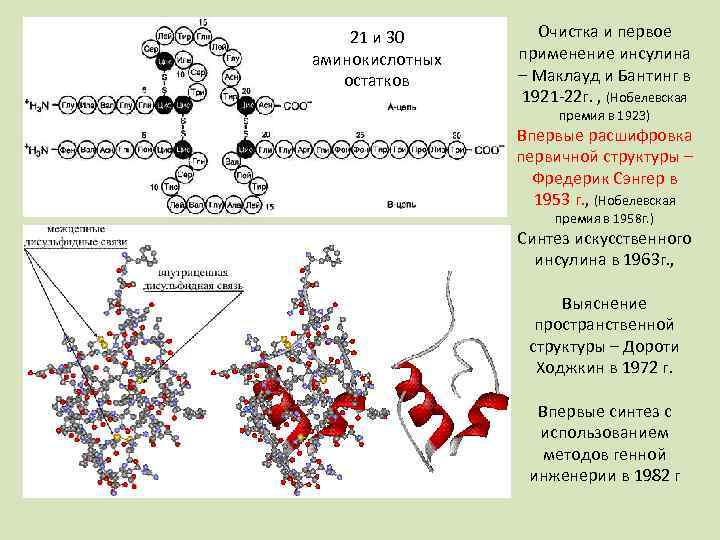
21 и 30 аминокислотных остатков Очистка и первое применение инсулина – Маклауд и Бантинг в 1921 -22 г. , (Нобелевская премия в 1923) Впервые расшифровка первичной структуры – Фредерик Сэнгер в 1953 г. , (Нобелевская премия в 1958 г. ) Синтез искусственного инсулина в 1963 г. , Выяснение пространственной структуры – Дороти Ходжкин в 1972 г. Впервые синтез с использованием методов генной инженерии в 1982 г
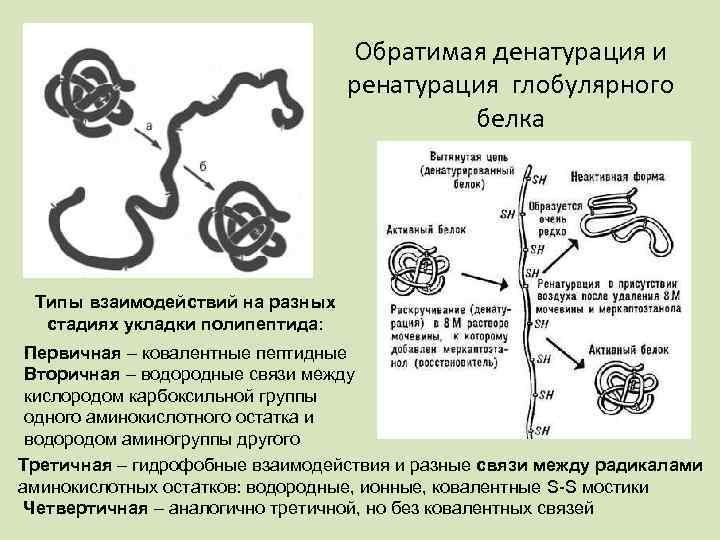
Обратимая денатурация и ренатурация глобулярного белка Типы взаимодействий на разных стадиях укладки полипептида: Первичная – ковалентные пептидные Вторичная – водородные связи между кислородом карбоксильной группы одного аминокислотного остатка и водородом аминогруппы другого Третичная – гидрофобные взаимодействия и разные связи между радикалами аминокислотных остатков: водородные, ионные, ковалентные S-S мостики Четвертичная – аналогично третичной, но без ковалентных связей
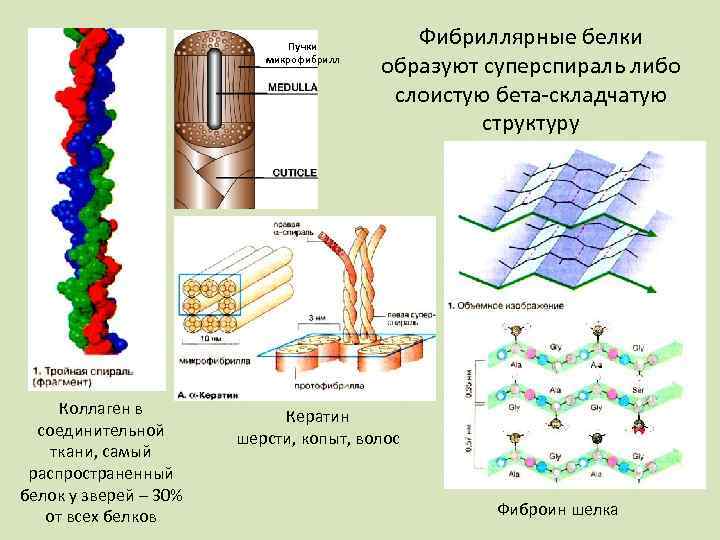
Пучки микрофибрилл Коллаген в соединительной ткани, самый распространенный белок у зверей – 30% от всех белков Фибриллярные белки образуют суперспираль либо слоистую бета-складчатую структуру Кератин шерсти, копыт, волос Фиброин шелка
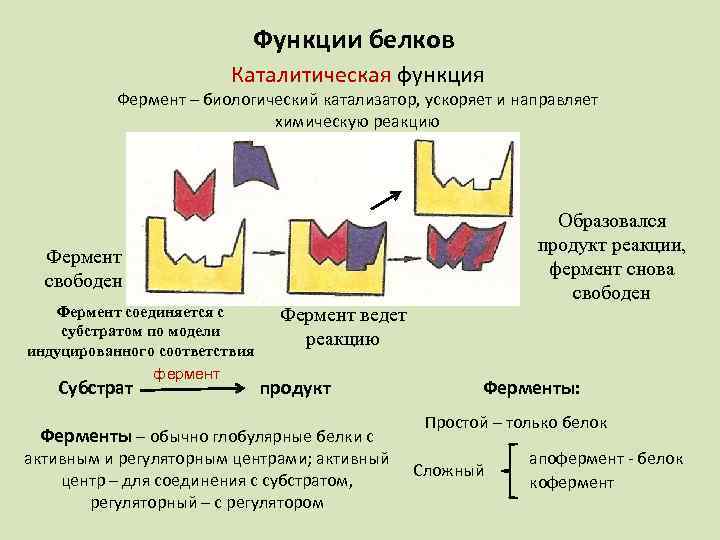
Функции белков Каталитическая функция Фермент – биологический катализатор, ускоряет и направляет химическую реакцию Образовался продукт реакции, фермент снова свободен Фермент соединяется с субстратом по модели индуцированного соответствия фермент Субстрат Фермент ведет реакцию продукт Ферменты – обычно глобулярные белки с активным и регуляторным центрами; активный центр – для соединения с субстратом, регуляторный – с регулятором Ферменты: Простой – только белок Сложный апофермент - белок кофермент
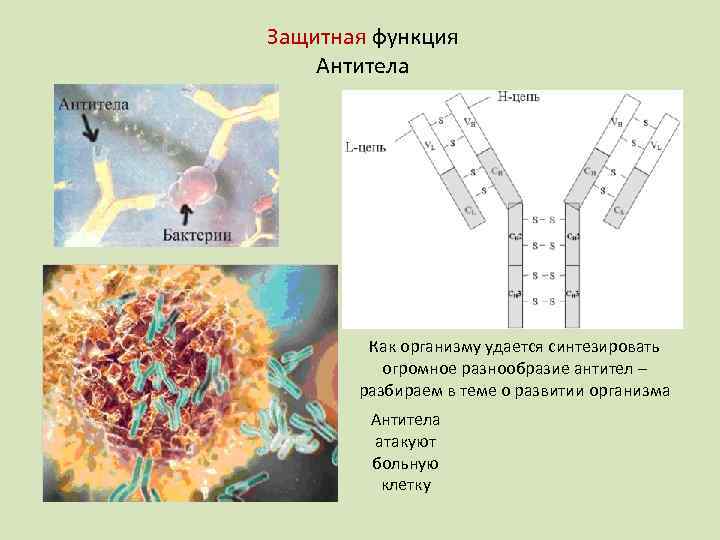
Защитная функция Антитела Как организму удается синтезировать огромное разнообразие антител – разбираем в теме о развитии организма Антитела атакуют больную клетку
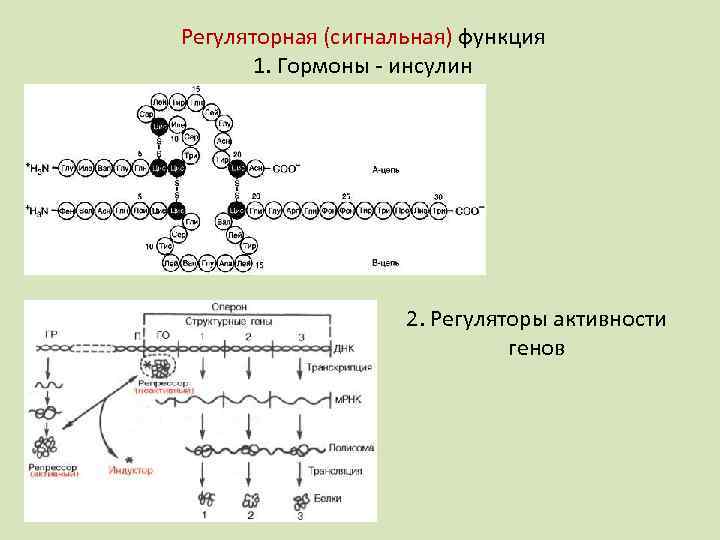
Регуляторная (сигнальная) функция 1. Гормоны - инсулин 2. Регуляторы активности генов
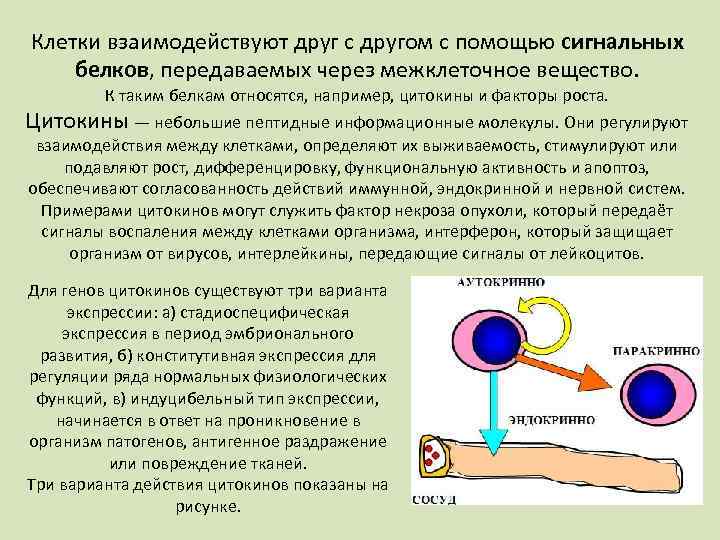
Клетки взаимодействуют друг с другом с помощью сигнальных белков, передаваемых через межклеточное вещество. К таким белкам относятся, например, цитокины и факторы роста. Цитокины — небольшие пептидные информационные молекулы. Они регулируют взаимодействия между клетками, определяют их выживаемость, стимулируют или подавляют рост, дифференцировку, функциональную активность и апоптоз, обеспечивают согласованность действий иммунной, эндокринной и нервной систем. Примерами цитокинов могут служить фактор некроза опухоли, который передаёт сигналы воспаления между клетками организма, интерферон, который защищает организм от вирусов, интерлейкины, передающие сигналы от лейкоцитов. Для генов цитокинов существуют три варианта экспрессии: а) стадиоспецифическая экспрессия в период эмбрионального развития, б) конститутивная экспрессия для регуляции ряда нормальных физиологических функций, в) индуцибельный тип экспрессии, начинается в ответ на проникновение в организм патогенов, антигенное раздражение или повреждение тканей. Три варианта действия цитокинов показаны на рисунке.
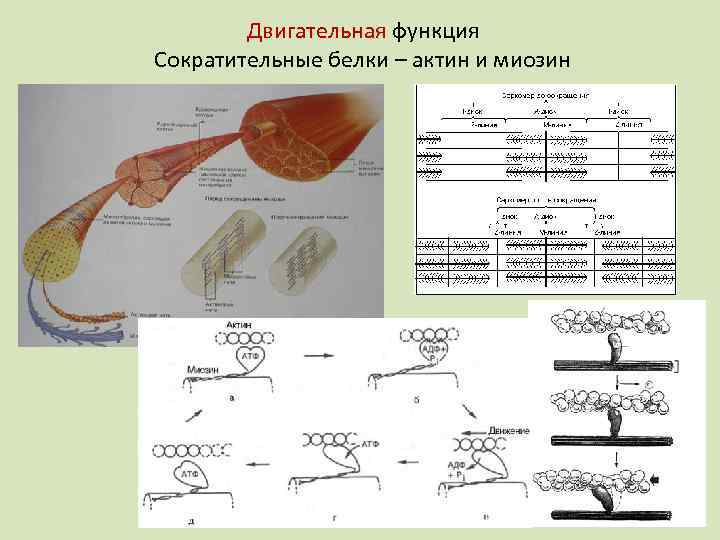
Двигательная функция Сократительные белки – актин и миозин
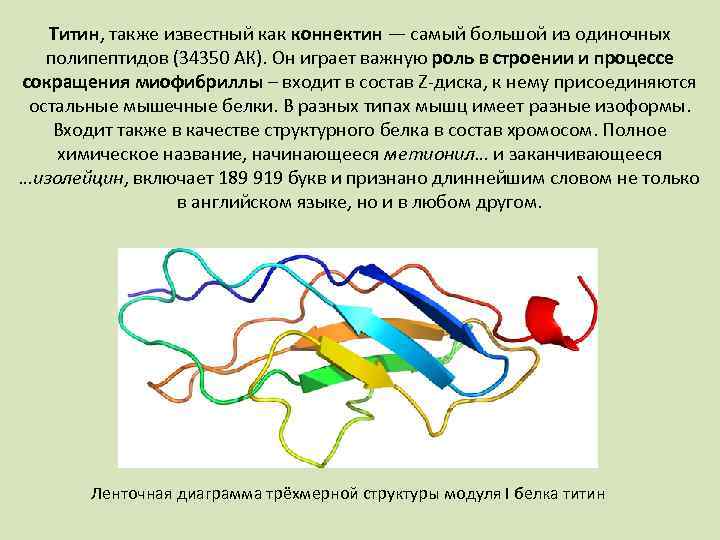
Титин, также известный как коннектин — самый большой из одиночных полипептидов (34350 АК). Он играет важную роль в строении и процессе сокращения миофибриллы – входит в состав Z-диска, к нему присоединяются остальные мышечные белки. В разных типах мышц имеет разные изоформы. Входит также в качестве структурного белка в состав хромосом. Полное химическое название, начинающееся метионил… и заканчивающееся …изолейцин, включает 189 919 букв и признано длиннейшим словом не только в английском языке, но и в любом другом. Ленточная диаграмма трёхмерной структуры модуля I белка титин
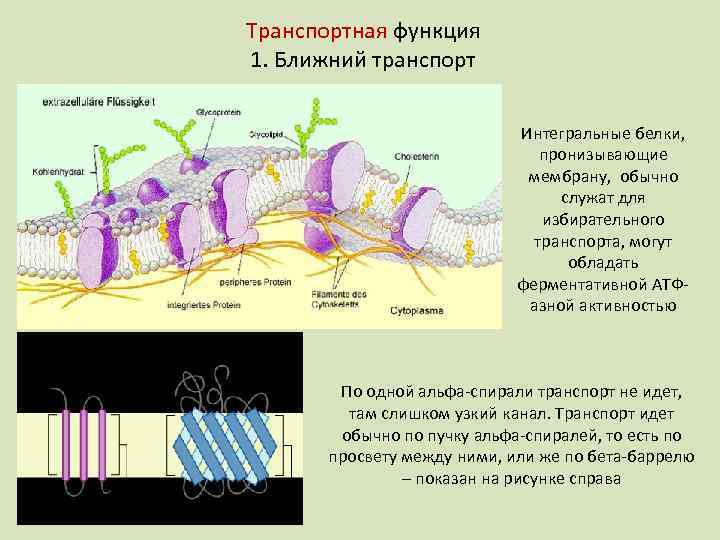
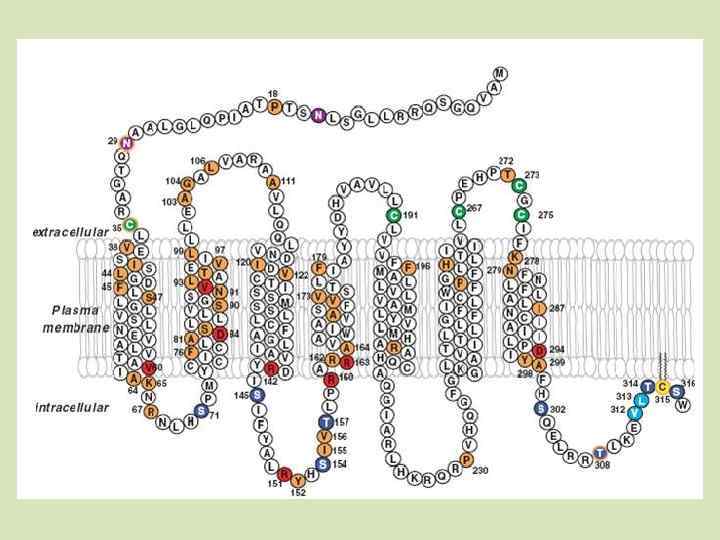
Транспортная функция 1. Ближний транспорт Интегральные белки, пронизывающие мембрану, обычно служат для избирательного транспорта, могут обладать ферментативной АТФазной активностью По одной альфа-спирали транспорт не идет, там слишком узкий канал. Транспорт идет обычно по пучку альфа-спиралей, то есть по просвету между ними, или же по бета-баррелю – показан на рисунке справа
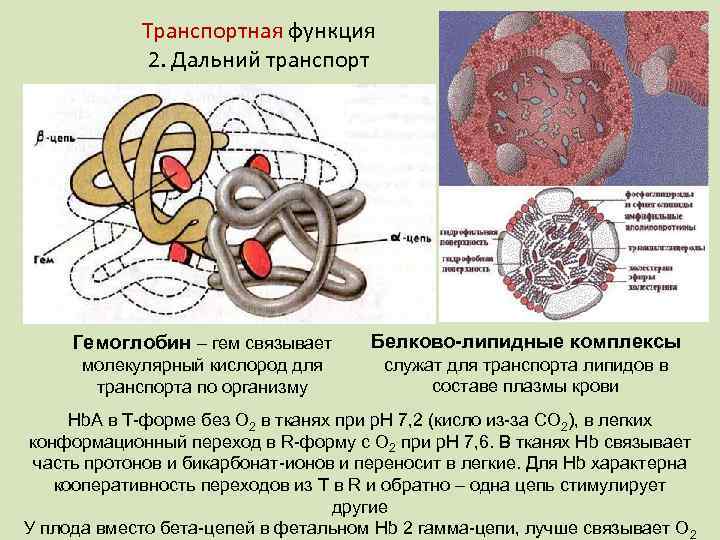
Транспортная функция 2. Дальний транспорт Гемоглобин – гем связывает Белково-липидные комплексы молекулярный кислород для транспорта по организму служат для транспорта липидов в составе плазмы крови Hb. A в Т-форме без О 2 в тканях при р. Н 7, 2 (кисло из-за СО 2), в легких конформационный переход в R-форму с О 2 при р. Н 7, 6. В тканях Нb связывает часть протонов и бикарбонат-ионов и переносит в легкие. Для Hb характерна кооперативность переходов из T в R и обратно – одна цепь стимулирует другие У плода вместо бета-цепей в фетальном Hb 2 гамма-цепи, лучше связывает О 2
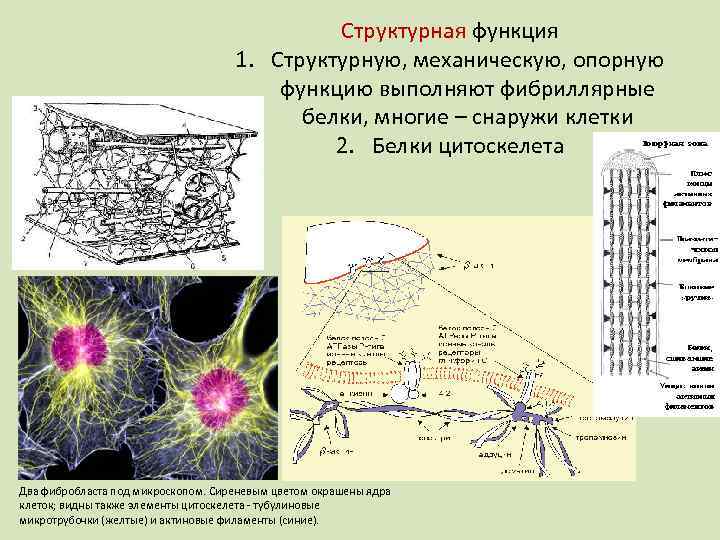
Структурная функция 1. Структурную, механическую, опорную функцию выполняют фибриллярные белки, многие – снаружи клетки 2. Белки цитоскелета Два фибробласта под микроскопом. Сиреневым цветом окрашены ядра клеток; видны также элементы цитоскелета - тубулиновые микротрубочки (желтые) и актиновые филаменты (синие).
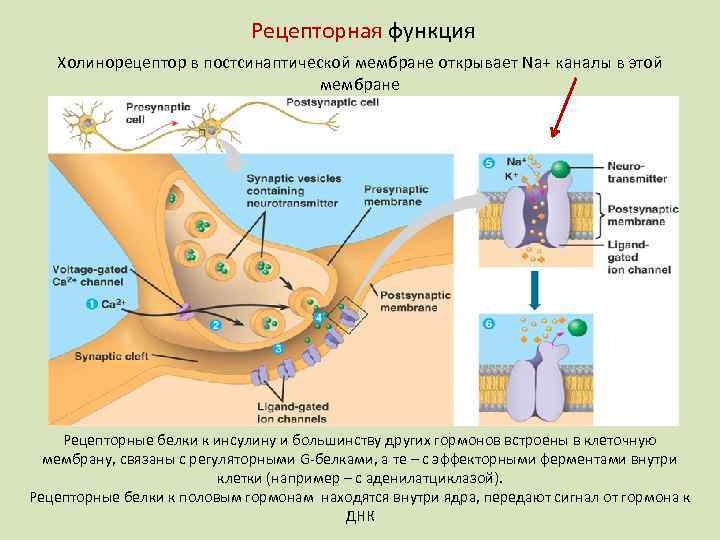
Рецепторная функция Холинорецептор в постсинаптической мембране открывает Na+ каналы в этой мембране Рецепторные белки к инсулину и большинству других гормонов встроены в клеточную мембрану, связаны с регуляторными G-белками, а те – с эффекторными ферментами внутри клетки (например – с аденилатциклазой). Рецепторные белки к половым гормонам находятся внутри ядра, передают сигнал от гормона к ДНК
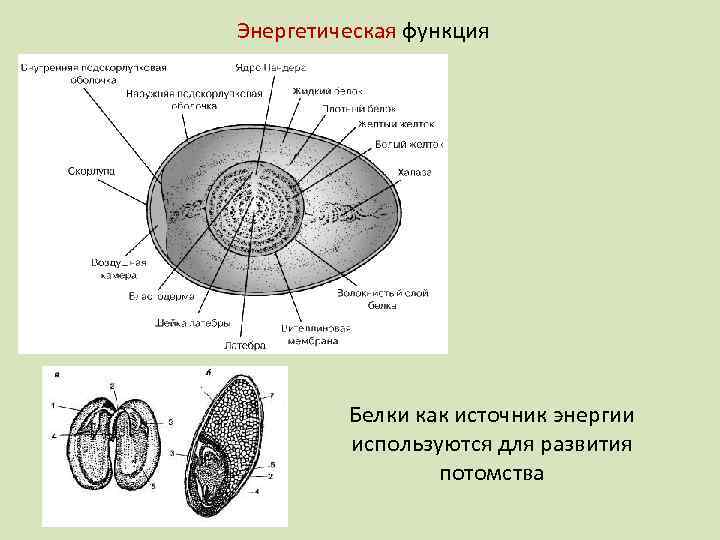
Энергетическая функция Белки как источник энергии используются для развития потомства

Классификация белков по их функции достаточно условна, потому что у эукариот один и тот же белок может выполнять несколько функций. Примеры: лизил-т. РНК-синтетаза — фермент, который не только присоединяет лизин к т. РНК, но и регулирует транскрипцию нескольких генов; миозин - двигательный белок и одновременно фермент; транспортный белок калий-натриевая АТФаза расщепляет АТФ для получения энергии

Дополнения В процессе эволюции формируется стабильная конформация белка, которая обладает минимальной свободной энергией по сравнению с другими возможными конформациями этого полипептида. Тем не менее, в клетках существует группа белков-шаперонов, функция которых — обеспечение восстановления структуры белков после повреждения, а также создание и диссоциация белковых комплексов. Концентрация многих шаперонов в клетке возрастает при резком повышении температуры окружающей среды, поэтому они относятся к группе Hsp (heat shock proteins — белки теплового шока). Важность нормальной работы шаперонов для функционирования организма видна на примере шаперона α-кристаллина, входящего в состав хрусталика глаза человека. Мутации в этом белке приводят к помутнению хрусталика из-за агрегирования белков и, как результат, к катаракте. В капиллярах покоящихся мышц, где давление О 2 составляет около 40 мм рт. ст. , большая часть кислорода возвращается в составе оксигемоглобина обратно в лёгкие. При физической работе давление О 2 в капиллярах мышц падает до 10 -20 мм рт. ст. Именно в этой области (от 10 до 40 мм рт. ст. ) располагается "крутая часть" Sобразной кривой, где в наибольшей степени проявляется свойство кооперативной работы протомеров. Следовательно, благодаря уникальной структуре каждый из рассмотренных белков приспособлен выполнять свою функцию: миоглобин - присоединять О 2, высвобождаемый гемоглобином, накапливать в клетке и отдавать в случае крайней необходимости; гемоглобин - присоединять О 2 в лёгких, где его насыщение доходит до 100%, и отдавать О 2 в капиллярах тканей в зависимости от изменения в них давления О 2
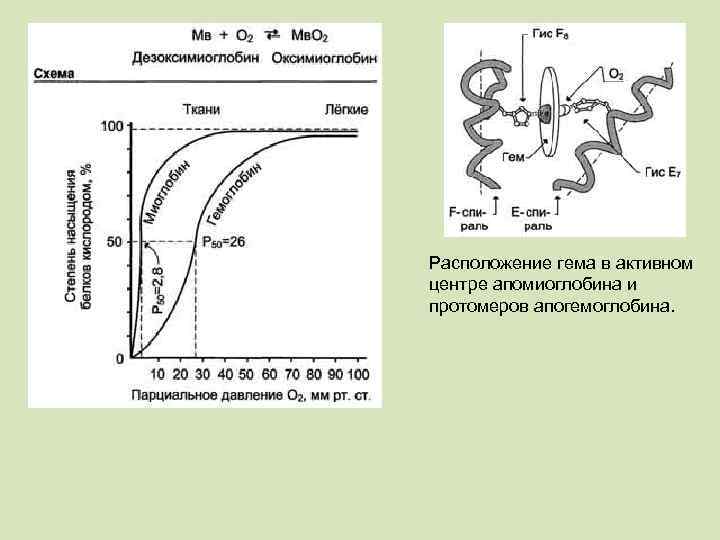
Расположение гема в активном центре апомиоглобина и протомеров апогемоглобина.

Окисление органических веществ с целью получения энергии происходит в митохондриях клеток с использованием О 2, доставляемого гемоглобином из лёгких. В результате окисления веществ образуются конечные продукты распада - СО 2 и Н 2 О, количество которых пропорционально интенсивности процессов окисления. СО 2, образовавшийся в тканях, транспортируется в эритроциты. Там под действием фермента карбангидразы происходит увеличение скорости образования Н 2 СО 3. Слабая угольная кислота может диссоциировать на Н+ и НСО 3 - СО 2 + Н 2 О - H 2 CO 3 - H+ + HCO 3 -. Равновесие реакции в эритроцитах, находящихся в капиллярах тканей, смещается вправо, так как образующиеся в результате диссоциации угольной кислоты протоны могут присоединяться к специфическим участкам молекулы гемоглобина: к радикалам Гис146 двух ? -цепей, радикалам Гис122 и концевым ? аминогруппам двух ? -цепей. Все эти 6 участков при переходе гемоглобина от окси- к дезоксиформе приобретают большее сродство к Н+ в результате локального изменения аминокислотного окружения вокруг этих участков (приближения к ним отрицательно заряженных карбоксильных групп аминокислот). Присоединение 3 пар протонов к гемоглобину уменьшает его сродство к О 2 и усиливает транспорт О 2 в ткани, нуждающиеся в нём (рис. 1 -36, А). Увеличение освобождения О 2 гемоглобином в зависимости от концентрации Н+ называют эффектом Бора (по имени датского физиолога Христиана Бора, впервые открывшего этот эффект). В капиллярах лёгких высокое парциальное давление О 2 приводит к оксигенированию гемоглобина и удалению 6 протонов. Реакция СО 2 + Н 2 О - Н 2 СО 3 - Н+ + НСО 3 - сдвигается влево и образующийся СО 2 выделяется в альвеолярное пространство и удаляется с выдыхаемым воздухом (рис. 1 -36, Б). Следовательно, молекула гемоглобина в ходе эволюции приобрела способность воспринимать и реагировать на информацию, получаемую из окружающей среды. Увеличение концентрации протонов в среде снижает сродство О 2 к гемоглобину и усиливает его транспорт в ткани (рис. 1 -37). Большая часть СО 2 транспортируется кровью в виде бикарбоната НСО 3 -. Небольшое количество СО 2 (около 1520%) может переноситься в лёгкие, обратимо присоединяясь к неионизированным концевым ? -аминогруппам. R-NH 2+ СО 2 = R-NH-COO + Н+, в результате образуется карбогемоглобин, где R - полипептидная цепь гемоглобина. Присоединение СО 2 к гемоглобину также снижает его сродство к О 2.
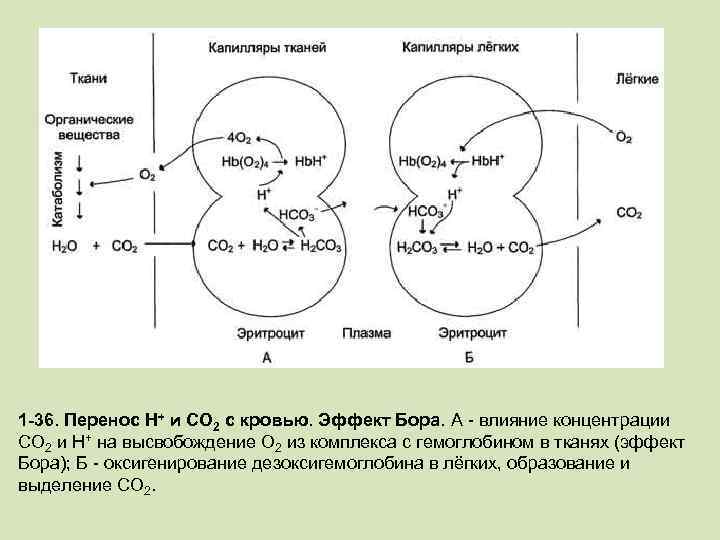
1 -36. Перенос Н+ и СО 2 с кровью. Эффект Бора. А - влияние концентрации СО 2 и Н+ на высвобождение О 2 из комплекса с гемоглобином в тканях (эффект Бора); Б - оксигенирование дезоксигемоглобина в лёгких, образование и выделение СО 2.

В молекуле гемоглобина S (так назван аномальный гемоглобин) мутантными оказались 2 ? -цепи, в которых глутамат, высокополярная отрицательно заряженная аминокислота в положении 6 была заменена валином, содержащим гидрофобный радикал. В дезоксигемоглобине S имеется участок, комплементарный другому участку таких же молекул, содержащему изменённую аминокислоту. В результате молекулы дезоксигемоглобина начинают "слипаться", образуя удлинённые фибриллярные агрегаты, деформирующие эритроцит и приводящие к образованию аномальных эритроцитов в виде серпа (рис. 1 -40). В оксигемоглобине S комплементарный участок "замаскирован" в результате изменения конформации белка. Недоступность участка препятствует соединению молекул оксигемоглобина S друг с другом. Следовательно, образованию агрегатов Hb. S способствуют условия, повышающие концентрацию дезоксигемоглобина в клетках (физическая работа, гипоксия, уменьшение р. Н, условия высокогорья, полёт на самолёте). Так как "серповидные" эритроциты плохо проходят через капилляры тканей, они часто закупоривают сосуды и создают тем самым локальную гипоксию. Это повышает концентрацию дезоксигемоглобина S в эритроцитах, скорость образования агрегатов гемоглобина S и ещё большую деформацию эритроцитов. Нарушение доставки О 2 в ткани вызывает боли "даже некроз клеток в данной области. Серповидно-клеточная анемия - гомозиготное рецессивное заболевание; проявляется только в том случае, когда от обоих родителей наследуются 2 мутантных гена ? -цепей глобина. После рождения ребёнка болезнь не проявляется до тех пор, пока значительные количества Hb. F не заместятся на Hb. S. У больных выявляют клинические симптомы, характерные для анемии: головокружение и головные боли, одышка, учащённое сердцебиение, боли в конечностях, повышенную восприимчивость к инфекционным заболеваниям. Гетерозиготные индивидуумы, имеющие один нормальный ген НЬА, а другой ген Hb. S, в крови имеют лишь следовые количества серповидных клеток и нормальную продолжительность жизни; клинические симптомы болезни у них обычно не проявляются. 1 2 3 4 5 6 7 8 Нв. А ? цепь Вал- Гис- Лей- Тре- Про- Глу - Лиз- He. S ? цепь Вал- Гис- Лей- Тре- Про- Вал- Глу - Лиз-

1 -40. Ассоциация молекул дезоксигемоглобина S. Для диагностики наличия Hb. S в эритроцитах человека используют метод электрофореза, основанного на движении заряженных белков в электрическом поле. Так как в Hb. S отрицательно заряженные группы глутамата в ? -цепях заменены незаряженным валином, Hb. S в щелочной среде будет двигаться медленнее, чем НЬА. Высокая частота гена Hb. S среди жителей Африки (до 40% населения в некоторых районах) обусловлена тем, что гетерозиготы менее чувствительны к малярии, чем люди с нормальным гемоглобином A. Plasmodium falciparum - возбудитель малярии, облигатную часть своего жизненного цикла он проводит в эритроцитах. Так как эритроциты гетерозиготных по Hb. S людей имеют более короткий срок жизни, чем нормальные эритроциты, возбудитель малярии не успевает закончить необходимую стадию развития. Это создаёт избирательное преимущество для гетерозиготных по Hb. S людей в тех областях, где малярия вызывает гибель многих людей.

Внутриклеточный транспорт и сортировка белков Синтезируемые в цитоплазме на рибосомах белки должны попадать в разные компартменты клетки — ядро, митохондрии, ЭПР, аппарат Гольджи, лизосомы и др. , а некоторые белки должны попасть во внеклеточную среду. Для попадания в определённый компартмент белок должен обладать специфической меткой. В большинстве случаев такой меткой является часть аминокислотной последовательности самого белка (лидерный пептид, или сигнальная последовательность белка). В некоторых случаях меткой служат посттрансляционно присоединённые к белку олигосахариды. Транспорт белков в ЭПР осуществляется по мере их синтеза, так как рибосомы, синтезирующие белки с сигнальной последовательностью для ЭПР, «садятся» на специальные транслокационные комплексы на мембране ЭПР. Из ЭПР в аппарат Гольджи, а оттуда в лизосомы, на внешнюю мембрану или во внеклеточную среду белки попадают путём везикулярного транспорта. В ядро белки, обладающие сигнальной последовательностью для ядра, попадают через ядерные поры. В митохондрии и хлоропласты белки, обладающие соответствующими сигнальными последовательностями, попадают через специфические белковые поры-транслокаторы при участии шаперонов.
10 урок 3 белки.ppt