
Белки

История нахождения белков 1. Еще в 80 -х гг. XX в. русский биохимик Д. Я. Данилевский указал на наличие пептидных групп в белковой молекуле. 2. В начале XX в. немецкий ученый Э. Фишер выдвинул полипептидную теорию, согласно которой молекулы белка представляют собой длинные цепи остатков аминокислот, соединенных пептидными (амидными) связями. 3. Э. Фишеру и другим ученым удалось синтетически получить полипептиды, в молекулы которых входили различные аминокислотные остатки, соединенные пептидными связями. 4. Полипептидная теория строения белка в настоящее время считается общепризнанной.

Белки в природе: 1) белки представляют наиболее важную составную часть организмов; 2) они содержатся в протоплазме и ядре всех растительных и животных клеток и являются главными носителями жизни; 3) по определению Ф. Энгельса, «жизнь есть способ существования белковых тел» ; 4) молекулярная масса белков выражается десятками и сотнями тысяч, а у некоторых белков достигает нескольких миллионов.

Функции белков в организме 1. Белки служат тем пластическим материалом, из которого построены опорные, мышечные и покровные ткани. 2. С помощью белков осуществляется перенос веществ в организме, например доставка кислорода из легких в ткани и выведение образовавшегося оксида углерода (IV). 3. Белки-ферменты катализируют в организме многочисленные химические реакции. 4. Гормоны (среди них есть вещества белковой природы) обеспечивают согласованную работу органов. 5. В виде антител, вырабатываемых организмом, белки служат защитой от инфекции. Различных белковых веществ в организме тысячи, и каждый белок выполняет строго определенную функцию. 6. Для любой химической реакции, протекающей в организме, существует свой отдельный белок-катализатор (фермент).

Состав и строение белков 1. При гидролизе любого белка получается смесь α-аминокислот, причем наиболее часто встречаются в составе белков двадцать аминокислот. 2. Молекулы аминокислот содержат в радикале группы атомов: – SH, – ОН, – СООН, – NH 2 и даже бензольное кольцо.
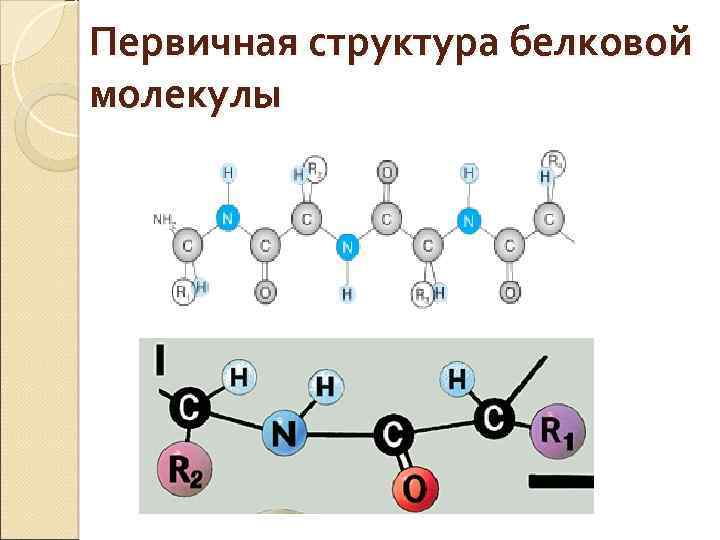
Первичная структура белковой молекулы
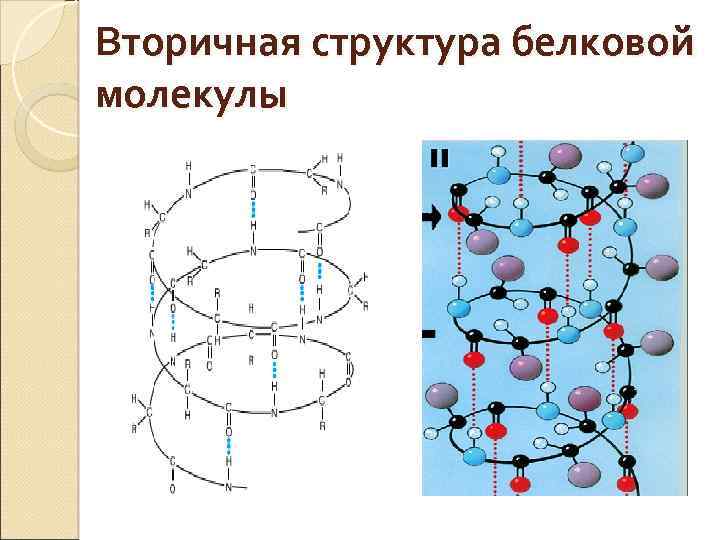
Вторичная структура белковой молекулы

Третичная структура белковой молекулы
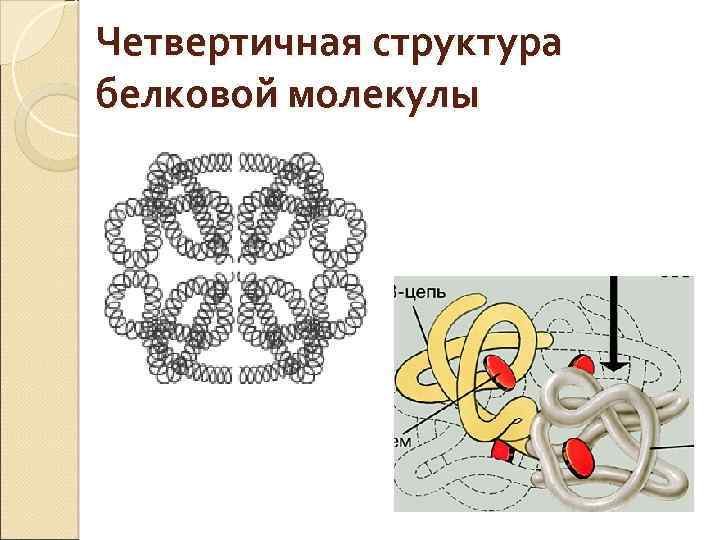
Четвертичная структура белковой молекулы

Свойства белков Имея сложное строение, белки обладают, естественно, и весьма разнообразными свойствами: 1) одни белки, например белок куриного яйца, растворяются в воде, образуя при этом коллоидные растворы, другие – в разбавленных растворах солей; 2) некоторые белки совсем не обладают свойством растворимости;

Свойства белков 1) наличие в молекулах белков (в радикалах аминокислотных звеньев) групп – СООН и – NН 2 делает белки амфотерными; 2) важным свойством белков является способность к гидролизу. Гидролиз проводится при действии ферментов или путем нагревания белка с раствором кислоты или щелочи. В результате гидролиза образуются α-аминокислоты. 3) Под влиянием ряда факторов (нагревания, действия радиации, даже сильного встряхивания) может нарушиться конфигурация молекулы. Этот процесс называется денатурацией белка.

Сущность денатурации белка 1) состоит в разрушении водородных связей, солевых и иных мостиков, поддерживающих вторичную и третичную структуру молекулы; 2) она теряет специфическую пространственную форму, дезориентируется и утрачивает свое биологическое действие. 3) денатурация белка происходит при варке яиц, приготовлении пищи и т. д. ; 4) сильное нагревание вызывает не только денатурацию белков, но и их разложение с выделением летучих продуктов. 1 2 3

Превращение белков в организме 1. Животные организмы строят свои белки из аминокислот тех белков, которые они получают с пищей. Поэтому наряду с жирами и углеводами белки – обязательный компонент нашей пищи. 2. В процессе переваривания пищи происходит гидролиз белков под влиянием ферментов. В желудке они расщепляются на более или менее крупные «осколки» – пептиды, которые далее в кишечнике гидролизуются до аминокислот. Последние всасываются ворсинками кишечника в кровь и поступают во все ткани и клетки организма. В отличие от углеводов и жиров, аминокислоты в запас не откладываются.

Цветные реакции белков 1) Ксантопротеиновая реакция 2) Биуретовая реакция

Проблема синтеза белков Причины невозможности получения белков синтетическим путем. 1. Причина – в чрезвычайной сложности белковых молекул. 2. Чтобы получить заданный белок, необходимо выяснить его аминокислотный состав, установить первичную структуру, т. е. порядок чередования аминокислот, определить пространственную конфигурацию белковой молекулы и искусственно воспроизвести все это. 3. Установление аминокислотного состава белков путем их гидролиза – наиболее легкая задача. 4. Первый белок, у которого удалось расшифровать первичную структуру, был инсулин (1954 г. ), регулирующий содержание сахара в крови. 5. На установление порядка чередования аминокислот в инсулине было затрачено почти десять лет. 6. Его молекула состоит из двух полипептидных цепочек, одна из которых содержит двадцать один аминокислотный остаток, а другая – тридцать.

В настоящее время искусственное получение белков осуществляется посредством микробиологического синтеза 1) размножаясь в соответствующей питательной среде, некоторые микроорганизмы могут создавать обильную белковую массу; 2) на отходах гидролизного производства спирта из древесины, например, выращивают кормовые дрожжи для животноводства; 3) быстро развивается микробиологический синтез белков на основе использования парафинов нефти; 4) при помощи микроорганизмов производятся и другие вещества, например некоторые аминокислоты, витамины; 5) использование продуктов микробиологического синтеза в животноводстве позволяет значительно повышать его продуктивность.

Домашнее задание Подготовить сообщения на тему: 1) ДНК 2) РНК 3) Химия и здоровье человека