НИП "Белки и жизнь".ppt
- Количество слайдов: 28

Белки и жизнь Исполнитель: ученица 9 «В» МБОУ СОШ № 7 Жигалова Олеся

«Повсюду, где мы встречаем жизнь, мы находим, что она связана с каким-либо белковым телом» . Ф. Энгельс Гипотезы Белкам принадлежит особая роль в жизнедеятельности живых организмов. Белки – это польза или вред для моего организма?

Объект моего исследования Обнаружение белка в некоторых продуктах питания

Предмет моей работы Качественные реакции на белки

Цель моего реферата Выявление положительных свойств белков и влияния их на организм человека

Задачи Познакомиться с историей изучения белков. n Изучить физические, химические, биологические свойства белков. n Изучить строение и свойства аминокислот, входящих с состав белков. n Познакомиться с классификацией и функциями белков. n Изучить синтез белков. n Рассмотреть влияние недостатка и избытка белков на организм человека. n Ознакомиться с наиболее распространенными заболеваниями, требующими снижения или повышенного содержания поступления белков с пищей. n Выявить продукты питания, содержащие повышенное и сниженное количество белков. n

ИСТОРИЯ ИЗУЧЕНИЯ БЕЛКОВ nв XVIII веке - белки были выделены в отдельный класс биологических молекул в XVIII веке в результате работ французского химика Антуана Фуркруаи других учёных. n 1836 год - голландский химик Геррит Мульдер в 1836 году провёл анализ состава белков и выдвинул гипотезу, что практически все белки имеют сходную эмпирическую формулу. Ученый предложил первую модель химического строения белков. n 1838 год - предложен шведским химиком Якобом Берцелиусом термин «протеин» для обозначения подобных молекул. n. Конец XIX века - исследовано большинство аминокислот, которые входят в состав белков. n 1894 год - немецкий физиолог Альбрехт Коссель выдвинул теорию, согласно которой именно аминокислоты являются основными структурными элементами белков.

ИСТОРИЯ ИЗУЧЕНИЯ БЕЛКОВ nначало XX века немецкий химик Эмиль Фишер экспериментально доказал, что белки состоят из аминокислотных остатков, соединённых пептидными связями. Он же осуществил первый анализ аминокислотной последовательности белка и объяснил явление протеолиза. n 1926 год - американский химик Джеймс Самнер показал, что фермент уреаза является белком. n 1933 год - Лайнус Полинг считается первым учёным, который смог успешно предсказать вторичную структуру белков. n. Позднее Уолтер Каузман, опираясь на работы Кая Линдерстрём. Ланга, внёс весомый вклад в понимание законов образования третичной структуры белков и роли в этом процессе гидрофобных взаимодействий. n 1949 году - Фредерик Сенгер определил аминокислотную последовательность инсулина, продемонстрировав таким способом, что белки - это линейные полимеры аминокислот, а не их разветвлённые.

СВОЙСТВА БЕЛКОВ Размер белка может измеряться в числе аминокислот или в дальтонах (молекулярная масса), чаще из-за относительно большой величины молекулы в производных единицах - килодальтонах (к. Да). n Белки дрожжей, в среднем, состоят из 466 аминокислот и имеют молекулярную массу 53 к. Да. n. Самый большой из известных в настоящее время белков - титин - является компонентом саркомеров мускулов; молекулярная масса его различных изоформ варьирует в интервале от 3000 до 3700 к. Да, он состоит из 38 138 аминокислот. Гемоглобин - С 3032 H 4816 O 872 N 780 S 8 Fe 4 Mr белка яйца = 36 000, Mr белка мышц = 1 500 000 n

СВОЙСТВА БЕЛКОВ n. Белки различаются по степени растворимости в воде, но большинство белков в ней растворяются. К нерастворимым относятся, например, кератин и фиброин. n. Денатурация белков Денатурация – нарушение природной структуры белка под действием нагревания и химических реагентов. а) высокая или низкая температура б) механическое воздействие; в) облучение; г) яды; д) действие спирта; е) действие солей тяжелых металлов (Pb, Hg и др. ) Денатурированный белок теряет свои биологические свойства.

АМИНОКИСЛОТЫ, ВХОДЯЩИХ В СОСТАВ БЕЛКОВ n. Белки - полимерные молекулы, в которых мономерами служат аминокислоты. n. Аминокислота (amino acid) – органическое соединение, которое является основной составляющей всех белков. В состав белков входят: углерод – 51 - 55%, кислород - 21 – 24%, азот - 15 -18%, водород - 6, 5 -7%, сера - 0, 3 -1, 5%, фосфор – 0, 5 -1, 7%, Железо – 0, 1 -1, 1%, другие элементы.

АМИНОКИСЛОТЫ, ВХОДЯЩИХ В СОСТАВ БЕЛКОВ Известно около 80 природных аминокислот, но в обычной пище встречаются лишь 22 из них. n В составе белков в организме человека встречают только 20 α-аминокислот, аминокислотный состав белков определяется генетическим кодом. n Считается, что 12 аминокислот может синтезировать и человек, поэтому они называются заменимыми. Остальные 10 аминокислот в обычных условиях человеческий организм не производит. Их называют незаменимыми. n Помимо природных, существуют и синтетические аминокислоты. Из такой искусственной аминокислоты состоит, например, капрон. n

УРОВНИ ОРГАНИЗАЦИИ БЕЛКОВ. СТРУКТУРА БЕЛКОВ n n n Все белки являются полипептидами, но не всякий полипептид является белком. Каждый белок имеет свое специфическое строение. Пептиды и белки различают в зависимости от величины молекулярной массы. Условно считают, что пептиды содержат в молекуле до 100 (соответствует молекулярной массе до 10000), а белки - свыше 100 аминокислотных остатков (молекулярная масса от 10000 до нескольких миллионов). В пептидах различают олигопептиды, содержащие в цепи не более 10 аминокислотных остатков, и полипептиды, содержащие до 100 аминокислотных остатков.

Белки Жизнь – это форма существования белковых тел n. Белок – это мышцы, соединительные ткани (сухожилия, связки, хрящи). n Белковые молекулы включены в состав костной ткани. n. Из особых форм белка сотканы волосы, ногти, зубы, кожный покров. n. Из белковых молекул образуются отдельные очень важные гормоны, от которых зависит здоровье. n. Большинство ферментов также включают белковые фрагменты, а от ферментов зависит качество и интенсивность происходящих в организме физиологических и биохимических процессов. n. Содержание белков в различных тканях человека неодинаково. Так, мышцы содержат до 80% белка, селезенка, кровь, легкие – 72%, кожа – 63%, печень – 57%, мозг – 15%, жировая ткань, костная и ткань зубов – 14– 28%.

Строение белков В начале 20 века Э. Фишер в результате гидролиза белковые молекул получил смесь аминокислот и выдвинул полипептидную теорию. Белки образуются в результате реакции поликонденсации. Подобная реакция происходит в молекулярной машине по образованию белка -рибосоме. H 2 N – CH – COОН │ CH 3 аланин + Н – N – CH - COOH → │ │ H CH 3 аланин H 2 N –CH – C – N – CH – COOH + Н 2 О │ ║ | │ CH 3 О Н CH 3 дипептид
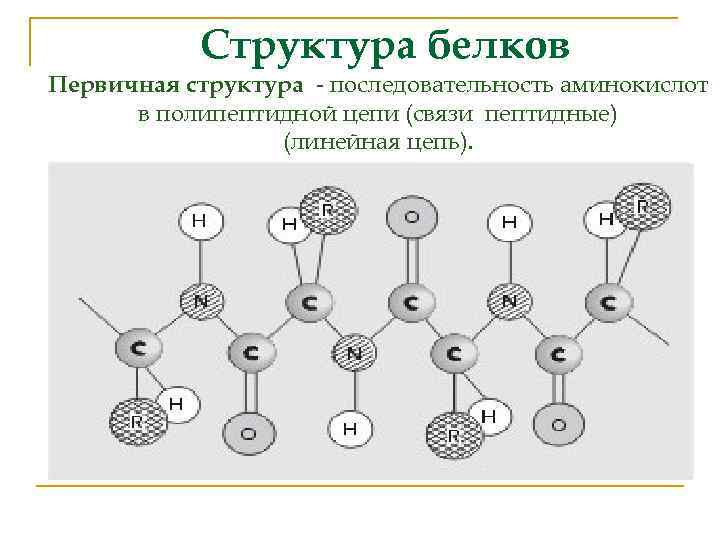
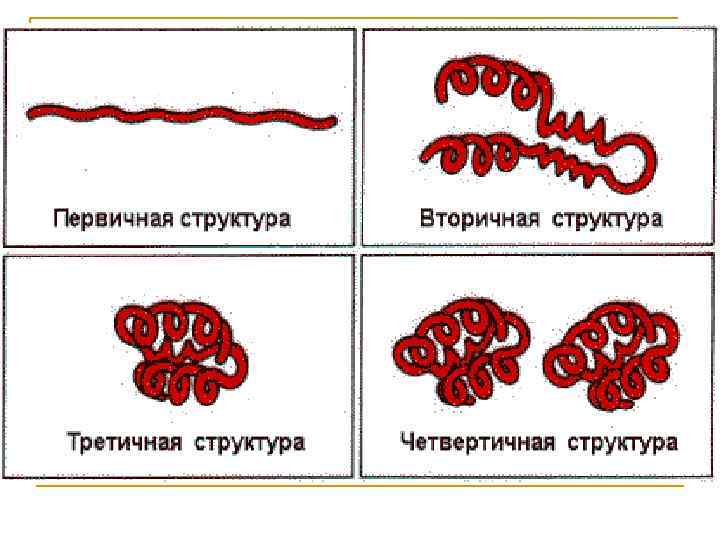
Структура белков Первичная структура - последовательность аминокислот в полипептидной цепи (связи пептидные) (линейная цепь).
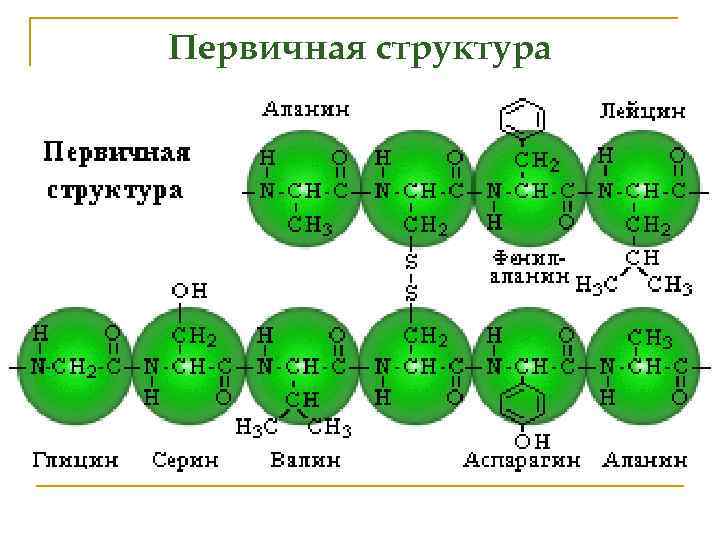
Первичная структура
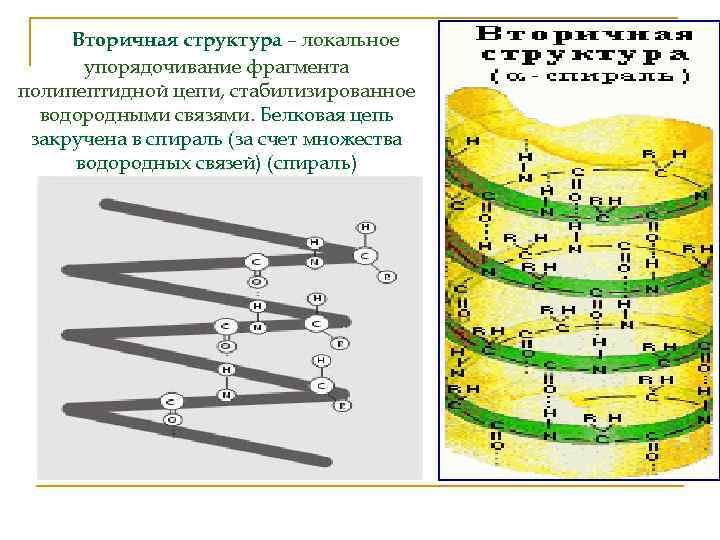
Вторичная структура – локальное упорядочивание фрагмента полипептидной цепи, стабилизированное водородными связями. Белковая цепь закручена в спираль (за счет множества водородных связей) (спираль)

Третичная структура – реальная трехмерная конфигурация, которую принимает в пространстве закрученная спираль (за счет гидрофобных связей), у некоторых белков – S–S-связи (бисульфидные связи). Структурно состоит из элементов вторичной структуры, стабилизированных различными типами взаимодействий. (клубок)

Третичной структурой объясняется специфичность белковой молекулы и ее биологическая активность.
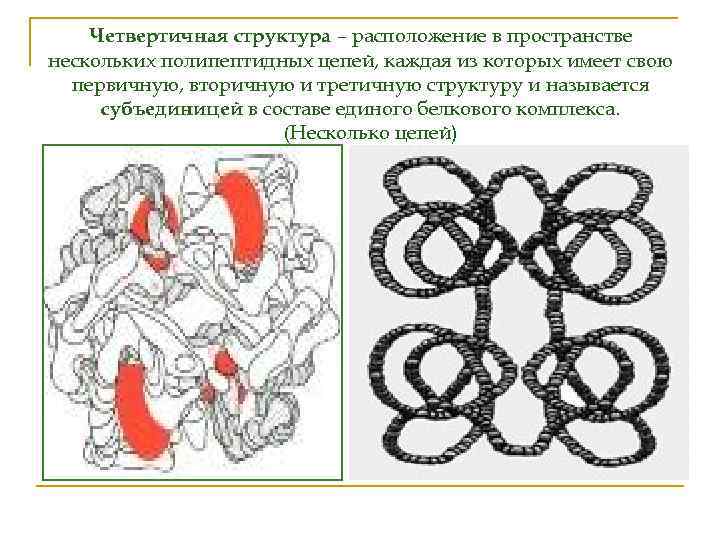
Четвертичная структура – расположение в пространстве нескольких полипептидных цепей, каждая из которых имеет свою первичную, вторичную и третичную структуру и называется субъединицей в составе единого белкового комплекса. (Несколько цепей)

Функции белков Строительная (структурная, пластическая) – белки участвуют в образовании оболочки клетки, органоидов и мембран клетки. n Каталитическая – все клеточные катализаторы – белки (активные центры фермента). n Транспортная – транспортировка необходимых химических элементов, соединений в самые отдаленные участки тела. n Двигательная (моторная) - сократительные белки вызывают всякое движение. n Транспортная – белок крови гемоглобин присоединяет кислород и разносит его по всем тканям. n Защитная – выработка белковых тел и антител для обезвреживания чужеродных веществ. n Рецепторная (сигнальная)– реакция на внешний раздражитель. n Запасная (резервная) – это белки, которые запасаются в качестве источника энергии в семенах растений и яйцеклетках животных. n Энергетическая – 1 г белка эквивалентен 17, 6 к. Дж, при окислении 1 г белка дает 16, 7 к. Дж. n
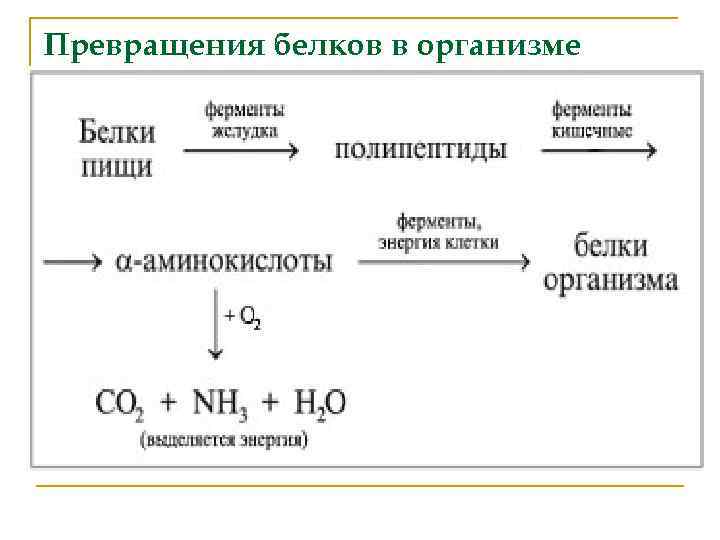
Превращения белков в организме n

Цветные реакции на белки 1. Ксантопротеиновая – взаимодействие белков с концентрированной азотной кислотой, которое сопровождается появлением желтой окраски. 2. Биуретовая – взаимодействие слабощелочных растворов белков с раствором сульфата меди (II), в результате которой появляется фиолетово-синяя окраска.

РЕЗУЛЬТАТЫ ЭКСПЕРИМЕНТА Провела качественные реакции на белки. Я выяснила, что яичный альбумин, мясной, рыбный бульоны содержит белки. В овощном бульоне белков не обнаружено. n Биуретовая реакция показала, что в мясном и рыбном бульонах, яичном альбумине действительно присутствуют белки. Фиолетовый цвет медного комплекса с белками в условиях проведения биуретовой реакции указывает на преобладание в сложных белковых частицах трипептидных группировок. n Ксантопротеиновая реакция обнаруживает наличие в белках мясного, рыбного бульонов и яичного альбумина одиночных или конденсированных ароматических ядер, т. е. остатков таких кислот, как: фенилаланин, тирозин и другие. n Я провела реакции осаждения белков тяжелыми металлами. В результате опыта образуются осадки труднорастворимых солеобразных соединений белка. Опыт иллюстрирует применение белка как противоядия при отравлении солями тяжелых металлов. n

ВЫВОДЫ В ходе работы были подробно изучены строение аминокислот, белков, их физические и биологические свойства, особенности белкового обмена у человека. Подробнее я рассмотрела наиболее распространенные заболевания, требующие повышенного и низкого поступления белков с пищей. n В ходе проведенного исследования я выявила по литературным источникам имеющуюся информацию о цветных качественных реакциях на белковые аминокислоты; выполнила ряд перечисленных реакций и составила базу данных. Эта база может быть использована в школьной практике как в теоретическом плане, так и в практическом, потому что. я привожу краткие, но подробные описания выполнения всех опытов. n Из предложенных качественных реакций каждая практически осуществима в школьном курсе химии и биологии, имеет важное практическое значение. n Были проведены качественные реакции по обнаружению белков в различных растворах. Исследовала денатурацию различных белков. n Я считаю, что выбранная мной тема очень актуальна, потому что белковые тела играют выдающуюся роль и в построении живой материи, и в осуществлении процессов жизнедеятельности. Она всегда остается современной, потому что в любую эпоху человеку необходимы не только знания о белках, но и практические рекомендации по выбору продуктов питания. n

Значение белков n n n Отдельные белки находят применение в народном хозяйстве, например белки шерсти, шелка, кожи и рогов животных. Выяснение структуры белков, их многообразных функций в организме позволяет понять механизм наследственности, что в свою очередь, имеет большое значение для выведения высокопродуктивных пород животных и сортов растений. Изучение белков важно и для выяснения природы заболеваний, наблюдаемых у человека и животных.
НИП "Белки и жизнь".ppt