Белки и аминокислоты.ppt
- Количество слайдов: 37

Белки и аминокислоты. Классификация, структура

• 1. Белки, структура белков, связи. • 2. Аминокислоты. Классификация аминокислот. • 3. Разделение, выделение и идентификация белков. • 4. Анализ аминокислотных последовательностей: определение первичной структуры.

. 1. Белки, структура белков, связи. • Белки называют также протеинами (греч. «протео» – занимаю 1 -е место). Все основные функции организма связаны со специфическими белками. Они присутствуют в каждой клетке и каждом клеточном органоиде.

• Свойства белков, на которых основана классификация, крайне разнообразны. Так, склеропротеины (кератин и коллаген) нерастворимы и обладают фибриллярной структурой.
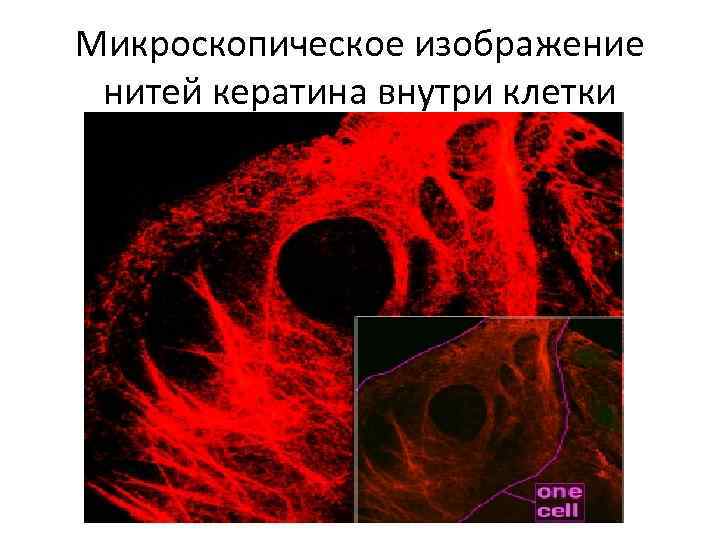
Микроскопическое изображение нитей кератина внутри клетки
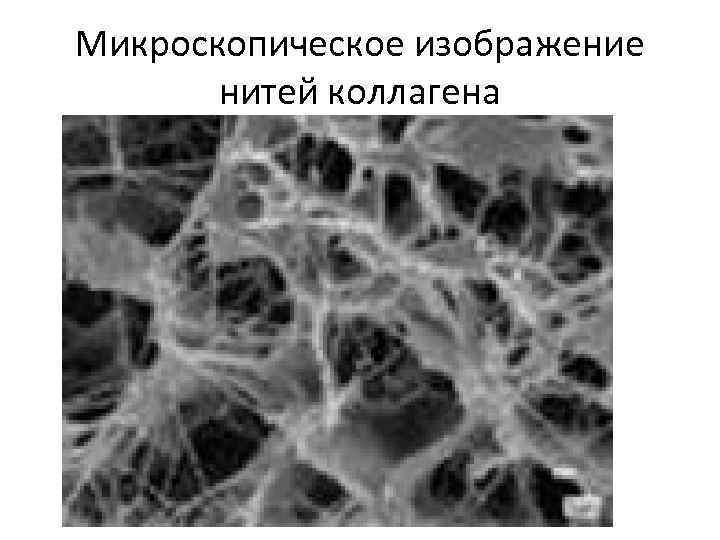
Микроскопическое изображение нитей коллагена

• Глобулярные белки (яичный альбумин и белки сыворотки) растворимы в воде и солевых растворах и имеют сферическую форму.
Белки острой фазы воспаления

• Имеются сложные белки, в молекулу которых входит небелковая часть (простетическая группа). К ним принадлежат нуклеопротеиды, липопротеиды, хромопротеиды (гемоглобин, цитохромы, гемоцианин) и гликопротеиды.

• Полипептидная цепь, построенная из аминокислот, представляет собой первичную структуру белковой молекулы. Это наиболее важная специфическая структура, определяющая вторичную и третичную структуры. Последовательность расположения аминокислот обуславливает свойства белков.

• Молекула белка состоит из нескольких сотен аминокислот, поэтому она изогнута определенным образом и образует вторичную структуру. • В глобулярных белках полипептидные цепи свернуты определенным образом и образуют компактную, третичную структуру.
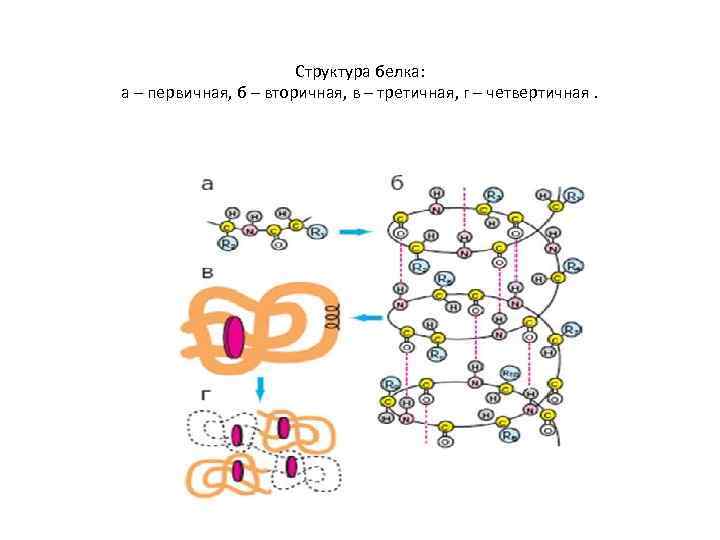
Структура белка: а – первичная, б – вторичная, в – третичная, г – четвертичная.

В структуре белков встречаются различные типы связей. • Первичная структура определяется ковалентными (химическими) пептидными связями. Вторичная и третичная структуры стабилизируются следующими видами связей: • ионные (электростатические) – между положительными и отрицательными ионами, находящимися на расстоянии 2 -3 А, • водородные – (длина связи 2, 5 -3, 2 А) более слабые, чем ионные, образуются между 2 -мя сильно отрицательными атомами – C, N, O, • связи, образующиеся за счет вандерваальсовых сил при взаимодействии полярных боковых цепей, • взаимодействие неполярных боковых цепей.
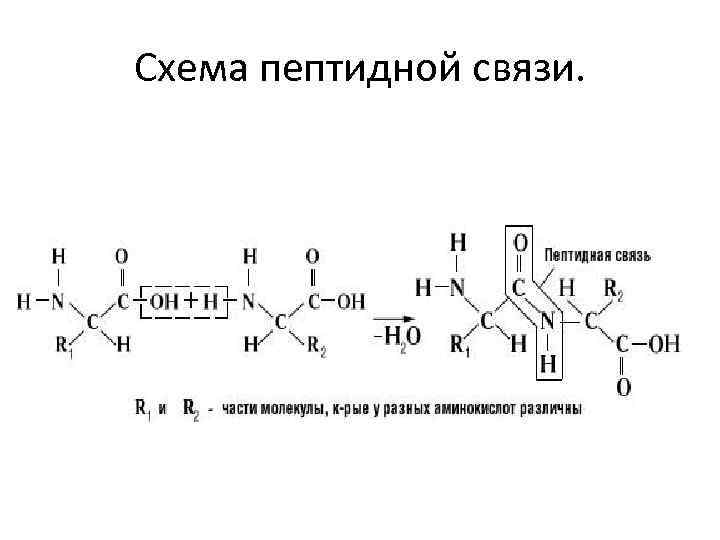
Схема пептидной связи.

Аминокислоты. Классификация аминокислот. • Аминокислота – производное органической кислоты соединение, в котором водород в αположении замещен на аминогруппу. Т. к. в а. к. присутствуют одновременно кислая и основная группы, они амфотерны. • Присутствующие в клетке свободные а. к. образуются в результате расщепления белков или поступают из межклеточной жидкости. Свободные а. к. составляют аминокислотный фонд, из которого клетка черпает строительные блоки для синтеза новых белков.
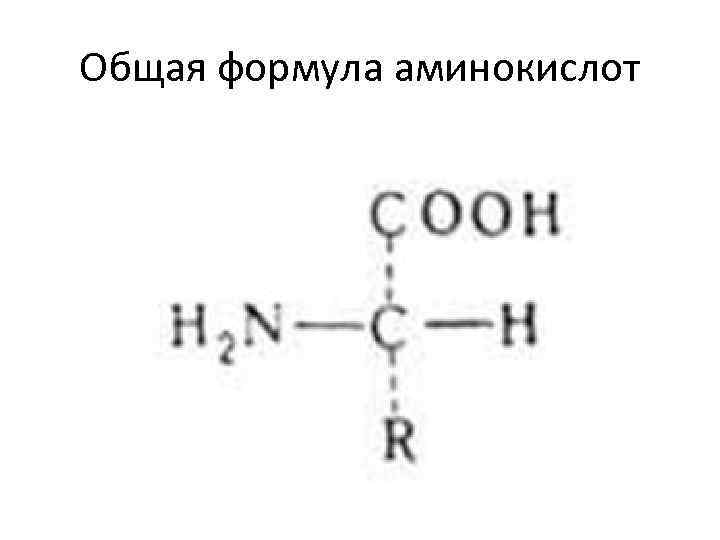
Общая формула аминокислот
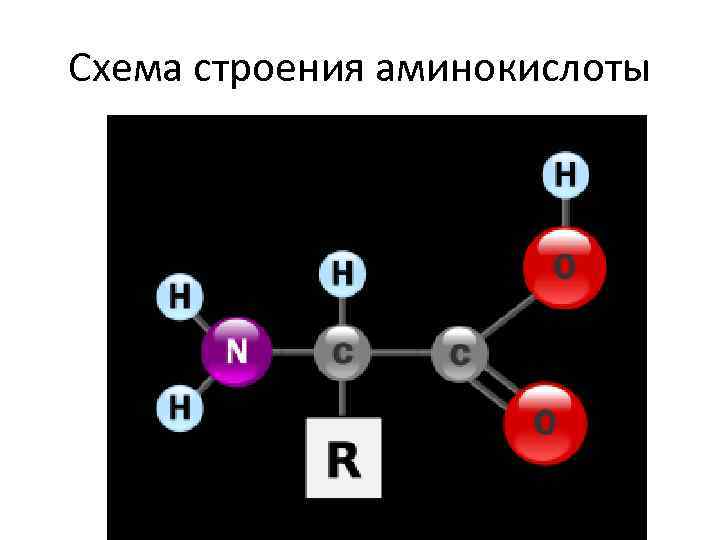
Схема строения аминокислоты

• Связь –NH–CO– называется пептидной связью. Комбинация из двух аминокислот – дипептид, из 3 -х – трипептид. Пептид, состоящий из небольшого числа аминокислот – олигопептид, из большого – полипептид.

• Расстояние между двумя пептидными связями равно примерно 3, 5 А, а средний объем аминокислотного остатка равен 3, 5 х4, 6 х10 А, или 161 А 3. Следовательно, например, молекула белка с молекулярным весом 30 000, состоящая из 300 аминокислотных остатков, в полностью вытянутом состоянии должна иметь длину 1000 А, ширину 10 А и толщину 4, 6 А.

Белки построены из 20 различных а. к. , которые можно классифицировать следующим образом: • • Моноаминомонокарбоновые: глицин (гли), аланин (ала), валин(вал), лейцин (лей), изолейцин (илей). Моноаминодикарбоновые: глутаминовая кислота (глу), аспарагиновая кислота (асп). Диаминомонокарбоновые: аргинин (арг), лизин (лиз), оксилизин (олиз). Гидроксилсодержащие: треонин (тре), серин (сер). Серусодержащие: цистин (цис), метионин (мет). Ароматические: фенилаланин (фен), тирозин (тир). Гетероциклические: триптофан (три), пролин (про), оксипролин (опро), гистидин (гис).

3. Разделение, выделение и идентификация белков. • Большинство методов выделения пригодно в основном для гидрофильных белков. В качестве растворителей используются ионные и неионные детергенты, такие как додецилсульфат натрия, холат натрия, соли желчных кислот и др. • Процедура очистки белка, как правило, состоит из ряда этапов обогащения.

Метод обогащения считают эффективным: • если специфическая активность на единицу веса всего белка увеличивается (например, возрастает каталитическая активность фермента на 1 мг белка в пробе). • Общая активность после данного этапа обогащения существенно не уменьшается.

Для оценки чистоты белкового препарата используют следующие критерии: • кристаллизуемость; • кинетика растворимости; • гомогенность при ультрацентрифугировании или электрофорезе; • однозначность данных при определении аминокислотной последовательности; • однотипность каталитической активности (отсутствие побочных активностей); • гомогенность при изучении хроматографическими методами (при использовании различных систем растворителей).

• При выделении белка их тканей или клеток необходимо разрушить клеточную структуру, не повредив структуру изучаемого белка. С этой целью используют следующие методы: • 1) растирание, • 2) фрагментация, • 3) воздействие ультразвуком, • 4) воздействие химическими и (или) ферментативными агентами. • При выделении белков используют буферы, учитывают температуру и ионную силу, а также время очищения белка.

• Для очистки белка часто используют высаливание (добавление соли), оно, как правило, обратимо. Одним из лучших высаливающих агентов служит (NH 4)2 SO 4, т. к. соль растворима в больших концентрациях. Из органических растворителей для высаливания используют ацетон, уксусную кислоту, диметилсульфоксид и др.

• Для дальнейшей очистки и обогащения белков используют различия в следующих свойствах: • 1) в молекулярной массе, • 2) в растворимости, • 3) в электрическом заряде, • 4) в адсорбируемости определенными веществами, • 5) в сродстве к другим молекулам.

• Существуют 3 основных способа разделения белков на основе их молекулярной массы: • 1. Разделение в поле тяготения (центрифугирование). • 2. Метод молекулярного сита. Он основан на том, что поры в мембране или между частицами проницаемы для молекул только в том случае, если d молекул < d пор.

• 3. Гель-электрофорез с додецилсульфатом натрия (ДСН). ДСН гидрофобной частью связывается с молекулой белка. Молекула ДСН несет отрицательный заряд и, т. о. , комплекс белок-ДСН становится сильно электроотрицательным. Собственный заряд белка почти не изменяется. Общий заряд комплекса прямо пропорционален величине белковой молекулы. Подвижность в электрическом поле зависит не только от общего заряда молекулы, а в первую очередь от распределения этого заряда.

• Обычный электрофорез не позволяет разделять одинаково заряженные частицы. При гель-электрофорезе с ДСН дополнительно используется диффузионный эффект при прохождении через гель. Небольшие молекулы проходят быстрее, чем крупные. Скорость прохождения пропорциональна их величине. • Метод гель-электрофореза относительно прост, он является стандартным методом определения молекулярной массы. Однако в результате получаются лишь относительные величины и необходимо использовать подходящие молекулы в качестве стандарта.

4. Анализ аминокислотных последовательностей: определение первичной структуры. • Первичная структура белка – это последовательность аминокислот в его пептидной цепи. • Аминокислотную последовательность белка впервые определил Сэнгер в 1953 г. Этим белком был инсулин. В настоящее время известны полные или частичные последовательности более чем 700 различных белков.

• Для определения аминокислотной последовательности белок очищают до гомогенного состояния. В первую очередь определяют, какие из 20 а. к. имеются в этом белке. Для этого белок гидролизуют сильной кислотой до свободных а. к. Гидролизат (смесь аминокислот) разделяют.

• Для количественного определения применяется ионообменная хроматография. При стандартных условиях с использованием автоматического анализатора аминокислот, а. к. появляются в элюате совершенно определенной последовательности. Здесь также применяют органические растворители (буферные системы). Площадь под кривыми для отдельных аминокислот отражает содержание этих а. к. в смеси (однако коэффициенты экстинкции разных а. к. отличаются друг от друга).

• Для определения аминокислотного состава молекулу белка расщепляют на фрагменты. При этом важно, чтобы молекула распадалась на определенное число фрагментов определенной длины и чтобы полипептидная цепь разрывалась в определенных местах. Это осуществляют с помощью протеолитических ферментов (трипсин, химотрипсин, пепсин, папаин и др. ) •

• Наибольшей специфичностью обладает трипсин. Примерно через каждые 5– 15 а. к. в белке встречаются остатки аргинина или лизина; поэтому после обработки пептида трипсином образуются фрагменты длиной 5– 15 аминокислот. Эти фрагменты отделяют друг от друга хроматографически или электрофоретически. После этого каждый фрагмент анализируют отдельно: сначала устанавливают аминокислотный состав, а затем последовательность а. к.

• С-концевые а. к. остатки идентифицируются по их отщеплению карбоксипептидазой. А. к. освобождаются последовательно. Около некоторых а. к. , например, пролина, карбоксипептидаза связи вообще не расщепляет.

• N-концевые остатки в пептидах определяют чаще всего «расщеплением по Эдману» (аминопептидаза работает хуже карбоксипептидазы, поэтому ее применяют редко). При этом методе к пептиду добавляют фенилизотиоцианат, что ведет к освобождению соответсвующего производного N-концевой а. к. Это производное относительно легко отделить от остального пептида и идентифицировать.

• Оставшийся пептид можно вновь подвергнуть той же обработке. При этом, чем длиннее пептид, тем лучше работает метод. Лаурсен модифицировал этот метод, связав пептид с твердым носителем (твердофазный метод), и т. о. распространил применимость этого метода на область коротких пептидов.
Белки и аминокислоты.ppt