trx-Pc talk-110313.ppt
- Количество слайдов: 98

Белки групп триторакса и поликомба (trx. G/Pc. G) как ключевые эпигенетические факторы поддержания клеточной дифференцировки Докладчик - Тиллиб Сергей Владимирович Лаборатория молекулярных биотехнологий ФГБУН Институт биологии гена РАН 119334 Москва, ул. Вавилова, 34/5 tillib@genebiology. ru 2013

• Хроматин содержит белки, которые служат структурными организаторами геномной ДНК, способствуют формированию структур более высокого порядка и, в конечном счете, собственно самой хромосомы. • Хроматин ограничивает доступ факторов транскрипции к ДНК. • Белки групп поликомба и триторакса участвуют в «ремоделировании» хроматина, изменяя доступность ДНК для других факторов, требующихся для транскрипции данного гена. • Гены группы поликомба участвуют в репрессии генов, опосредованной формированием «закрытого» хроматина, тогда как гены группы триторакса противодействуют этой репрессии и участвуют в поддержании транскрипции гена и соответственно структуры «открытого» локального хроматина.
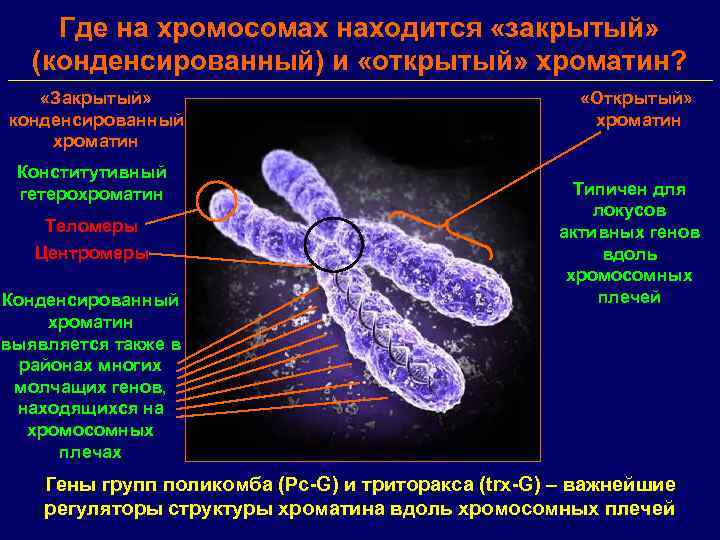
Где на хромосомах находится «закрытый» (конденсированный) и «открытый» хроматин? «Закрытый» конденсированный хроматин Конститутивный гетерохроматин Теломеры Центромеры Конденсированный хроматин выявляется также в районах многих молчащих генов, находящихся на хромосомных плечах «Открытый» хроматин Типичен для локусов активных генов вдоль хромосомных плечей Гены групп поликомба (Pc-G) и триторакса (trx-G) – важнейшие регуляторы структуры хроматина вдоль хромосомных плечей

Если до недавнего времени хроматин условно подразделяли на два подтипа, гетерохроматин и эухроматин, то ряд новых исследований предлагает существенно углубить наше представление о типах хроматина. Так, ван Штинсель (van Steensel) и др. [Fillon et al. , 2010] использовали интегративный анализ экспериментальных данных по обогащению в определенных местах генома 53 негистоновых хроматиновых белков и четырех ключевых гистоновых модификаций (с помощью присоединенной к ним бактеральной ДНК-метилазы и последующего картирования сайтов метилирования аденина). По крайней мере, 5 различных типов хроматина, характеризующихся уникальными комбинациями хроматиновых архитектурных белков и гистоновых модификаций, были идентифицированы в клетках Кс167 Drosophila.

Были идентифицированы 3 различных класса репрессированного хроматина: 1) классический гетерохроматин, обнаруживаемый в центромерном райне и обогащенный НР 1, Su(var)3 -9 и гистоновой модификацией H 3 K 9 мe 2 2) факультативный гетерохроматин, содержащий белки группы Поликомба и маркированный гистновой модификацией H 3 K 27 мe 3 Картирование с высоким разрешением (базирующееся на специфичесой иммунопреципитации и последующем анализе последовательностей обогащяющихся фрагментов хроматина) в геноме Drosophila выявило существование протяженных доменов (в несколько десятков тыс. п. н. длиной), содержащих характерные маркеры связывания белков группы Поликомба, модификацированные гистоны Н 3 К 27 ме 3 и белок PC, а также расположенные в более локализованых участках в этих доменах другие белки группы Pc. G. Эти домены были названы «Поликомб» -доменами [Nerge et al. , 2006; Tolhuis et al. , 2006; Schwartz et al. , 2006]. 3) новый мажорный вариант ( «чёрный хроматин» , покрывает примерно 48% генома и образует домены в несколько десятков тыс. п. н. ), маркированный уникальной комбинацией семи обогощенных белков: гистон Н 1, ламин, SUUR (супрессор недорепликации), Su(Hw), D 1 (белок, содержащий «АТ-Hook» -домен, IAL (Ipl 1 -aurora-like kinase), EFF (Effete). Этот новый 3 тип репрессированного хроматина в основном обеднен генами и захватывает наиболее молчащие гены. Гистоновая модификация Н 4 К 20 мe 3, предположительно, может играть важную роль в формировании этого 3 типа репрессированного хроматина.

В отличие от репрессированных типов хроматина оба идентифицированных типа активного хроматина обогащены гистоновыми модификациями, характерными для активно транскрибирующегося хроматина (Н 3 К 4 мe 3 и H 3 K 79 мe 3), и содержат несколько одинаковых хроматиновых белков, вовлеченных в модифицирование гистонов и деконденсацию хроматина. Основные же их отличия следующие. Один тип активного хроматина обогащен гистоновой модификацией – метилированием по Н 3 К 36, а также соответствующим лигандом для этой модификации – Mrg 15. Второй же тип активного хроматина отличается тем, что очень рано реплицируется и обогащен большими регуляторными белковыми комплексами.

Белки групп поликомба (Polycomb Group, Pc. G) и триторакса (trithorax Group, trx. G): эпигенетические регуляторы функционирования генома - Исходно открытые в Drosophila как регуляторы гомеотических (или HOX) генов, отвечают за спецификацию плана формирования тела, а также регулируют многие гены, участвующие в клеточной дифференцировке и пролиферации - Поддерживают тканеспецифическое распределение экспрессии генов, передаваемое по наследству дочерним клеткам (эпигенетическая регуляция, «клеточная память» ) - Предполагаемый механизм функционирования: специфическое привлечение хроматин-ремоделирующих активностей к конкретным хромосомным участкам генов-мишеней ( «гистоновый код» ); комбинация цис- и транс-взаимодействий между отдалёнными регуляторными хромосомными элементами ( «модули клеточной памяти» ) - Эволюционно консервативные механизмы - У млекопитающих (у человека), эти белки поддерживают дифференцировку клеток, а также их функция необходима для пролиферации и поддержания разных типов стволовых клеток, включая эмбриональные стволовые клетки. Наконец, эти белки регулируют Х-инактивацию у самок и «геномный импринтинг» . - Мутации, нарушающие работу этих эпигенетических факторов (Pc. G и trx. G), ведут к серьезным патологиям, индуцируют многие типы раковых заболеваний

• Геномный импринтинг — эпигенетический процесс, при котором экспрессия определенных генов осуществляется в зависимости от того, от какого родителя поступил аллель гена. Это ненаследуемый процесс, который не подчиняется наследованию по Менделю. Примеры: импринтинг генов вызывает экспрессию аллелей гена полученных только от матери в случае генов H 19 или CDKN 1 C и только аллелей от отца в случае гена IGF 2. Импринтинг некоторых генов в составе генома показан для насекомых, млекопитающих и цветковых растений.
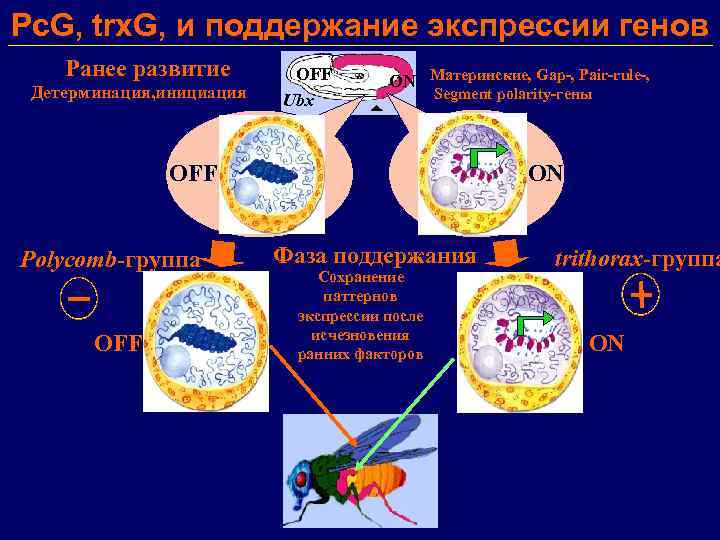
Pc. G, trx. G, и поддержание экспрессии генов Ранее развитие Детерминация, инициация OFF Ubx ON Mатеринские, Gap-, Pair-rule-, Segment polarity-гены OFF Polycomb-группа OFF ON Фаза поддержания Сохранение паттернов экспрессии после исчезновения ранних факторов trithorax-группа ON
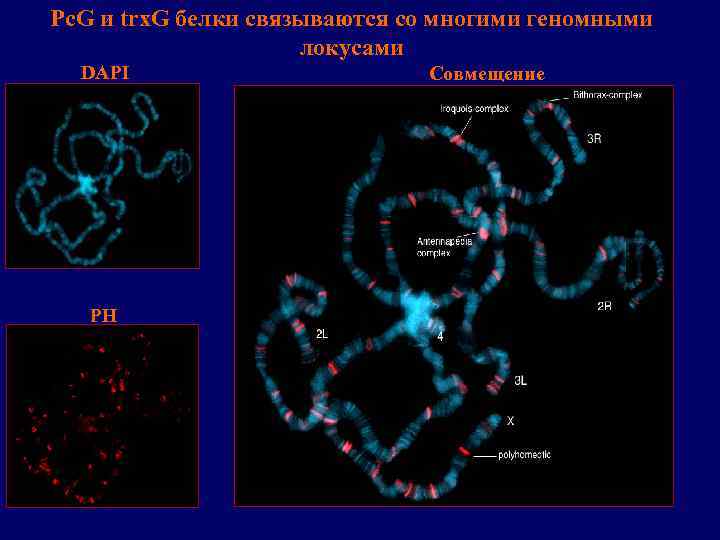
Pc. G и trx. G белки связываются со многими геномными локусами DAPI PH Совмещение
Pс. G и trx. G белки формируют ядерные компартменты ( «speckled» распределение в ядре)

Pc. G и trx. G белки осуществляют свою функцию посредством взаимодействия со специфическими регуляторными цисэлементами, PRE/TRE Связаны с Pc. G/trx. G-белками in vivo (на политенных хромосомах, в Х-Сh. IP экспериментах) Связывание необходимо для поддержания репрессии (или усиления уровня экспрессии) репортерных генов Репрессия (или активация) усиливаются в присутствии множественных копий PRE/TRE (“pairing”эффект) PRE и TRE обычно колокализуются (перекрываются)

Анализ нескольких PRE/TRE дрозофилы не обнаружил в них протяженных гомологичных последовательностей, однако выявил их обогащение участками связывания для нескольких ДНК-связывающих белков: Pleihomeotic (PHO) and Pleihomeotic-like (PHOL), GAGA factor (GAF)/Pipsqueak (PSQ), Zeste, DSP (Dorsal switch protein), Ct. BP Grainyhead (GRH) и членов семейства Sp 1/KLF. [GAF, Pipsqueak и Zeste не консервативны у позвоночных]. Число и топологическая организация этих сайтов существенно варьируют в разных PRE/TRE на сегодняшний день были функционально охарактеризованы только в геноме Drosophila. PRE/TRE определяются как элементы хромосом, которые необходимы и достаточны для рекрутирования Pc. G/trx. G-комплексов и для соответствующего поддержания в репрессированном/активном состоянии фланкирующих промоторов.
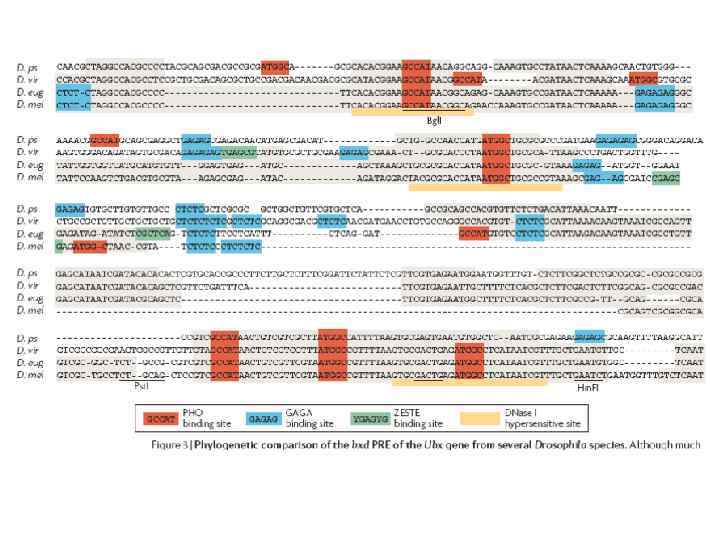

Мотивы потенциальных участков связывания, часто обогащённые в PRE/TRE

Pc. G-белки выявляются в составе многокомпонентных комплексов • 1 комплекс, Pho. RC, содержит ДНК-связывающий белок PHO (его гомолог у млекопитающих - YY 1) и белок d. Sfmbt, узнающий моно- и диметилированные по Н 3 К 9 и Н 4 К 20 концы гистонов Н 3 и Н 4 • 2 комплекс, E(Z)/ESC, или Polycomb Repressive Complex 2 (PRC 2), содержит 4 коровых белка: гистон-метилтрансферазу Enhancer of Zeste (E(Z)), Extra sex combs (ESC), Suppressor of zeste-12 (SU(Z)12), и ремоделирующий нуклеосому фактор 55 (NURF-55). E(Z) триметилирует лизин 27 гистона H 3 (H 3 K 27 me 3), и, несколько менее выраженно, лизин 9 гистона H 3 (H 3 K 9 me 3). • 3 комплекс, PRC 1, узнает эти метилированные знаки с помощью «хромодомена» белка Polycomb (PC). PC является стехиометрическим компонентом PRC 1 наряду с Polyhomeotic (PH), Posterior Sex Combs (PSC), and d. RING. • У млекопитающих дупликация многих Pc. G-генов способствует большей вариабельности в составе комплексов, различающихся в разных типах клеток и на разных стадиях развития.
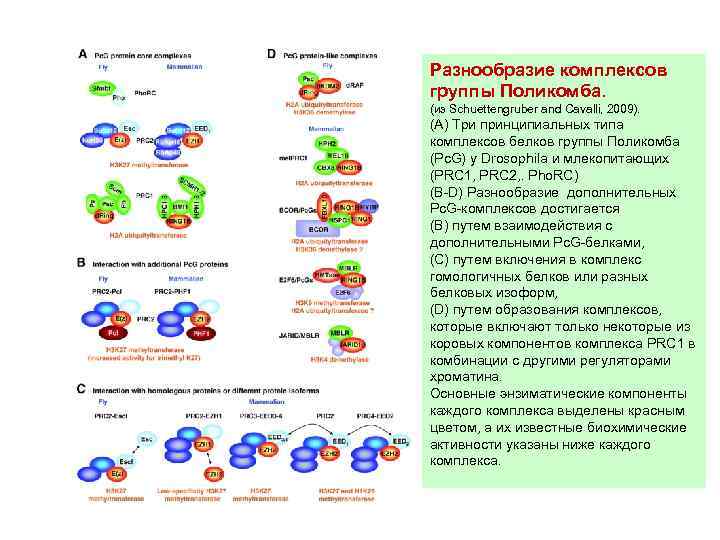
Разнообразие комплексов группы Поликомба. (из Schuettengruber and Cavalli, 2009). (A) Три принципиальных типа комплексов белков группы Поликомба (Pc. G) у Drosophila и млекопитающих (PRC 1, PRC 2, . Pho. RC) (B-D) Разнообразие дополнительных Pc. G-комплексов достигается (В) путем взаимодействия с дополнительными Pc. G-белками, (С) путем включения в комплекс гомологичных белков или разных белковых изоформ, (D) путем образования комплексов, которые включают только некоторые из коровых компонентов комплекса PRC 1 в комбинации с другими регуляторами хроматина. Основные энзиматические компоненты каждого комплекса выделены красным цветом, а их известные биохимические активности указаны ниже каждого комплекса.

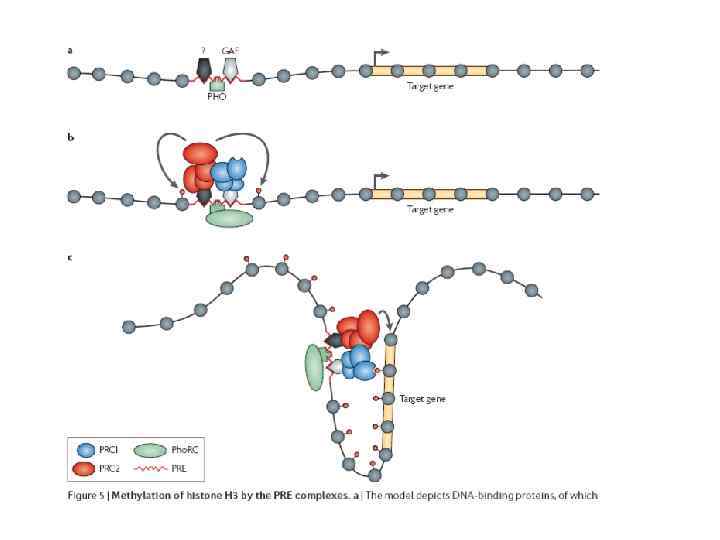
Предполагаемый ступенчатый процесс формирования репрессионного комплекса 1 - Связывание комплекса Pho. RC 2 - Привлечение комплекса PRC 2 через взаимодействие с Pho. RC 3 - PRC 2 -зависимая модификация гистонов (H 3 K 27 me 3) в месте формирования комплекса 4 - Привлечение комплекса PRC 1 через узнавание и связывание РС с H 3 K 27 me 3 -Однако, это лишь очень упрощённое представление. -Только лишь PHO/PHOL-сайты связывания не достаточны для образования РС-репрессионного комплекса.
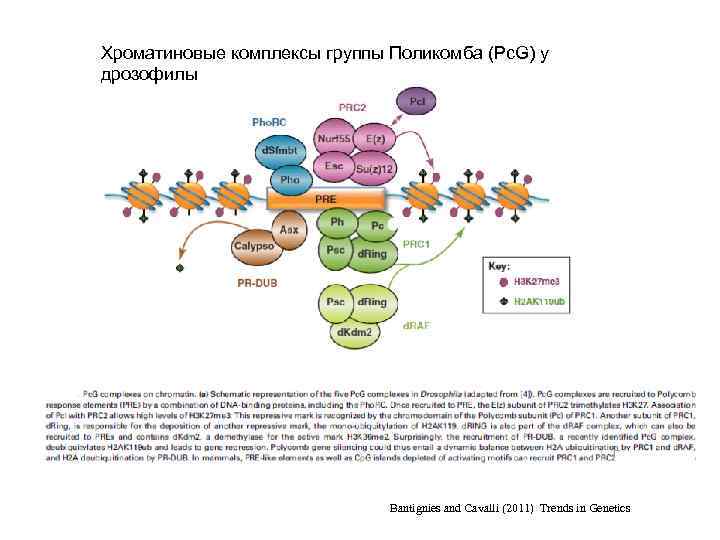
Хроматиновые комплексы группы Поликомба (Pc. G) у дрозофилы Bantignies and Cavalli (2011) Trends in Genetics
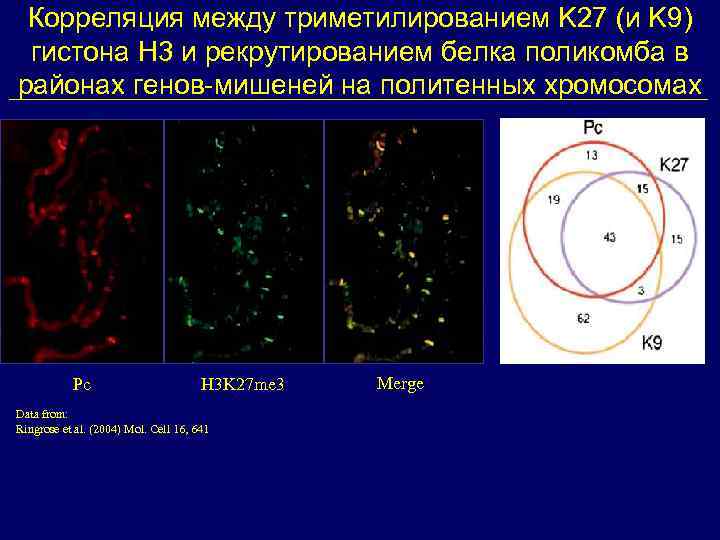
Корреляция между триметилированием K 27 (и K 9) гистона Н 3 и рекрутированием белка поликомба в районах генов-мишеней на политенных хромосомах Pc H 3 K 27 me 3 Data from: Ringrose et al. (2004) Mol. Cell 16, 641 Merge
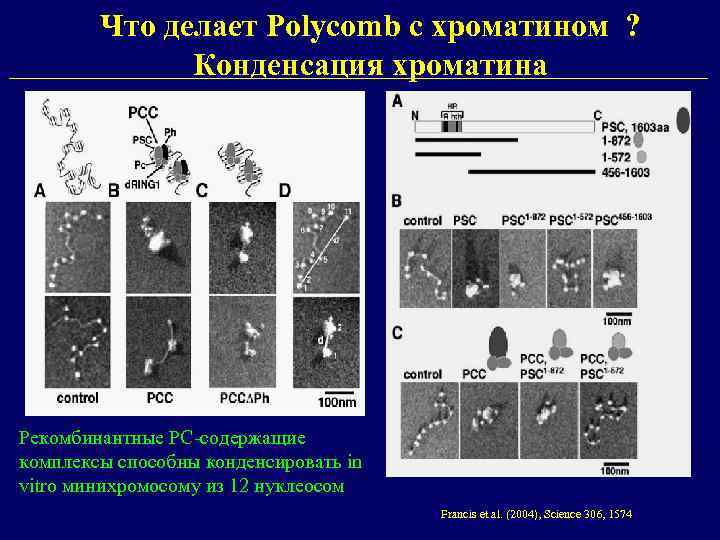
Что делает Polycomb с хроматином ? Конденсация хроматина Рекомбинантные PC-содержащие комплексы способны конденсировать in vitro минихромосому из 12 нуклеосом Francis et al. (2004), Science 306, 1574
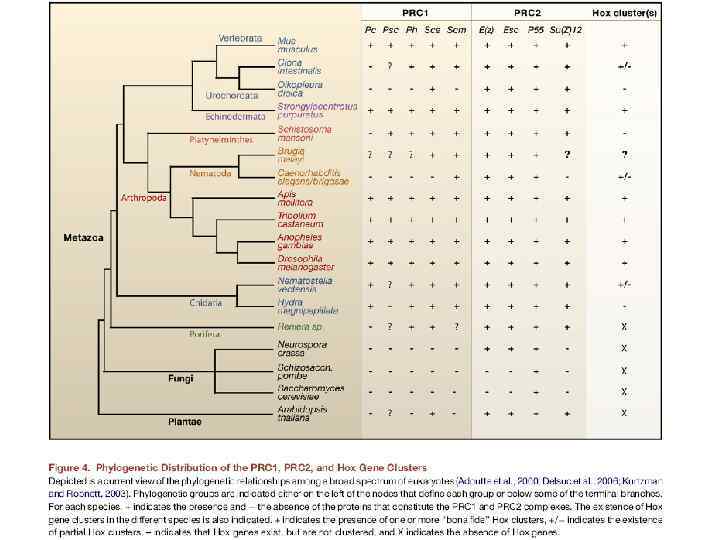
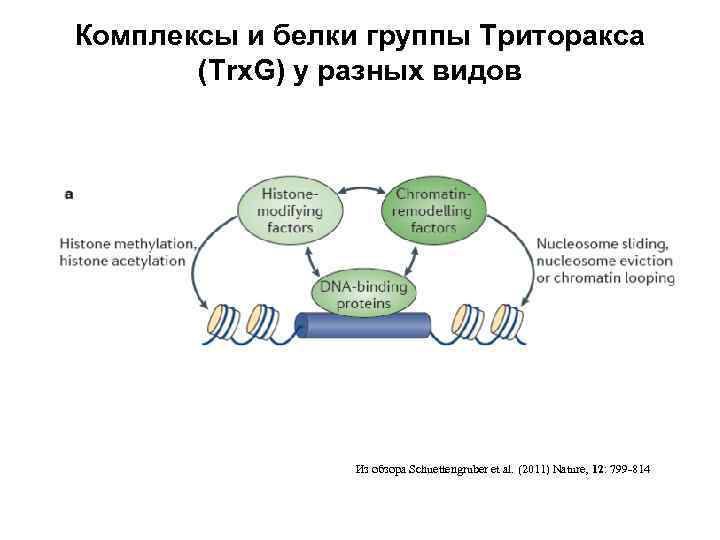
Комплексы и белки группы Триторакса (Trx. G) у разных видов Из обзора Schuettengruber et al. (2011) Nature, 12: 799 -814
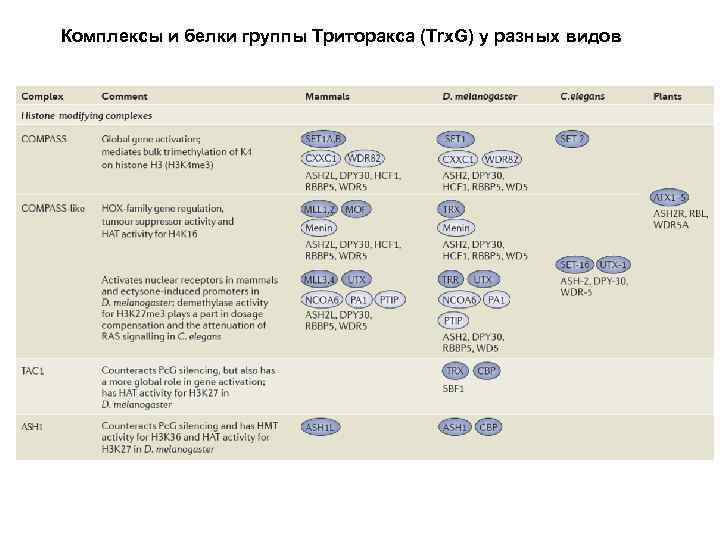
Комплексы и белки группы Триторакса (Trx. G) у разных видов
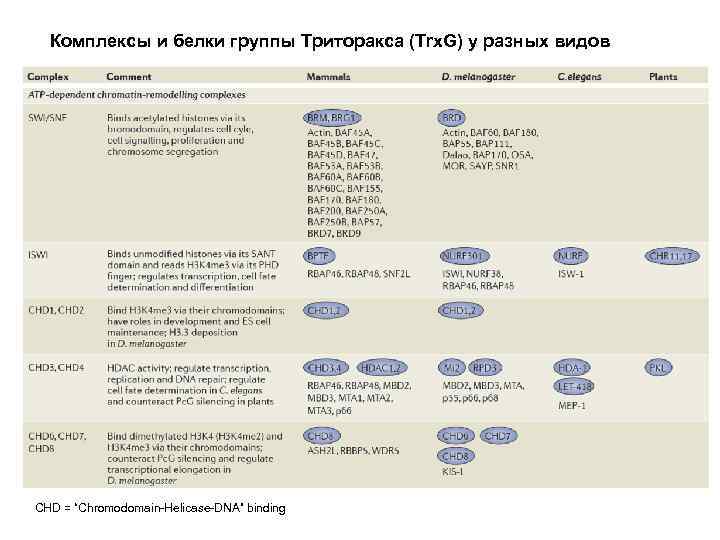
Комплексы и белки группы Триторакса (Trx. G) у разных видов CHD = “Chromodomain-Helicase-DNA” binding
![Эволюционное разнообразие SWI/SNF-комплексов (из [Ho and Crabtree, 2010]). Гомологичные субъединицы комплексов дрожжей Saccharomyces cerevisiae Эволюционное разнообразие SWI/SNF-комплексов (из [Ho and Crabtree, 2010]). Гомологичные субъединицы комплексов дрожжей Saccharomyces cerevisiae](https://present5.com/presentation/5088598_171178400/image-27.jpg)
Эволюционное разнообразие SWI/SNF-комплексов (из [Ho and Crabtree, 2010]). Гомологичные субъединицы комплексов дрожжей Saccharomyces cerevisiae (Yeast Swi/Snf), Drosophila melanogaster (BAP, Brahma(BRM)-ассоциированные белки, и PBAP, polybromo-содержащий BAP; на рис. оба варианта показаны вместе как ВАР-комплексы) и мыши (комбинаций различных субъединиц ведут к образованию огромного разнообразия BAF-комплексов, содержащих brahmaассоциированные факторы, BAF) обозначены одинаковыми фигурами и выделены одним цветом. Домены субъединиц, которые могут взаимодействовать с ДНК или гистоновыми модификациями показаны на поверхности соответствующих белков (объяснение - на рисунке сверху слева). В случае комплексов дрозофилы обозначены белки группы Триторакса: MOR (Moira), OSA, BRM (Brahma), SAYP (“supporter of activation of yellow protein”, E(y)3).
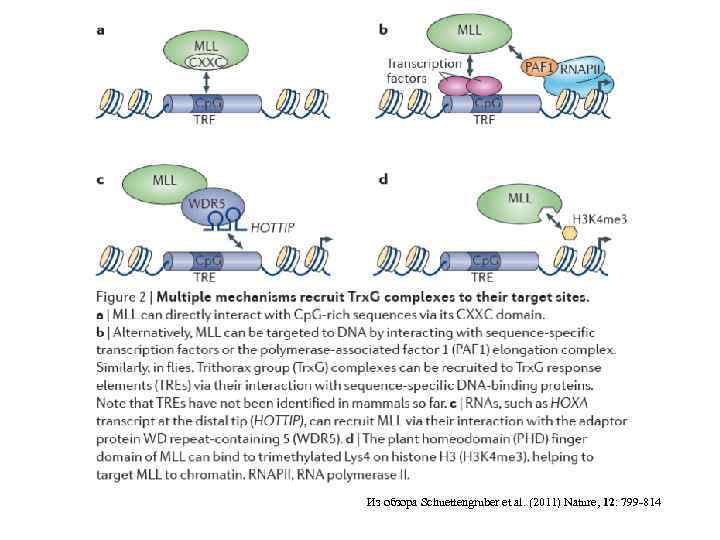
Из обзора Schuettengruber et al. (2011) Nature, 12: 799 -814
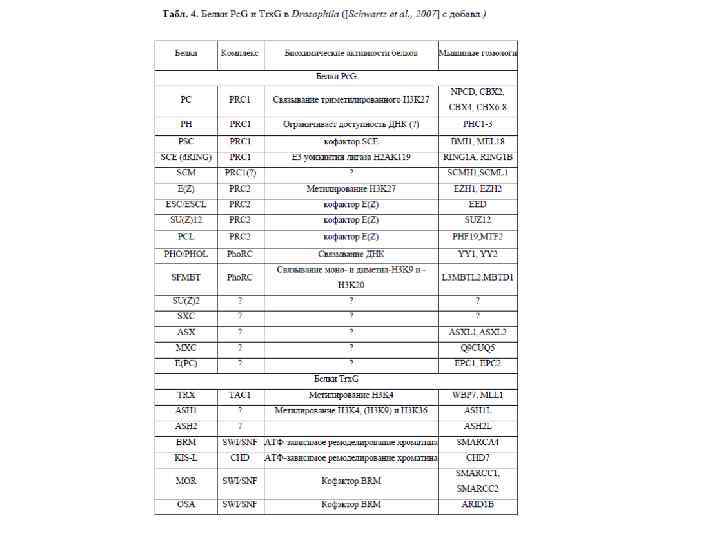
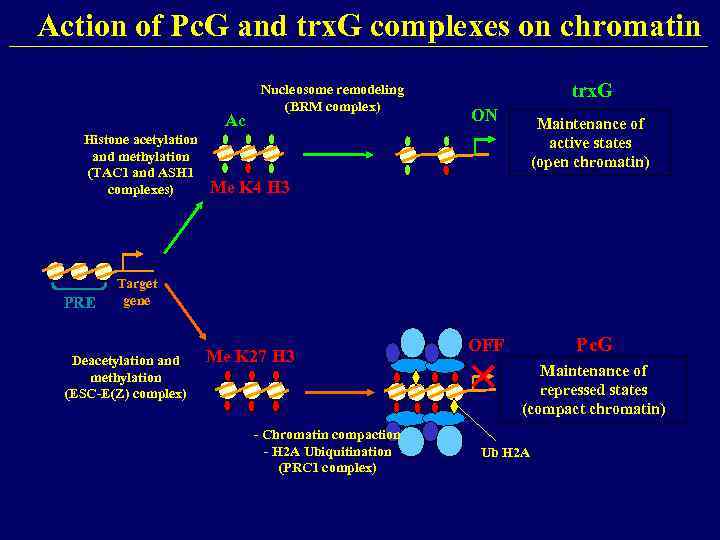
Action of Pc. G and trx. G complexes on chromatin Ac Histone acetylation and methylation (TAC 1 and ASH 1 complexes) PRE Nucleosome remodeling (BRM complex) trx. G ON Maintenance of active states (open chromatin) Me K 4 H 3 Target gene Deacetylation and methylation (ESC-E(Z) complex) Me K 27 H 3 - Chromatin compaction - H 2 A Ubiquitination (PRC 1 complex) Pc. G OFF Maintenance of repressed states (compact chromatin) Ub H 2 A
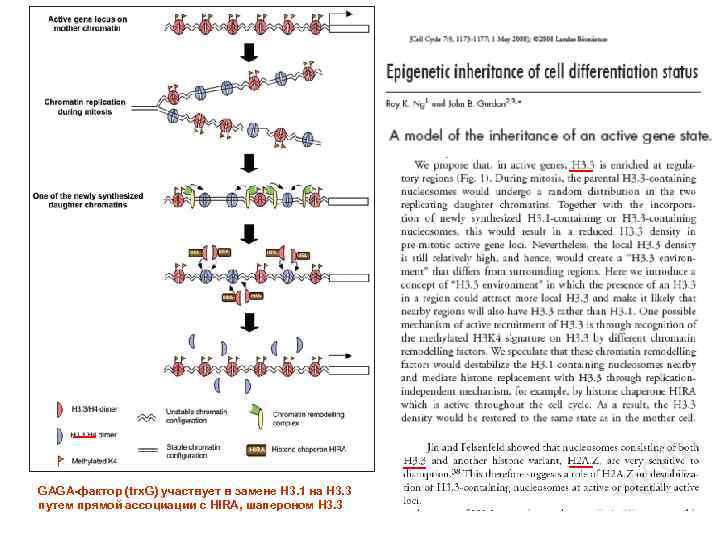
GAGA-фактор (trx. G) участвует в замене H 3. 1 на Н 3. 3 путем прямой ассоциации с HIRA, шапероном Н 3. 3
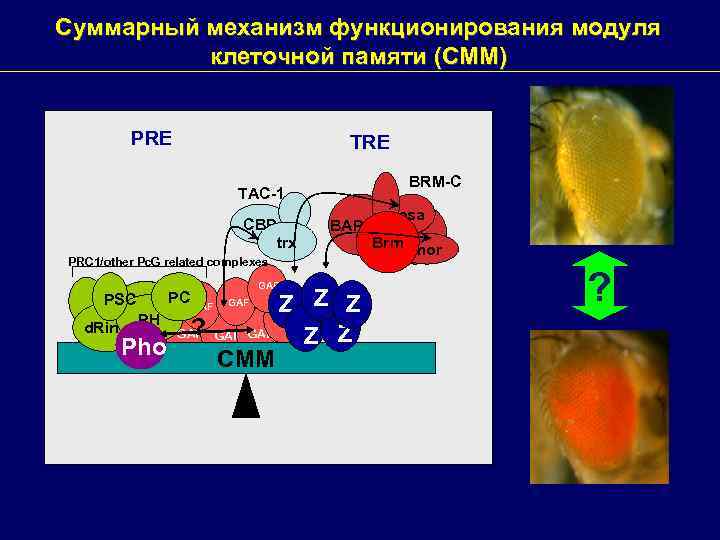
Суммарный механизм функционирования модуля клеточной памяти (CMM) PRE TRE BRM-C TAC-1 CBP trx PRC 1/other Pc. G related complexes GAF osa BAP 111 Brm mor Z Z Z PH GAF d. Ring ? GAF GAF Z Z Pho CMM PSC PC GAF ?
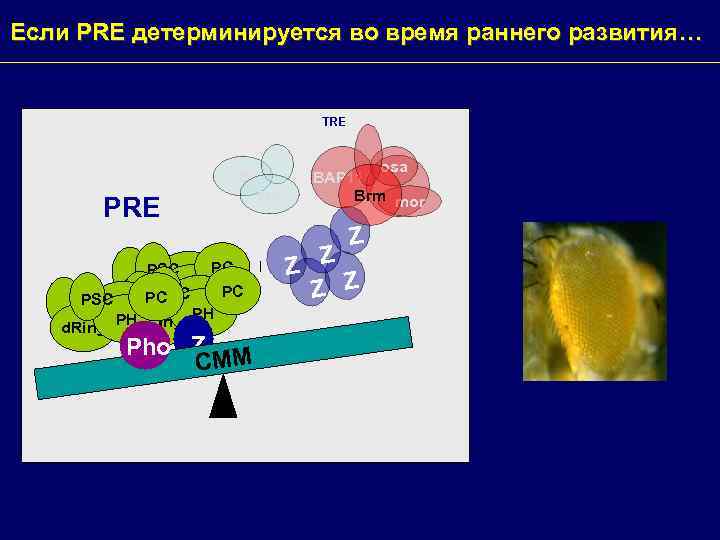
Если PRE детерминируется во время раннего развития… TRE PRE CBP trx osa BAP 111 Brm mor Z PC PSC PH PC PSC d. Ring PHd. Ring. ZPH d. Ring Pho Z M CM Z Z
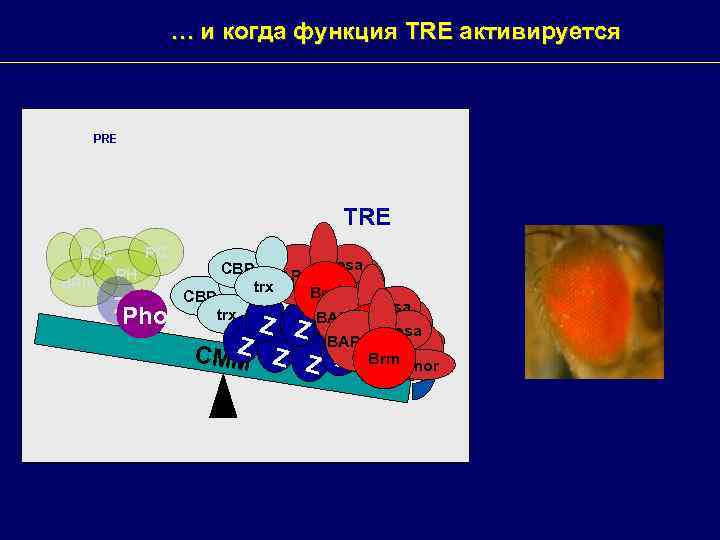
… и когда функция TRE активируется PRE TRE PC PSC d. Ring PH Z Pho CBP BAP 111 osa trx Brm mor CBP osa trx BAP 111 Z Z Z Brm osa BAP 111 mor Z Z CMM Z Z Brm mor
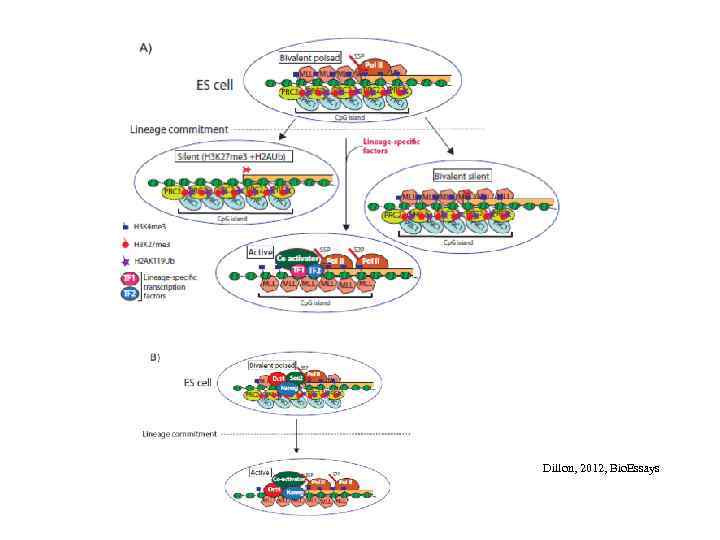
Dillon, 2012, Bio. Essays

Стабильное сохранение наследуемых потенциально обратимых модификаций локального хроматина (сохранение «клеточной памяти» ). Механизмы поддержания эпигенетической информации на двух принципиальных стадиях клеточного цикла: репликации и митоза. ØЭпигенетическими называют такие «наследуемые изменения функционирования гена, которые не могут быть объяснены изменениями в последовательности ДНК» этого гена ØПри репликации ДНК эпигенетическая информация должна быть передана в полной мере обеим дочерним цепям ДНК ØВо время митоза хроматин может конденсироваться в 10000 раз ØОсновные описанные молекулярные механизмы: - метилирование ДНК, - модификации гистонов, - белки групп Polycomb-G/Trithorax-G, - некодирующие РНК, - структурная организация генома в ядре
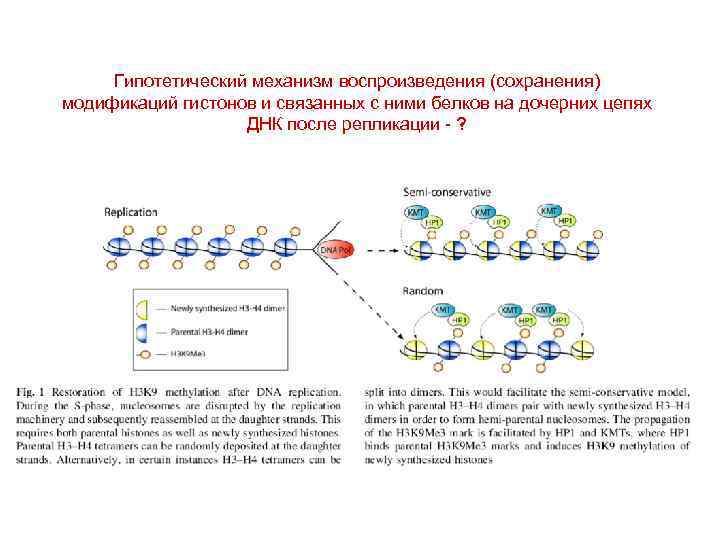
Гипотетический механизм воспроизведения (сохранения) модификаций гистонов и связанных с ними белков на дочерних цепях ДНК после репликации - ?
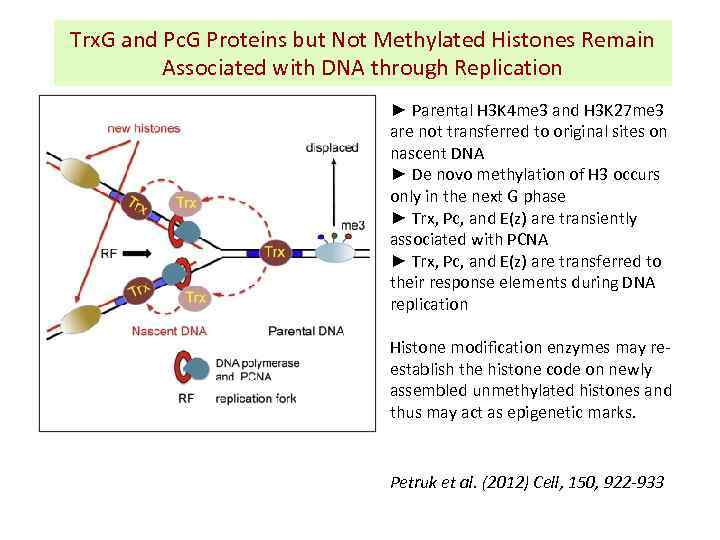
Trx. G and Pc. G Proteins but Not Methylated Histones Remain Associated with DNA through Replication ► Parental H 3 K 4 me 3 and H 3 K 27 me 3 are not transferred to original sites on nascent DNA ► De novo methylation of H 3 occurs only in the next G phase ► Trx, Pc, and E(z) are transiently associated with PCNA ► Trx, Pc, and E(z) are transferred to their response elements during DNA replication Histone modification enzymes may reestablish the histone code on newly assembled unmethylated histones and thus may act as epigenetic marks. Petruk et al. (2012) Cell, 150, 922 -933
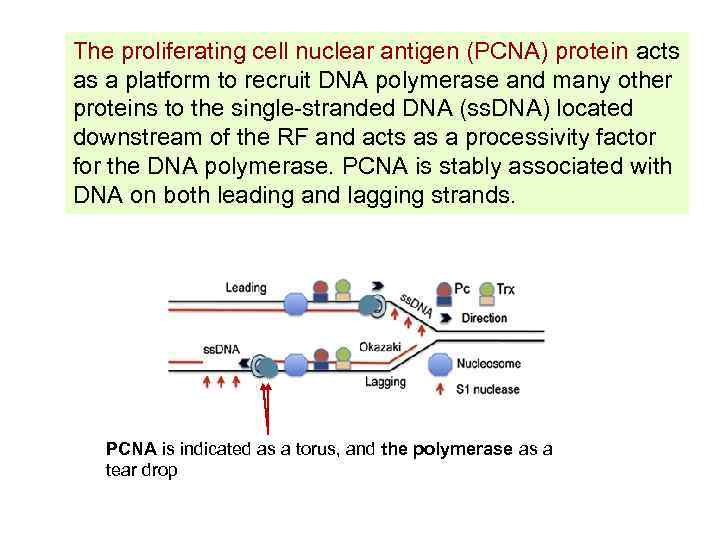
The proliferating cell nuclear antigen (PCNA) protein acts as a platform to recruit DNA polymerase and many other proteins to the single-stranded DNA (ss. DNA) located downstream of the RF and acts as a processivity factor for the DNA polymerase. PCNA is stably associated with DNA on both leading and lagging strands. PCNA is indicated as a torus, and the polymerase as a tear drop
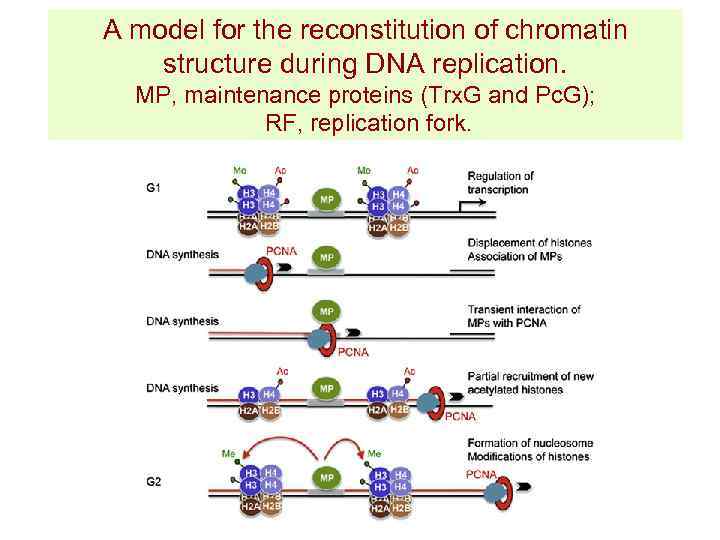
A model for the reconstitution of chromatin structure during DNA replication. MP, maintenance proteins (Trx. G and Pc. G); RF, replication fork.


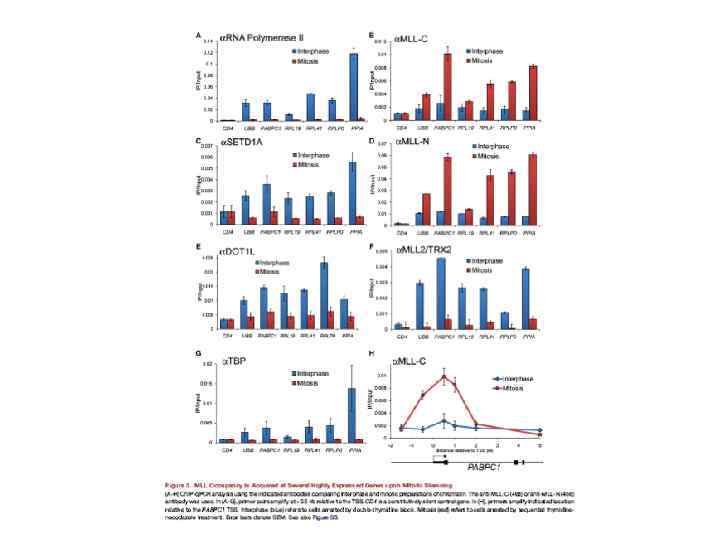
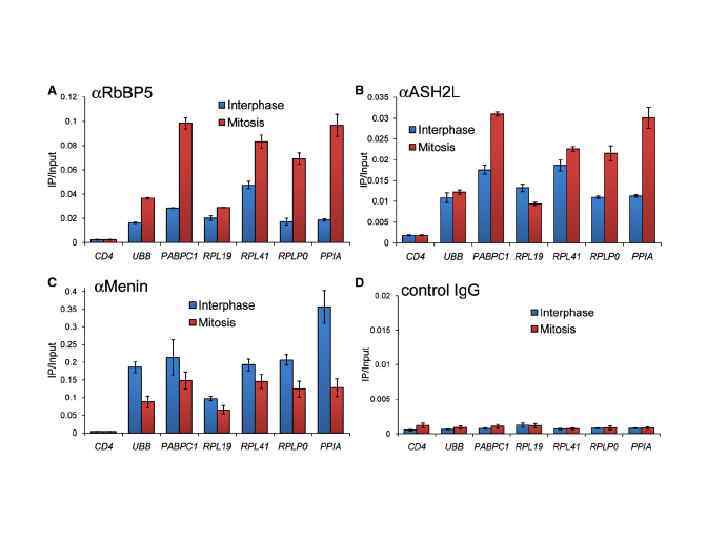

Механизмы репрессии и активации, ассоциированные с белками групп Поликомба (Pc. G) и Триторакса (Trx. G). (из Blomen and Boonstra, 2011). Комплекс PRC 2 функционирует путем метилирования лизина 27 в гистоне Н 3. Гистоновая модификация H 3 K 27 Me 3, в свою очередь, рекрутирует PRC 2, способствуя распространению этой же гистоновой модификации на соседние нуклеосомы. H 3 K 27 Me 3 также рекрутирует комплекс PRC 1, который индуцирует транскрипционную репрессию путем нескольких механизмов: компактизации хроматина, образования петель, убиквитинилирования гистона Н 2 по лизину 119. Белки группы Триторакса регулируют поддержание транскрипционно активного состояния хроматина путем триметилирования лизина 4 в гистоне Н 3 (Н 3 К 4 Ме 3). Дополнительно, Trx. G-белки (GAF) участвуют в введении в нуклеосому гистона Н 3. 3. Trx. G- и Pc. G-белки ассоциированы также с лизиновыми деметилазами (KDM), которые удаляют H 3 K 27 Me 3 и Н 3 К 4 Ме 3, соответственно.
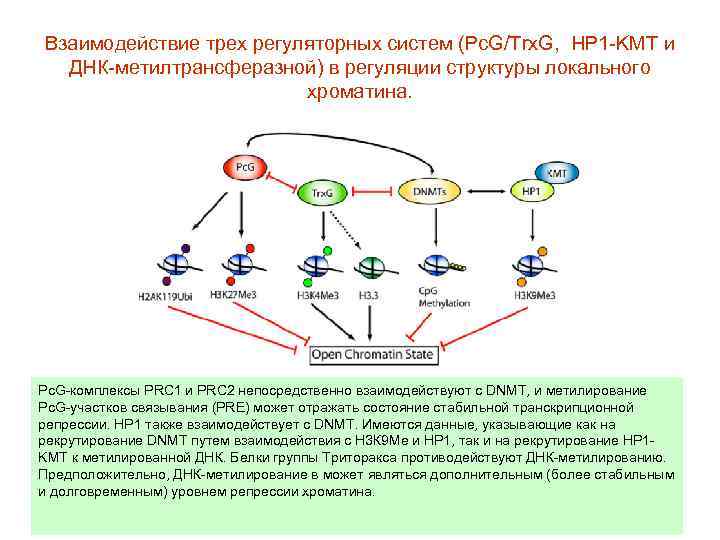
Взаимодействие трех регуляторных систем (Pc. G/Trx. G, HP 1 -KMT и ДНК-метилтрансферазной) в регуляции структуры локального хроматина. Pc. G-комплексы PRC 1 и PRC 2 непосредственно взаимодействуют с DNMT, и метилирование Pc. G-участков связывания (PRE) может отражать состояние стабильной транскрипционной репрессии. HP 1 также взаимодействует с DNMT. Имеются данные, указывающие как на рекрутирование DNMT путем взаимодействия с Н 3 К 9 Ме и HP 1, так и на рекрутирование HP 1 KMT к метилированной ДНК. Белки группы Триторакса противодействуют ДНК-метилированию. Предположительно, ДНК-метилирование в может являться дополнительным (более стабильным и долговременным) уровнем репрессии хроматина.
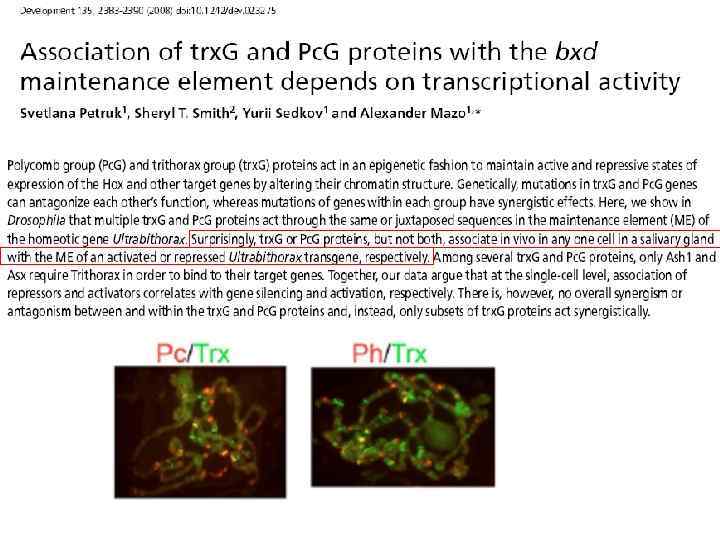

Особенности PRE и TRE, и примеры того, как их изучают в случае Drosophila (У позвоночных они пока совсем мало изучены )
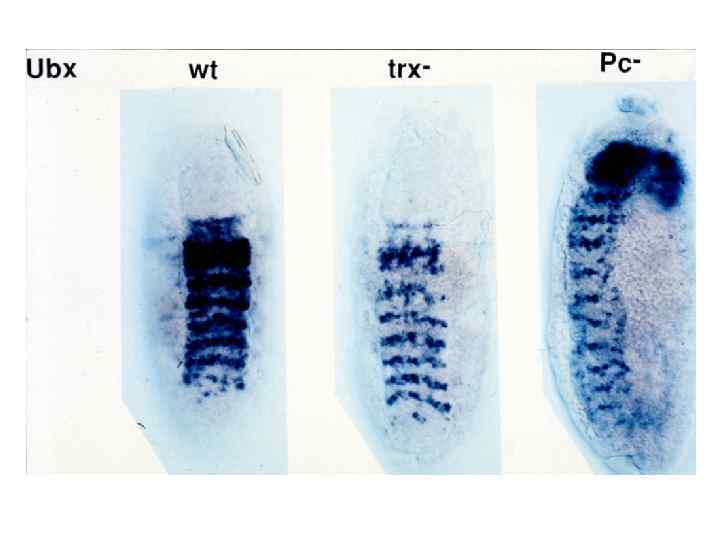
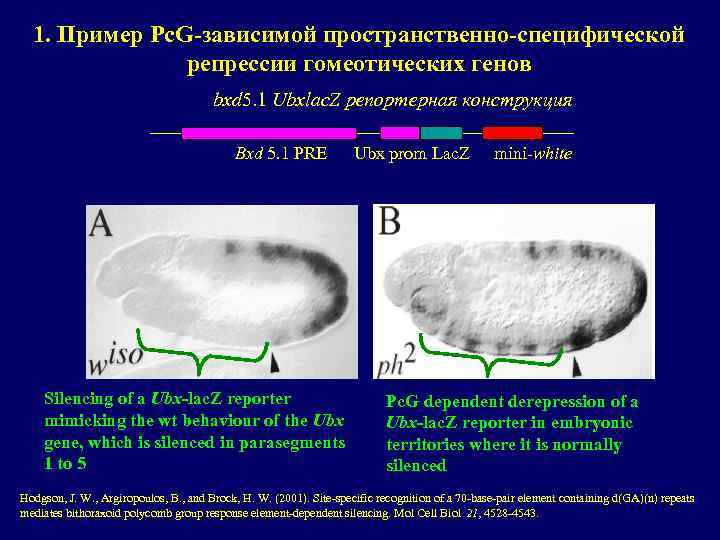
1. Пример Pc. G-зависимой пространственно-специфической репрессии гомеотических генов bxd 5. 1 Ubxlac. Z репортерная конструкция Bxd 5. 1 PRE Silencing of a Ubx-lac. Z reporter mimicking the wt behaviour of the Ubx gene, which is silenced in parasegments 1 to 5 Ubx prom Lac. Z mini-white Pc. G dependent derepression of a Ubx-lac. Z reporter in embryonic territories where it is normally silenced Hodgson, J. W. , Argiropoulos, B. , and Brock, H. W. (2001). Site-specific recognition of a 70 -base-pair element containing d(GA)(n) repeats mediates bithoraxoid polycomb group response element-dependent silencing. Mol Cell Biol 21, 4528 -4543.
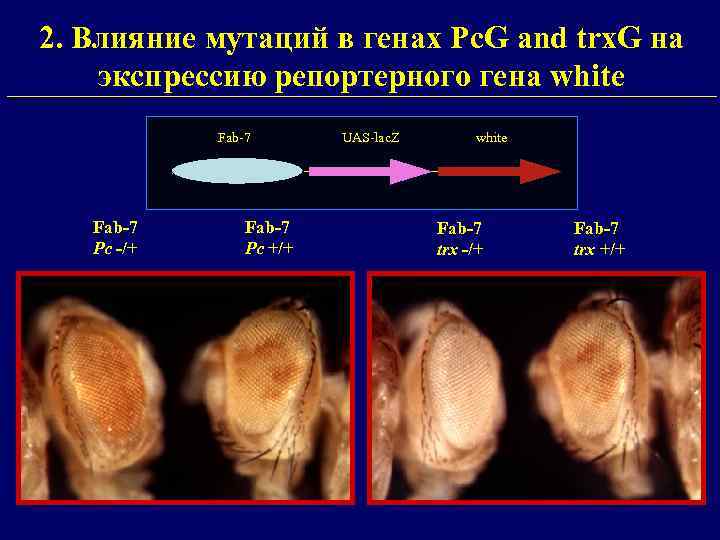
2. Влияние мутаций в генах Pc. G and trx. G на экспрессию репортерного гена white Fab-7 Pc -/+ Fab-7 Pc +/+ UAS-lac. Z white Fab-7 trx -/+ Fab-7 trx +/+
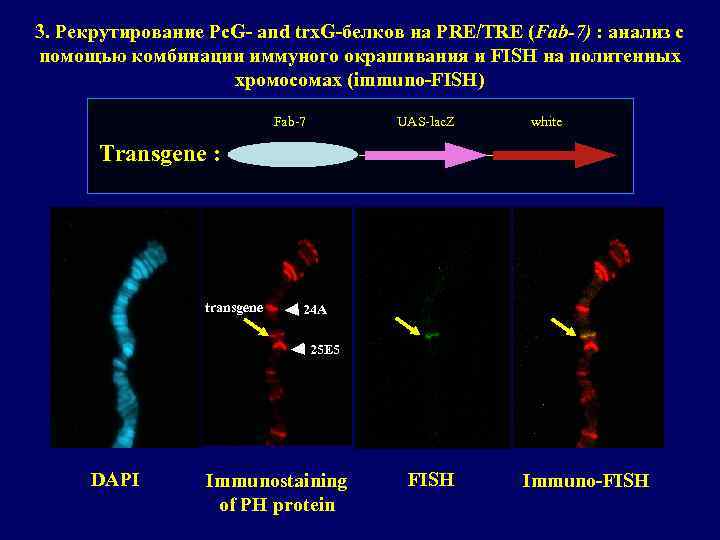
3. Рекрутирование Pc. G- and trx. G-белков на PRE/TRE (Fab-7) : анализ с помощью комбинации иммуного окрашивания и FISH на политенных хромосомах (immuno-FISH) Fab-7 UAS-lac. Z white Transgene : transgene 24 A 25 E 5 DAPI Immunostaining of PH protein FISH Immuno-FISH
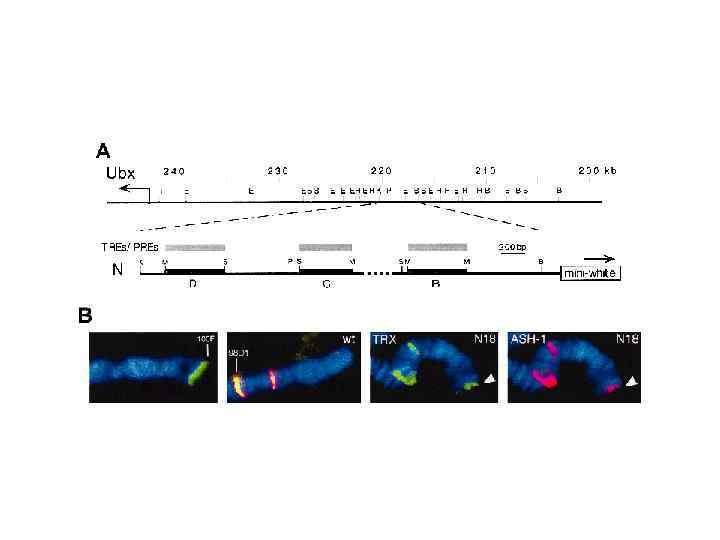

Рекрутирование Pc. G- and trx. Gбелков на PRE/TRE: анализ с помощью Ch. IP (иммунопреципитации сшитого in vivo и затем дробленого ультразвуком хроматина)
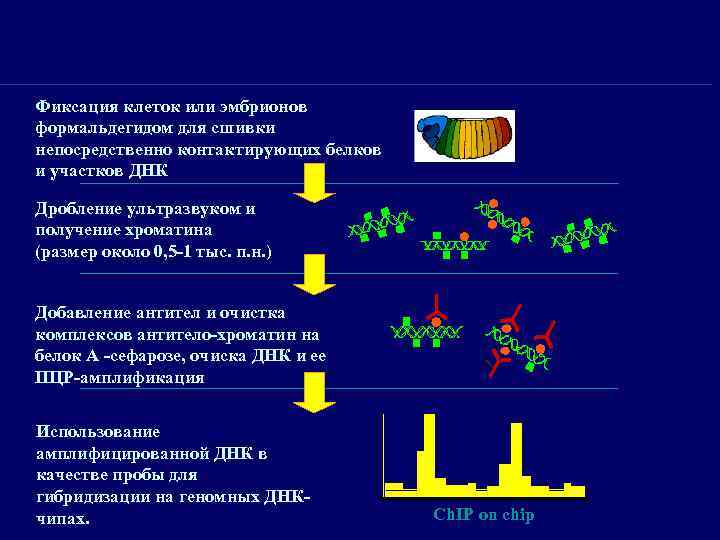
Фиксация клеток или эмбрионов формальдегидом для сшивки непосредственно контактирующих белков и участков ДНК Дробление ультразвуком и получение хроматина (размер около 0, 5 -1 тыс. п. н. ) Добавление антител и очистка комплексов антитело-хроматин на белок А -сефарозе, очиска ДНК и ее ПЦР-амплификация Использование амплифицированной ДНК в качестве пробы для гибридизации на геномных ДНКчипах. Ch. IP on chip
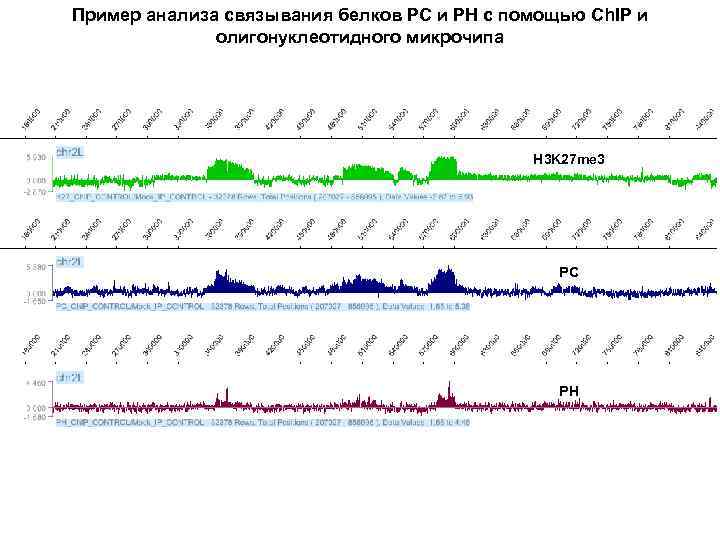
Пример анализа связывания белков PC и PH с помощью Ch. IP и олигонуклеотидного микрочипа H 3 K 27 me 3 PC PH
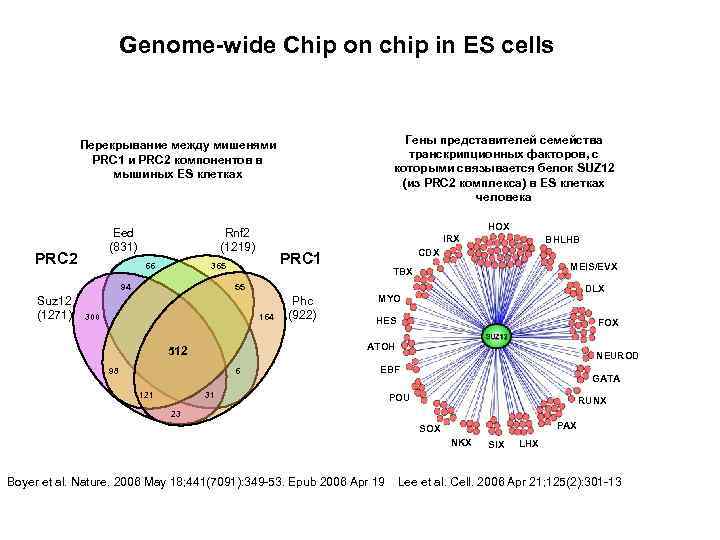
Genome-wide Chip on chip in ES cells Гены представителей семейства транскрипционных факторов, с которыми связывается белок SUZ 12 (из PRC 2 комплекса) в ES клетках человека Перекрывание между мишенями PRC 1 и PRC 2 компонентов в мышиных ES клетках Eed (831) PRC 2 66 IRX BHLHB CDX PRC 1 365 94 Suz 12 (1271) HOX Rnf 2 (1219) MEIS/EVX TBX 55 300 164 HES FOX ATOH 512 98 6 121 Phc (922) DLX MYO NEUROD EBF 31 GATA POU RUNX 23 PAX SOX NKX Boyer et al. Nature. 2006 May 18; 441(7091): 349 -53. Epub 2006 Apr 19 SIX LHX Lee et al. Cell. 2006 Apr 21; 125(2): 301 -13

Иммуннопреципитационное картирование TRX-ассоциированных элементов хроматина в промоторной области гена fkh в клетках слюнных желёз D. melanogaster
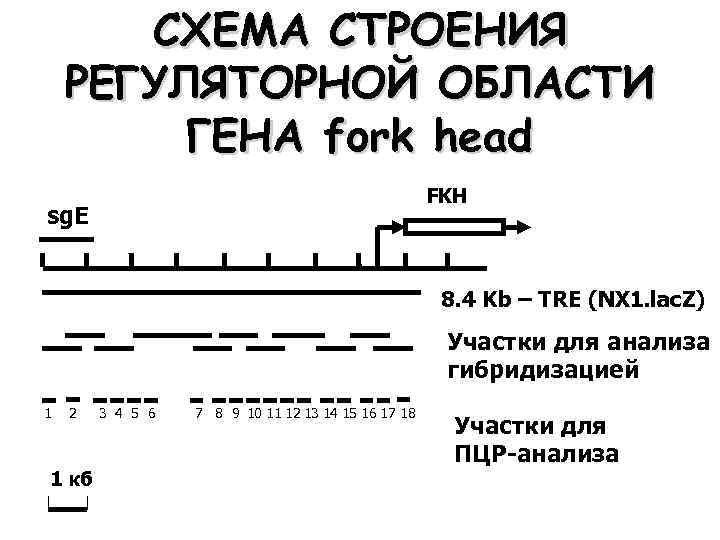
СХЕМА СТРОЕНИЯ РЕГУЛЯТОРНОЙ ОБЛАСТИ ГЕНА fork head FKH sg. E 8. 4 Kb – TRE (NX 1. lac. Z) Участки для анализа гибридизацией 1 2 1 кб 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 Участки для ПЦР-анализа
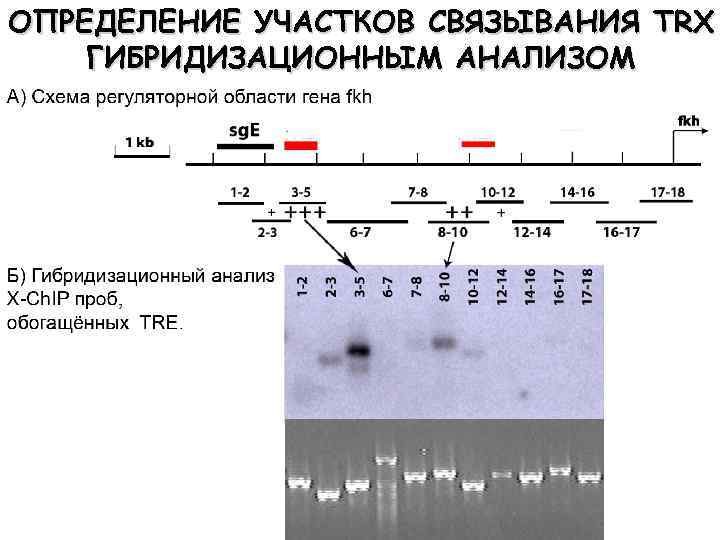
ОПРЕДЕЛЕНИЕ УЧАСТКОВ СВЯЗЫВАНИЯ TRX ГИБРИДИЗАЦИОННЫМ АНАЛИЗОМ
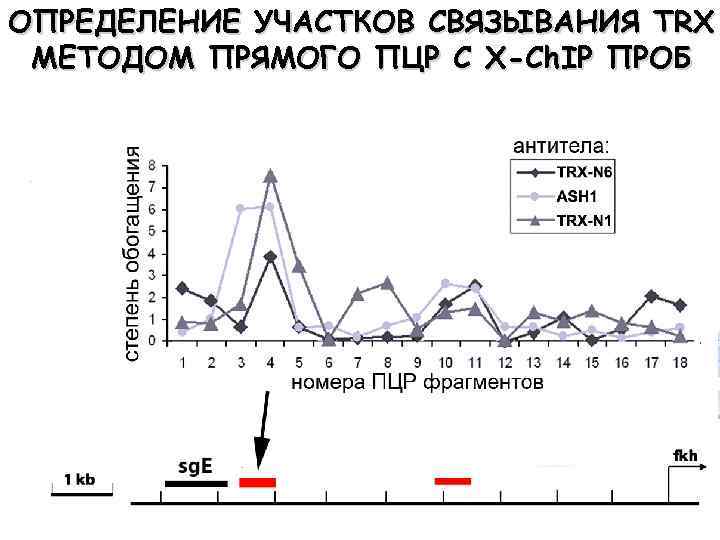
ОПРЕДЕЛЕНИЕ УЧАСТКОВ СВЯЗЫВАНИЯ TRX МЕТОДОМ ПРЯМОГО ПЦР С X-Ch. IP ПРОБ
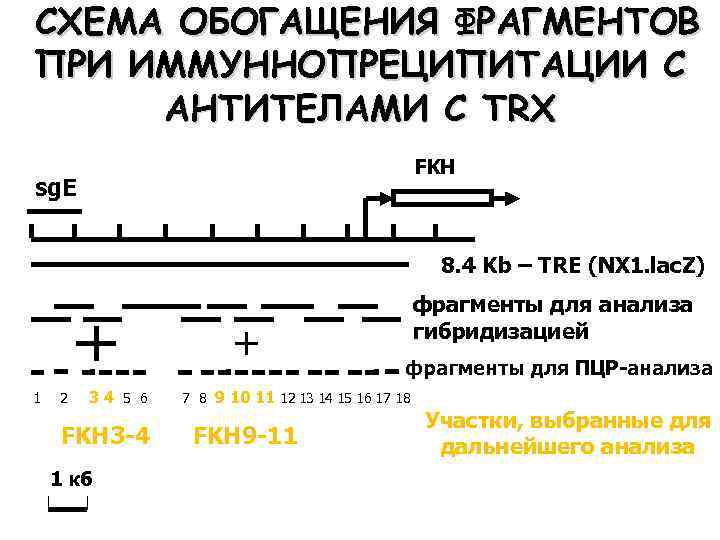
СХЕМА ОБОГАЩЕНИЯ ФРАГМЕНТОВ ПРИ ИММУННОПРЕЦИПИТАЦИИ С АНТИТЕЛАМИ С TRX FKH sg. E 8. 4 Kb – TRE (NX 1. lac. Z) фрагменты для анализа гибридизацией фрагменты для ПЦР-анализа 1 2 34 5 6 FKH 3 -4 1 кб 7 8 9 10 11 12 13 14 15 16 17 18 FKH 9 -11 Участки, выбранные для дальнейшего анализа

Исследование функциональной значимости гипотетических TRE in vivo при помощи трансгенных конструкций
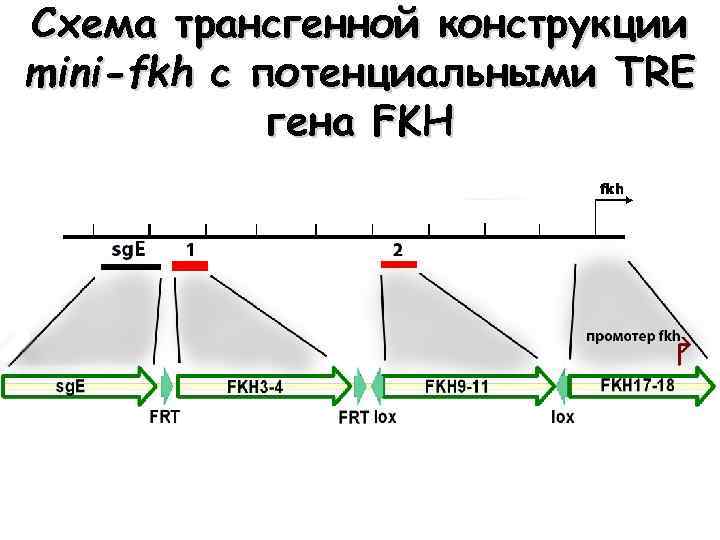
Схема трансгенной конструкции mini-fkh с потенциальными TRE гена FKH
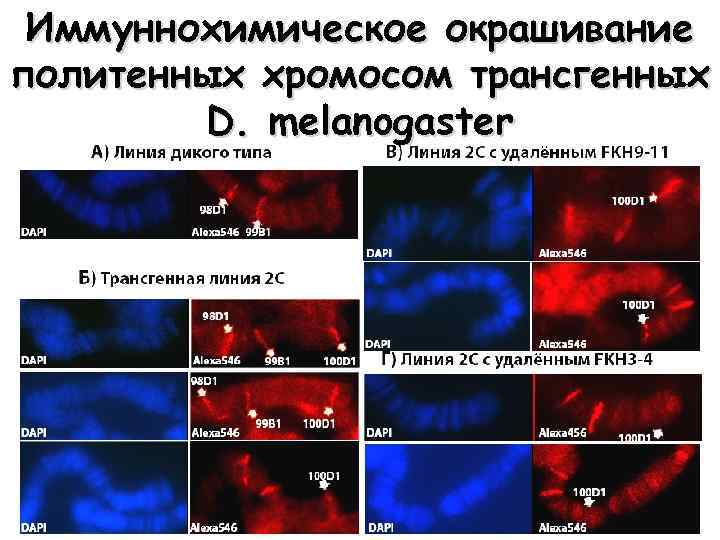
Иммуннохимическое окрашивание политенных хромосом трансгенных D. melanogaster
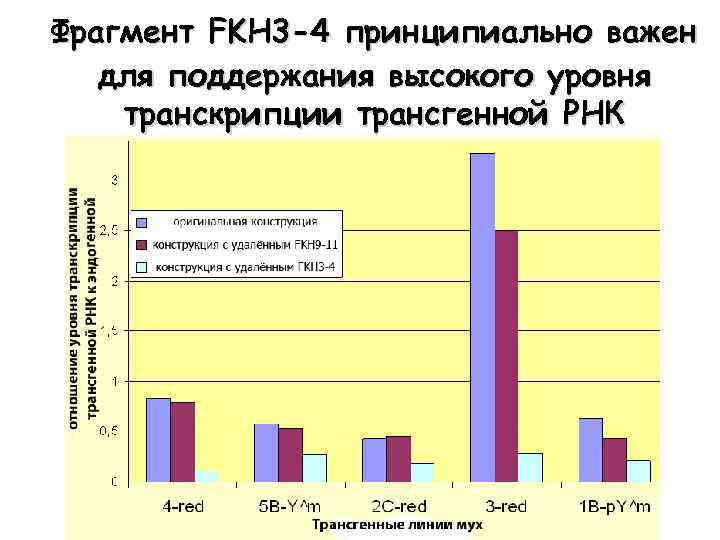
Фрагмент FKH 3 -4 принципиально важен для поддержания высокого уровня транскрипции трансгенной РНК

Анализ распределения модифицированных гистонов в промоторной области гена fkh
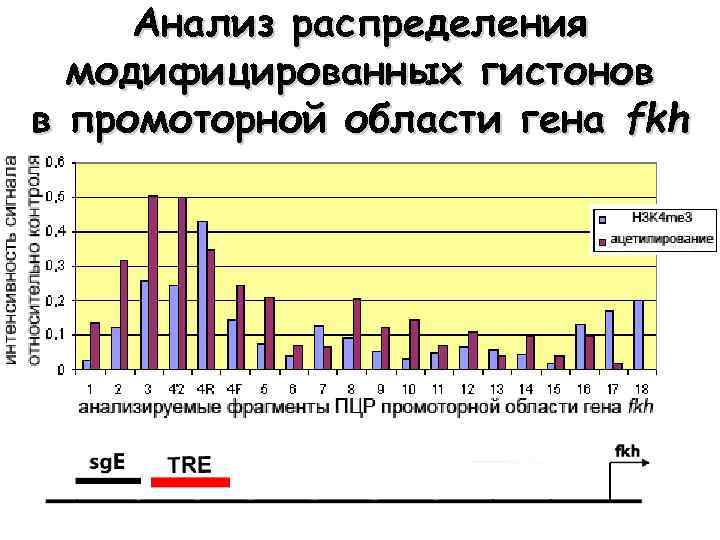
Анализ распределения модифицированных гистонов в промоторной области гена fkh

Демонстрация колокализации TRE c элементами хроматина, ассоциированными со структурами ядерного скелета
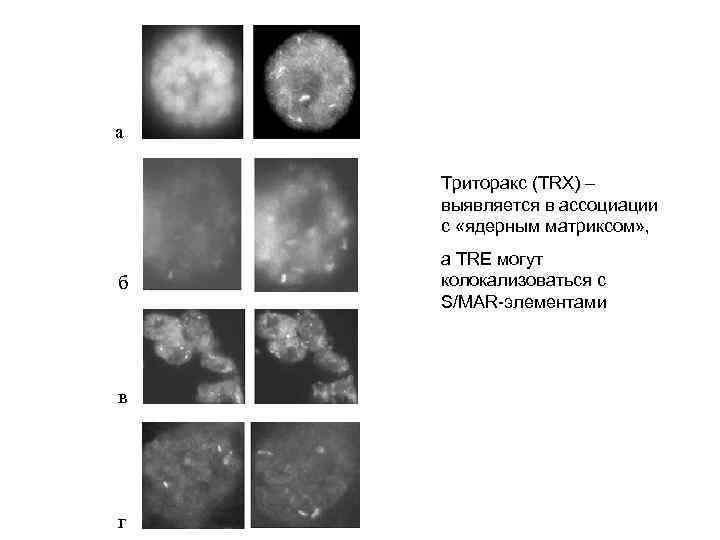
а Триторакс (TRX) – выявляется в ассоциации с «ядерным матриксом» , б в г а TRE могут колокализоваться с S/MAR-элементами

Взаимодействие между различными (копиями) PREs
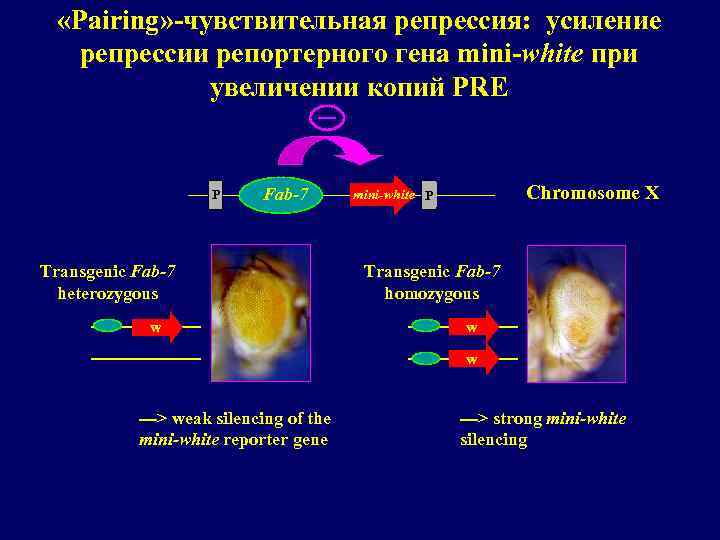
«Pairing» -чувствительная репрессия: усиление репрессии репортерного гена mini-white при увеличении копий PRE P Fab-7 Transgenic Fab-7 heterozygous w Chromosome X mini-white P Transgenic Fab-7 homozygous w w ---> weak silencing of the mini-white reporter gene ---> strong mini-white silencing
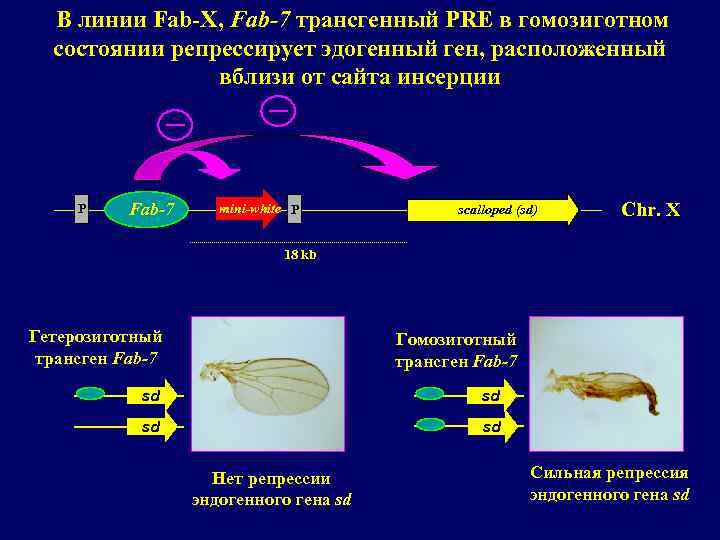
В линии Fab-X, Fab-7 трансгенный PRE в гомозиготном состоянии репрессирует эдогенный ген, расположенный вблизи от сайта инсерции P Fab-7 mini-white P scalloped (sd) Chr. X 18 kb Гетерозиготный трансген Fab-7 Гомозиготный трансген Fab-7 sd sd Нет репрессии эндогенного гена sd Сильная репрессия эндогенного гена sd
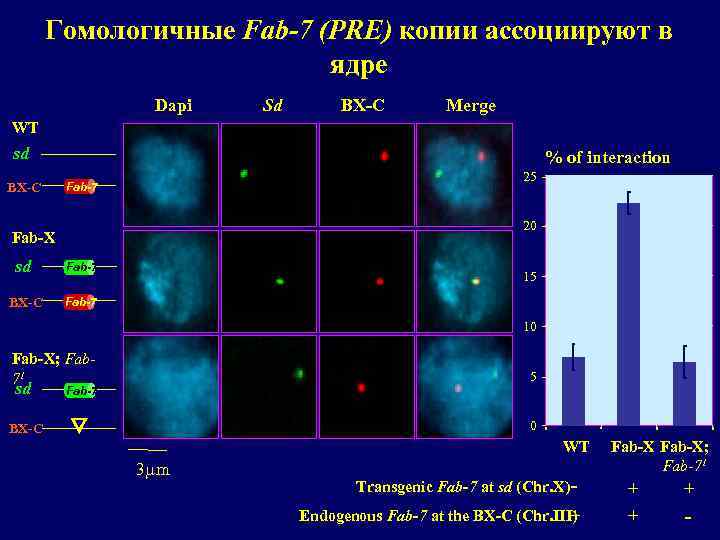
Гомологичные Fab-7 (PRE) копии ассоциируют в ядре Dapi Sd BX-C Merge WT sd BX-C % of interaction 25 - Fab-7 20 - 15 - 10 - Fab-X; Fab 71 5 - BX-C 0 - Fab-X sd Fab-7 BX-C Fab-7 sd Fab-7 WT 3 mm Transgenic Fab-7 at sd (Chr. X) - + Endogenous Fab-7 at the BX-C (Chr. III) Fab-X; Fab-71 + + + -

Два идентичных Fab-7, находящиеся на различных хромосомах (!) могут взаимодействовать в ядре, что ведет к усилению Pc. G-зависимой репрессии

Interactions among Polycomb Domains Are Guided by Chromosome Architecture (Tolhuis et al. (2011) PLo. S Genet. 7(3): e 1001343. ) Polycomb group (Pc. G) proteins bind and regulate hundreds of genes. Previous evidence has suggested that long-range chromatin interactions may contribute to the regulation of Pc. G target genes. We adapted the Chromosome Conformation Capture on Chip (4 C) assay to systematically map chromosomal interactions in Drosophila melanogaster larval brain tissue. Our results demonstrate that Pc. G target genes interact extensively with each other in nuclear space. These interactions are highly specific for Pc. G target genes, because non-target genes with either low or high expression show distinct interactions. Notably, interactions are mostly limited to genes on the same chromosome arm, and we demonstrate that a topological rather than a sequence-based mechanism is responsible for this constraint. Our results demonstrate that many interactions among Pc. G target genes exist and that these interactions are guided by overall chromosome architecture.

Участие некодирующих РНК в работе эпигенетических регуляторных систем

Мир некодирующих РНК (нк. РНК) • Недавние исследования показали, что большая часть генома человека транскрибируется как нк. РНК • Белок-кодирующая фракция геномной ДНК обратно пропорциональна сложности организма (Taft et al. , 2007): у прокариот – 90% генома, в дрожжах – 68%, у нематод 25%, у насекомых – 17%, у человека – 1% (!) • В последние несколько лет наблюдается все возрастающее накопление данных о центральной роли нк. РНК в разнообразных эпигенетических механизмах регуляции тканеспецифической активности генов (в развитии) и ремоделирования хроматина

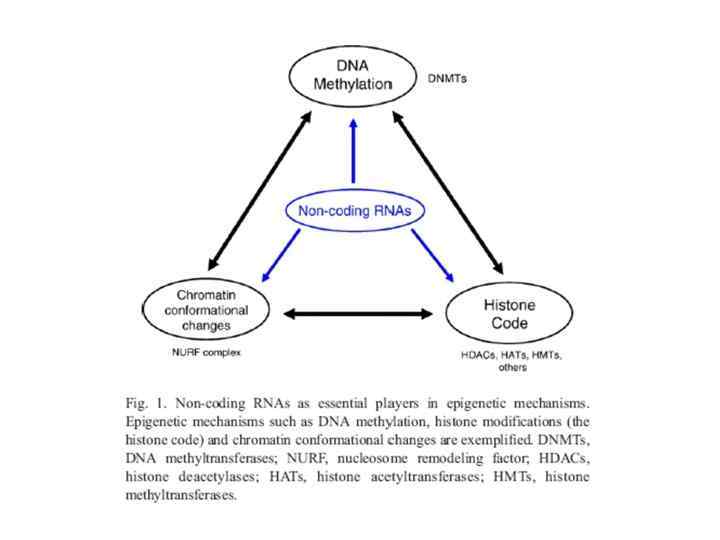

нк. РНК разделяют на 2 класса • 1 - короткие нк. РНК, функционирование которых зависит от комплементаности их последовательности: mi. RNA, si. RNA, pi. RNA или rasi. RNA (piwi-interacting, repeat-associated RNA); репрессия генов-мишеней • 2 - длинные некодирующие РНК (0. 3 -несколько тыс. нуклеотидов), могут работать in trans и in cis, не зависят от комплементарности последовательности

micro RNA and small interfering RNA • Транскрибируются как более длинные предшественники, формирующие шпильки; обрезаются в ядре ферментом Drosha (RNase III) до ~65 п. н. ; • После транспортировки из ядра в цитоплазму пре-ми. РНК обрабатывается (обрезается) ферментом Dicer, в результате чего получается дуплекс 19 -25 п. н. , который включается в mi. RNAinducible silencing complex (mi. RISC), содержащий белки семейства Argonaute и другие факторы; • этот комплекс связывается с м. РНК-мишенью и или деградирует её, или ингибирует ее трансляцию с помощью других механизмов • Dicer и другие компоненты этой системы очень важны для процессов развития (мутации обычно ведут к смерти эмбрионов)

Piwi-interacting RNAs (repeat-associated RNAs) • имеют размер около 24 -30 нукл. ; продуцируются Dicerнезависимым механизмом (в отличие от mi. RNAs) • были клонированы в результате совместной очистки со сперматогенез-специфическим членом семейства белков Argonaute – белками PIWI • места их транскрипции картитруются в основном в повторяющихся элементах • важны для поддержания требуемой специфичности половых клеток • участвуют в консервативных в эволюции механизмах репрессии транскрипции повторяющихся элементов (у мух, рыб, млекопитающих)
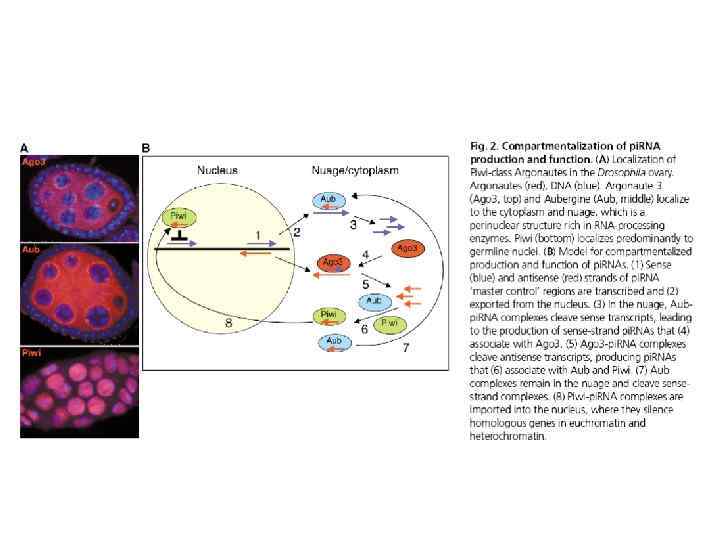

- Transgenic (+hs. GAL 4/UAS-lac. Z) assay is used to show that early embryonic transcription through a memory element (CMM, or PRE/TRE: bxd, MCP, Fab 7) correlated with the relief of silencing imposed by the Polycomb group proteins - A memory element remodeled by the process of transcription was able to maintain active expression of a reporter gene throughout development - In the BX-C of D. melanogaster, the segment-specific expression of noncoding intergenic transcripts during embryogenesis could fulfill this switching role for memory elements regulated by the Pc- and trx-proteins

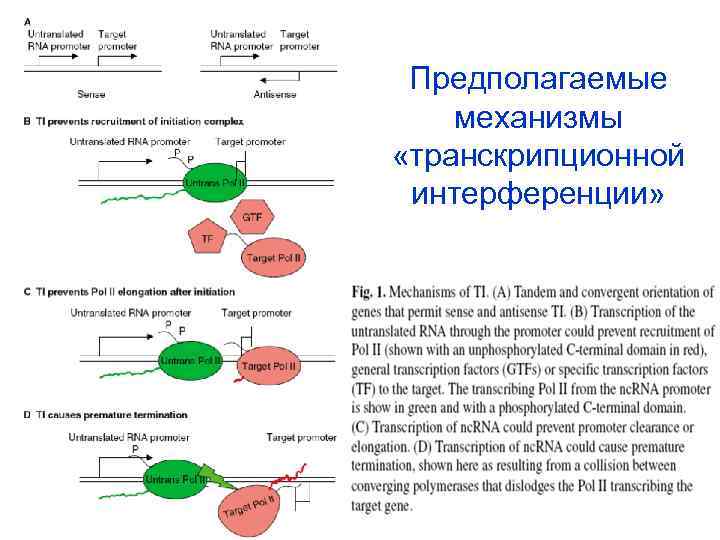
Предполагаемые механизмы «транскрипционной интерференции»
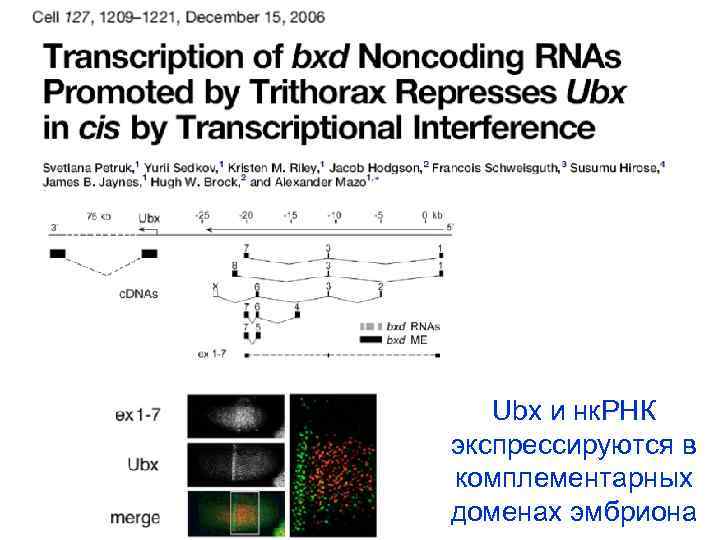
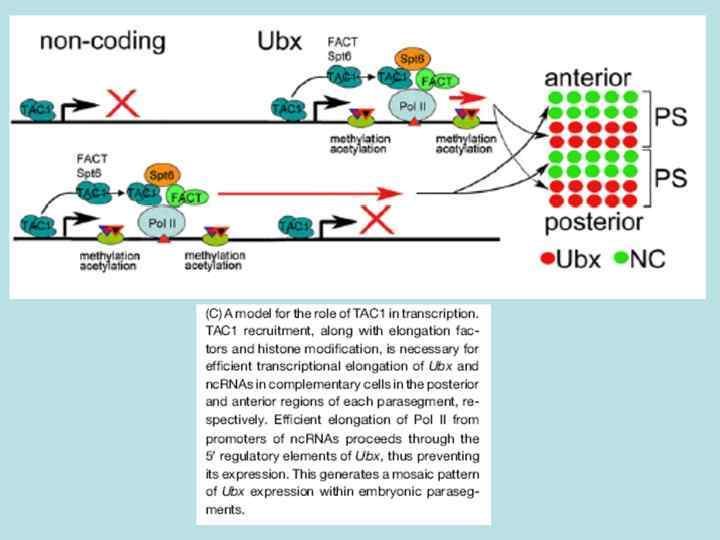
Ubx и нк. РНК экспрессируются в комплементарных доменах эмбриона
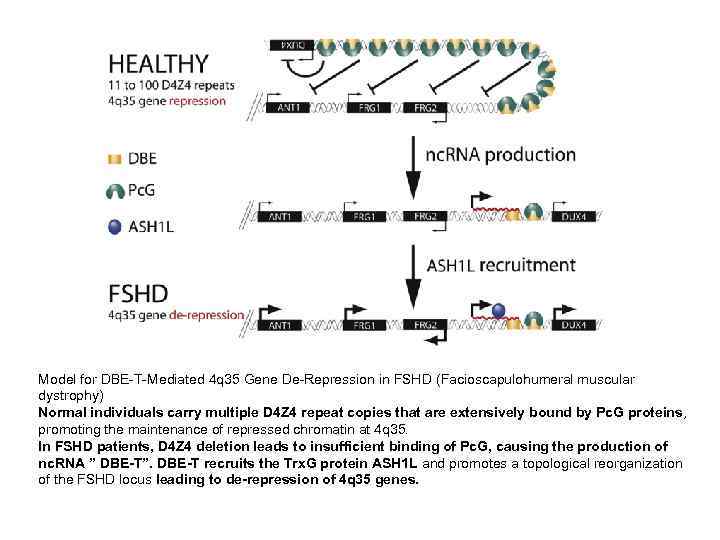
Model for DBE-T-Mediated 4 q 35 Gene De-Repression in FSHD (Facioscapulohumeral muscular dystrophy) Normal individuals carry multiple D 4 Z 4 repeat copies that are extensively bound by Pc. G proteins, promoting the maintenance of repressed chromatin at 4 q 35. In FSHD patients, D 4 Z 4 deletion leads to insufficient binding of Pc. G, causing the production of nc. RNA ” DBE-T”. DBE-T recruits the Trx. G protein ASH 1 L and promotes a topological reorganization of the FSHD locus leading to de-repression of 4 q 35 genes.
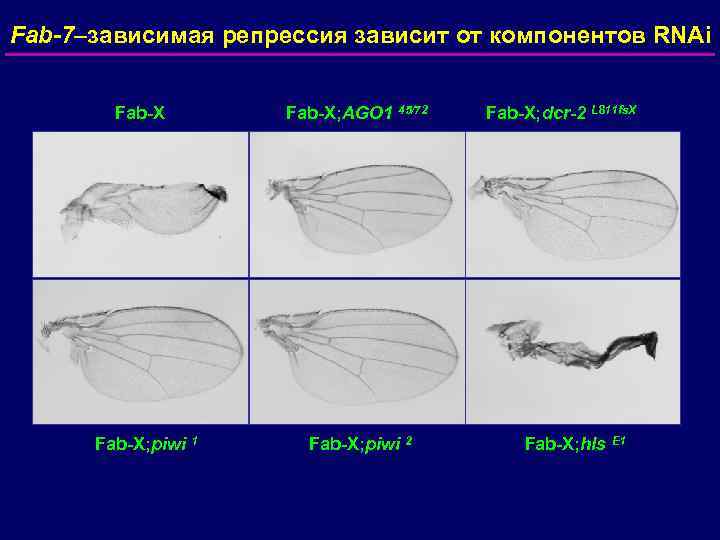
Fab-7–зависимая репрессия зависит от компонентов RNAi Fab-X; piwi 1 Fab-X; AGO 1 45/72 Fab-X; piwi 2 Fab-X; dcr-2 L 811 fs. X Fab-X; hls E 1

Ядерные RNAi-компоненты требуются для Pc. G-зависимой репрессии трансгенов …но не для рекрутирования Pc. G-белков на PRE (за исключением piwi) Взаимодействия далеко расположенных PRE нарушаются в RNAi-мутантах
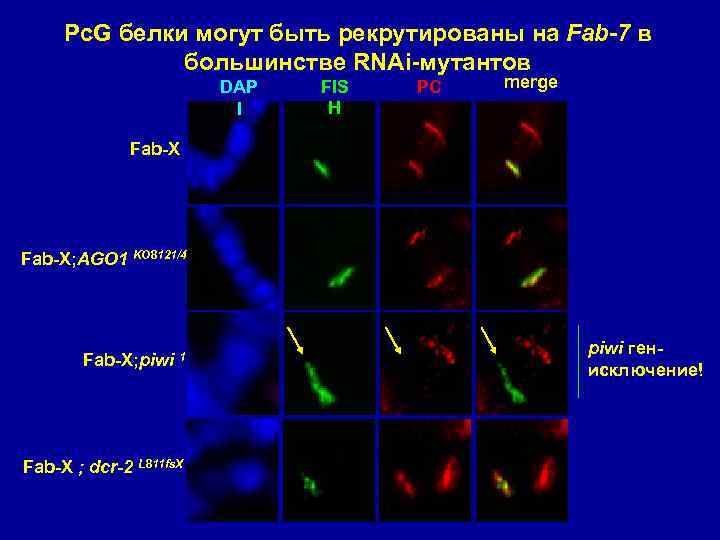
Pc. G белки могут быть рекрутированы на Fab-7 в большинстве RNAi-мутантов DAP I FIS H PC merge Fab-X; AGO 1 KO 8121/45 Fab-X; piwi 1 Fab-X ; dcr-2 L 811 fs. X piwi генисключение!
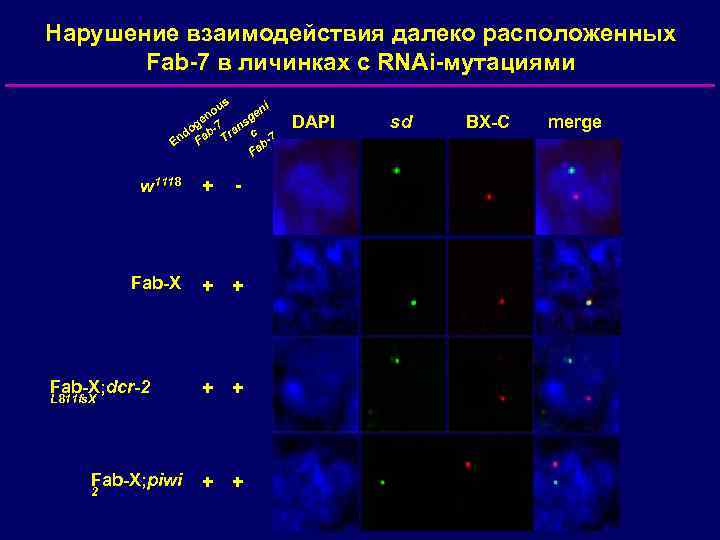
Нарушение взаимодействия далеко расположенных Fab-7 в личинках с RNAi-мутациями s ni ou n ge ge 7 ns do ab- Tra c 7 En F b. Fa w 1118 Fab-X; dcr-2 L 811 fs. X Fab-X; piwi 2 + - + + + DAPI sd BX-C merge

Спасибо за внимание
trx-Pc talk-110313.ppt