Лекция 1 Для всех специальностей.pptx
- Количество слайдов: 31

Белки – биополимеры, мономерами которых являются аминокислоты, связанные пептидными связями

Биохимия — наука о химическом составе живых организмов и о химических процессах, лежащих в основе их жизнедеятельности • Термин "биохимия" предложен в 1903 К. Нейбергом.

Строение и свойства аминокислот Общая структурная формула аминокислоты α
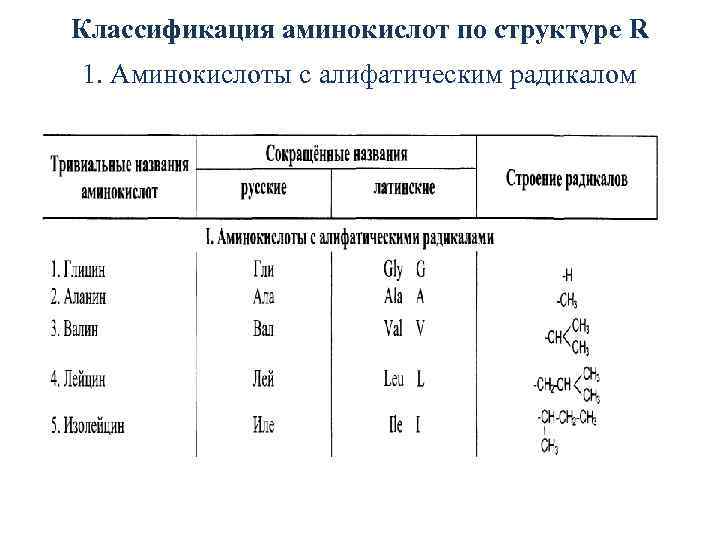
Классификация аминокислот по структуре R 1. Аминокислоты с алифатическим радикалом

Аминокислоты В организме человека содержится около 60 различных аминокислот непротеиногенные • 1. Основные : • 19 аминокислот и иминокислота – ПРОЛИН • • • 2. Редкие: • γ- карбоксиглутаминовая; • гидроксипролин; гидроксилизин; аминолимонная кислота – производные основных аминокислот • Большое разнообразие непритеиногенных аминокислот присутствует в грибах и растениях: • β-циано-аланин; дьенколевая кислота и другие Орнитин; Цитруллин; γ-амино-масляная кислота; β-аланин ;

2. Моноаминодикарбоновые аминокислоты

3. Диаминомонокарбоновые Гуанидиновая группировка

4. Серосодержащие

5. Аминокислоты, содержащие ароматический и гетероциклический радикал
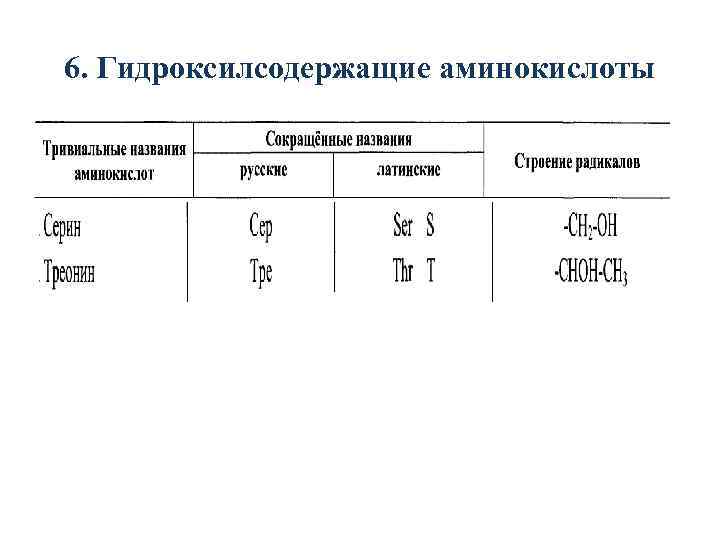
6. Гидроксилсодержащие аминокислоты
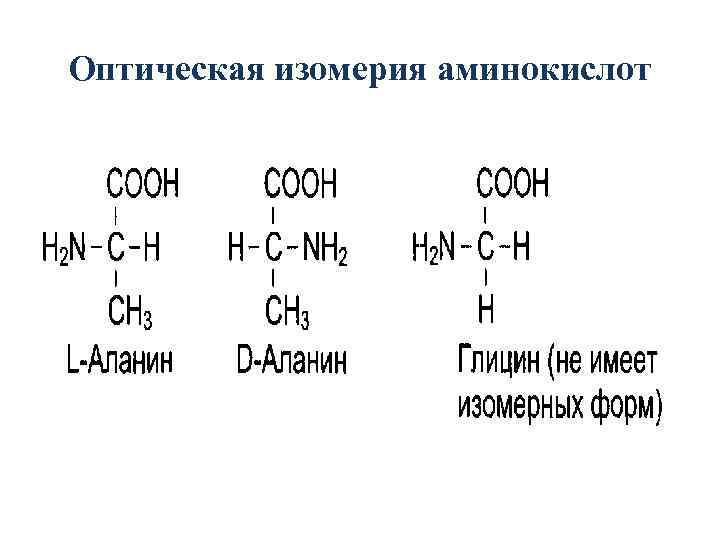
Оптическая изомерия аминокислот

Рацемизация - • неферментативное взаимопревращение D и L стериоизомеров

В белки включаются L- оптические изомеры аминокислот Исключения:

Физико-химические свойства аминокислот 1. Амфотерные электролиты; 2. В водных растворах аминокислоты находятся в виде диполя, или цвиттер-иона 1. Хорошо растворимы в воде и полярных растворителях, кристаллизуются

Изменение суммарного заряда аминокислот в зависимости от р. Н среды

Аминокислоты проявляют все химические свойства карбоновых кислот и аминов
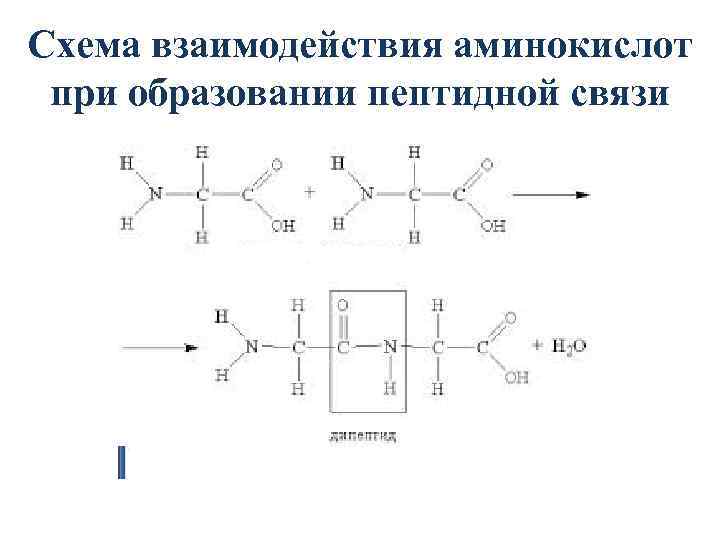
Схема взаимодействия аминокислот при образовании пептидной связи
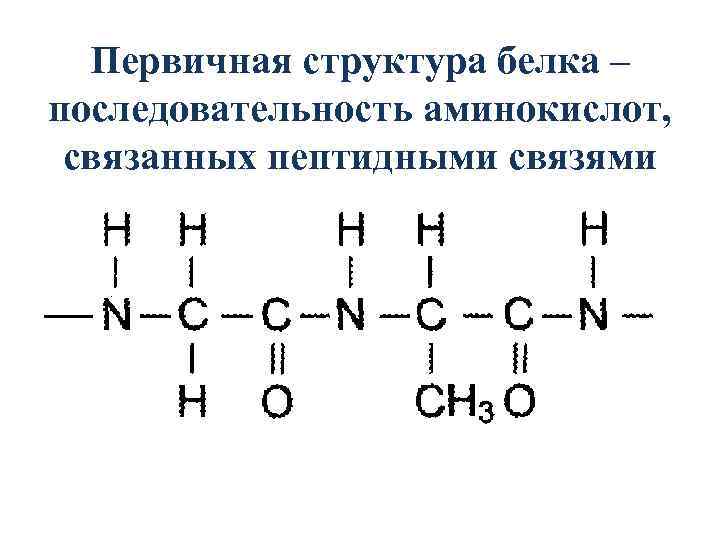
Первичная структура белка – последовательность аминокислот, связанных пептидными связями

Уровни организации белковой молекулы

Виды вторичной структуры • Регулярные • 1. α-спираль • «тугая» спираль , пролиновая спираль, • π-спираль • 2. β-листы, складчатые слои • Нерегулярные 1. повороты — нерегулярные участки полипептидной цепи, которые обеспечивают поворот её направления на 180° 2. полуповороты

Взаимодействия, стабилизирующие вторичную структуру • 1. Водородные связи • 2. Ван-дер-Ваальсовые взаимодействия • Вторичная структура формируется произвольно по принципу достижения минимальной внутренней энергии молекулы
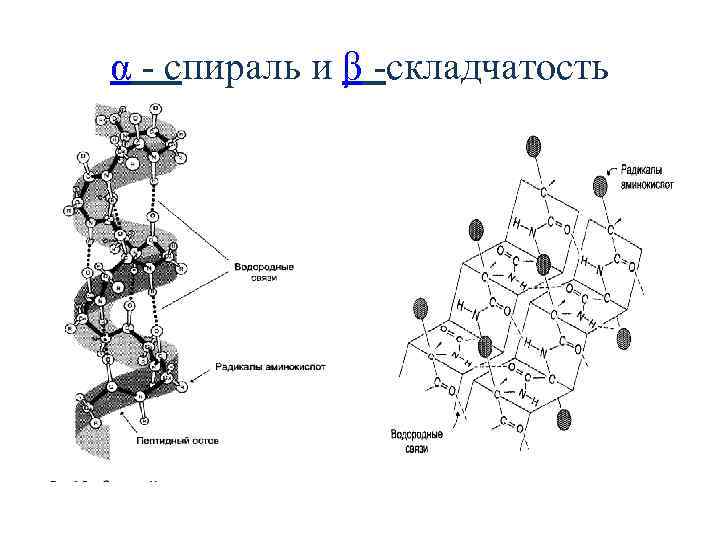
α - спираль и β -складчатость
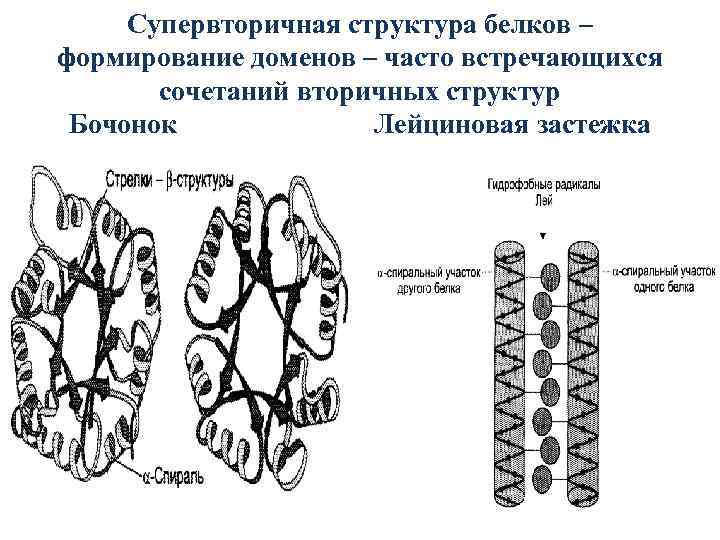
Супервторичная структура белков – формирование доменов – часто встречающихся сочетаний вторичных структур Бочонок Лейциновая застежка

Связи, стабилизирующие третичную структуру белка • 1. Гидрофобные • 2. Ионные • 3. Водородные • 4. Ковалентные (S-S)

Образование третичной структуры белка – ФОЛДИНГ – требует вспомогательных соединений • 1. ЩАПЕРОНЫ • 2. ФЕРМЕНТЫ ФОЛДИНГА

Механизм действия шаперонов
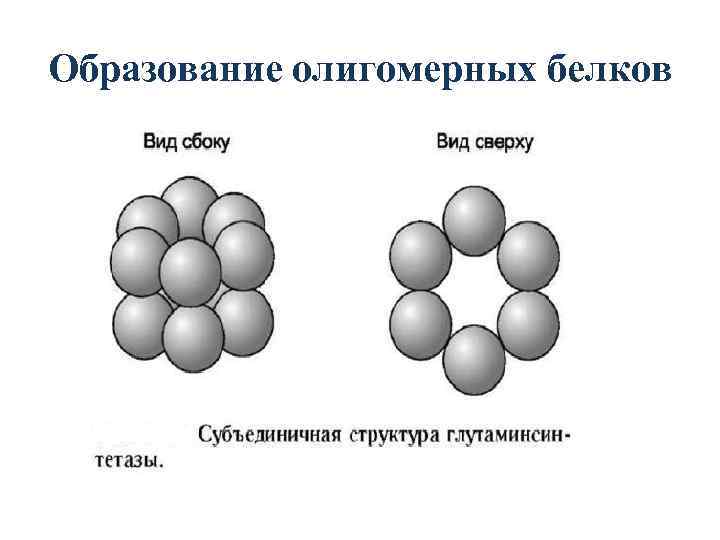
Образование олигомерных белков

Классификация белков по форме молекулы • Глобулярные Фибриллярные • D/d<10 D/d> 10

Классификация белков по структуре СЛОЖНЫЕ ПРОСТЫЕ

Классификация белков по функциям • 1. СТРУКТУРНЫЕ • 4. РЕЦЕПТОРНЫЕ • 2. КАТАЛИТИЧЕСКИЕ • 5. ТРАНСПОРТНЫЕ • 3. РЕГУЛЯТОРНЫЕ • 6. ЗАЩИТНЫЕ • 7. СОКРАТИТЕЛЬНЫЕ

БЕЛКОВЫЕ СУПЕРСКМЕЙСТВА ОРГАНИЗМА ЧЕЛОВЕКА – белки, имеющие сходную структуру и функции • 3. Семейство • 1. Семейство сериновых протеаз рецепторов Тлимфоцитов • 4. Семейство белков • 2. Суперсемейство ГЛАВНОГО иммуноглобулино КОМПЛЕКСА в ГИСТОСОВМЕСТ ИМОСТИ
Лекция 1 Для всех специальностей.pptx