База схем и рисунков.физиология.ppt
- Количество слайдов: 81

База схем и рисунков вся физиология
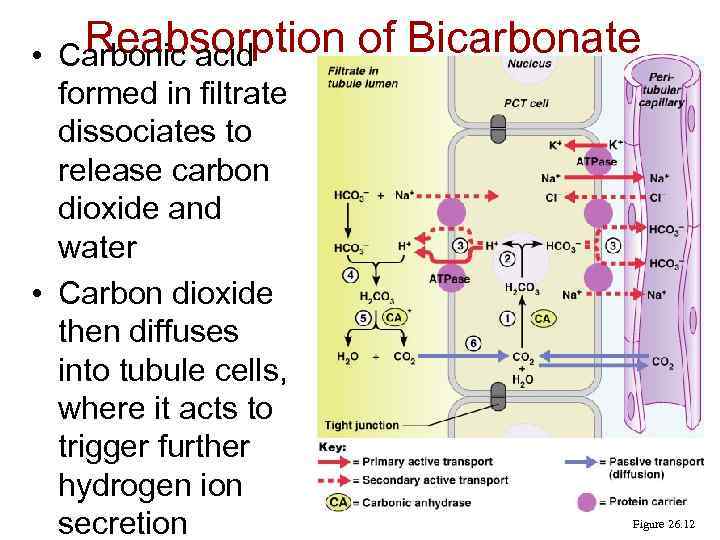
Reabsorption of Bicarbonate • Carbonic acid formed in filtrate dissociates to release carbon dioxide and water • Carbon dioxide then diffuses into tubule cells, where it acts to trigger further hydrogen ion secretion Figure 26. 12

Hydrogen Ion Excretion • In response to acidosis: – Kidneys generate bicarbonate ions and add them to the blood – An equal amount of hydrogen ions are added to the urine Figure 26. 13
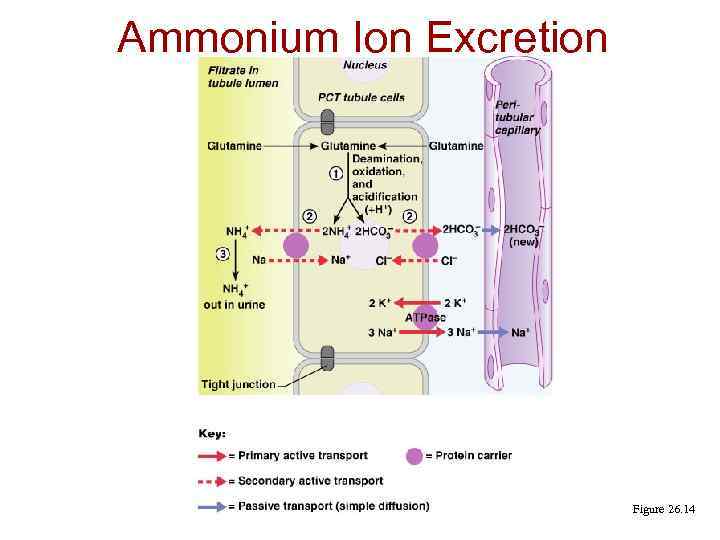
Ammonium Ion Excretion Figure 26. 14
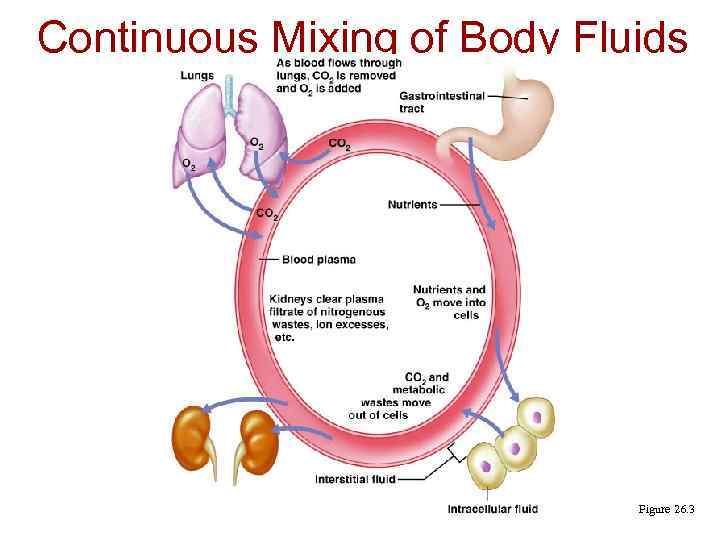
Continuous Mixing of Body Fluids Figure 26. 3
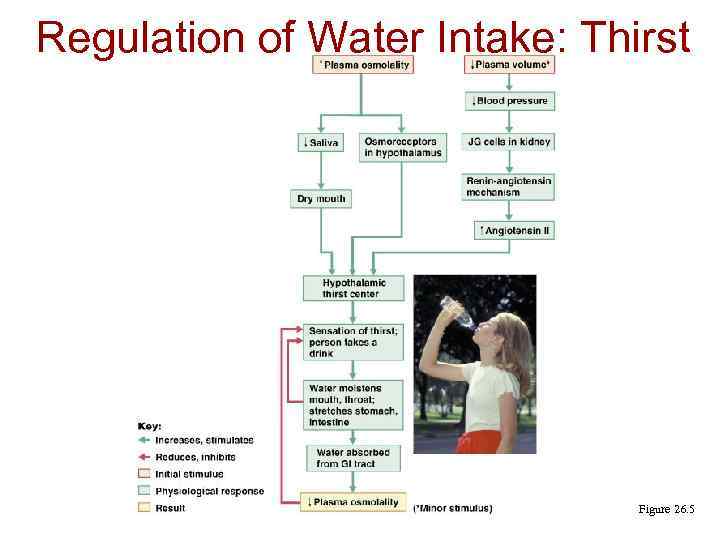
Regulation of Water Intake: Thirst Mechanism Figure 26. 5
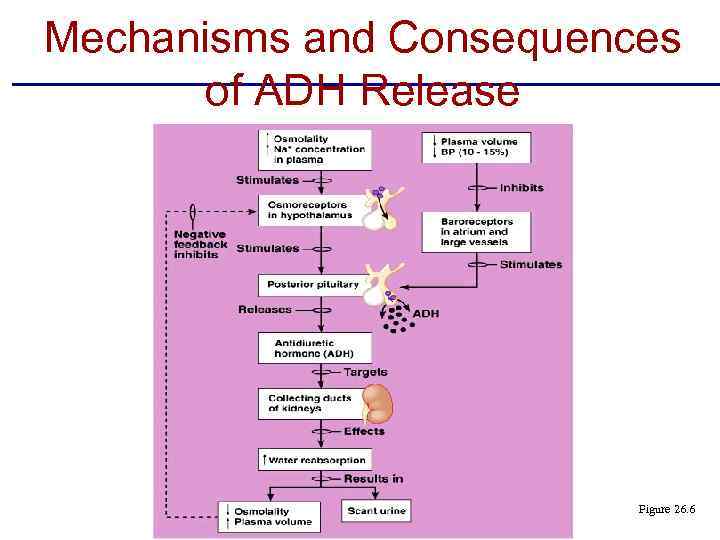
Mechanisms and Consequences of ADH Release Figure 26. 6
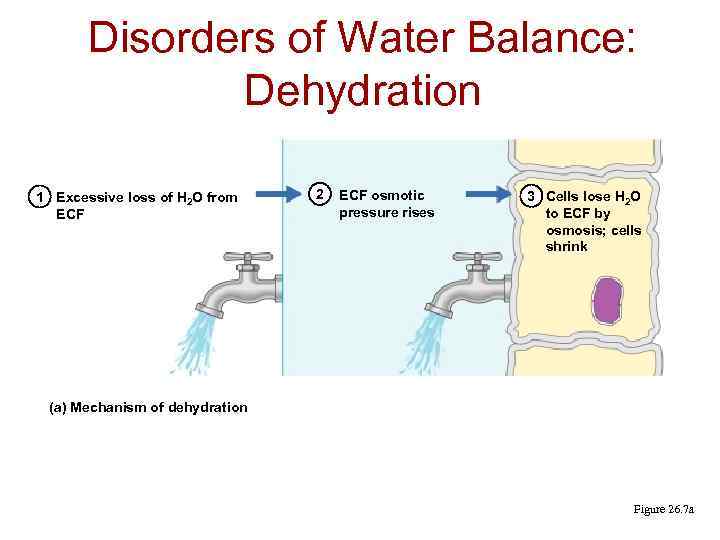
Disorders of Water Balance: Dehydration 1 Excessive loss of H 2 O from ECF 2 ECF osmotic pressure rises 3 Cells lose H 2 O to ECF by osmosis; cells shrink (a) Mechanism of dehydration Figure 26. 7 a
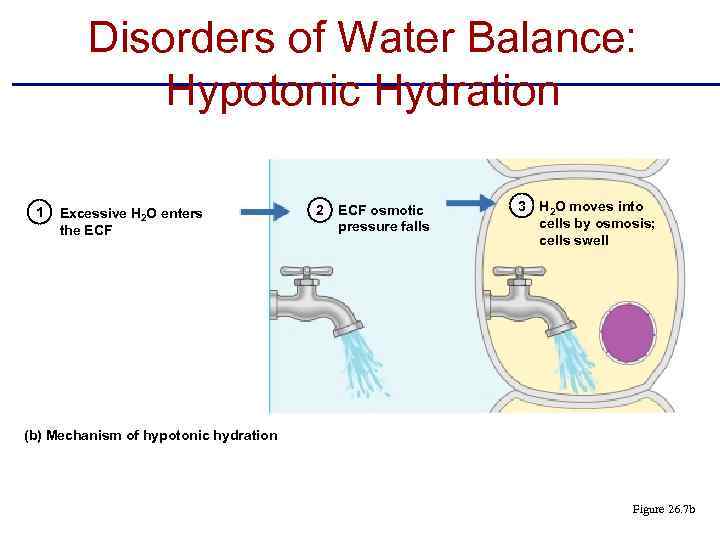
Disorders of Water Balance: Hypotonic Hydration 1 Excessive H 2 O enters the ECF 2 ECF osmotic pressure falls 3 H 2 O moves into cells by osmosis; cells swell (b) Mechanism of hypotonic hydration Figure 26. 7 b
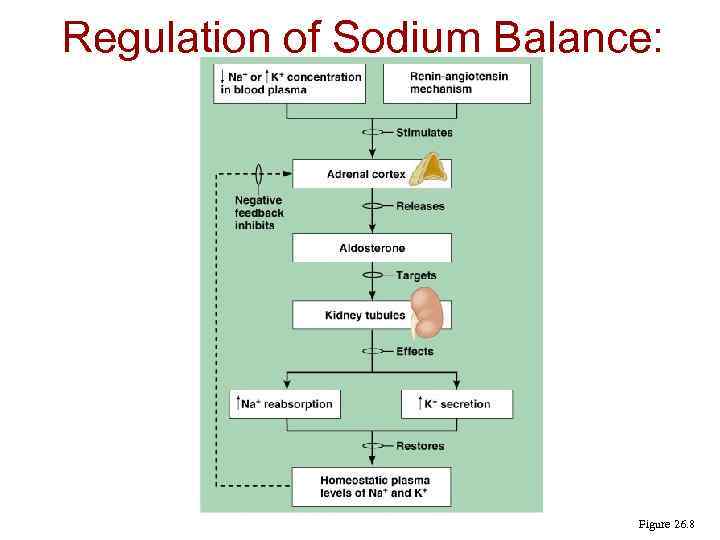
Regulation of Sodium Balance: Aldosterone Figure 26. 8
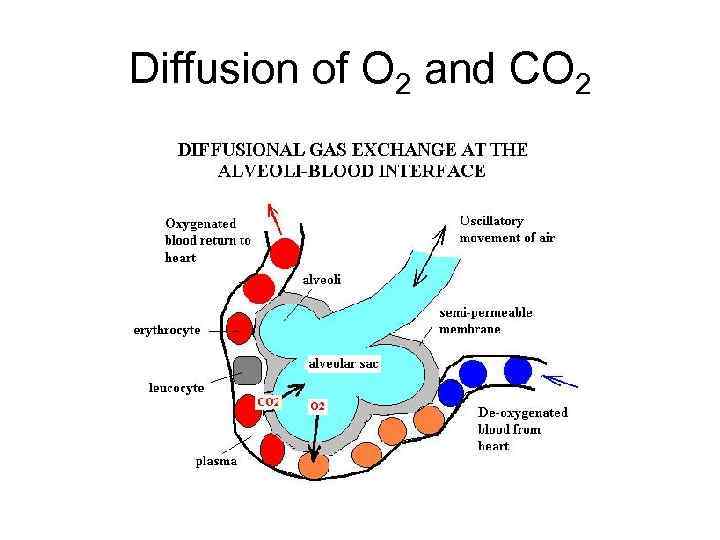
Diffusion of O 2 and CO 2
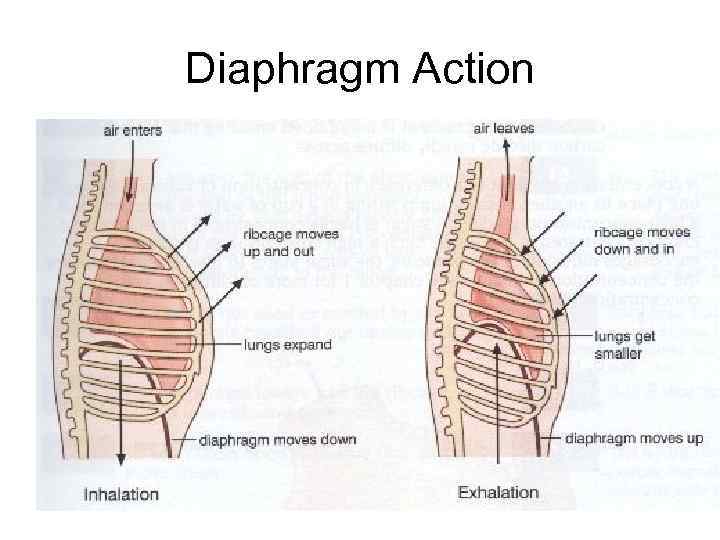
Diaphragm Action
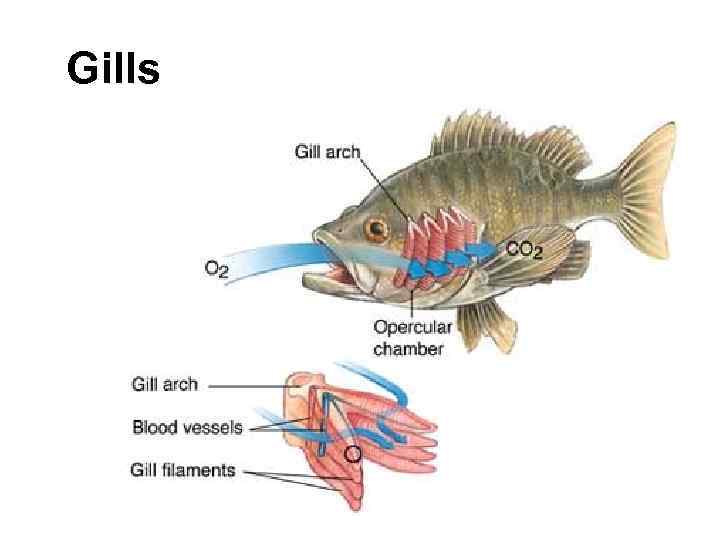
Gills
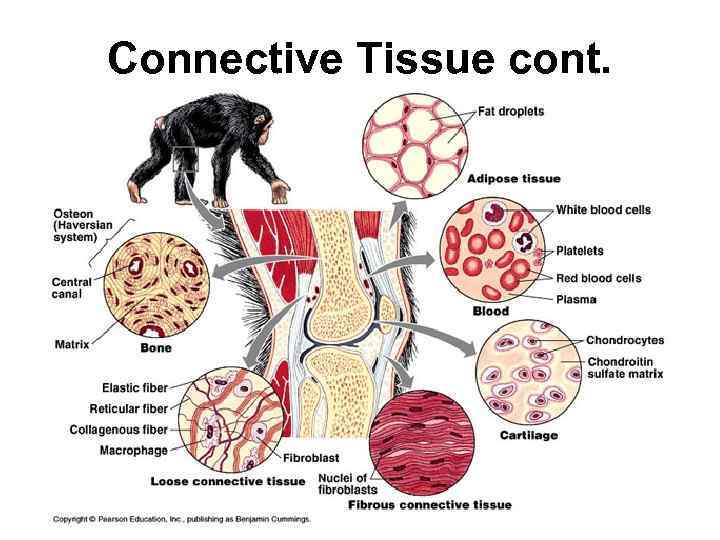
Connective Tissue cont.
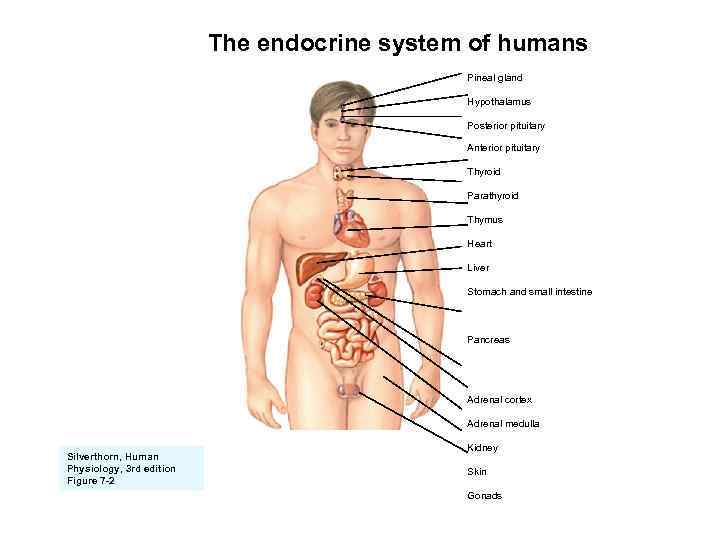
The endocrine system of humans Pineal gland Hypothalamus Posterior pituitary Anterior pituitary Thyroid Parathyroid Thymus Heart Liver Stomach and small intestine Pancreas Adrenal cortex Adrenal medulla Silverthorn, Human Physiology, 3 rd edition Figure 7 -2 Kidney Skin Gonads
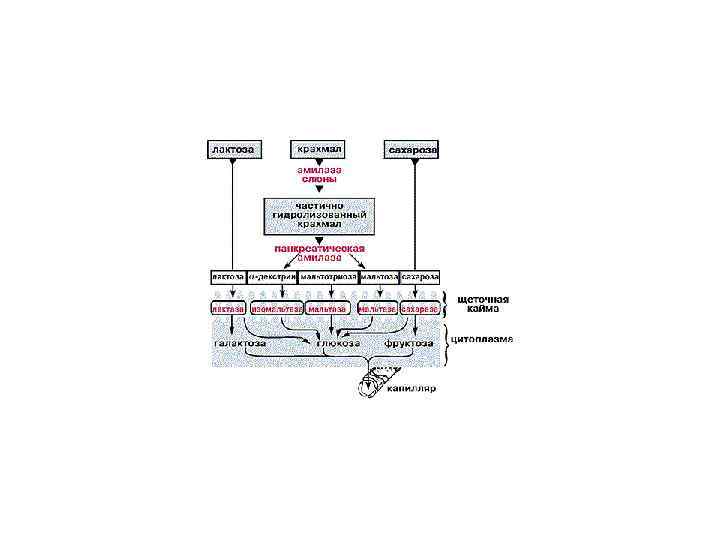
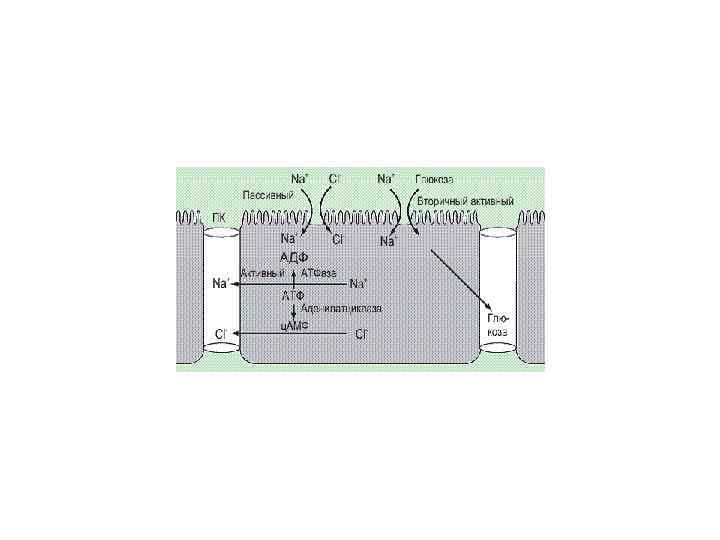
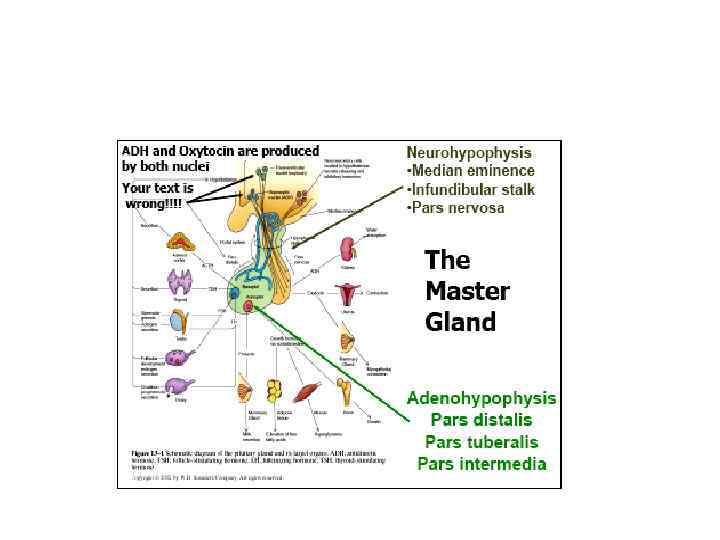
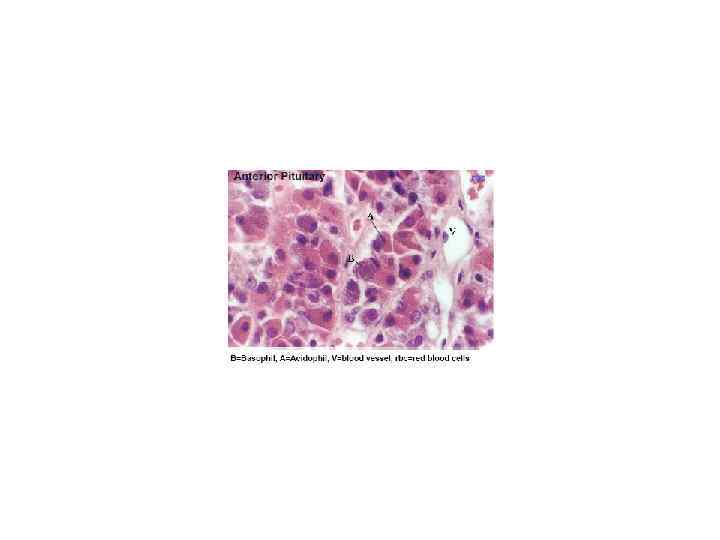
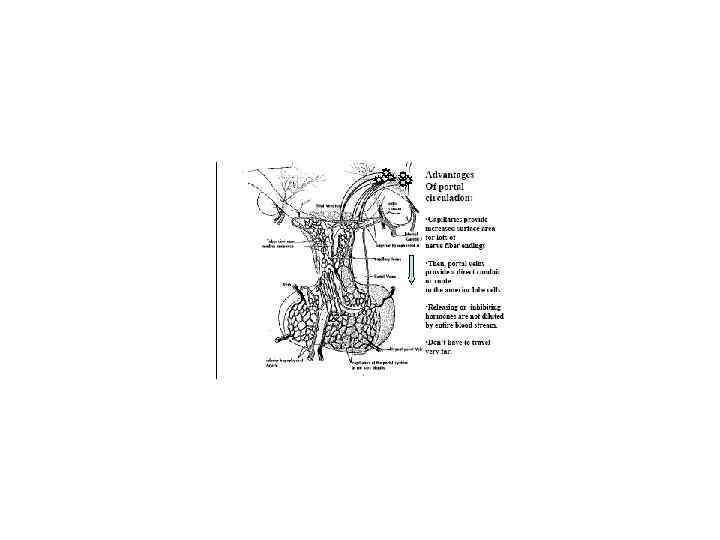
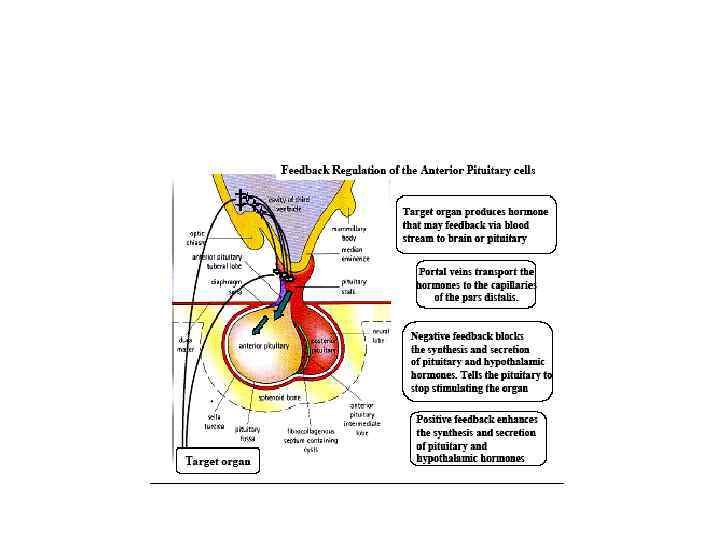
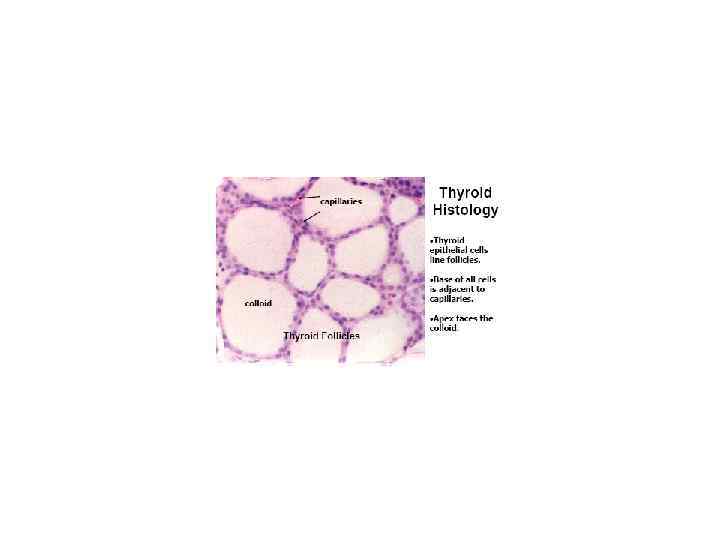

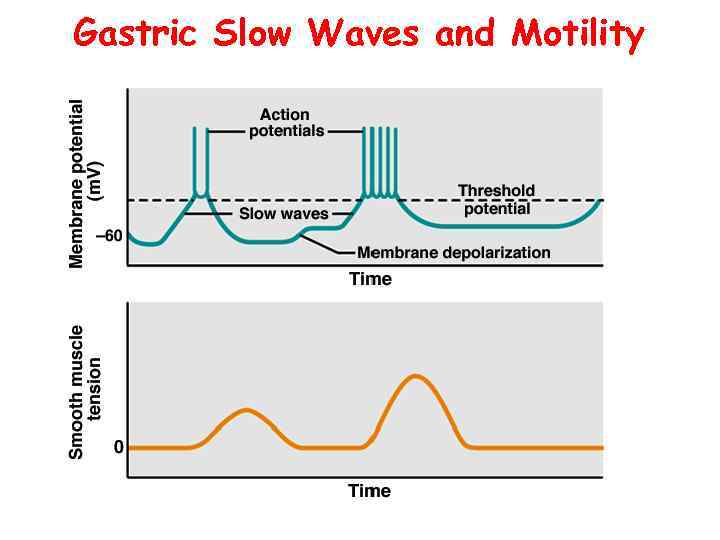
Gastric Slow Waves and Motility
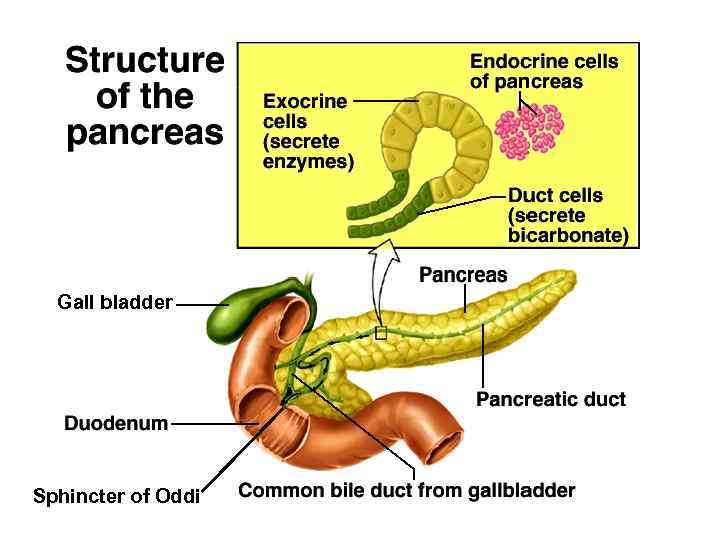
Gall bladder Sphincter of Oddi
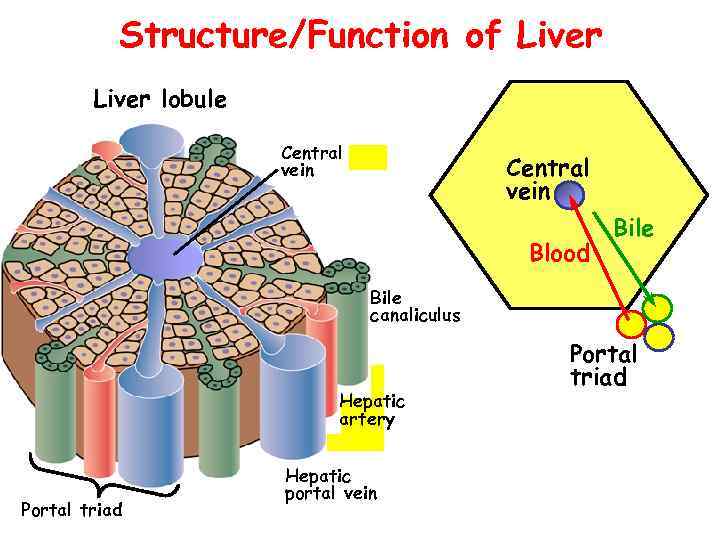
Structure/Function of Liver lobule Central vein Blood Bile canaliculus Hepatic artery Portal triad Hepatic portal vein Portal triad
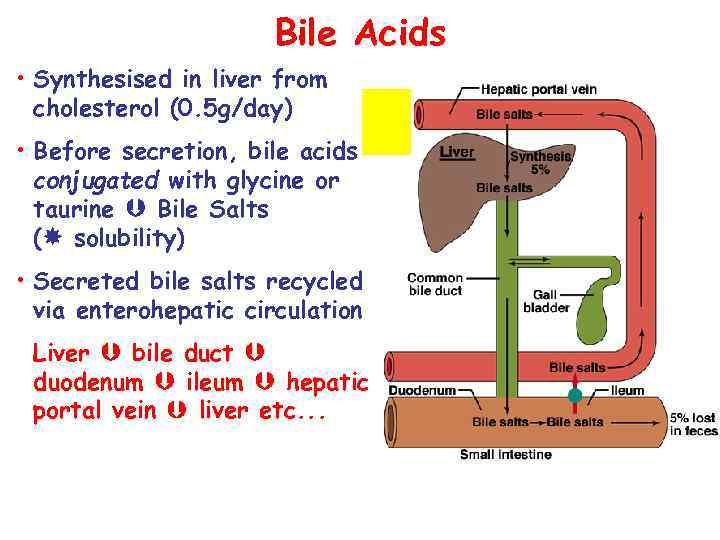
Bile Acids • Synthesised in liver from cholesterol (0. 5 g/day) • Before secretion, bile acids conjugated with glycine or taurine Bile Salts ( solubility) • Secreted bile salts recycled via enterohepatic circulation Liver bile duct duodenum ileum hepatic portal vein liver etc. . .

Физиологическая роль оксида азота
N=O NO Про/антиоксидант NO NO Высокая NO реакционноспособность Период полураспада от 2 до 30 мс
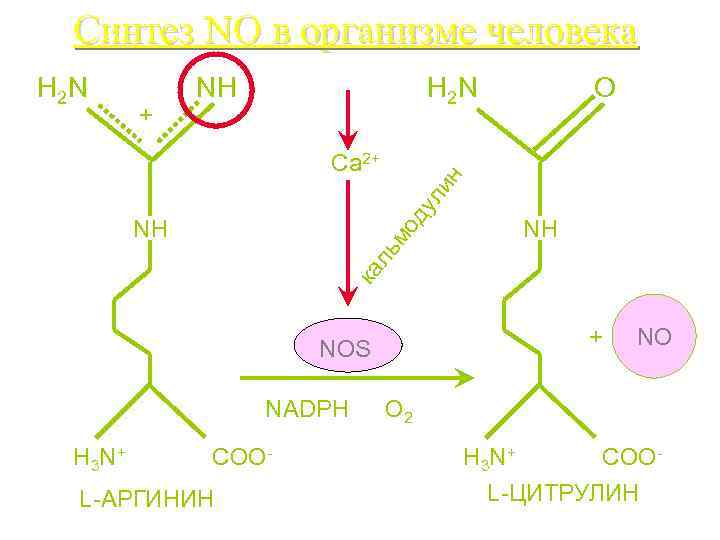
Синтез NO в организме человека H 2 N O H 2 N NH + ду ли н Ca 2+ NH ка ль мо NH + NO NOS NADPH H 3 N+ COOL-АРГИНИН O 2 H 3 N+ COOL-ЦИТРУЛИН
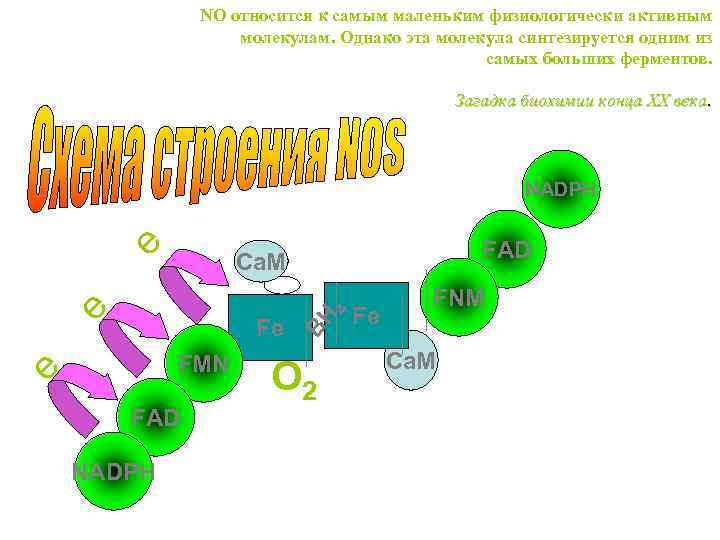
NO относится к самым маленьким физиологически активным молекулам. Однако эта молекула синтезируется одним из самых больших ферментов. Загадка биохимии конца ХХ века. e NADPH e FMN FAD 4 BH e Fe NADPH FAD Ca. M O 2 Fe FNM Ca. M
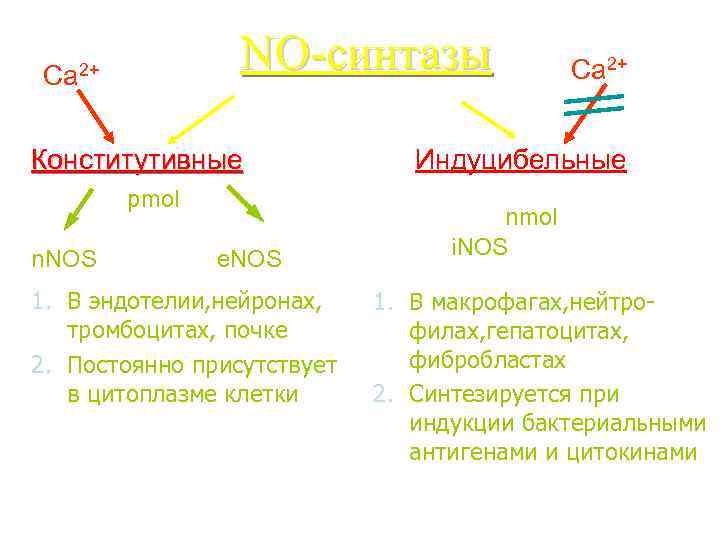
NO-синтазы Ca 2+ Конститутивные pmol n. NOS e. NOS 1. В эндотелии, нейронах, тромбоцитах, почке 2. Постоянно присутствует в цитоплазме клетки Ca 2+ Индуцибельные nmol i. NOS 1. В макрофагах, нейтрофилах, гепатоцитах, фибробластах 2. Синтезируется при индукции бактериальными антигенами и цитокинами

АД, Адгезия тромбоцитов NANC-нейроны, длительная потенциация Почечная гемодинамика, гломерулярная фильтрация Гепатопротекторное действие, моторику ЖКТ, защита слизистой Очищение слизистой, бронходилатация Антимикробное действие
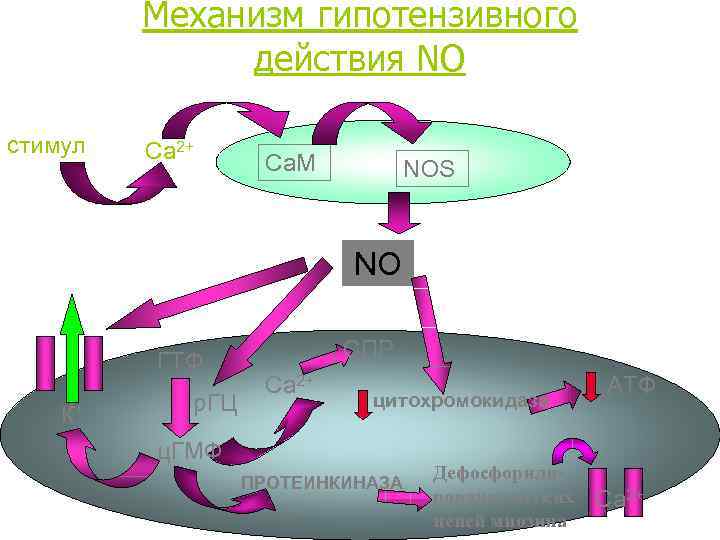
Механизм гипотензивного действия NO стимул Са 2+ Ca. M NOS NO ГTФ К+ р. ГЦ СПР Са 2+ цитохромокидаза ц. ГМФ ПРОТЕИНКИНАЗА Дефосфорилирование легких цепей миозина АТФ Са 2+
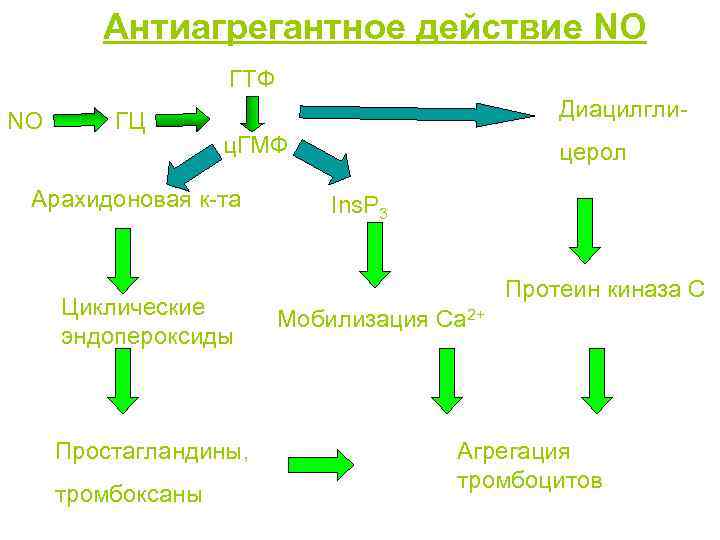
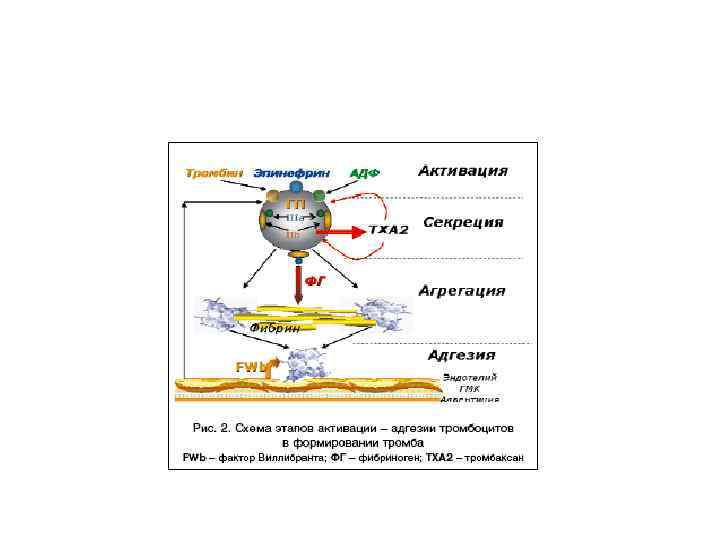
Антиагрегантное действие NO ГТФ NO ГЦ Диацилглиц. ГМФ Арахидоновая к-та Циклические эндопероксиды Простагландины, тромбоксаны церол Ins. Р 3 Протеин киназа С Мобилизация Са 2+ Агрегация тромбоцитов
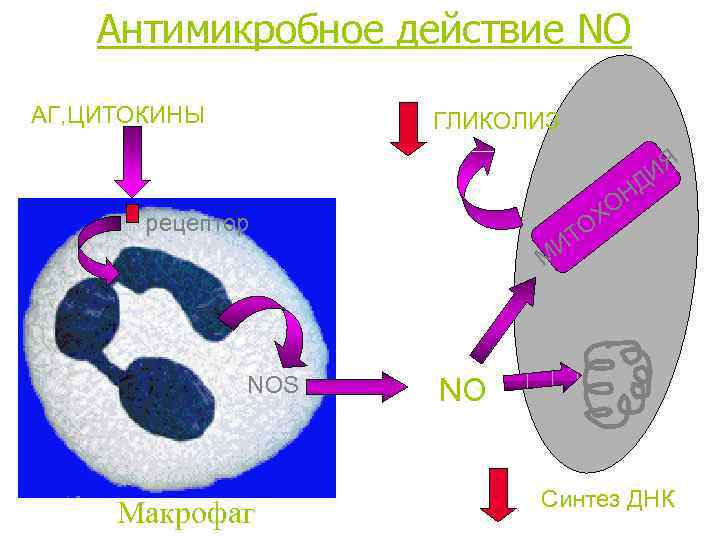
Антимикробное действие NO АГ, ЦИТОКИНЫ ГЛИКОЛИЗ ИЯ Д рецептор ТО И ОН Х М NOS Макрофаг NO Синтез ДНК
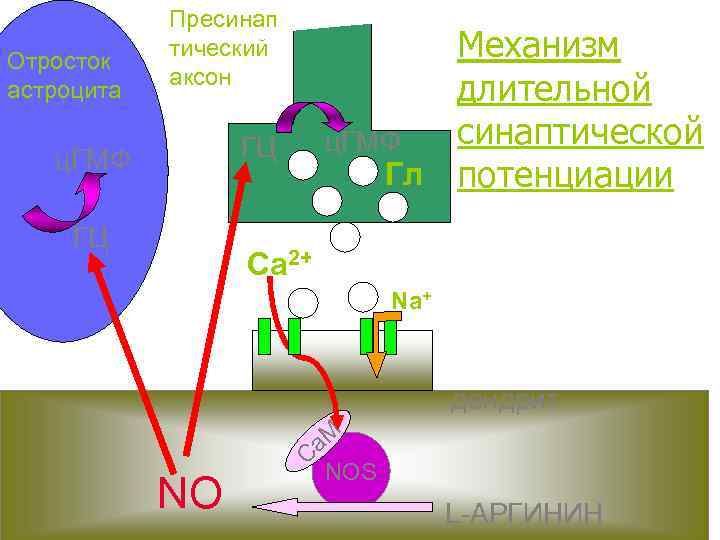
Отросток астроцита Пресинап тический аксон Механизм длительной синаптической ц. ГМФ Гл потенциации ГЦ ц. ГМФ ГЦ Са 2+ Na+ дендрит NO a. M C NOS L-АРГИНИН
Клиническое применение NO Препараты, освобождающие NO при попадании в организм (нитроглицерин) Ингаляции NO (лечение бронхоспазма, бронхиальной астмы, ПЛГ) Терапия опухолевых заболеваний

Резюме: • NO принадлежит к новому классу низкомолекулярных посредников • Оказывает большое количество физиологических эффектов • В больших дозах оказывает разрушающее воздействие на ткани • Находит клиническое применение для лечения некоторых заболеваний

Физиологические эффекты активных форм кислорода.

Основные механизмы образования АФК. +4 e + H+

Реакция Фентона

NAD(P)H-оксидазы - главные физиологические продуценты АФК в клетках сосудов. NAD(P)H-оксидаза - 4 субъединицы: • цитохром b 558: gp 91 phox и p 22 phox • 2 цитозольных компонента: р47 phox и p 67 phox. G-белок rac-семейства участвует в сборке активного комплекса. Точно неизвестно, какие субъединицы функционально активны для производства АФК в разных типах клеток.

Уровень АФК строго контролируется: АФК - внутриклет. «реостат» , модулирующий активность биохимических реакций.
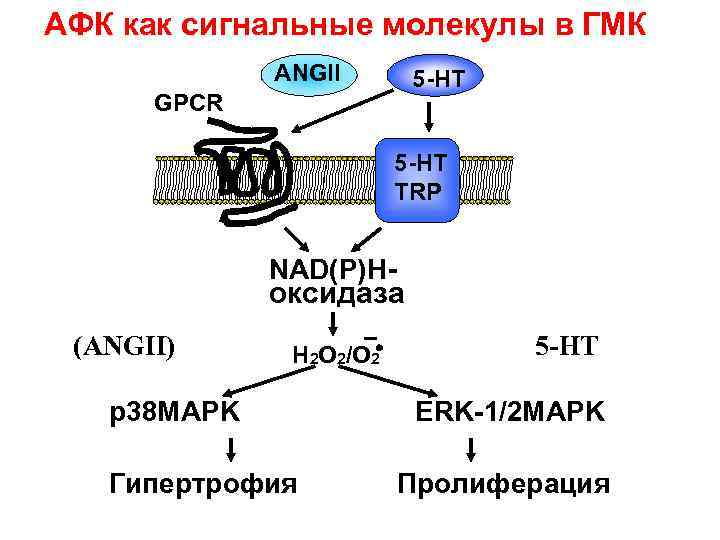
АФК как сигнальные молекулы в ГМК ANGII 5 -HT GPCR 5 -HT TRP NAD(P)H- оксидаза (ANGII) Н 2 О 2/O 2 p 38 MAPK Гипертрофия 5 -HT ERK-1/2 MAPK Пролиферация
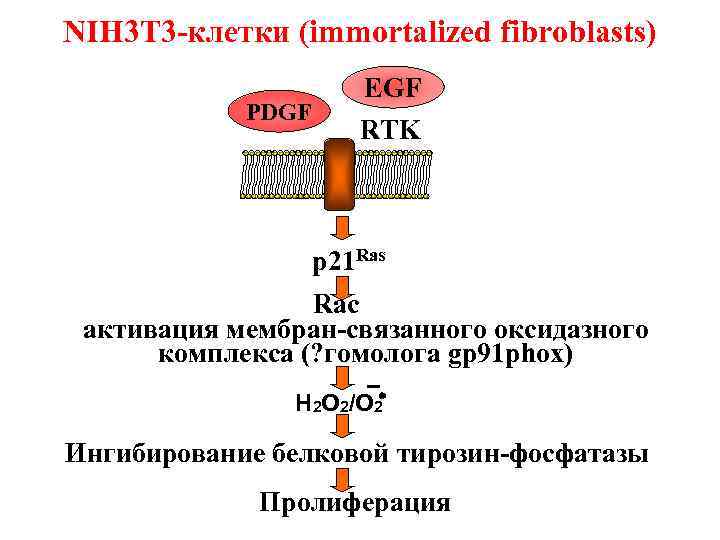
NIH 3 T 3 -клетки (immortalized fibroblasts) PDGF EGF RTK p 21 Ras Raс активация мембран-связанного оксидазного комплекса (? гомолога gp 91 phox) Н 2 О 2/O 2 Ингибирование белковой тирозин-фосфатазы Пролиферация
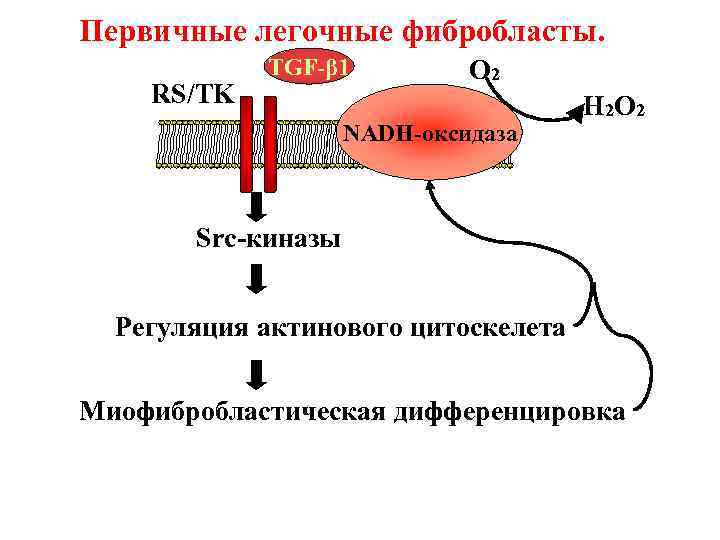
Первичные легочные фибробласты. RS/TK TGF-β 1 О 2 NADH-оксидаза Н 2 О 2 Src-киназы Регуляция актинового цитоскелета Миофибробластическая дифференцировка
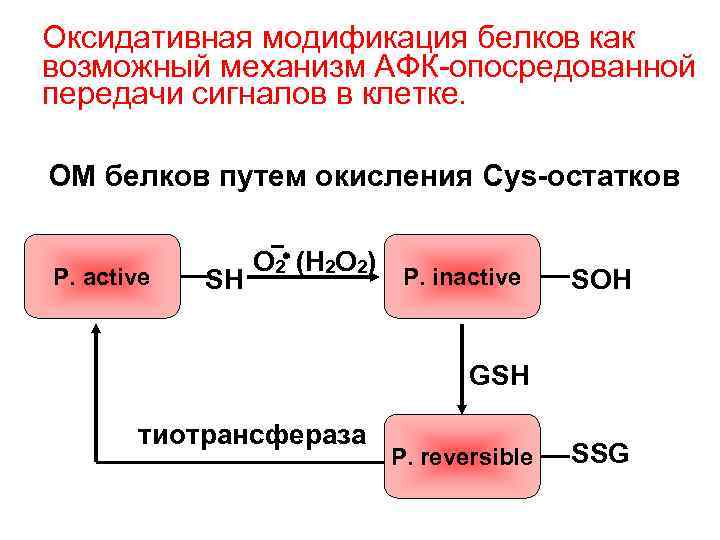
Оксидативная модификация белков как возможный механизм АФК-опосредованной передачи сигналов в клетке. ОМ белков путем окисления Cys-остатков P. active SH O 2 (H 2 O 2) P. inactive SOH GSH тиотрансфераза P. reversible SSG
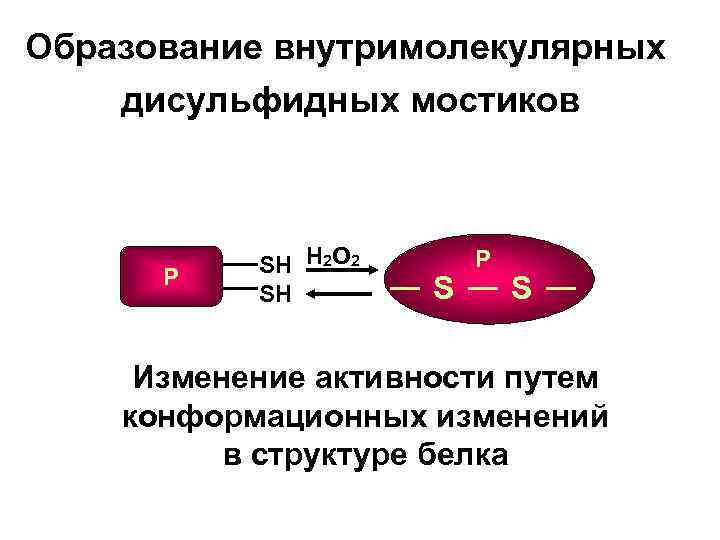
Образование внутримолекулярных дисульфидных мостиков Р SH H 2 O 2 SH S Р S Изменение активности путем конформационных изменений в структуре белка
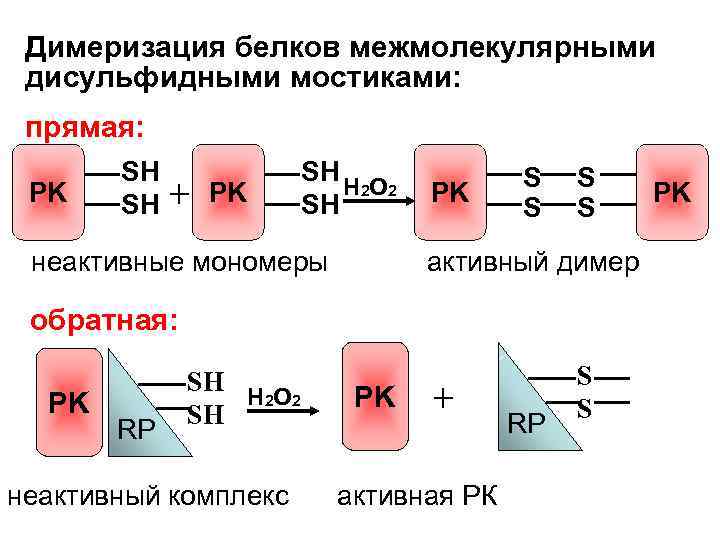
Димеризация белков межмолекулярными дисульфидными мостиками: прямая: PK SH SH + PK SH H 2 O 2 SH неактивные мономеры PK S S активный димер обратная: PK RP SH H 2 O 2 SH неактивный комплекс PK + активная РК RP S S PK
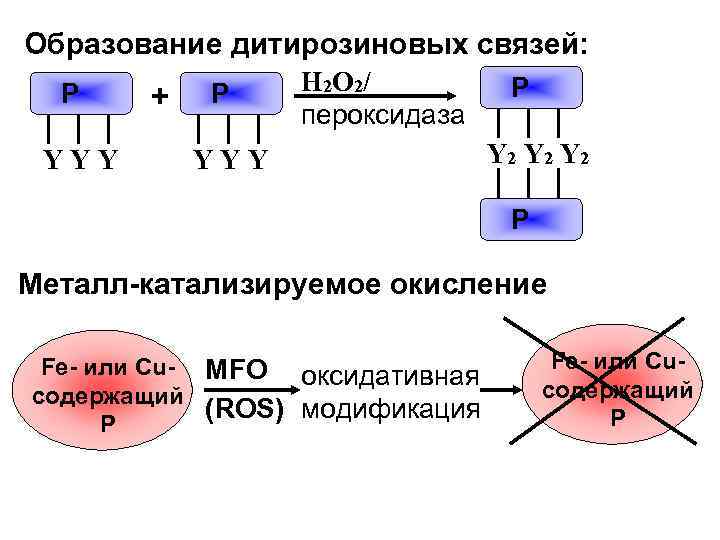
Образование дитирозиновых связей: Р YYY + Р H 2 O 2/ пероксидаза YYY Р Y 2 Y 2 Р Металл-катализируемое окисление Fe- или Cu- MFO оксидативная содержащий (ROS) модификация Р Fe- или Cuсодержащий Р

Методы изучения АФК Люцигенин - хемилюминесцентный субстрат для определения О 2 в клетке.
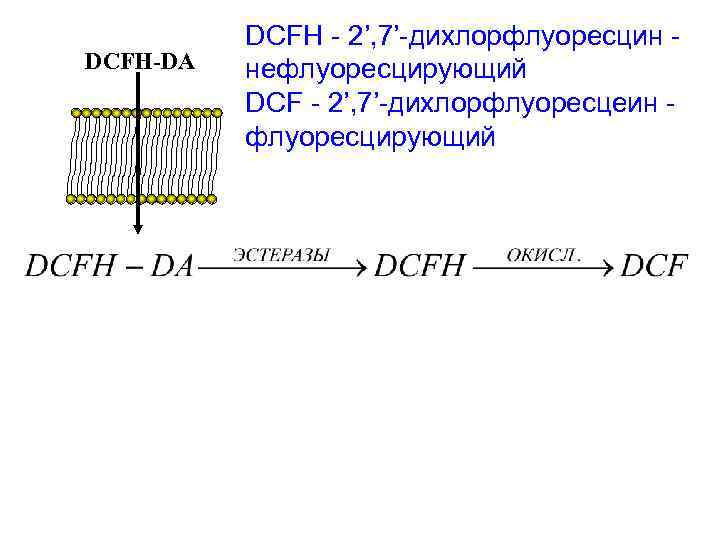
DCFH-DA DCFH - 2’, 7’-дихлорфлуоресцин нефлуоресцирующий DCF - 2’, 7’-дихлорфлуоресцеин флуоресцирующий

Флуориметрический метод, основанный на способности гем-пероксидаз катализировать Н 2 О 2 -зависимую димеризацию замещенных фенольных элементов. Высокая специфичность и чувствительность к Н 2 О 2. Наиболее часто используется пероксидаза хрена.
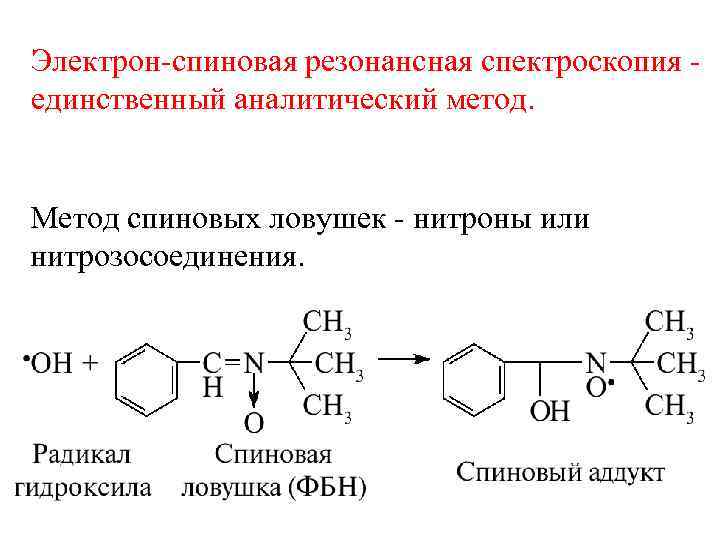
Электрон-спиновая резонансная спектроскопия единственный аналитический метод. Метод спиновых ловушек - нитроны или нитрозосоединения.

РЕЗЮМЕ: • АФК не только вредные побочные продукты клеточного метаболизма, но и важные регуляторы жизнедеятельности клетки. • Уровень АФК строго контролируется • Передача сигналов в клетке с помощью АФК осуществляется путем оксидативной модификаций с клеточными компонентами, такими как киназы, белки или ДНК.


Образование СО 1. Метаболизм гема 2. Перекисное окисление липидов 3. Метаболизм ксенобиотиков 86% 14%

Типы гем оксигеназ (НО): 1. НО-1 (индуцируемая) – защита клетки от оксидативного стресса • антиоксидантное действие • противовоспалительное действие • подавление апоптоза 2. НО-2 (конститутивная) – работает постоянно. Обнаружена в ЦНС и эндотелии сосудов. 3. НО-3 – активность сильно меньше, чем у НО-2
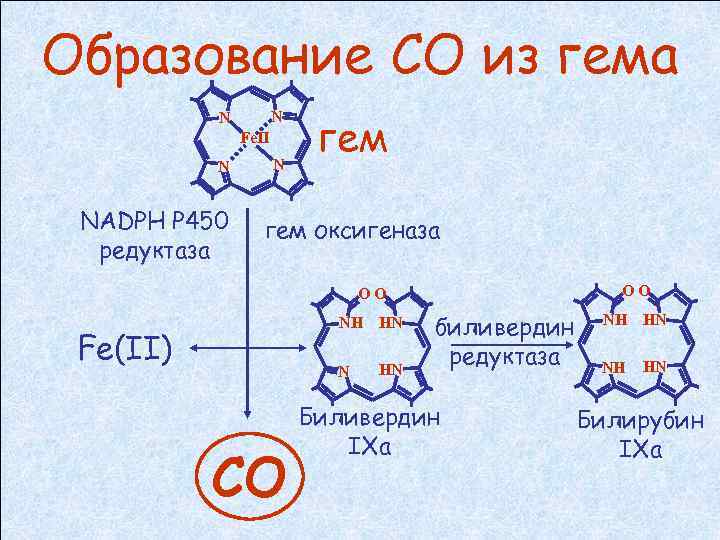
Образование СО из гема N N Fe. II N NADPH P 450 редуктаза N гем оксигеназа ОО ОО NН НN Fe(II) N CO НN биливердин редуктаза Биливердин IXa NН НN Билирубин IXa
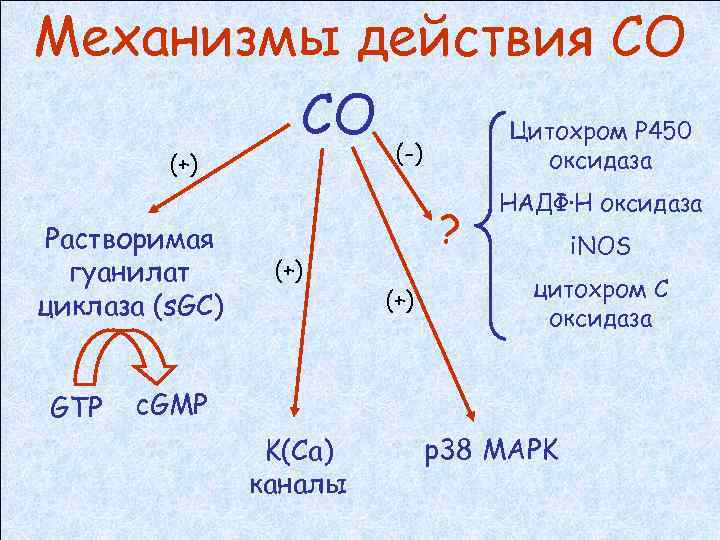
Механизмы действия СО СО Цитохром Р 450 (-) (+) Растворимая гуанилат циклаза (s. GC) GTР (+) оксидаза ? (+) НАДФ·Н оксидаза i. NOS цитохром С оксидаза c. GMP K(Ca) каналы p 38 MAPK

Физиологические функции СО, обеспеченные активацией s. GC: 1. Нейротрансмиссия 2. Расширение сосудов 3. Расслабление гладкой мускулатуры внутренних органов 4. Подавление агрегации тромбоцитов 5. Анти-пролиферативный эффект

с. GMP-независимые механизмы расслабления гладких мышц сосуда 1. Активация K(Ca) каналов (приводящая к гиперполяризации) 2. Цитохром Р 450 -зависимый механизм 3. Эндотелин-зависимый механизм ? проводимости К(Са) каналов стимулируется: концентрации Са внутри клетки мембранной деполяризаций
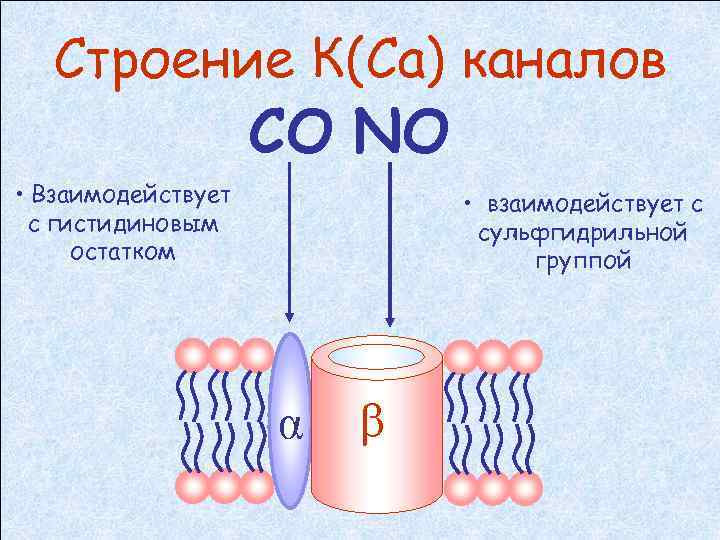
Строение К(Ca) каналов СО NO • Взаимодействует с гистидиновым остатком • взаимодействует с сульфгидрильной группой α β
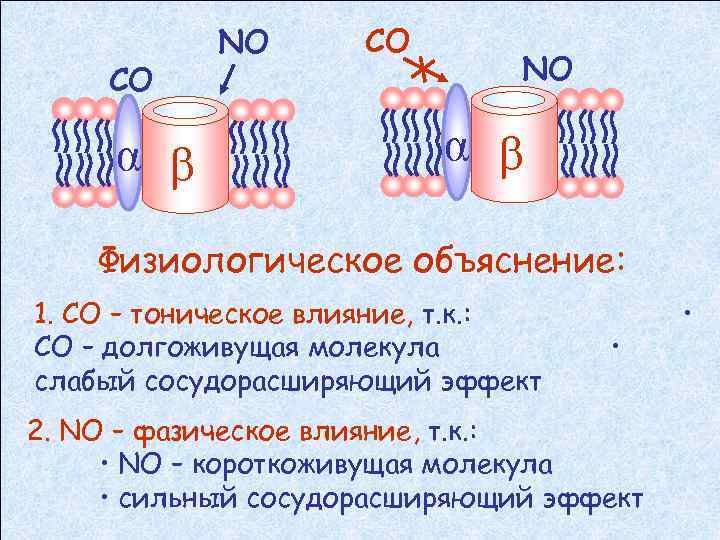
СО α β NO СО NO α β Физиологическое объяснение: 1. СО – тоническое влияние, т. к. : СО – долгоживущая молекула слабый сосудорасширяющий эффект • 2. NO – фазическое влияние, т. к. : • NO – короткоживущая молекула • сильный сосудорасширяющий эффект •

Влияние на пролиферацию 1, 2 СО 1. эндотелин 1 2. Выделяемого тромбоцитом ростового фактора β СО подавляет рост кровеносных сосудов

Регуляция кровяного давления 1. Ингибиторы НО (Zn. DBPG) кровеносного давление у крыс с гипертензией. 2. Лечение крыс с гипертензией индукторами НО-1 (Sn. Cl 2, гемин) показало • кровеносного давления • активности НО в почках 3. СО выделяемый в структурах ЦНС (NTS), обеспечивает механизм давления, связанный с подавлением активности барорецепторов.
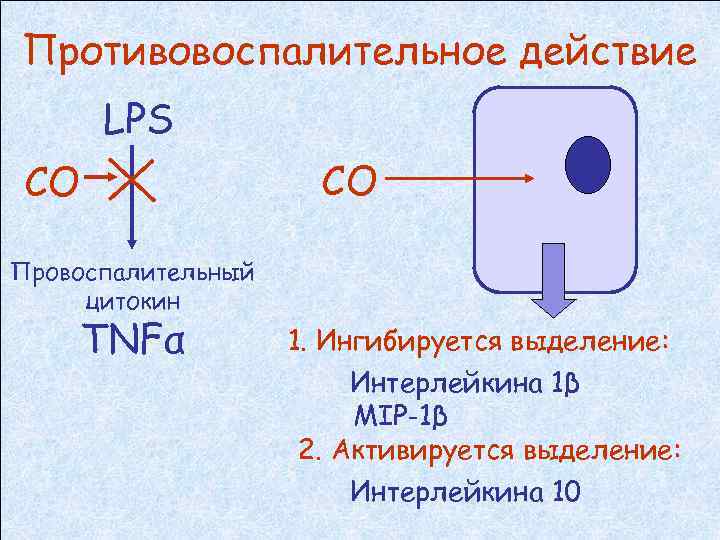
Противовоспалительное действие LPS CO CO Провоспалительный цитокин TNFα 1. Ингибируется выделение: Интерлейкина 1β MIP-1β 2. Активируется выделение: Интерлейкина 10

Функции СО: Резюме: 1. Сосудорасширяющая функция ССС НС 2. Подавление агрегации тромбоцитов 3. Подавление пролиферации 4. Регуляция кровяного давления 5. Нейротрансмиссия 6. Противовоспалительное действие 7. Подавление апоптоза 8. Расслабление гладкой мускулатуры внутренних органов 9. Участвует в почечной перфузии
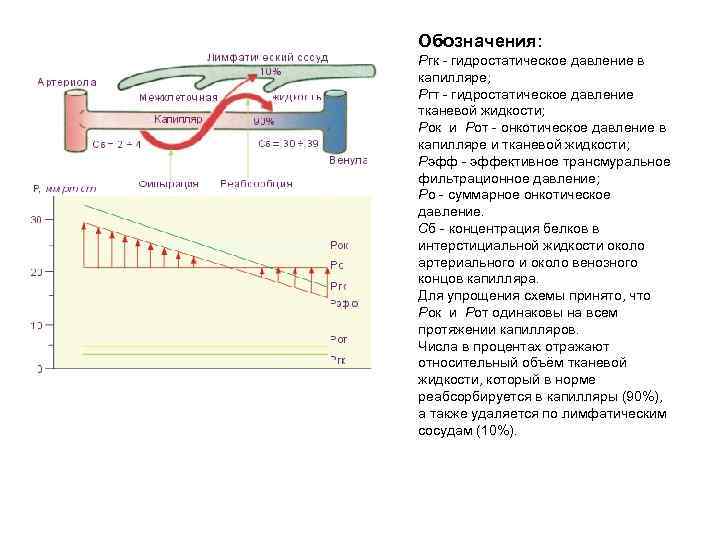
Обозначения: Pгк - гидростатическое давление в капилляре; Pгт - гидростатическое давление тканевой жидкости; Pок и Pот - онкотическое давление в капилляре и тканевой жидкости; Pэфф - эффективное трансмуральное фильтрационное давление; Pо - суммарное онкотическое давление. Сб - концентрация белков в интерстициальной жидкости около артериального и около венозного концов капилляра. Для упрощения схемы принято, что Pок и Pот одинаковы на всем протяжении капилляров. Числа в процентах отражают относительный объём тканевой жидкости, который в норме реабсорбируется в капилляры (90%), а также удаляется по лимфатическим сосудам (10%).
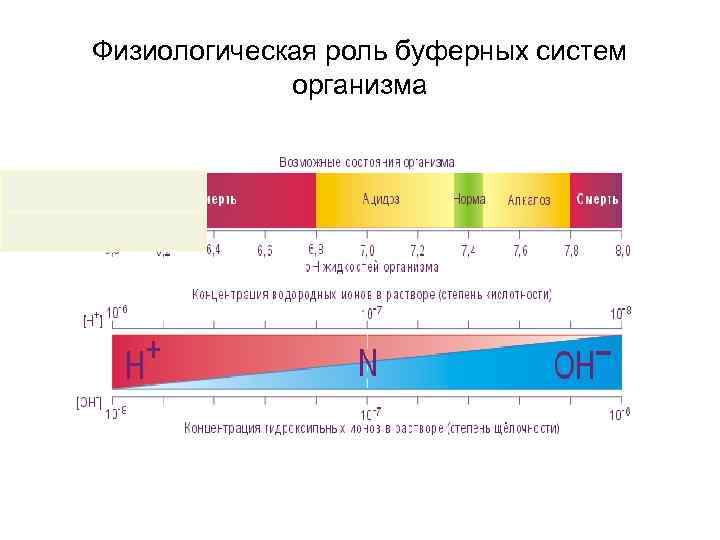
Физиологическая роль буферных систем организма
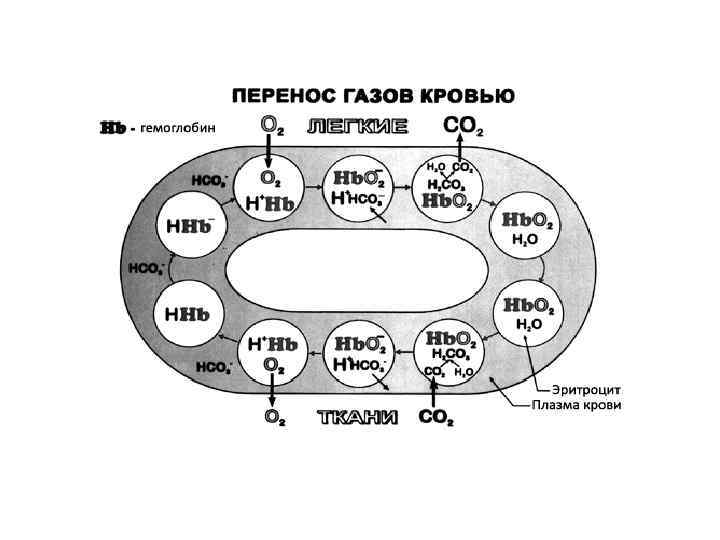
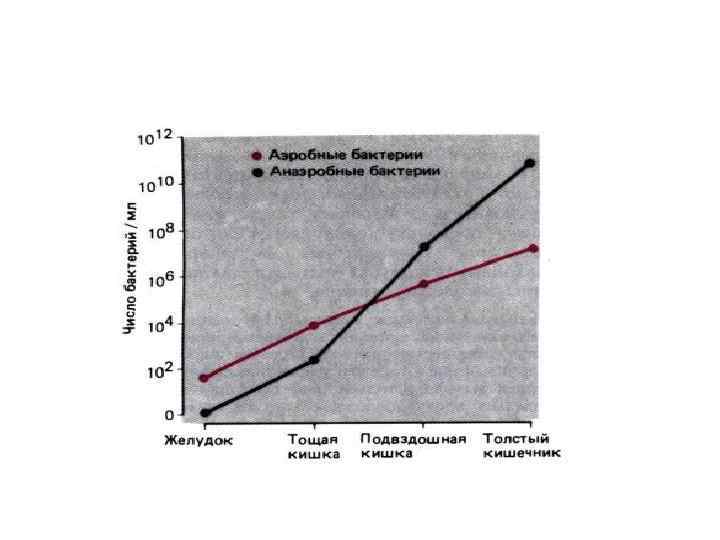
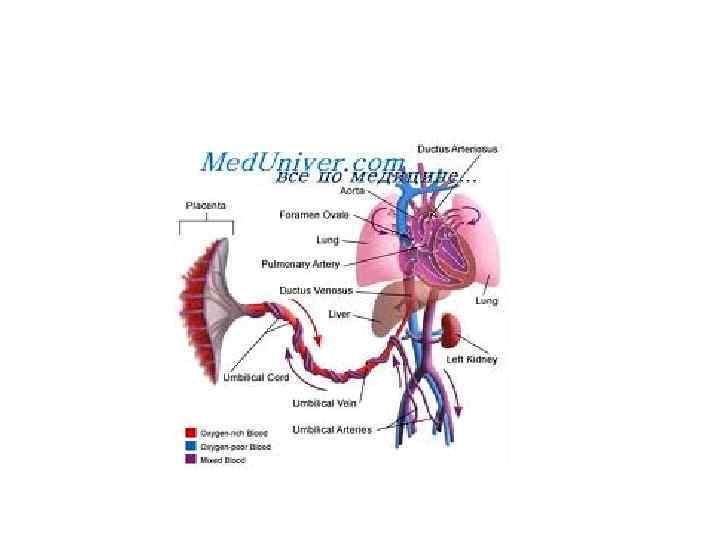
База схем и рисунков.физиология.ppt