Лекция 2 Основы химической кинетики.ppt
- Количество слайдов: 21

Балтийский федеральный университет им. И. Канта БИОФИЗИКА Лекция 3. Основы химической кинетики Жуков Валерий Валентинович, к. биол. н. доцент кафедры молекулярной физиологии и биофизики Калининград 2013

ХИМИЧЕСКАЯ КИНЕТИКА – изучение закономерностей протекания химической реакции во времени, её механизма и скорости.
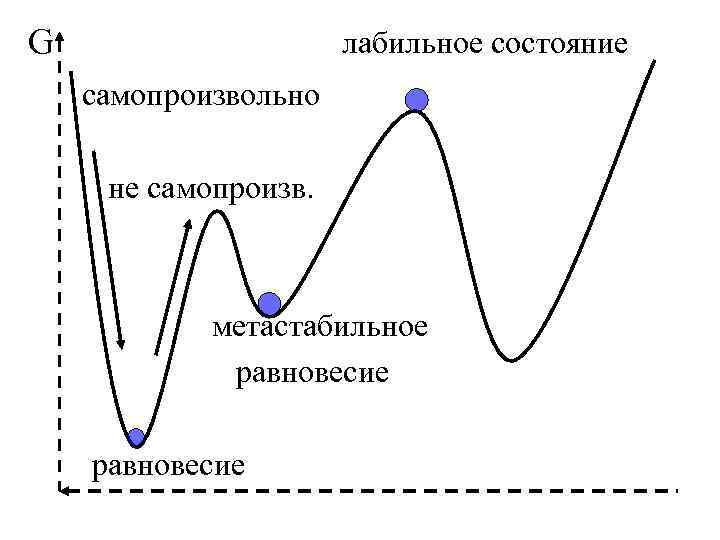
G лабильное состояние самопроизвольно не самопроизв. метастабильное равновесие
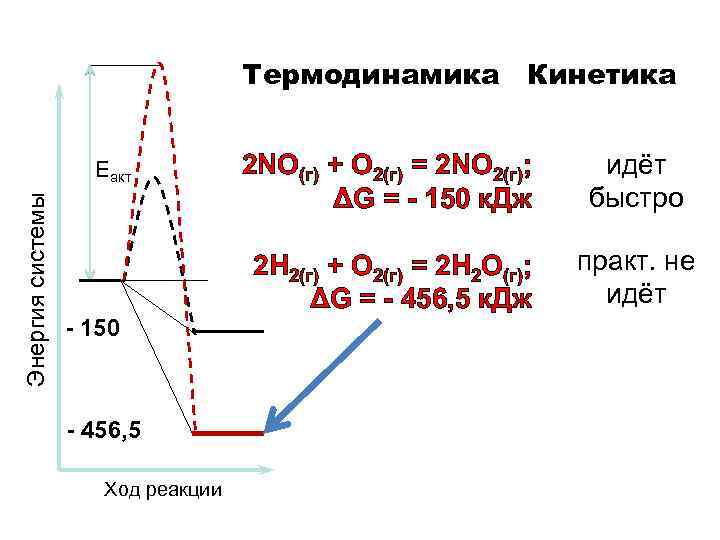
Термодинамика Кинетика Энергия системы Еакт - 150 - 456, 5 Ход реакции 2 NO(г) + О 2(г) = 2 NO 2(г); ΔG = - 150 к. Дж идёт быстро 2 Н 2(г) + О 2(г) = 2 Н 2 О(г); ΔG = - 456, 5 к. Дж практ. не идёт
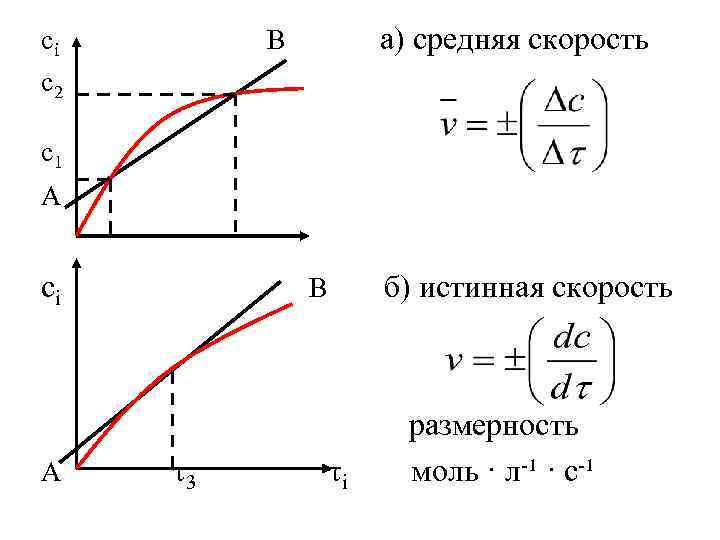
сi с2 а) средняя скорость В с1 А сi А б) истинная скорость В τ3 τi размерность моль · л-¹ · с-¹

Скорость реакции

2 А + В = А 2 В 1. А + В → АВ 2. АВ + А → А 2 В 2 А + В = А 2 В 1. если 1 < 2, то стадия 1 - лимитирующая р-ции = 1 = К 1·[A]·[В] 2. если 1 > 2, то стадия 2 - лимитирующая р-ции = 2 = К 2·[A]·[AВ] ~ K 3[A]p·[В]q ~ К 4·[A]p 3. если механизмзм простой (одна стадия), то р-ции = К·[A]2·[В]

1864 – 1867 гг. - К. Гульдберг, П. Вааге Закон действующих масс А + В = АВ R A +B

А=Х А+В+С=Х А + 2 В = Х К - константа скорости: К = v при Сi = 1

Молекулярность – число молекул, участвующих в элементарном акте химического взаимодействия Порядок – макрохарактеристика реакционной смеси Молекулярность – микрохарактеристика реакционной смеси
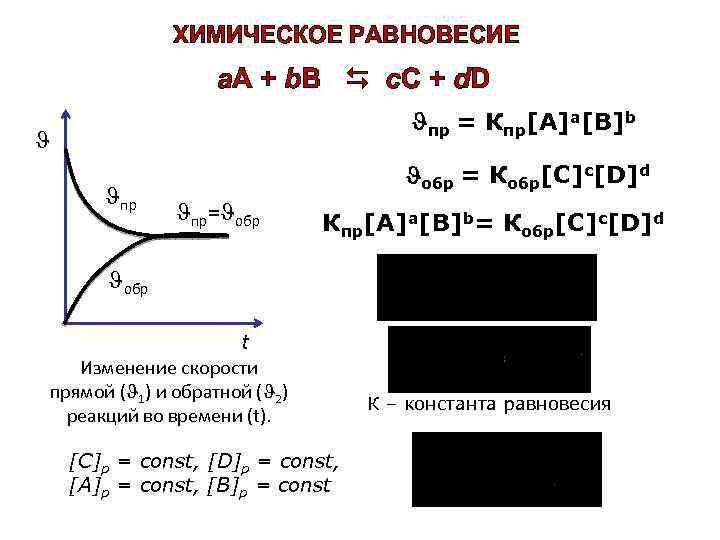
ХИМИЧЕСКОЕ РАВНОВЕСИЕ a. A + b. B c. C + d. D пр = Кпр[A]а[B]b пр обр = Кобр[C]c[D]d пр= обр Кпр[A]а[B]b= Кобр[C]c[D]d обр t Изменение скорости прямой ( 1) и обратной ( 2) реакций во времени (t). [C]p = const, [D]p = const, [A]p = const, [B]p = const К – константа равновесия

МОДЕЛЬ ХИМИЧЕСКОГО РАВНОВЕСИЯ
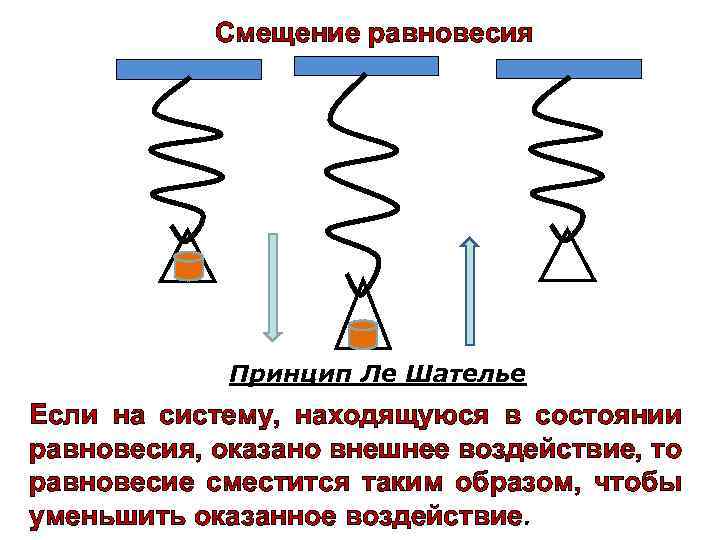
Смещение равновесия Принцип Ле Шателье Если на систему, находящуюся в состоянии равновесия, оказано внешнее воздействие, то равновесие сместится таким образом, чтобы уменьшить оказанное воздействие.
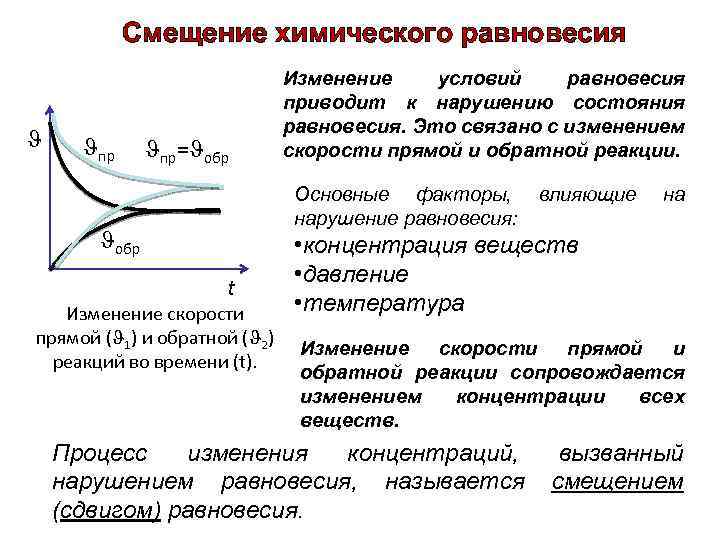
Смещение химического равновесия пр= обр Изменение условий равновесия приводит к нарушению состояния равновесия. Это связано с изменением скорости прямой и обратной реакции. Основные факторы, нарушение равновесия: обр t Изменение скорости прямой ( 1) и обратной ( 2) реакций во времени (t). влияющие на • концентрация веществ • давление • температура Изменение скорости прямой и обратной реакции сопровождается изменением концентрации всех веществ. Процесс изменения концентраций, нарушением равновесия, называется (сдвигом) равновесия. вызванный смещением

Правило Вант-Гофа где 2 и 1 – скорость реакции при температурах Т 2 и Т 1, соответственно; - температурный коэффициент реакции (значения от 2 до 4). Якоб Хендрик Вант-Гофф Jacobus Henricus (Henry) van 't Hoff 1852 — 1911 первый лауреат Нобелевской премии по химии (1901 год) «В знак признания огромной важности открытия законов химической динамики и осмотического давления в растворах» .
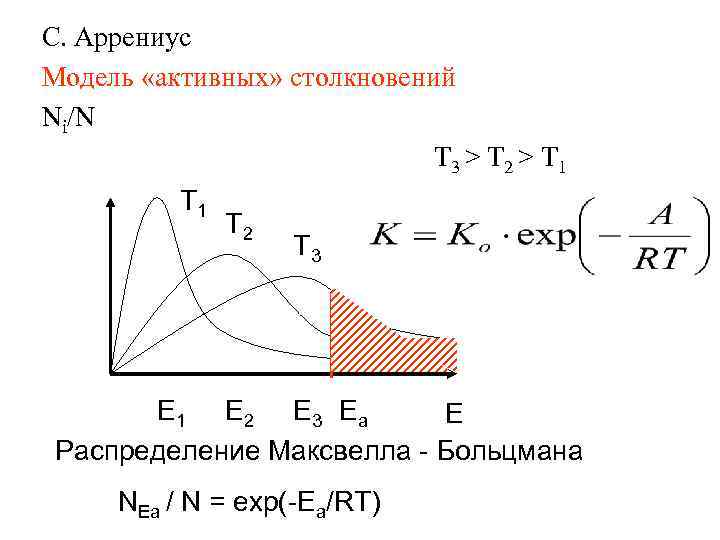
С. Аррениус Модель «активных» столкновений Ni/N T 3 > T 2 > T 1 T 2 T 3 E 1 E 2 E 3 Ea E Распределение Максвелла - Больцмана NEa / N = exp(-Ea/RT)

Сванте Август Аррениус Svante August Arrhenius 1859 — 1927 лауреат Нобелевской премии по химии(1903).
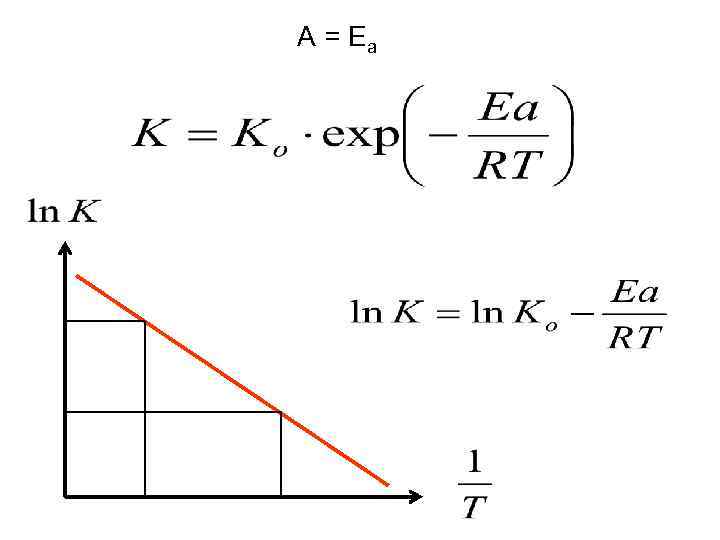
A = Ea
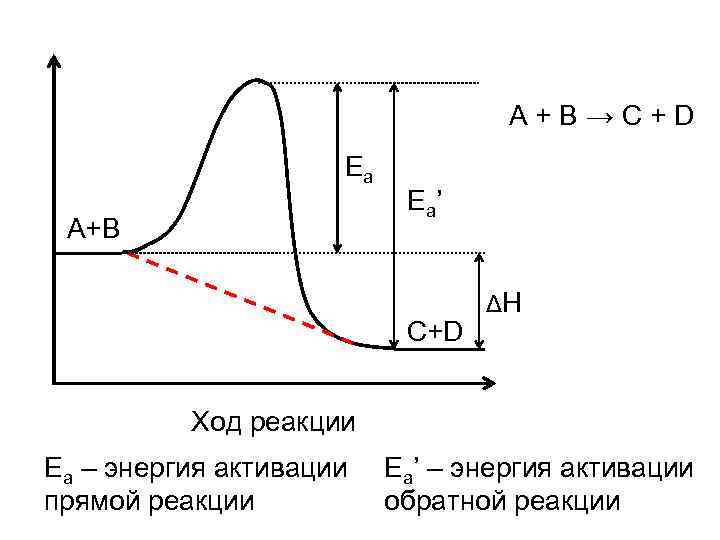
A+B→C+D Ea A+B E a’ C+D ΔH Ход реакции Ea – энергия активации прямой реакции Ea’ – энергия активации обратной реакции

уравнение Эйринга Ea = f(τ) ΔGa = ΔHa – TΔSa

Генри Эйринг Henry Eyring (1901 – 1981) Совместно с М. Поляни и М. Г. Эвансом разработал (1935) теорию абсолютных скоростей реакции, включающую метод переходного состояния. Ввёл в химию (1935) термин "активированный комплекс".
Лекция 2 Основы химической кинетики.ppt