Азотсодержащие соединения Амины 10 класс.ppt
- Количество слайдов: 53
 Азотсодержащие соединения Амины Вы растете и живете, Словно, плавая в …. ! Знайте, в воздухе у нас Это самый первый газ. Все живое – все цветы, Все деревья и кусты Все животные не могут Без аминокислоты! А в составе тех кислот Непременно есть …! 10 класс
Азотсодержащие соединения Амины Вы растете и живете, Словно, плавая в …. ! Знайте, в воздухе у нас Это самый первый газ. Все живое – все цветы, Все деревья и кусты Все животные не могут Без аминокислоты! А в составе тех кислот Непременно есть …! 10 класс
 Цели урока • Дать понятие об аминах, их классификации, изомерии и номенклатуре, свойствах в сравнении с аммиаком • Рассмотреть способы получения аминов и особенно анилина • Показать основные области применения аминов • Дать понятие об амидах и на их основе о синтетических полиамидных материалах
Цели урока • Дать понятие об аминах, их классификации, изомерии и номенклатуре, свойствах в сравнении с аммиаком • Рассмотреть способы получения аминов и особенно анилина • Показать основные области применения аминов • Дать понятие об амидах и на их основе о синтетических полиамидных материалах
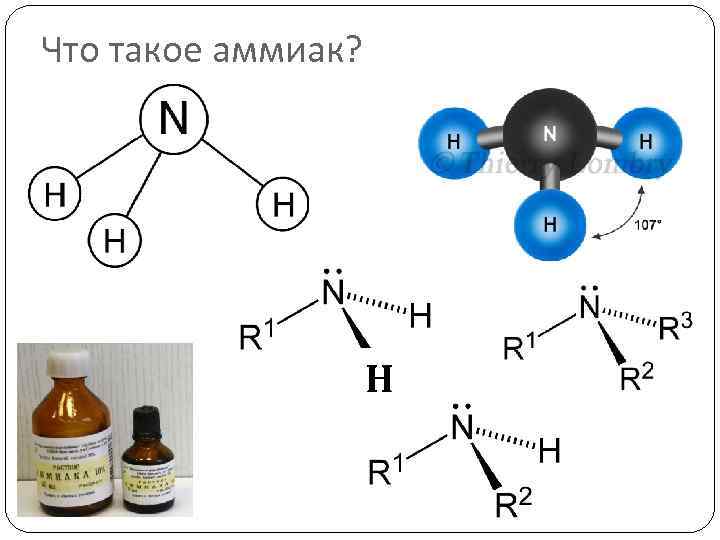 Что такое аммиак? Н
Что такое аммиак? Н
 Амины Производные аммиака (NH 3), в молекулах которого один или несколько атомов водорода замещены на углеводородные группы NH 2 – CH 3 -NH-CH 3 -N-CH 3 метиламин диметиламин триметиламин аминометан NH 2 -группа аминогруппа
Амины Производные аммиака (NH 3), в молекулах которого один или несколько атомов водорода замещены на углеводородные группы NH 2 – CH 3 -NH-CH 3 -N-CH 3 метиламин диметиламин триметиламин аминометан NH 2 -группа аминогруппа
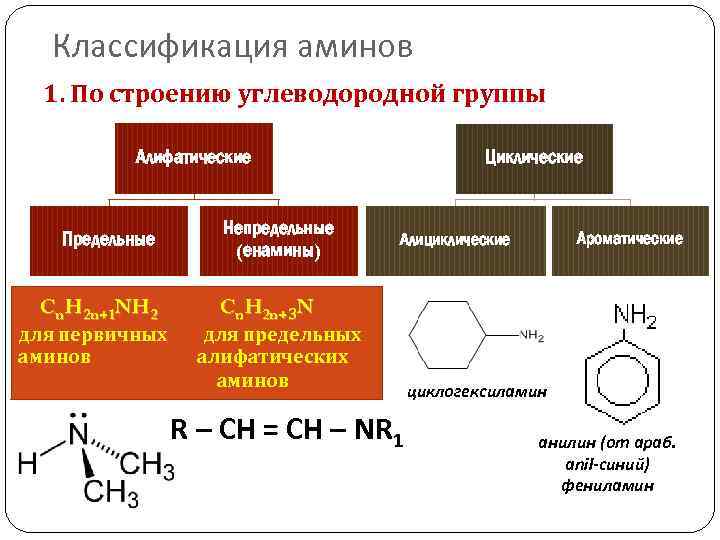 Классификация аминов 1. По строению углеводородной группы Алифатические Предельные Непредельные (енамины) Циклические Ароматические Алициклические Cn. H 2 n+1 NH 2 Cn. H 2 n+3 N для первичных для предельных аминов алифатических аминов R – CH = CH – NR 1 циклогексиламин анилин (от араб. аnil-синий) фениламин
Классификация аминов 1. По строению углеводородной группы Алифатические Предельные Непредельные (енамины) Циклические Ароматические Алициклические Cn. H 2 n+1 NH 2 Cn. H 2 n+3 N для первичных для предельных аминов алифатических аминов R – CH = CH – NR 1 циклогексиламин анилин (от араб. аnil-синий) фениламин
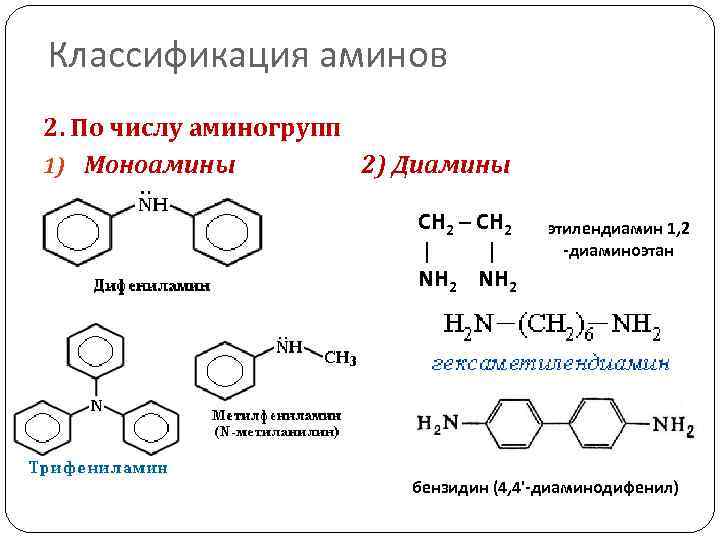 Классификация аминов 2. По числу аминогрупп 1) Моноамины 2) Диамины СН 2 – СН 2 | | NH 2 этилендиамин 1, 2 -диаминоэтан бензидин (4, 4'-диаминодифенил)
Классификация аминов 2. По числу аминогрупп 1) Моноамины 2) Диамины СН 2 – СН 2 | | NH 2 этилендиамин 1, 2 -диаминоэтан бензидин (4, 4'-диаминодифенил)
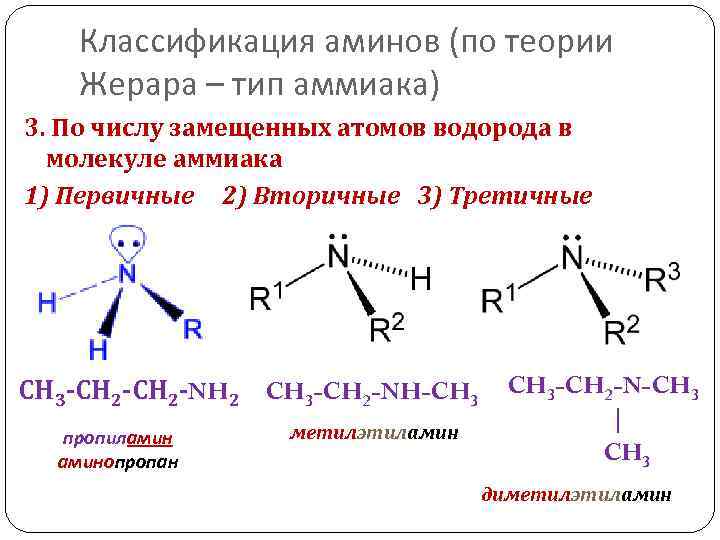 Классификация аминов (по теории Жерара – тип аммиака) 3. По числу замещенных атомов водорода в молекуле аммиака 1) Первичные 2) Вторичные 3) Третичные СН 3 -СН 2 -NH 2 CH 3 -CH 2 -NH-CH 3 пропиламинопропан метилэтиламин CH 3 -CH 2 -N-CH 3 | CH 3 диметилэтиламин
Классификация аминов (по теории Жерара – тип аммиака) 3. По числу замещенных атомов водорода в молекуле аммиака 1) Первичные 2) Вторичные 3) Третичные СН 3 -СН 2 -NH 2 CH 3 -CH 2 -NH-CH 3 пропиламинопропан метилэтиламин CH 3 -CH 2 -N-CH 3 | CH 3 диметилэтиламин
 Электронное и пространственное строение аминов Каково положение азота в ПС? Каков заряд ядра атома азота? Сколько энергетических уровней у атома азота? Сколько электронов имеет атом этого элемента на каждом уровне? Составьте электронную формулу атома азота
Электронное и пространственное строение аминов Каково положение азота в ПС? Каков заряд ядра атома азота? Сколько энергетических уровней у атома азота? Сколько электронов имеет атом этого элемента на каждом уровне? Составьте электронную формулу атома азота
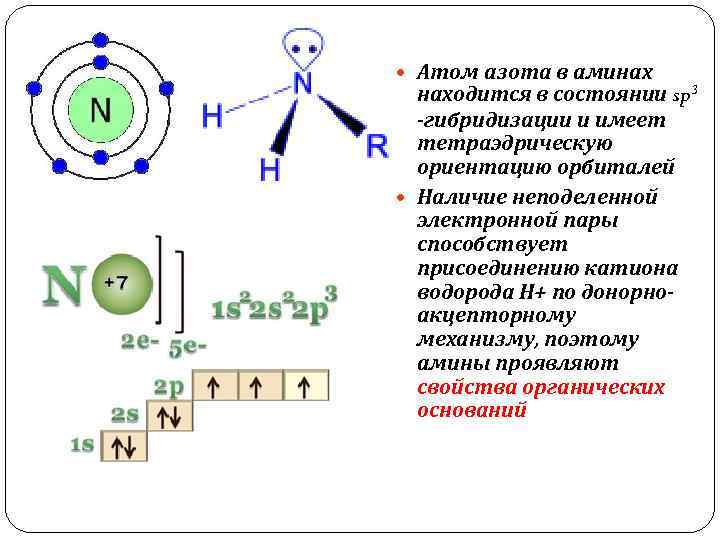 Атом азота в аминах находится в состоянии sp 3 -гибридизации и имеет тетраэдрическую ориентацию орбиталей Наличие неподеленной электронной пары способствует присоединению катиона водорода Н+ по донорноакцепторному механизму, поэтому амины проявляют свойства органических оснований
Атом азота в аминах находится в состоянии sp 3 -гибридизации и имеет тетраэдрическую ориентацию орбиталей Наличие неподеленной электронной пары способствует присоединению катиона водорода Н+ по донорноакцепторному механизму, поэтому амины проявляют свойства органических оснований
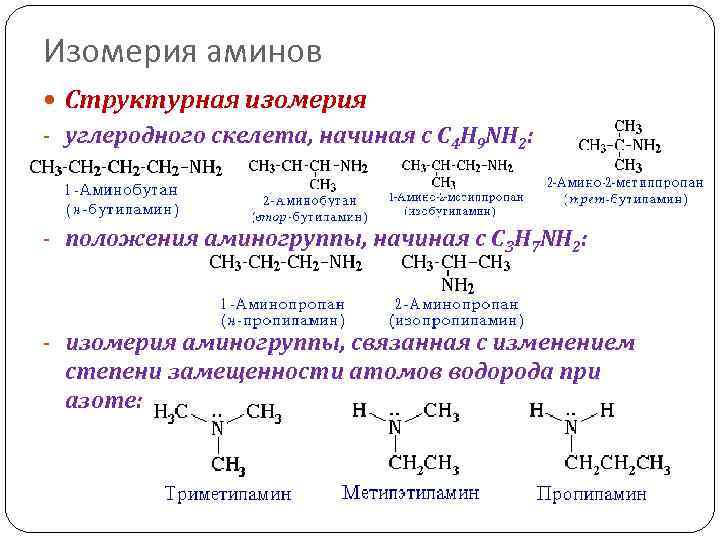 Изомерия аминов Структурная изомерия - углеродного скелета, начиная с С 4 H 9 NH 2: - положения аминогруппы, начиная с С 3 H 7 NH 2: - изомерия аминогруппы, связанная с изменением степени замещенности атомов водорода при азоте:
Изомерия аминов Структурная изомерия - углеродного скелета, начиная с С 4 H 9 NH 2: - положения аминогруппы, начиная с С 3 H 7 NH 2: - изомерия аминогруппы, связанная с изменением степени замещенности атомов водорода при азоте:
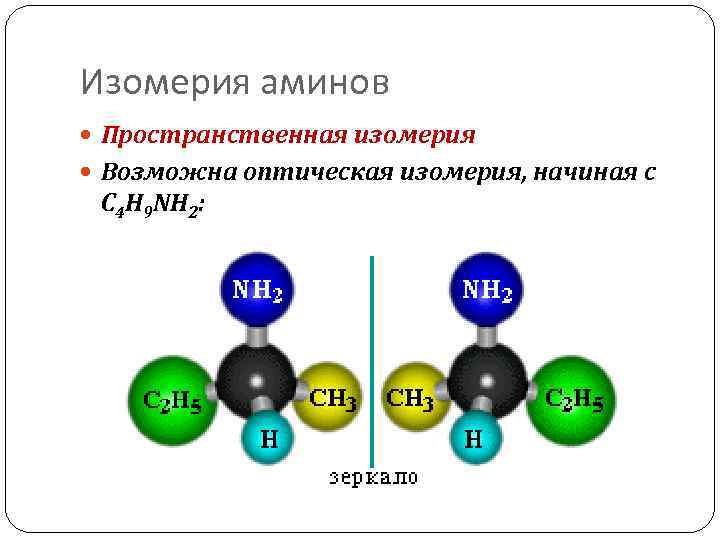 Изомерия аминов Пространственная изомерия Возможна оптическая изомерия, начиная с С 4 H 9 NH 2:
Изомерия аминов Пространственная изомерия Возможна оптическая изомерия, начиная с С 4 H 9 NH 2:
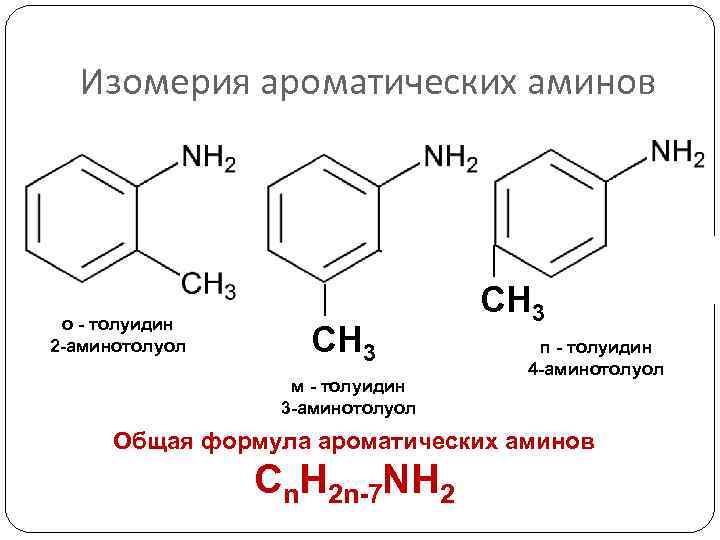 Изомерия ароматических аминов о - толуидин 2 -аминотолуол | СН 3 м - толуидин 3 -аминотолуол | СН 3 п - толуидин 4 -аминотолуол Общая формула ароматических аминов Сn. H 2 n-7 NH 2
Изомерия ароматических аминов о - толуидин 2 -аминотолуол | СН 3 м - толуидин 3 -аминотолуол | СН 3 п - толуидин 4 -аминотолуол Общая формула ароматических аминов Сn. H 2 n-7 NH 2
 Получение аминов 1. Общий метод – восстановление нитросоединений Анилин образуется при восстановлении нитробензола (восстановители - водород в присутствии металлических катализаторов, Fe + HCl, сульфиды): С 6 Н 5 NO 2 + 3 (NH 4)2 S → С 6 Н 5 NH 2 + 2 H 2 O + 3 S↓ + 6 NH 3↑ Реакция Н. Н. Зинина, 1842 г.
Получение аминов 1. Общий метод – восстановление нитросоединений Анилин образуется при восстановлении нитробензола (восстановители - водород в присутствии металлических катализаторов, Fe + HCl, сульфиды): С 6 Н 5 NO 2 + 3 (NH 4)2 S → С 6 Н 5 NH 2 + 2 H 2 O + 3 S↓ + 6 NH 3↑ Реакция Н. Н. Зинина, 1842 г.
 ЗИНИН Николай Николаевич (25. VIII. 1812 - 18. II. 1880) Русский химик-органик, акад. Петербургской Академии Наук (с 1865 г. ). Родился в Шуше (Азербайджан). Окончил Казанский университет (1833). Работал там же, с 1837 г. - в лабораториях и на заводах в Германии, Франции, Англии. В 1841 -1848 профессор Казанского университета, в 1848 -1874 - Медико-хирургической академии в Петербурге. Один из организаторов Русского химического общества и первый его президент (1868 -1877). Научные исследования посвящены органической химии. Открыл (1842) реакцию восстановления ароматических нитросоединений, послужившую основой отрасли химической промышленности - анилино-красочной. Разработал (1841) один из универсальных способов получения ароматических кетонов (бензоиновая конденсация). Показал, что амины - основания, способные образовывать соли с различными кислотами. Впервые синтезировал большое число новых соединений различных классов (аллиловый спирт, аллиловый эфир изотиоциановой кислоты - "летучее горчичное масло", ди- и тетрахлорбензолы, толан, стильбен и др. ). Открыл "бензидиновую перегруппировку" (1845), уреиды (1854) и др. Совместно с А. А. Воскресенским является основателем большой школы русских химиков. В числе его учеников были А. М. Бутлеров, Н. Н. Бекетов, А. П. Бородин и др.
ЗИНИН Николай Николаевич (25. VIII. 1812 - 18. II. 1880) Русский химик-органик, акад. Петербургской Академии Наук (с 1865 г. ). Родился в Шуше (Азербайджан). Окончил Казанский университет (1833). Работал там же, с 1837 г. - в лабораториях и на заводах в Германии, Франции, Англии. В 1841 -1848 профессор Казанского университета, в 1848 -1874 - Медико-хирургической академии в Петербурге. Один из организаторов Русского химического общества и первый его президент (1868 -1877). Научные исследования посвящены органической химии. Открыл (1842) реакцию восстановления ароматических нитросоединений, послужившую основой отрасли химической промышленности - анилино-красочной. Разработал (1841) один из универсальных способов получения ароматических кетонов (бензоиновая конденсация). Показал, что амины - основания, способные образовывать соли с различными кислотами. Впервые синтезировал большое число новых соединений различных классов (аллиловый спирт, аллиловый эфир изотиоциановой кислоты - "летучее горчичное масло", ди- и тетрахлорбензолы, толан, стильбен и др. ). Открыл "бензидиновую перегруппировку" (1845), уреиды (1854) и др. Совместно с А. А. Воскресенским является основателем большой школы русских химиков. В числе его учеников были А. М. Бутлеров, Н. Н. Бекетов, А. П. Бородин и др.
 Вклад И. Н. Зинина в развитие химии «Если бы Зинин не сделал ничего более, кроме превращения нитробензола в анилин, то имя его и тогда осталось бы записанным золотыми буквами в историю химии» (Август Вильгельм Гофман)
Вклад И. Н. Зинина в развитие химии «Если бы Зинин не сделал ничего более, кроме превращения нитробензола в анилин, то имя его и тогда осталось бы записанным золотыми буквами в историю химии» (Август Вильгельм Гофман)
 2. Восстановление амидов (восстановитель - алюмогидрид лития Li. Al. H 4): CH 3 – CONH 2 + KOH → CH 3 -NH 2 + K 2 CO 3 + H 2 O уменьшение углеродной цепи
2. Восстановление амидов (восстановитель - алюмогидрид лития Li. Al. H 4): CH 3 – CONH 2 + KOH → CH 3 -NH 2 + K 2 CO 3 + H 2 O уменьшение углеродной цепи
![Получение аминов 3. Восстановление нитрилов с образованием первичных аминов: R-C≡N + 4[H] → R-CH Получение аминов 3. Восстановление нитрилов с образованием первичных аминов: R-C≡N + 4[H] → R-CH](https://present5.com/presentation/31501208_181896356/image-17.jpg) Получение аминов 3. Восстановление нитрилов с образованием первичных аминов: R-C≡N + 4[H] → R-CH 2 NH 2 Ni или Na cпирт. р-р С 2 Н 5 -С ≡ N + 2 H 2 → С 2 Н 5 – СН 2 – NH 2 Этим способом в промышленности получают гексаметилендиамин, который используется в производстве полиамидного волокна найлон.
Получение аминов 3. Восстановление нитрилов с образованием первичных аминов: R-C≡N + 4[H] → R-CH 2 NH 2 Ni или Na cпирт. р-р С 2 Н 5 -С ≡ N + 2 H 2 → С 2 Н 5 – СН 2 – NH 2 Этим способом в промышленности получают гексаметилендиамин, который используется в производстве полиамидного волокна найлон.
 4. Получение аминов путём введения алкильных групп в молекулы аммиака и аминов (реакции алкилирования) При нагревании галогеналканов с аммиаком образуется смесь первичных, вторичных и третичных аминов. • В основе этих превращений лежит реакция нуклеофильного замещения галогена в галогеналканах. • Роль нуклеофила играют молекулы аммиака и аминов, имеющие неподеленную пару электронов на атоме азота.
4. Получение аминов путём введения алкильных групп в молекулы аммиака и аминов (реакции алкилирования) При нагревании галогеналканов с аммиаком образуется смесь первичных, вторичных и третичных аминов. • В основе этих превращений лежит реакция нуклеофильного замещения галогена в галогеналканах. • Роль нуклеофила играют молекулы аммиака и аминов, имеющие неподеленную пару электронов на атоме азота.
 Получение аминов В промышленности алкилирование аммиака в большинстве случаев проводится не галогеналканами, а спиртами, в молекулах которых происходит нуклеофильное замещение ОНгруппы на аминогруппу. Действием галогеналканов на первичные алифатические и ароматические амины получают вторичные и третичные амины, в том числе, смешанные.
Получение аминов В промышленности алкилирование аммиака в большинстве случаев проводится не галогеналканами, а спиртами, в молекулах которых происходит нуклеофильное замещение ОНгруппы на аминогруппу. Действием галогеналканов на первичные алифатические и ароматические амины получают вторичные и третичные амины, в том числе, смешанные.
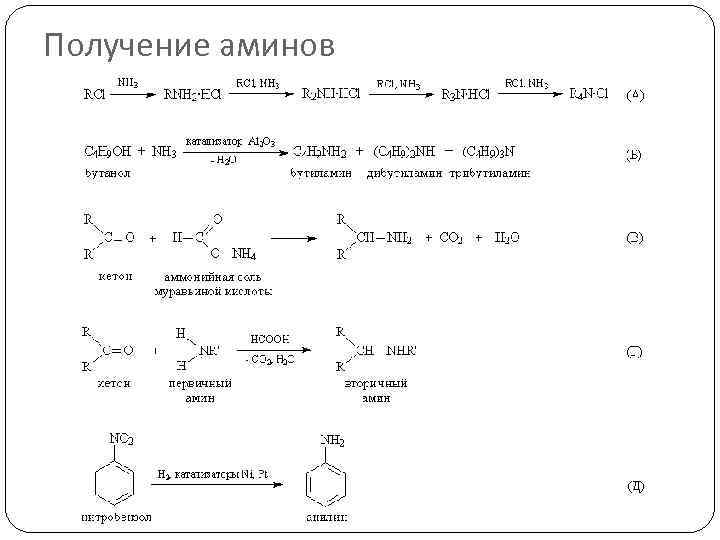 Получение аминов
Получение аминов
 Физические свойства аминов Первые представители – метиламин CH 3 NH 2, диметиламин (CH 3)2 NH, триметиламин (CH 3)3 N и этиламин C 2 H 5 NH 2 – при комнатной температуре газообразные С 3 – С 9 – жидкости С 10 и более – кристаллические вещества Растворимость аминов в воде убывает по мере увеличения длины цепи R и при возрастании числа органических групп, связанных с азотом (переход к вторичным и третичным аминам). C 1 -C 4 – (р) неограниченно, высшие (н) Запах аминов напоминает запах аммиака, высшие (с большими R) амины практически лишены запаха. Могут образовывать межмолекулярные водородные связи Анилин – яд, бесцветная маслянистая (ж) со слабым бензинным запахом, быстро окисляется на воздухе, переходя в темную желто -коричневую окраску Соли анилина хорошо растворимы в воде (в отличие от самого анилина)
Физические свойства аминов Первые представители – метиламин CH 3 NH 2, диметиламин (CH 3)2 NH, триметиламин (CH 3)3 N и этиламин C 2 H 5 NH 2 – при комнатной температуре газообразные С 3 – С 9 – жидкости С 10 и более – кристаллические вещества Растворимость аминов в воде убывает по мере увеличения длины цепи R и при возрастании числа органических групп, связанных с азотом (переход к вторичным и третичным аминам). C 1 -C 4 – (р) неограниченно, высшие (н) Запах аминов напоминает запах аммиака, высшие (с большими R) амины практически лишены запаха. Могут образовывать межмолекулярные водородные связи Анилин – яд, бесцветная маслянистая (ж) со слабым бензинным запахом, быстро окисляется на воздухе, переходя в темную желто -коричневую окраску Соли анилина хорошо растворимы в воде (в отличие от самого анилина)
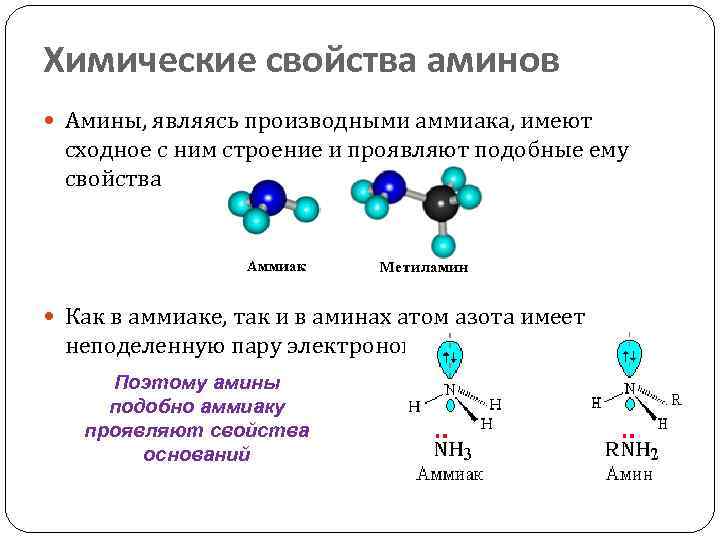 Химические свойства аминов Амины, являясь производными аммиака, имеют сходное с ним строение и проявляют подобные ему свойства Как в аммиаке, так и в аминах атом азота имеет неподеленную пару электронов: Поэтому амины подобно аммиаку проявляют свойства оснований
Химические свойства аминов Амины, являясь производными аммиака, имеют сходное с ним строение и проявляют подобные ему свойства Как в аммиаке, так и в аминах атом азота имеет неподеленную пару электронов: Поэтому амины подобно аммиаку проявляют свойства оснований
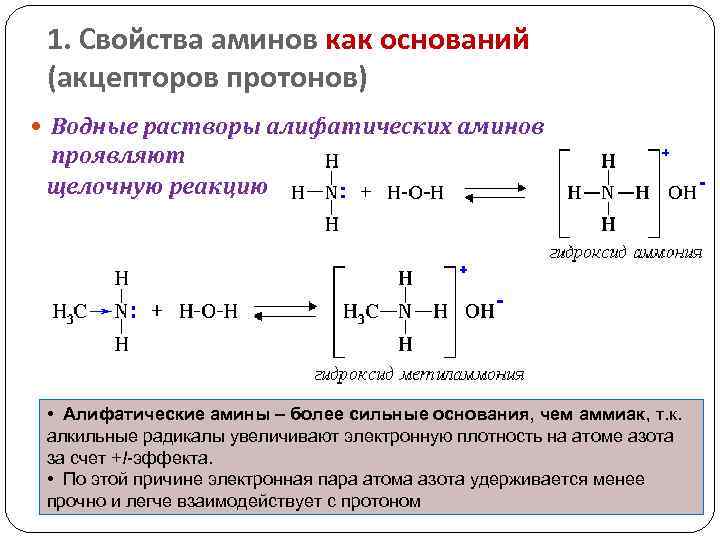 1. Свойства аминов как оснований (акцепторов протонов) Водные растворы алифатических аминов проявляют щелочную реакцию • Алифатические амины – более сильные основания, чем аммиак, т. к. алкильные радикалы увеличивают электронную плотность на атоме азота за счет +I-эффекта. • По этой причине электронная пара атома азота удерживается менее прочно и легче взаимодействует с протоном
1. Свойства аминов как оснований (акцепторов протонов) Водные растворы алифатических аминов проявляют щелочную реакцию • Алифатические амины – более сильные основания, чем аммиак, т. к. алкильные радикалы увеличивают электронную плотность на атоме азота за счет +I-эффекта. • По этой причине электронная пара атома азота удерживается менее прочно и легче взаимодействует с протоном
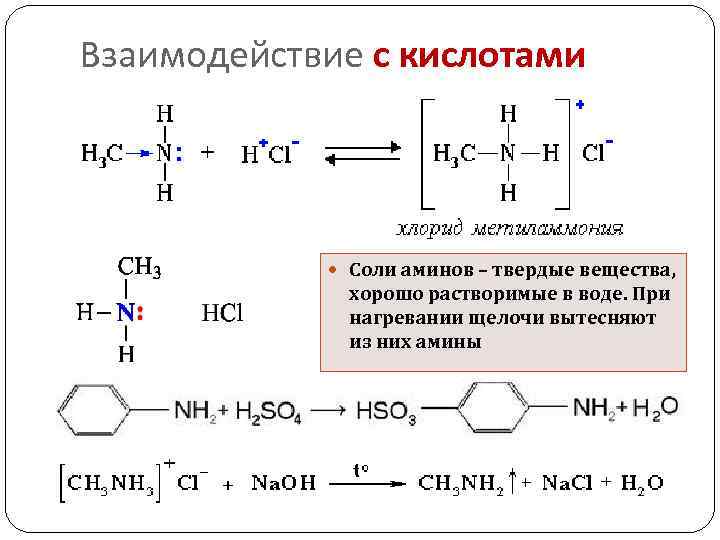 Взаимодействие с кислотами Соли аминов – твердые вещества, хорошо растворимые в воде. При нагревании щелочи вытесняют из них амины
Взаимодействие с кислотами Соли аминов – твердые вещества, хорошо растворимые в воде. При нагревании щелочи вытесняют из них амины
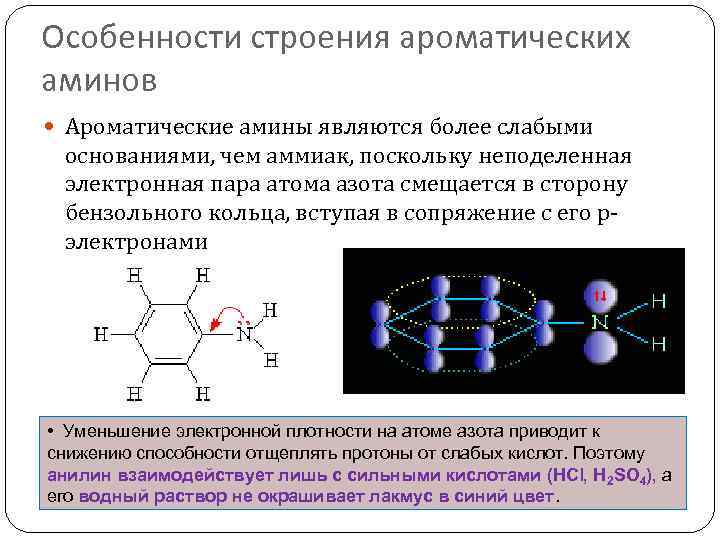 Особенности строения ароматических аминов Ароматические амины являются более слабыми основаниями, чем аммиак, поскольку неподеленная электронная пара атома азота смещается в сторону бензольного кольца, вступая в сопряжение с его pэлектронами • Уменьшение электронной плотности на атоме азота приводит к снижению способности отщеплять протоны от слабых кислот. Поэтому анилин взаимодействует лишь с сильными кислотами (HCl, H 2 SO 4), а его водный раствор не окрашивает лакмус в синий цвет.
Особенности строения ароматических аминов Ароматические амины являются более слабыми основаниями, чем аммиак, поскольку неподеленная электронная пара атома азота смещается в сторону бензольного кольца, вступая в сопряжение с его pэлектронами • Уменьшение электронной плотности на атоме азота приводит к снижению способности отщеплять протоны от слабых кислот. Поэтому анилин взаимодействует лишь с сильными кислотами (HCl, H 2 SO 4), а его водный раствор не окрашивает лакмус в синий цвет.
 Взаимное влияние групп в анилине NH 2 -группа на бензольное кольцо - Увеличение подвижности атомов водорода бензольного кольца в орто- и пара-положениях, облегчение протекания реакций замещения в молекуле анилина Бензольное кольцо на NH 2 -группу - Ослабление основных свойств анилина в сравнении с аммиаком и алифатическими аминами
Взаимное влияние групп в анилине NH 2 -группа на бензольное кольцо - Увеличение подвижности атомов водорода бензольного кольца в орто- и пара-положениях, облегчение протекания реакций замещения в молекуле анилина Бензольное кольцо на NH 2 -группу - Ослабление основных свойств анилина в сравнении с аммиаком и алифатическими аминами
 Как изменяются основные свойства у аммиака и аминов? C 6 H 5 NH 2 < NH 3 < RNH 2 < R 2 NH < R 3 N (в газовой фазе) Увеличение основных свойств
Как изменяются основные свойства у аммиака и аминов? C 6 H 5 NH 2 < NH 3 < RNH 2 < R 2 NH < R 3 N (в газовой фазе) Увеличение основных свойств
 2. Окисление аминов Амины, особенно ароматические, легко окисляются на воздухе. В отличие от аммиака, они способны воспламеняться от открытого пламени 4 СH 3 NH 2 + 9 O 2 → 4 CO 2 + 10 H 2 O + 2 N 2
2. Окисление аминов Амины, особенно ароматические, легко окисляются на воздухе. В отличие от аммиака, они способны воспламеняться от открытого пламени 4 СH 3 NH 2 + 9 O 2 → 4 CO 2 + 10 H 2 O + 2 N 2
 3. Взаимодействие с азотистой кислотой Азотистая кислота HNO 2 – неустойчивое соединение. Поэтому она используется только в момент выделения. Образуется HNO 2, как все слабые кислоты, действием на ее соль (нитрит) сильной кислотой: KNO 2 + HCl = НNO 2 + KCl NO 2 - + H+ = НNO 2 (сокращенное ионное уравнение) Строение продуктов реакции с азотистой кислотой зависит от характера амина. Поэтому данная реакция используется для различения первичных, вторичных и третичных аминов.
3. Взаимодействие с азотистой кислотой Азотистая кислота HNO 2 – неустойчивое соединение. Поэтому она используется только в момент выделения. Образуется HNO 2, как все слабые кислоты, действием на ее соль (нитрит) сильной кислотой: KNO 2 + HCl = НNO 2 + KCl NO 2 - + H+ = НNO 2 (сокращенное ионное уравнение) Строение продуктов реакции с азотистой кислотой зависит от характера амина. Поэтому данная реакция используется для различения первичных, вторичных и третичных аминов.
 Взаимодействие с азотистой кислотой Первичные алифатические амины c HNO 2 образуют спирты: R-NH 2 + HNO 2 → R-OH + N 2 + H 2 O Первичные ароматические амины при повышенной температуре реагируют аналогично, образуя фенолы. При низкой температуре (около 0° С) реакция идет иначе Вторичные амины (алифатические и ароматические) под действием HNO 2 превращаются в нитрозосоединения (вещества с характерным запахом): R 2 NH + H-O-N=O → R 2 N-N=O + H 2 O алкилнитрозамин Реакция с третичными аминами приводит к образованию неустойчивых солей и не имеет практического значения.
Взаимодействие с азотистой кислотой Первичные алифатические амины c HNO 2 образуют спирты: R-NH 2 + HNO 2 → R-OH + N 2 + H 2 O Первичные ароматические амины при повышенной температуре реагируют аналогично, образуя фенолы. При низкой температуре (около 0° С) реакция идет иначе Вторичные амины (алифатические и ароматические) под действием HNO 2 превращаются в нитрозосоединения (вещества с характерным запахом): R 2 NH + H-O-N=O → R 2 N-N=O + H 2 O алкилнитрозамин Реакция с третичными аминами приводит к образованию неустойчивых солей и не имеет практического значения.
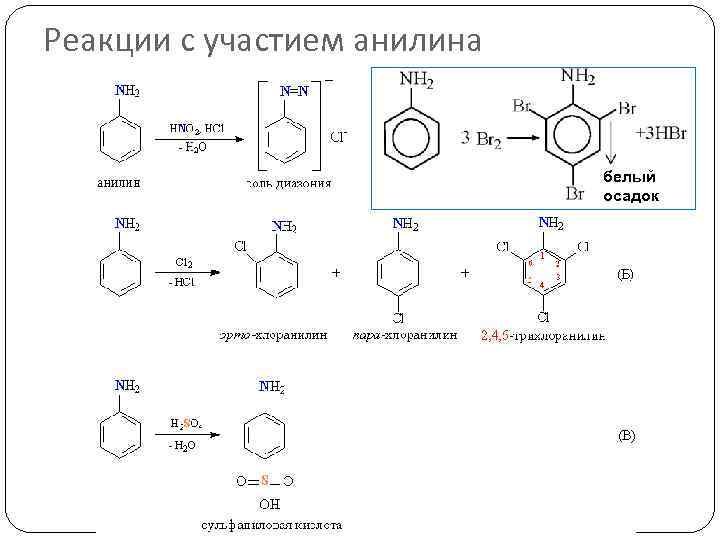 Реакции с участием анилина белый осадок
Реакции с участием анилина белый осадок
 4. Алкилирование Получение вторичных и третичных аминов Составьте уравнения реакций взаимодействия по цепочке превращений: -HCl + С 2 Н 5 Cl С 6 Н 5 NH 2 + C 2 H 5 Cl → С 6 Н 5 NHС 2 Н 5 → анилин N-этиланилин -HCl → С 6 Н 5 N(С 2 Н 5)2 N, N - диэтиланилин (СН 3) 3 N + CH 3 -Br → [(CH 3) 4 N]+Brбромид тетраметиламмония
4. Алкилирование Получение вторичных и третичных аминов Составьте уравнения реакций взаимодействия по цепочке превращений: -HCl + С 2 Н 5 Cl С 6 Н 5 NH 2 + C 2 H 5 Cl → С 6 Н 5 NHС 2 Н 5 → анилин N-этиланилин -HCl → С 6 Н 5 N(С 2 Н 5)2 N, N - диэтиланилин (СН 3) 3 N + CH 3 -Br → [(CH 3) 4 N]+Brбромид тетраметиламмония
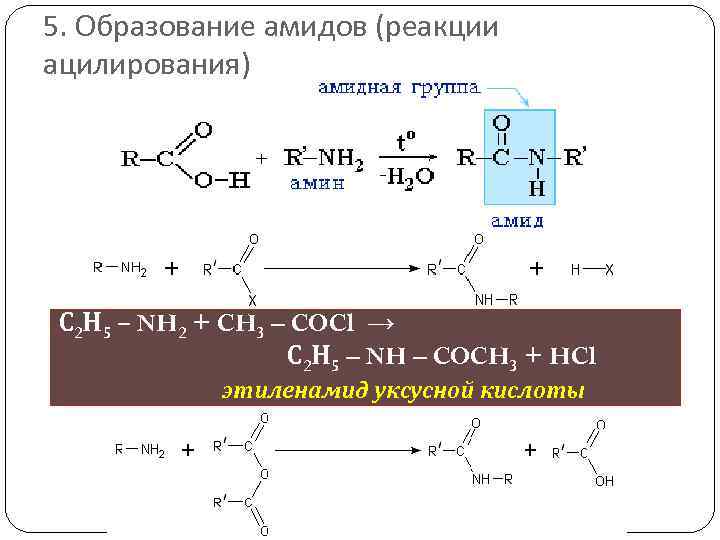 5. Образование амидов (реакции ацилирования) С 2 Н 5 – NH 2 + CH 3 – COCl → С 2 Н 5 – NH – COCH 3 + HCl этиленамид уксусной кислоты
5. Образование амидов (реакции ацилирования) С 2 Н 5 – NH 2 + CH 3 – COCl → С 2 Н 5 – NH – COCH 3 + HCl этиленамид уксусной кислоты
 Ацетилирование анилина Ацетилирование (т. е. замещение водорода на остаток уксусной кислоты - ацетил) анилина производят или нагревая его с избытком ледяной уксусной кислоты, или (что более удобно) путем взаимодействия анилина с уксусным ангидридом: ацетанилид
Ацетилирование анилина Ацетилирование (т. е. замещение водорода на остаток уксусной кислоты - ацетил) анилина производят или нагревая его с избытком ледяной уксусной кислоты, или (что более удобно) путем взаимодействия анилина с уксусным ангидридом: ацетанилид
 Синтетические полиамидные материалы С 20 -х гг. 20 в. американская химическая компания «Дюпон» стала лидером в разработке и производстве полимеров 1928 г. – Уоллес Хьюм Карозерс- получение синтетических полиамидов из диаминов и дикарбоновых кислот реакция поликонденсации → найлон
Синтетические полиамидные материалы С 20 -х гг. 20 в. американская химическая компания «Дюпон» стала лидером в разработке и производстве полимеров 1928 г. – Уоллес Хьюм Карозерс- получение синтетических полиамидов из диаминов и дикарбоновых кислот реакция поликонденсации → найлон
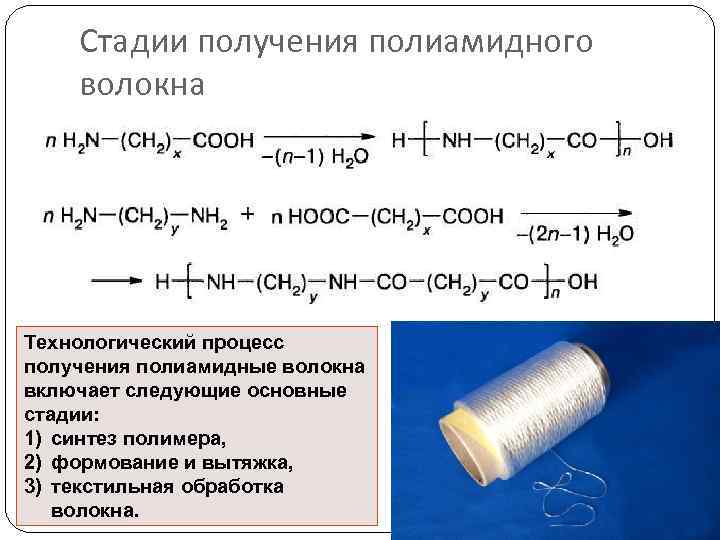 Стадии получения полиамидного волокна Технологический процесс получения полиамидные волокна включает следующие основные стадии: 1) синтез полимера, 2) формование и вытяжка, 3) текстильная обработка волокна.
Стадии получения полиамидного волокна Технологический процесс получения полиамидные волокна включает следующие основные стадии: 1) синтез полимера, 2) формование и вытяжка, 3) текстильная обработка волокна.
 Полиамидные волокна Синтетические волокна, формуемые из полиамидов. около 98% от общего производства полиамидные волокна составляют волокна из алифатических полиамидов, основная масса производится из поли-ε-капроамида (выпускается под торговыми названиями капрон, найлон-6, амилан, дедерон, стилон, лилион, релон, перлон, видлон, хемлон, энкалон и др. ) и полигексаметиленадипинамида (найлон-6, 6). Производство других видов алифатических полиамидных волокон очень незначительно, что объясняется экономическими проблемами, связанными с получением мономеров, техническими трудностями синтеза полимеров, переработки их в волокна и отсутствием у большинства этих волокон конкурентоспособных потребительских свойств.
Полиамидные волокна Синтетические волокна, формуемые из полиамидов. около 98% от общего производства полиамидные волокна составляют волокна из алифатических полиамидов, основная масса производится из поли-ε-капроамида (выпускается под торговыми названиями капрон, найлон-6, амилан, дедерон, стилон, лилион, релон, перлон, видлон, хемлон, энкалон и др. ) и полигексаметиленадипинамида (найлон-6, 6). Производство других видов алифатических полиамидных волокон очень незначительно, что объясняется экономическими проблемами, связанными с получением мономеров, техническими трудностями синтеза полимеров, переработки их в волокна и отсутствием у большинства этих волокон конкурентоспособных потребительских свойств.
 Полиамиды Пластмассы на основе линейных синтетических высокомолекулярных соединений, содержащих в основной цепи амидные группы —CONH—. Основная часть полиамидов — частично кристаллические термопластические полимеры, которые отличаются высокой прочностью, жесткостью и вязкостью, стойкостью к воздействию внешней среды. Большая часть свойств объясняется наличием амидных групп, которые связаны между собой с помощью водородных связей. Ряд свойств полиамидов зависит от их кристаллического устройства, в частности от содержания воды. Полиамиды взаимодействуют с окружающей средой обратимо впитывая влагу. Например в окружении воздуха, полиамид - 6 принимает примерно 2, 5 -3, 5% воды, а полиамид -6, 10 около 0, 5%. Влагопоглощение полиамидов напрямую влияет на их долговечность.
Полиамиды Пластмассы на основе линейных синтетических высокомолекулярных соединений, содержащих в основной цепи амидные группы —CONH—. Основная часть полиамидов — частично кристаллические термопластические полимеры, которые отличаются высокой прочностью, жесткостью и вязкостью, стойкостью к воздействию внешней среды. Большая часть свойств объясняется наличием амидных групп, которые связаны между собой с помощью водородных связей. Ряд свойств полиамидов зависит от их кристаллического устройства, в частности от содержания воды. Полиамиды взаимодействуют с окружающей средой обратимо впитывая влагу. Например в окружении воздуха, полиамид - 6 принимает примерно 2, 5 -3, 5% воды, а полиамид -6, 10 около 0, 5%. Влагопоглощение полиамидов напрямую влияет на их долговечность.
 Применение полиамидов В машиностроении - конструкционный материал, армирован следующими компонентами: стекловолокно, тальк, графит, масло, дисульфид молибдена Антикоррозийный материал для защиты металлов и бетона. В медицинской промышленности полиамидные волокна используются для изготовления протезов, хирургических нитей, искусственных кровеносных сосудов. В текстильной промышленности из полиамида изготавливают нити, ткани. В народном хозяйстве полиамид часто используется в качестве пленки, клеёв. В пищевой промышленности из полиамида производят различные оболочки для колбасных изделий.
Применение полиамидов В машиностроении - конструкционный материал, армирован следующими компонентами: стекловолокно, тальк, графит, масло, дисульфид молибдена Антикоррозийный материал для защиты металлов и бетона. В медицинской промышленности полиамидные волокна используются для изготовления протезов, хирургических нитей, искусственных кровеносных сосудов. В текстильной промышленности из полиамида изготавливают нити, ткани. В народном хозяйстве полиамид часто используется в качестве пленки, клеёв. В пищевой промышленности из полиамида производят различные оболочки для колбасных изделий.
 Найлон-6, 6 и 6, 10 n H 2 N-(CH 2)6 -NH 2 + n. HOOC- (CH 2)4 -COOH → 1, 6 -диаминогексан адипиновая (гексадикарбоновая) кислота [-NH- (CH 2)6 -NH-CO- (CH 2)4 -CO-]n + 2 n H 2 O n H 2 N-(CH 2)6 -NH 2 + n. Cl. OC- (CH 2)8 -COCl → 1, 6 -диаминогексан дихлорангидрид декандикарбоновой (себациновой) кислоты [-NH- (CH 2)6 -NH-CO- (CH 2)8 -CO-]n + 2 n HCl 1935 г. – синтез Карозерса, 1938 г. – первая зубная щетка с синтетической щетиной, 1939 г. – первые найлоновые чулки, искусственный шелк, парашюты
Найлон-6, 6 и 6, 10 n H 2 N-(CH 2)6 -NH 2 + n. HOOC- (CH 2)4 -COOH → 1, 6 -диаминогексан адипиновая (гексадикарбоновая) кислота [-NH- (CH 2)6 -NH-CO- (CH 2)4 -CO-]n + 2 n H 2 O n H 2 N-(CH 2)6 -NH 2 + n. Cl. OC- (CH 2)8 -COCl → 1, 6 -диаминогексан дихлорангидрид декандикарбоновой (себациновой) кислоты [-NH- (CH 2)6 -NH-CO- (CH 2)8 -CO-]n + 2 n HCl 1935 г. – синтез Карозерса, 1938 г. – первая зубная щетка с синтетической щетиной, 1939 г. – первые найлоновые чулки, искусственный шелк, парашюты

 Суперволокно- кевлар n H 2 N-C 6 H 4 -NH 2 + n. HOOC-C 6 H 4 -COOH → 1, 4 -диаминобензол терефталевая кислота [-NH-C 6 H 4 -NH-CO-C 6 H 4 -CO-]n + 2 n H 2 O Огнестойкий, гибкий материал, плотность в 4 раза меньше стали, но в 5 раз прочнее Изготавливают канаты, защитные костюмы пожарных и гонщиков «Формулы-1» , детали крыльев самолетов, корды для автомобильных шин, пуленепробиваемые жилеты, куртки фехтовальщиков
Суперволокно- кевлар n H 2 N-C 6 H 4 -NH 2 + n. HOOC-C 6 H 4 -COOH → 1, 4 -диаминобензол терефталевая кислота [-NH-C 6 H 4 -NH-CO-C 6 H 4 -CO-]n + 2 n H 2 O Огнестойкий, гибкий материал, плотность в 4 раза меньше стали, но в 5 раз прочнее Изготавливают канаты, защитные костюмы пожарных и гонщиков «Формулы-1» , детали крыльев самолетов, корды для автомобильных шин, пуленепробиваемые жилеты, куртки фехтовальщиков
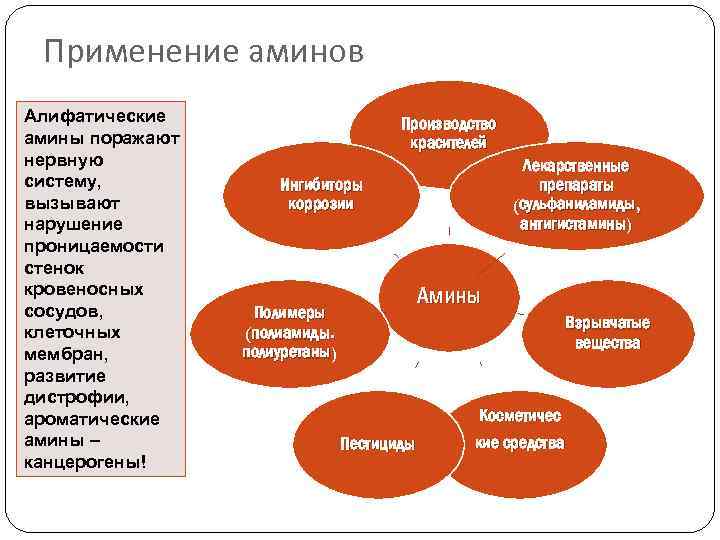 Применение аминов Алифатические амины поражают нервную систему, вызывают нарушение проницаемости стенок кровеносных сосудов, клеточных мембран, развитие дистрофии, ароматические амины – канцерогены! Производство красителей Лекарственные препараты (сульфаниламиды, антигистамины) Ингибиторы коррозии Амины Полимеры (полиамиды. полиуретаны) Взрывчатые вещества Пестициды Косметичес кие средства
Применение аминов Алифатические амины поражают нервную систему, вызывают нарушение проницаемости стенок кровеносных сосудов, клеточных мембран, развитие дистрофии, ароматические амины – канцерогены! Производство красителей Лекарственные препараты (сульфаниламиды, антигистамины) Ингибиторы коррозии Амины Полимеры (полиамиды. полиуретаны) Взрывчатые вещества Пестициды Косметичес кие средства
 Осуществите цепочку превращений Этан → этилен → ацетилен → бензол → → нитробензол → анилин → 2, 4, 6 -триброманилин Метан → хлорметан → метиламин → → сульфат метиламмония Метан → нитрометан → метиламин → азот
Осуществите цепочку превращений Этан → этилен → ацетилен → бензол → → нитробензол → анилин → 2, 4, 6 -триброманилин Метан → хлорметан → метиламин → → сульфат метиламмония Метан → нитрометан → метиламин → азот
 Составьте формулы аминов Этиламин 2 -аминопропан Метилпропиламин Пропиламин Метилэтиламин Триэтиламин 2 -пропиланилин Диметилфениламин Диаминоэтан 2. Напишите структурные формулы всех изомерных первичных аминов состава С 4 Н 11 N и назовите их. 3. По молекулярным формулам определите, к каким гомологическим рядам можно отнести следующие соединения: С 3 Н 8, С 3 Н 6, С 3 Н 4, С 3 Н 8 О, С 3 Н 6 О, С 3 Н 6 О 2, С 3 Н 9 N. Какие из формул могут принадлежать веществам различных классов и почему? Напишите структурные формулы всех возможных изомеров азотсодержащего вещества
Составьте формулы аминов Этиламин 2 -аминопропан Метилпропиламин Пропиламин Метилэтиламин Триэтиламин 2 -пропиланилин Диметилфениламин Диаминоэтан 2. Напишите структурные формулы всех изомерных первичных аминов состава С 4 Н 11 N и назовите их. 3. По молекулярным формулам определите, к каким гомологическим рядам можно отнести следующие соединения: С 3 Н 8, С 3 Н 6, С 3 Н 4, С 3 Н 8 О, С 3 Н 6 О, С 3 Н 6 О 2, С 3 Н 9 N. Какие из формул могут принадлежать веществам различных классов и почему? Напишите структурные формулы всех возможных изомеров азотсодержащего вещества
 Определите формулу вещества Органическое вещество содержит 38, 7% углерода, 45, 15% азота, 16, 15% водорода. Относительная плотность его паров по водороду равна 15, 5. определите формулу вещества При сгорании 5, 64 г органического вещества, состоящего из углерода, водорода, азота, образовалось 3, 84 г воды, 15, 94 г углекислого газа. Определите молекулярную формулу вещества.
Определите формулу вещества Органическое вещество содержит 38, 7% углерода, 45, 15% азота, 16, 15% водорода. Относительная плотность его паров по водороду равна 15, 5. определите формулу вещества При сгорании 5, 64 г органического вещества, состоящего из углерода, водорода, азота, образовалось 3, 84 г воды, 15, 94 г углекислого газа. Определите молекулярную формулу вещества.
 Расположите вещества в порядке усиления основных свойств 1) аммиак, этиламин, анилин 2) о-толуидин, анилин, п-нитроанилин, аммиак, гидроксид антрия, метиламин Осуществите цепочку превращений: Ca. C 2 →C 2 H 2 → C 6 H 6 → C 6 H 5 NO 2 → C 6 H 5 NH 2 → → C 6 H 2 Br 3 NH 2 2) CH 4 → CH 3 Br → CH 3 -NH 2 →(CH 3) 2 NH → →[(CH 3) 2 NH]HSO 4 C 6 H 5 CH 3 →C 6 H 5 CH 2 Cl →C 6 H 5 CH 2 NH 2 1)
Расположите вещества в порядке усиления основных свойств 1) аммиак, этиламин, анилин 2) о-толуидин, анилин, п-нитроанилин, аммиак, гидроксид антрия, метиламин Осуществите цепочку превращений: Ca. C 2 →C 2 H 2 → C 6 H 6 → C 6 H 5 NO 2 → C 6 H 5 NH 2 → → C 6 H 2 Br 3 NH 2 2) CH 4 → CH 3 Br → CH 3 -NH 2 →(CH 3) 2 NH → →[(CH 3) 2 NH]HSO 4 C 6 H 5 CH 3 →C 6 H 5 CH 2 Cl →C 6 H 5 CH 2 NH 2 1)
 Решите задачи Смешали 10 л газообразного метиламина и 10 г хлороводорода. Какой газ останется в избытке и каков его объем в тех же условиях? Смесь фенола и анилина полностью прореагировала с 40 г 5%-ного раствора гидроксида натрия. Такая же масса этой смеси может реагировать с бромной водой, содержащей 72 г брома. Определите массы фенола и анилина в исходной смеси
Решите задачи Смешали 10 л газообразного метиламина и 10 г хлороводорода. Какой газ останется в избытке и каков его объем в тех же условиях? Смесь фенола и анилина полностью прореагировала с 40 г 5%-ного раствора гидроксида натрия. Такая же масса этой смеси может реагировать с бромной водой, содержащей 72 г брома. Определите массы фенола и анилина в исходной смеси
 Химический диктант Инструкция: Прочитайте внимательно тексты. Вставьте пропущенные слова, словосочетания, формулы. 1 вариант 2 вариант 1. Амины по числу углеводородных радикалов можно разделить на три группы: …. , …, …. 2. Вещество с формулой С 2 Н 5 –NН–С 2 Н 5 называется … 1. Амины — производные …, в молекулах которых один или несколько атомов водорода замещены на углеводородный радикал. 2. Вещество с формулой С 2 Н 5 – NН 2 называется … 3. Метиламин — …. с резким 3. Анилин — …. . в воде жидкость с неприятным аммиачным запахом, быстро хорошо растворим в воде темнеющая на воздухе, очень ядовитая.
Химический диктант Инструкция: Прочитайте внимательно тексты. Вставьте пропущенные слова, словосочетания, формулы. 1 вариант 2 вариант 1. Амины по числу углеводородных радикалов можно разделить на три группы: …. , …, …. 2. Вещество с формулой С 2 Н 5 –NН–С 2 Н 5 называется … 1. Амины — производные …, в молекулах которых один или несколько атомов водорода замещены на углеводородный радикал. 2. Вещество с формулой С 2 Н 5 – NН 2 называется … 3. Метиламин — …. с резким 3. Анилин — …. . в воде жидкость с неприятным аммиачным запахом, быстро хорошо растворим в воде темнеющая на воздухе, очень ядовитая.
 Химический диктант 1 вариант 2 вариант 4. Горение метиламина выражается уравнением: 4 СН 3 NH 2 + 9 О 2 → 4… + 10…+ 2 N 2 5. Характерное химическое свойство аминов заключается в образовании солей при взаимодействии с кислотами, поэтому амины — органические …. 6. Качественной реакцией на анилин является реакция с …. 7. Впервые анилин получил русский химик … 4. Горение анилина выражается уравнением: 2 С 6 Н 5 NH 2 + 15, 5 О 2 → 12 … + + 7 … + N 2 5. Анилин более слабое …. , чем амины и аммиак. 6. При взаимодействии анилина с бромной водой образуется …. осадок. 7. В основе получения анилина лежит реакция восстановления …
Химический диктант 1 вариант 2 вариант 4. Горение метиламина выражается уравнением: 4 СН 3 NH 2 + 9 О 2 → 4… + 10…+ 2 N 2 5. Характерное химическое свойство аминов заключается в образовании солей при взаимодействии с кислотами, поэтому амины — органические …. 6. Качественной реакцией на анилин является реакция с …. 7. Впервые анилин получил русский химик … 4. Горение анилина выражается уравнением: 2 С 6 Н 5 NH 2 + 15, 5 О 2 → 12 … + + 7 … + N 2 5. Анилин более слабое …. , чем амины и аммиак. 6. При взаимодействии анилина с бромной водой образуется …. осадок. 7. В основе получения анилина лежит реакция восстановления …
 Ответы 1 вариант Первичные, вторичные, третичные. 1. Диэтиламин. 2. Бесцветный газ. 3. СО 2 Н 2 О. 4. Основания. 5. Бромной водой. 6. Зинин. 1. 2 вариант 1. Аммиака. 2. Этиламин. 3. Бесцветная нерастворимая. 4. СО 2 Н 2 О. 5. Основание. 6. Белый. 7. Нитробензола.
Ответы 1 вариант Первичные, вторичные, третичные. 1. Диэтиламин. 2. Бесцветный газ. 3. СО 2 Н 2 О. 4. Основания. 5. Бромной водой. 6. Зинин. 1. 2 вариант 1. Аммиака. 2. Этиламин. 3. Бесцветная нерастворимая. 4. СО 2 Н 2 О. 5. Основание. 6. Белый. 7. Нитробензола.
 Домашнее задание Параграф 25 Упражнения 3 – 9 (с. 226) Составить синквейн по теме 1. В первой строчке тема называется одним словом (обычно существительным). 2. Вторая строчка — это описание темы в двух словах (двумя прилагательными). 3. Третья строчка — это описание действия в рамках этой темы тремя словами (глаголами). 4. Четвертая строка — это фраза из четырех слов, показывающая отношение к теме. 5. Последняя строка — это синоним из одного слова, который повторяет суть темы. Например: 1. Анилин. 2. Бесцветный, ядовитый. 3. Пахнет, не растворяется, горит. 4. Без анилина нет красителей. 5. Амин.
Домашнее задание Параграф 25 Упражнения 3 – 9 (с. 226) Составить синквейн по теме 1. В первой строчке тема называется одним словом (обычно существительным). 2. Вторая строчка — это описание темы в двух словах (двумя прилагательными). 3. Третья строчка — это описание действия в рамках этой темы тремя словами (глаголами). 4. Четвертая строка — это фраза из четырех слов, показывающая отношение к теме. 5. Последняя строка — это синоним из одного слова, который повторяет суть темы. Например: 1. Анилин. 2. Бесцветный, ядовитый. 3. Пахнет, не растворяется, горит. 4. Без анилина нет красителей. 5. Амин.
 Литература О. С. Габриелян, И. Г. Остроумов. Настольная книга учителя химии 10 класс, «Блик и Ко» , 2001 Органическая химия. Весь школьный курс в таблицах, Минск, «Современная школа» , «Кузьма» , 2011 http: //www. chemistry. ssu. samara. ru http: //www. krugosvet. ru http: //c-books. narod. ru http: //www. newchemistry. ru http: //ru. wikipedia. org festival. 1 september. ru
Литература О. С. Габриелян, И. Г. Остроумов. Настольная книга учителя химии 10 класс, «Блик и Ко» , 2001 Органическая химия. Весь школьный курс в таблицах, Минск, «Современная школа» , «Кузьма» , 2011 http: //www. chemistry. ssu. samara. ru http: //www. krugosvet. ru http: //c-books. narod. ru http: //www. newchemistry. ru http: //ru. wikipedia. org festival. 1 september. ru


