10 Азотсодержащие органические соединения.pptx
- Количество слайдов: 37

 АЗОТСОДЕРЖАЩИЕ ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ Органические подразделяют на: соединения, – нитросоединения, – амины, – нитрилы и изоцианиды, – азо- и диазосоединения. содержащие азот,
АЗОТСОДЕРЖАЩИЕ ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ Органические подразделяют на: соединения, – нитросоединения, – амины, – нитрилы и изоцианиды, – азо- и диазосоединения. содержащие азот,

 СТРОЕНИЕ НИТРОСОЕДИНЕНИЯ Предельные нитросоединения имеют общую формулу Cn. H 2 n+1 NO 2 или R–NO 2. Они являются ИЗОМЕРАМИ ЭФИРОВ АЗОТИСТОЙ КИСЛОТЫ (АЛКИЛНИТРИТОВ) с общей формулой R–ONO. Между этими соединениями существуют различия: 1. Алкилнитриты КИПЯТ ПРИ БОЛЕЕ НИЗКОЙ ТЕМПЕРАТУРЕ, чем нитросоединения. 2. Нитросоединения СИЛЬНО ПОЛЯРНЫ и имеют БОЛЬШИЙ ДИПОЛЬНЫЙ МОМЕНТ. 3. Алкилнитриты ОМЫЛЯЮТСЯ ЩЕЛОЧАМИ И МИНЕРАЛЬНЫМИ КИСЛОТАМИ с образованием СПИРТОВ И АЗОТИСТОЙ КИСЛОТЫ ИЛИ ЕЕ СОЛИ. Нитросоединения таких веществ не образуют. 4. При восстановлении НИТРОСОЕДИНЕНИЙ образуются АМИНЫ, а АЛКИЛНИТРИТОВ – СПИРТЫ И ГИДРОКСИЛАМИН:
СТРОЕНИЕ НИТРОСОЕДИНЕНИЯ Предельные нитросоединения имеют общую формулу Cn. H 2 n+1 NO 2 или R–NO 2. Они являются ИЗОМЕРАМИ ЭФИРОВ АЗОТИСТОЙ КИСЛОТЫ (АЛКИЛНИТРИТОВ) с общей формулой R–ONO. Между этими соединениями существуют различия: 1. Алкилнитриты КИПЯТ ПРИ БОЛЕЕ НИЗКОЙ ТЕМПЕРАТУРЕ, чем нитросоединения. 2. Нитросоединения СИЛЬНО ПОЛЯРНЫ и имеют БОЛЬШИЙ ДИПОЛЬНЫЙ МОМЕНТ. 3. Алкилнитриты ОМЫЛЯЮТСЯ ЩЕЛОЧАМИ И МИНЕРАЛЬНЫМИ КИСЛОТАМИ с образованием СПИРТОВ И АЗОТИСТОЙ КИСЛОТЫ ИЛИ ЕЕ СОЛИ. Нитросоединения таких веществ не образуют. 4. При восстановлении НИТРОСОЕДИНЕНИЙ образуются АМИНЫ, а АЛКИЛНИТРИТОВ – СПИРТЫ И ГИДРОКСИЛАМИН:
 НИТРОСОЕДИНЕНИЯ R–ONO+2 Н 2 → R–ОН + NH 2 OH Структурная формула нитросоединений: Один из атомов кислорода образует с азотом двойную, другой – СЕМИПОЛЯРНУЮ СВЯЗЬ. Эта формула объясняет причину полярности нитросоединений, однако в молекуле связи обоих атомов кислорода с азотом не отличаются друг от друга. Поэтому нитросоединения изображают в виде ДВУХ ГРАНИЧНЫХ СТРУКТУР или ФОРМУЛОЙ С ДРОБНЫМИ ЗАРЯДАМИ: 5
НИТРОСОЕДИНЕНИЯ R–ONO+2 Н 2 → R–ОН + NH 2 OH Структурная формула нитросоединений: Один из атомов кислорода образует с азотом двойную, другой – СЕМИПОЛЯРНУЮ СВЯЗЬ. Эта формула объясняет причину полярности нитросоединений, однако в молекуле связи обоих атомов кислорода с азотом не отличаются друг от друга. Поэтому нитросоединения изображают в виде ДВУХ ГРАНИЧНЫХ СТРУКТУР или ФОРМУЛОЙ С ДРОБНЫМИ ЗАРЯДАМИ: 5
 НИТРОСОЕДИНЕНИЯ ИЗОМЕРИЯ. НОМЕНКЛАТУРА ИЗОМЕРИЯ НИТРОСОЕДИНЕНИЙ НАЧИНАЕТСЯ, как и у всех монозамещенных углеводородов (например, спиртов, галогеналкилов), С ПРОИЗВОДНЫХ ПРОПАНА. Различают ПЕРВИЧНЫЕ, ВТОРИЧНЫЕ И ТРЕТИЧНЫЕ НИТРОСОЕДИНЕНИЯ: R–R–СН 2–NO 2, R 2 CH–NO 2 И R 3 C–NO 2. НИТРОСОЕДИНЕНИЯ НАЗЫВАЮТ по углеводороду, добавляя приставку НИТРО-. ПО СИСТЕМАТИЧЕСКОЙ НОМЕНКЛАТУРЕ цифрой указывается местонахождение нитрогруппы: CH 3–NO 2 нитрометан нитроэтан СН 3–СН 2–NO 2 1 -нитропропан CH 3–CH 2–NO 2 CH 3–CH–CH 3 2 -нитропропан │ NO 2 6
НИТРОСОЕДИНЕНИЯ ИЗОМЕРИЯ. НОМЕНКЛАТУРА ИЗОМЕРИЯ НИТРОСОЕДИНЕНИЙ НАЧИНАЕТСЯ, как и у всех монозамещенных углеводородов (например, спиртов, галогеналкилов), С ПРОИЗВОДНЫХ ПРОПАНА. Различают ПЕРВИЧНЫЕ, ВТОРИЧНЫЕ И ТРЕТИЧНЫЕ НИТРОСОЕДИНЕНИЯ: R–R–СН 2–NO 2, R 2 CH–NO 2 И R 3 C–NO 2. НИТРОСОЕДИНЕНИЯ НАЗЫВАЮТ по углеводороду, добавляя приставку НИТРО-. ПО СИСТЕМАТИЧЕСКОЙ НОМЕНКЛАТУРЕ цифрой указывается местонахождение нитрогруппы: CH 3–NO 2 нитрометан нитроэтан СН 3–СН 2–NO 2 1 -нитропропан CH 3–CH 2–NO 2 CH 3–CH–CH 3 2 -нитропропан │ NO 2 6
 НИТРОСОЕДИНЕНИЯ СН 3–СН 2–СН 2–NO 2 CH 3–CH–CH 2–CH 3 │ NO 2 CH 3–CH–CH 2–NO 2 │ CH 3–CH–CH 3 │ NO 2 1 -интробутан 2 -нитробутан 1 -нитро-2 -метилпропан 2 -нитро-2 -метилпропан СПОСОБЫ ПОЛУЧЕНИЯ Нитросоединения получают: 1) НИТРОВАНИЕМ ПАРАФИНОВ В ГАЗОВОЙ ФАЗЕ 7 (РЕАКЦИЯ КОНОВАЛОВА):
НИТРОСОЕДИНЕНИЯ СН 3–СН 2–СН 2–NO 2 CH 3–CH–CH 2–CH 3 │ NO 2 CH 3–CH–CH 2–NO 2 │ CH 3–CH–CH 3 │ NO 2 1 -интробутан 2 -нитробутан 1 -нитро-2 -метилпропан 2 -нитро-2 -метилпропан СПОСОБЫ ПОЛУЧЕНИЯ Нитросоединения получают: 1) НИТРОВАНИЕМ ПАРАФИНОВ В ГАЗОВОЙ ФАЗЕ 7 (РЕАКЦИЯ КОНОВАЛОВА):
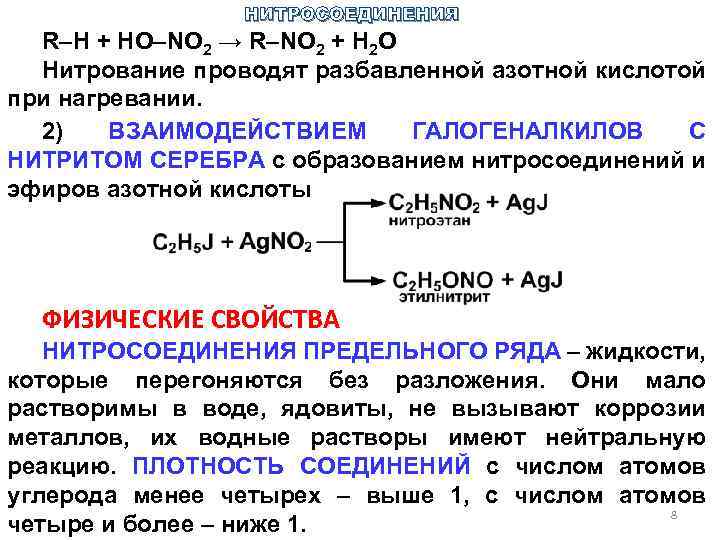 НИТРОСОЕДИНЕНИЯ R–H + HO–NO 2 → R–NO 2 + H 2 O Нитрование проводят разбавленной азотной кислотой при нагревании. 2) ВЗАИМОДЕЙСТВИЕМ ГАЛОГЕНАЛКИЛОВ С НИТРИТОМ СЕРЕБРА с образованием нитросоединений и эфиров азотной кислоты ФИЗИЧЕСКИЕ СВОЙСТВА НИТРОСОЕДИНЕНИЯ ПРЕДЕЛЬНОГО РЯДА – жидкости, которые перегоняются без разложения. Они мало растворимы в воде, ядовиты, не вызывают коррозии металлов, их водные растворы имеют нейтральную реакцию. ПЛОТНОСТЬ СОЕДИНЕНИЙ с числом атомов углерода менее четырех – выше 1, с числом атомов 8 четыре и более – ниже 1.
НИТРОСОЕДИНЕНИЯ R–H + HO–NO 2 → R–NO 2 + H 2 O Нитрование проводят разбавленной азотной кислотой при нагревании. 2) ВЗАИМОДЕЙСТВИЕМ ГАЛОГЕНАЛКИЛОВ С НИТРИТОМ СЕРЕБРА с образованием нитросоединений и эфиров азотной кислоты ФИЗИЧЕСКИЕ СВОЙСТВА НИТРОСОЕДИНЕНИЯ ПРЕДЕЛЬНОГО РЯДА – жидкости, которые перегоняются без разложения. Они мало растворимы в воде, ядовиты, не вызывают коррозии металлов, их водные растворы имеют нейтральную реакцию. ПЛОТНОСТЬ СОЕДИНЕНИЙ с числом атомов углерода менее четырех – выше 1, с числом атомов 8 четыре и более – ниже 1.
 НИТРОСОЕДИНЕНИЯ Нитросоединения – полярные вещества, поэтому они кипят при более высоких температурах, чем спирты или карбонильные соединения. ХИМИЧЕСКИЕ СВОЙСТВА Основные химические превращения нитросоединений определяются СТРУКТУРОЙ НИТРОГРУППЫ. 1) ПРИ ВОССТАНОВЛЕНИИ НИТРОСОЕДИНЕНИЙ ОБРАЗУЮТСЯ ПЕРВИЧНЫЕ АМИНЫ: R–NO 2 + 3 Н 2 → R–NH 2 + 2 Н 2 О 2) первичные и вторичные НИТРОСОЕДИНЕНИЯ РАСТВОРЯЮТСЯ В ЩЕЛОЧАХ С ОБРАЗОВАНИЕМ СОЛЕЙ. Это объясняется тем, что водородные атомы при атоме углерода, связанном непосредственно с нитрогруппой, под ее влиянием активируются и В ЩЕЛОЧНОЙ СРЕДЕ НИТРОСОЕДИНЕНИЯ ПЕРЕГРУППИРОВЫВАЮТСЯ В КИСЛОТНУЮ АЦИ-НИТРО-ФОРМУ. 9
НИТРОСОЕДИНЕНИЯ Нитросоединения – полярные вещества, поэтому они кипят при более высоких температурах, чем спирты или карбонильные соединения. ХИМИЧЕСКИЕ СВОЙСТВА Основные химические превращения нитросоединений определяются СТРУКТУРОЙ НИТРОГРУППЫ. 1) ПРИ ВОССТАНОВЛЕНИИ НИТРОСОЕДИНЕНИЙ ОБРАЗУЮТСЯ ПЕРВИЧНЫЕ АМИНЫ: R–NO 2 + 3 Н 2 → R–NH 2 + 2 Н 2 О 2) первичные и вторичные НИТРОСОЕДИНЕНИЯ РАСТВОРЯЮТСЯ В ЩЕЛОЧАХ С ОБРАЗОВАНИЕМ СОЛЕЙ. Это объясняется тем, что водородные атомы при атоме углерода, связанном непосредственно с нитрогруппой, под ее влиянием активируются и В ЩЕЛОЧНОЙ СРЕДЕ НИТРОСОЕДИНЕНИЯ ПЕРЕГРУППИРОВЫВАЮТСЯ В КИСЛОТНУЮ АЦИ-НИТРО-ФОРМУ. 9
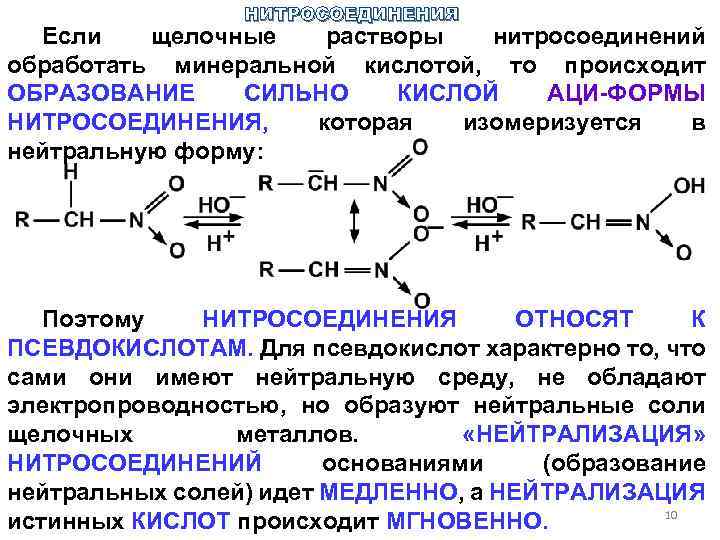 НИТРОСОЕДИНЕНИЯ Если щелочные растворы нитросоединений обработать минеральной кислотой, то происходит ОБРАЗОВАНИЕ СИЛЬНО КИСЛОЙ АЦИ-ФОРМЫ НИТРОСОЕДИНЕНИЯ, которая изомеризуется в нейтральную форму: Поэтому НИТРОСОЕДИНЕНИЯ ОТНОСЯТ К ПСЕВДОКИСЛОТАМ. Для псевдокислот характерно то, что сами они имеют нейтральную среду, не обладают электропроводностью, но образуют нейтральные соли щелочных металлов. «НЕЙТРАЛИЗАЦИЯ» НИТРОСОЕДИНЕНИЙ основаниями (образование нейтральных солей) идет МЕДЛЕННО, а НЕЙТРАЛИЗАЦИЯ 10 истинных КИСЛОТ происходит МГНОВЕННО.
НИТРОСОЕДИНЕНИЯ Если щелочные растворы нитросоединений обработать минеральной кислотой, то происходит ОБРАЗОВАНИЕ СИЛЬНО КИСЛОЙ АЦИ-ФОРМЫ НИТРОСОЕДИНЕНИЯ, которая изомеризуется в нейтральную форму: Поэтому НИТРОСОЕДИНЕНИЯ ОТНОСЯТ К ПСЕВДОКИСЛОТАМ. Для псевдокислот характерно то, что сами они имеют нейтральную среду, не обладают электропроводностью, но образуют нейтральные соли щелочных металлов. «НЕЙТРАЛИЗАЦИЯ» НИТРОСОЕДИНЕНИЙ основаниями (образование нейтральных солей) идет МЕДЛЕННО, а НЕЙТРАЛИЗАЦИЯ 10 истинных КИСЛОТ происходит МГНОВЕННО.
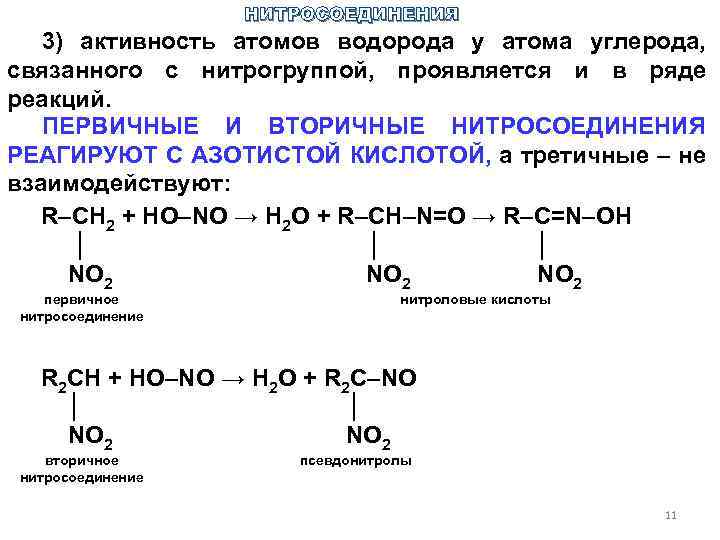 НИТРОСОЕДИНЕНИЯ 3) активность атомов водорода у атома углерода, связанного с нитрогруппой, проявляется и в ряде реакций. ПЕРВИЧНЫЕ И ВТОРИЧНЫЕ НИТРОСОЕДИНЕНИЯ РЕАГИРУЮТ С АЗОТИСТОЙ КИСЛОТОЙ, а третичные – не взаимодействуют: R–CH 2 + HO–NO → H 2 O + R–CH–N=O → R–C=N–ОН │ │ │ NO 2 первичное нитросоединение нитроловые кислоты R 2 CH + HO–NO → H 2 О + R 2 C–NO │ │ NO 2 вторичное нитросоединение псевдонитролы 11
НИТРОСОЕДИНЕНИЯ 3) активность атомов водорода у атома углерода, связанного с нитрогруппой, проявляется и в ряде реакций. ПЕРВИЧНЫЕ И ВТОРИЧНЫЕ НИТРОСОЕДИНЕНИЯ РЕАГИРУЮТ С АЗОТИСТОЙ КИСЛОТОЙ, а третичные – не взаимодействуют: R–CH 2 + HO–NO → H 2 O + R–CH–N=O → R–C=N–ОН │ │ │ NO 2 первичное нитросоединение нитроловые кислоты R 2 CH + HO–NO → H 2 О + R 2 C–NO │ │ NO 2 вторичное нитросоединение псевдонитролы 11
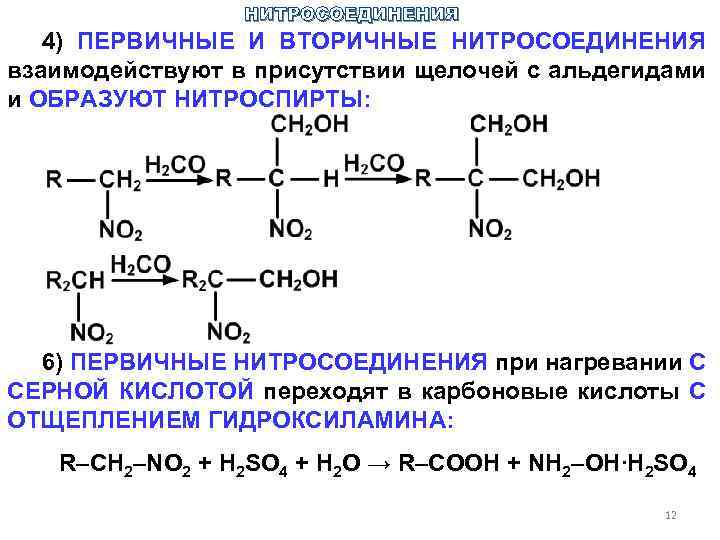 НИТРОСОЕДИНЕНИЯ 4) ПЕРВИЧНЫЕ И ВТОРИЧНЫЕ НИТРОСОЕДИНЕНИЯ взаимодействуют в присутствии щелочей с альдегидами и ОБРАЗУЮТ НИТРОСПИРТЫ: 6) ПЕРВИЧНЫЕ НИТРОСОЕДИНЕНИЯ при нагревании С СЕРНОЙ КИСЛОТОЙ переходят в карбоновые кислоты С ОТЩЕПЛЕНИЕМ ГИДРОКСИЛАМИНА: R–CH 2–NО 2 + H 2 SO 4 + H 2 O → R–COOH + NH 2–OH∙H 2 SO 4 12
НИТРОСОЕДИНЕНИЯ 4) ПЕРВИЧНЫЕ И ВТОРИЧНЫЕ НИТРОСОЕДИНЕНИЯ взаимодействуют в присутствии щелочей с альдегидами и ОБРАЗУЮТ НИТРОСПИРТЫ: 6) ПЕРВИЧНЫЕ НИТРОСОЕДИНЕНИЯ при нагревании С СЕРНОЙ КИСЛОТОЙ переходят в карбоновые кислоты С ОТЩЕПЛЕНИЕМ ГИДРОКСИЛАМИНА: R–CH 2–NО 2 + H 2 SO 4 + H 2 O → R–COOH + NH 2–OH∙H 2 SO 4 12
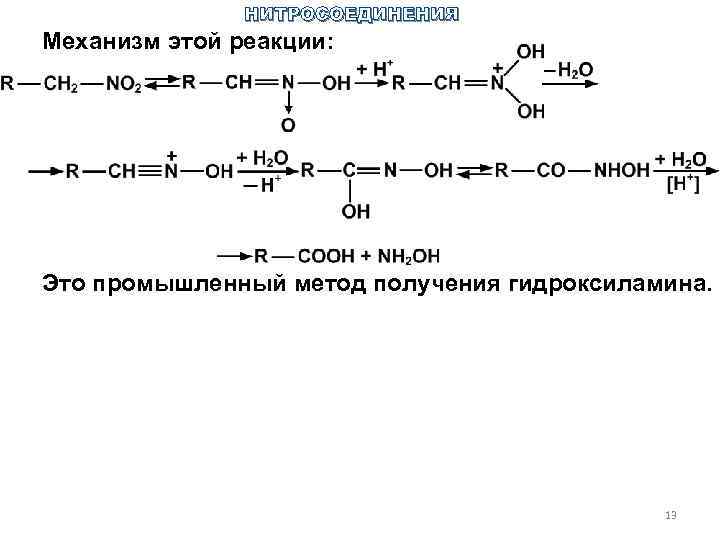 НИТРОСОЕДИНЕНИЯ Механизм этой реакции: Это промышленный метод получения гидроксиламина. 13
НИТРОСОЕДИНЕНИЯ Механизм этой реакции: Это промышленный метод получения гидроксиламина. 13

 АМИНЫ Амины ‒ соединения, образующиеся в результате замещения водородных атомов в аммиаке алкильными группами. В зависимости от того, сколько атомов водорода замещено радикалами, различают АМИНЫ ПЕРВИЧНЫЕ RNH 2, ВТОРИЧНЫЕ R 2 NH И ТРЕТИЧНЫЕ R 3 N. Таким образом, ПОНЯТИЯ ПЕРВИЧНЫЙ, ВТОРИЧНЫЙ И ТРЕТИЧНЫЙ СВЯЗАНЫ не с характером углеродного атома, а СО СТЕПЕНЬЮ ЗАМЕЩЕНИЯ ВОДОРОДОВ ПРИ АТОМЕ АЗОТА АММИАКА. ИЗОМЕРИЯ. НОМЕНКЛАТУРА ИЗОМЕРИЯ аминов ЗАВИСИТ ОТ ПОЛОЖЕНИЯ АМИНОГРУППЫ В УГЛЕРОДНОЙ ЦЕПИ И ОТ КОЛИЧЕСТВА И СТРОЕНИЯ РАДИКАЛОВ, СВЯЗАННЫХ С АТОМОМ АЗОТА. Амины называют ПО РАЦИОНАЛЬНОЙ НОМЕНКЛАТУРЕ как алкилзамещенные аммиака. 15
АМИНЫ Амины ‒ соединения, образующиеся в результате замещения водородных атомов в аммиаке алкильными группами. В зависимости от того, сколько атомов водорода замещено радикалами, различают АМИНЫ ПЕРВИЧНЫЕ RNH 2, ВТОРИЧНЫЕ R 2 NH И ТРЕТИЧНЫЕ R 3 N. Таким образом, ПОНЯТИЯ ПЕРВИЧНЫЙ, ВТОРИЧНЫЙ И ТРЕТИЧНЫЙ СВЯЗАНЫ не с характером углеродного атома, а СО СТЕПЕНЬЮ ЗАМЕЩЕНИЯ ВОДОРОДОВ ПРИ АТОМЕ АЗОТА АММИАКА. ИЗОМЕРИЯ. НОМЕНКЛАТУРА ИЗОМЕРИЯ аминов ЗАВИСИТ ОТ ПОЛОЖЕНИЯ АМИНОГРУППЫ В УГЛЕРОДНОЙ ЦЕПИ И ОТ КОЛИЧЕСТВА И СТРОЕНИЯ РАДИКАЛОВ, СВЯЗАННЫХ С АТОМОМ АЗОТА. Амины называют ПО РАЦИОНАЛЬНОЙ НОМЕНКЛАТУРЕ как алкилзамещенные аммиака. 15
 АМИНЫ ПО СИСТЕМАТИЧЕСКОЙ НОМЕНКЛАТУРЕ названия аминов образуются добавлением суффикса -АМИН к названию соответствующего радикала. Приведем названия аминов состава С 4 H 11 N: CH 2 NH 2–СН 2–CH 3 бутиламин, 1 -аминобутан СН 3–CH(NH 2)–СН 2–СН 3 втор-бутиламин, 1 -метилпропиламин изобутиламин, 1 -амино-2 -метилпропан, 2 -метилпропиламин (СН 3)2 СН–СН 2–NH 2 (СН 3)3 С–NH 2 тpeт-бутиламин, 2 -амино-2 -метилпропан, 1, 1 -диметилэтиламин СН 3–NH–СН 2–СН 3 метилпропиламин, N-метилпропиламин 16
АМИНЫ ПО СИСТЕМАТИЧЕСКОЙ НОМЕНКЛАТУРЕ названия аминов образуются добавлением суффикса -АМИН к названию соответствующего радикала. Приведем названия аминов состава С 4 H 11 N: CH 2 NH 2–СН 2–CH 3 бутиламин, 1 -аминобутан СН 3–CH(NH 2)–СН 2–СН 3 втор-бутиламин, 1 -метилпропиламин изобутиламин, 1 -амино-2 -метилпропан, 2 -метилпропиламин (СН 3)2 СН–СН 2–NH 2 (СН 3)3 С–NH 2 тpeт-бутиламин, 2 -амино-2 -метилпропан, 1, 1 -диметилэтиламин СН 3–NH–СН 2–СН 3 метилпропиламин, N-метилпропиламин 16
 АМИНЫ С 2 Н 5–NH–С 2 Н 5 СН 3–NH–СН(СН 3)2 диэтиламин метилизопропиламин, N-метил-1 -метилэтиламин (СН 3)2 N–С 2 Н 5 диметилэтиламин, N, N-диметилэтиламин Таким образом, формуле С 4 Н 11 N отвечают четыре первичных амина, три вторичных и один третичный. СПОСОБЫ ПОЛУЧЕНИЯ Амины широко применяют в технике и лабораторной практике. Поэтому разработано множество способов их получения. 1. ПРОПУСКАНИЕМ ПАРОВ СПИРТОВ И АММИАКА при 300 ºС над катализатором (Аl 2 О 3; Th. O 2) получают СМЕСЬ ПЕРВИЧНЫХ, ВТОРИЧНЫХ И ТРЕТИЧНЫХ АМИНОВ с преобладанием первичных: 17
АМИНЫ С 2 Н 5–NH–С 2 Н 5 СН 3–NH–СН(СН 3)2 диэтиламин метилизопропиламин, N-метил-1 -метилэтиламин (СН 3)2 N–С 2 Н 5 диметилэтиламин, N, N-диметилэтиламин Таким образом, формуле С 4 Н 11 N отвечают четыре первичных амина, три вторичных и один третичный. СПОСОБЫ ПОЛУЧЕНИЯ Амины широко применяют в технике и лабораторной практике. Поэтому разработано множество способов их получения. 1. ПРОПУСКАНИЕМ ПАРОВ СПИРТОВ И АММИАКА при 300 ºС над катализатором (Аl 2 О 3; Th. O 2) получают СМЕСЬ ПЕРВИЧНЫХ, ВТОРИЧНЫХ И ТРЕТИЧНЫХ АМИНОВ с преобладанием первичных: 17
 АМИНЫ 2. ДЕЙСТВИЕМ АММИАКА НА ГАЛОГЕНОПРОИЗВОДНЫЕ (реакция нуклеофильного замещения) получают смесь солей различных аминов, так как ОБРАЗУЮЩИЕСЯ в ходе реакции АМИНЫ (благодаря частичному разложению солей аммиаком) ВСТУПАЮТ в свою очередь В РЕАКЦИЮ С ГАЛОГЕНАЛКИЛАМИ: Последний продукт является полностью ЗАМЕЩЕННЫМ АММОНИЕВЫМ СОЕДИНЕНИЕМ, которое называют ИОДИСТЫМ ТЕТРАМЕТИЛАММОНИЕМ. 18
АМИНЫ 2. ДЕЙСТВИЕМ АММИАКА НА ГАЛОГЕНОПРОИЗВОДНЫЕ (реакция нуклеофильного замещения) получают смесь солей различных аминов, так как ОБРАЗУЮЩИЕСЯ в ходе реакции АМИНЫ (благодаря частичному разложению солей аммиаком) ВСТУПАЮТ в свою очередь В РЕАКЦИЮ С ГАЛОГЕНАЛКИЛАМИ: Последний продукт является полностью ЗАМЕЩЕННЫМ АММОНИЕВЫМ СОЕДИНЕНИЕМ, которое называют ИОДИСТЫМ ТЕТРАМЕТИЛАММОНИЕМ. 18
 АМИНЫ Эту смесь обрабатывают щелочью и подвергают перегонке с водяным паром. Первичные, вторичные и третичные амины отгоняют с водяным паром, а гидроксид полностью замещенного аммония [(CH 3)4 N]ОН остается в перегонной колбе. РАЗДЕЛЕНИЕ АМИНОВ ПРОИЗВОДЯТ, ПОЛЬЗУЯСЬ ИХ РАЗЛИЧНОЙ РЕАКЦИОННОЙ СПОСОБНОСТЬЮ. 3. АМИДЫ КИСЛОТ ПРИ РАСЩЕПЛЕНИИ ГИПОБРОМИТОМ ИЛИ ГИПОХЛОРИТОМ КАЛИЯ ОБРАЗУЮТ ПЕРВИЧНЫЕ АМИНЫ: 4. НИТРОСОЕДИНЕНИЯ ВОССТАНАВЛИВАЮТСЯ ВОДОРОДОМ в присутствии катализаторов Pt, Pd, Ni или другими способами С ОБРАЗОВАНИЕМ ПЕРВИЧНЫХ АМИНОВ: R–NO 2 + 3 H 2 → R–NH 2 + 2 H 2 O. 19
АМИНЫ Эту смесь обрабатывают щелочью и подвергают перегонке с водяным паром. Первичные, вторичные и третичные амины отгоняют с водяным паром, а гидроксид полностью замещенного аммония [(CH 3)4 N]ОН остается в перегонной колбе. РАЗДЕЛЕНИЕ АМИНОВ ПРОИЗВОДЯТ, ПОЛЬЗУЯСЬ ИХ РАЗЛИЧНОЙ РЕАКЦИОННОЙ СПОСОБНОСТЬЮ. 3. АМИДЫ КИСЛОТ ПРИ РАСЩЕПЛЕНИИ ГИПОБРОМИТОМ ИЛИ ГИПОХЛОРИТОМ КАЛИЯ ОБРАЗУЮТ ПЕРВИЧНЫЕ АМИНЫ: 4. НИТРОСОЕДИНЕНИЯ ВОССТАНАВЛИВАЮТСЯ ВОДОРОДОМ в присутствии катализаторов Pt, Pd, Ni или другими способами С ОБРАЗОВАНИЕМ ПЕРВИЧНЫХ АМИНОВ: R–NO 2 + 3 H 2 → R–NH 2 + 2 H 2 O. 19
 АМИНЫ 5. НИТРИЛЫ при взаимодействии С ВОССТАНОВИТЕЛЯМИ ИЛИ ВОДОРОДОМ в присутствии катализаторов Pt, Pd, Ni образуют ПЕРВИЧНЫЕ АМИНЫ. При восстановлении изоцианидов образуются вторичные амины: R–CN + 2 H 2 → R–CH 2–NH 2 R–NC + 2 Н 2 → R–NH–CH 3 ФИЗИЧЕСКИЕ СВОЙСТВА Простейшие амины – МЕТИЛАМИН, ДИМЕТИЛАМИН И ТРИМЕТИЛАМИН – ГАЗЫ, хорошо растворимые в воде и обладающие запахом аммиака. Остальные НИЗШИЕ АМИНЫ – ЖИДКОСТИ С ЗАПАХОМ АММИАКА. Более сложные амины – жидкости с неприятным запахом рыбы. ВЫСШИЕ АМИНЫ – ТВЕРДЫЕ, нерастворимые в воде вещества, без запаха. 20
АМИНЫ 5. НИТРИЛЫ при взаимодействии С ВОССТАНОВИТЕЛЯМИ ИЛИ ВОДОРОДОМ в присутствии катализаторов Pt, Pd, Ni образуют ПЕРВИЧНЫЕ АМИНЫ. При восстановлении изоцианидов образуются вторичные амины: R–CN + 2 H 2 → R–CH 2–NH 2 R–NC + 2 Н 2 → R–NH–CH 3 ФИЗИЧЕСКИЕ СВОЙСТВА Простейшие амины – МЕТИЛАМИН, ДИМЕТИЛАМИН И ТРИМЕТИЛАМИН – ГАЗЫ, хорошо растворимые в воде и обладающие запахом аммиака. Остальные НИЗШИЕ АМИНЫ – ЖИДКОСТИ С ЗАПАХОМ АММИАКА. Более сложные амины – жидкости с неприятным запахом рыбы. ВЫСШИЕ АМИНЫ – ТВЕРДЫЕ, нерастворимые в воде вещества, без запаха. 20
 АМИНЫ АССОЦИИРОВАНЫ МЕНЕЕ СПИРТОВ, и потому ОНИ КИПЯТ ПРИ БОЛЕЕ НИЗКИХ ТЕМПЕРАТУРАХ, ЧЕМ СПИРТЫ С ТЕМ ЖЕ ЧИСЛОМ УГЛЕРОДНЫХ АТОМОВ. При равном числе атомов углерода ВЫШЕ ВСЕГО ТЕМПЕРАТУРА КИПЕНИЯ ПЕРВИЧНЫХ И НИЖЕ ВСЕГО ТРЕТИЧНЫХ АМИНОВ. Диэтиламин кипит при 56 °С, а бутиламин – при 76 °С, н-гексиламин (первичный) кипит при 129 °С, дипропиламин (вторичный) – при 110, 7 °С, а триэтиламин (третичный) – при 89, 5 °С. Простейшие АМИНЫ в отличие от аммиака ГОРЯТ НА ВОЗДУХЕ. В ИК-спектрах первичных и вторичных аминов существует ОБЛАСТЬ ПОГЛОЩЕНИЯ при 3300– 3500 см– 1, которая СООТВЕТСТВУЕТ ВАЛЕНТНЫМ КОЛЕБАНИЯМ N– Н-СВЯЗИ. Полосы поглощения, соответствующие валентным колебаниям связи N–С, располагаются в области длин волн 1100– 1300 см– 1 и трудно идентифицируются. 21
АМИНЫ АССОЦИИРОВАНЫ МЕНЕЕ СПИРТОВ, и потому ОНИ КИПЯТ ПРИ БОЛЕЕ НИЗКИХ ТЕМПЕРАТУРАХ, ЧЕМ СПИРТЫ С ТЕМ ЖЕ ЧИСЛОМ УГЛЕРОДНЫХ АТОМОВ. При равном числе атомов углерода ВЫШЕ ВСЕГО ТЕМПЕРАТУРА КИПЕНИЯ ПЕРВИЧНЫХ И НИЖЕ ВСЕГО ТРЕТИЧНЫХ АМИНОВ. Диэтиламин кипит при 56 °С, а бутиламин – при 76 °С, н-гексиламин (первичный) кипит при 129 °С, дипропиламин (вторичный) – при 110, 7 °С, а триэтиламин (третичный) – при 89, 5 °С. Простейшие АМИНЫ в отличие от аммиака ГОРЯТ НА ВОЗДУХЕ. В ИК-спектрах первичных и вторичных аминов существует ОБЛАСТЬ ПОГЛОЩЕНИЯ при 3300– 3500 см– 1, которая СООТВЕТСТВУЕТ ВАЛЕНТНЫМ КОЛЕБАНИЯМ N– Н-СВЯЗИ. Полосы поглощения, соответствующие валентным колебаниям связи N–С, располагаются в области длин волн 1100– 1300 см– 1 и трудно идентифицируются. 21
 АМИНЫ ХИМИЧЕСКИЕ СВОЙСТВА По химическим свойствам АМИНЫ СХОДНЫ С АММИАКОМ: вступают в различные реакции как НУКЛЕОФИЛЬНЫЕ РЕАГЕНТЫ. МОЛЕКУЛЫ АМИНОВ, как и аммиака, ИМЕЮТ ПИРАМИДАЛЬНУЮ СИММЕТРИЮ, причем обращение конфигурации происходит 103– 108 раз в 1 с (у аммиака 4· 1010 раз в 1 с). НУКЛЕОФИЛЬНЫЕ СВОЙСТВА аминов связаны С НАЛИЧИЕМ У АТОМА АЗОТА ПАРЫ НЕПОДЕЛЕННЫХ ЭЛЕКТРОНОВ. При образовании за счет этих электронов химической связи образуются АММОНИЙНЫЕ ИОНЫ, имеющие тетраэдрическую структуру. 1. Водные РАСТВОРЫ АМИНОВ ИМЕЮТ ОСНОВНОЙ ХАРАКТЕР. Это объясняется образованием полностью ИОНИЗИРОВАННЫХ АЛКИЛ-ЗАМЕЩЕННЫХ ГИДРОКСИДА АММОНИЯ: 22
АМИНЫ ХИМИЧЕСКИЕ СВОЙСТВА По химическим свойствам АМИНЫ СХОДНЫ С АММИАКОМ: вступают в различные реакции как НУКЛЕОФИЛЬНЫЕ РЕАГЕНТЫ. МОЛЕКУЛЫ АМИНОВ, как и аммиака, ИМЕЮТ ПИРАМИДАЛЬНУЮ СИММЕТРИЮ, причем обращение конфигурации происходит 103– 108 раз в 1 с (у аммиака 4· 1010 раз в 1 с). НУКЛЕОФИЛЬНЫЕ СВОЙСТВА аминов связаны С НАЛИЧИЕМ У АТОМА АЗОТА ПАРЫ НЕПОДЕЛЕННЫХ ЭЛЕКТРОНОВ. При образовании за счет этих электронов химической связи образуются АММОНИЙНЫЕ ИОНЫ, имеющие тетраэдрическую структуру. 1. Водные РАСТВОРЫ АМИНОВ ИМЕЮТ ОСНОВНОЙ ХАРАКТЕР. Это объясняется образованием полностью ИОНИЗИРОВАННЫХ АЛКИЛ-ЗАМЕЩЕННЫХ ГИДРОКСИДА АММОНИЯ: 22
 АМИНЫ 2. Амины с минеральными кислотами образуют АЛКИЛЗАМЕЩЕННЫЕ АММОНИЙНЫЕ СОЛИ: R–NH 2 + HCl → [R–NH 3]+Cl– хлорид алкиламмония Основные свойства аминов (Kb ~ 10– 4) обусловлены СПОСОБНОСТЬЮ СВОБОДНЫХ (НЕПОДЕЛЕННЫХ) ЭЛЕКТРОНОВ АТОМА АЗОТА ПРИСОЕДИНЯТЬ ПРОТОН (координационная связь): Основность аминов выше, чем аммиака, благодаря тому, что ИНДУКЦИОННЫЙ ЭФФЕКТ РАДИКАЛОВ УВЕЛИЧИВАЕТ ЭЛЕКТРОННУЮ ПЛОТНОСТЬ НА АТОМЕ АЗОТА, ДЕЛАЕТ ЭЛЕКТРОНЫ АЗОТА БОЛЕЕ АКТИВНЫМИ (они прочнее связывают протон). 23
АМИНЫ 2. Амины с минеральными кислотами образуют АЛКИЛЗАМЕЩЕННЫЕ АММОНИЙНЫЕ СОЛИ: R–NH 2 + HCl → [R–NH 3]+Cl– хлорид алкиламмония Основные свойства аминов (Kb ~ 10– 4) обусловлены СПОСОБНОСТЬЮ СВОБОДНЫХ (НЕПОДЕЛЕННЫХ) ЭЛЕКТРОНОВ АТОМА АЗОТА ПРИСОЕДИНЯТЬ ПРОТОН (координационная связь): Основность аминов выше, чем аммиака, благодаря тому, что ИНДУКЦИОННЫЙ ЭФФЕКТ РАДИКАЛОВ УВЕЛИЧИВАЕТ ЭЛЕКТРОННУЮ ПЛОТНОСТЬ НА АТОМЕ АЗОТА, ДЕЛАЕТ ЭЛЕКТРОНЫ АЗОТА БОЛЕЕ АКТИВНЫМИ (они прочнее связывают протон). 23
 АМИНЫ ПЕРВИЧНЫЕ И ВТОРИЧНЫЕ АМИНЫ проявляют и очень слабые КИСЛОТНЫЕ СВОЙСТВА. Они образуют с щелочными металлами соли – АЛКИЛИЛИ ДИАЛКИЛАМИДЫ: 2 R 2 NH + 2 Na → 2 R 2 N–Na + H 2. 3. Амины способны к АЛКИЛИРОВАНИЮ, т. е. замещению атома Н на алкильный радикал. 4. Для аминов характерна РЕАКЦИЯ АЦИЛИРОВАНИЯ, в частности АЦЕТИЛИРОВАНИЯ, действием уксусного ангидрида или хлористого ацетила: C 2 H 5–NH 2+(CН 3–CO)2 O→С 2 H 5–NН–CO–CH 3+CH 3–COOH ацетилэтиламин или этилацетамид РЕАКЦИЯ АЦИЛИРОВАНИЯ – типичная реакция НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ – может проходить по механизму нуклеофильного замещения SN 1 ИЛИ SN 2, который описан в разделе 24 МОНОГАЛОГЕНПРОИЗВОДНЫЕ АЛКАНОВ).
АМИНЫ ПЕРВИЧНЫЕ И ВТОРИЧНЫЕ АМИНЫ проявляют и очень слабые КИСЛОТНЫЕ СВОЙСТВА. Они образуют с щелочными металлами соли – АЛКИЛИЛИ ДИАЛКИЛАМИДЫ: 2 R 2 NH + 2 Na → 2 R 2 N–Na + H 2. 3. Амины способны к АЛКИЛИРОВАНИЮ, т. е. замещению атома Н на алкильный радикал. 4. Для аминов характерна РЕАКЦИЯ АЦИЛИРОВАНИЯ, в частности АЦЕТИЛИРОВАНИЯ, действием уксусного ангидрида или хлористого ацетила: C 2 H 5–NH 2+(CН 3–CO)2 O→С 2 H 5–NН–CO–CH 3+CH 3–COOH ацетилэтиламин или этилацетамид РЕАКЦИЯ АЦИЛИРОВАНИЯ – типичная реакция НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ – может проходить по механизму нуклеофильного замещения SN 1 ИЛИ SN 2, который описан в разделе 24 МОНОГАЛОГЕНПРОИЗВОДНЫЕ АЛКАНОВ).
 АМИНЫ 5. АЗОТИСТАЯ КИСЛОТА взаимодействует С ПЕРВИЧНЫМИ АМИНАМИ с выделением азота и ОБРАЗОВАНИЕМ СПИРТОВ, АЛКЕНОВ или других веществ: R–NH 2 + HNO 2 → R–ОН + N 2 + H 2 O, со ВТОРИЧНЫМИ АМИНАМИ образуются НИТРОЗАМИНЫ: R 2 NH + HONO → R 2 N–NO + H 2 O. С ТРЕТИЧНЫМИ АМИНАМИ азотистая кислота не реагирует. При взаимодействии аминов с азотистой кислотой АКТИВНЫМ РЕАГЕНТОМ ЯВЛЯЕТСЯ N 2 O 3. Схема процесса: 25
АМИНЫ 5. АЗОТИСТАЯ КИСЛОТА взаимодействует С ПЕРВИЧНЫМИ АМИНАМИ с выделением азота и ОБРАЗОВАНИЕМ СПИРТОВ, АЛКЕНОВ или других веществ: R–NH 2 + HNO 2 → R–ОН + N 2 + H 2 O, со ВТОРИЧНЫМИ АМИНАМИ образуются НИТРОЗАМИНЫ: R 2 NH + HONO → R 2 N–NO + H 2 O. С ТРЕТИЧНЫМИ АМИНАМИ азотистая кислота не реагирует. При взаимодействии аминов с азотистой кислотой АКТИВНЫМ РЕАГЕНТОМ ЯВЛЯЕТСЯ N 2 O 3. Схема процесса: 25
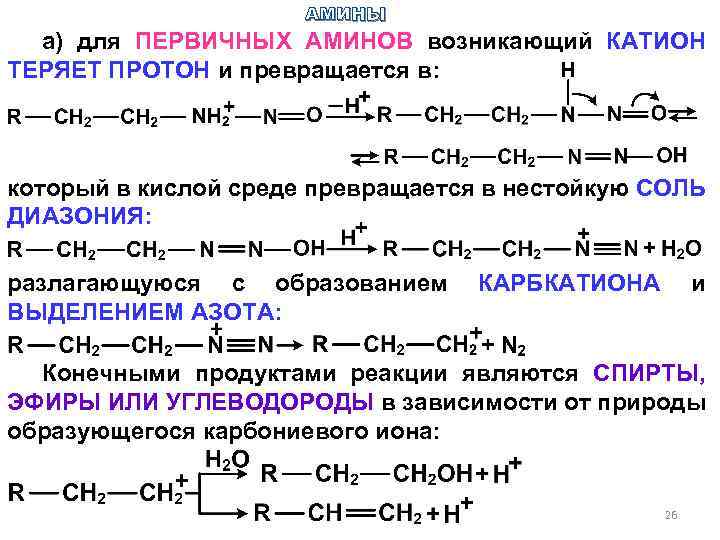 АМИНЫ а) для ПЕРВИЧНЫХ АМИНОВ возникающий КАТИОН ТЕРЯЕТ ПРОТОН и превращается в: который в кислой среде превращается в нестойкую СОЛЬ ДИАЗОНИЯ: разлагающуюся с образованием ВЫДЕЛЕНИЕМ АЗОТА: КАРБКАТИОНА и Конечными продуктами реакции являются СПИРТЫ, ЭФИРЫ ИЛИ УГЛЕВОДОРОДЫ в зависимости от природы образующегося карбониевого иона: 26
АМИНЫ а) для ПЕРВИЧНЫХ АМИНОВ возникающий КАТИОН ТЕРЯЕТ ПРОТОН и превращается в: который в кислой среде превращается в нестойкую СОЛЬ ДИАЗОНИЯ: разлагающуюся с образованием ВЫДЕЛЕНИЕМ АЗОТА: КАРБКАТИОНА и Конечными продуктами реакции являются СПИРТЫ, ЭФИРЫ ИЛИ УГЛЕВОДОРОДЫ в зависимости от природы образующегося карбониевого иона: 26
 АМИНЫ МЕТИЛАМИН образует ДИМЕТИЛОВЫЙ ЭФИР, ЭТИЛАМИН – ЭТИЛОВЫЙ СПИРТ (выход 60 %), а ПРОПИЛАМИН – ПРОПИЛОВЫЙ СПИРТ (7 %), ИЗОПРОПИЛОВЫЙ СПИРТ (32 %), ПРОПИЛЕН, ЦИКЛОПРОПЕН, а также ПРОПИЛИ ИЗОПРОПИЛНИТРИТЫ. Для высших аминов еще более характерна ИЗОМЕРИЗАЦИЯ КАРБОНИЕВОГО ИОНА. б) у ВТОРИЧНЫХ АМИНОВ катион отщепляет протон с образованием НИТРОЗАМИНА: НИТРОЗАМИНЫ – желтые или оранжевые масла. Концентрированными кислотами они РАСЩЕПЛЯЮТСЯ НА ИСХОДНЫЙ АМИН И АЗОТИСТУЮ КИСЛОТУ. в) ТРЕТИЧНЫЕ АМИНЫ в слабокислой среде (р. Н 3 -6) при нагревании расщепляются с образованием ВТОРИЧНОГО АМИНА И АЛЬДЕГИДА: 27
АМИНЫ МЕТИЛАМИН образует ДИМЕТИЛОВЫЙ ЭФИР, ЭТИЛАМИН – ЭТИЛОВЫЙ СПИРТ (выход 60 %), а ПРОПИЛАМИН – ПРОПИЛОВЫЙ СПИРТ (7 %), ИЗОПРОПИЛОВЫЙ СПИРТ (32 %), ПРОПИЛЕН, ЦИКЛОПРОПЕН, а также ПРОПИЛИ ИЗОПРОПИЛНИТРИТЫ. Для высших аминов еще более характерна ИЗОМЕРИЗАЦИЯ КАРБОНИЕВОГО ИОНА. б) у ВТОРИЧНЫХ АМИНОВ катион отщепляет протон с образованием НИТРОЗАМИНА: НИТРОЗАМИНЫ – желтые или оранжевые масла. Концентрированными кислотами они РАСЩЕПЛЯЮТСЯ НА ИСХОДНЫЙ АМИН И АЗОТИСТУЮ КИСЛОТУ. в) ТРЕТИЧНЫЕ АМИНЫ в слабокислой среде (р. Н 3 -6) при нагревании расщепляются с образованием ВТОРИЧНОГО АМИНА И АЛЬДЕГИДА: 27
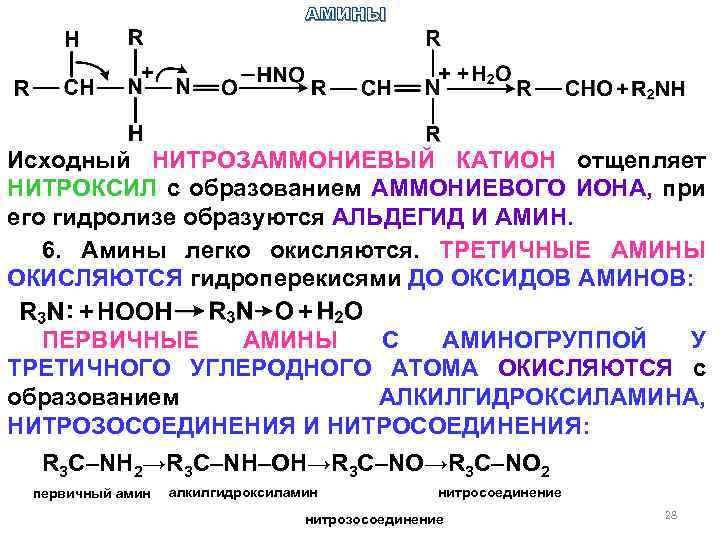 АМИНЫ Исходный НИТРОЗАММОНИЕВЫЙ КАТИОН отщепляет НИТРОКСИЛ с образованием АММОНИЕВОГО ИОНА, при его гидролизе образуются АЛЬДЕГИД И АМИН. 6. Амины легко окисляются. ТРЕТИЧНЫЕ АМИНЫ ОКИСЛЯЮТСЯ гидроперекисями ДО ОКСИДОВ АМИНОВ: ПЕРВИЧНЫЕ АМИНЫ С АМИНОГРУППОЙ У ТРЕТИЧНОГО УГЛЕРОДНОГО АТОМА ОКИСЛЯЮТСЯ с образованием АЛКИЛГИДРОКСИЛАМИНА, НИТРОЗОСОЕДИНЕНИЯ И НИТРОСОЕДИНЕНИЯ: R 3 C–NH 2→R 3 C–NH–ОН→R 3 C–NO 2 первичный амин алкилгидроксиламин нитросоединение нитрозосоединение 28
АМИНЫ Исходный НИТРОЗАММОНИЕВЫЙ КАТИОН отщепляет НИТРОКСИЛ с образованием АММОНИЕВОГО ИОНА, при его гидролизе образуются АЛЬДЕГИД И АМИН. 6. Амины легко окисляются. ТРЕТИЧНЫЕ АМИНЫ ОКИСЛЯЮТСЯ гидроперекисями ДО ОКСИДОВ АМИНОВ: ПЕРВИЧНЫЕ АМИНЫ С АМИНОГРУППОЙ У ТРЕТИЧНОГО УГЛЕРОДНОГО АТОМА ОКИСЛЯЮТСЯ с образованием АЛКИЛГИДРОКСИЛАМИНА, НИТРОЗОСОЕДИНЕНИЯ И НИТРОСОЕДИНЕНИЯ: R 3 C–NH 2→R 3 C–NH–ОН→R 3 C–NO 2 первичный амин алкилгидроксиламин нитросоединение нитрозосоединение 28
 АМИНЫ В реакциях окисления ДРУГИХ ПЕРВИЧНЫХ И ВТОРИЧНЫХ АМИНОВ образуются СЛОЖНЫЕ СМЕСИ ПРОДУКТОВ ОКИСЛЕНИЯ. ПРИМЕНЕНИЕ Амины применяются в качестве ОРГАНИЧЕСКИХ ОСНОВАНИЙ и ДЛЯ РЕАКЦИИ АМИНИРОВАНИЯ. Некоторые амины применяются как СЕЛЕКТИВНЫЕ РАСТВОРИТЕЛИ ДЛЯ ИЗВЛЕЧЕНИЯ УРАНА ИЗ СЕРНОКИСЛОТНЫХ РАСТВОРОВ. Амины, обладающие запахом рыбы, используются как приманка в борьбе с полевыми грызунами. 29
АМИНЫ В реакциях окисления ДРУГИХ ПЕРВИЧНЫХ И ВТОРИЧНЫХ АМИНОВ образуются СЛОЖНЫЕ СМЕСИ ПРОДУКТОВ ОКИСЛЕНИЯ. ПРИМЕНЕНИЕ Амины применяются в качестве ОРГАНИЧЕСКИХ ОСНОВАНИЙ и ДЛЯ РЕАКЦИИ АМИНИРОВАНИЯ. Некоторые амины применяются как СЕЛЕКТИВНЫЕ РАСТВОРИТЕЛИ ДЛЯ ИЗВЛЕЧЕНИЯ УРАНА ИЗ СЕРНОКИСЛОТНЫХ РАСТВОРОВ. Амины, обладающие запахом рыбы, используются как приманка в борьбе с полевыми грызунами. 29

 АМИНЫ 31
АМИНЫ 31
 АМИНЫ 32
АМИНЫ 32
 АМИНЫ 33
АМИНЫ 33
 АМИНЫ 34
АМИНЫ 34
 АМИНЫ 35
АМИНЫ 35
 АМИНЫ 36
АМИНЫ 36
 АМИНЫ 37
АМИНЫ 37


