азот.ppt
- Количество слайдов: 80
 АЗОТСОДЕРЖАЩИЕ ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ амины, аминоспирты, амиды
АЗОТСОДЕРЖАЩИЕ ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ амины, аминоспирты, амиды
 Амины - органические соединения, содержащие в своём составе аминогруппу –NH 2 или замещённую аминогруппу (-NHR или NR 2) - производные аммиака, в котором один или несколько атомов водорода замещены углеводородными радикалами
Амины - органические соединения, содержащие в своём составе аминогруппу –NH 2 или замещённую аминогруппу (-NHR или NR 2) - производные аммиака, в котором один или несколько атомов водорода замещены углеводородными радикалами
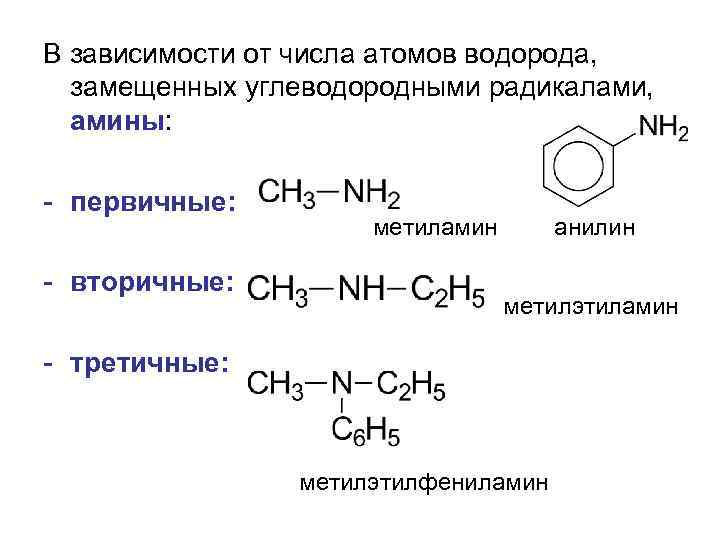 В зависимости от числа атомов водорода, замещенных углеводородными радикалами, амины: - первичные: - вторичные: метиламин анилин метилэтиламин - третичные: метилэтилфениламин
В зависимости от числа атомов водорода, замещенных углеводородными радикалами, амины: - первичные: - вторичные: метиламин анилин метилэтиламин - третичные: метилэтилфениламин
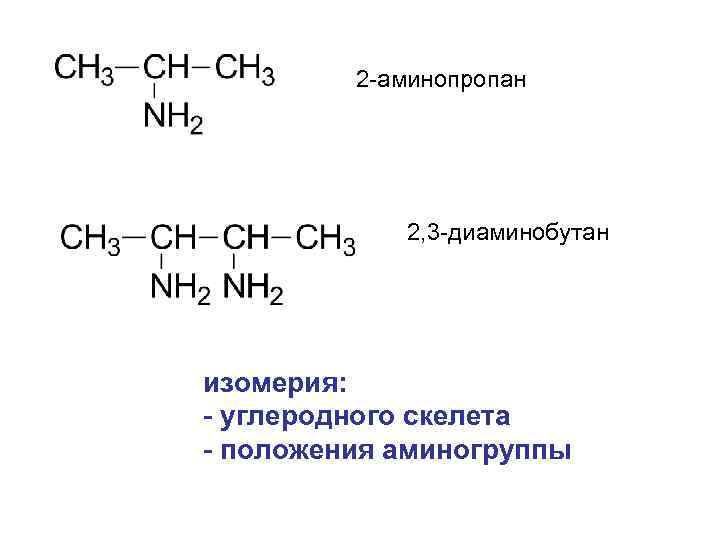 2 -аминопропан 2, 3 -диаминобутан изомерия: - углеродного скелета - положения аминогруппы
2 -аминопропан 2, 3 -диаминобутан изомерия: - углеродного скелета - положения аминогруппы
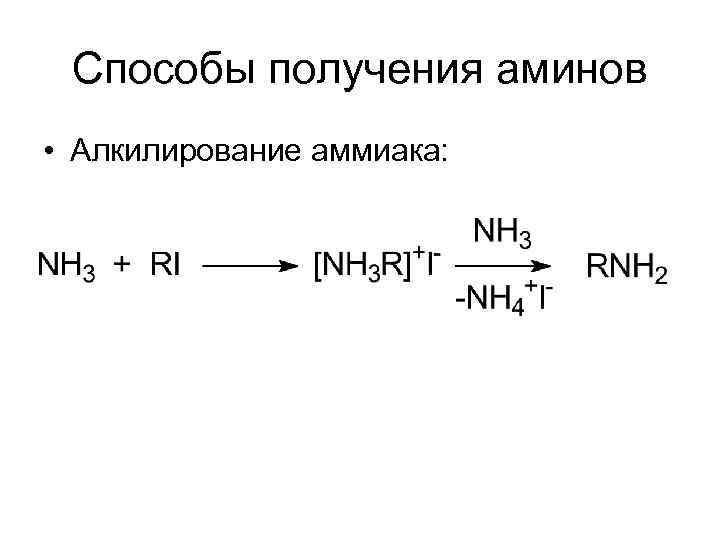 Способы получения аминов • Алкилирование аммиака:
Способы получения аминов • Алкилирование аммиака:
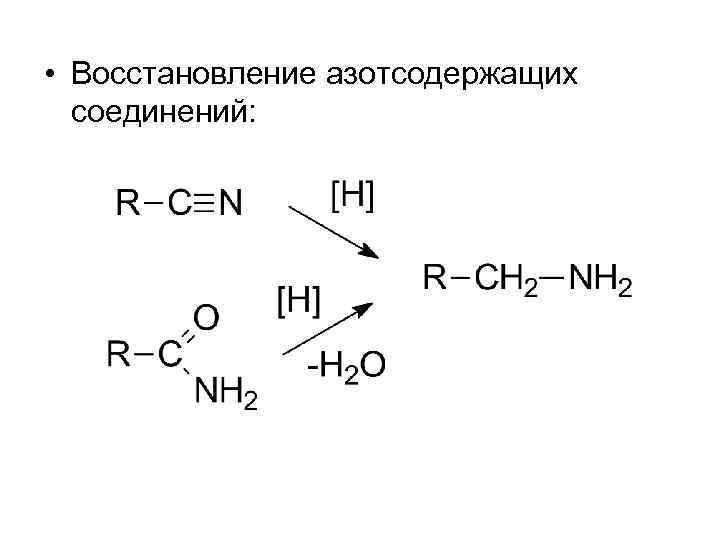 • Восстановление азотсодержащих соединений:
• Восстановление азотсодержащих соединений:
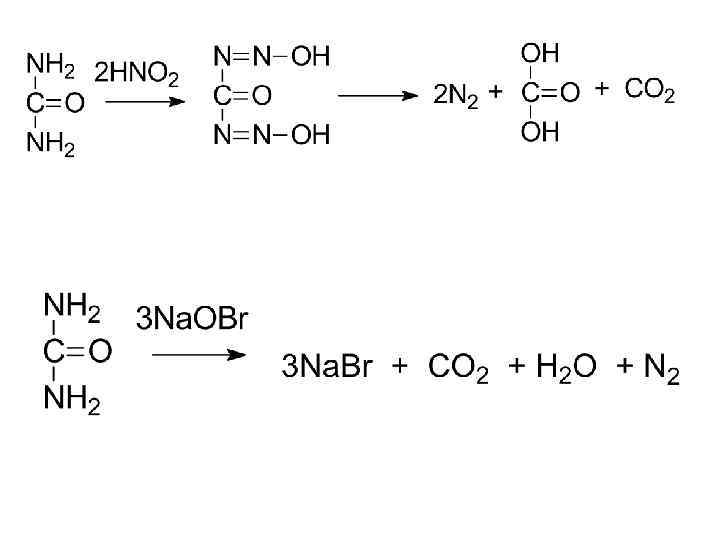
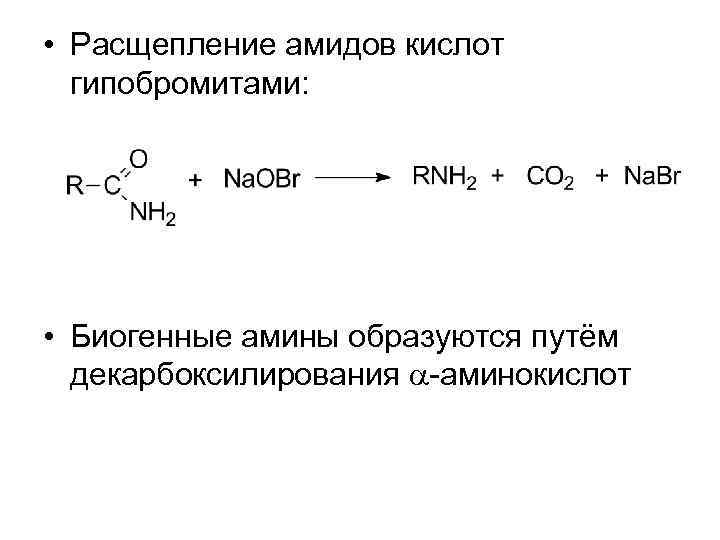 • Расщепление амидов кислот гипобромитами: • Биогенные амины образуются путём декарбоксилирования -аминокислот
• Расщепление амидов кислот гипобромитами: • Биогенные амины образуются путём декарбоксилирования -аминокислот
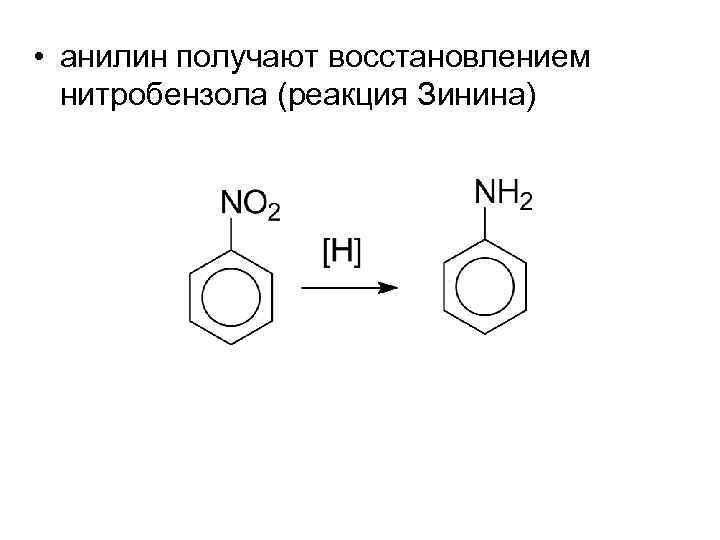 • анилин получают восстановлением нитробензола (реакция Зинина)
• анилин получают восстановлением нитробензола (реакция Зинина)
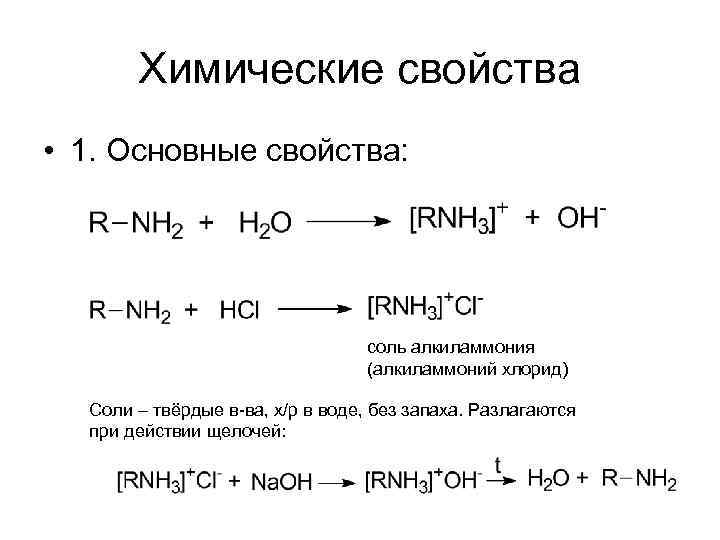 Химические свойства • 1. Основные свойства: соль алкиламмония (алкиламмоний хлорид) Соли – твёрдые в-ва, х/р в воде, без запаха. Разлагаются при действии щелочей:
Химические свойства • 1. Основные свойства: соль алкиламмония (алкиламмоний хлорид) Соли – твёрдые в-ва, х/р в воде, без запаха. Разлагаются при действии щелочей:
 • Амины жирного ряда обладают более выраженными основными свойствами, чем аммиак. • У аминов ароматического ряда основные свойства слабые. Наличие основных свойств доказывается реакцией образования солей при взаимодействии с кислотами: солянокислый анилин
• Амины жирного ряда обладают более выраженными основными свойствами, чем аммиак. • У аминов ароматического ряда основные свойства слабые. Наличие основных свойств доказывается реакцией образования солей при взаимодействии с кислотами: солянокислый анилин
 • 2. Взаимодействие с азотистой кислотой проходит с образованием различных продуктов для аминов разного строения. Это качественная реакция, позволяющая различить первичный, вторичный, третичный амины.
• 2. Взаимодействие с азотистой кислотой проходит с образованием различных продуктов для аминов разного строения. Это качественная реакция, позволяющая различить первичный, вторичный, третичный амины.
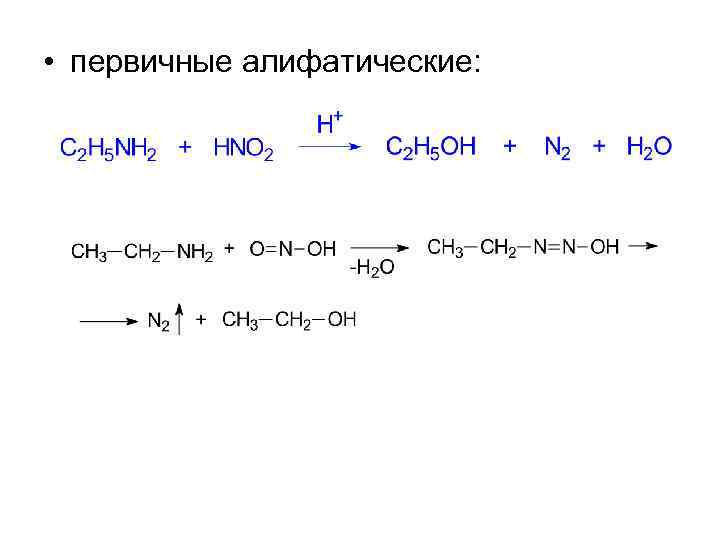 • первичные алифатические:
• первичные алифатические:
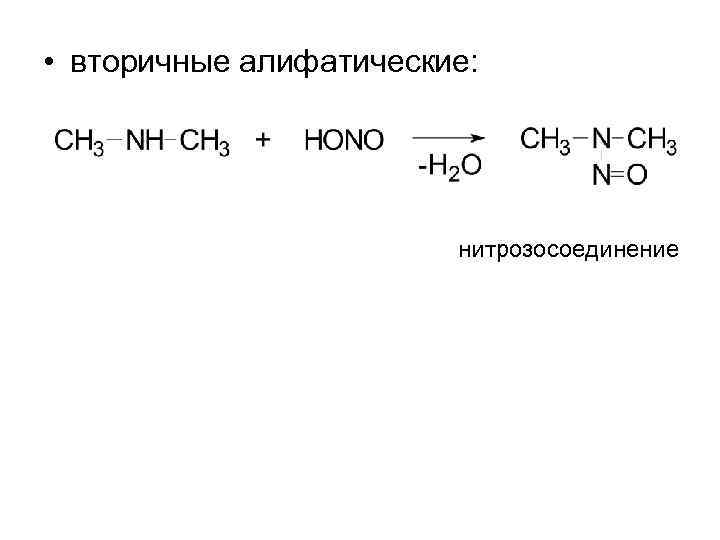 • вторичные алифатические: нитрозосоединение
• вторичные алифатические: нитрозосоединение
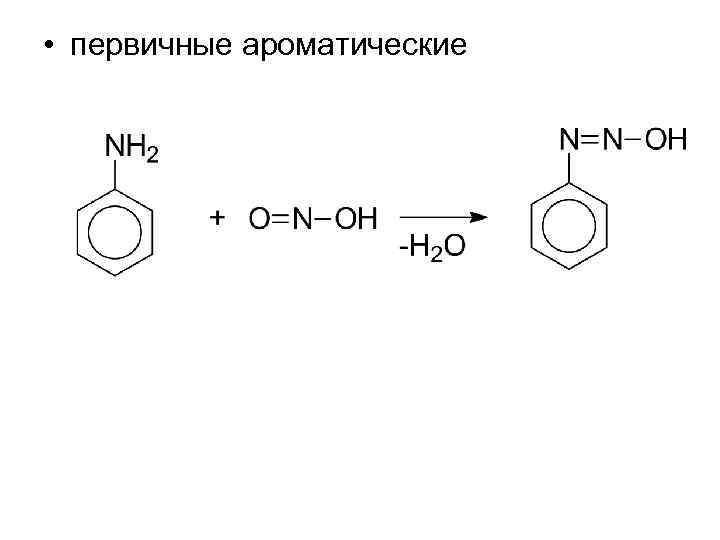 • первичные ароматические
• первичные ароматические
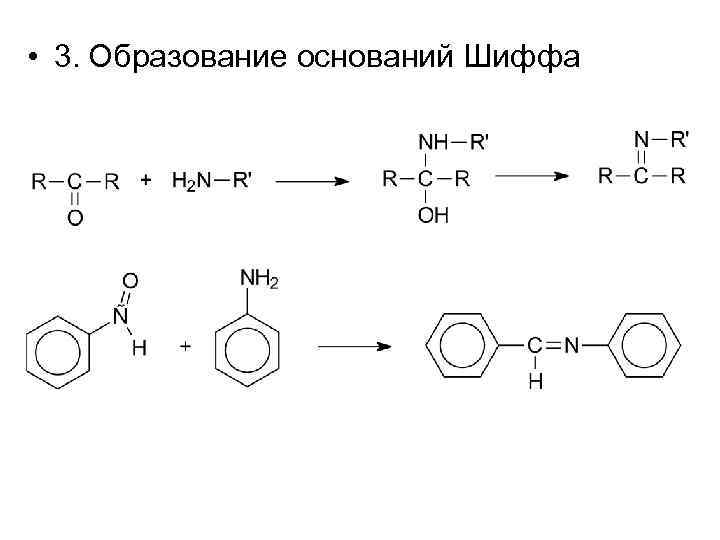 • 3. Образование оснований Шиффа
• 3. Образование оснований Шиффа
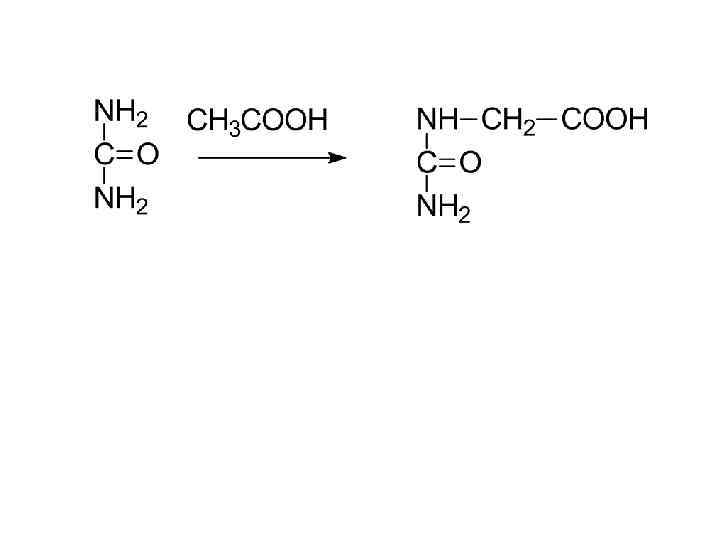
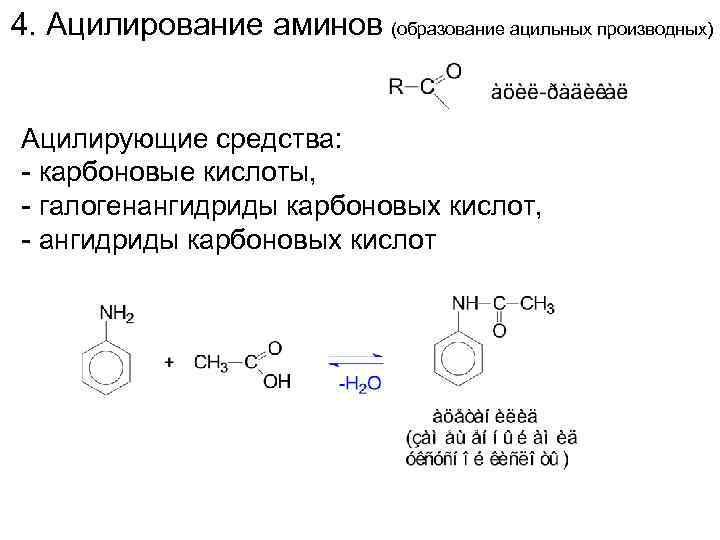 4. Ацилирование аминов (образование ацильных производных) Ацилирующие средства: - карбоновые кислоты, - галогенангидриды карбоновых кислот, - ангидриды карбоновых кислот
4. Ацилирование аминов (образование ацильных производных) Ацилирующие средства: - карбоновые кислоты, - галогенангидриды карбоновых кислот, - ангидриды карбоновых кислот
 5. Реакции электрофильного замещения для ароматических аминов а) галогенирование
5. Реакции электрофильного замещения для ароматических аминов а) галогенирование
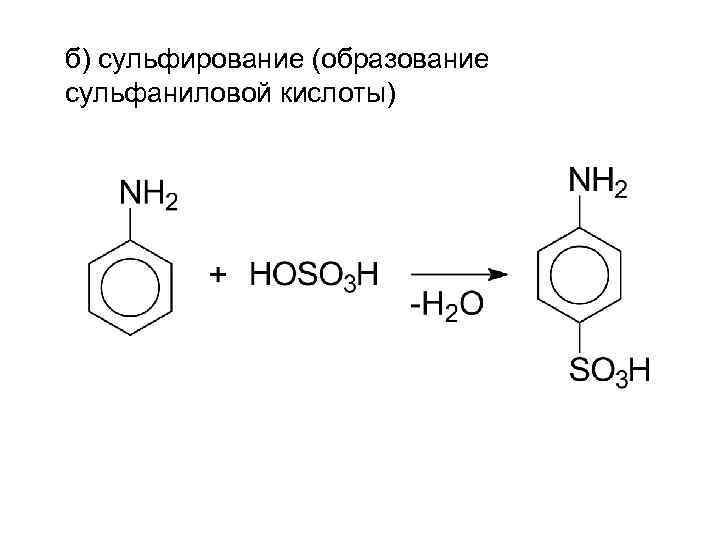 б) сульфирование (образование сульфаниловой кислоты)
б) сульфирование (образование сульфаниловой кислоты)
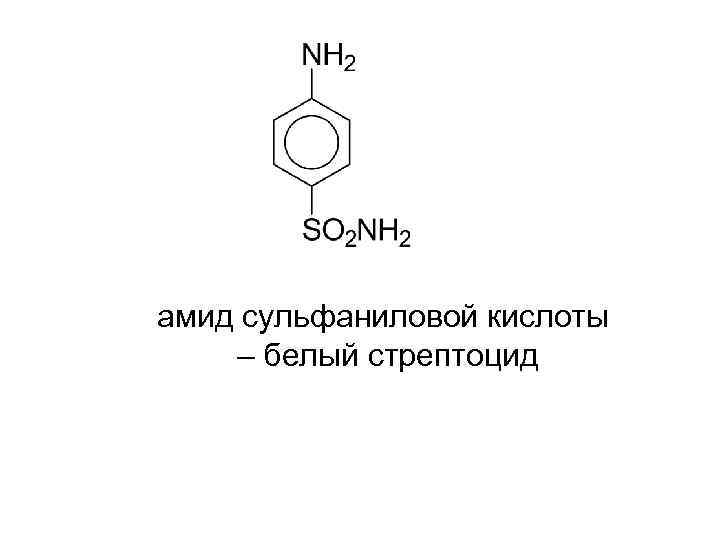 амид сульфаниловой кислоты – белый стрептоцид
амид сульфаниловой кислоты – белый стрептоцид
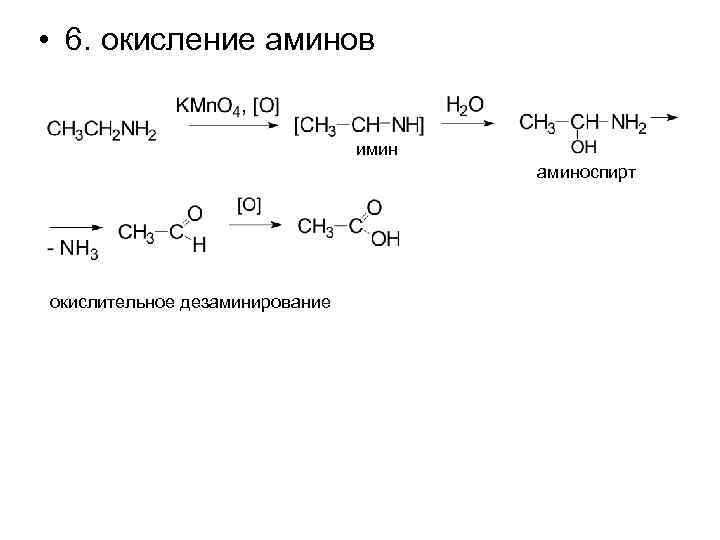 • 6. окисление аминов имин аминоспирт окислительное дезаминирование
• 6. окисление аминов имин аминоспирт окислительное дезаминирование
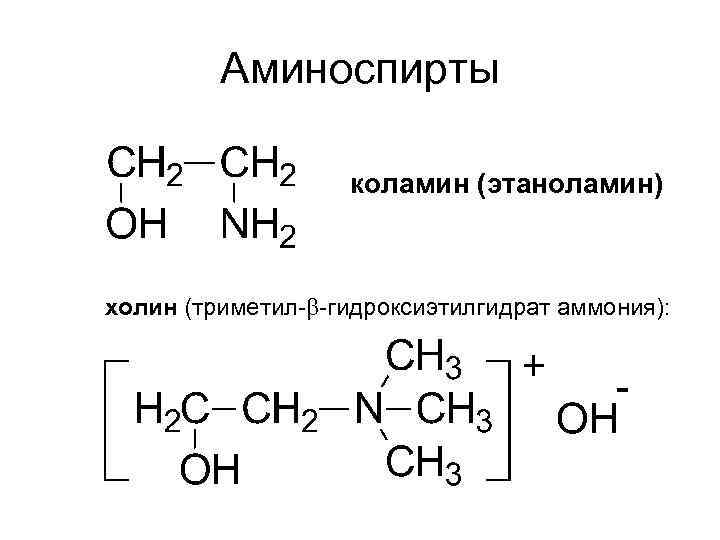 Аминоспирты коламин (этаноламин) холин (триметил- -гидроксиэтилгидрат аммония):
Аминоспирты коламин (этаноламин) холин (триметил- -гидроксиэтилгидрат аммония):
 Амиды кислот • См. лекцию по карбоновым кислотам
Амиды кислот • См. лекцию по карбоновым кислотам
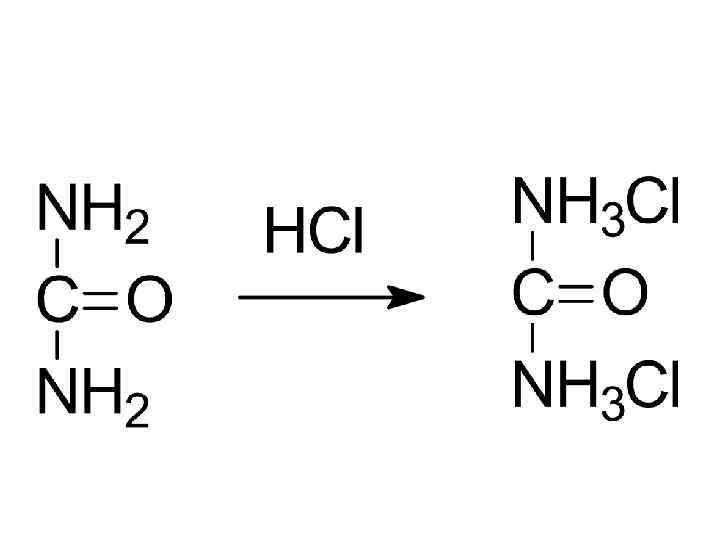
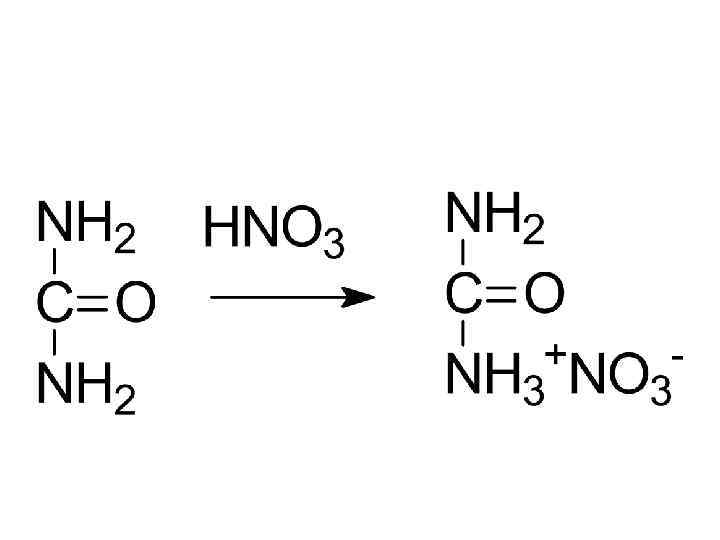
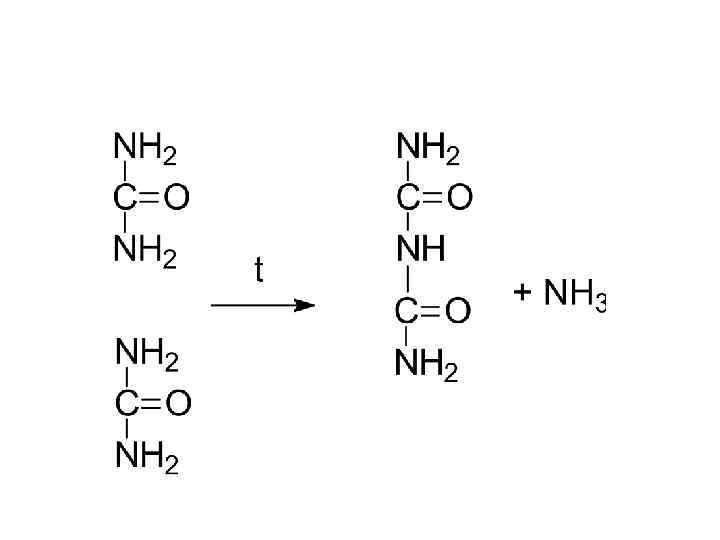
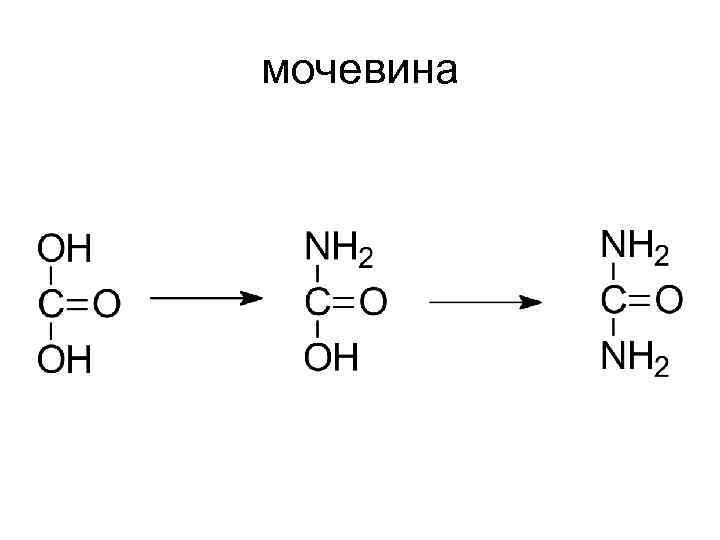 мочевина
мочевина
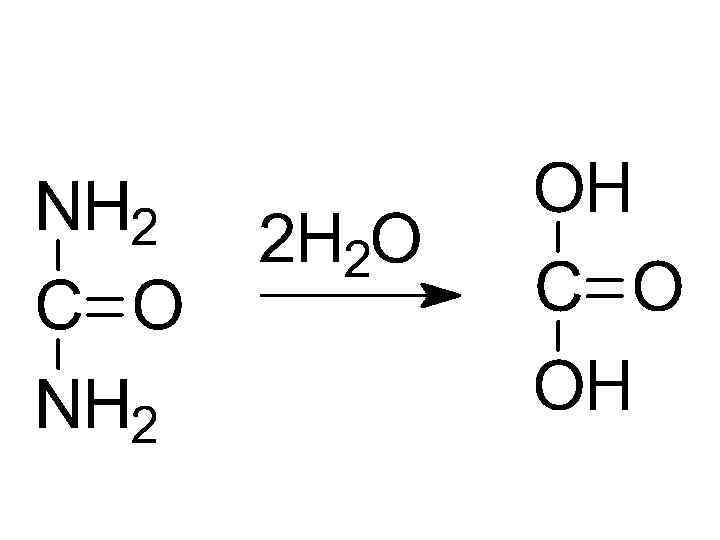
 Гетероциклические соединения. Гетероциклическими называют циклические органические соединения, в состав цикла которых, помимо атомов углерода, входят один или несколько атомов других элементов (гетероатомов).
Гетероциклические соединения. Гетероциклическими называют циклические органические соединения, в состав цикла которых, помимо атомов углерода, входят один или несколько атомов других элементов (гетероатомов).
 Классификационные признаки: • • природа гетероатома число гетероатомов размер цикла степень насыщенности
Классификационные признаки: • • природа гетероатома число гетероатомов размер цикла степень насыщенности
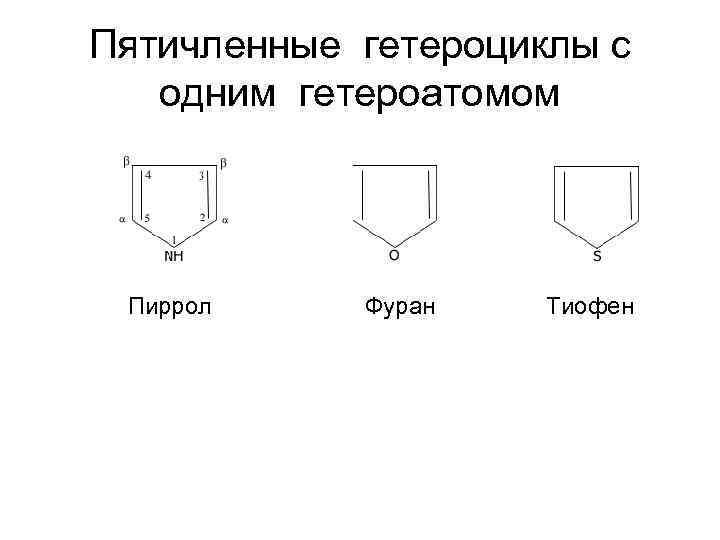 Пятичленные гетероциклы с одним гетероатомом Пиррол Фуран Тиофен
Пятичленные гетероциклы с одним гетероатомом Пиррол Фуран Тиофен
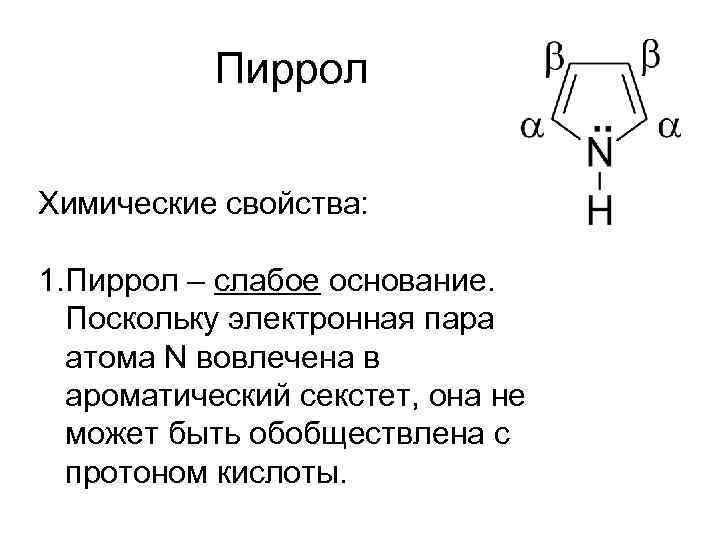 Пиррол Химические свойства: 1. Пиррол – слабое основание. Поскольку электронная пара атома N вовлечена в ароматический секстет, она не может быть обобществлена с протоном кислоты.
Пиррол Химические свойства: 1. Пиррол – слабое основание. Поскольку электронная пара атома N вовлечена в ароматический секстет, она не может быть обобществлена с протоном кислоты.
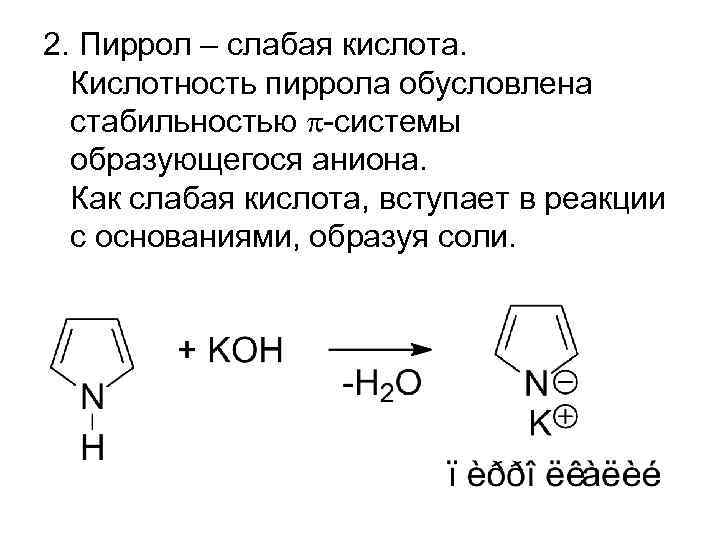 2. Пиррол – слабая кислота. Кислотность пиррола обусловлена стабильностью -системы образующегося аниона. Как слабая кислота, вступает в реакции с основаниями, образуя соли.
2. Пиррол – слабая кислота. Кислотность пиррола обусловлена стабильностью -системы образующегося аниона. Как слабая кислота, вступает в реакции с основаниями, образуя соли.
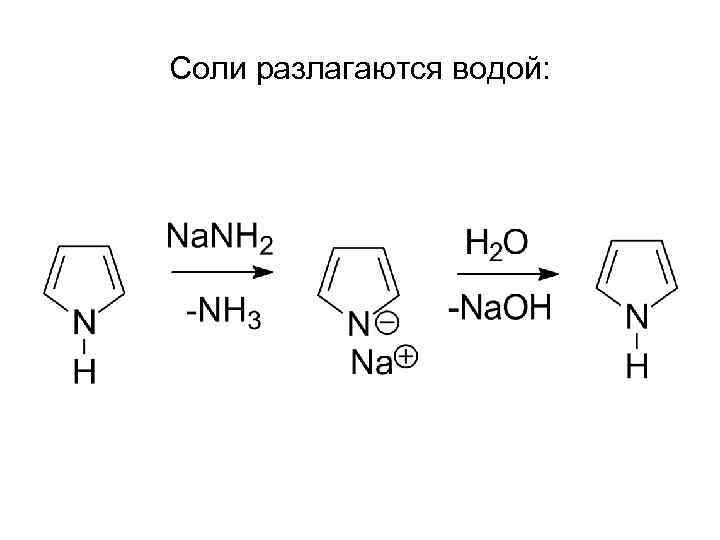 Соли разлагаются водой:
Соли разлагаются водой:
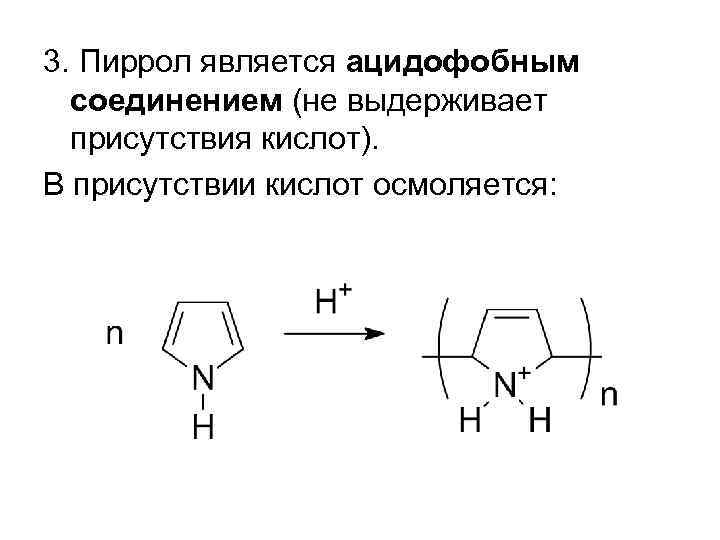 3. Пиррол является ацидофобным соединением (не выдерживает присутствия кислот). В присутствии кислот осмоляется:
3. Пиррол является ацидофобным соединением (не выдерживает присутствия кислот). В присутствии кислот осмоляется:
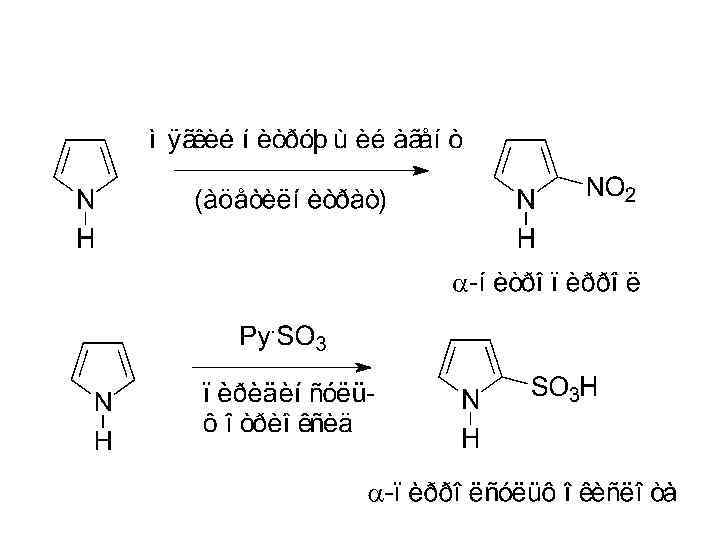
 4. Пиррол, являясь типично ароматическим соединением, вступает в реакции электрофильного замещения. Причём обладает высокой реакционной способностью. Наиболее реакционно способно -положение (гетероатом ЭД-заместитель).
4. Пиррол, являясь типично ароматическим соединением, вступает в реакции электрофильного замещения. Причём обладает высокой реакционной способностью. Наиболее реакционно способно -положение (гетероатом ЭД-заместитель).
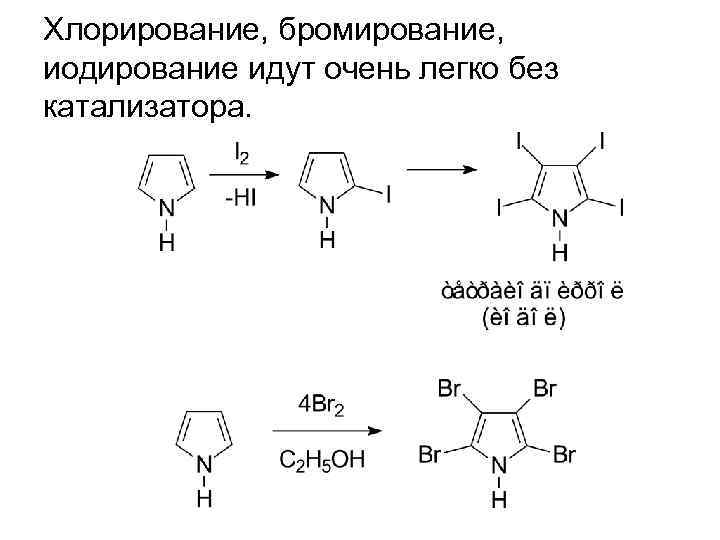 Хлорирование, бромирование, иодирование идут очень легко без катализатора.
Хлорирование, бромирование, иодирование идут очень легко без катализатора.
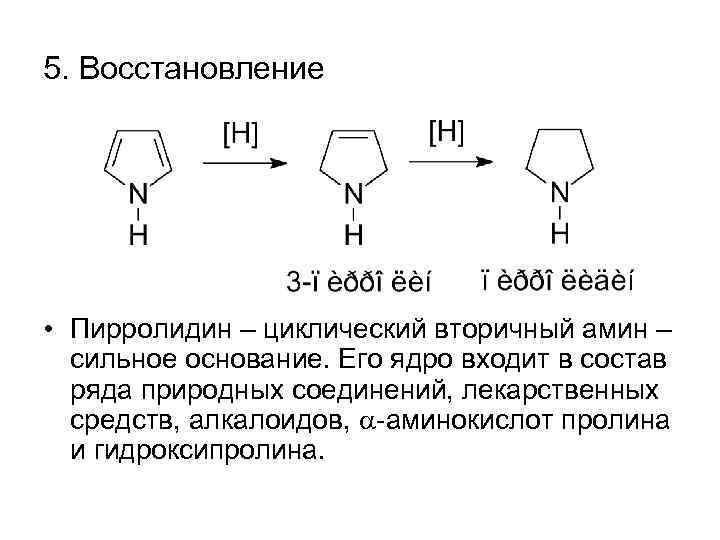 5. Восстановление • Пирролидин – циклический вторичный амин – сильное основание. Его ядро входит в состав ряда природных соединений, лекарственных средств, алкалоидов, -аминокислот пролина и гидроксипролина.
5. Восстановление • Пирролидин – циклический вторичный амин – сильное основание. Его ядро входит в состав ряда природных соединений, лекарственных средств, алкалоидов, -аминокислот пролина и гидроксипролина.
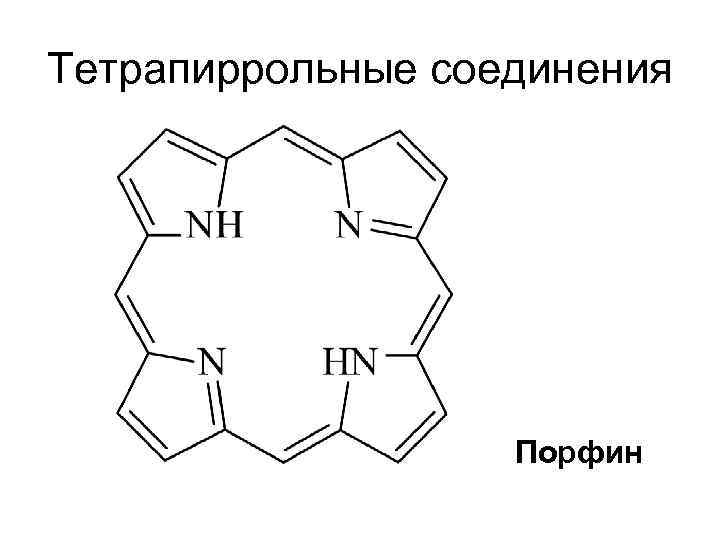 Тетрапиррольные соединения Порфин
Тетрапиррольные соединения Порфин
 Гем
Гем
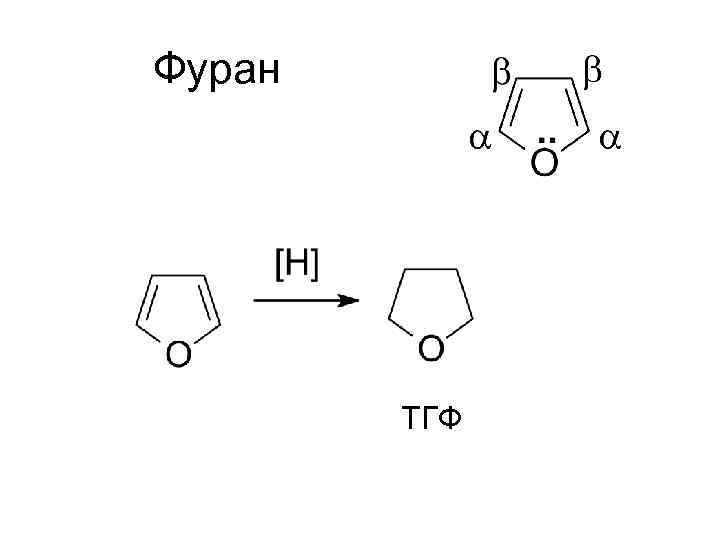 Фуран ТГФ
Фуран ТГФ
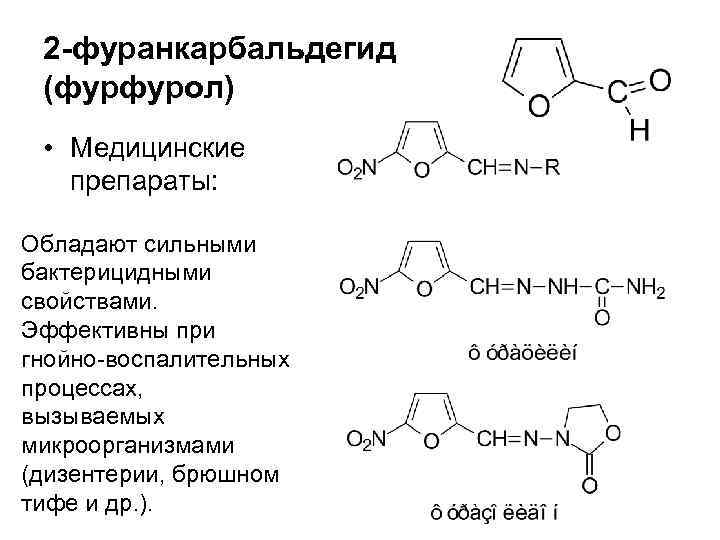 2 -фуранкарбальдегид (фурфурол) • Медицинские препараты: Обладают сильными бактерицидными свойствами. Эффективны при гнойно-воспалительных процессах, вызываемых микроорганизмами (дизентерии, брюшном тифе и др. ).
2 -фуранкарбальдегид (фурфурол) • Медицинские препараты: Обладают сильными бактерицидными свойствами. Эффективны при гнойно-воспалительных процессах, вызываемых микроорганизмами (дизентерии, брюшном тифе и др. ).
 От слова фуран происходит название циклической формы моносахаридов. Например: Рибоза – рибофураноза, Глюкоза – глюкофураноза.
От слова фуран происходит название циклической формы моносахаридов. Например: Рибоза – рибофураноза, Глюкоза – глюкофураноза.
 Тиофен Производные тиофена входят в состав ихтиоловой мази (противовоспалительное, антисептическое, местное обезболивающее действие). Тетрагидротиофеновое кольцо входит в состав витамина Н – биотина. Отсутствие биотина в пище приводит к нарушению обмена белков и жиров в организме и ведёт к кожным заболеваниям.
Тиофен Производные тиофена входят в состав ихтиоловой мази (противовоспалительное, антисептическое, местное обезболивающее действие). Тетрагидротиофеновое кольцо входит в состав витамина Н – биотина. Отсутствие биотина в пище приводит к нарушению обмена белков и жиров в организме и ведёт к кожным заболеваниям.
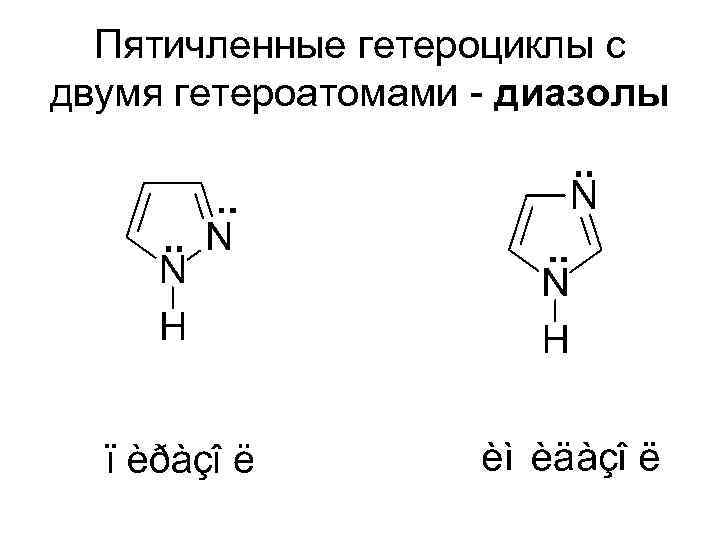 Пятичленные гетероциклы с двумя гетероатомами - диазолы
Пятичленные гетероциклы с двумя гетероатомами - диазолы
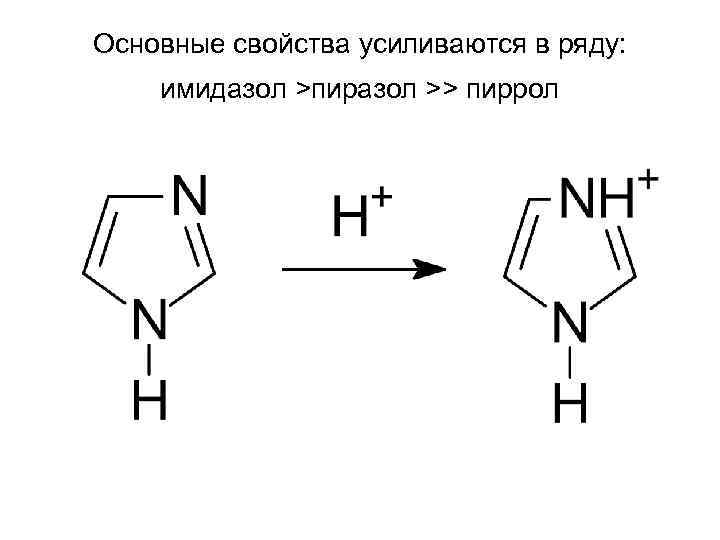 Основные свойства усиливаются в ряду: имидазол >пиразол >> пиррол
Основные свойства усиливаются в ряду: имидазол >пиразол >> пиррол
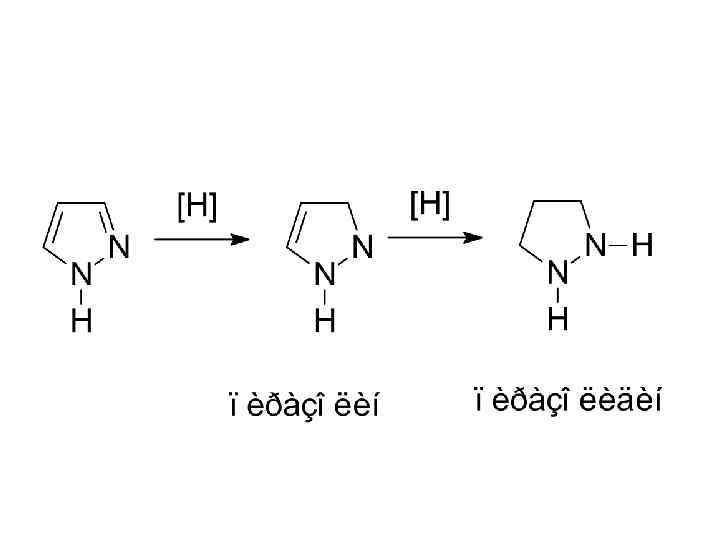
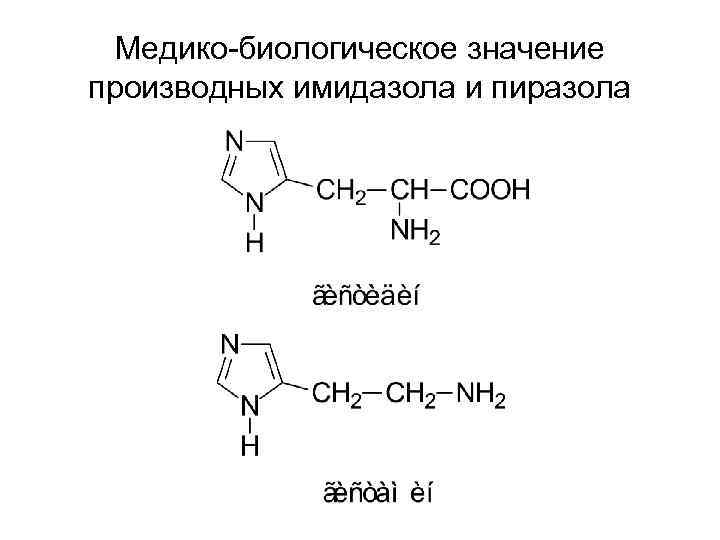 Медико-биологическое значение производных имидазола и пиразола
Медико-биологическое значение производных имидазола и пиразола


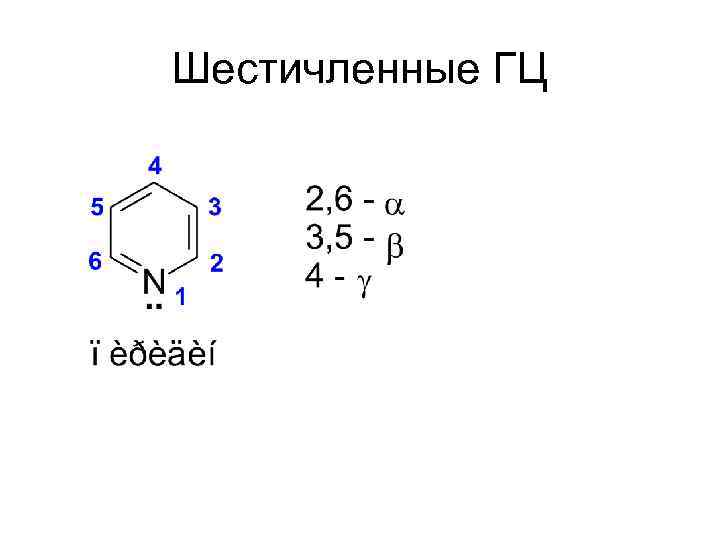 Шестичленные ГЦ
Шестичленные ГЦ
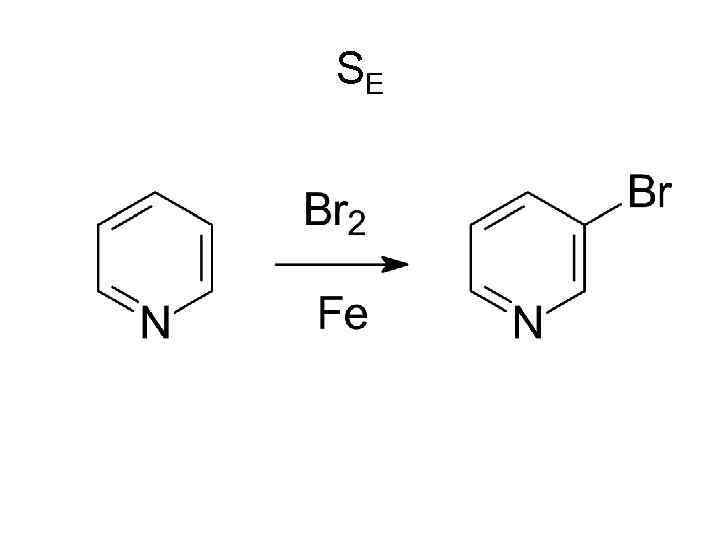 SE
SE
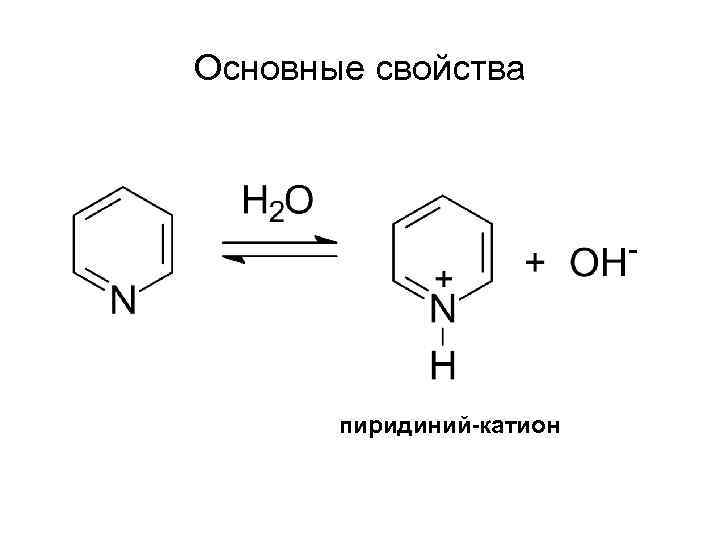 Основные свойства пиридиний-катион
Основные свойства пиридиний-катион
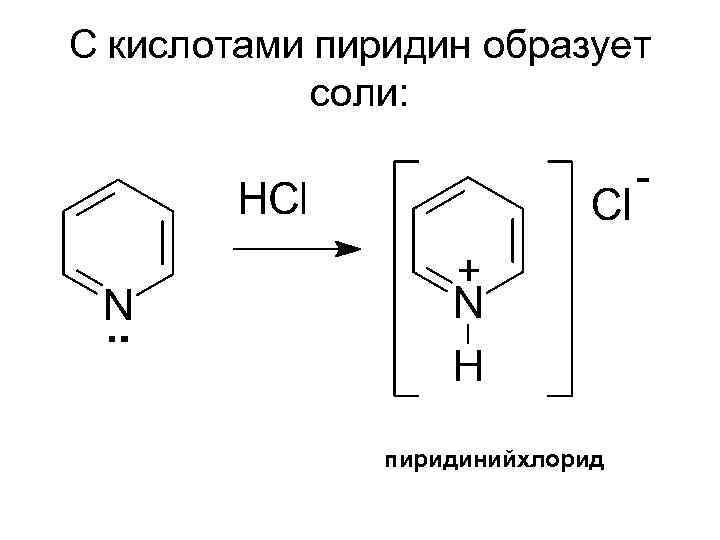 С кислотами пиридин образует соли: пиридинийхлорид
С кислотами пиридин образует соли: пиридинийхлорид
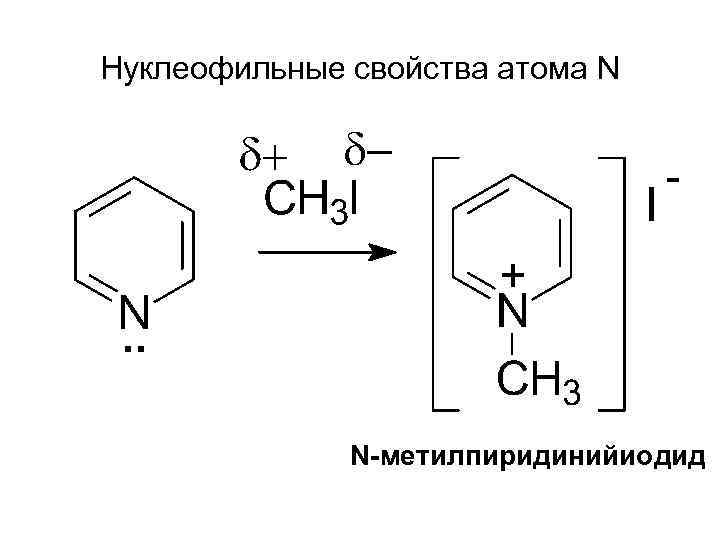 Нуклеофильные свойства атома N N-метилпиридинийиодид
Нуклеофильные свойства атома N N-метилпиридинийиодид
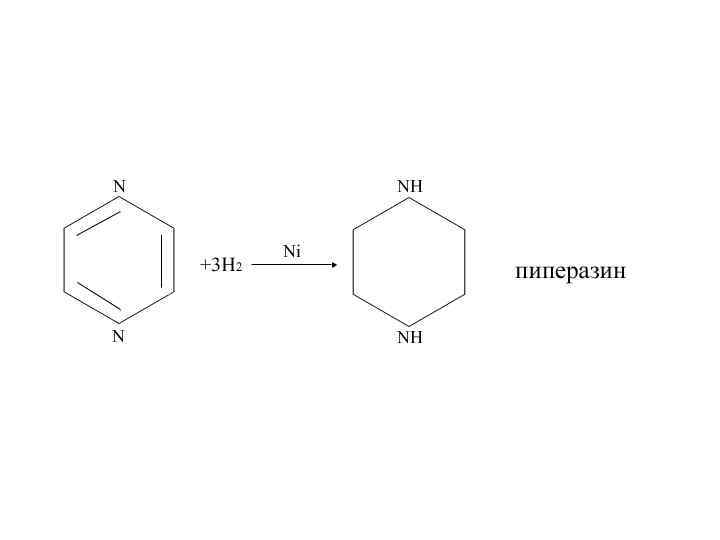
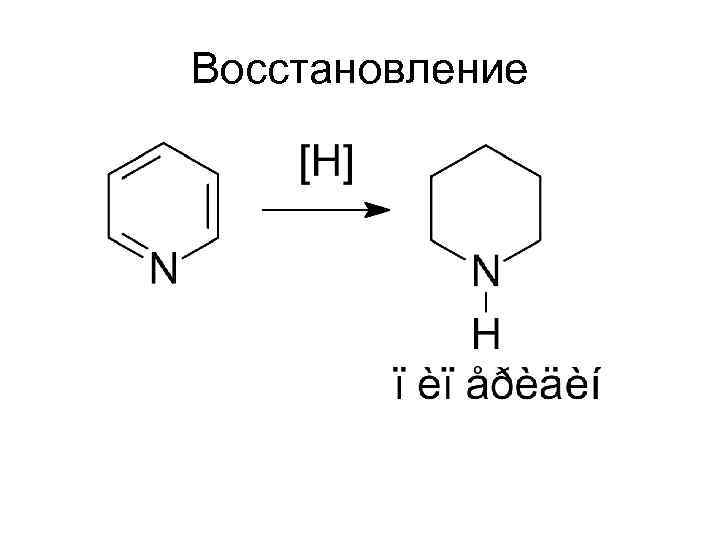 Восстановление
Восстановление
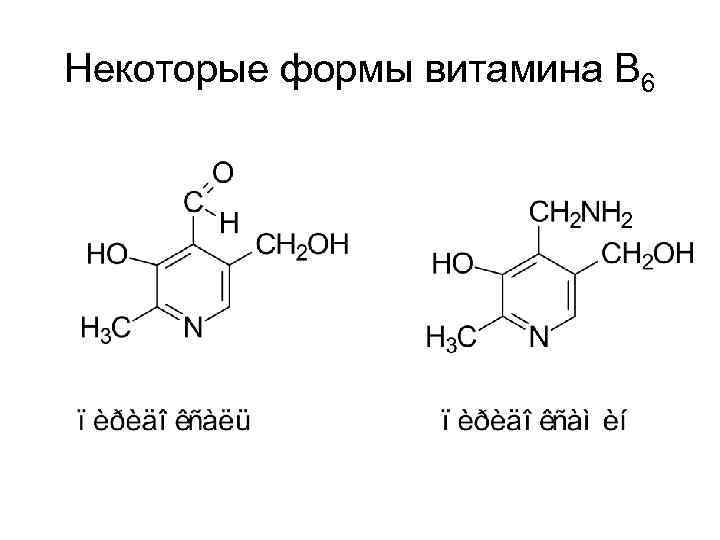 Некоторые формы витамина В 6
Некоторые формы витамина В 6
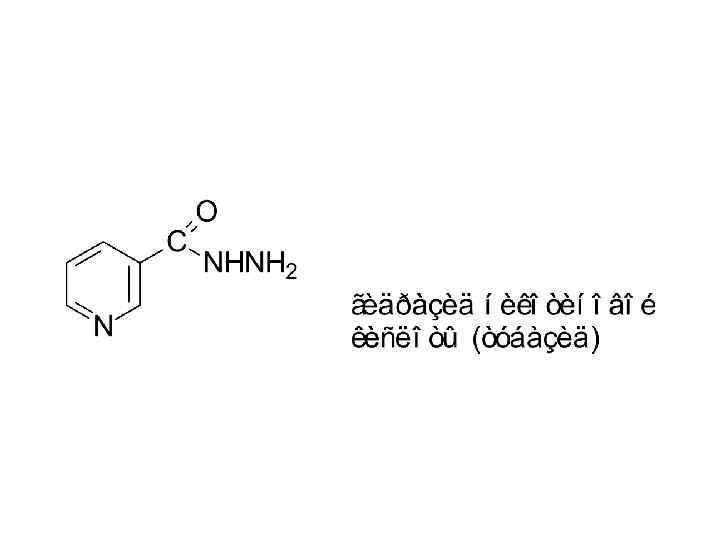
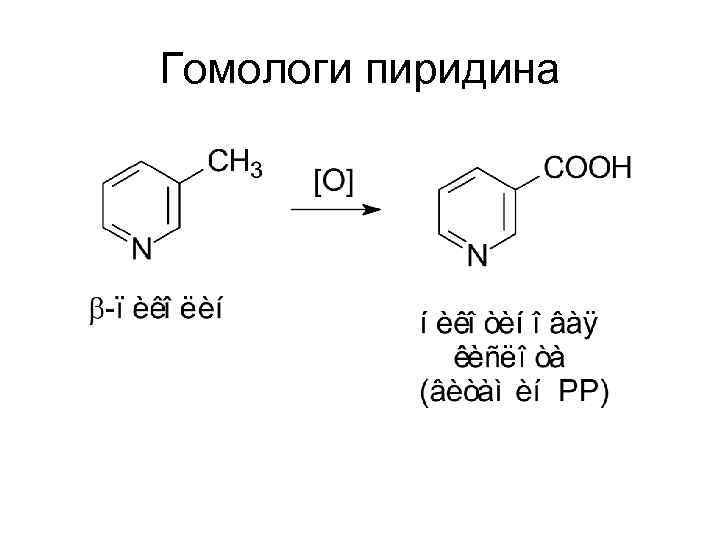 Гомологи пиридина
Гомологи пиридина
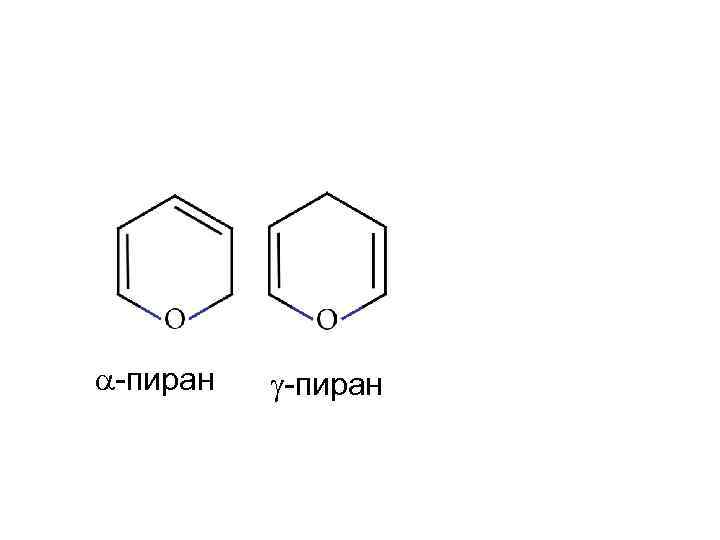 -пиран
-пиран
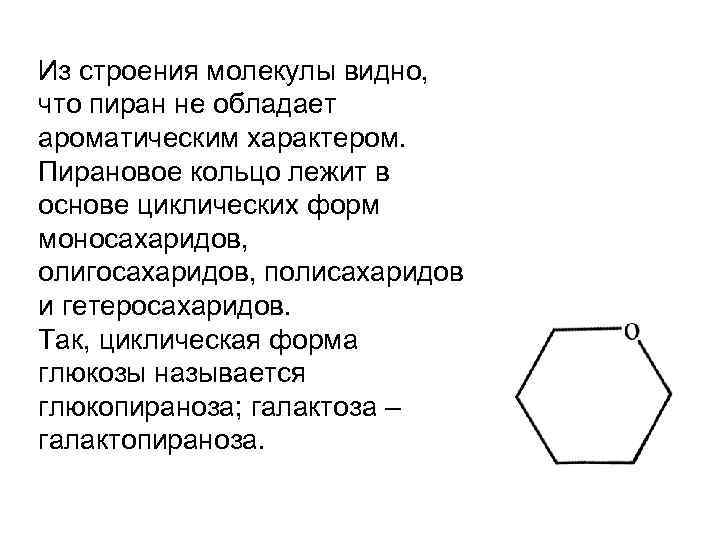 Из строения молекулы видно, что пиран не обладает ароматическим характером. Пирановое кольцо лежит в основе циклических форм моносахаридов, олигосахаридов, полисахаридов и гетеросахаридов. Так, циклическая форма глюкозы называется глюкопираноза; галактоза – галактопираноза.
Из строения молекулы видно, что пиран не обладает ароматическим характером. Пирановое кольцо лежит в основе циклических форм моносахаридов, олигосахаридов, полисахаридов и гетеросахаридов. Так, циклическая форма глюкозы называется глюкопираноза; галактоза – галактопираноза.
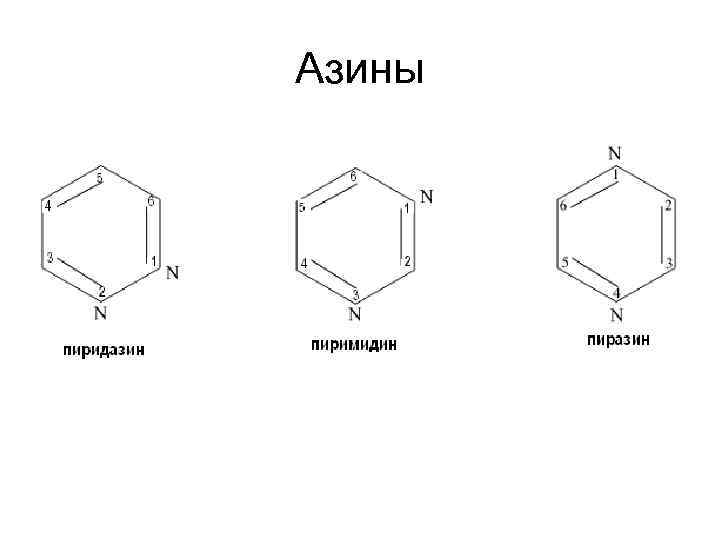 Азины
Азины
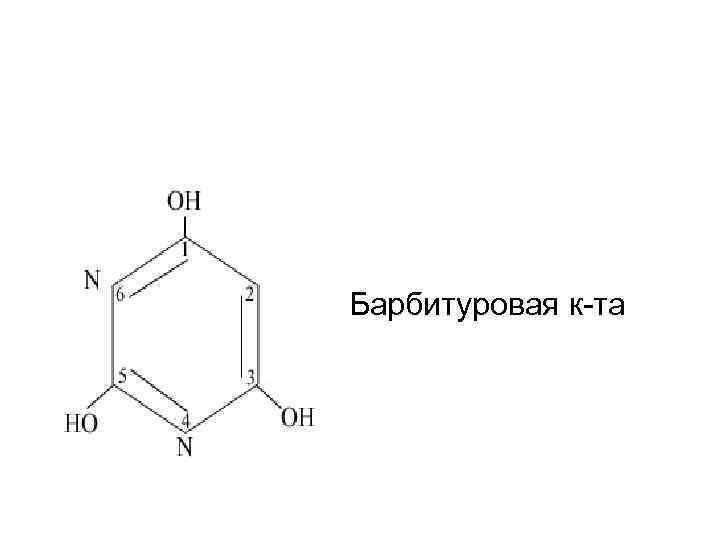 Барбитуровая к-та
Барбитуровая к-та
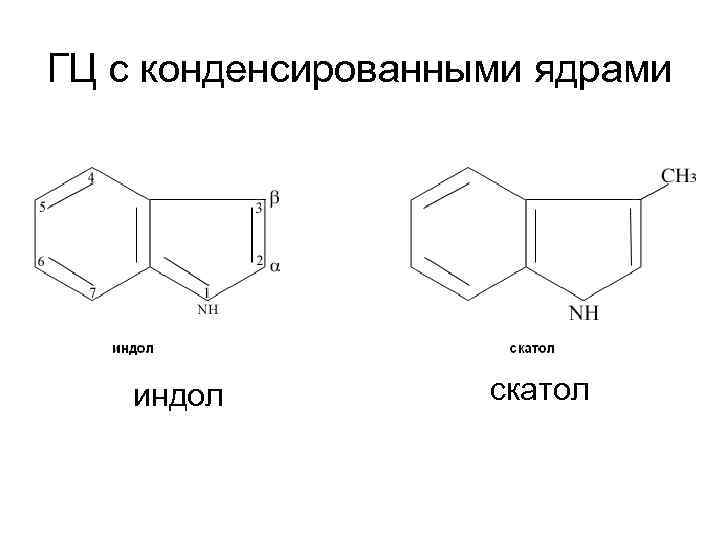 ГЦ с конденсированными ядрами индол скатол
ГЦ с конденсированными ядрами индол скатол
 триптофан
триптофан
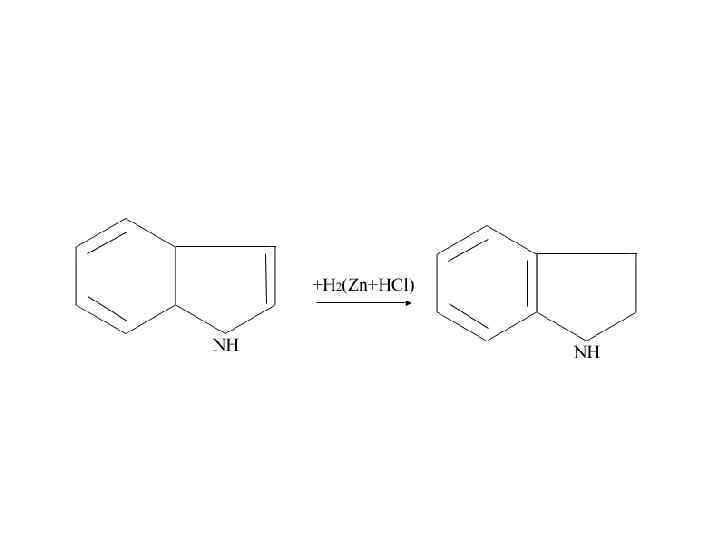
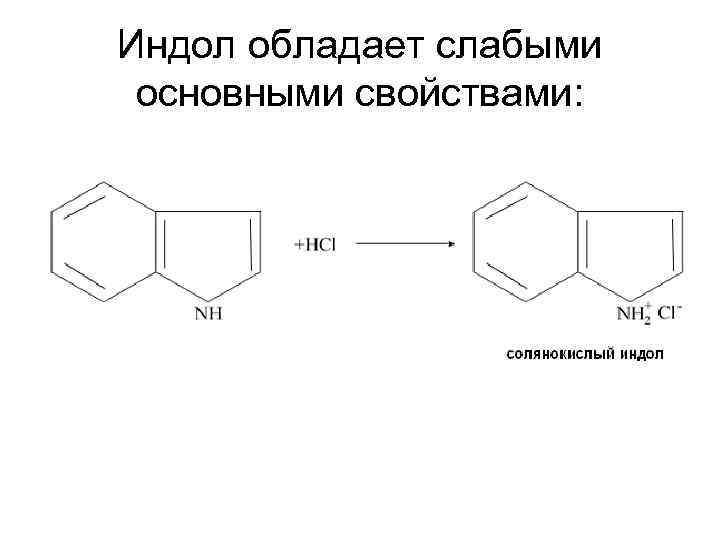 Индол обладает слабыми основными свойствами:
Индол обладает слабыми основными свойствами:

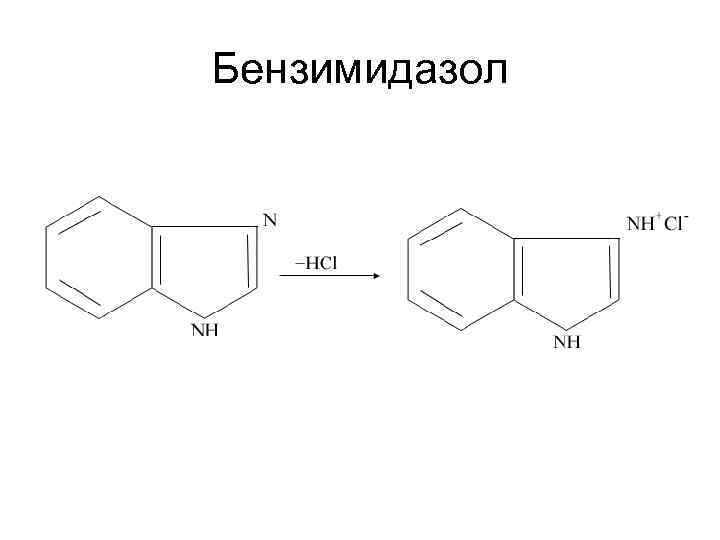 Бензимидазол
Бензимидазол
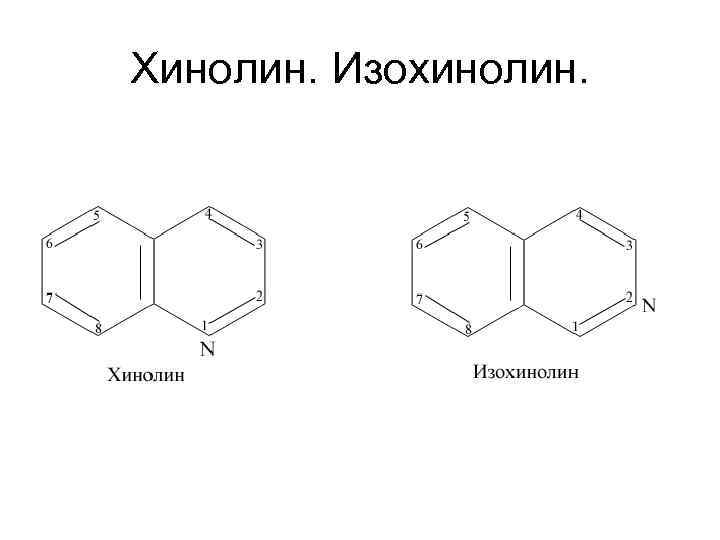 Хинолин. Изохинолин.
Хинолин. Изохинолин.
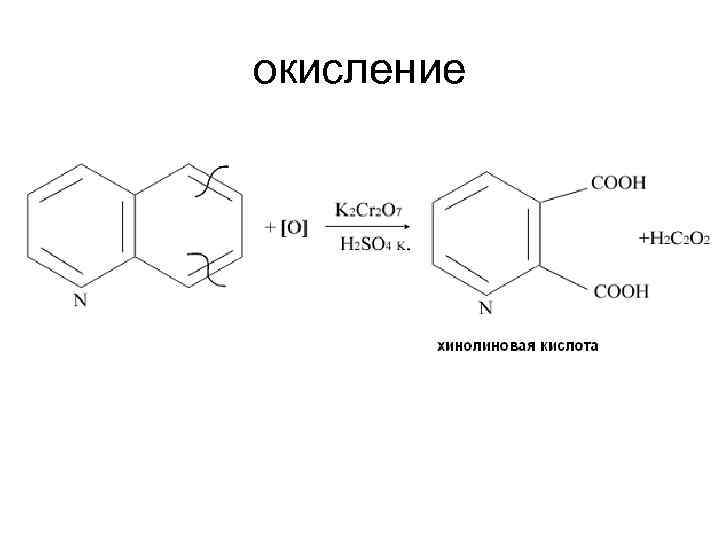 окисление
окисление
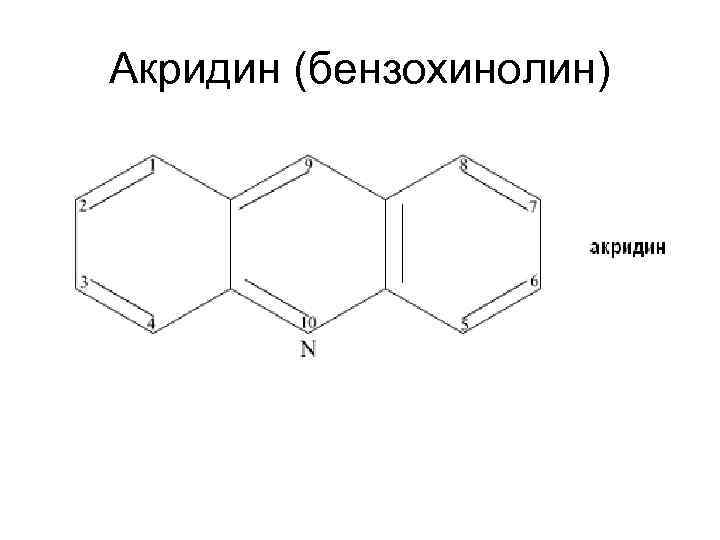 Акридин (бензохинолин)
Акридин (бензохинолин)
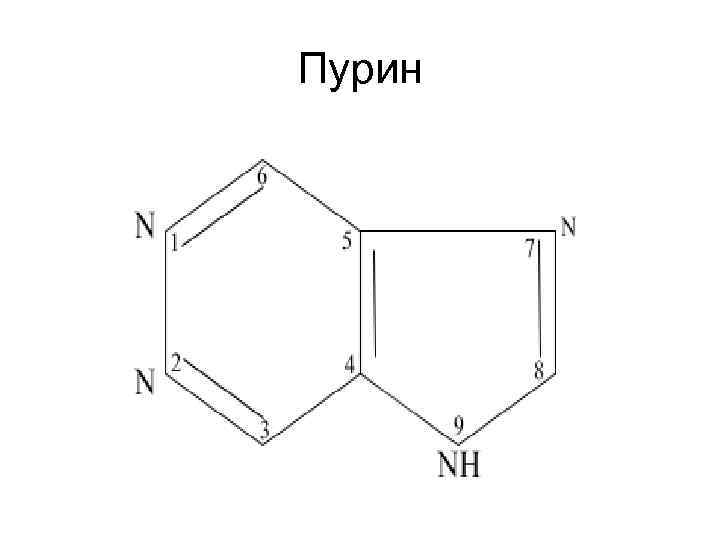 Пурин
Пурин
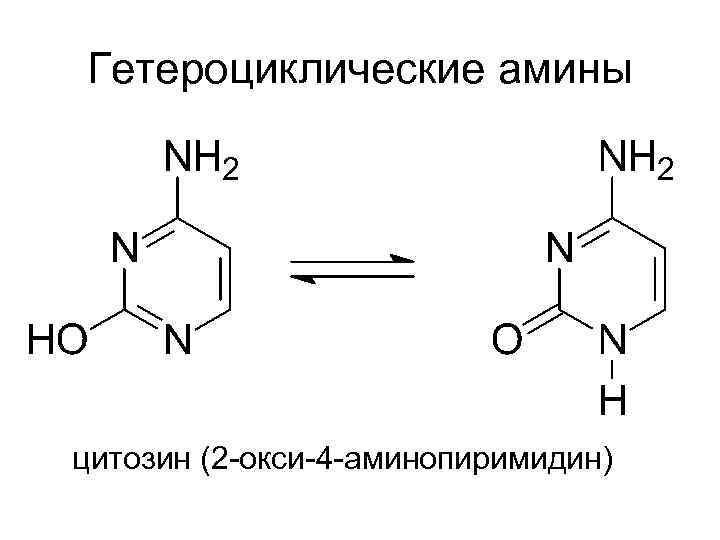 Гетероциклические амины цитозин (2 -окси-4 -аминопиримидин)
Гетероциклические амины цитозин (2 -окси-4 -аминопиримидин)
 аденин (6 -аминопурин) гуанин (2 -амино-6 -оксипурин)
аденин (6 -аминопурин) гуанин (2 -амино-6 -оксипурин)
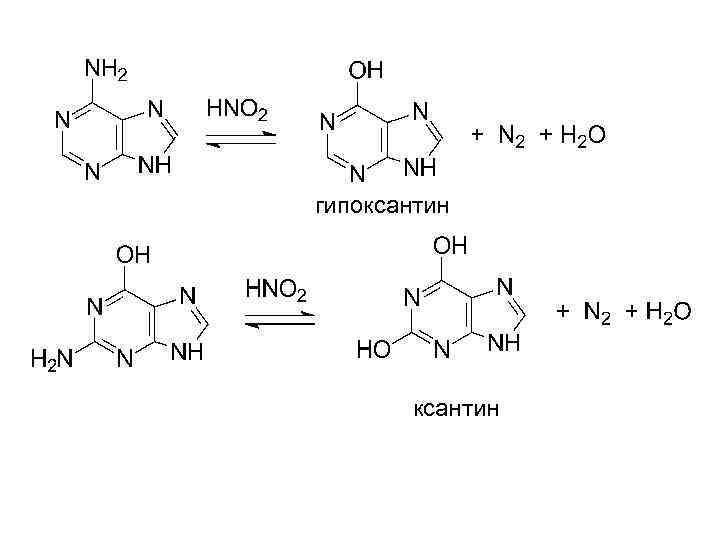 гипоксантин
гипоксантин


