9 - Производство азотных удобрений.pptx
- Количество слайдов: 61

Азотные удобрения

Характеристика азотных удобрений Азотные удобрения содержат азот в форме свободного аммиака и аминов (аммиакаты), ионов NH 4+ и NO 3–, аминогруппы NH 2, а также в их сочетании. В соответствии с этим различают следующие виды азотных удобрений: Ø аммиачные; Ø аммонийные; Ø нитратные; Ø амидные; Ø аммонийно-нитратные. Все азотные удобрения хорошо растворимы в воде и хорошо усваиваются растениями. По агрегатному состоянию азотные удобрения делятся на твёрдые и жидкие.
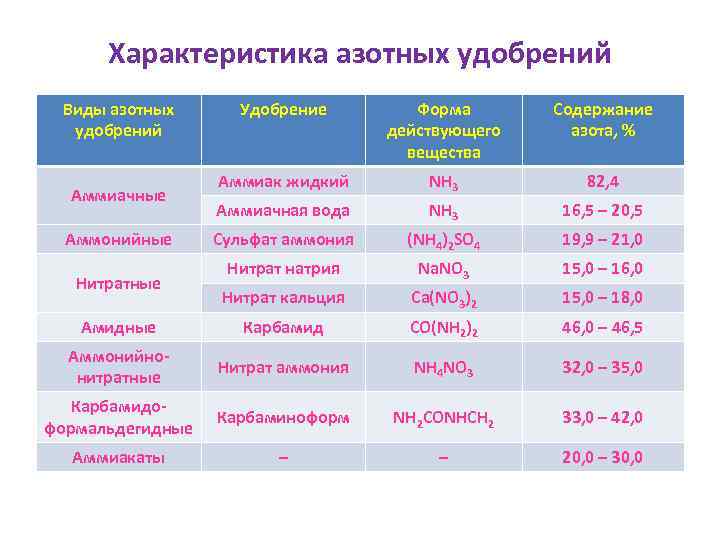
Характеристика азотных удобрений Виды азотных удобрений Удобрение Форма действующего вещества Содержание азота, % Аммиак жидкий NH 3 82, 4 Аммиачная вода NH 3 16, 5 – 20, 5 Сульфат аммония (NH 4)2 SO 4 19, 9 – 21, 0 Нитрат натрия Na. NO 3 15, 0 – 16, 0 Нитрат кальция Ca(NO 3)2 15, 0 – 18, 0 Амидные Карбамид CO(NH 2)2 46, 0 – 46, 5 Аммонийнонитратные Нитрат аммония NH 4 NO 3 32, 0 – 35, 0 Карбамидоформальдегидные Карбаминоформ NH 2 CONHCH 2 33, 0 – 42, 0 Аммиакаты – – 20, 0 – 30, 0 Аммиачные Аммонийные Нитратные

Производство аммиачной селитры

Свойства аммиачной селитры Нитрат аммония NH 4 NO 3 – кристаллическое вещество с температурой плавления 169, 6 0 С, хорошо растворяется в воде. Нитрат аммония сильно гигроскопичен и легко поглощает влагу из атмосферы. В зависимости от температуры может существовать в пяти кристаллических модификациях, различающихся плотностью и структурой кристаллов. Вследствие высокой растворимости в воде, гигроскопичности и полиморфных превращений, сопровождающихся выделением тепла, нитрат аммония легко слёживается.

Свойства аммиачной селитры Для уменьшения слёживаемости в промышленности используют следующие меры: Ø перед складированием полученный продукт охлаждают до температуры ниже 32 0 С, так как в интервале температур от 32 0 С до – 17 0 С нитрат аммония находится в стабильной ромбической модификации; Ø выпускают товарный продукт в гранулированном виде, обрабатывая поверхность гранул ПАВ, образующими на них гидрофобную плёнку; Ø вводят в состав продукта кондиционирующие добавки в виде нитрата магния и других солей, которые связывают свободную воду и препятствуют переходу одной модификации в другую.

Свойства аммиачной селитры Нитрат аммония в твёрдом состоянии или в виде плава при нагревании выше 180 – 200 0 С разлагается по реакции: NH 4 NO 3 = N 2 O + 2 H 2 O + 37 к. Дж При быстром нагревании в замкнутом пространстве до 400 – 500 0 С или инициировании нитрат аммония разлагается со взрывом по реакции: NH 4 NO 3 = N 2 + 2 H 2 O + 1/2 O 2 + 118 к. Дж Разложение ускоряется в присутствии минеральных кислот и органических веществ. На этом свойстве основано применение нитрата аммония для производства взрывчатых веществ. Нитрат аммония является безбалластным азотным удобрением и содержит 34, 8 % азота, из них на аммонийную и нитратную формы приходится по 17, 4 %.

Физико-химические основы процесса Производство нитрата аммония основано на реакции нейтрализации азотной кислоты газообразным аммиаком с последующим упариванием полученного раствора. Нейтрализация азотной кислоты аммиаком – необратимый гетерогенный процесс хемосорбции, протекающий по реакции: HNO 3 + NH 3 = NH 4 NO 3 + 145 к. Дж Реакция идёт в диффузионной области и её скорость лимитируется диффузией аммиака из газа к поверхности жидкости.
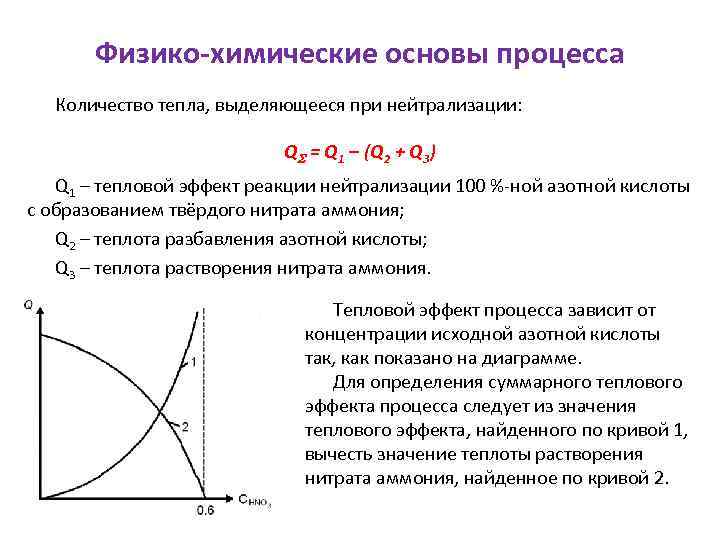
Физико-химические основы процесса Количество тепла, выделяющееся при нейтрализации: QS = Q 1 – (Q 2 + Q 3) Q 1 – тепловой эффект реакции нейтрализации 100 %-ной азотной кислоты с образованием твёрдого нитрата аммония; Q 2 – теплота разбавления азотной кислоты; Q 3 – теплота растворения нитрата аммония. Тепловой эффект процесса зависит от концентрации исходной азотной кислоты так, как показано на диаграмме. Для определения суммарного теплового эффекта процесса следует из значения теплового эффекта, найденного по кривой 1, вычесть значение теплоты растворения нитрата аммония, найденное по кривой 2.

Физико-химические основы процесса В результате нейтрализации образуется водный раствор нитрата аммония. При этом за счёт теплового эффекта реакции нейтрализации часть воды испаряется в виде сокового пара. Интенсивность испарения зависит от величины теплового эффекта и температуры процесса. Поэтому, концентрация образующегося раствора определяется как концентрацией азотной кислоты, так и температурой. Для испарения воды и концентрирования раствора нитрата аммония можно использовать как внешнее тепло, так и тепло нейтрализации:

Физико-химические основы процесса Использование теплоты нейтрализации для упаривания раствора позволяет: Ø снизить затраты внешнего тепла; Ø обеспечить за счёт отвода тепла из системы оптимальный температурный режим процесса нейтрализации и избежать опасных перегревов; Ø исключить применение сложных охладительных устройств.

Физико-химические основы процесса Возможны следующие принципиально различные схемы получения аммиачной селитры с использованием тепла нейтрализации: Ø установки, работающие при атмосферном давлении (избыточное давление сокового пара 0, 15 - 0, 2 ат); Ø установки с вакуум-испарителем; Ø установки, работающие под давлением, с однократным использованием тепла сокового пара; Ø установки, работающие под давлением, с двукратным использованием тепла сокового пара (получение концентрированного плава). В промышленной практике нашли широкое применение как наиболее эффективные установки, работающие при атмосферном давлении, с использованием тепла нейтрализации и частично установки с вакуум-испарителем.
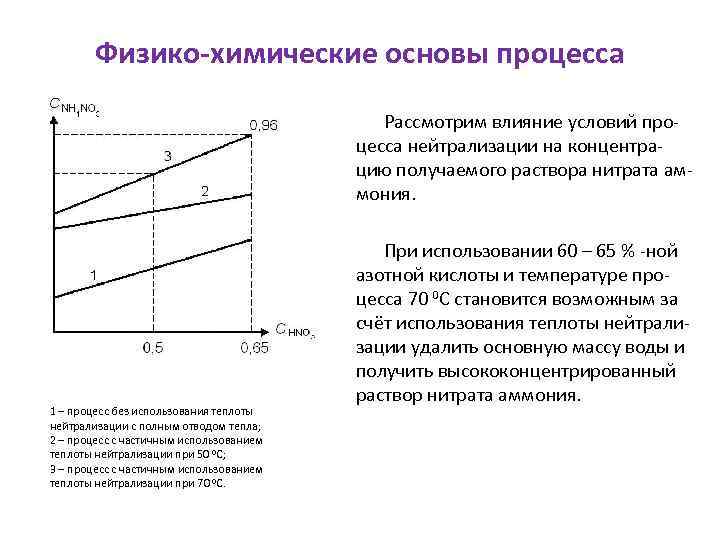
Физико-химические основы процесса Рассмотрим влияние условий процесса нейтрализации на концентрацию получаемого раствора нитрата аммония. 1 – процесс без использования теплоты нейтрализации с полным отводом тепла; 2 – процесс с частичным использованием теплоты нейтрализации при 50 0 С; 3 – процесс с частичным использованием теплоты нейтрализации при 70 0 С. При использовании 60 – 65 % -ной азотной кислоты и температуре процесса 70 0 С становится возможным за счёт использования теплоты нейтрализации удалить основную массу воды и получить высококонцентрированный раствор нитрата аммония.

Физико-химические основы процесса В соответствии с принципом использования тепла все существующие варианты технологического процесса производства нитрата аммония под -разделяются на две группы. 1 группа – без упаривания раствора Концентрирование раствора осуществляется исключительно за счёт теплоты нейтрализации 65 %-ной азотной кислоты. При этом образуется 96 %-ный плав нитрата аммония. 2 группа – с упариванием раствора Концентрирование раствора осуществляется как за счёт частичного использования теплоты нейтрализации, так и за счёт внешнего тепла. При этом, в зависимости от концентрации азотной кислоты упаривание раствора нитрата аммония осуществляется: при 58 %-ной кислоте в одну ступень; при 50 %-ной кислоте в две ступени.
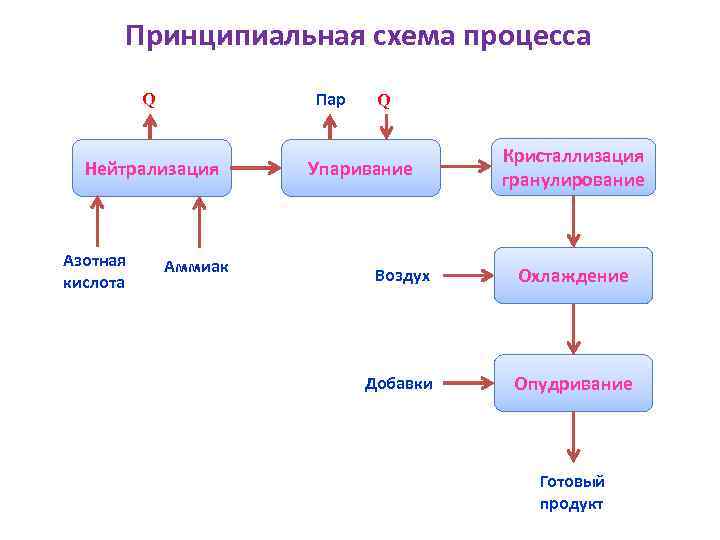
Принципиальная схема процесса Пар Q Нейтрализация Азотная кислота Аммиак Q Упаривание Кристаллизация гранулирование Воздух Охлаждение Добавки Опудривание Готовый продукт
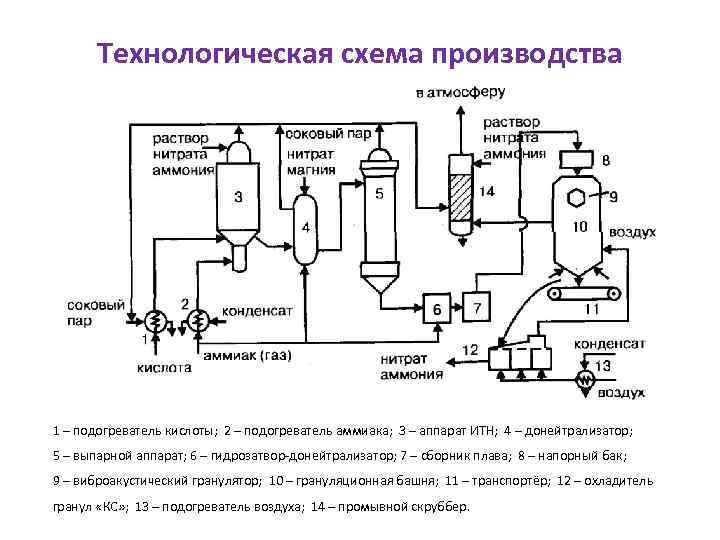
Технологическая схема производства 1 – подогреватель кислоты; 2 – подогреватель аммиака; 3 – аппарат ИТН; 4 – донейтрализатор; 5 – выпарной аппарат; 6 – гидрозатвор-донейтрализатор; 7 – сборник плава; 8 – напорный бак; 9 – виброакустический гранулятор; 10 – грануляционная башня; 11 – транспортёр; 12 – охладитель гранул «КС» ; 13 – подогреватель воздуха; 14 – промывной скруббер.
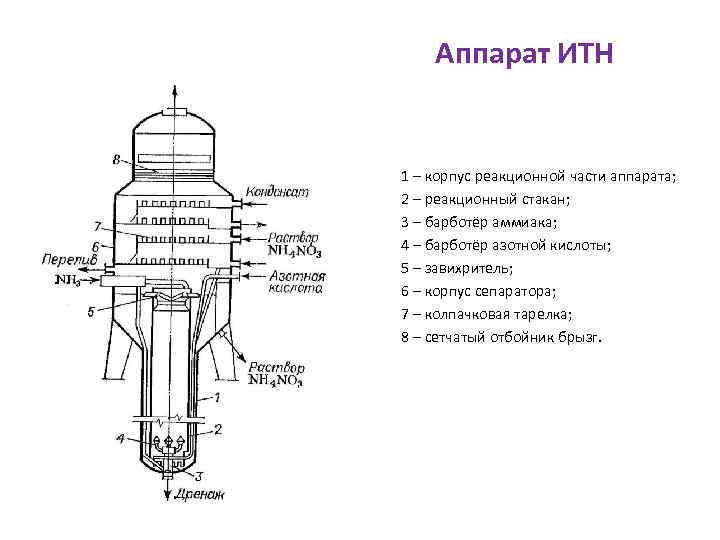
Аппарат ИТН 1 – корпус реакционной части аппарата; 2 – реакционный стакан; 3 – барботёр аммиака; 4 – барботёр азотной кислоты; 5 – завихритель; 6 – корпус сепаратора; 7 – колпачковая тарелка; 8 – сетчатый отбойник брызг.

Производство нитрата аммония безупарочным методом Принципиальными отличиями технологической схемы производства нитрата аммония безупарочним методом являются: Ø использование более концентрированной азотной кислоты; Ø проведение процесса нейтрализации при повышенном (0, 4 МПа) давлении; Ø быстрый контакт нагретых компонентов. В этих условиях на стадии нейтрализации образуется парожидкостная эмульсия, после разделения которой получают плав с концентрацией нитрата аммония 98, 5 %. Это позволяет исключить отдельную стадию выпаривания раствора.
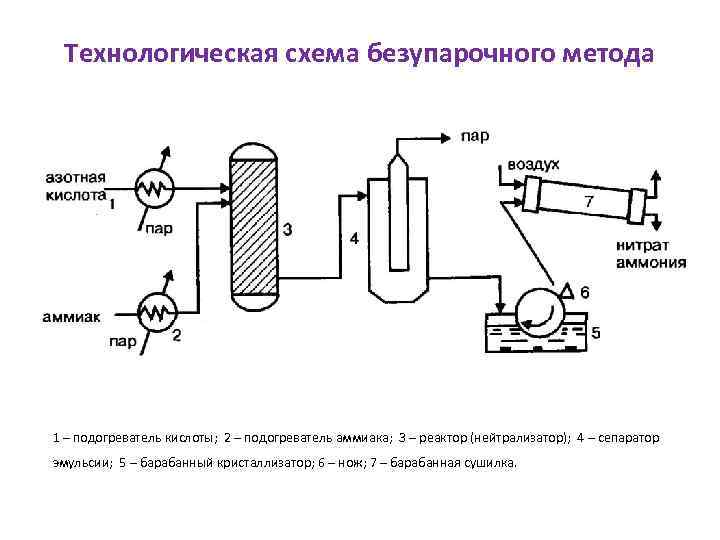
Технологическая схема безупарочного метода 1 – подогреватель кислоты; 2 – подогреватель аммиака; 3 – реактор (нейтрализатор); 4 – сепаратор эмульсии; 5 – барабанный кристаллизатор; 6 – нож; 7 – барабанная сушилка.

Производство карбамида

Свойства карбамида Карбамид (мочевина) CO(NH 2)2 – диамид угольной или амид карбаминовой кислот. Генетическая связь производных угольной кислоты выражается схемой: Карбамид представляет собой кристаллическое вещество с температурой плавления 132, 7 0 С. Хорошо растворим в воде, этаноле и жидком аммиаке, что используется для получения аммиакатов.

Свойства карбамида При нагревании выше 130 0 С подвергается термической диссоциации с образованием биурета и выделением аммиака: 2 CO(NH 2)2 = H 2 N – CO – NH 2 + NH 3 Водные растворы карбамида устойчивы до 80 0 С, при более высокой температуре карбамид гидролизуется по схеме: CO(NH 2)2 + 2 H 2 O (NH 4)2 CO 3 NH 4 HCO 3 + NH 3 CO 2 + H 2 O + 2 NH 3 Карбамид – безбалластное высококонцентрированное минеральное удобрение, содержание азота в амидной форме составляет 46, 6 %. Преимущества карбамида перед амселитрой: ü ü большее содержание азота; меньшая слёживаемость; взрывобезопасность в смесях с органическими веществами; пролонгированное действие.

Физико-химические основы синтеза карбамида В основе получения карбамида лежит взаимодействие аммиака с диоксидом углерода с последующей дистилляцией продуктов синтеза и перера -боткой полученных растворов. При синтезе карбамида последовательно протекают две обратимые реакции: Ø образование карбамата аммония: 2 NH 3 + CO 2 H 2 N – CO – ONH 4 + 126 к. Дж (1) Ø дегидратация карбамата аммония до карбамида: H 2 N – CO – ONH 4 CO(NH 2)2 + H 2 O – 16 к. Дж Процесс синтеза описывается суммарным уравнением: 2 NH 3 + CO 2 = CO(NH 2)2 + H 2 O + 110 к. Дж (2)

Физико-химические основы синтеза карбамида 2 NH 3 + CO 2 H 2 N – CO – ONH 4 + 126 к. Дж (1) H 2 N – CO – ONH 4 CO(NH 2)2 + H 2 O – 16 к. Дж (2) Скорости реакций 1 и 2 различны. Реакция 1 протекает значительно быстрее реакции 2, поэтому лимитирующей стадией процесса синтеза является дегидратация карбамата аммония. Состояние равновесия и скорость процесса определяются температурой, давлением, соотношением аммиака и диоксида углерода и содержанием воды в реакционной смеси.

Физико-химические основы синтеза карбамида •
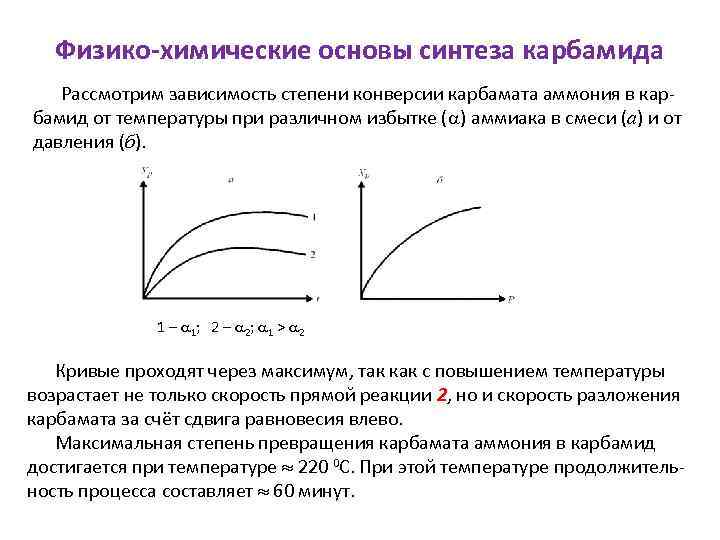
Физико-химические основы синтеза карбамида Рассмотрим зависимость степени конверсии карбамата аммония в карбамид от температуры при различном избытке ( ) аммиака в смеси (а) и от давления (б). 1 – 1; 2 – 2; 1 > 2 Кривые проходят через максимум, так как с повышением температуры возрастает не только скорость прямой реакции 2, но и скорость разложения карбамата за счёт сдвига равновесия влево. Максимальная степень превращения карбамата аммония в карбамид достигается при температуре 220 0 С. При этой температуре продолжительность процесса составляет 60 минут.
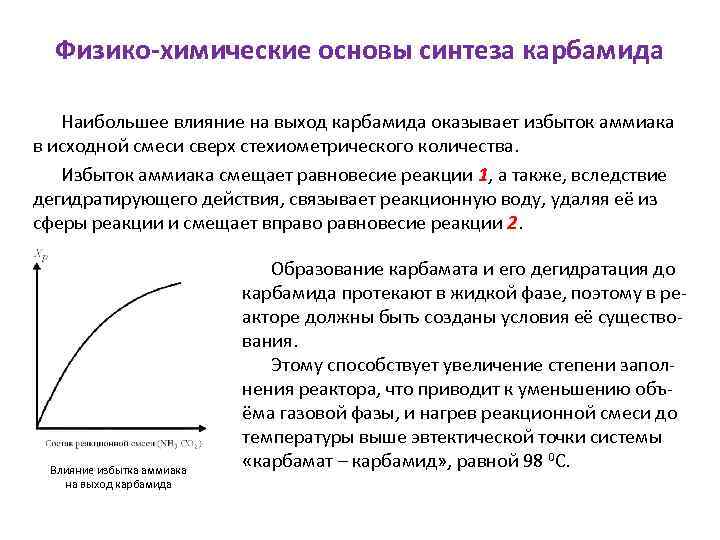
Физико-химические основы синтеза карбамида Наибольшее влияние на выход карбамида оказывает избыток аммиака в исходной смеси сверх стехиометрического количества. Избыток аммиака смещает равновесие реакции 1, а также, вследствие дегидратирующего действия, связывает реакционную воду, удаляя её из сферы реакции и смещает вправо равновесие реакции 2. Влияние избытка аммиака на выход карбамида Образование карбамата и его дегидратация до карбамида протекают в жидкой фазе, поэтому в реакторе должны быть созданы условия её существования. Этому способствует увеличение степени заполнения реактора, что приводит к уменьшению объёма газовой фазы, и нагрев реакционной смеси до температуры выше эвтектической точки системы «карбамат – карбамид» , равной 98 0 С.
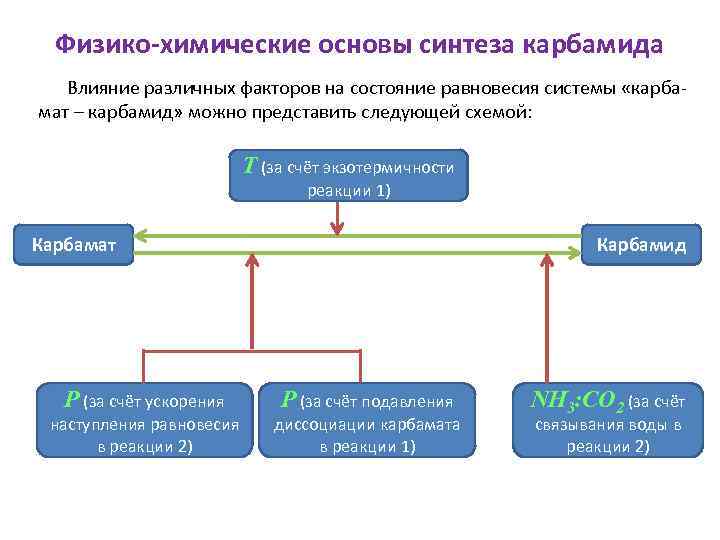
Физико-химические основы синтеза карбамида Влияние различных факторов на состояние равновесия системы «карбамат – карбамид» можно представить следующей схемой: Т (за счёт экзотермичности реакции 1) Карбамат Карбамид Р (за счёт ускорения Р (за счёт подавления наступления равновесия в реакции 2) диссоциации карбамата в реакции 1) NH 3: CO 2 (за счёт связывания воды в реакции 2)

Физико-химические основы синтеза карбамида Оптимальный режим процесса синтеза карбамида должен обеспечить: быстрое и полное протекание реакции 1, протекание реакции 2 не менее, чем на 75 %. Этим условиям отвечают следующие параметры процесса: температура 180 – 200 0 С, давление 20 МПа, отношение NH 3: CO 2 = 4: 1

Виды технологических схем В результате взаимодействия аммиака и диоксида углерода образуется сложная система, состоящая из целевого продукта (карбамида), полупродукта (карбамат аммония), воды, карбонатов аммония и избытка аммиака. Для выделения из неё твёрдого карбамида и утилизации не вступивших в реакцию остальных компонентов и карбамата полученный раствор подвергается дистилляции. В процессе дистилляции отгоняется избыточный аммиак и вода и происходит разложение карбамата и карбонатов аммония. В зависимости от того, возвращаются эти продукты в процесс, или после отделения карбамида используются в других производствах, технологические схемы производства карбамида подразделяются на две группы: Ø без возвращения продуктов дистилляции в цикл (разомкнутая схема без рецикла); Ø с возвращением продуктов дистилляции в цикл (замкнутая схема с рециклом).

Виды технологических схем В первом случае весь выделившийся при дистилляции аммиак направляется на получение других продуктов (аммиачной селитры и др. ). Во втором случае продукты дистилляции частично (частичный рецикл) или полностью (полный рецикл) возвращаются в цикл синтеза карбамида. Существует два варианта полного рецикла: Ø газовый рецикл, при котором продукты дистилляции возвращаются в газообразном виде; Ø жидкостной рецикл, при котором продукты дистилляции возвращаются в виде раствора аммонийных солей. Наиболее экономична технологическая схема с полным жидкостным рециклом, так как в ней не требуется сжатия возвращаемых в цикл горячих газов, что может вызвать засорение трубопроводов образующимся твёрдым карбамидом и их коррозию.
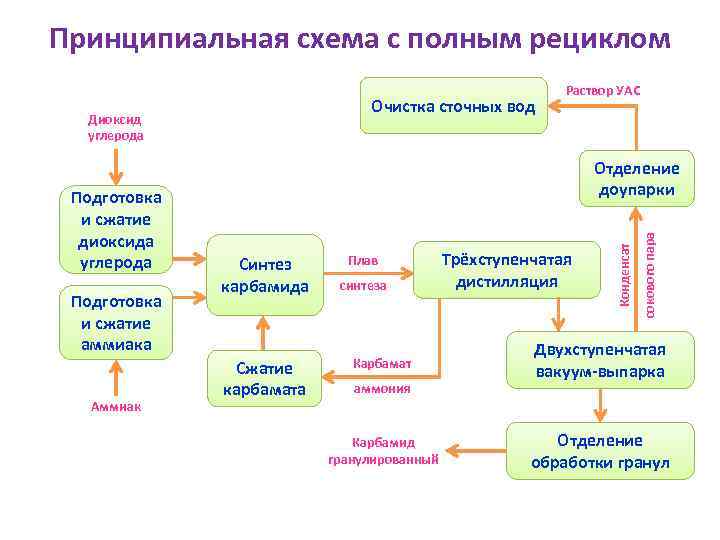
Принципиальная схема с полным рециклом Очистка сточных вод Диоксид углерода Аммиак Синтез карбамида Сжатие карбамата Плав синтеза Карбамат аммония Карбамид гранулированный Трёхступенчатая дистилляция сокового пара Подготовка и сжатие аммиака Отделение доупарки Конденсат Подготовка и сжатие диоксида углерода Раствор УАС Двухступенчатая вакуум-выпарка Отделение обработки гранул

Производство сульфата аммония

Характеристика сульфата аммония Сульфат аммония (NН 4)2 SО 4 – бесцветное кристаллическое вещество, содержит 21, 21 % азота, при нагревании до 513 0 С полностью разлагается на аммиак и серную кислоту; частичное разложение с образованием кислых солей начинается выше 200 0 С. Сульфат аммония применяется исключительно в качестве удобрения. Это удобрение обладает весьма небольшой гигроскопичностью, мало слёживается, и внесение его в почву не вызывает затруднений. Недостатком является большая физиологическая кислотность. При его применении в почве, если она не содержит достаточного количества оснований, постепенно накапливается серная кислота, для нейтрализации которой необходимо периодически производить известкование почвы.

Способы производства сульфата аммония Основные промышленные способы производства сульфата аммония базируются на нейтрализации серной кислоты аммиаком. Для производства сульфата аммония используют аммиак, содержащийся в газах сухой перегонки каменного угля в коксохимической и газовой промышленности, а также синтетический аммиак. Сульфат аммония получают также, обрабатывая гипс растворами карбоната аммония и из растворов, являющихся отходами производства кап -ролактама, используемого для получения капрона.

Способы производства сульфата аммония Сульфат аммония получается по реакции путем нейтрализации газообразного аммиака серной кислотой: 2 NН 3(газ) + Н 2 SО 4 = (NН 4)2 SО 4 + 280 к. Дж Процесс нейтрализации может осуществляться по мокрому и сухому способам. При мокром способе производства продукт кристаллизуется из пересыщенных растворов. При насыщении аммиаком серной кислоты в реакционном аппарате выделяется большое количество тепла, достаточное для нагрева реакционной смеси до температуры кипения и для испарения из нее значительного количества воды.

Способы производства сульфата аммония При мокром способе важно обеспечить кристаллизацию из горячего реакционного раствора средней соли, не допуская выделения кислых солей. Находящиеся в серной кислоте примеси, особенно сульфаты железа и алюминия, затрудняют кристаллизацию сульфата аммония. При нейтрализации кислоты осаждаются коллоидные гидроксиды железа и алюминия, обволакивающие кристаллы сульфата аммония и тормозящие их рост. Для устранения этого явления кислоту нейтрализуют не полностью – в непрерывно действующих реакторах поддерживают кислую реакцию среды.

Способы производства сульфата аммония Сухой способ заключается в распылении серной кислоты в камере с газообразным аммиаком. Мелкие брызги серной кислоты почти мгновенно нейтрализуются аммиаком и превращаются в твердые сухие кристаллики сульфата аммония, так как вносимая с серной кислотой вода испаряется за счет теплоты реакции и уносится из аппарата в виде пара. Сухой продукт падает на дно реакционной камеры. Получаемый сухим способом сульфат аммония представляет собой очень мелкий, пылящий порошок. С целью уменьшения потерь от пыления при перегрузке и транспортировке его подвергают грануляции. Для этого кристаллы смачивают небольшим количеством слабой аммиачной воды и гранулируют в барабанных грануляторах, полученные гранулы высушиваются при 105 – 110 0 С.

Способы производства сульфата аммония Производство сульфата аммония из аммиака коксового газа В коксовом газе содержится 6 -14 г/м 3 аммиака. Его можно переработать в сульфат аммония тремя способами: Ø по косвенному способу коксовый газ охлаждают, причем из него конденсируется смола и надсмольная вода, насыщенная аммиаком; оставшийся в газе аммиак поглощают водой в аммиачных скрубберах. Из полученной аммиачной воды и из надсмольной воды отгоняют в дистилляционных колоннах аммиак и поглощают его серной кислотой. Этот способ требует громоздкого оборудования и значительного расхода энергии.

Способы производства сульфата аммония Производство сульфата аммония из аммиака коксового газа В коксовом газе содержится 6 -14 г/м 3 аммиака. Его можно переработать в сульфат аммония тремя способами: Ø по прямому способу поглощение аммиака серной кислотой с образованием сульфата аммония производят непосредственно из коксового газа, предварительно охлажденного до 68 0 С и очищенного от смолы в электрофильтрах.

Способы производства сульфата аммония Производство сульфата аммония из аммиака коксового газа В коксовом газе содержится 6 -14 г/м 3 аммиака. Его можно переработать в сульфат аммония тремя способами: Ø наиболее экономичен и широко распространен полупрямой способ. Коксовый газ сначала охлаждают до 25 -30 0 С для конденсации смолы. Конденсат расслаивается на два слоя: нижний - смолу и верхний – надсмольную воду, в которой растворена часть аммиака. Надсмольную воду обрабатывают в дистилляционной колонне известковым молоком, и выделившийся аммиак поглощают серной кислотой вместе с аммиаком, оставшимся в доочищенном в электрофильтрах от смолы коксовом газе.

Способы производства сульфата аммония Производство сульфата аммония из аммиака коксового газа Поглощение аммиака из коксового газа можно производить в сатураторах барботажного типа (сатураторный способ) или в скрубберах (бессатураторный способ). В сатураторном способе поглощение аммиака из коксового газа и кристаллизация сульфата аммония совмещены в одном аппарате – сатураторе. Это ограничивает возможность выбора технологического режима, который был бы оптимальным одновременно для обоих процессов, то есть обеспечивающего наиболее полное поглощение аммиака и образование крупнокристаллического сульфата аммония, легко отделяемого и отмываемого от маточного раствора. К недостаткам сатураторного способа относятся: получение мелкокристаллического, сильно пылящего при сушке продукта; большой расход энергии на преодоление гидравлического сопротивления.

Способы производства сульфата аммония Производство сульфата аммония из аммиака коксового газа В бессатураторных способах процессы абсорбции и кристаллизации ведут раздельно - поглощение аммиака в скрубберах, а кристаллизацию сульфата аммония - в кристаллизаторах. В бессатураторных процессах абсорбцию аммиака из коксового газа ведут в полых скрубберах или кислым ненасыщенным раствором сульфата аммония с последующей вакуум-выпаркой на кристалл, или кислым насыщенным раствором с выращиванием образовавшихся мелких кристаллов в кристаллизаторах под атмосферным давлением. Чаще используют первый способ - орошение абсорбера ненасыщенным раствором предотвращает их засоление, а кристаллизация в выпарных аппаратах позволяет регулировать размеры получаемых кристаллов.

Производство нитрата натрия

Свойства нитрата натрия Нитрат натрия (натриевая селитра) Nа. NО 3 – бесцветные, прозрачные кристаллы, плавящиеся при 309, 5 0 С. Выше 380 0 С нитрат натрия разлагается ни нитрит натрия и кислород. Нитрат натрия почти не гигроскопичен; в присутствии небольших примесей хлоридов его гигроскопичность сильно возрастает. Нитрат натрия выпускают двух сортов: Ø продукт 1 -го сорта содержит н/м 99, 5 % Nа. NО 3 (в пересчете на сухое вещество) и н/б 1 % влаги, в продукте 1 -го сорта не должно быть более 0, 05 % нерастворимых в воде веществ, 0, 5 % хлоридов (Nа. Сl), 0, 02 % окисляемых веществ (Nа. NО 2). Ø продукт 2 -го сорта содержит 99 % Nа. NО 3 и н/б 1, 8 % влаги.

Свойства нитрата натрия Нитрат натрия является ценным физиологически щелочным удобрением, применение которого особенно эффективно на кислых почвах. Несмотря на это его применяют в небольших масштабах из-за малого содержания азота (в чистом Nа. NО 3 16, 47 % N) и относительно высокой его стоимости. В основном его используют для технических целей. Нитрат натрия нередко встречается в природных условиях, однако почти все его залежи вследствие низкой концентрации Nа. NО 3 не имеют промышленного значения. Мощное месторождение натриевой селитры имеется в Чили, где и производится его добыча.

Методы получения нитрата натрия Наиболее простой метод получения натриевой селитры нейтрализацией соды или едкого натра азотной кислотой в промышленности практически не применяется, так как расходовать на этот процесс азотную кисло -ту не экономично. В большинстве случаев Nа. NО 3 получают нейтрализацией соды или едкого натра выхлопными нитрозными газами, отходящими из абсорбционных систем в производстве азотной кислоты (главным образом, работающих под атмосферным давлением). Этим достигается обезвреживание выбрасываемых в атмосферу газов с одновременной утилизацией содержащихся в них оксидов азота.

Методы получения нитрата натрия При абсорбции оксидов азота содой идут следующие реакции: Nа 2 СО 3 + NО 2 = 2 Nа. NО 2 + СО 2 Nа 2 СО 3 + 2 NО 2 = 2 Nа. NО 2 + Nа. NО 3 + СО 2 Получаемые растворы содержат нитрат и нитрит натрия. Соотношение между ними зависит от температуры и степени окисленности нитрозных газов. Чем меньше в газе NО и чем больше NО 2, тем больше получается в растворе нитрата натрия. Для хорошего поглощения оксидов азота необходимо, чтобы степень окисленности нитрозного газа была не меньше 50 %. Температуру раствора следует поддерживать на уровне 20 -25 0 С. Обычно отношение нитрита к нитрату в получаемом щелоке равно 4: 1. «Сырой» нитрит-нитратный щелок содержит 250 -400 г/л Nа. NО 2, 50 -80 г/л Nа. NО 3, 3 -5 г/л Nа. НСО 3 и Nа 2 СО 3, 2 -4 г/л Nа. Сl.

Методы получения нитрата натрия Для перевода нитрита натрия в нитрат щелок обрабатывают 50 % азотной кислотой. Этот процесс, называемый инверсией, идет по схеме: 3 Nа. NО 2 + 3 НNО 3 = 3 Nа. NО 3 + 3 НNО 2 = НNО 3 + 2 NО + Н 2 О 3 Nа. NО 2 + 2 НNО 3 = Nа. NО 3 + 2 NО + Н 2 О Скорость процесса увеличивается с повышением температуры, так как при этом ускоряется распад свободной азотистой кислоты, вытесняемой из нитрита натрия азотной кислотой. Избыток азотной кислоты и перемешивание реакционной смеси воздухом также ускоряют процесс. Кислород воздуха окисляет выделяющуюся при инверсии окись азота в двуокись, которая действует инвертирующим образом подобно азотной кислоте.

Методы получения нитрата натрия Представляют интерес способы получения нитрата натрия, не требующие затраты соды или едкого натра. К таким способам относятся получение нитрата натрия из поваренной соли и оксидов азота и метод катионного обмена. Процесс получения натриевой селитры методом катионного обмена состоит из трех основных стадий: 1) получение раствора Са(NО 3)2; 2) катионный обмен и регенерация катионита (обмен ионов кальция на ион натрия). Реакции, протекающие на этой стадии процесса, могут быть схематически выражены следующими уравнениями: Са(NО 3)2 + 2 RNа ↔ 2 Nа. NО 3 + R 2 Са + 2 Nа. Сl ↔ 2 RNа + Са. Сl 2 Происходит непрерывное чередование конверсии кальциевой селитры и регенерации катионита растворами хлористого натрия. 3) выпаривание растворов Nа. NО 3, кристаллизация соли, центрифугирование, сушка и упаковка.

Производство жидких азотных удобрений

Характеристика ЖАУ Жидкие азотные удобрения представляют собой растворы аммиачной селитры, карбамида, кальциевой селитры и их смесей в жидком аммиаке или в концентрированной аммиачной воде – так называемые аммиакаты. В качестве жидких удобрений применяют также жидкий аммиак и аммиачную воду (22 – 25 % NН 3). Аммиак и аммиакаты также усваиваются растениями и дают такой же эффект, как и обычные твердые азотные удобрения, производство же их проще и дешевле, чем производство твердых удобрений. Аммиакаты на основе нитрата аммония и карбамида применяют и для аммонизации суперфосфата и тукосмесей. Жидкие удобрения можно изготовлять и без применения аммиака, например, из диаммонийфосфата, карбамида и хлорида калия. Эти вещества легко растворяются в воде, образуя почти нейтральный раствор (р. Н = 7, 8). Применение жидких азотных удобрений обеспечивает возможность полной механизации работ по погрузке, выгрузке и внесению удобрений.

Характеристика ЖАУ Непосредственное использование аммиака и аммиачной воды в качестве жидких азотных удобрений обеспечивает возможность ускоренного строительства азотных заводов по «короткой» схеме, без цехов переработки аммиака в азотную кислоту и аммиачную селитру. Значительно сокращаются и эксплуатационные затраты и, следовательно, удешевляются удобрения. При применении жидких удобрений отпадает необходимость в таре – мешках, расход которых на упаковку продукции од-ного завода составляет много миллионов штук. Кроме того, жидкие удобрения не обладают такими отрицательными свойствами твердых удобрений, как гигроскопичность, слеживаемость и т. п.

Характеристика ЖАУ Наряду с преимуществами у жидких удобрений имеются и недостатки: Ø в жидких удобрениях – водных растворах солей – в случае большой их концентрации происходит высаливание, кристаллизация солей при понижении температуры. Применение же менее концентрированных растворов приводит к необходимости перевозить большие количества растворителя – воды. Поэтому стремятся найти такие композиции жидких удобрений, которые имели бы высокие концентрации и низкие темпера -туры кристаллизации; Ø требуется сооружение резервуаров большой емкости для хранения жидких удобрений, так как они расходуются в течение относительно короткого времени; Ø существенным недостатком некоторых жидких удобрений является их корродирующее действие. В особенности это относится к растворам аммиакатов нитрата аммония, обладающим повышенными коррозионными свойствами по отношению к черным металлам. Это затрудняет перевозку, хранение и внесение удобрений в почву.

Жидкий аммиак содержит 83, 2 % N и является самым концентрированным азотным удобрением. Под атмосферным давлением аммиак кипит при – 33, 5 0 С и замерзает при – 77, 7 0 С. Жидкий аммиак хранят и транспортируют в стальных цистернах, рассчитанных на давление 20 -30 ат. Плотность газообразного аммиака при нормальных условиях 0, 77 кг/м 3. Аммиак очень хорошо растворяется в воде: 1 объем воды при 0 0 С и при парциальном давлении NН 3, равном атмосферному, растворяет 1176 объемов аммиака, а при 20 0 С – 702 объема. Под атмосферным давлением максимальная концентрация аммиака в воде равна 46, 7 %, а при 50 0 С – 18, 6 %. С повышением давления растворимость аммиака в воде увеличивается.

Аммиачная вода Аммиачную воду производят двух марок: марка А – для удобрения сельскохозяйственных культур; марка Б – для промышленности. Каждая марка имеет два сорта, отличающихся содержанием аммиака. Вследствие относительно небольшого давления пара над аммиачной водой ее хранят и транспортируют в стальных закрытых цистернах или резервуарах.

Аммиакаты Твердые аммиакаты представляют собой комплексные кристаллические соединения, образующиеся при взаимодействии некоторых твердых солей или их водных растворов с жидким или газообразным аммиаком. Состав аммиакатов, полученных на основе аммиачной селитры, соответствует формуле NН 4 NО 3×n. NН 3×m. Н 2 О. Аммиакаты на основе кальциевой и аммиачной селитры имеют следующий состав Са(NО 3)2×х. NН 4 NО 3×n. NН 3×m. Н 2 О. Твердый нитрат аммония при температуре от – 15 до +25 0 С энергично поглощает газообразный аммиак и переходит в жидкое состояние. При – 10 0 С состав отвечает формуле NН 4 NО 3× 2 NН 3. С повышением температуры происходит выделение аммиака и при 28 0 С образуется твердая соль NН 4 NО 3×NН 3, которая легко теряет аммиак.

Аммиакаты Применяемые в качестве удобрений жидкие аммиакаты – растворы NH 4 NO 3, (NH 2)2 CO, Ca(NO 3)2, (NH 4)2 CO 3 в водном аммиаке – представляют собой светлые жидкости, плотность их зависит от состава и колеблется в пределах 0, 9 -1, 25 г/см 3. Давление пара над аммиакатами значительно ниже, чем над жидким аммиаком. Температура высаливания аммиакатов понижается с увеличением содержания в них аммиака и уменьшением содержания воды. Аммиакат состава 55, 14 % NН 4 NО 3, 25, 69 % NН 3 и 18, 97 % Н 2 О имеет температуру высаливания – 27, 5 0 С. Введение в аммиакат карбамида или нитрата кальция также приводит к понижению температуры высаливания.
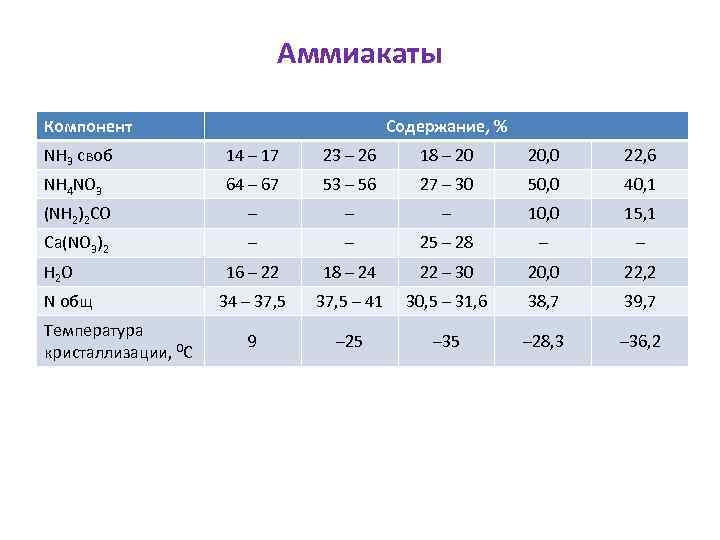
Аммиакаты Компонент Содержание, % NH 3 своб 14 – 17 23 – 26 18 – 20 20, 0 22, 6 NH 4 NO 3 64 – 67 53 – 56 27 – 30 50, 0 40, 1 (NH 2)2 CO – – – 10, 0 15, 1 Ca(NO 3)2 – – 25 – 28 – – 16 – 22 18 – 24 22 – 30 20, 0 22, 2 34 – 37, 5 – 41 30, 5 – 31, 6 38, 7 39, 7 9 – 25 – 35 – 28, 3 – 36, 2 H 2 O N общ Температура кристаллизации, 0 С

Растворы КАС В последнее время широкое применение получили растворы карбамида и аммиачной селитры. В них в качестве ингибиторов коррозии добавляют 0, 5 % NH 3 и 0, 2 % Р 2 О 5 в виде фосфатов аммония. Их выпускают с содержанием 28, 30, 32 и 34 % общего азота КАС-28 содержит 30, 0 % (NH 2)2 CO и 40, 1 % NH 4 NO 3, имеет плотность при 16 0 С 1283 кг/м 3 и начинает кристаллизоваться при – 18 0 С. КАС-32 содержит 36, 4 % (NH 2)2 CO и 43, 3 % NH 4 NO 3, имеет плотность при 16 0 С 1327 кг/м 3 и начинает кристаллизоваться при – 2 0 С. Для гарантии взрывобезопасности количество NH 4 NO 3 в растворах КАС не должно превышать 45 %.

Растворы КАС Преимущества растворов КАС перед аммиакатами: Ø отсутствие потерь азота вследствие малого содержания летучего аммиака; Ø возможность хранения и транспортировки в резервуарах и цистернах, изготовленных из дешёвой углеродистой стали и не рассчитанных на повышенное давление; Ø более простые приёмы внесения в почву.
9 - Производство азотных удобрений.pptx