Азот.Шакиров1212.pptx
- Количество слайдов: 17
 Азот выполнил Шакиров И. Х. г. Нижнекамск, 2013 г.
Азот выполнил Шакиров И. Х. г. Нижнекамск, 2013 г.
 История открытия азота 1772 г. К. Шееле и Г. Кавендиш получили азот В 1772 году азот как простое вещество описал Даниэль Резерфорд, он опубликовал магистерскую диссертацию, где указал основные свойства азота Г. Кавендиш Д. Резерфорд К. Шееле
История открытия азота 1772 г. К. Шееле и Г. Кавендиш получили азот В 1772 году азот как простое вещество описал Даниэль Резерфорд, он опубликовал магистерскую диссертацию, где указал основные свойства азота Г. Кавендиш Д. Резерфорд К. Шееле
 Способы получения В лаборатории – разложением нитритов при нагревании: NH 4 NO 2 = N 2 + 2 H 2 O В промышленности получают фракционной перегонкой жидкого воздуха.
Способы получения В лаборатории – разложением нитритов при нагревании: NH 4 NO 2 = N 2 + 2 H 2 O В промышленности получают фракционной перегонкой жидкого воздуха.
 Нахождение в природе в свободном состоянии в атмосфере:
Нахождение в природе в свободном состоянии в атмосфере:
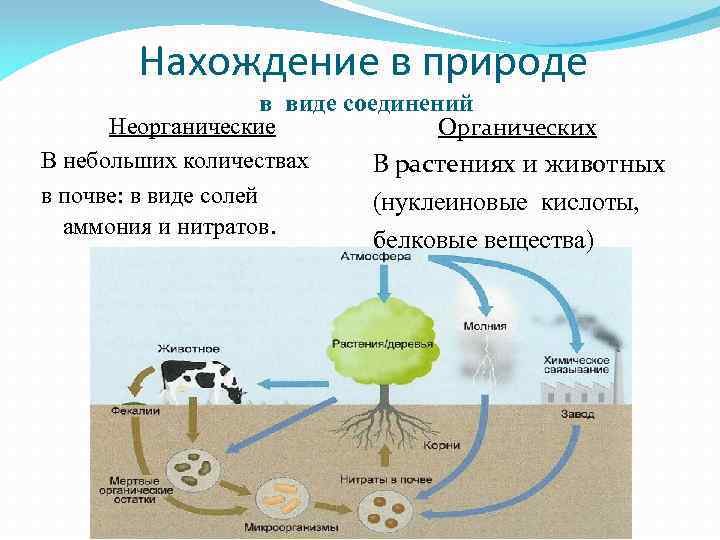 Нахождение в природе в виде соединений Неорганические Органических В небольших количествах В растениях и животных в почве: в виде солей (нуклеиновые кислоты, аммония и нитратов. белковые вещества)
Нахождение в природе в виде соединений Неорганические Органических В небольших количествах В растениях и животных в почве: в виде солей (нуклеиновые кислоты, аммония и нитратов. белковые вещества)
 Физические свойства Бесцветный газ Не имеет запаха Мало растворим в воде Немного легче воздуха Температура кипения -1960 С Температура плавления -2100 С
Физические свойства Бесцветный газ Не имеет запаха Мало растворим в воде Немного легче воздуха Температура кипения -1960 С Температура плавления -2100 С
 Химические свойства При обычных условиях соединение азота с металлом не происходит; он вступает в реакцию только с литием: 6 Li + N 2 → 2 Li 3 N При нагревании он может вступать в реакции с металлами и неметаллами, при этом также образуются нитриды: 3 Mg + N 2 → Mg 3 N 2 2 B + N 2 → 2 BN
Химические свойства При обычных условиях соединение азота с металлом не происходит; он вступает в реакцию только с литием: 6 Li + N 2 → 2 Li 3 N При нагревании он может вступать в реакции с металлами и неметаллами, при этом также образуются нитриды: 3 Mg + N 2 → Mg 3 N 2 2 B + N 2 → 2 BN
 Оксиды азота N 2 O – закись азота. Физические свойства: бесцветный газ со слабым приятным запахом и сладковатым вкусом, растворим в воде, несолеобразующий оксид Химические свойства: при нагревании проявляет свойства окислителя: При нагревании N 2 O разлагается: NO – окись азота. Физические свойства: бесцветный газ, плохо растворим в воде. Химические свойства: Окисление NO кислородом воздуха: Проявляет окислительно-восстановительные свойства : Восст. Окис.
Оксиды азота N 2 O – закись азота. Физические свойства: бесцветный газ со слабым приятным запахом и сладковатым вкусом, растворим в воде, несолеобразующий оксид Химические свойства: при нагревании проявляет свойства окислителя: При нагревании N 2 O разлагается: NO – окись азота. Физические свойства: бесцветный газ, плохо растворим в воде. Химические свойства: Окисление NO кислородом воздуха: Проявляет окислительно-восстановительные свойства : Восст. Окис.
 Оксиды азота N 2 O 3. Физические свойства: темно-синяя жидкость Химические свойства: кислотный оксид. N 2 O 3 подвержен термической диссоциации: Взаимодействует с водой: Взаимодействует растворами щелочей:
Оксиды азота N 2 O 3. Физические свойства: темно-синяя жидкость Химические свойства: кислотный оксид. N 2 O 3 подвержен термической диссоциации: Взаимодействует с водой: Взаимодействует растворами щелочей:
 Оксиды азота NO 2 Физические свойства: ядовитый газ бурого цвета с резким запахом. Химические свойства: NO 2 отличается высокой химической активностью. Он взаимодействует с неметаллами. В этой реакции NO 2 — окислитель: Окисляет SO 2 в SO 3 : Растворяется в воде и щелочах:
Оксиды азота NO 2 Физические свойства: ядовитый газ бурого цвета с резким запахом. Химические свойства: NO 2 отличается высокой химической активностью. Он взаимодействует с неметаллами. В этой реакции NO 2 — окислитель: Окисляет SO 2 в SO 3 : Растворяется в воде и щелочах:
 Оксиды азота N 2 O 5 - азотный ангидрид. Физические свойства: белое твердое вещество, бесцветный газ и жидкость. Химические свойства: Типичный кислотный оксид. N 2 O 5 легко летуч и крайне неустойчив. Разложение происходит со взрывом: Растворяется в воде и в щелочах:
Оксиды азота N 2 O 5 - азотный ангидрид. Физические свойства: белое твердое вещество, бесцветный газ и жидкость. Химические свойства: Типичный кислотный оксид. N 2 O 5 легко летуч и крайне неустойчив. Разложение происходит со взрывом: Растворяется в воде и в щелочах:
 Разложение нитратов Первая группа: 2 КNО 3 = 2 КNО 2 + О 2↑. Вторая группа: 2 Сu(NО 3)2 = 2 Сu. О + 4 NО 2 + O 2 Третья группа: Hg(NО 3)2 = Нg + 2 NО 2 + О 2 Четвертая группа: NН 4 NО 3 = N 2 О + 2 Н 2 O
Разложение нитратов Первая группа: 2 КNО 3 = 2 КNО 2 + О 2↑. Вторая группа: 2 Сu(NО 3)2 = 2 Сu. О + 4 NО 2 + O 2 Третья группа: Hg(NО 3)2 = Нg + 2 NО 2 + О 2 Четвертая группа: NН 4 NО 3 = N 2 О + 2 Н 2 O
 Способы получения HNO 3 В лаборатории : KNO 3 + H 2 SO 4 конц. = HNO 3 + KHSO 4 В промышленности: 4 NH 3 + 5 O 2 = 4 NO + 6 H 2 O + Q 2 NO + O 2 = 2 NO 2 4 NO 2 + 2 H 2 O = 4 HNO 3
Способы получения HNO 3 В лаборатории : KNO 3 + H 2 SO 4 конц. = HNO 3 + KHSO 4 В промышленности: 4 NH 3 + 5 O 2 = 4 NO + 6 H 2 O + Q 2 NO + O 2 = 2 NO 2 4 NO 2 + 2 H 2 O = 4 HNO 3
 Химические свойства Взаимодействие с металлами и неметаллами: а) с металлами, стоящими в ряду напряжений правее водорода: б) с металлами, стоящими в ряду напряжений левее водорода: в) С неметаллами, например с фосфором: 5 HNO 3 конц. + P = H 3 PO 4 + 5 NO 2 + H 2 O
Химические свойства Взаимодействие с металлами и неметаллами: а) с металлами, стоящими в ряду напряжений правее водорода: б) с металлами, стоящими в ряду напряжений левее водорода: в) С неметаллами, например с фосфором: 5 HNO 3 конц. + P = H 3 PO 4 + 5 NO 2 + H 2 O
 Области применения
Области применения
 Перспективы развития Азид натрия можно рассматривать как альтернативу существующим дезинфектантам, учитывая невысокую стоимость, экологичность и хорошие характеристики качества дезинфекции окружающей среды. Роль оксида азота изучается и при ожоговой травме. В настоящее время ведутся интенсивные разработки по получению лекарственных средств.
Перспективы развития Азид натрия можно рассматривать как альтернативу существующим дезинфектантам, учитывая невысокую стоимость, экологичность и хорошие характеристики качества дезинфекции окружающей среды. Роль оксида азота изучается и при ожоговой травме. В настоящее время ведутся интенсивные разработки по получению лекарственных средств.
 Спасибо за внимание!
Спасибо за внимание!


