Azot_i_ego_soedinenia.pptx
- Количество слайдов: 53
 Азот и его соединения
Азот и его соединения
 Нахождение в природе. В литосфере на долю связанного азота приходится лишь 0, 01%. Основная часть находится свободного азота приходится на атмосферу: 78, 09% по объему или 65, 6% по массе.
Нахождение в природе. В литосфере на долю связанного азота приходится лишь 0, 01%. Основная часть находится свободного азота приходится на атмосферу: 78, 09% по объему или 65, 6% по массе.
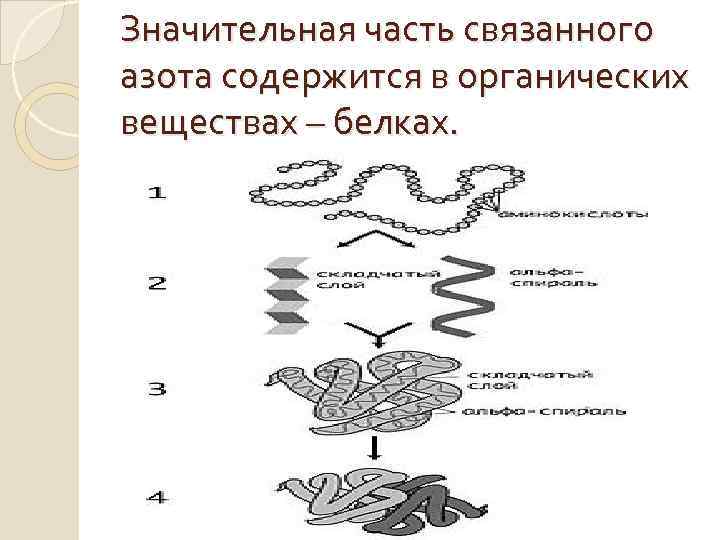 Значительная часть связанного азота содержится в органических веществах – белках.
Значительная часть связанного азота содержится в органических веществах – белках.
 Получение. Как и кислород, в промышленности азот получают фракционной перегонкой жидкого воздуха. В лаборатории азот получают разложением нитрита аммония: NH 4 NO 2 → N 2↑ + 2 H 2 O
Получение. Как и кислород, в промышленности азот получают фракционной перегонкой жидкого воздуха. В лаборатории азот получают разложением нитрита аммония: NH 4 NO 2 → N 2↑ + 2 H 2 O
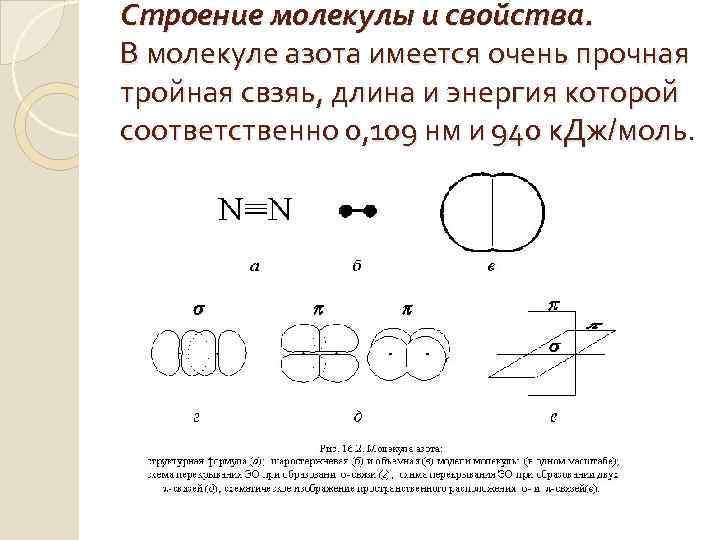 Строение молекулы и свойства. В молекуле азота имеется очень прочная тройная свзяь, длина и энергия которой соответственно 0, 109 нм и 940 к. Дж/моль.
Строение молекулы и свойства. В молекуле азота имеется очень прочная тройная свзяь, длина и энергия которой соответственно 0, 109 нм и 940 к. Дж/моль.
 Азот – бесцветный газ без запаха и вкуса. Так как молекула азота неполярна, то он имеет очень низкие температуру плавления(210) и кипения(-196). Очень плохо растворим в воде.
Азот – бесцветный газ без запаха и вкуса. Так как молекула азота неполярна, то он имеет очень низкие температуру плавления(210) и кипения(-196). Очень плохо растворим в воде.
 По электроотрицательности азот уступает только фтору и кислороду, поэтому для него характерны окислительные свойства.
По электроотрицательности азот уступает только фтору и кислороду, поэтому для него характерны окислительные свойства.
 Химические свойства азота: С металлами при нагревании он образует нитриды: 3 Mg + N 2 → Mg 3 N 2 2 Al+ N 2 → 2 Al. N При обычных условиях азот соединяется только с литием: 6 Li + N 2 → 2 Li 3 N
Химические свойства азота: С металлами при нагревании он образует нитриды: 3 Mg + N 2 → Mg 3 N 2 2 Al+ N 2 → 2 Al. N При обычных условиях азот соединяется только с литием: 6 Li + N 2 → 2 Li 3 N
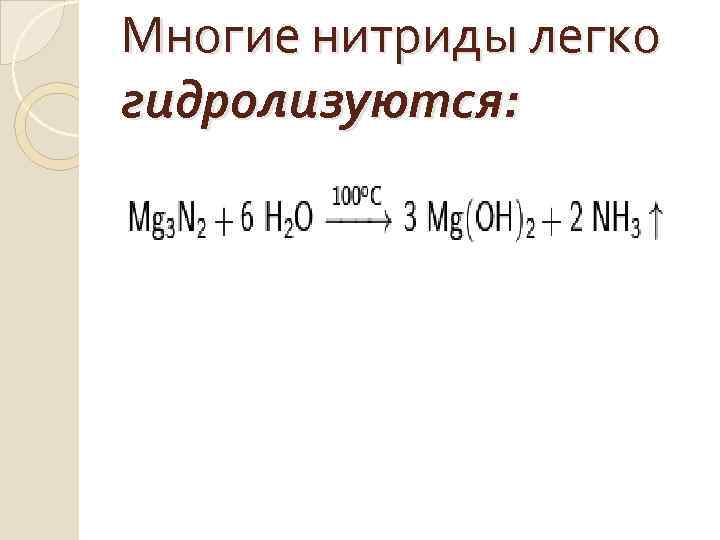 Многие нитриды легко гидролизуются:
Многие нитриды легко гидролизуются:
 В реакции с водородом азот вступает также в роли окислителя и обратимо взаимодействует с ним при высокой температуре и давлении в присутствии катализатора: 3 H 2 + N 2 ↔ 2 NH 3
В реакции с водородом азот вступает также в роли окислителя и обратимо взаимодействует с ним при высокой температуре и давлении в присутствии катализатора: 3 H 2 + N 2 ↔ 2 NH 3
 В реакции с кислородом азот выступает в роли восстановителя: N 2 + O 2 (2000° C) = 2 NO Азот не реагирует ни с кислотами, ни со щелочами.
В реакции с кислородом азот выступает в роли восстановителя: N 2 + O 2 (2000° C) = 2 NO Азот не реагирует ни с кислотами, ни со щелочами.
 При взаимодействии азота с карбидом кальция образуется цианамид кальция: Ca. C 2 + N 2 → Ca. CN 2 + C. Цианамид разлагается водой с образование аммиака: Ca. CN 2+3 H 2 O = Ca. CO 3+2 NH 3
При взаимодействии азота с карбидом кальция образуется цианамид кальция: Ca. C 2 + N 2 → Ca. CN 2 + C. Цианамид разлагается водой с образование аммиака: Ca. CN 2+3 H 2 O = Ca. CO 3+2 NH 3
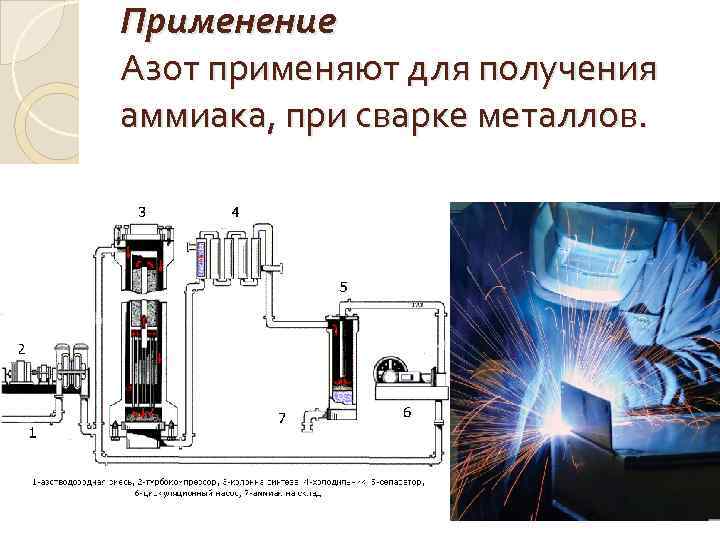 Применение Азот применяют для получения аммиака, при сварке металлов.
Применение Азот применяют для получения аммиака, при сварке металлов.
 В медицине чистый азот используется в качестве инертной среды при лечении туберкулеза легких, а жидкий азот – при лечении заболеваний позвоночника, суставов, кожных заболеваний.
В медицине чистый азот используется в качестве инертной среды при лечении туберкулеза легких, а жидкий азот – при лечении заболеваний позвоночника, суставов, кожных заболеваний.
 Аммиак. Получение: В лаборатории аммиак обычно получают слабым нагреванием смеси гашеной извести с нашатырем: 2 NH 4 Cl + Ca(OH)2 -> Ca. Cl 2 + 2 NH 3 + 2 H 2 O
Аммиак. Получение: В лаборатории аммиак обычно получают слабым нагреванием смеси гашеной извести с нашатырем: 2 NH 4 Cl + Ca(OH)2 -> Ca. Cl 2 + 2 NH 3 + 2 H 2 O
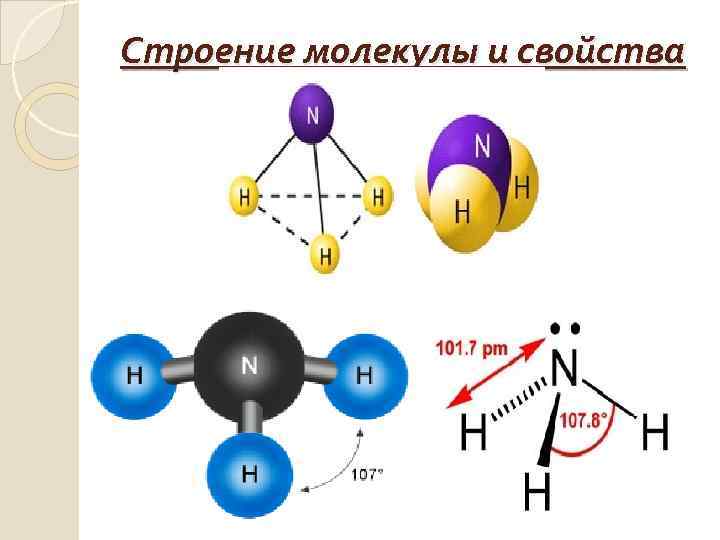 Строение молекулы и свойства
Строение молекулы и свойства
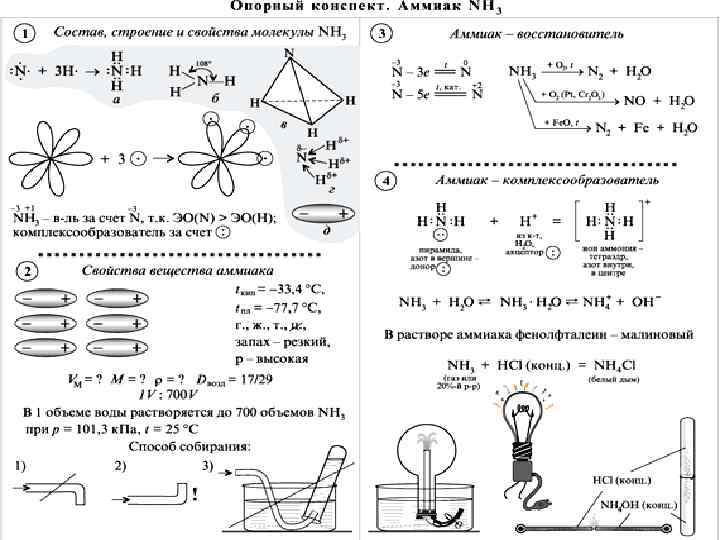
 Аммиак хорошо растворяется в воде и по этому свойству занимает первое место среди всех газов. Аммиак очень реакционноспособен. Для него характерны шесть групп реакций.
Аммиак хорошо растворяется в воде и по этому свойству занимает первое место среди всех газов. Аммиак очень реакционноспособен. Для него характерны шесть групп реакций.
 1. Основные свойства аммиак проявляет за счет присоединения протона к атому азота по донорноакцепторному механизму:
1. Основные свойства аммиак проявляет за счет присоединения протона к атому азота по донорноакцепторному механизму:
 Растворение аммиака в воде сопровождается обратимым химическим взаимодействием с ней:
Растворение аммиака в воде сопровождается обратимым химическим взаимодействием с ней:
 Водный раствор аммиака проявляет слабые основные свойства, имеет щелочную и изменяет окраску индикаторов
Водный раствор аммиака проявляет слабые основные свойства, имеет щелочную и изменяет окраску индикаторов
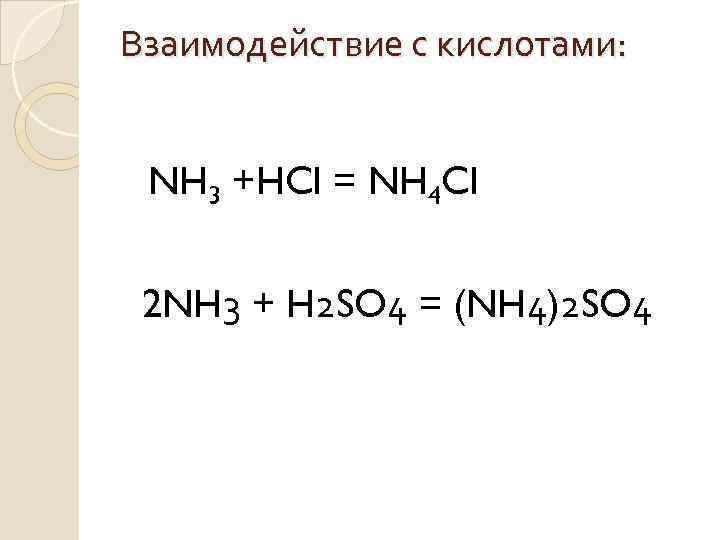 Взаимодействие с кислотами: NH 3 +HCl = NH 4 Cl 2 NH 3 + H 2 SO 4 = (NH 4)2 SO 4
Взаимодействие с кислотами: NH 3 +HCl = NH 4 Cl 2 NH 3 + H 2 SO 4 = (NH 4)2 SO 4
 2. Аммиак вступает во множество реакций комплексообразования: Cu. SO 4 + 4 NH 3 → [Cu(NH 3)4]SO 4 Гидроксид тетрааммин меди (II)
2. Аммиак вступает во множество реакций комплексообразования: Cu. SO 4 + 4 NH 3 → [Cu(NH 3)4]SO 4 Гидроксид тетрааммин меди (II)
 3. Аммиак за счет азота в степени окисления -3 проявляет сильные восстановительные свойства. Без катализатора С катализатором
3. Аммиак за счет азота в степени окисления -3 проявляет сильные восстановительные свойства. Без катализатора С катализатором
 4. Аммиак вступает в реакции с органическими веществами: CH 2=CH–COOH + NH 3 H 2 N–CH 2– COOH
4. Аммиак вступает в реакции с органическими веществами: CH 2=CH–COOH + NH 3 H 2 N–CH 2– COOH
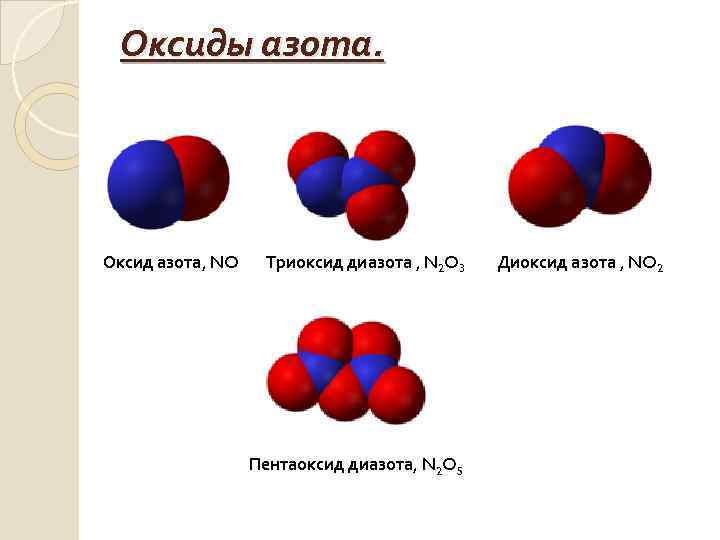 Оксиды азота. Оксид азота, NO Триоксид диазота , N 2 O 3 Пентаоксид диазота, N 2 O 5 Диоксид азота , NO 2
Оксиды азота. Оксид азота, NO Триоксид диазота , N 2 O 3 Пентаоксид диазота, N 2 O 5 Диоксид азота , NO 2
 Оксид азота(I) N 2 O-Несолеобразующий оксид. При нагревании разлагается на азот и кислород. При высоких концентрациях N 2 O возбуждает нервную систему ( «веселящий газ» ). В медицине N 2 O применяют как слабое средство для наркоза.
Оксид азота(I) N 2 O-Несолеобразующий оксид. При нагревании разлагается на азот и кислород. При высоких концентрациях N 2 O возбуждает нервную систему ( «веселящий газ» ). В медицине N 2 O применяют как слабое средство для наркоза.
 Получение: Закись азота получают нагреванием сухого нитрата аммония. Разложение начинается при 170 °C и сопровождается выделением тепла. Поэтому, чтобы не дать протекать ему слишком бурно, следует вовремя прекратить нагревание, так как при температурах более 300 °C нитрат аммония разлагается со взрывом:
Получение: Закись азота получают нагреванием сухого нитрата аммония. Разложение начинается при 170 °C и сопровождается выделением тепла. Поэтому, чтобы не дать протекать ему слишком бурно, следует вовремя прекратить нагревание, так как при температурах более 300 °C нитрат аммония разлагается со взрывом:
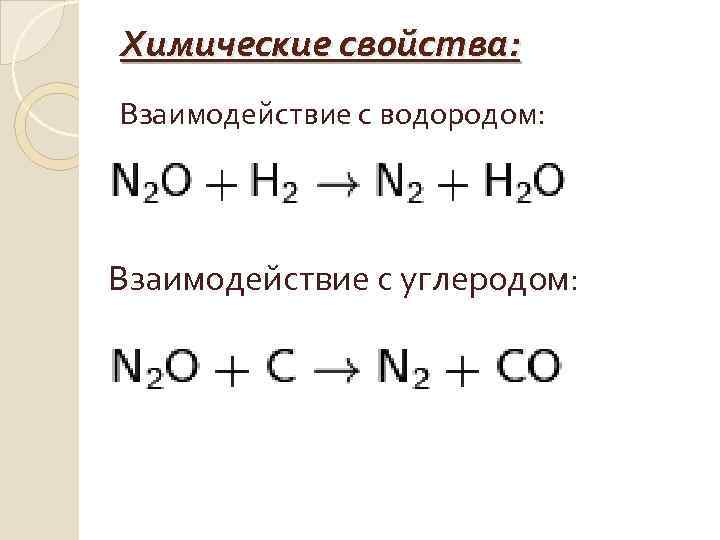 Химические свойства: Взаимодействие с водородом: Взаимодействие с углеродом:
Химические свойства: Взаимодействие с водородом: Взаимодействие с углеродом:
 Оксид азота(II) NO (монооксид азота) — бесцветный газ, незначительно растворим в воде. Не взаимодействует с водой, растворами кислот и щелоче. Оксид NO получают каталитическим окислением при производстве азотной кислоты.
Оксид азота(II) NO (монооксид азота) — бесцветный газ, незначительно растворим в воде. Не взаимодействует с водой, растворами кислот и щелоче. Оксид NO получают каталитическим окислением при производстве азотной кислоты.
 Химические свойства: При комнатной температуре и атмосферном давлении происходит окисление NO кислородом воздуха:
Химические свойства: При комнатной температуре и атмосферном давлении происходит окисление NO кислородом воздуха:
 С галогенами: Хлорид нитрозила В присутствии более сильных восстановителей NO проявляет окислительные свойства:
С галогенами: Хлорид нитрозила В присутствии более сильных восстановителей NO проявляет окислительные свойства:
 Оксид азота(III) Оксид N 2 O 3 (триоксид диазота, азотистый ангидрид) — темносиняя жидкость, неустойчивая при обычных условиях, взаимодействует с водой, образуя азотистую кислоту HNO 2.
Оксид азота(III) Оксид N 2 O 3 (триоксид диазота, азотистый ангидрид) — темносиняя жидкость, неустойчивая при обычных условиях, взаимодействует с водой, образуя азотистую кислоту HNO 2.
 Получение: При пропускании электрического разряда через жидкий воздух N 2 O 3 можно получить в виде порошка голубого цвета:
Получение: При пропускании электрического разряда через жидкий воздух N 2 O 3 можно получить в виде порошка голубого цвета:
 Химические свойства: Кислотный оксид N 2 O 3 подвержен термической диссоциации: Являясь азотистым ангидридом, при взаимодействии с водой N 2 O 3 даёт азотистую кислоту:
Химические свойства: Кислотный оксид N 2 O 3 подвержен термической диссоциации: Являясь азотистым ангидридом, при взаимодействии с водой N 2 O 3 даёт азотистую кислоту:
 При взаимодействии с растворами щелочей образую тся соответствующие нитриты:
При взаимодействии с растворами щелочей образую тся соответствующие нитриты:
 Оксид азота(IV) Оксид азота NO 2, N 2 O 4 (диоксид азота) — бурый газ, токсичен, тяжелее воздуха, легко сжижается.
Оксид азота(IV) Оксид азота NO 2, N 2 O 4 (диоксид азота) — бурый газ, токсичен, тяжелее воздуха, легко сжижается.
 Получение: В лаборатории NO 2 обычно получают воздействием концентрированной азотной кислотой на медь:
Получение: В лаборатории NO 2 обычно получают воздействием концентрированной азотной кислотой на медь:
 Химические свойства: Взаимодействие с водой С растворами щелочей:
Химические свойства: Взаимодействие с водой С растворами щелочей:
 Взаимодействует с неметаллами (фосфор и углерод горят в нём). В этих реакциях NO 2 — окислитель:
Взаимодействует с неметаллами (фосфор и углерод горят в нём). В этих реакциях NO 2 — окислитель:
 Окисляет SO 2 в SO 3 — на этой реакции основан нитрозный метод получения серной кислоты:
Окисляет SO 2 в SO 3 — на этой реакции основан нитрозный метод получения серной кислоты:
 Оксид азота(V) Оксид азота N 2 O 5 (пентаоксид диазота, азотный ангидрид) — бесцветное кристаллическое вещество, легко разлагается на NO 2 и О 2. Сильный окислитель. В воде легко растворяется с образованием азотной кислоты HNO 3.
Оксид азота(V) Оксид азота N 2 O 5 (пентаоксид диазота, азотный ангидрид) — бесцветное кристаллическое вещество, легко разлагается на NO 2 и О 2. Сильный окислитель. В воде легко растворяется с образованием азотной кислоты HNO 3.
 Получение: Путём взаимодействия оксида азота(IV) с озоном:
Получение: Путём взаимодействия оксида азота(IV) с озоном:
 Химические свойства: Растворяется в воде с образованием азотной кислоты (обратимая реакция): Растворяется в щелочах с образованием нитратов:
Химические свойства: Растворяется в воде с образованием азотной кислоты (обратимая реакция): Растворяется в щелочах с образованием нитратов:
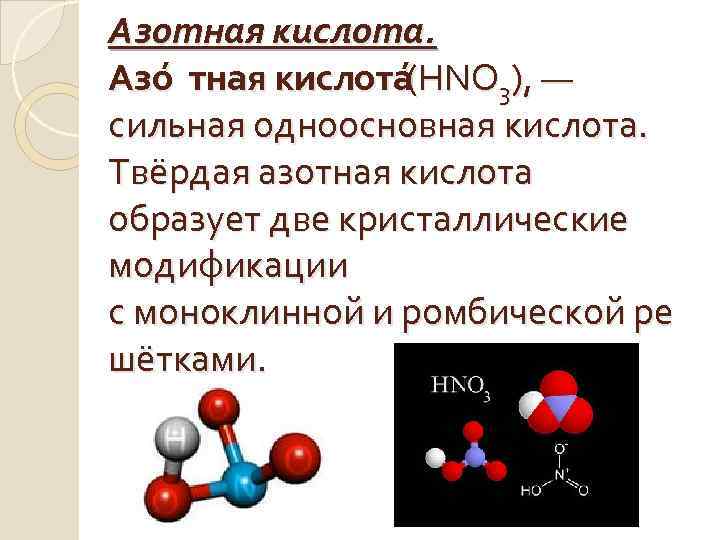 Азотная кислота. Азо тная кислота (HNO 3), — сильная одноосновная кислота. Твёрдая азотная кислота образует две кристаллические модификации с моноклинной и ромбической ре шётками.
Азотная кислота. Азо тная кислота (HNO 3), — сильная одноосновная кислота. Твёрдая азотная кислота образует две кристаллические модификации с моноклинной и ромбической ре шётками.
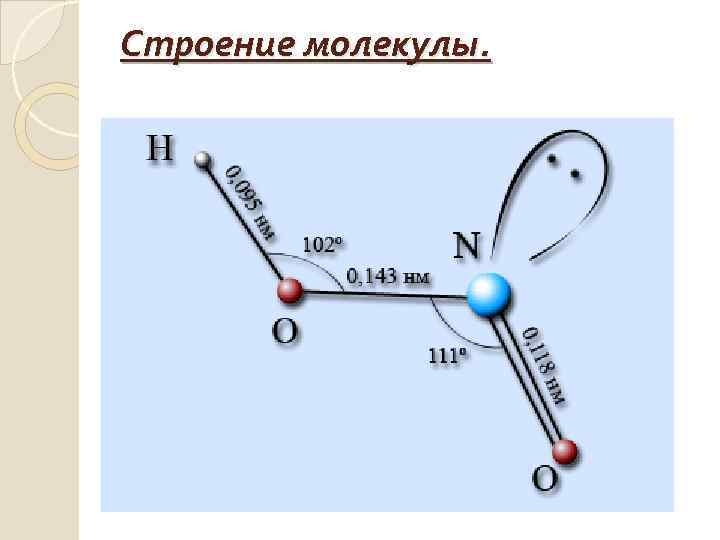 Строение молекулы.
Строение молекулы.
 Химические свойства: 1. Азотная кислота проявляет все типичные свойства кислот – взаимодействует с оксидами металлов, основаниями, солями:
Химические свойства: 1. Азотная кислота проявляет все типичные свойства кислот – взаимодействует с оксидами металлов, основаниями, солями:
 2. Взаимодействие с металлами:
2. Взаимодействие с металлами:
 3. Взаимодействие с неметаллами:
3. Взаимодействие с неметаллами:
 4. Концентрированная азотная кислота взаимодействует со сложными веществами, окисляя их:
4. Концентрированная азотная кислота взаимодействует со сложными веществами, окисляя их:
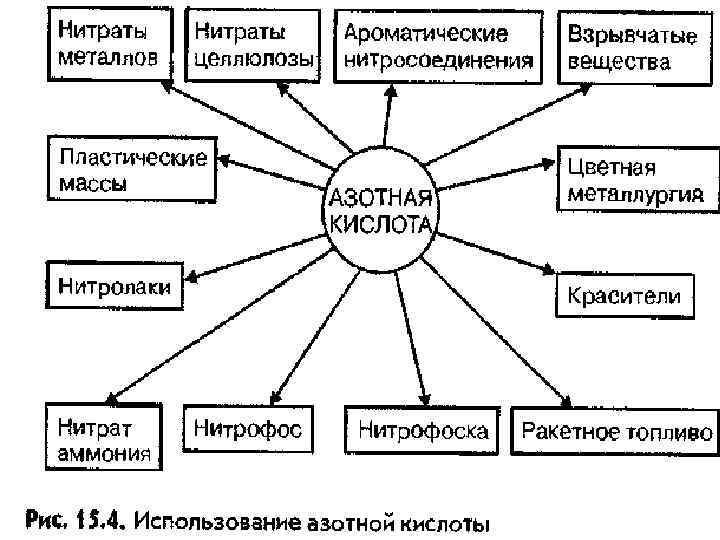
 Применение азотной кислоты
Применение азотной кислоты