Основные классы неорганических веществ.ppt
- Количество слайдов: 27
 Автор: Винюков А. В. Преподаватель Химии МОУДД ЦДОДД «Импульс» г. Черноголовка Учебное пособие для 8 -9 классов «ОСНОВНЫЕ КЛАССЫ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ»
Автор: Винюков А. В. Преподаватель Химии МОУДД ЦДОДД «Импульс» г. Черноголовка Учебное пособие для 8 -9 классов «ОСНОВНЫЕ КЛАССЫ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ»
 ОКСИДЫ ОСНОВАНИЯ СОЛИ КИСЛОТЫ Выберите класс неорганических соединений нажатием левой клавиши мыши. Дополнительные сведения по теме раздела находятся в приложении Приложения
ОКСИДЫ ОСНОВАНИЯ СОЛИ КИСЛОТЫ Выберите класс неорганических соединений нажатием левой клавиши мыши. Дополнительные сведения по теме раздела находятся в приложении Приложения
 ОКСИДЫ ОПРЕДЕЛЕНИЕ. ОБЩАЯ ФОРМУЛА ОКСИДОВ ХИМИЧЕСКИЕ СВОЙСТВА ОКСИДОВ КЛАССИФИКАЦИЯ ОКСИДОВ ОТДЕЛЬНЫЕ ПРЕДСТАВИТЕЛИ КЛАССА ОКСИДОВ СПОСОБЫ ПОЛУЧЕНИЯ ОКСИДОВ ПРОВЕРЬ СЕБЯ !!! Для выбора следующего класса неорганических соединений нажмите левой клавишей мышки на «домик»
ОКСИДЫ ОПРЕДЕЛЕНИЕ. ОБЩАЯ ФОРМУЛА ОКСИДОВ ХИМИЧЕСКИЕ СВОЙСТВА ОКСИДОВ КЛАССИФИКАЦИЯ ОКСИДОВ ОТДЕЛЬНЫЕ ПРЕДСТАВИТЕЛИ КЛАССА ОКСИДОВ СПОСОБЫ ПОЛУЧЕНИЯ ОКСИДОВ ПРОВЕРЬ СЕБЯ !!! Для выбора следующего класса неорганических соединений нажмите левой клавишей мышки на «домик»
 ОСНОВАНИЯ ОПРЕДЕЛЕНИЕ. ОБЩАЯ ФОРМУЛА ОСНОВАНИЙ ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ КЛАССИФИКАЦИЯ ОСНОВАНИЙ ОТДЕЛЬНЫЕ ПРЕДСТАВИТЕЛИ КЛАССА ОСНОВАНИЙ СПОСОБЫ ПОЛУЧЕНИЯ ОСНОВАНИЙ ПРОВЕРЬ СЕБЯ !!! Для выбора следующего класса неорганических соединений нажмите левой клавишей мышки на «домик»
ОСНОВАНИЯ ОПРЕДЕЛЕНИЕ. ОБЩАЯ ФОРМУЛА ОСНОВАНИЙ ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ КЛАССИФИКАЦИЯ ОСНОВАНИЙ ОТДЕЛЬНЫЕ ПРЕДСТАВИТЕЛИ КЛАССА ОСНОВАНИЙ СПОСОБЫ ПОЛУЧЕНИЯ ОСНОВАНИЙ ПРОВЕРЬ СЕБЯ !!! Для выбора следующего класса неорганических соединений нажмите левой клавишей мышки на «домик»
 КИСЛОТЫ ОПРЕДЕЛЕНИЕ. ОБЩАЯ ФОРМУЛА КИСЛОТ ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОТ КЛАССИФИКАЦИЯ КИСЛОТ ОТДЕЛЬНЫЕ ПРЕДСТАВИТЕЛИ КЛАССА КИСЛОТ СПОСОБЫ ПОЛУЧЕНИЯ КИСЛОТ ПРОВЕРЬ СЕБЯ !!! Для выбора следующего класса неорганических соединений нажмите левой клавишей мышки на «домик»
КИСЛОТЫ ОПРЕДЕЛЕНИЕ. ОБЩАЯ ФОРМУЛА КИСЛОТ ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОТ КЛАССИФИКАЦИЯ КИСЛОТ ОТДЕЛЬНЫЕ ПРЕДСТАВИТЕЛИ КЛАССА КИСЛОТ СПОСОБЫ ПОЛУЧЕНИЯ КИСЛОТ ПРОВЕРЬ СЕБЯ !!! Для выбора следующего класса неорганических соединений нажмите левой клавишей мышки на «домик»
 СОЛИ ОПРЕДЕЛЕНИЕ. ОБЩАЯ ФОРМУЛА СОЛЕЙ ХИМИЧЕСКИЕ СВОЙСТВА СОЛЕЙ КЛАССИФИКАЦИЯ СОЛЕЙ ОТДЕЛЬНЫЕ ПРЕДСТАВИТЕЛИ КЛАССА СОЛЕЙ СПОСОБЫ ПОЛУЧЕНИЯ СОЛЕЙ ПРОВЕРЬ СЕБЯ !!! Для выбора следующего класса неорганических соединений нажмите левой клавишей мышки на «домик»
СОЛИ ОПРЕДЕЛЕНИЕ. ОБЩАЯ ФОРМУЛА СОЛЕЙ ХИМИЧЕСКИЕ СВОЙСТВА СОЛЕЙ КЛАССИФИКАЦИЯ СОЛЕЙ ОТДЕЛЬНЫЕ ПРЕДСТАВИТЕЛИ КЛАССА СОЛЕЙ СПОСОБЫ ПОЛУЧЕНИЯ СОЛЕЙ ПРОВЕРЬ СЕБЯ !!! Для выбора следующего класса неорганических соединений нажмите левой клавишей мышки на «домик»
 -это сложные вещества, состоящие из двух элементов, один из которых кислород +n Э -2 O n = валентность элемента
-это сложные вещества, состоящие из двух элементов, один из которых кислород +n Э -2 O n = валентность элемента
 - это сложные вещества, состоящие из атомов металлов и гидроксильных групп ОН. +n Ме (OH)n n = валентность металла
- это сложные вещества, состоящие из атомов металлов и гидроксильных групп ОН. +n Ме (OH)n n = валентность металла
 это сложные вещества, которые состоят из атомов водорода и кислотного остатка Н+ Кост-n Значение n смотри в таблице растворимости
это сложные вещества, которые состоят из атомов водорода и кислотного остатка Н+ Кост-n Значение n смотри в таблице растворимости
 это сложные вещества, молекулы которых состоят из атомов металла и кислотного остатка Ме+m Кост-n m – валентность металла Значение n смотри в таблице растворимости Na. Cl Na. HCO 3 Ca. CO 3
это сложные вещества, молекулы которых состоят из атомов металла и кислотного остатка Ме+m Кост-n m – валентность металла Значение n смотри в таблице растворимости Na. Cl Na. HCO 3 Ca. CO 3
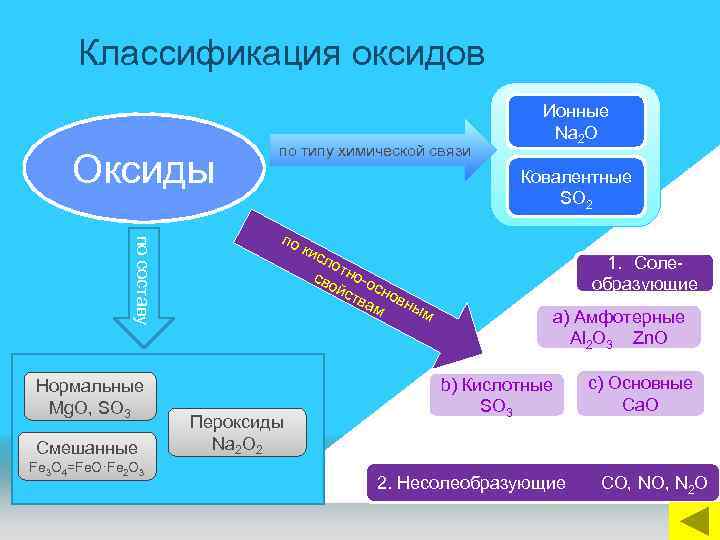 Классификация оксидов Оксиды по составу Нормальные Mg. O, SO 3 Смешанные Fe 3 O 4=Fe. O·Fe 2 O 3 по типу химической связи Ионные Na 2 O Ковалентные SO 2 по Пероксиды Na 2 O 2 кис ло т сво но-о йст сно ва вны м м 1. Солеобразующие a) Амфотерные Аl 2 O 3 Zn. O b) Кислотные SO 3 2. Несолеобразующие c) Основные Ca. O СО, NO, N 2 O
Классификация оксидов Оксиды по составу Нормальные Mg. O, SO 3 Смешанные Fe 3 O 4=Fe. O·Fe 2 O 3 по типу химической связи Ионные Na 2 O Ковалентные SO 2 по Пероксиды Na 2 O 2 кис ло т сво но-о йст сно ва вны м м 1. Солеобразующие a) Амфотерные Аl 2 O 3 Zn. O b) Кислотные SO 3 2. Несолеобразующие c) Основные Ca. O СО, NO, N 2 O
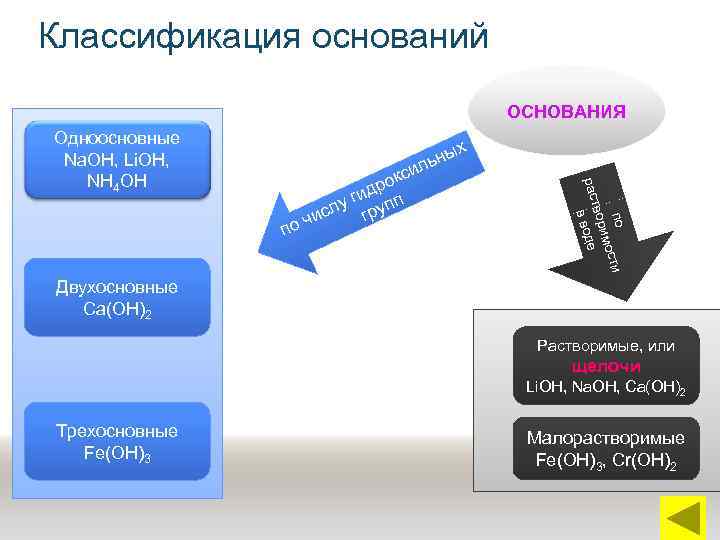 Классификация оснований ОСНОВАНИЯ Одноосновные Na. ОН, Li. ОН, NН 4 ОН х ч по ти мос вори раст воде в по с рок д у ги упп исл гр ьны ил Двухосновные Са(ОН)2 Растворимые, или щелочи Li. ОН, Nа. ОН, Са(ОН)2 Трехосновные Fe(ОН)3 Малорастворимые Fe(ОН)3, Сr(ОН)2
Классификация оснований ОСНОВАНИЯ Одноосновные Na. ОН, Li. ОН, NН 4 ОН х ч по ти мос вори раст воде в по с рок д у ги упп исл гр ьны ил Двухосновные Са(ОН)2 Растворимые, или щелочи Li. ОН, Nа. ОН, Са(ОН)2 Трехосновные Fe(ОН)3 Малорастворимые Fe(ОН)3, Сr(ОН)2
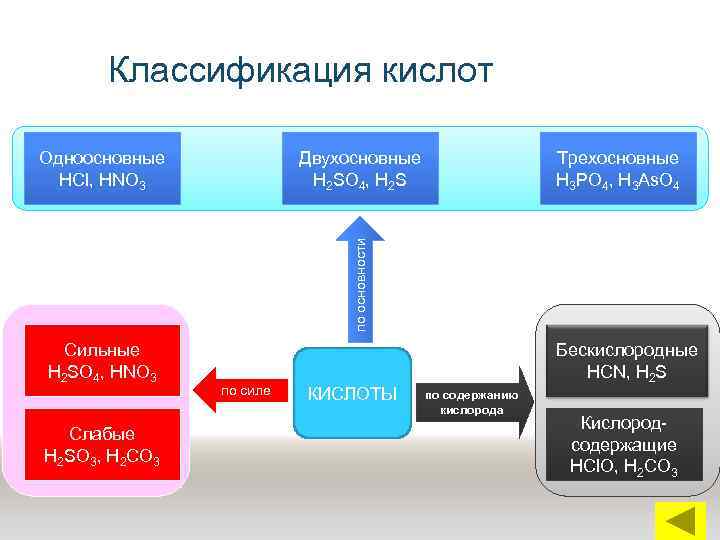 Классификация кислот Двухосновные Н 2 SO 4, Н 2 S Трехосновные Н 3 РО 4, Н 3 Аs. О 4 по основности Одноосновные НСl, НNО 3 Сильные Н 2 SO 4, НNО 3 Слабые Н 2 SО 3, Н 2 СО 3 по силе КИСЛОТЫ Бескислородные НСN, Н 2 S по содержанию кислорода Кислородсодержащие НСl. О, Н 2 СО 3
Классификация кислот Двухосновные Н 2 SO 4, Н 2 S Трехосновные Н 3 РО 4, Н 3 Аs. О 4 по основности Одноосновные НСl, НNО 3 Сильные Н 2 SO 4, НNО 3 Слабые Н 2 SО 3, Н 2 СО 3 по силе КИСЛОТЫ Бескислородные НСN, Н 2 S по содержанию кислорода Кислородсодержащие НСl. О, Н 2 СО 3
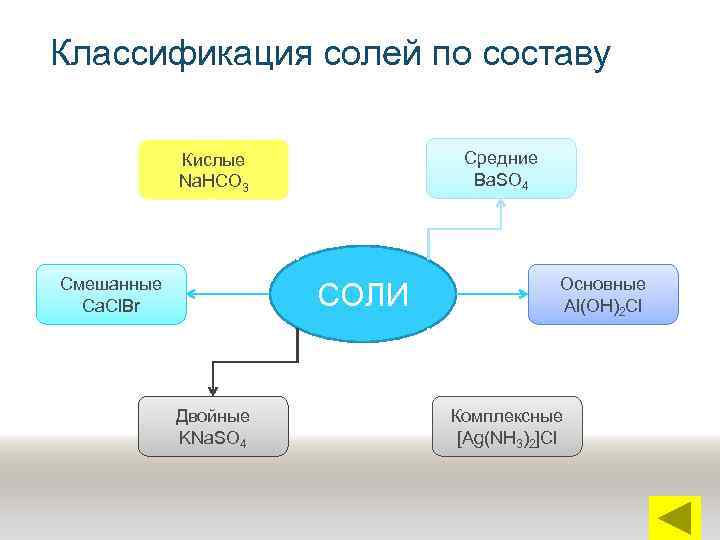 Классификация солей по составу Средние Ba. SO 4 Кислые Na. HCO 3 Смешанные Ca. Cl. Br СОЛИ Двойные KNa. SO 4 Основные Al(OH)2 Cl Комплексные [Ag(NH 3)2]Cl
Классификация солей по составу Средние Ba. SO 4 Кислые Na. HCO 3 Смешанные Ca. Cl. Br СОЛИ Двойные KNa. SO 4 Основные Al(OH)2 Cl Комплексные [Ag(NH 3)2]Cl
 ПОЛУЧЕНИЕ ОКСИДОВ 1. Взаимодействие простых веществ с кислородом a) Me + O 2 = b) не. Ме + О 2 = 2. Горение сложных веществ 3. Окисление оксидов СН 4 + О 2 = СО 2 + Н 2 О 2 СО + О 2 = 2 СО 2 4. Разложение солей при нагревании Са. СО 3 = Са. О + СО 2 5. Разложение кислот при нагревании Н 2 СО 3 = СО 2 + Н 2 О 6. Разложение нерастворимых оснований при нагревании Сu(ОН)2 = Сu. О + СО 2
ПОЛУЧЕНИЕ ОКСИДОВ 1. Взаимодействие простых веществ с кислородом a) Me + O 2 = b) не. Ме + О 2 = 2. Горение сложных веществ 3. Окисление оксидов СН 4 + О 2 = СО 2 + Н 2 О 2 СО + О 2 = 2 СО 2 4. Разложение солей при нагревании Са. СО 3 = Са. О + СО 2 5. Разложение кислот при нагревании Н 2 СО 3 = СО 2 + Н 2 О 6. Разложение нерастворимых оснований при нагревании Сu(ОН)2 = Сu. О + СО 2
 ПОЛУЧЕНИЕ ОСНОВАНИЙ 1. Взаимодействие активных металлов с водой Me + Н 2 O = Ме. ОН + Н 2 2. Взаимодействие оксидов активных металлов с водой Me. О + Н 2 O = Ме. ОН 3. Электролиз расплавов солей (получение Na. OH, KOH в промышленности) Na. Cl + H 2 O = Na. ОН + HСl (для щелочей) Cu. Cl 2 + 2 Na. OH = Cu(OH)2 + 2 Na. Cl (для нерастворимых оснований обязательно присутствие щелочи)
ПОЛУЧЕНИЕ ОСНОВАНИЙ 1. Взаимодействие активных металлов с водой Me + Н 2 O = Ме. ОН + Н 2 2. Взаимодействие оксидов активных металлов с водой Me. О + Н 2 O = Ме. ОН 3. Электролиз расплавов солей (получение Na. OH, KOH в промышленности) Na. Cl + H 2 O = Na. ОН + HСl (для щелочей) Cu. Cl 2 + 2 Na. OH = Cu(OH)2 + 2 Na. Cl (для нерастворимых оснований обязательно присутствие щелочи)
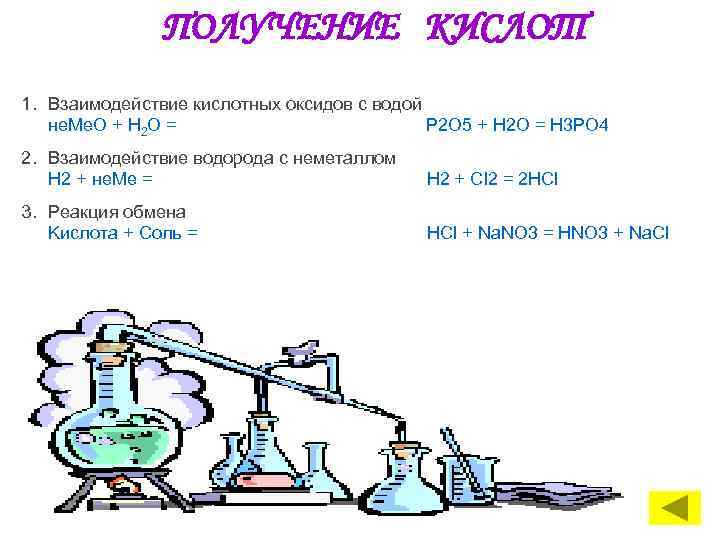 ПОЛУЧЕНИЕ КИСЛОТ 1. Взаимодействие кислотных оксидов с водой не. Me. О + Н 2 O = P 2 O 5 + H 2 O = H 3 PO 4 2. Взаимодействие водорода с неметаллом Н 2 + не. Ме = Н 2 + Сl 2 = 2 HCl 3. Реакция обмена Kислота + Cоль = HCl + Na. NO 3 = HNO 3 + Na. Cl
ПОЛУЧЕНИЕ КИСЛОТ 1. Взаимодействие кислотных оксидов с водой не. Me. О + Н 2 O = P 2 O 5 + H 2 O = H 3 PO 4 2. Взаимодействие водорода с неметаллом Н 2 + не. Ме = Н 2 + Сl 2 = 2 HCl 3. Реакция обмена Kислота + Cоль = HCl + Na. NO 3 = HNO 3 + Na. Cl
 ПОЛУЧЕНИЕ СОЛЕЙ Взаимодействием: • Металла с неметаллом Са + Сl 2 = Са. Сl • Основного оксида с кислотным оксидом Са. О + СО 2 = Са. СО 3 • Основного оксида с кислотой Са. О + 2 НСl = Ca. Cl 2 + H 2 О • Кислотного оксида с основанием CO 2 + Ca(OH)2 = Ca. CO 3 + H 2 O • Кислоты с основанием (р. нейтрализации) 2 HCl + Ca(OH)2 = Ca. Cl 2 + 2 H 2 O • Соли с кислотой Na. Cl + HNO 3 = Na. NO 3 + HCl • Соли с щелочью Na. Cl + KOH = Na. OH + KCl • Соли с солью Na. Cl + Ag. NO 3 = Na. NO 3 + Ag. Cl • Металла с солью (см. ряд активности металлов) Na + Ag. NO 3 = Na. NO 3 + Ag • Металла с кислотой (см. ряд активн. металлов) Са + 2 НСl = Ca. Cl 2 + H 2
ПОЛУЧЕНИЕ СОЛЕЙ Взаимодействием: • Металла с неметаллом Са + Сl 2 = Са. Сl • Основного оксида с кислотным оксидом Са. О + СО 2 = Са. СО 3 • Основного оксида с кислотой Са. О + 2 НСl = Ca. Cl 2 + H 2 О • Кислотного оксида с основанием CO 2 + Ca(OH)2 = Ca. CO 3 + H 2 O • Кислоты с основанием (р. нейтрализации) 2 HCl + Ca(OH)2 = Ca. Cl 2 + 2 H 2 O • Соли с кислотой Na. Cl + HNO 3 = Na. NO 3 + HCl • Соли с щелочью Na. Cl + KOH = Na. OH + KCl • Соли с солью Na. Cl + Ag. NO 3 = Na. NO 3 + Ag. Cl • Металла с солью (см. ряд активности металлов) Na + Ag. NO 3 = Na. NO 3 + Ag • Металла с кислотой (см. ряд активн. металлов) Са + 2 НСl = Ca. Cl 2 + H 2
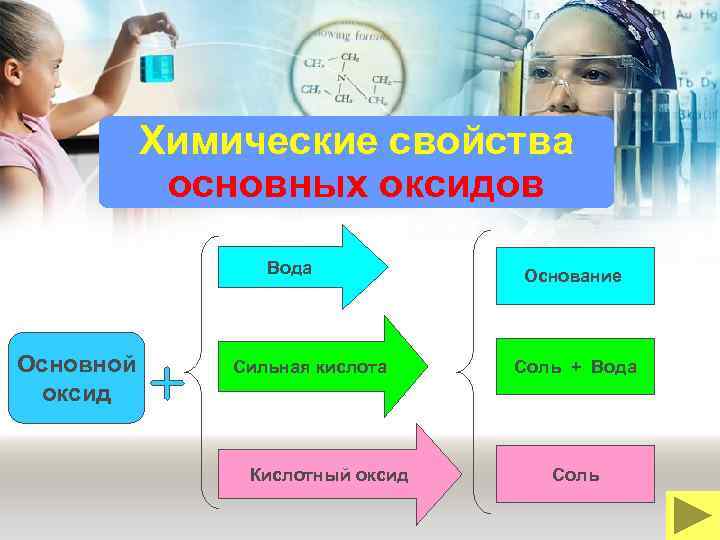 Химические свойства основных оксидов Вода Основной оксид Сильная кислота Кислотный оксид Основание Соль + Вода Соль
Химические свойства основных оксидов Вода Основной оксид Сильная кислота Кислотный оксид Основание Соль + Вода Соль
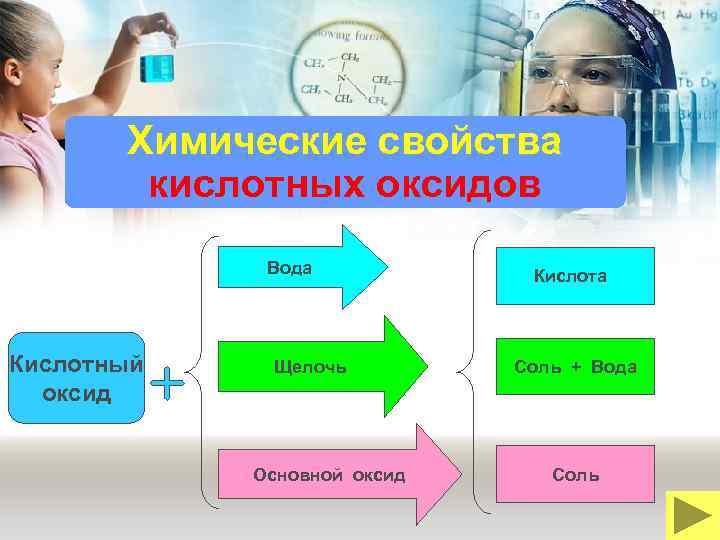 Химические свойства кислотных оксидов Вода Кислотный оксид Щелочь Основной оксид Кислота Соль + Вода Соль
Химические свойства кислотных оксидов Вода Кислотный оксид Щелочь Основной оксид Кислота Соль + Вода Соль
 Химические свойства амфотерных оксидов
Химические свойства амфотерных оксидов
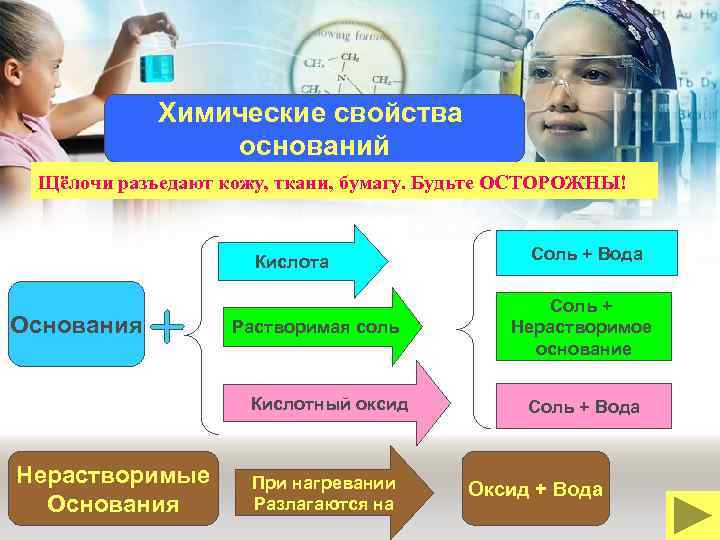 Химические свойства оснований Щёлочи разъедают кожу, ткани, бумагу. Будьте ОСТОРОЖНЫ! Кислота Основания Растворимая соль Кислотный оксид Нерастворимые Основания При нагревании Разлагаются на Соль + Вода Соль + Нерастворимое основание Соль + Вода Оксид + Вода
Химические свойства оснований Щёлочи разъедают кожу, ткани, бумагу. Будьте ОСТОРОЖНЫ! Кислота Основания Растворимая соль Кислотный оксид Нерастворимые Основания При нагревании Разлагаются на Соль + Вода Соль + Нерастворимое основание Соль + Вода Оксид + Вода
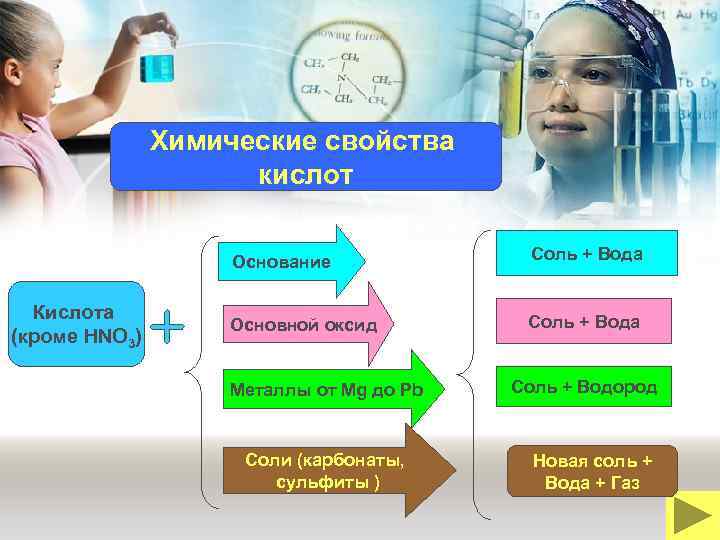 Химические свойства кислот Основание Кислота (кроме HNO 3) Соль + Вода Основной оксид Соль + Вода Металлы от Mg до Pb Соли (карбонаты, сульфиты ) Соль + Водород Новая соль + Вода + Газ
Химические свойства кислот Основание Кислота (кроме HNO 3) Соль + Вода Основной оксид Соль + Вода Металлы от Mg до Pb Соли (карбонаты, сульфиты ) Соль + Водород Новая соль + Вода + Газ
 ТБ при работе с кислотами Запомни правило: «Сначала вода, потом кислота, иначе произойдет ужасное» . Если же сделать наоборот, то первые же порции воды, оставшись наверху (вода легче кислоты) и взаимодействуя с кислотой, разогреваются так сильно, что вскипают и разбрызгиваются вместе с кислотой; могут попасть в глаза, на лицо и одежду. v. При попадании концентрированных кислот на кожу рук или лицо: их смывают вначале большим количеством воды под краном в течение 10 -15 минут, а затем 3% раствором питьевой соды.
ТБ при работе с кислотами Запомни правило: «Сначала вода, потом кислота, иначе произойдет ужасное» . Если же сделать наоборот, то первые же порции воды, оставшись наверху (вода легче кислоты) и взаимодействуя с кислотой, разогреваются так сильно, что вскипают и разбрызгиваются вместе с кислотой; могут попасть в глаза, на лицо и одежду. v. При попадании концентрированных кислот на кожу рук или лицо: их смывают вначале большим количеством воды под краном в течение 10 -15 минут, а затем 3% раствором питьевой соды.
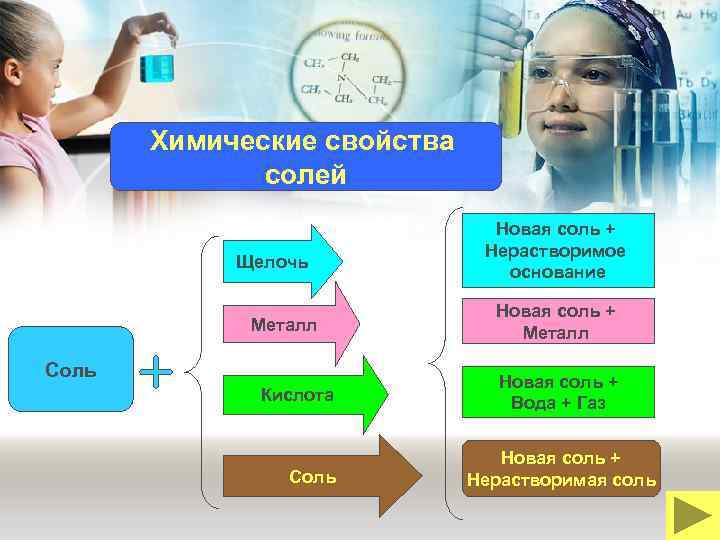 Химические свойства солей Щелочь Металл Соль Кислота Соль Новая соль + Нерастворимое основание Новая соль + Металл Новая соль + Вода + Газ Новая соль + Нерастворимая соль
Химические свойства солей Щелочь Металл Соль Кислота Соль Новая соль + Нерастворимое основание Новая соль + Металл Новая соль + Вода + Газ Новая соль + Нерастворимая соль
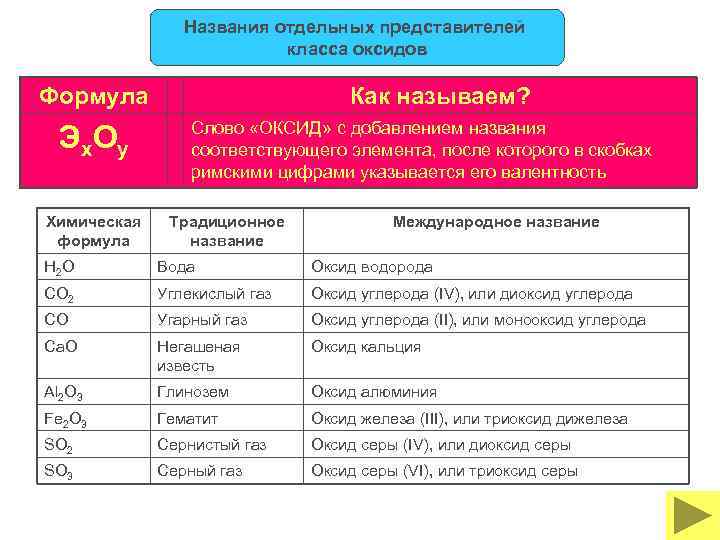 Названия отдельных представителей класса оксидов Формула Э х. О у Химическая формула Как называем? Слово «ОКСИД» с добавлением названия соответствующего элемента, после которого в скобках римскими цифрами указывается его валентность Традиционное название Международное название H 2 O Вода Оксид водорода CO 2 Углекислый газ Оксид углерода (IV), или диоксид углерода CO Угарный газ Оксид углерода (II), или монооксид углерода Ca. O Негашеная известь Оксид кальция Al 2 O 3 Глинозем Оксид алюминия Fe 2 O 3 Гематит Оксид железа (III), или триоксид дижелеза SO 2 Сернистый газ Оксид серы (IV), или диоксид серы SO 3 Серный газ Оксид серы (VI), или триоксид серы
Названия отдельных представителей класса оксидов Формула Э х. О у Химическая формула Как называем? Слово «ОКСИД» с добавлением названия соответствующего элемента, после которого в скобках римскими цифрами указывается его валентность Традиционное название Международное название H 2 O Вода Оксид водорода CO 2 Углекислый газ Оксид углерода (IV), или диоксид углерода CO Угарный газ Оксид углерода (II), или монооксид углерода Ca. O Негашеная известь Оксид кальция Al 2 O 3 Глинозем Оксид алюминия Fe 2 O 3 Гематит Оксид железа (III), или триоксид дижелеза SO 2 Сернистый газ Оксид серы (IV), или диоксид серы SO 3 Серный газ Оксид серы (VI), или триоксид серы



