Аутоиммунная патология.ppt
- Количество слайдов: 86

Аутоиммунная патология. Классификация. Механизмы развития. Иммунодиагностика. профессор Бажукова Т. А. зав. каф. микробиологии, вирусологии и иммунологии

Аутоиммунные заболевания • Аутоиммунные заболевания, развивающиеся в результате реакций ИС на аутоантигены, которые приводят к повреждению клеток, экспрессирующих на своей поверхности аутоантигены. • Аутоиммунные реакции – реакции ИС на структурные компоненты органов и тканей собственного организма, называемые аутоантигенами.
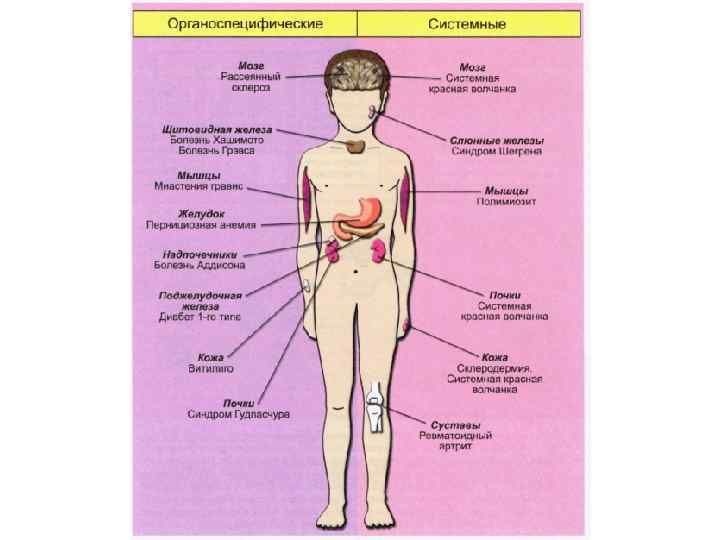
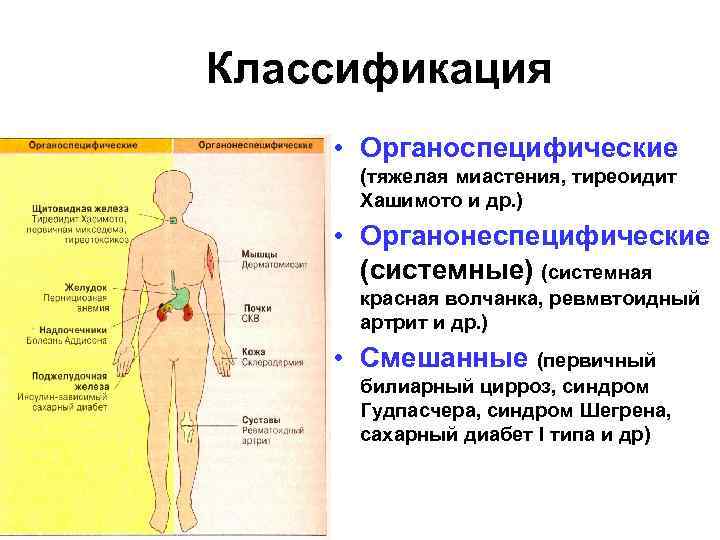
Классификация • Органоспецифические (тяжелая миастения, тиреоидит Хашимото и др. ) • Органонеспецифические (системные) (системная красная волчанка, ревмвтоидный артрит и др. ) • Смешанные (первичный билиарный цирроз, синдром Гудпасчера, синдром Шегрена, сахарный диабет I типа и др)
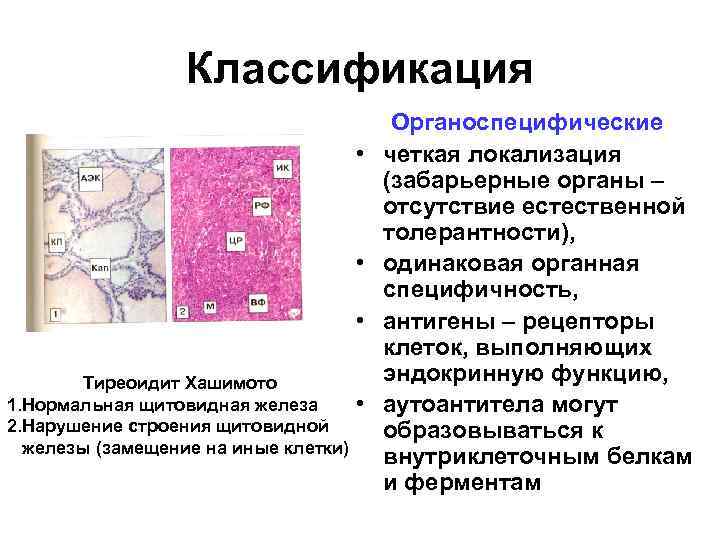
Классификация • • • Тиреоидит Хашимото 1. Нормальная щитовидная железа 2. Нарушение строения щитовидной железы (замещение на иные клетки) • Органоспецифические четкая локализация (забарьерные органы – отсутствие естественной толерантности), одинаковая органная специфичность, антигены – рецепторы клеток, выполняющих эндокринную функцию, аутоантитела могут образовываться к внутриклеточным белкам и ферментам
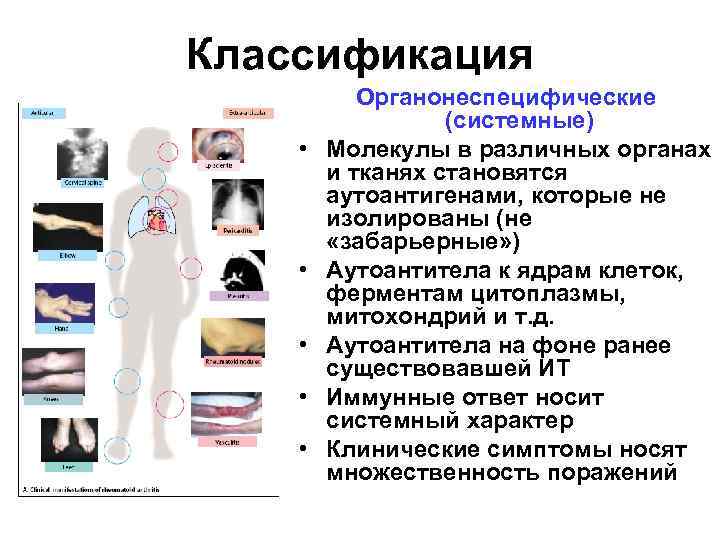
Классификация • • • Органонеспецифические (системные) Молекулы в различных органах и тканях становятся аутоантигенами, которые не изолированы (не «забарьерные» ) Аутоантитела к ядрам клеток, ферментам цитоплазмы, митохондрий и т. д. Аутоантитела на фоне ранее существовавшей ИТ Иммунные ответ носит системный характер Клинические симптомы носят множественность поражений
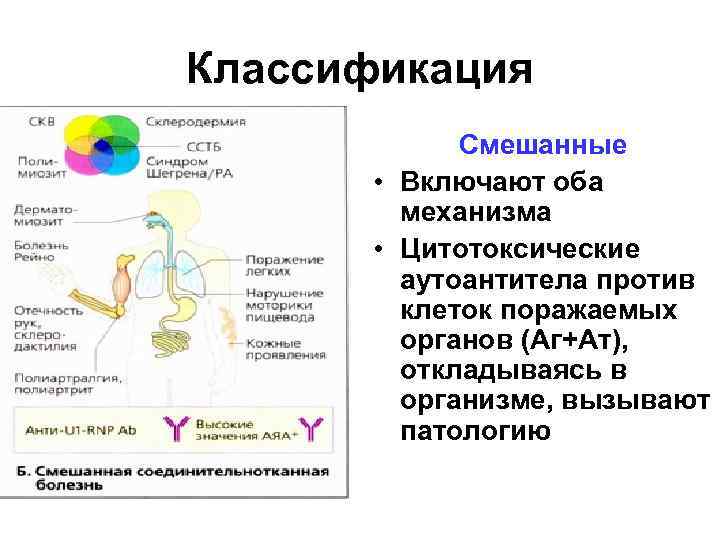
Классификация Смешанные • Включают оба механизма • Цитотоксические аутоантитела против клеток поражаемых органов (Аг+Ат), откладываясь в организме, вызывают патологию
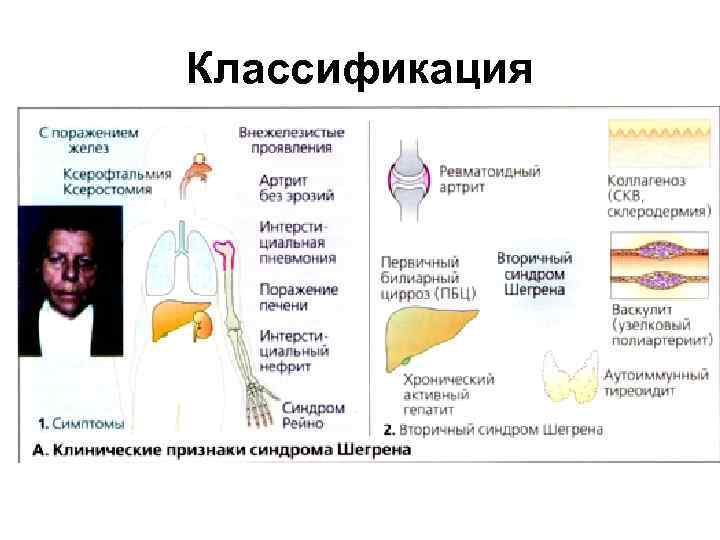
Классификация
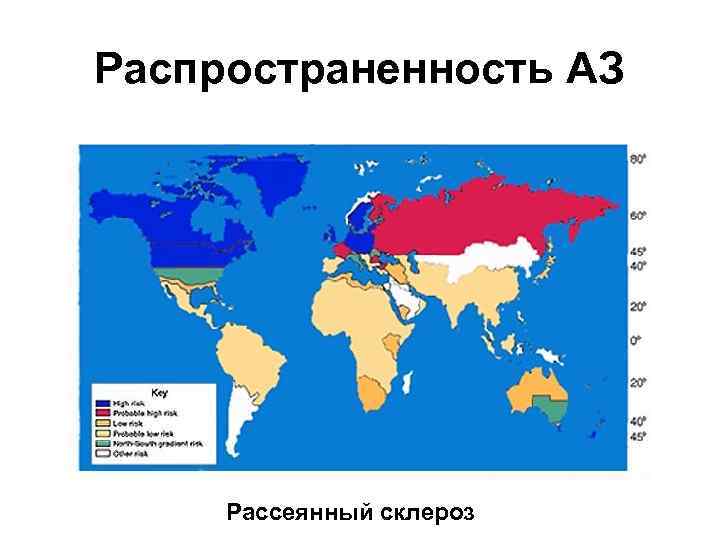
Распространенность АЗ Рассеянный склероз
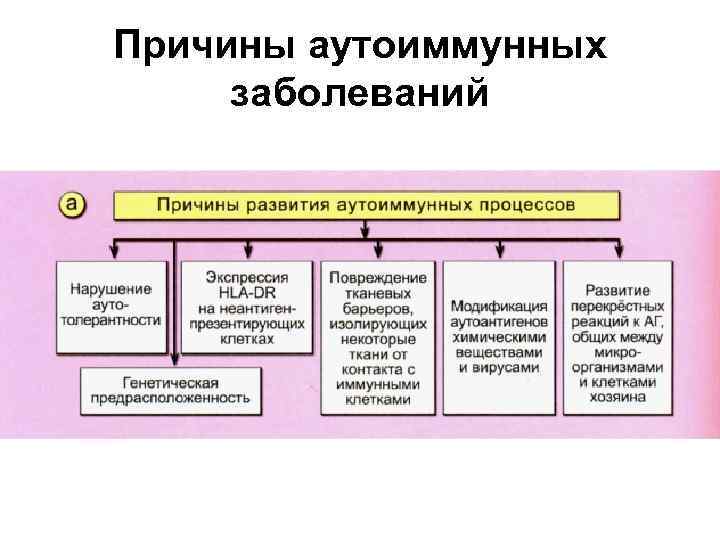
Причины аутоиммунных заболеваний
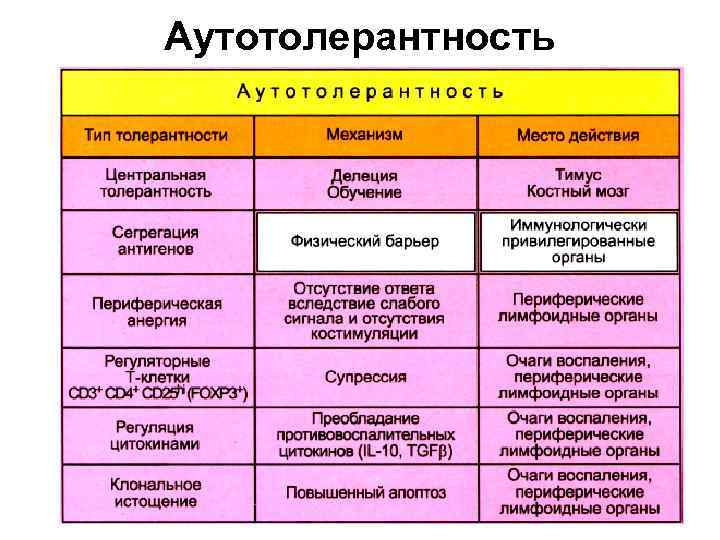
Аутотолерантность

Механизмы аутотолерантности • Центральная толерантность • Периферическая толерантность • В-клеточная толерантность

Центральная толерантность • Центральная толерантность – процесс формирования иммунологической толерантности, основанный на элиминации из организма аутореактивных ИКК, происходящий в центральных органах ИС (тимусе и костном мозге) • Тимус – положительная селекция тимоцитов ( выбраковка клеток неспособных распознать пептиды, представленные в составе МНС на эпителиальных клетках тимуса)
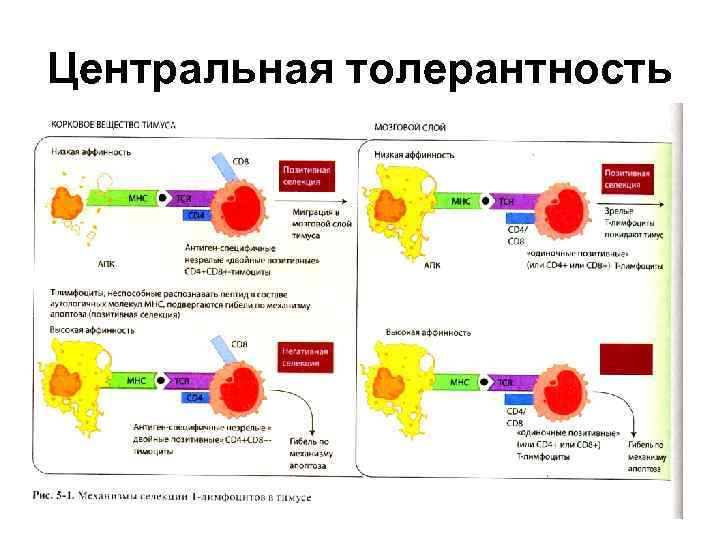
Центральная толерантность

Периферическая толерантность • Периферическая толерантность – подавление функциональной активности и элиминация аутореактивных клонов , выживших после отрицательной селекции в тимусе и покинувших вилочковую железу. • Механизмы : • Игнорирование антигена • Раздельное местонахождение аутореактивных Т-клеток и аутоантигенов • Ко-стимуляция и анергия • Супрессорные и регуляторные механизмы

Периферическая толерантность Игнорирование антигена • Слабо выраженная экспрессия антигенного пептида или его недоступность для распознавания аутореактивными клонами Т-лимфоцитов • Экспрессия Аг в плохо кровоснабжаемых тканях. • Отсутствие презентации Аг в составе молекулы МНС (ограниченное представительство АПК в тканях нелимфоидного происхождения
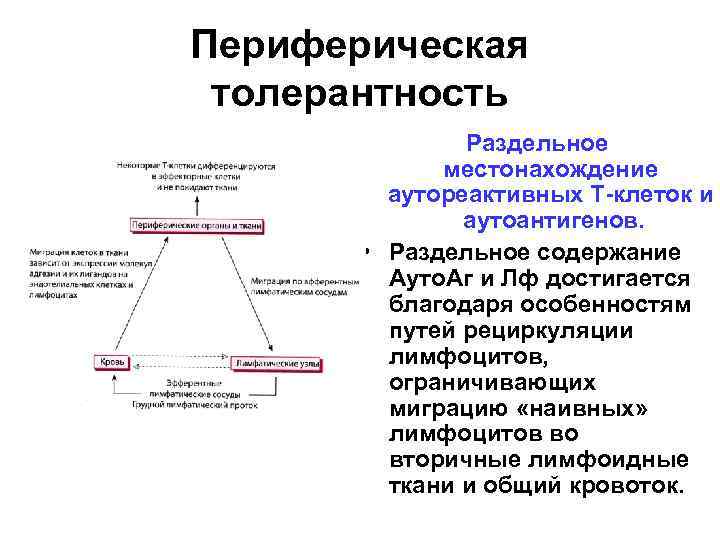
Периферическая толерантность Раздельное местонахождение аутореактивных Т-клеток и аутоантигенов. • Раздельное содержание Ауто. Аг и Лф достигается благодаря особенностям путей рециркуляции лимфоцитов, ограничивающих миграцию «наивных» лимфоцитов во вторичные лимфоидные ткани и общий кровоток.
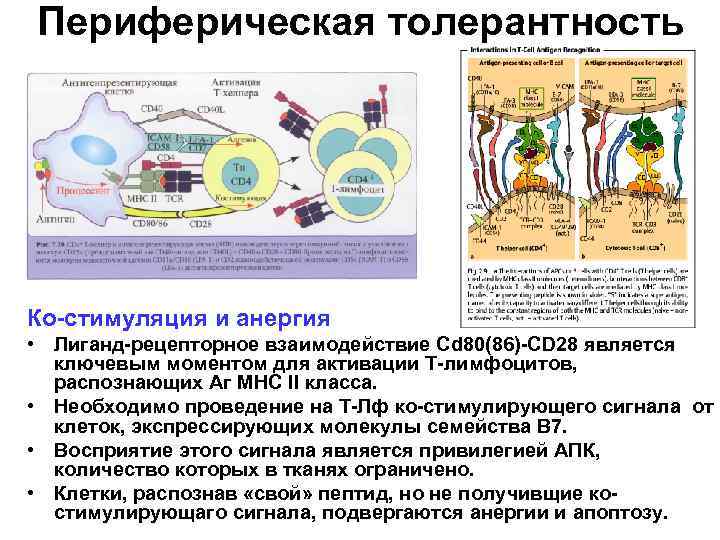
Периферическая толерантность Ко-стимуляция и анергия • Лиганд-рецепторное взаимодействие Cd 80(86)-CD 28 является ключевым моментом для активации Т-лимфоцитов, распознающих Аг МНС II класса. • Необходимо проведение на Т-Лф ко-стимулирующего сигнала от клеток, экспрессирующих молекулы семейства В 7. • Восприятие этого сигнала является привилегией АПК, количество которых в тканях ограничено. • Клетки, распознав «свой» пептид, но не получивщие костимулирующаго сигнала, подвергаются анергии и апоптозу.
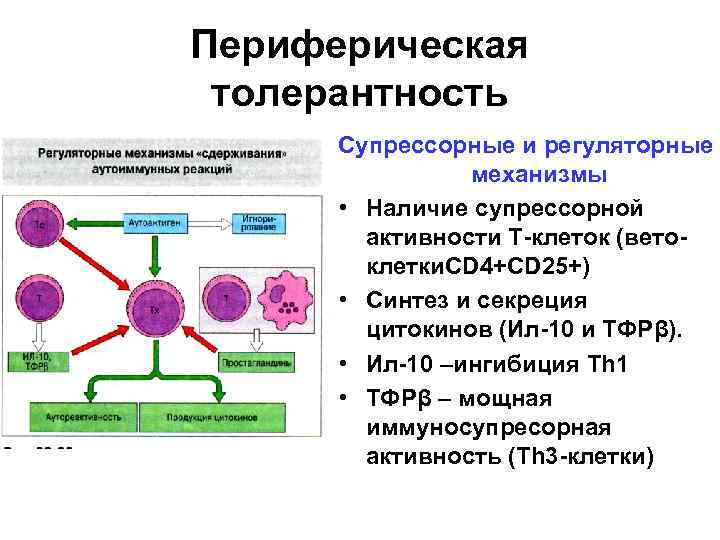
Периферическая толерантность Супрессорные и регуляторные механизмы • Наличие супрессорной активности Т-клеток (ветоклетки. CD 4+CD 25+) • Синтез и секреция цитокинов (Ил-10 и ТФРβ). • Ил-10 –ингибиция Тh 1 • ТФРβ – мощная иммуносупресорная активность (Тh 3 -клетки)
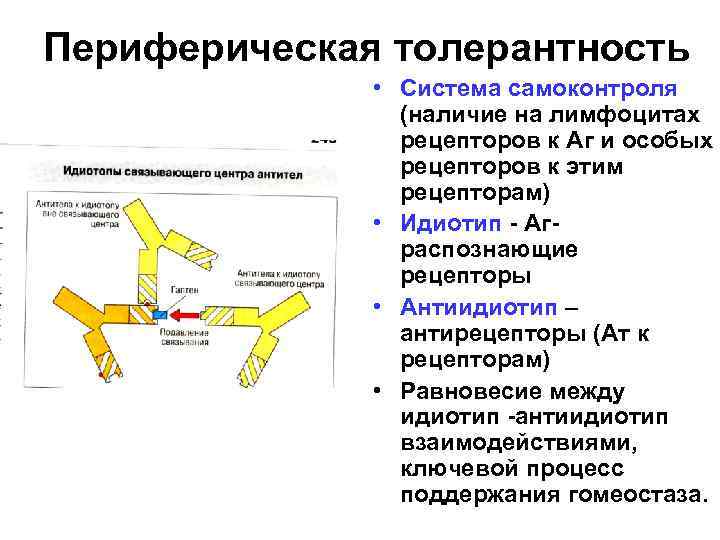
Периферическая толерантность • Система самоконтроля (наличие на лимфоцитах рецепторов к Аг и особых рецепторов к этим рецепторам) • Идиотип - Аграспознающие рецепторы • Антиидиотип – антирецепторы (Ат к рецепторам) • Равновесие между идиотип -антиидиотип взаимодействиями, ключевой процесс поддержания гомеостаза.

В-клеточная толерантность * • Отрицательная селекция Влимфоцитов осуществляется в костном мозге на стадии незрелых В -клеток, погибающих по механизму апоптоза в результате перекрестного связывания мембранного Ig. M. • Неполноценная активация В-лф приводит к анергии и апоптозу. • В –клетки нуждаются в костимулирующем сигнале от Т-клеток (молекула CD 40 экспрессируемая Т-лф)

Механизмы преодоления толерантности • Теория «запретных» клонов • Теория секвестрированных (забарьерных) антигенов • Теория рассройства иммунологической регуляции • Теория нарушения идиотип-антиидиотипических взаимодействий • Теория поликлональной активации В-лимфоцитов • Теория развития аутоиммунитета под влиянием суперантигенов • Теория генетической предрасположенности • Теория молекулярной мимикрии
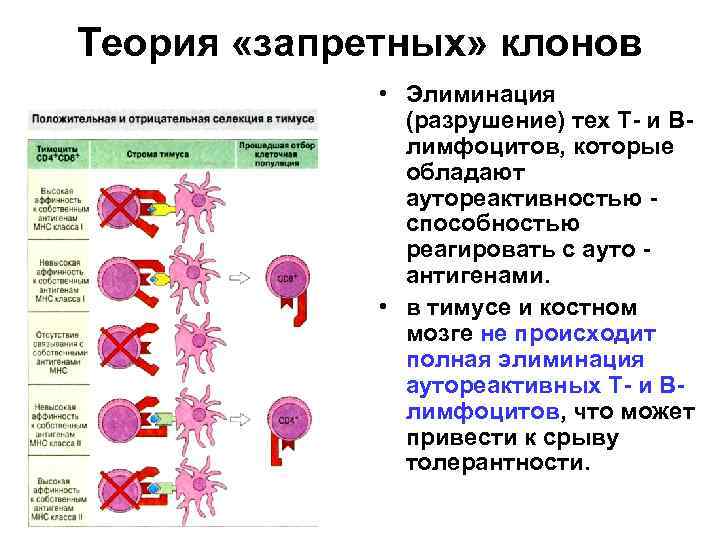
Теория «запретных» клонов • Элиминация (разрушение) тех Т- и Влимфоцитов, которые обладают аутореактивностью способностью реагировать с ауто антигенами. • в тимусе и костном мозге не происходит полная элиминация аутореактивных Т- и Влимфоцитов, что может привести к срыву толерантности.
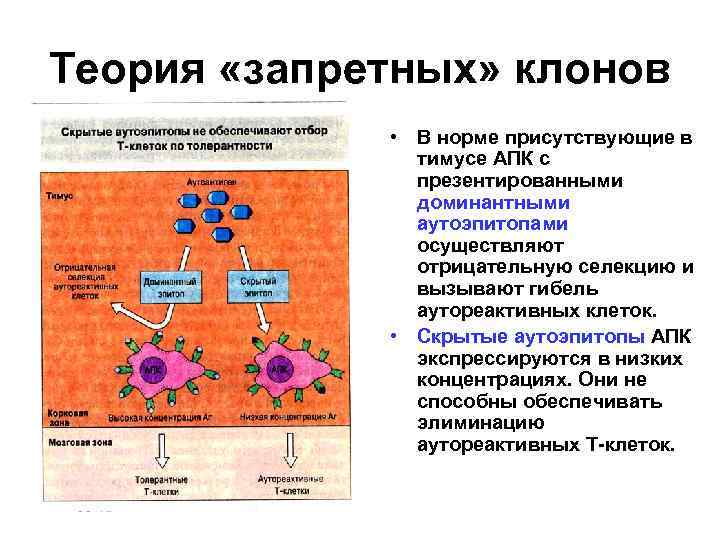
Теория «запретных» клонов • В норме присутствующие в тимусе АПК с презентированными доминантными аутоэпитопами осуществляют отрицательную селекцию и вызывают гибель аутореактивных клеток. • Скрытые аутоэпитопы АПК экспрессируются в низких концентрациях. Они не способны обеспечивать элиминацию аутореактивных Т-клеток.
Теория секвестрированных (забарьерных) антигенов • Определенные ткани ограждены гистогематическими барьерами (половые железы, ткани глаза, мозга, щитовидной железы и др. ). • Антигены таких тканей не контактируют с лимфоцитами и не происходит элиминации соответствующих клонов клеток. • При нарушении гистогематического барьера и попадании антигенов в кровоток собственные ИКК распознают их как чужеродные и запускают весь механизм иммунного ответа.
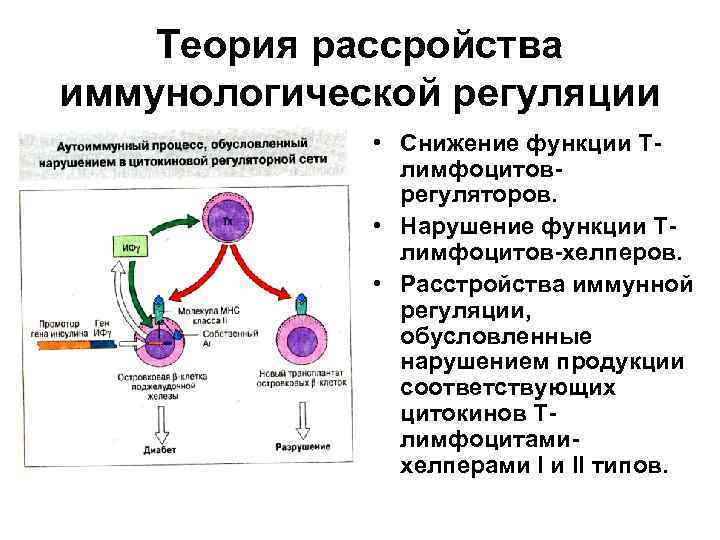
Теория рассройства иммунологической регуляции • Снижение функции Тлимфоцитоврегуляторов. • Нарушение функции Тлимфоцитов-хелперов. • Расстройства иммунной регуляции, обусловленные нарушением продукции соответствующих цитокинов Тлимфоцитамихелперами I и II типов.
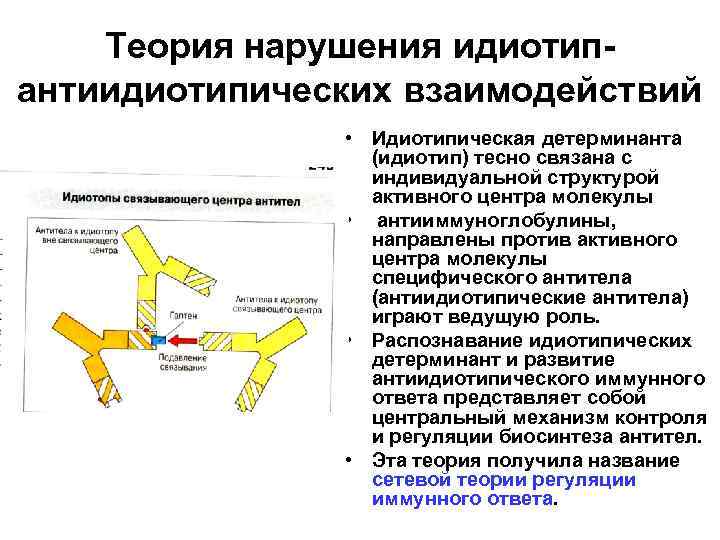
Теория нарушения идиотипантиидиотипических взаимодействий • Идиотипическая детерминанта (идиотип) тесно связана с индивидуальной структурой активного центра молекулы • антииммуноглобулины, направлены против активного центра молекулы специфического антитела (антиидиотипические антитела) играют ведущую роль. • Распознавание идиотипических детерминант и развитие антиидиотипического иммунного ответа представляет собой центральный механизм контроля и регуляции биосинтеза антител. • Эта теория получила название сетевой теории регуляции иммунного ответа.

Теория нарушения идиотипантиидиотипических взаимодействий • В теории Ерне можно выделить два основных положения: 1. Иммуноглобулины, а также Ig рецепторы на поверхности антигенреактивных Т- и В-лимфоцитов имеют детерминанты, обладающие (ауто-) антигенными свойствами, и получившие название “идиотип” (идиотипические детерминанты); 2. В организме есть лимфоциты, способные в норме распознать своими рецепторами идиотипические детерминанты и реализовать антиидиотипический ответ. Антиидиотипическое антитело также может быть распознано и на него вырабатываются антиаyтиидиотипические антитела до тех пор, пока иммунный ответ не угаснет. • Нарушение идиотип-антиидиотипических взаимодействий будет способствовать развитию аутоиммунных заболеваний
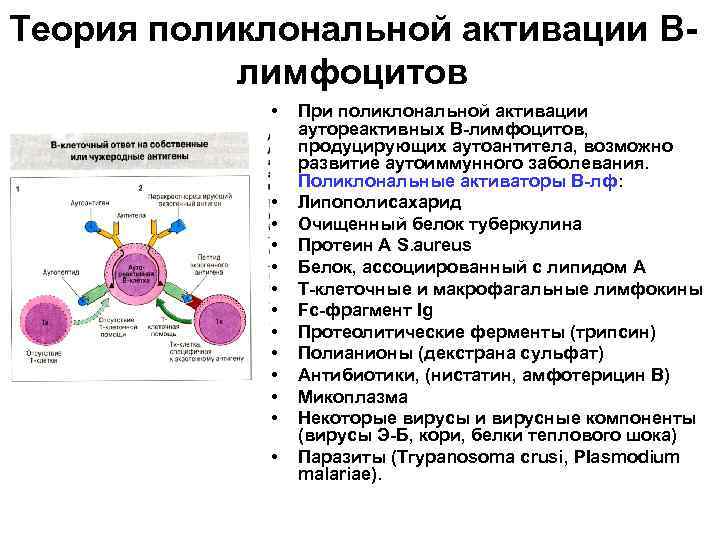
Теория поликлональной активации Влимфоцитов • • • • При поликлональной активации аутореактивных В-лимфоцитов, продуцирующих аутоантитела, возможно развитие аутоиммунного заболевания. Поликлональные активаторы В-лф: Липополисахарид Очищенный белок туберкулина Протеин А S. aureus Белок, ассоциированный с липидом А Т-клеточные и макрофагальные лимфокины Fс-фрагмент Ig Протеолитические ферменты (трипсин) Полианионы (декстрана сульфат) Антибиотики, (нистатин, амфотерицин В) Микоплазма Некоторые вирусы и вирусные компоненты (вирусы Э-Б, кори, белки теплового шока) Паразиты (Тгураnоsoma crusi, РIаsmodium malariae).
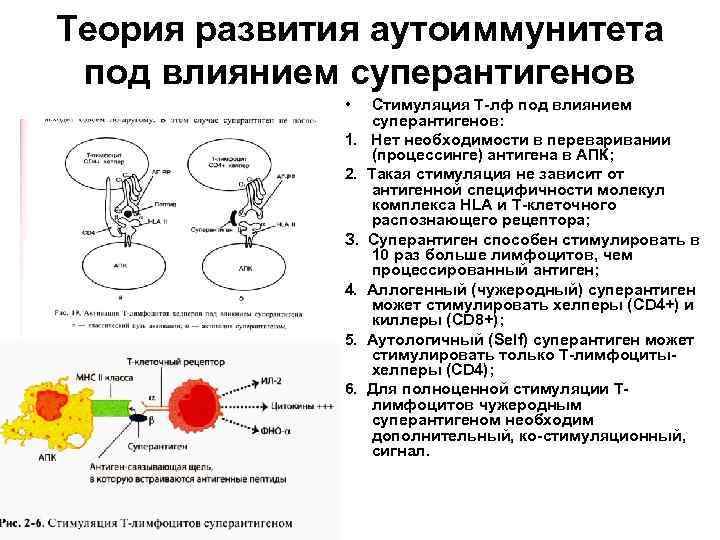
Теория развития аутоиммунитета под влиянием суперантигенов • 1. 2. З. 4. 5. 6. Стимуляция Т-лф под влиянием суперантигенов: Нет необходимости в переваривании (процессинге) антигена в АПК; Такая стимуляция не зависит от антигенной специфичности молекул комплекса НLA и Т-клеточного распознающего рецептора; Суперантиген способен стимулировать в 10 раз больше лимфоцитов, чем процессированный антиген; Аллогенный (чужеродный) суперантиген может стимулировать хелперы (СD 4+) и киллеры (СD 8+); Аутологичный (Sе. If) суперантиген может стимулировать только Т-лимфоцитыхелперы (СD 4); Для полноценной стимуляции Тлимфоцитов чужеродным суперантигеном необходим дополнительный, ко-стимуляционный, сигнал.

Теория развития аутоиммунитета под влиянием суперантигенов А. Активация аутореактивных Т-лимфоцитов. • Суперантигены могут непосредственно активировать аутореактивные Тлимфоциты, которые затем мигрируют в соответствующие ткани и • вызывают аутоиммунные нарушения, продуцируя цитокины и/или реализуя свою киллинговую функцию.

Теория развития аутоиммунитета под влиянием суперантигенов • • Б. Активация аутореактивных В-лимфоцитов. Суперантиген связывает молекулы комплекса НLA класса II, имеющиеся на В-лимфоцитах, с молекулой Т -клеточного антигенраспознающего рецептора. Активация Т-пим фоцитов происходит без специфического распознавания антигена, а неспецифически под влиянием суперантигена. Т-лимфоцит продуцирует соответствующие цитокины, которые способствуют тому, что активированный аутореактивный В-лимфоцит начинает продуцировать аутоантитела. Последние образуют иммунные комплексы и, оседая в тканях, вызывают их повреждение. В-лимфоциты могут активироваться и через собственный антигенраспознающий иммуноглобулиновый рецептор.

Теория развития аутоиммунитета под влиянием суперантигенов В. Активация антагенпредставляющих клеток • Суперантигены могут активировать АПК (макрофаги). • Это приводит к высвобождению из них цитокинов, супероксидных анионов и других медиаторов воспаления. • Активация макрофагов может привести к нарушению переваривания (процессинга) антигенов с последующей презентацией аутоантигенов аутореактивным Т-лимфоцитам.

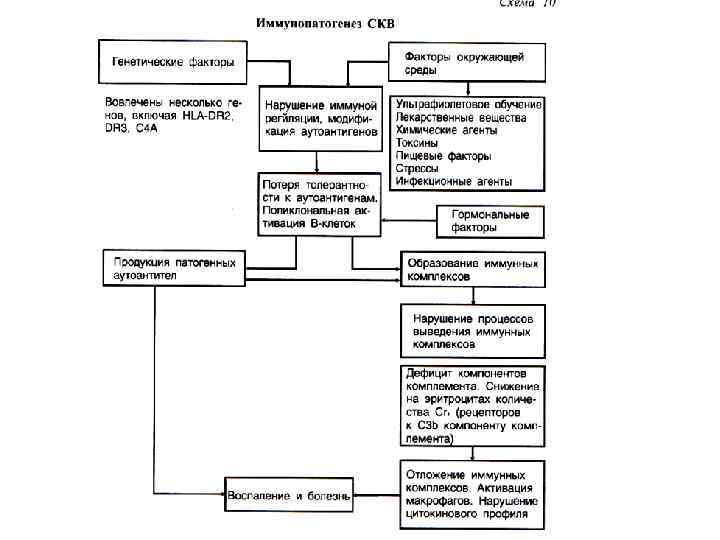
Теория генетической предрасположенности Триггеры аутоиммунных заболеваний А. Согласно рецепторной гипотезе, определенные НLА-антигены являются рецепторами для вирусов, облегчающими их фиксацию и проникновение в клетку. Б. Гипотеза о модификации (изменении) аутологичного, своего, антигена (altered self). Модифицированный аутологичный антиген распознается иммунной системой как чужеродный (nonself)), что приводит к срыву толерантности. В. Гипотеза о влиянии гипотетического Ir-гена на предрасположенность к заболеваниям (нарушение селекции антигенных детерминант, наличие “дыр” в репертуаре Тлимфоцитов, нарушение супрессии, опосредованной Тлимфоцитами). Г. Гинотеза о влиянии неклассических генов, картирующихся в пределах системы НLА. Например гены НSP-70, ТNF, недостаточность С 4 а, С 2 ассоциируются с системной красной волчанкой и пиогенной инфекцией.
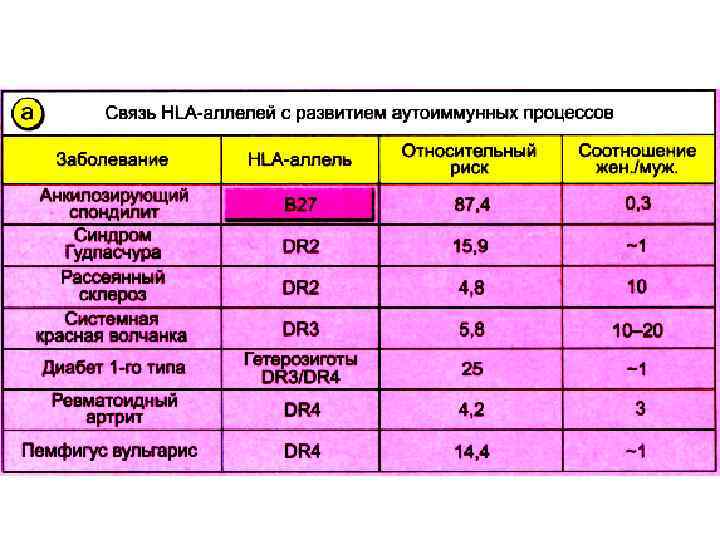

Теория генетической предрасположенности • Тиреоидит Хашимото – HLA DR 3, DR 5 • Инсулинзависимый сахарный диабет DR 3, DR 4 • Рассеянный склероз – DR 2, DR 4 • Тяжелая миастения - DR 3 • Ревматоидный артрит – DR 7, DR 21 • Системная красная волчанка - DR 3, DR 2 • Витилиго - DR 4
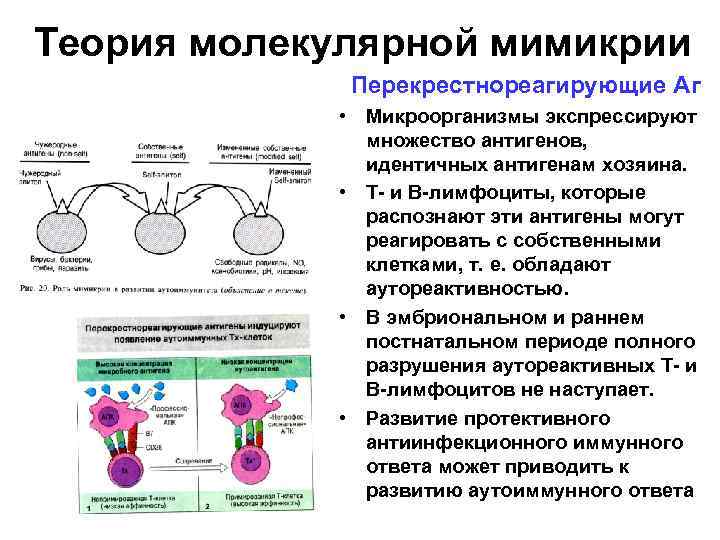
Теория молекулярной мимикрии Перекрестнореагирующие Аг • Микроорганизмы экспрессируют множество антигенов, идентичных антигенам хозяина. • Т- и В-лимфоциты, которые распознают эти антигены могут реагировать с собственными клетками, т. е. обладают аутореактивностью. • В эмбриональном и раннем постнатальном периоде полного разрушения аутореактивных Т- и В-лимфоцитов не наступает. • Развитие протективного антиинфекционного иммунного ответа может приводить к развитию аутоиммунного ответа
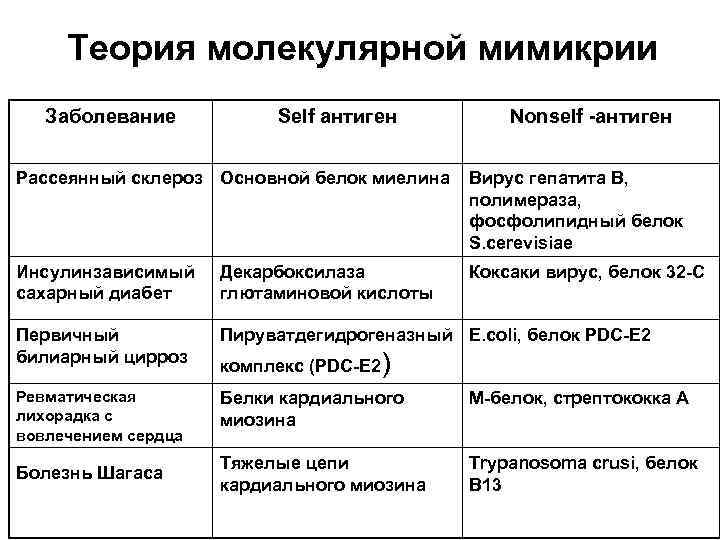
Теория молекулярной мимикрии Заболевание Self антиген Nonself -антиген Рассеянный склероз Основной белок миелина Вирус гепатита В, полимераза, фосфолипидный белок S. cerevisiae Инсулинзависимый сахарный диабет Декарбоксилаза глютаминовой кислоты Коксаки вирус, белок 32 -С Первичный билиарный цирроз Пируватдегидрогеназный E. coli, белок PDC-E 2 Ревматическая лихорадка с вовлечением сердца Белки кардиального миозина М-белок, стрептококка А Болезнь Шагаса Тяжелые цепи кардиального миозина Trypanosoma crusi, белок В 13 комплекс (PDC-E 2)

Теория молекулярной мимикрии • Собственные антигены хозяина могут модифицироваться под влиянием различных факторов: • длительного воздействия инфекционных агентов, • влияния свободных радикалов, • NO, • ксенобиотиков, • лекарственных средств, • воздействия факторов окружающей среды (ионизирующее и ультрафиолетовое излучение, воздействие низких температур и т. п. ). • В результате таких воздействий аутоантигены изменяются и распознаются иммунной системой как чужеродные Продуцирующиеся аутоантитела и цитотоксические лимфоциты связываются не только с модифицированными аутоантигенами, но и с истинными аутоантигенами за счет все той же перекрестной реактивности.

Факторы окружающей среды • Инфекции (вирусы группы герпеса) • Лекарственные вещества (допегит – гемолитическая анемия; апрессин – СКВ; сульфаниламиды – узелковый периартериит) • Иммуностимулирующими свойствами обладают: • • • Антибиотики противогрибковые Нитрофураны (фуразолидон) Антисептики (хлорофиллипт) Стимуляторы метаболизма (оротат К, рибоксин) Психотропные препараты (ноотропил, пирацетам, фенапам) • Плазмозамещающие растворы (гемодез, реополиглюкин) • Роль других факторов (УФО, стрессы, алиментарные факторы) • Роль гормонов (дисбаланс гормонов – начало репродуктивного периода- эстрогены, пролактин)

Механизмы повреждения тканей при аутоиммунных заболеваниях Реакции гуморального имунититета: • Гиперчувствительность II и III типа Реакции клеточного иммунитета: • Гиперчувствительность IV типа

Реакции гуморального имунититета • Гиперчувствительн ость II типа: • Тип IIА – • Идиопатическая тромбоцитопениче ская пурпура • Аутоиммунная гемолитическая анемия • Миастения гравис
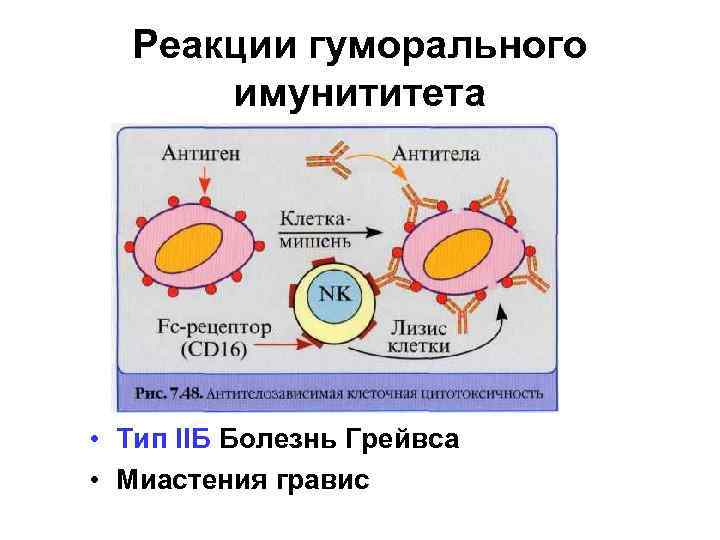
Реакции гуморального имунититета • Тип IIБ Болезнь Грейвса • Миастения гравис
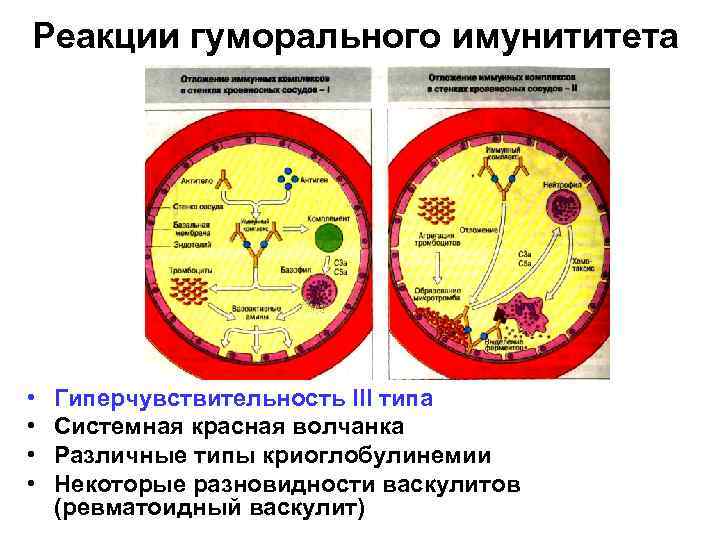
Реакции гуморального имунититета • • Гиперчувствительность III типа Системная красная волчанка Различные типы криоглобулинемии Некоторые разновидности васкулитов (ревматоидный васкулит)
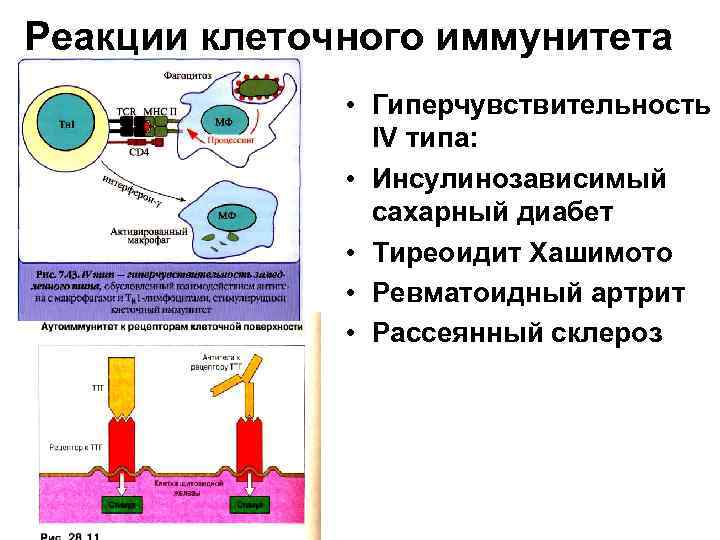
Реакции клеточного иммунитета • Гиперчувствительность IV типа: • Инсулинозависимый сахарный диабет • Тиреоидит Хашимото • Ревматоидный артрит • Рассеянный склероз

Системная красная волчанка Эпителиальные клетки фолликулов окрашены при воздействии Аг цитоплазмы с Ат тиреоидит Хасимото Ат взаимодействуют с ядрами клеток, оставляя цитоплазму неокрашенной СКВ • Аутоиммунное заболевание с системным поражением соединительной ткани, с отложением коллагена и формированием васкулитов. • Характеризуется полисимптомностью, как правило, развивается у лиц молодого возраста. • В процесс вовлекаются практически все органы и многие суставы, фатальным оказывается поражение почек.

Системная красная волчанка • При этой патологии образуются антинуклеарные аутоантитела к ДНК, в том числе нативной, нуклеопротеинам, антигенам цитоплазмы и цитоскелета, микробным белкам. • Ауто. АТ к ДНК появляются в результате образования ее иммуногенной формы в комплексе с белком, • либо Ig. M аутоантителом анти-ДНК специфичности, возникшим в эмбриональном периоде, или • взаимодействия идиотипа-антиидиотипа и компонентов клеток при микробной или вирусной инфекции.

Системная красная волчанка • Определенная роль принадлежит апоптозу клеток, вызывающему при СКВ (под влиянием каспазы 3) расщепление нуклеопротеосомного комплекса ядра с образованием ряда продуктов, реагирующих с соответствующими аутоантителами. • В крови больных с СКВ резко повышено содержание нуклеосом. • Аутоантитела к нативной ДНК являются наиболее диагностически значимыми.

Системная красная волчанка • Обнаружена у ДНК-связывающих аутоантител и ферментативная способность гидролизовать молекулу ДНК без комплемента. Такое антитело назвали ДНК-абзимом. • Эта фундаментальная закономерность реализуется не только при СКВ, играет громадное значение в патогенезе аутоиммунных заболеваний. • Анти-ДНК аутоантитело обладает цитотоксической активностью по отношению к клетке, которая реализуется двумя механизмами: • рецептор-опосредованным апоптозом и • катализом ДНК-абзима.
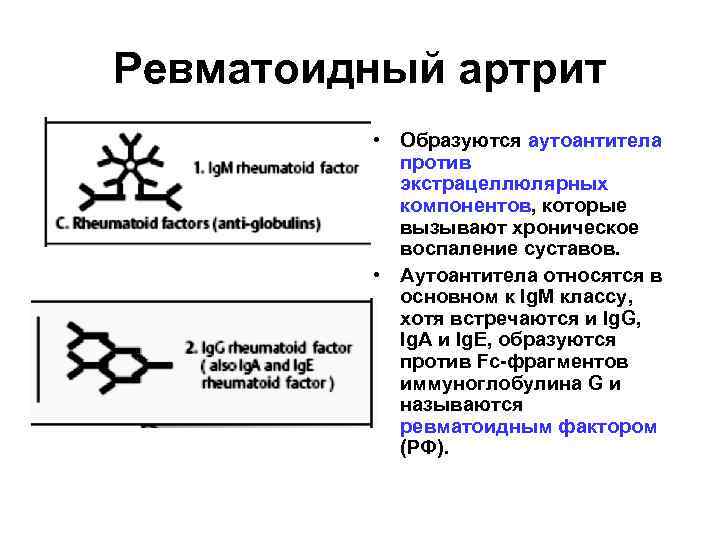
Ревматоидный артрит • Образуются аутоантитела против экстрацеллюлярных компонентов, которые вызывают хроническое воспаление суставов. • Аутоантитела относятся в основном к Ig. M классу, хотя встречаются и Ig. G, Ig. А и Ig. Е, образуются против Fс-фрагментов иммуноглобулина G и называются ревматоидным фактором (РФ).

Ревматоидный артрит • Cинтезируются аутоантитела к кератогиалиновым зернам (антиперинуклеарный фактор), • кератину (антикератиновые АТ), • коллагену. • Аутоантитела к коллагену неспецифичны • Антиперинуклеарный фактор является предвестником формирования РА. • Обнаружение Ig. M-РФ позволяет классифицировать серопозитивный или серонегативный РА, а Ig. А-РФ оказывается критерием высокоактивного процесса.
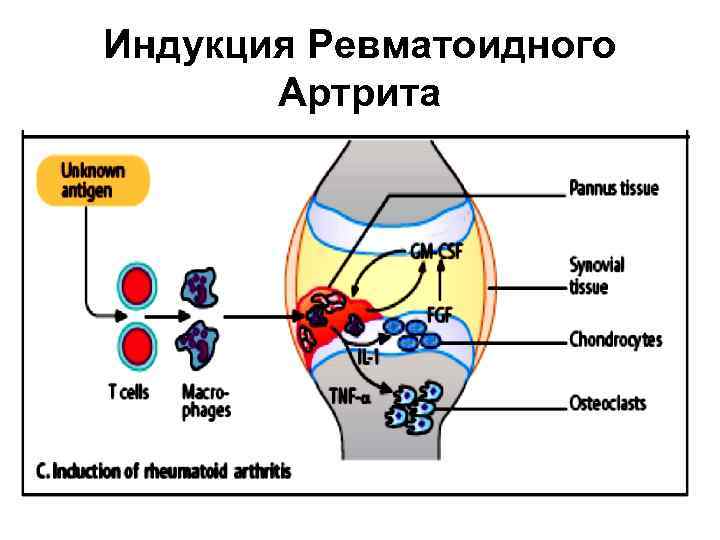
Индукция Ревматоидного Артрита
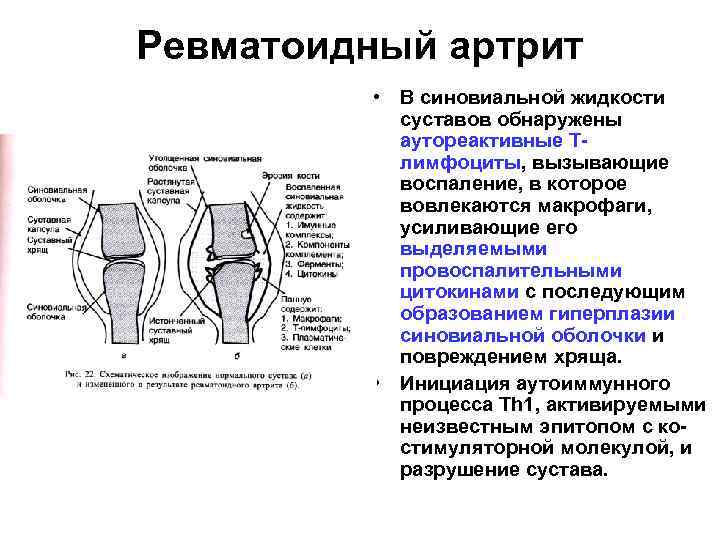
Ревматоидный артрит • В синовиальной жидкости суставов обнаружены аутореактивные Тлимфоциты, вызывающие воспаление, в которое вовлекаются макрофаги, усиливающие его выделяемыми провоспалительными цитокинами с последующим образованием гиперплазии синовиальной оболочки и повреждением хряща. • Инициация аутоиммунного процесса Тh 1, активируемыми неизвестным эпитопом с костимуляторной молекулой, и разрушение сустава.
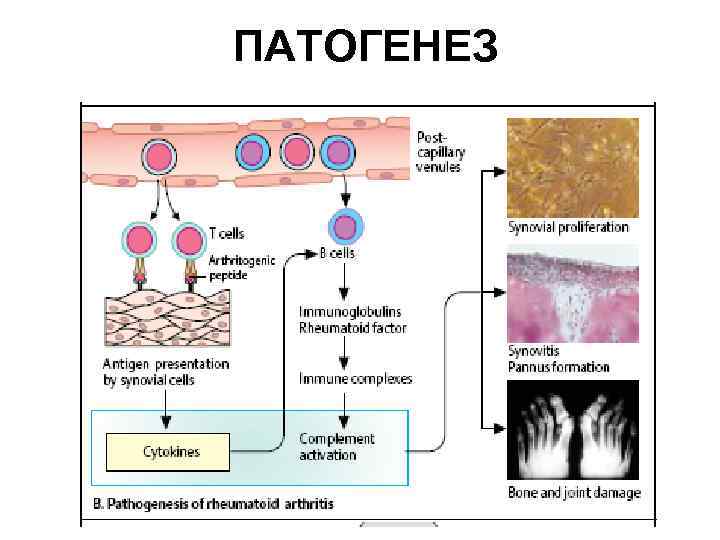
ПАТОГЕНЕЗ
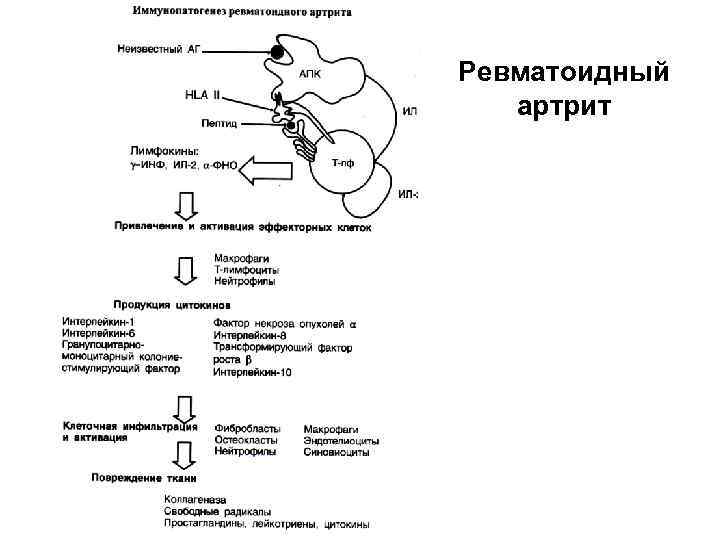
Ревматоидный артрит

Аутоиммунный тиреоидит Хашимото • Заболевание щитовидной железы, сопровождающееся ее функциональной неполноценностью с асептическим воспалением паренхимы, которая нередко инфильтрирована лимфоцитами и в последующем замещается соединительной тканью, образующей в железе уплотнения. • Заболевание проявляется тремя формами • тиреоидитом Хашимото (аутоантиген тиреоглобулин), • первичной микседемой (аутоантиген белки клеточной поверхности и цитоплазмы) и • Тиреотоксикозом или болезнью Грейвса. • Две первые формы характеризуются гипотиреозом.

Аутоиммунный тиреоидит Хашимото • Ключевое влияние на функцию щитовидной железы оказывают аутоантитела к • тиреоглобулину, • рецептору тиреоид-стимулирующего гормона и • тиреопероксидазе, • они же используются в диагностике патологии. • Аутоантитела подавляют синтез гормонов щитовидной железой, что отражается на ее функции. • В-лимфоциты связываются с аутоантигенами (эпитопами), влияют на пролиферацию Т-хелперов обоих типов, что сопровождается развитием аутоиммунного заболевания.

Аутоиммунный миокардит • При этом заболевании ключевая роль принадлежит вирусной инфекции, которая скорее всего является его пусковым механизмом. • Именно при нем наиболее четко прослеживается роль мимикрирующих антигенов. • У пациентов с данной патологией обнаруживаются аутоантитела к • кардиомиозину, • рецепторам наружной мембраны миоцитов • к белкам вирусов Коксаки и • цитомегаловирусам.

Аутоиммунный миокардит • При этих инфекциях в крови выявляется очень высокая виремия, вирусные антигены в процессированной форме скапливаются на профессиональных АПК, которые могут активировать непримированные клоны аутореактивных Тлимфоцитов. • Последние начинают взаимодействовать с непрофессиональными антиген-представляющими клетками, т. к. не нуждаются в костимулирующем сигнале, и взаимодействуют с клетками миокарда, на которых в силу активации антигенами резко повышается экспрессия адгезионных молекул (IСАМ 1, VСАМ-1, Е-селектин). • Процесс взаимодействия аутореактивных Тлимфоцитов также резко усиливается и облегчается за счет повышения на кардиомиоцитах экспрессии молекул НLA II класса. • Аутоантигены миокардиоцитов распознаются Тхелперами.

Аутоиммунный миокардит • Развитие аутоиммунного процесса и вирусной инфекции: • вначале мощная виремия и высокие титры антивирусных аутоантител, • далее - снижение виремии вплоть до вирусонегативности и противовирусных антител, • нарастание антимиокардиальных аутоантител с развитием аутоиммунного заболевания сердца. • В экспериментах был четко продемонстрован аутоиммунный механизм процесса, при котором перенос Т-лимфоцитов от инфицированных мышей с миокардитом индуцировал у здоровых животных заболевание. С другой стороны, подавление Т клеток сопровождалось резким положительным терапевтически м эффектом.
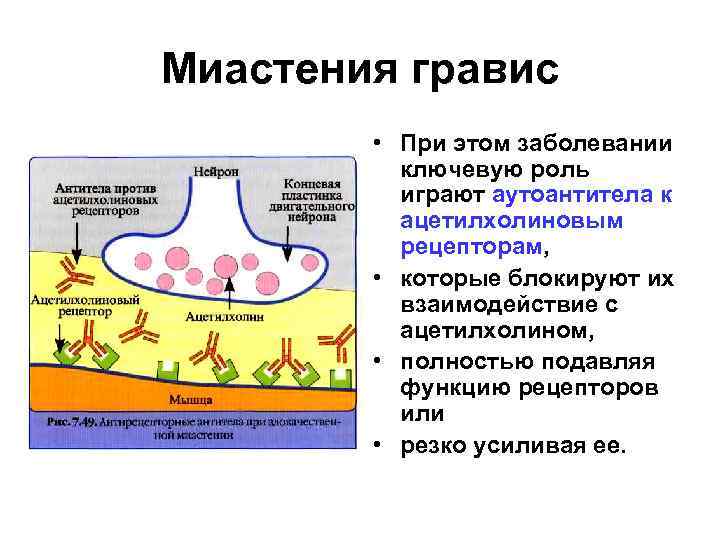
Миастения гравис • При этом заболевании ключевую роль играют аутоантитела к ацетилхолиновым рецепторам, • которые блокируют их взаимодействие с ацетилхолином, • полностью подавляя функцию рецепторов или • резко усиливая ее.
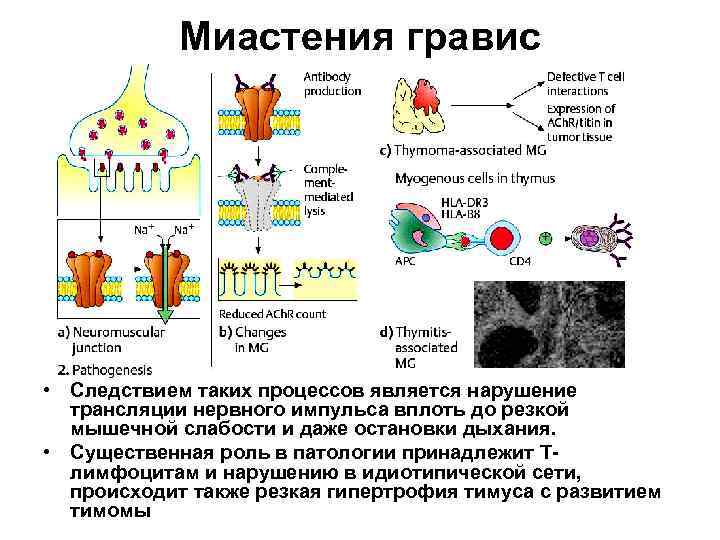
Миастения гравис • Следствием таких процессов является нарушение трансляции нервного импульса вплоть до резкой мышечной слабости и даже остановки дыхания. • Существенная роль в патологии принадлежит Тлимфоцитам и нарушению в идиотипической сети, происходит также резкая гипертрофия тимуса с развитием тимомы

Аутоиммунный увеит • Роль в развитии аутоиммунного увеита, при котором развивается аутоиммунное хроническое воспаление увеаретинального тракта, играет инфицирование простейшими Тохорlasma gondii и вирусами цитомегалии и простого герпеса. • При этом ключевая роль принадлежит мимикрирующим антигенам возбудителей, которые имеют общие детерминанты с тканями глаза. • При данном заболевании появляются аутоантитела к аутоантигенам ткани глаза и микробным белкам. • Эта патология является истинно аутоиммунной, поскольку введение пяти очищенных антигенов глаза экспериментальным животным вызывает развитие у них классического аутоиммунного увеита за счет образования соответствующих аутоантител и поражения ими увеальной оболочки.

Инсулинзависимый сахарный диабет • Аутоиммунное заболевание, при котором иммунная аутоагрессия направлена против аутоантигенов клеток островков Лангерганса, они разрушаются, что сопровождается подавлением синтеза инсулина и следующими за ним глубочайшими метаболическими изменениями в организме. • Это заболевание опосредовано в основном функционированием цитотоксических Т-лимфоцитов, которые сенсибилизированы, по-видимому, к внутриклеточной декарбоксилазе глутаминовой кислоты и белку р40. • При этой патологии выявляют и аутоантитела к инсулину, но их патогенетическая роль пока не ясна.

Инсулинзависимый сахарный диабет • Необходимо рассматривать аутоиммунные реакции при диабете с трех позиций: 1. Диабет - типичное аутоиммунное заболевание с аутоагрессией против аутоантигенов β-клеток; 2. Образование антиинсулиновых аутоантител носит вторичный характер, формирующий синдром аутоиммунной инсулинорезистентности; 3. При диабете развиваются другие иммунопатологические процессы, как например, появление аутоантител к тканям глаза, почек и т. д. и их соответствующие поражения.

Болезнь Крона • Гранулематозный колит - тяжелое рецидивирующее аутоиммунное воспалительное заболевание толстой кишки с сегментарным поражением стенки кишки лимфоцитарными гранулемами с образованием проникающих щелевидных язв. • Заболевание встречается с частотой 1: 4000, чаще страдают молодые женщины. • Ассоциировано с антигеном НLA B 27 и обусловлено образованием аутоантител к тканям слизистой оболочки кишечника при снижении количества и функциональной активности супрессорных Тлимфоцитов и к мимикрирующим микробным антигенам. • В толстой кишке обнаружено повышенное количество Ig. G-содержащих лимфоцитов, специфичных к туберкулезу. • Появились сообщения об успешном лечении этого заболевания с помощью антител к β-ФНО, которые подавляют активность аутореактивных Т-лимфоцитов.

Рассеянный склероз • При этой патологии также ключевую роль играют аутореактивные Т-клетки с участием Тh 1, которые обусловливают разрушение миелиновой оболочки нервов с последующим развитием тяжелейшей симптоматики. • Аутоантигеном является основной белок миелина, на который формируются сенсибилизированные Тклетки. • Немалая роль в патологии принадлежит апоптозу, проявления которого могут обусловить различные типы течения процесса — прогрессирующий или ремитирующий. • В экспериментальной модели (экспериментальный энцефаломиелит) воспроизводится при иммунизации животных основным миелиновым белком. • Не исключают определенную роль в этиологии рассеянного склероза вирусной инфекции
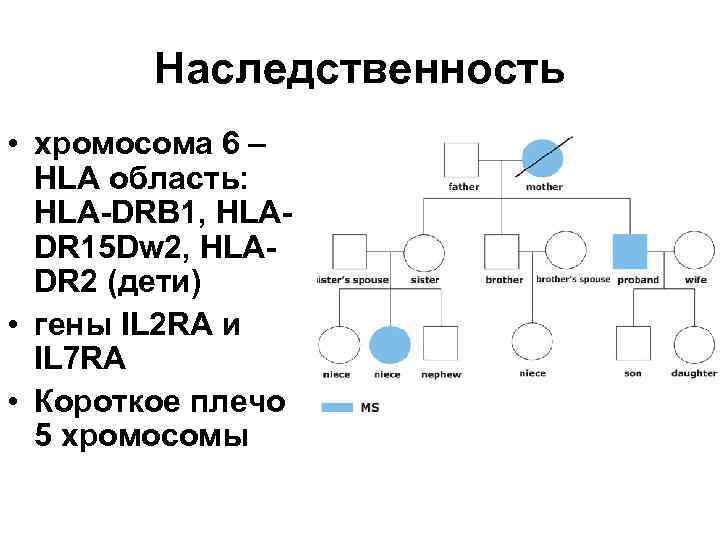
Наследственность • хромосома 6 – HLA область: HLA-DRB 1, HLADR 15 Dw 2, HLADR 2 (дети) • гены IL 2 RA и IL 7 RA • Короткое плечо 5 хромосомы

Предрасполагающие факторы • Инфекция: герпес (HHV-6, HHV-8), вирус Зостер, вирус Эпштейна Барр, chlamydia pneumoniaе, ретровирус человека (HERV) • Возможный механизм развития: молекулярная мимикрия между антигенами ЦНС и вирусными антигенами • • Вакцинация Стресс Курение Беременность (последний триместр)
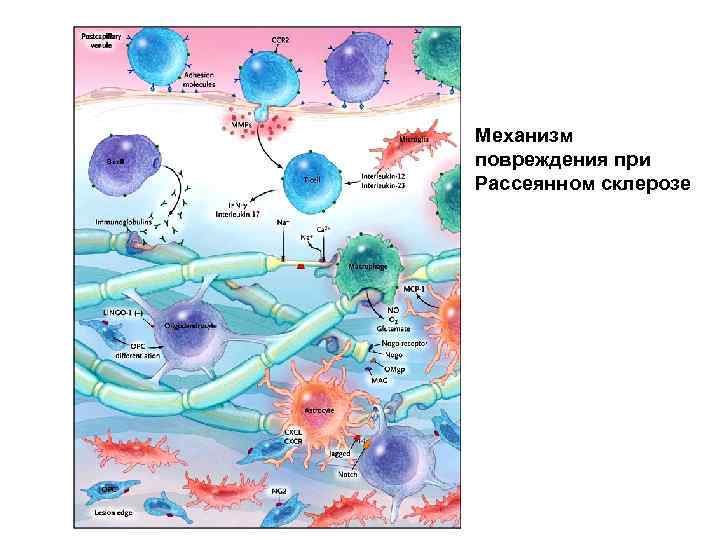
Механизм повреждения при Рассеянном склерозе

Рассеянный склероз • Критическое событие в развитии РС – поломка гематоэнцефалического барьера • Для развития заболевания необходима активация Т лимфоцитов • На поверхности Т лимфоцитов синтезируются молекулы адгезии (интегрины), они обуславливают взаимодействие лимфоцитов с эндотелием сосудов и обеспечивают выход из кровеносного русла • Аутоиммунный ответ стимулируется за счет Th 1, которые продуцируют ИФН • ИЛ-12 и ИФН активируют фактор транскрипции Stat-4 в Т лимфоцитах, что приводит к их дифференциации в Th 1 • ИЛ-23 стимулирует секрецию ИЛ-17 Т лимфоцитами. ИЛ-17 считается основным цитокинов при воспалении мозговой ткани. • При РС повышен синтез иммуноглобулинов

Аутоиммунные заболевания системы крови • • Аутоиммунная гемолитическая анемия и Нейтропения, Тромбоцитопеническая пурпура. Обусловлены образованием аутоантител к клеткам крови. Анемия возникает, когда антиэритроцитарные Ig. G аутоантитела вызывают лизис эритроцитов вне сосудов при участии К-клеток, к которым относятся макрофаги и естественные киллеры, фиксирующие аутоантитела через рецептор к Ес-фрагменту Ig. G на эритроцитах. Аутоантитела Ig. M класса (холодовые) лизируют эритроциты при снижении температуры тела до 30° С. Нейтропения обусловлена разрушением гранулоцитов специфическими антигранулоцитарными аутоантителами, тромбоцитопения - антитромбоцитарными.
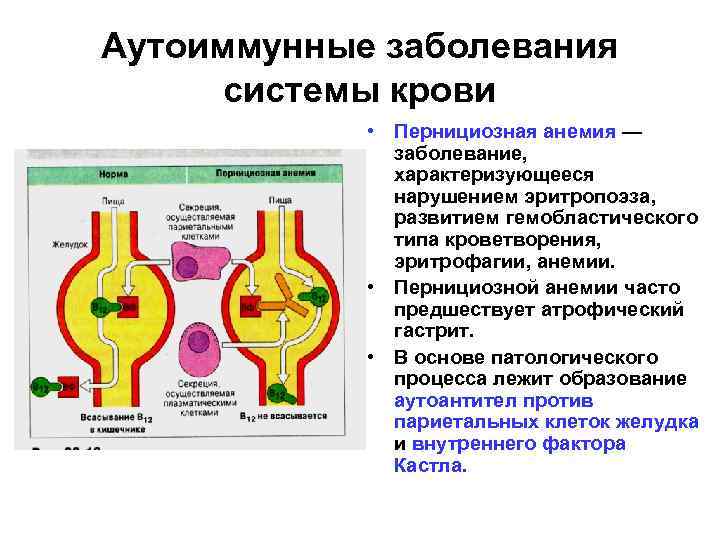
Аутоиммунные заболевания системы крови • Пернициозная анемия — заболевание, характеризующееся нарушением эритропоэза, развитием гемобластического типа кроветворения, эритрофагии, анемии. • Пернициозной анемии часто предшествует атрофический гастрит. • В основе патологического процесса лежит образование аутоантител против париетальных клеток желудка и внутреннего фактора Кастла.

Болезнь Аддисона • Проявляется в гормональной недостаточности коры надпочечников с хроническим течением. • Характерны — гипотония, адинамия, падение уровня сахара в крови, 17 -ОКС — в моче. • В сыворотке крови определяются аутоантитела против митохондрий и микросом клеток железы, которые и обусловливают атрофию и деструкцию надпочечников.

Целиакия • Целиакия (глютеновая болезнь, глютеновая энтеропатая) • Хроническое заболевание тонкой кишки, в основе которого лежит дефект слизистой оболочки в образовании пептидаз, расщепляющих растительный белок глютенклецивину, содержащуюся в злаках. • Чаще страдают женщины. • Клинически заболевание проявляется энтеритом, особенно при употреблении в пищу продуктов, богатых клейковиной. • У пациентов часто обнаруживают антитела к глютену, недостаточность Ig. A

Синдром Гудпасчера • Системный капиллярит с преимущественным поражением легких и почек по типу геморрагического пневмонита и гломерулонефрита. • Заболевают чаще мужчины в возрасте 20 -30 лет. • Прослеживается связь заболевания с вирусными и бактериальными инфекциями, переохлаждениями. • Начинается остро с высокой лихорадкой, хрипами в легких, с быстрым прогрессированием гломерулонефрита с исходом в почечную недостаточность. Характерны кровохарканье, гематурия, анемия. • Обнаруживаются аутоантитела к базальным мембранам почек, которые также реагируют с базальными мембранами легких.

Синдром Шегрена • Хроническое воспаление экзокринных желез (слюнных, слезных) с лимфоидной их инфильтрацией с последующей атрофией, может сочетаться с сухим кератоконъюнктивитом, глосситом, кариесом зубов, лекарственной непереносимостью, болями и припухлостью суставов. • Ткань желез поражается вследствие аутосенсибилизации и появления иммунных комплексов. • Болезнь чаще поражает мужчин в возрасте 20—ЗО лет.

Болезнь Уиппла • Болезнь Уиппла (кишечная липодистрофия) • Хроническое заболевание с поражением тонкой кишки с развитием диспепсии, полиартрита, реже - поражением клапанов сердца, полисерозитом, лимфоаденопатией, диффузной пигментацией кожи.

Неспецифический язвенный колит • Заболевание, развивающееся по типу диффузного хронического воспаления слизистой оболочки кишечника с образованием обширных неглубоких язв. • Отмечается образование аутоантител против слизистой оболочки толстой кишки. у 50 -80% пациентов обнаруживаются антитела к цитоплазматическим антигенам нейтрофилов, а в лимфоидно-плазмоклеточном инфильтрате слизистой и подслизистой толстой кишки среди иммуноглобулин содержащих клеток выявляется 40 -50% клеток, синтезирующих Ig. G (в норме около 5 -10%). • Недавно в толстой кишке и крови обнаружено повышенное число лимфоцитов, экспрессирующих рецепторы к микобактериям паратуберкулеза.

Болезнь Бехчета • Хронический патологический процесс с периодическими обострениями. Для заболевания характерна следующая триада симптомов: • поражение слизистой оболочки рта (стоматит), • слизистой оболочки глаз (конъюктивит), • сосудистой оболочки глаз (увеит), • а также половых органов. • У больных образуются афты, язвы с рубцеванием. • В крови обнаруживаются антитела, реагирующие с эпителием слизистой оболочки рта.

Принципы иммунодиагностики 1. Наличие специфических аутоантител; 2. Наличие специфической клеточной сенсибилизации (РБТ и теста ингибиции миграции лейкоцитов в присутствии соответствующего аутоантигена); З. Повышение уровня γ-глобулина и/или Ig; 4. Изменение количества Т-CD 4+ и Т- CD 8+, приводящее к повышению иммунорегуляторного индекса; 5. Снижение уровня СЗ и С 4 компонентов комплемента; 6. Отложения иммунных комплексов в пораженных тканях (Ig. G, Ig. M, СЗ, С 4 и фибрин); 7. Лимфоидно-клеточная инфильтрация пораженных тканей; 8. Определение НLA-фенотипа

Лечение аутоиммунных заболеваний Принципы терапии 1. Элиминация «запрещенных» клонов сенсибилизированных лимфоцитов ( «аутореактивных лимфоцитов» ). 2. Удаление иммуногена или адъюванта. Это воздействие не всегда можно реализовать. Нельзя, скажем, удалить ДНК у больных СКВ. С другой стороны, элиминация возбудителя при соответствующих формах заболеваний, токсинов и других веществ методом плазмафереза дает позитивный результат. З. Иммуносупрессорная терапия должна быть дифференцированной и по возможности короткой. 4. Блокада медиаторов иммунных реакций антигистаминными препаратами, ядом кобры, разрушающим комплемент, и т. д.

Принципы терапии 5. Заместительная терапия необходимыми метаболитами: при пернициозной анемии витамином В 12 при микседеме - тироксином. 6. Противовоспалительные средства: кортикостероиды, препараты салициловой кислоты. 7. Иммунотерапия: десенсибилизация причинными аллергенами, при наличии гиперчувствительности немедленного типа - стимуляция синтеза специфических Ig. G (или их введение), «конкурирующих» с Ig. Е 8. Иммунокоррекция дефицита или функционального дефекта Т-супрессоров.
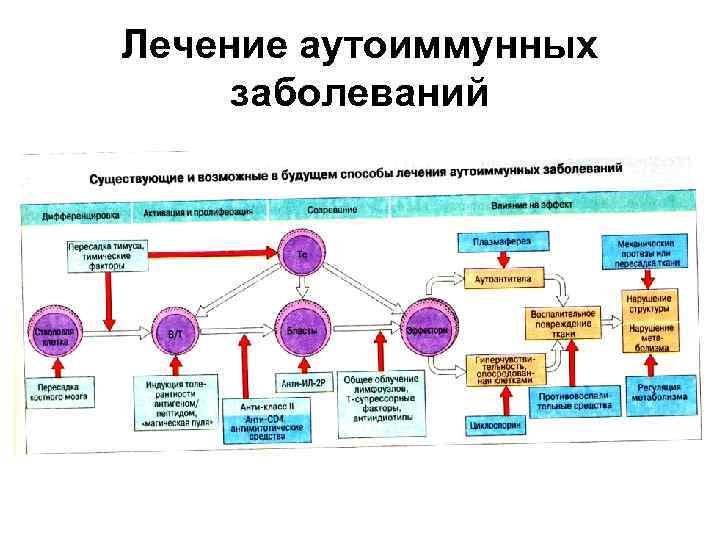
Лечение аутоиммунных заболеваний
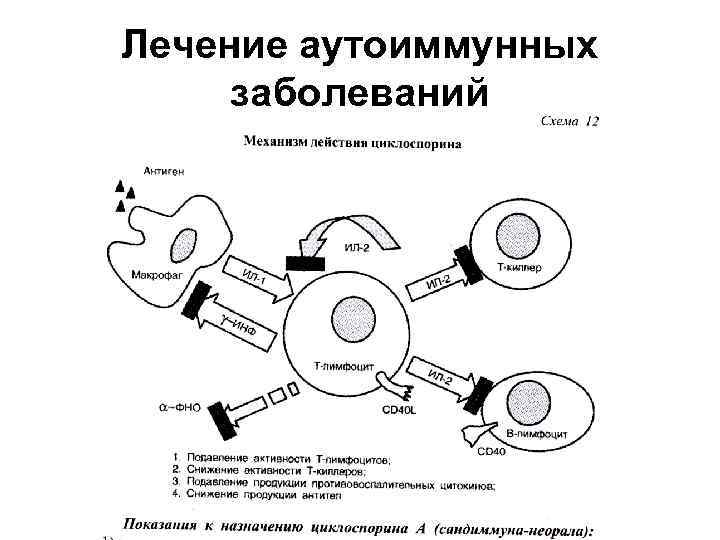
Лечение аутоиммунных заболеваний
Аутоиммунная патология.ppt