Атомно-молекулярное учение.ppt
- Количество слайдов: 38
 Атомно-молекулярное учение
Атомно-молекулярное учение
 Химия- наука, изучающая состав, строение и превращения веществ «Широко распростирает химия руки свои в дела человеческие. . . Куда ни посмотрим, куда не оглянемся, везде обращаются перед очами нашими успехи её прилежания» М. В. Ломоносов «Слово о пользе химии» , 1751 г.
Химия- наука, изучающая состав, строение и превращения веществ «Широко распростирает химия руки свои в дела человеческие. . . Куда ни посмотрим, куда не оглянемся, везде обращаются перед очами нашими успехи её прилежания» М. В. Ломоносов «Слово о пользе химии» , 1751 г.
 Разделы химии Агрохимия ·Аналитическая химия ·Биоорганическая химия и ·биохимия ·Вычислительная химия ·Геохимия ·Квантовая химия ·Коллоидная химия ·Неорганическая химия ·Органическая химия ·Нефтехимия ·Общая химия ·Радиохимия Физическая химия Химия высокомолекулярных соединений
Разделы химии Агрохимия ·Аналитическая химия ·Биоорганическая химия и ·биохимия ·Вычислительная химия ·Геохимия ·Квантовая химия ·Коллоидная химия ·Неорганическая химия ·Органическая химия ·Нефтехимия ·Общая химия ·Радиохимия Физическая химия Химия высокомолекулярных соединений
 Нефтехимия, область химии изучающая состав, свойства и химические превращения компонентов нефти и природного газа, а также процессы их переработки. , , Задачи: Изучение состава нефти Изучение взаимных превращений углеводородов при переработке нефти и газа Синтез функциональных производных из нефтяного и газового сырья Разработать наиболее рациональные пути переработки и использования нефти и газа,
Нефтехимия, область химии изучающая состав, свойства и химические превращения компонентов нефти и природного газа, а также процессы их переработки. , , Задачи: Изучение состава нефти Изучение взаимных превращений углеводородов при переработке нефти и газа Синтез функциональных производных из нефтяного и газового сырья Разработать наиболее рациональные пути переработки и использования нефти и газа,
 , Современные задачи химии Синтез новых веществ и композиций с заданными свойствами, необходимых для решения различных , задач Разработка и создание новых источников энергии Выяснение механизма биохимических процессов и их реализация в искусственных условиях Охрана окружающей среды
, Современные задачи химии Синтез новых веществ и композиций с заданными свойствами, необходимых для решения различных , задач Разработка и создание новых источников энергии Выяснение механизма биохимических процессов и их реализация в искусственных условиях Охрана окружающей среды
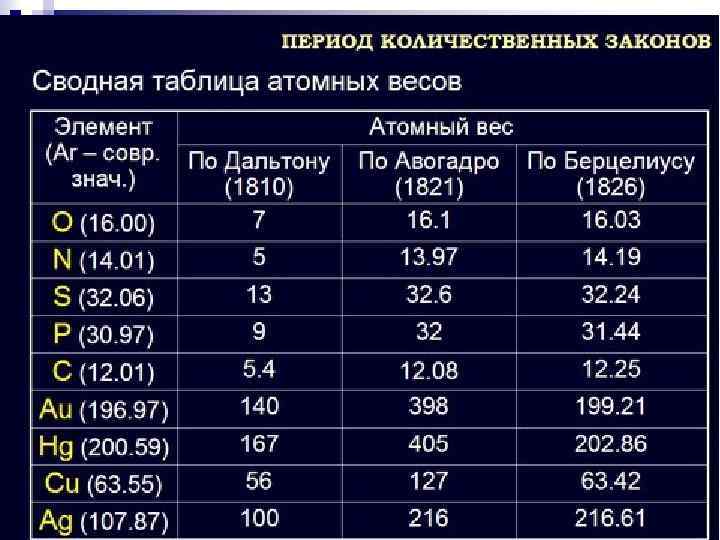
 Основные этапы развития химии Предалхимический период (до IIIв. н. э. ) Алхимический период(III-XVIIв. ) Период становления (XVII-XVIIIв. ) Период количественных законов (17891860 г. ) Период классической химии(1860 г. -конец XIXв. ) Химия XX-XXI века
Основные этапы развития химии Предалхимический период (до IIIв. н. э. ) Алхимический период(III-XVIIв. ) Период становления (XVII-XVIIIв. ) Период количественных законов (17891860 г. ) Период классической химии(1860 г. -конец XIXв. ) Химия XX-XXI века

 Ремесленная химия Металлургия Изготовление керамики Крашение ткани Дубление кожи Производство парфюмерии Фармация
Ремесленная химия Металлургия Изготовление керамики Крашение ткани Дубление кожи Производство парфюмерии Фармация


 Основная задача алхимии- поиск философского камня (эликсира), считавшегося необходимым для осуществления трансмутации металлов. Алхимия тесно переплетена с астрологией и мистикой. Для алхимии характерно использование аллегорий для обозначения понятий, веществ, процессов.
Основная задача алхимии- поиск философского камня (эликсира), считавшегося необходимым для осуществления трансмутации металлов. Алхимия тесно переплетена с астрологией и мистикой. Для алхимии характерно использование аллегорий для обозначения понятий, веществ, процессов.

 Рецепт философского камня. Раймунд Луллий, XIII век. «Чтобы приготовить эликсир мудрецов, или философский камень, возьми, сын мой, философской ртути и накаливай, пока она не превратится в зеленого льва. После этого прокаливай сильнее, и она превратится в красного льва. Дигерируй этого красного льва на песчаной бане с кислым виноградным спиртом, выпари жидкость, и ртуть превратится в камедеобразное вещество, которое можно резать ножом. Положи его в обмазанную глиной реторту и не спеша дистиллируй. Собери отдельно жидкости различной природы, которые появятся при этом. Ты получишь безвкусную флегму, спирт и красные капли. Киммерийские тени покроют реторту своим темным покрывалом, и ты найдешь внутри нее истинного дракона, потому что он пожирает свой хвост. Возьми этого черного дракона, разотри на камне и прикоснись к нему раскаленным углем. Он загорится и, приняв вскоре великолепный лимонный цвет, вновь воспроизведет зеленого льва. Сделай так, чтобы он пожрал свой хвост, и снова дистиллируй продукт. Наконец, мой сын, тщательно ректифицируй, и ты увидишь появление горючей воды и человеческой крови. . . »
Рецепт философского камня. Раймунд Луллий, XIII век. «Чтобы приготовить эликсир мудрецов, или философский камень, возьми, сын мой, философской ртути и накаливай, пока она не превратится в зеленого льва. После этого прокаливай сильнее, и она превратится в красного льва. Дигерируй этого красного льва на песчаной бане с кислым виноградным спиртом, выпари жидкость, и ртуть превратится в камедеобразное вещество, которое можно резать ножом. Положи его в обмазанную глиной реторту и не спеша дистиллируй. Собери отдельно жидкости различной природы, которые появятся при этом. Ты получишь безвкусную флегму, спирт и красные капли. Киммерийские тени покроют реторту своим темным покрывалом, и ты найдешь внутри нее истинного дракона, потому что он пожирает свой хвост. Возьми этого черного дракона, разотри на камне и прикоснись к нему раскаленным углем. Он загорится и, приняв вскоре великолепный лимонный цвет, вновь воспроизведет зеленого льва. Сделай так, чтобы он пожрал свой хвост, и снова дистиллируй продукт. Наконец, мой сын, тщательно ректифицируй, и ты увидишь появление горючей воды и человеческой крови. . . »
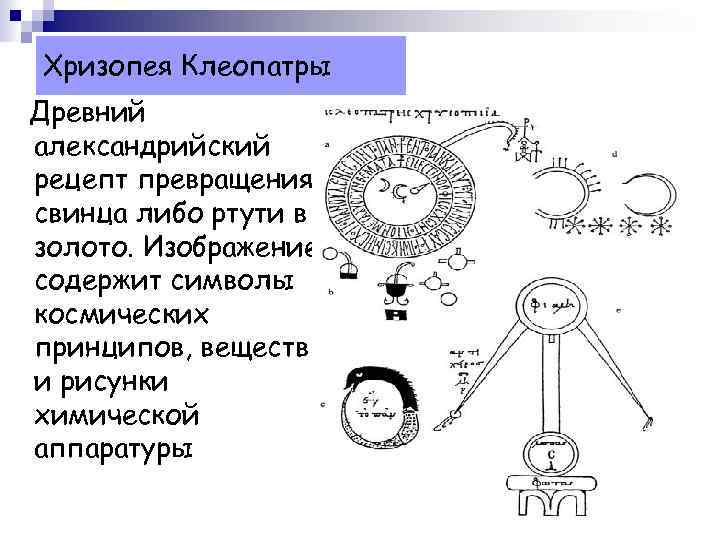 Хризопея Клеопатры Древний александрийский рецепт превращения свинца либо ртути в золото. Изображение содержит символы космических принципов, веществ и рисунки химической аппаратуры
Хризопея Клеопатры Древний александрийский рецепт превращения свинца либо ртути в золото. Изображение содержит символы космических принципов, веществ и рисунки химической аппаратуры

 Итоги алхимического периода Накоплены навыки экспериментальной работы и наблюдений Разработаны новые методы выделения и очистки веществ (фосфор, царская водка, порох, лекарства, . . ) Разработаны новые лабораторные приборы
Итоги алхимического периода Накоплены навыки экспериментальной работы и наблюдений Разработаны новые методы выделения и очистки веществ (фосфор, царская водка, порох, лекарства, . . ) Разработаны новые лабораторные приборы

 Стехиометрия — раздел химии, в котором рассматриваются массовые или объемные соотношения между реагирующими веществами. • Закон сохранения массы • Закон эквивалентов • Закон постоянства состава вещества • Закон кратных отношений • Закон Авогадро Все законы стехиометрии обусловлены атомномолекулярным строением веществ
Стехиометрия — раздел химии, в котором рассматриваются массовые или объемные соотношения между реагирующими веществами. • Закон сохранения массы • Закон эквивалентов • Закон постоянства состава вещества • Закон кратных отношений • Закон Авогадро Все законы стехиометрии обусловлены атомномолекулярным строением веществ
 Закон сохранения массы вещества (Антуан Лоран Лавуазье, 1789 г. ) Масса веществ, вступающих в химическую реакцию, равна массе веществ, образующихся в результате реакции. М. В. Ломоносов, 1748 г «Все перемены в натуре случающиеся такого суть состояния, что сколько чего у одного тела отнимается, столько присовокупится к другому. Так, ежели где убудет несколько материи, то умножится в другом месте»
Закон сохранения массы вещества (Антуан Лоран Лавуазье, 1789 г. ) Масса веществ, вступающих в химическую реакцию, равна массе веществ, образующихся в результате реакции. М. В. Ломоносов, 1748 г «Все перемены в натуре случающиеся такого суть состояния, что сколько чего у одного тела отнимается, столько присовокупится к другому. Так, ежели где убудет несколько материи, то умножится в другом месте»
 Связь между массой и энергией определяется уравнением Эйнштейна Е=m·c 2 , где с - скорость света в вакууме(300 000 км/с) Для Е= 100 к. Дж: m=E/c 2=100· 1000 / (3· 105. 103)2 =1, 1· 10 -9 г В пределах точности измерительных приборов закон сохранения массы практически справедлив для химических реакций (но не для ядерных)
Связь между массой и энергией определяется уравнением Эйнштейна Е=m·c 2 , где с - скорость света в вакууме(300 000 км/с) Для Е= 100 к. Дж: m=E/c 2=100· 1000 / (3· 105. 103)2 =1, 1· 10 -9 г В пределах точности измерительных приборов закон сохранения массы практически справедлив для химических реакций (но не для ядерных)

 Эквивалент ( моль) -количество вещества, которое присоединяет (замещает) один моль атомов водорода или принимает(отдает) один моль электронов. Эквивалентная масса или мольная масса эквивалента (Мэ или Э, г/моль) -масса одного эквивалента вещества
Эквивалент ( моль) -количество вещества, которое присоединяет (замещает) один моль атомов водорода или принимает(отдает) один моль электронов. Эквивалентная масса или мольная масса эквивалента (Мэ или Э, г/моль) -масса одного эквивалента вещества
 • H 2 O Э(O)= 1/2 моль MЭ (O)= 8 г/моль • NH 3 Э(N)= 1/3 моль MЭ (N)= 14/3 г/моль • Zn + 2 HCl= Zn. Cl 2 + H 2 Э(Zn)= 1/2 моль MЭ (Zn)= 65/2 г/моль • Zn. O + 2 HCl= Zn. Cl 2 + H 2 O Э(Zn. O)= 1/2 моль MЭ (Zn. O)= 81/2 г/моль
• H 2 O Э(O)= 1/2 моль MЭ (O)= 8 г/моль • NH 3 Э(N)= 1/3 моль MЭ (N)= 14/3 г/моль • Zn + 2 HCl= Zn. Cl 2 + H 2 Э(Zn)= 1/2 моль MЭ (Zn)= 65/2 г/моль • Zn. O + 2 HCl= Zn. Cl 2 + H 2 O Э(Zn. O)= 1/2 моль MЭ (Zn. O)= 81/2 г/моль
 Расчет эквивалентной массы Элемент Mэ = М/валентность Кислота Mэ = М/(число Н+ в кислоте) Основание Mэ = М/(число ОН- в основании) Соль Mэ = М/(число металла)⋅ (валентность металла)
Расчет эквивалентной массы Элемент Mэ = М/валентность Кислота Mэ = М/(число Н+ в кислоте) Основание Mэ = М/(число ОН- в основании) Соль Mэ = М/(число металла)⋅ (валентность металла)
 Закон эквивалентов Массы реагирующих друг с другом веществ, а также продуктов реакции, прямо пропорциональны их эквивалентным массам (вещества реагируют и получаются в эквивалентных количествах) m 1 /m 2 = МЭ 1/МЭ 2
Закон эквивалентов Массы реагирующих друг с другом веществ, а также продуктов реакции, прямо пропорциональны их эквивалентным массам (вещества реагируют и получаются в эквивалентных количествах) m 1 /m 2 = МЭ 1/МЭ 2
 Закон постоянства состава (Жозеф Луи Пруст, 1808 г. ) Любое сложное вещество, независимо от способа его получения, имеет постоянный качественный и количественный состав «От одного полюса Земли до другого соединения имеют одинаковый состав и одинаковые свойства. Никакой разницы нет между оксидом железа из Южного полушария и Северного. Малахит из Сибири имеет тот же состав, как и малахит из Испании»
Закон постоянства состава (Жозеф Луи Пруст, 1808 г. ) Любое сложное вещество, независимо от способа его получения, имеет постоянный качественный и количественный состав «От одного полюса Земли до другого соединения имеют одинаковый состав и одинаковые свойства. Никакой разницы нет между оксидом железа из Южного полушария и Северного. Малахит из Сибири имеет тот же состав, как и малахит из Испании»

 Химические соединения постоянного состава называются дальтонидами (имеют молекулярную структуру) Химические соединения переменного состава называются бертоллидами. Имеют немолекулярную структуру -атомные, ионные, металлические решетки ( гидриды, оксиды, сульфиды, нитриды, карбиды. . . ) UO 3. . UO 2. 5 Nax WO 3 (0, 3 ≤ x ≤ 0, 9) Ti. N x (x = 0, 38− 1, 20
Химические соединения постоянного состава называются дальтонидами (имеют молекулярную структуру) Химические соединения переменного состава называются бертоллидами. Имеют немолекулярную структуру -атомные, ионные, металлические решетки ( гидриды, оксиды, сульфиды, нитриды, карбиды. . . ) UO 3. . UO 2. 5 Nax WO 3 (0, 3 ≤ x ≤ 0, 9) Ti. N x (x = 0, 38− 1, 20
 Закон кратных отношений (Джон Дальтон, 1803 г. ) Если два элемента (вещества) образуют друг с другом несколько химических соединений, то масса одного из элементов, приходящихся в этих соединениях на одну и ту же массу другого, относятся между собой как небольшие целые числа
Закон кратных отношений (Джон Дальтон, 1803 г. ) Если два элемента (вещества) образуют друг с другом несколько химических соединений, то масса одного из элементов, приходящихся в этих соединениях на одну и ту же массу другого, относятся между собой как небольшие целые числа

 Закон объемных отношений (Жосеф Луи Гей-Люссак, 1808 г. ) Объемы газов, вступающих в химические реакции, и объемы газов, образующихся в результате реакции, относятся между собой как небольшие целые числа 1 об. водорода + 1 об. хлора= 2 об. хлороводорода 2 об. водорода + 1 об. кислорода = 2 об. воды
Закон объемных отношений (Жосеф Луи Гей-Люссак, 1808 г. ) Объемы газов, вступающих в химические реакции, и объемы газов, образующихся в результате реакции, относятся между собой как небольшие целые числа 1 об. водорода + 1 об. хлора= 2 об. хлороводорода 2 об. водорода + 1 об. кислорода = 2 об. воды

 Гипотеза (закон) Авогадро (Амедео Авогадро, 1811 г. ) Равные объёмы газов при одинаковых давлении и температуре содержат одинаковое число молекул 1. При одинаковых условиях равные количества различных газов занимают равные объёмы. При нормальных условиях (0 o. C, 1 атм) 1 моль различных газов занимает объем равный 22, 4 л (молярный объем газа Vm=22/4 л/моль при н. у. ) 2. Отношение масс одинаковых объемов газов (относительная плотность одного газа по другому) равно отношению их молярных масс D= m 1/m 2 = M 1/M 2 DH 2=M/2 DB=M/29
Гипотеза (закон) Авогадро (Амедео Авогадро, 1811 г. ) Равные объёмы газов при одинаковых давлении и температуре содержат одинаковое число молекул 1. При одинаковых условиях равные количества различных газов занимают равные объёмы. При нормальных условиях (0 o. C, 1 атм) 1 моль различных газов занимает объем равный 22, 4 л (молярный объем газа Vm=22/4 л/моль при н. у. ) 2. Отношение масс одинаковых объемов газов (относительная плотность одного газа по другому) равно отношению их молярных масс D= m 1/m 2 = M 1/M 2 DH 2=M/2 DB=M/29