Атомно-молекулярне вчення.ppt
- Количество слайдов: 23
 Атомно-молекулярне вчення. Періодичний закон 1. Періодичний закон. Ядерна модель будова атома. Ізотопи. Ізотони. Ізобари. 2. Розподіл електронів по енергетичних рівнях і підрівнях. 3. Структура періодичної системи з точки зору будови атома. 1
Атомно-молекулярне вчення. Періодичний закон 1. Періодичний закон. Ядерна модель будова атома. Ізотопи. Ізотони. Ізобари. 2. Розподіл електронів по енергетичних рівнях і підрівнях. 3. Структура періодичної системи з точки зору будови атома. 1
 Література 1. Романко П. Д. , Побережний Л. Я. , Загальна хімія (лаб. пр. з комп'ютерною підтримкою), ІФНТУНГ „Факел", 2003. 2. Г. Романко, Л. Побережний, П. Романко, Загальна хімія (конспект лекцій), ІФНТУНГ „Факел", 2002. 3. Романко Г. А. , Романко П. Д. , Побережний Л. Я. , Методичні вказівки для самостійної роботи, розділ „Основні поняття та закони хімії", ІФНТУНГ „Факел", 2000. 4. Романко Г. А. , Романко П. Д. , Побережний Л. Я. , „Задачі і вправи з хімії", ІФНТУНГ „Факел", 2002. 5. Романко Г. А. , Романко П. Д. , Побережний Л. Я. , „Хімія"(приклади і розв'язки), гриф МОН України, ІФНТУНГ „Факел", 2005. 6. Мельник О. Д. , „Загальна хімія" (конспект лекцій), ч. І, гриф МОН України, ІФНТУНГ „Факел", 2004. 7. Мельник О. Д. , „Загальна хімія"(конспект лекцій), ч. II, ІФНТУНГ „Факел", 2005. 8. Романко Г. А. , Романко, П. Д. Мельник О. Д. , Калин Т. І. , Хімія (тести, приклади, розв'язки), гриф МОН України, ІФНТУНГ „Факел". 2
Література 1. Романко П. Д. , Побережний Л. Я. , Загальна хімія (лаб. пр. з комп'ютерною підтримкою), ІФНТУНГ „Факел", 2003. 2. Г. Романко, Л. Побережний, П. Романко, Загальна хімія (конспект лекцій), ІФНТУНГ „Факел", 2002. 3. Романко Г. А. , Романко П. Д. , Побережний Л. Я. , Методичні вказівки для самостійної роботи, розділ „Основні поняття та закони хімії", ІФНТУНГ „Факел", 2000. 4. Романко Г. А. , Романко П. Д. , Побережний Л. Я. , „Задачі і вправи з хімії", ІФНТУНГ „Факел", 2002. 5. Романко Г. А. , Романко П. Д. , Побережний Л. Я. , „Хімія"(приклади і розв'язки), гриф МОН України, ІФНТУНГ „Факел", 2005. 6. Мельник О. Д. , „Загальна хімія" (конспект лекцій), ч. І, гриф МОН України, ІФНТУНГ „Факел", 2004. 7. Мельник О. Д. , „Загальна хімія"(конспект лекцій), ч. II, ІФНТУНГ „Факел", 2005. 8. Романко Г. А. , Романко, П. Д. Мельник О. Д. , Калин Т. І. , Хімія (тести, приклади, розв'язки), гриф МОН України, ІФНТУНГ „Факел". 2
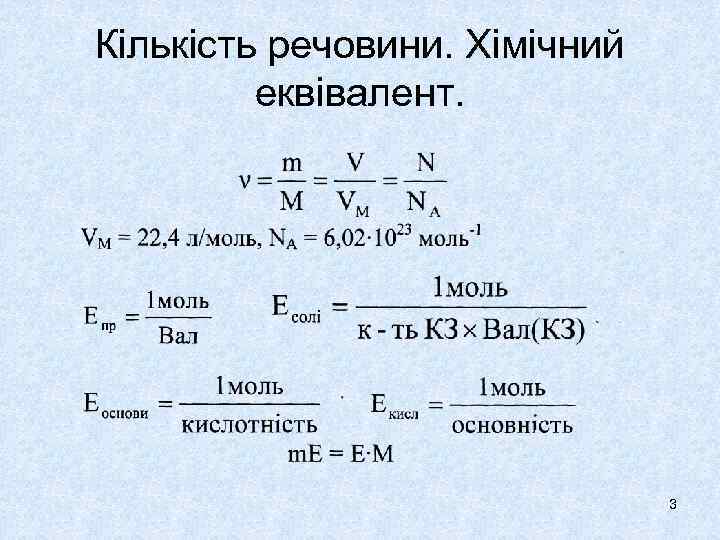 Кількість речовини. Хімічний еквівалент. 3
Кількість речовини. Хімічний еквівалент. 3
 4
4
 5
5
 6
6
 7
7
 Відносна густина газів 8
Відносна густина газів 8
 9
9
 Будова атома Планетарна модель Сучасне уявлення 10
Будова атома Планетарна модель Сучасне уявлення 10
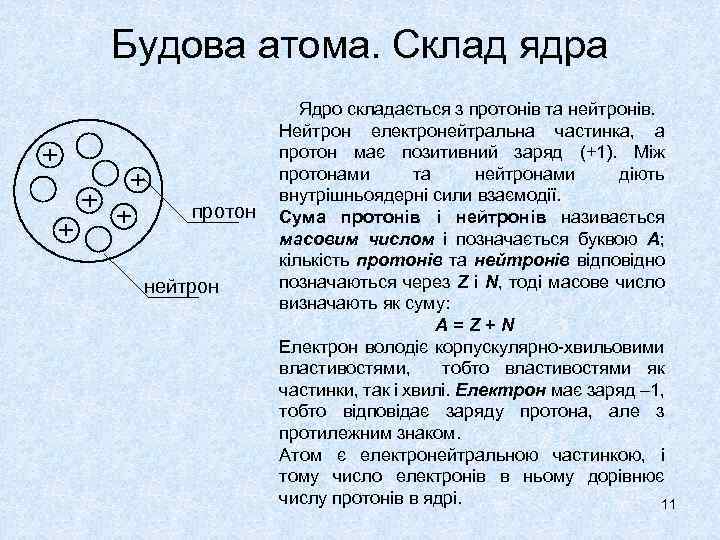 Будова атома. Склад ядра протон нейтрон Ядро складається з протонів та нейтронів. Нейтрон електронейтральна частинка, а протон має позитивний заряд (+1). Між протонами та нейтронами діють внутрішньоядерні сили взаємодії. Сума протонів і нейтронів називається масовим числом і позначається буквою А; кількість протонів та нейтронів відповідно позначаються через Z і N, тоді масове число визначають як суму: А=Z+N Електрон володіє корпускулярно-хвильовими властивостями, тобто властивостями як частинки, так і хвилі. Електрон має заряд – 1, тобто відповідає заряду протона, але з протилежним знаком. Атом є електронейтральною частинкою, і тому число електронів в ньому дорівнює числу протонів в ядрі. 11
Будова атома. Склад ядра протон нейтрон Ядро складається з протонів та нейтронів. Нейтрон електронейтральна частинка, а протон має позитивний заряд (+1). Між протонами та нейтронами діють внутрішньоядерні сили взаємодії. Сума протонів і нейтронів називається масовим числом і позначається буквою А; кількість протонів та нейтронів відповідно позначаються через Z і N, тоді масове число визначають як суму: А=Z+N Електрон володіє корпускулярно-хвильовими властивостями, тобто властивостями як частинки, так і хвилі. Електрон має заряд – 1, тобто відповідає заряду протона, але з протилежним знаком. Атом є електронейтральною частинкою, і тому число електронів в ньому дорівнює числу протонів в ядрі. 11
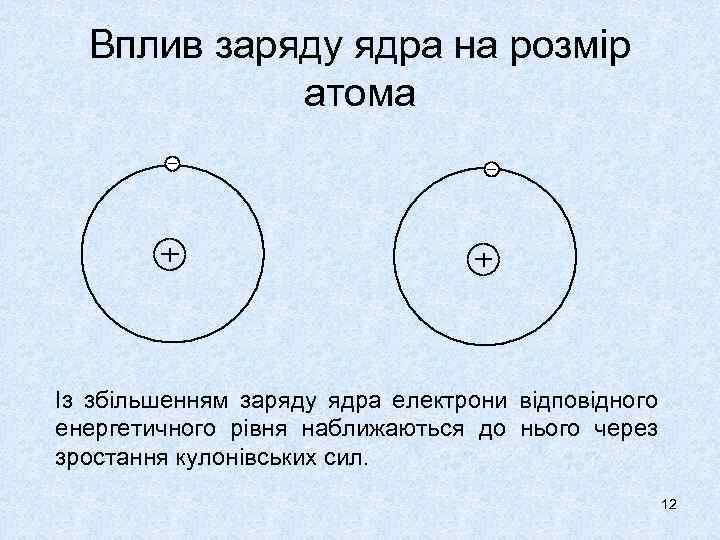 Вплив заряду ядра на розмір атома Із збільшенням заряду ядра електрони відповідного енергетичного рівня наближаються до нього через зростання кулонівських сил. 12
Вплив заряду ядра на розмір атома Із збільшенням заряду ядра електрони відповідного енергетичного рівня наближаються до нього через зростання кулонівських сил. 12
 Ізотопи, ізобари Маса атома дорівнює масовому числу А, тобто є цілим числом, але, як правило, атомні маси хімічних елементів не є цілими числами. Це пояснюється тим, що в природі існують атоми з однаковим зарядом ядра та однаковою кількістю електронів, але з різними масами – ізотопи. Вони відрізняються між собою кількістю ней тронів у ядрі. Атоми з різним числом протонів і нейтронів, але з однаковим числом нуклонів (атомні ядра складаються з елементарних частинок протонів n, які об’єднуються під загальною назвою нуклони) називаються ізобарами. ізотопи ізобари (20 р, 20 n) (18 р, 22 n) (20 р, 22 n) (19 р, 21 n) 13
Ізотопи, ізобари Маса атома дорівнює масовому числу А, тобто є цілим числом, але, як правило, атомні маси хімічних елементів не є цілими числами. Це пояснюється тим, що в природі існують атоми з однаковим зарядом ядра та однаковою кількістю електронів, але з різними масами – ізотопи. Вони відрізняються між собою кількістю ней тронів у ядрі. Атоми з різним числом протонів і нейтронів, але з однаковим числом нуклонів (атомні ядра складаються з елементарних частинок протонів n, які об’єднуються під загальною назвою нуклони) називаються ізобарами. ізотопи ізобари (20 р, 20 n) (18 р, 22 n) (20 р, 22 n) (19 р, 21 n) 13
 Будова атома. Періодичний закон. 14
Будова атома. Періодичний закон. 14
 Квантові числа N – головне квантове число визначає енергію орбіталі, енергетичний рівень. Можливі значення: цілі числа від 1 до ∞. N = 1, 2, 3 … l – побічне квантове число. Показує підрівень енергетичного рівня, на якому знаходиться електрон. l = 0 … (N – 1) m – магнітне квантове число. Показує кількість електронних орбіталей на енергетичному підрівні. m = +l. . . –l s – спінове квантове число. Показує кількість електронів на енергетичному підрівні. s = +1/2 і -1/2.
Квантові числа N – головне квантове число визначає енергію орбіталі, енергетичний рівень. Можливі значення: цілі числа від 1 до ∞. N = 1, 2, 3 … l – побічне квантове число. Показує підрівень енергетичного рівня, на якому знаходиться електрон. l = 0 … (N – 1) m – магнітне квантове число. Показує кількість електронних орбіталей на енергетичному підрівні. m = +l. . . –l s – спінове квантове число. Показує кількість електронів на енергетичному підрівні. s = +1/2 і -1/2.
 Правила заповнення енергетичних рівнів 1 Принцип мінімуму енергії: найстійкішому стану ē в атомі відповідає мінімальна енергія, тобто електрон займає атомну орбіталь з найнижчою енергією. 2 Принцип Паулі: Атом не може мати двох електронів з однаковими значеннями всіх чотирьох квантових чисел. 3 Правило Гунда: Сумарне спінове число електронів певного підрівня повинно бути максимальним (вказує порядок заповнення рівноцінних атомних орбіталей: ↑ ↑ ↑ вірно ↑↓ ↑ невірно 16
Правила заповнення енергетичних рівнів 1 Принцип мінімуму енергії: найстійкішому стану ē в атомі відповідає мінімальна енергія, тобто електрон займає атомну орбіталь з найнижчою енергією. 2 Принцип Паулі: Атом не може мати двох електронів з однаковими значеннями всіх чотирьох квантових чисел. 3 Правило Гунда: Сумарне спінове число електронів певного підрівня повинно бути максимальним (вказує порядок заповнення рівноцінних атомних орбіталей: ↑ ↑ ↑ вірно ↑↓ ↑ невірно 16
 Правила заповнення енергетичних рівнів Період 1 2 3 4 5 6 7 Заповнення електронних орбіталей 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 104 p 6 5 s 2 4 d 105 p 6 6 s 2 5 d 14 f 145 d 96 p 6 7 s 2 6 d 15 f 146 d 5 17
Правила заповнення енергетичних рівнів Період 1 2 3 4 5 6 7 Заповнення електронних орбіталей 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 104 p 6 5 s 2 4 d 105 p 6 6 s 2 5 d 14 f 145 d 96 p 6 7 s 2 6 d 15 f 146 d 5 17
 Історія відкриття періодичного закону Систематизацією хімічних елементів займалися Шанкуртуа у Франції, Мейер і Деберейнер у Німеччині, Ньюлендс в Англії. Деберейнер склав тріади з подібних за хімічними властивостями елементів, вказуючи, що в тріадах атомна вага середнього елемента приблизно дорівнює середньому арифметичному атомних ваг двох крайніх елементів. Ньюлендс помітив, що при розміщенні елементів у порядку зростання їх атомних ваг хімічні властивості восьмого елемента подібні до властивостей першого. Цій закономірності він дав назву закон октав. Мейер, розмістивши елементи в порядку збільшення їхніх атомних ваг, одержав шість груп подібних елементів. Вивчаючи властивості хімічних елементів, Д. І. Менделєєв, як Ньюлендс та Мейєр, в основу систематики елементів поклав атомну масу. Перший варіант періодичної системи елементів Д. І. Менделєєв опублікував в 1869 р. 18
Історія відкриття періодичного закону Систематизацією хімічних елементів займалися Шанкуртуа у Франції, Мейер і Деберейнер у Німеччині, Ньюлендс в Англії. Деберейнер склав тріади з подібних за хімічними властивостями елементів, вказуючи, що в тріадах атомна вага середнього елемента приблизно дорівнює середньому арифметичному атомних ваг двох крайніх елементів. Ньюлендс помітив, що при розміщенні елементів у порядку зростання їх атомних ваг хімічні властивості восьмого елемента подібні до властивостей першого. Цій закономірності він дав назву закон октав. Мейер, розмістивши елементи в порядку збільшення їхніх атомних ваг, одержав шість груп подібних елементів. Вивчаючи властивості хімічних елементів, Д. І. Менделєєв, як Ньюлендс та Мейєр, в основу систематики елементів поклав атомну масу. Перший варіант періодичної системи елементів Д. І. Менделєєв опублікував в 1869 р. 18
 Формулювання періодичного закону: Д. І. Менделєєва властивості простих тіл, а також форми й властивості сполук елементів перебувають у періодичній залежності від величини атомних ваг елементів. Сучасне властивості хімічних елементів перебувають у періодичній залежності від заряду їх атомних ядер. 19
Формулювання періодичного закону: Д. І. Менделєєва властивості простих тіл, а також форми й властивості сполук елементів перебувають у періодичній залежності від величини атомних ваг елементів. Сучасне властивості хімічних елементів перебувають у періодичній залежності від заряду їх атомних ядер. 19
 Структура періодичної системи з точки зору будови атома. Періодична система складається з 7 періодів та 8 груп. Період, який складається з одного ряду, називається малим, а з двох рядів – великим. Група складається з двох підгруп головної і побічної. Періоди – горизонтальні ряди періодичної системи, що починаються лужним металом і закінчуються інертним газом. Номер періоду відповідає числу енергетичних рівнів, на яких розміщуються електрони. Групи – вертикальні стовпчики, що містять подібні за властивостями елементи. Номер групи визначає максимальну кількість валентних (неспарених) електронів. Головні підгрупи складаються з елементів малих і великих періодів. Елементи кожної підгрупи – хімічні аналоги. Побічні підгрупи складаються лише з елементів великих періодів. 20
Структура періодичної системи з точки зору будови атома. Періодична система складається з 7 періодів та 8 груп. Період, який складається з одного ряду, називається малим, а з двох рядів – великим. Група складається з двох підгруп головної і побічної. Періоди – горизонтальні ряди періодичної системи, що починаються лужним металом і закінчуються інертним газом. Номер періоду відповідає числу енергетичних рівнів, на яких розміщуються електрони. Групи – вертикальні стовпчики, що містять подібні за властивостями елементи. Номер групи визначає максимальну кількість валентних (неспарених) електронів. Головні підгрупи складаються з елементів малих і великих періодів. Елементи кожної підгрупи – хімічні аналоги. Побічні підгрупи складаються лише з елементів великих періодів. 20
 Періодичний закон Енергія йонізації – це мінімальна енергія, необхідна для відриву електрона від нейтрального атома. Е - 1ē = Е+ - А(і) Спорідненість до електрона – це енергія, що виділяється в разі приєднання електрона до нейтрального атома Е + 1ē = Е- + А(сп) Електронегативність – це умовна величина, що характеризує здатність атомів у хімічних сполуках відтягнути до себе електрони. Чисельно рівна півсумі енергії йонізації та спорідненості до електрона: ЕН = (А(і) + А(сп))/2 21
Періодичний закон Енергія йонізації – це мінімальна енергія, необхідна для відриву електрона від нейтрального атома. Е - 1ē = Е+ - А(і) Спорідненість до електрона – це енергія, що виділяється в разі приєднання електрона до нейтрального атома Е + 1ē = Е- + А(сп) Електронегативність – це умовна величина, що характеризує здатність атомів у хімічних сполуках відтягнути до себе електрони. Чисельно рівна півсумі енергії йонізації та спорідненості до електрона: ЕН = (А(і) + А(сп))/2 21
 Електронні формули елементів 15 P 1 s 22 p 63 s 23 p 3 25 Mn 1 s 22 p 63 s 23 p 64 s 23 d 5 72 Hf 1 s 22 p 63 s 23 p 64 s 23 d 104 р65 s 24 d 105 р6 6 s 25 d 14 f 145 d 1 72 Hf 1 s 22 p 63 s 23 p 64 s 23 d 104 р65 s 24 d 105 р6 6 s 24 f 145 d 2 83 Bi 1 s 22 p 63 s 23 p 64 s 23 d 104 р65 s 24 d 105 р6 6 s 24 f 145 d 10 6 р3
Електронні формули елементів 15 P 1 s 22 p 63 s 23 p 3 25 Mn 1 s 22 p 63 s 23 p 64 s 23 d 5 72 Hf 1 s 22 p 63 s 23 p 64 s 23 d 104 р65 s 24 d 105 р6 6 s 25 d 14 f 145 d 1 72 Hf 1 s 22 p 63 s 23 p 64 s 23 d 104 р65 s 24 d 105 р6 6 s 24 f 145 d 2 83 Bi 1 s 22 p 63 s 23 p 64 s 23 d 104 р65 s 24 d 105 р6 6 s 24 f 145 d 10 6 р3
 Зміна розмірів атома та хімічних властивостей 23
Зміна розмірів атома та хімічних властивостей 23


