физика1.ppt
- Количество слайдов: 9

Атомная физика и квантовая механика Н. Ф. Кубраков Теоретический отдел, Институт общей физики РАН 2015

Атомная физика дает возможность объяснить физические и химические свойства различных веществ. Основа атомной физики - квантовая механика, которая адекватно объясняет явления происходящие в микромире. Некоторые эксперименты и теоретические модели атома, благодаря которым появилась современная квантовая механика. Модель Томсона (1913) Атом имеет форму шара. Положительный заряд распределен равномерно по всему объему этого шара, а электроны находятся внутри него. Радиус атома равен примерно . Эксперименты доказали ошибочность этой модели. Joseph John Thomson 1856 -1940

Опыты Резерфорда (1906). Планетарная модель атома Новая модель атома предложена Резерфордом после проделанных опытов по изучению рассеяния α-частиц на атомах Au. Ernest Rutherford 1871 -1937 Экран при отсутствии фольги и после ее внесения в поток α-частиц Узкий пучок α-частиц (протоны атомов гелия He 2+, которые испускаются радиоактивным радием Ra) направляются на тонкую золотую фольгу. За ней помещался полупрозрачный экран, покрытый слоем сульфида цинка, который светился под ударами αчастиц. Вспышки (сцинтилляции) на экране наблюдаются с помощью микроскопа. Большая часть α-частиц проходит через фольгу почти без отклонения от направления движения, но весьма малое их число может отклоняться на очень большие углы. Резерфорд показал, что такое рассеяние происходит, если положительный заряд в атоме не распределен так, как в модели Томсона, а локализован в центральной части атома – атомном ядре, где сосредоточена почти вся масса атома. Радиус ядра . Размер самого атома . При таком малом радиусе напряженность электрического поля вблизи ядра слишком велика и наблюдаемые экспериментальные результаты связаны с действием кулоновской силы. Планетарная (ядерная) модель атома (Резерфорд, 1913): электроны обращаются вокруг ядра атома как планеты вокруг Солнца. Радиус орбиты самого удаленного электрона – радиус атома.

Боровская теория атома водорода Планетарная модель объяснила результаты опытов по рассеянию α-частиц, но встретилась с принципиальной трудностью: классические законы движения электронов противоречили законам электродинамики. Электрон, движущийся с ускорением, должен излучать свет – электромагнитные волны с частотой, равной частоте обращения вокруг ядра. Это должно приводить к уменьшению энергии электрона, постепенному его приближению к ядру и неизбежному падению на него через . Согласно классической механики атом неустойчив. В действительности атомы устойчивы и в невозбужденном состоянии не излучают свет. Это противоречие было разрешено теорией Бора для водорода и водородоподобных ионов. – уравнение движения электрона – электрическая постоянная Нет ограничений на радиус орбиты r (проблема размера атома). Классическая механика позволяет атому иметь любой размер, что противоречит опыту . Проблемы были решены Бором (1913) на основе следующих постулатов. Первый постулат Бора Существуют стационарные состояния атома, находясь в которых он не излучает электромагнитных волн Стационарные состояния соответствуют дискретному ряду разрешенных значений полной энергии электрона Изменение энергии связано с квантовым переходом электрона из одного стационарного состояния в другое. Условие стационарности состояния атома – квантование момента импульса электрона Niels Bohr 1885 -1962 – постоянная Планка, n – главное квантовое число

Второй постулат Бора Излучение испускается или поглощается в виде квантов энергии , когда электрон переходит из одного стационарного состояния в другое. Энергия кванта (фотона) равна разности энергий стационарных состояний атома, между которыми происходит переход – энергии стационарных состояний до и после квантового перехода – фотон излучается, – атом поглощает фотон – радиусы стационарных орбит – боровский радиус – полная энергия атома – энергия стационарного состояния атома водорода –энергия основного состояния (n = 1)

Формула Ридберга – формула Ридберга для длины волны излучения – постоянная Ридберга – формула Ридберга для частоты излучения Johannes Rydberg 1854 -1919 Согласно теории Бора спектр атома водорода имеет линейчатый характер. Наблюдаемые линии объединены в спектральные серии. Серия определяется номером m уровня, на который происходит квантовый переход.
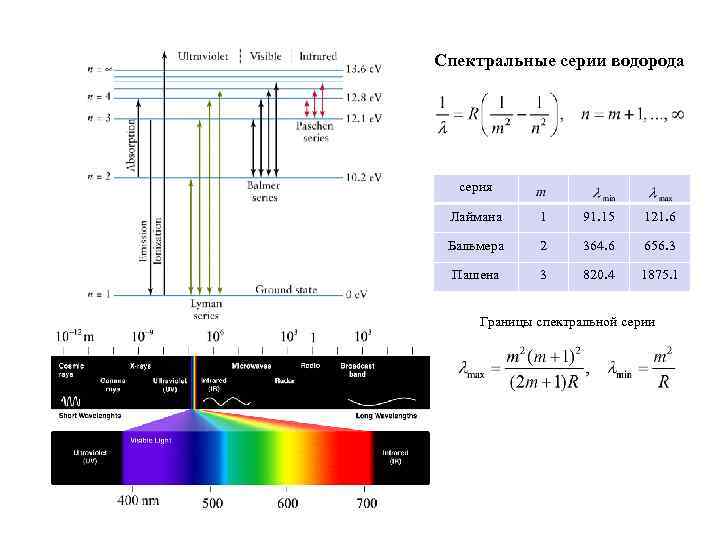
Спектральные серии водорода серия Лаймана 1 91. 15 121. 6 Бальмера 2 364. 6 656. 3 Пашена 3 820. 4 1875. 1 Границы спектральной серии
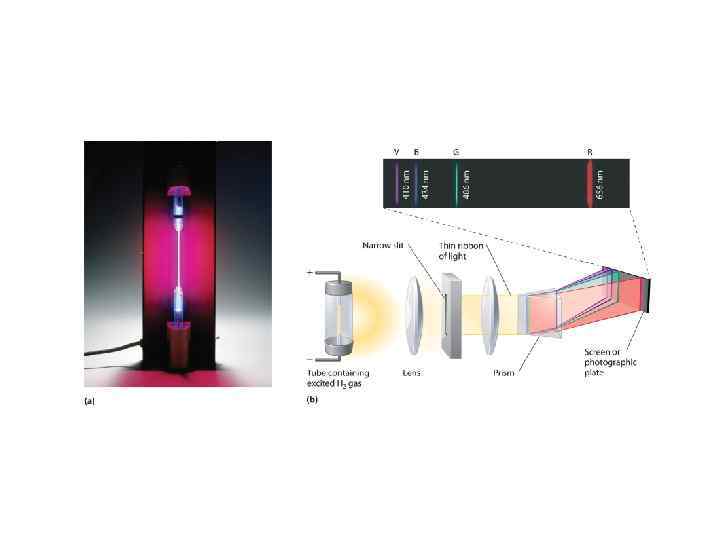
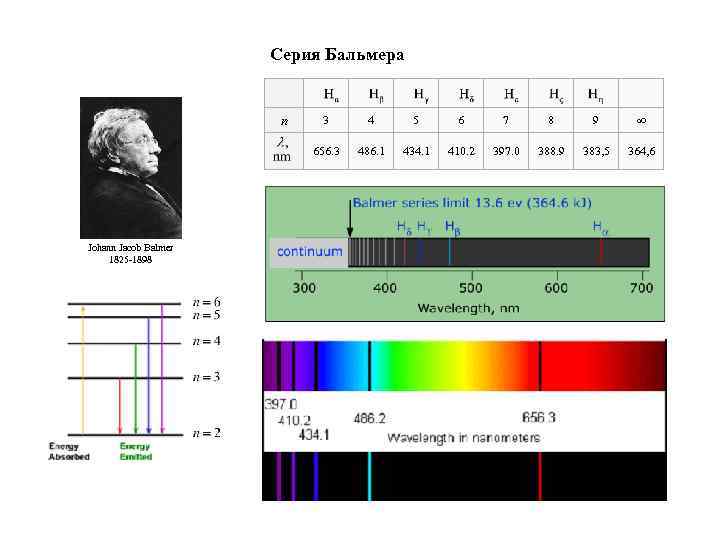
Серия Бальмера n 4 5 6 7 8 9 ∞ 656. 3 Johann Jacob Balmer 1825 -1898 3 486. 1 434. 1 410. 2 397. 0 388. 9 383, 5 364, 6
физика1.ppt