Fizika-2_Atom_fizikasy[1].pptx
- Количество слайдов: 44

АТОМДЫҚ ФИЗИКА Атом физикасы атомның түзілісі және физикалық қасиеттерін зерттейтін физиканың бөлімі. Сутегі атомының спектрлері Жарық сәулелерінің толқын ұзындығы және интенсивтілігі бойынша жіктелуін спектр деп атайды. Ол 3 түрге бөлінеді. l Сызықтық спектр: атомдар сәулеленуі кезінде сызықтық спектр шығарады. l Жолақ спектр: молекулалардың шығаратын спектрі. l Тұтас спектр: қатты денелерді қыздырған кезде тұтас спектр шығарады.
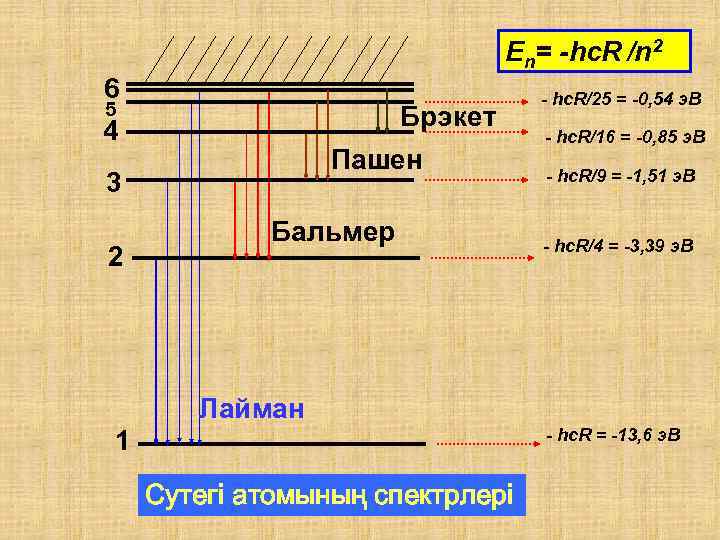
En= -hc. R /n 2 6 5 4 Брэкет Пашен 3 2 Бальмер - hc. R/25 = -0, 54 э. В - hc. R/16 = -0, 85 э. В - hc. R/9 = -1, 51 э. В - hc. R/4 = -3, 39 э. В Лайман 1 - hc. R = -13, 6 э. В Сутегі атомының спектрлері

1885 жылы Бальмер сутегі атомы спектрінің көрінетін бөлігінің тоғызыншы сызығының толқын ұзындығын өрнегімен сипаттауға мүмкін болатынын тағайындады. Ридберг тұрақтысы деп аталады, n=3, 4, 5, … Толқын ұзындығына кері шама толқын саны деп аталады. Бальмер өрнегін сәулеленудің жиілігі үшін мына түрде жазуға болады.

Сутегі атомы спектрлерінің жалпы өрнегі Лайман сериясы үшін: Бальмер сериясы үшін: Пашен сериясы үшін: Брэкет сериясы үшін:

Атом моделі үшін Бордың тағайындаған үш постулаты Бордың бірінші постулаты: атом, кейбір стационар күйлерде, өзінен энергия шығармайды және энергияны жұтпайды. Бордың екінші постулаты: бір стационар күйден екінші стационар күйге көшкенде атом бір квант энергиясын шығарады немесе жұтады. Бордың үшінші постулаты: атомның стационар күйіндегі электроның импульс моменті Планк тұрақтысына еселік болатын дөңгелектік орбита бойынша қозғалады, яғни мына шартты қанағаттандырады: n=1, 2, 3, … сутегі атомының энергетикалық деңгейлерінің ретін анықтайтын бүтін сандар, олар бас кванттық сандар деп аталады.

Сутегі атомындағы электрон орбитасының радиусы м Сутегі атомындағы электронның толық энергиясы Ридберг тұрақтысын қолдансақ
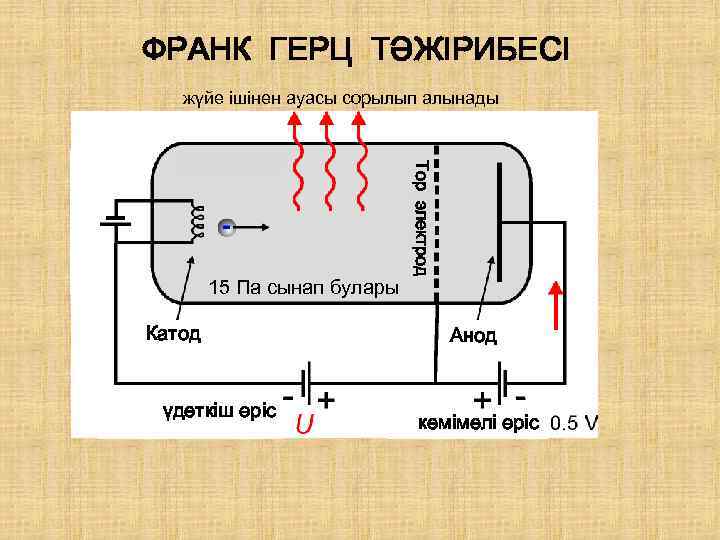
ФРАНК ГЕРЦ ТӘЖІРИБЕСІ жүйе ішінен ауасы сорылып алынады Катод үдеткіш өріс Тор электрод 15 Па сынап булары Анод кемімелі өріс
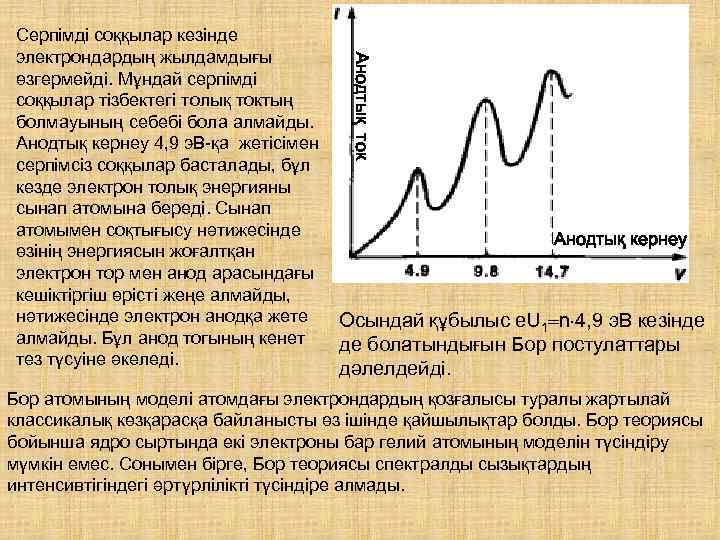
Анодтық ток Серпімді соққылар кезінде электрондардың жылдамдығы өзгермейді. Мұндай серпімді соққылар тізбектегі толық токтың болмауының себебі бола алмайды. Анодтық кернеу 4, 9 э. В-қа жетісімен серпімсіз соққылар басталады, бұл кезде электрон толық энергияны сынап атомына береді. Сынап атомымен соқтығысу нәтижесінде өзінің энергиясын жоғалтқан электрон тор мен анод арасындағы кешіктіргіш өрісті жеңе алмайды, нәтижесінде электрон анодқа жете алмайды. Бұл анод тогының кенет тез түсуіне әкеледі. Анодтық кернеу Осындай құбылыс е. U 1 n 4, 9 э. В кезінде де болатындығын Бор постулаттары дәлелдейді. Бор атомының моделі атомдағы электрондардың қозғалысы туралы жартылай классикалық көзқарасқа байланысты өз ішінде қайшылықтар болды. Бор теориясы бойынша ядро сыртында екі электроны бар гелий атомының моделін түсіндіру мүмкін емес. Сонымен бірге, Бор теориясы спектралды сызықтардың интенсивтігіндегі әртүрлілікті түсіндіре алмады.
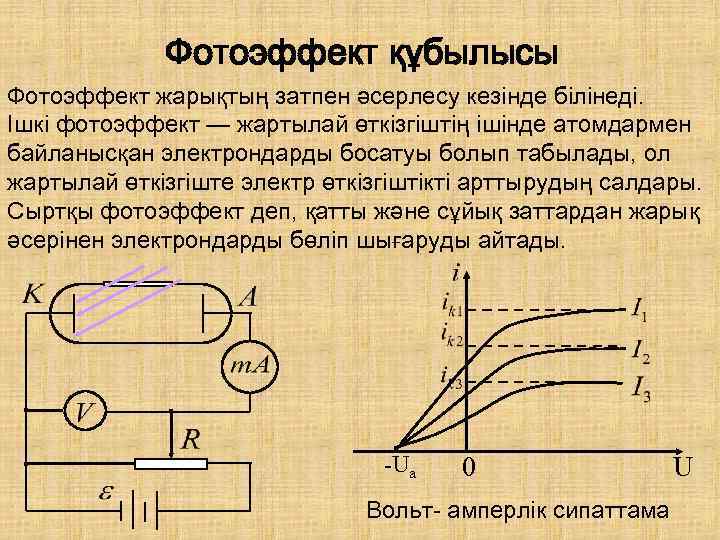
Фотоэффект құбылысы Фотоэффект жарықтың затпен әсерлесу кезінде білінеді. Ішкі фотоэффект — жартылай өткізгіштің ішінде атомдармен байланысқан электрондарды босатуы болып табылады, ол жартылай өткізгіште электр өткізгіштікті арттырудың салдары. Сыртқы фотоэффект деп, қатты және сұйық заттардан жарық әсерінен электрондарды бөліп шығаруды айтады. -Ua 0 Вольт- амперлік сипаттама U

Қанығу фототогы – катодтан шыққан барлық электрондар түгелімен анодқа жеткендігін сипаттайды. Iқанығу=en, мұндағы n – 1 секунд ішінде катодтан шыққан электрондар саны. U=0 болған кезде де фототок жоғалмайды, өйткені фотоэлектрондардың катодтан шығар кезінде бастапқы жылдамдықтары болады. Фототок нөлге теңелген кездегі кернеу тежегіш кернеу U 0 деп аталады. Фотоэффект үшін Эйнштейн тендеуі

Столетов тағайындаған фотоэффект заңдары 1. Уақыт бірлігі ішінде катодтан ыршып шығатын фотоэлектрондардың саны жарық интенсивтілігіне (фотондардың санына) тура пропорционал болады. 2. Фотоэлектрондардың бастапқы максимал жылдамдықтары тек қана түскен жарықтың жиілігімен (энергиясымен ) анықталады. 3. Әрбір зат үшін фотоэффектінің қызыл шегі болады. Фотоэффектінің қызыл шегі деп фотоэффект құбылысын пайда қылатын металға түскен жарықтың ең кішкене жиілігін немесе ең үлкен толқын ұзындығын айтады.

Комптон эффекті

Жарықтың бөлшектік – толқындық екіжақтылығы Жарық бір мезгілде үздіксіз шексіз таралатын толқындық және бөлшектік (фотондар) қасиетке ие болады. 1924 жылы Француз физигі Луи де Бройль бөлшектік және толқындық табиғаты бар сипаттамалар тек электромагниттік толқындар үшін ғана емес, кез келген дененің қозғалыстағы бөлшектерінің барлығына қолдануға болады деген болжамды ортаға қойды. Оның бұл болжамы 1927 ж электрондардың шашырауын бақылаған Дэвиссон мен Джермердің тәжірибелерінде расталды. де Бройль формуласы: Мұнда P дене бөлшегінің импульсі, h Планл тұрақтысы.

Фото және Комптон эффекттің ұқсастығы, айырмашылығы Ұқсастығы : • Екі эффекттің екеуі де жарықтың бөлшектік қасиетін сипаттайды. • Екеуі де фотон мен электронның өзара әсерлесуі нәтижесінде пайда болады. Айырмашылығы : • Фотоэффект құбылысы кезінде бір электрон бір фотонды толық жұтып алады. Ал Комптон эффектісі кезінде фотон бір бөлім энергиясын электронға береді де, өзі шашырап шығып кетеді. Шашыраған сәуленің энергиясы (жиілігі) азайғандықтан толқын ұзындығы ұзарады. • Фотоэффект байланысқан электронмен, Комптон эффекті еркін электронмен өзара әсерлеседі.

Гейзенбергтің анықталмаушылық қатынасы Кеңістіктегі орны белгілі ықималдықпен анықталған микробөлшектің импульсі немесе жылдамдығы тек қандай да бір қателікпен анықталуы мүмкін. Микробөлшектердің бір уақытта орны мен импульсін дәл анықтауға болмайды. Атомдағы электрон ядроны қоршайтын шар қабатында кейбір ықтималдықпен тұруы мүмкін, бұл кезде электрон энергиясын анықтаудағы қателік ∆Е шамасына тең болады. Микробөлшектердің қозғалысын траекториямен сипаттауға болмайды.

ШРЕДИНГЕР ТЕҢДЕУІ Берілген уақыт мезетінде тұрған бөлшектің ықтималдылығын сипаттау үшін деп аталатын толқындық функция енгізіледі. Толқындық функциясының жеке өз бетінше физикалық мәні болмайды, тек толқындық функция модулінің квадратының мәні болады. Ықтималдылық тығыздығы: кеңістіктің берілген нүктесінде бөлшектің болу ықтималдылығын анықтайды. Толқындық функция келесі шартты қанағаттандыруы керек Шексіз кеңістіктегі қандай да бір нүктенің табылуы ықтималдылығы бірге тең.

Жалпы жағдайда Шредингер теңдеуінің түрі мұндағы m – бөлшек массасы, Дж с – Планк тұрақтысы 2 -ға бөлінген, – жорамал өлшем, (x, y, z, t) - толқындық функция, U(x, y, z, t) – күш өрісіндегі бөлшектің потенциялық энергиясы. – Лаплас операторы. Шредингер теңдеуі v « c жылдамдықпен қозғалатын кезкелген бөлшек үшін орынды.

Теңдеудің оң және сол жағын көбейтіндісіне бөлеміз: Теңдеудің сол жағы координатқа, оң жағы уақытқа тәуелді. Біріншісі тек уақытқа тәуелді : Екіншісі тек координатқа тәуелді : Шредингердің стационарлы теңдеуі: (толық энергия)

Толқындық функция : мұндағы 0 – функциясының бастапқы мәні. Сутегі атомындағы электронның күйі үшін шредингердің стационарлы теңдеуі :

Сутегі атомындағы электронның күйі Электронның күйі 4 кванттық саны арқылы анықталады. 1. Бас кванттық сан n : сутегі атомындағы электронның энергетикалық деңгейлерін сипаттайды. n = 1, 2, 3, . . . , 4. Спинді кванттық сан ms = 1/2 : электронның өз өсі бойынша айналуынан болатын меншікті импульс моментін сипаттайды.

Паули принципі Кез келген атомда төрт кванттық сандары бірдей екі электронның болуы мүмкін емес. Кванттық сан n күйдегі электрондардың жалпы саны:
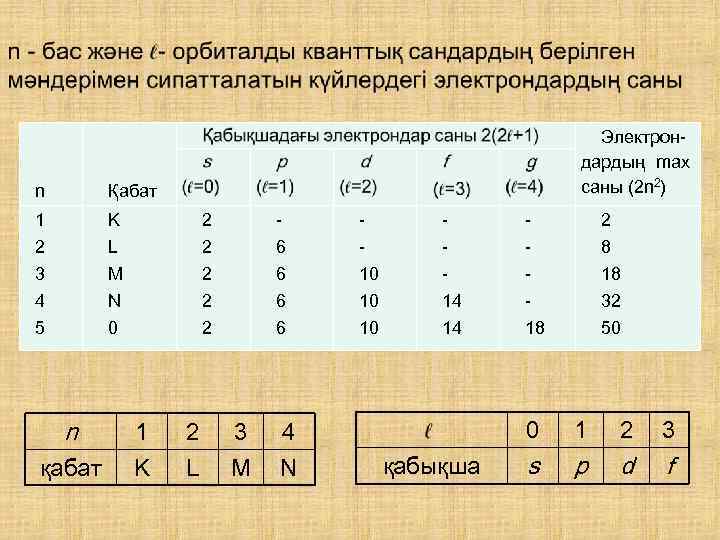
Электрондардың max саны (2 n 2) n Қабат 1 K 2 - - 2 2 L 2 6 - - - 8 3 M 2 6 10 - - 18 4 N 2 6 10 14 - 32 5 0 2 6 10 14 18 50 n қабат 1 K 2 L 3 M 4 N 0 қабықша 1 2 3 s p d f
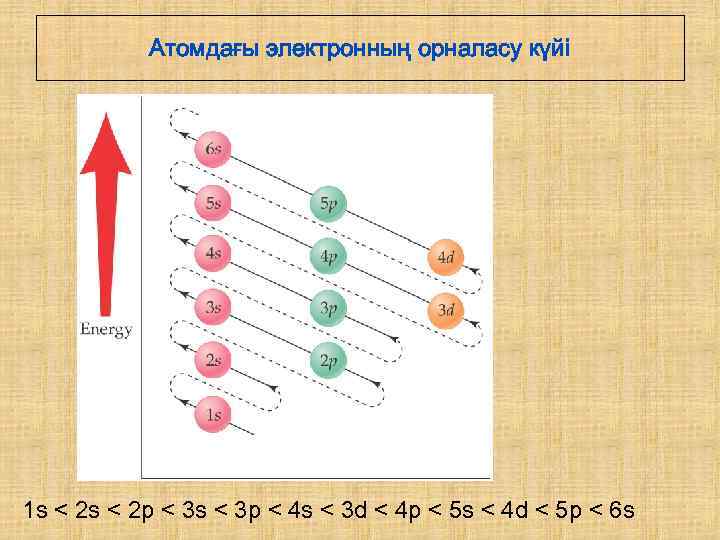
Атомдағы электронның орналасу күйі 1 s < 2 p < 3 s < 3 p < 4 s < 3 d < 4 p < 5 s < 4 d < 5 p < 6 s

Mg атомы электрондарының орналасу күйі ? Mg 12 электрон 1 s < 2 p < 3 s < 3 p < 4 s 1 s 22 p 63 s 2 ns 2 + 6 + 2 = 12 электрон 2(2ℓ+1) : қабықшадағы электрондар саны. n: электронның энергиялық деңгейі: n = 1, 2, 3, . . . , s (ℓ=0), p (ℓ=1), d (ℓ=2) : қабықшадағы электрон күйі Cl атомы электрондарының орналасу күйі ? Cl 17 электрон 1 s < 2 p < 3 s < 3 p < 4 s 1 s 22 p 63 s 23 p 5 2 + 6 + 2 + 5 = 17 электрон
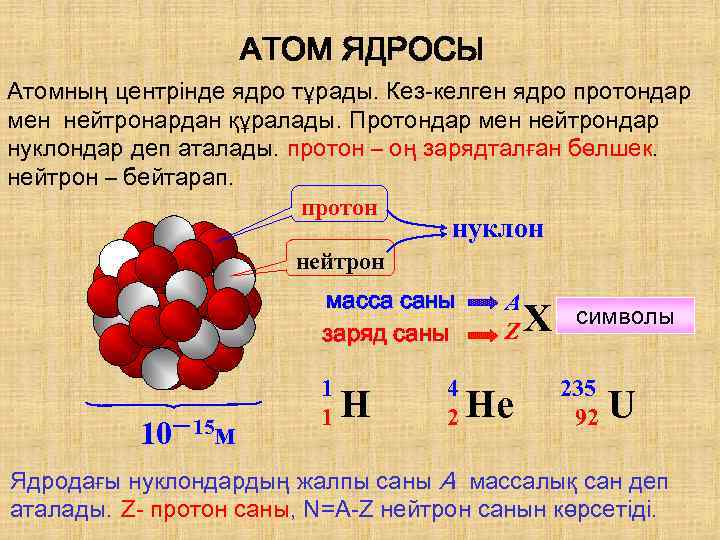
АТОМ ЯДРОСЫ Атомның центрінде ядро тұрады. Кез-келген ядро протондар мен нейтронардан құралады. Протондар мен нейтрондар нуклондар деп аталады. протон – оң зарядталған бөлшек. нейтрон – бейтарап. протон нуклон нейтрон масса саны заряд саны 10-15 м 1 1 H 4 2 A Z He X символы 235 92 U Ядродағы нуклондардың жалпы саны А массалық сан деп аталады. Z- протон саны, N=A-Z нейтрон санын көрсетіді.

Изотоптар: протондар саны бірдей, ал нейтрондар саны немесе массалық саны әртүрлі болатын ядролар. (протий). (дейтрий). (тритий) Изобарлар: нуклидтер саны немесе массалық саны бірдей, ал протондардың әртүрлі ядролар.

Ядроның массасы мен заряды Протонның тыныштық массасы Нейтронның тыныштық массасы Атомның салыстырмалы массасы u Атом ядросының заряды: Электрон заряды мен протон санының көбейтіндісіне тең.

Ядроның радиусы мен тығыздығы Атом ядросының радиусы мұндағы м, А – нуклондар саны. Ядроның көлемі: Ядроның тығыздығы: Ядро тығыздығы өте үлкен шама болып табылады. Материалдығына қарай радиусы 200 м болатын шар, Жер шарының массасын берген болар еді.

Байланыс энергиясы. Масса ақауы Ядроның байланыс энергиясы деп, ядроны нуклондарға ажырату үшін қажет болатын энергияны айтады. мұндағы протонның, нейтронның және ядроның массалары. Масса деффектісі: Меншікті байланыс энергиясы (бір бөлшекке келетін байланыс энергиясы)

Радиоактивті сәулелену және оның түрлері Ядроның өздігінен ыдырауы кезінде сәулелері шығарылады. Мұны радиоактивті сәулелену деп атайды. сәулелері – гелий ( ) атом ядросының ағыны; сәулелері – жылдам электрондар ағыны; сәулелері – қысқа толқынды электромагнитті сәулелену Гамма сәулелері не электр өрісінде, не магнит өрісінде ауытқымайды. Альфа сәулесі электр өріс бағыты бойынша, ал бетта сәулесі электр өрісіне қарама-қарсы бағытта ауытқиды. Альфа сәулесі магнит өрісінде бас бармақ бағыты бойынша, ал бетта сәулесі бас бармаққа қарамақарсы бағытта ауытқиды (сол қол ережесі бойынша).
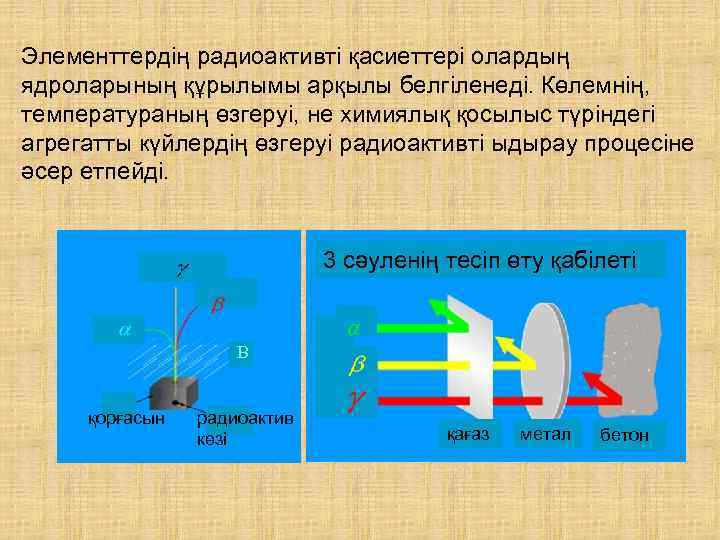
Элементтердің радиоактивті қасиеттері олардың ядроларының құрылымы арқылы белгіленеді. Көлемнің, температураның өзгеруі, не химиялық қосылыс түріндегі агрегатты күйлердің өзгеруі радиоактивті ыдырау процесіне әсер етпейді. 3 сәуленің тесіп өту қабілеті B қорғасын радиоактив көзі қағаз метал бетон

Радиоактивті ыдырау заңы мұндағы N 0 – бастапқы t=0 кездегі ыдырамаған ядролардың саны, N – бастапқыдан t уақыт өткен кездегі ядродағы әлі ыдырап үлгімремей қалған ядролар саны. – радиоактивті ыдырау тұрақтысы, e – натурал логарифмдердің негізі. Жартылай ыдырау периоды – барлық ядроның жартысы ыдырауға кеткен уақыт. Орташа өмір сүру уақыты:

Радиоактивті изотоптың А активтілігі деп бір секунд уақыт ішінде ыдыраған ядролар санын айтады. немесе СИ жүйесіндегі активтіліктің өлшемі – беккерель (Бк ). Активтіліктің жүйе сыртындағы өлшемі кюри (Ки ). Бк Радиоактивті изотопты құрайтын атомдар саны: мұндағы – m изотоп массасы, М – молярлы масса, Na – Авогадро саны.

Ығысу ережесі α – ыдырау мына схема бойынша жүргізіледі (α) β – ыдырау кезінде: Уран радиоактивтік ыдырау арқылы қорғасынға айналу барысында қанша рет α – ыдырау, қанша рет β – ыдырау болады? Алдымен массаның сақталу заңы, одан кейін зарядтың сақталу заңы бойынша қарастырамыз.

Гамма сәулеленуі және оның қасиеттері Гамма сәулеленуі өте қысқа толқынды электромагнитті сәулелену. Ол әрқашан атом ядроларының альфа және бетта ыдыраулармен өтеді. Қозған күйде болатын туынды ядролар негізгі күйге қайта көшкенде бірқатар аралық күйлерден өту арқылы гамма сәулеленуі пайда болады. Гамма сәулеленуі қысқатолқындық болғандықтан, ол толқындық қасиетті нашар көрсетеді. Сондықтан, гамма сәулеленуі гамма кванттардың ағыны ретінде қарастырылады. Гамма кванттарының энергиясы 10 кэв-тан 5 Мэв-қа дейінгі аралықтағы мәндерді қабылдайды.

Гамма кванттарының 3 түрлі өзара әсері 1. Фотоэффект. Гамма квант энергиясы : Кэ. В. 2. Комптон эффект. ~ 0, 5 Мэ. В. 3. Электронды-позитронды қосақтың пайда болу процесі. Гамма квант энергиясы : > 1, 02 Мэ. В Позитрон - электронның антибөлшегі, бұл бөлшек тек өте үлкен кинетикалық энергияға ие болғанда ғана өмір сүреді. Егер гамма кванттарының энергиясы бірнеше мега электронвольтқа артса, онда олар ядродан протондарды, нейтрондарды, α-бөлшектерді жұлып алуы мүмкін, яғни ядролық реакцияны пайда болады.

Ядролық реакция деп, атомдық ядроның басқа ядролармен немесе элементар бөлшектермен өзара әсерлесуі кезінде атомдық ядролардың алмасуын айтады. Ядролық реакцияны символды түрін былай жазуға болады немесе мұндағы х және y шығарылған және соңғы ядро, α және b ядролық реакциядағы атқылаушы және шығарылған бөлшектер. Мысалы, немесе

Энергетикалық Q эффектісі Ядролық реакция энергияның бөлінуі бойынша да (экзотермиялық реакция), сонымен бірге сырттан алынған энергияны жұтумен де (термиялық реакция) өтуі мүмкін. Ядролық реакциялардағы бөлінетін және жұтылатын энергияны Q эффектісі деп атайды. Ядролық реакциялар кезінде энергияның, импульстың және импульс моментінің сақталу заңдары орындалады.
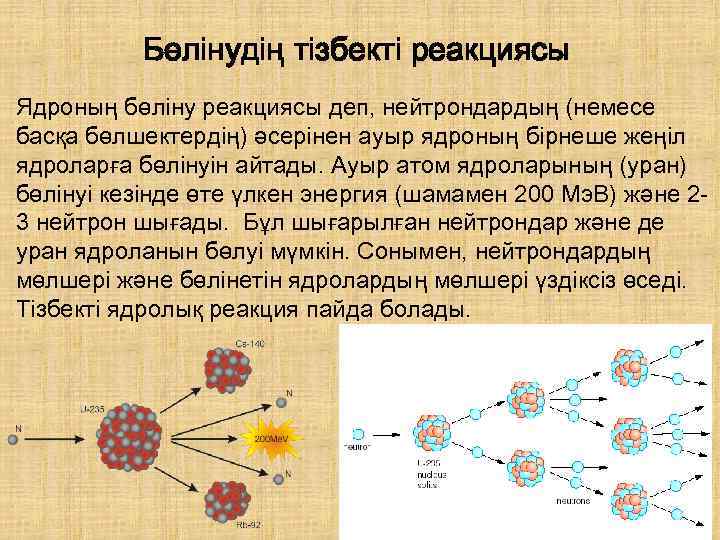
Бөлінудің тізбекті реакциясы Ядроның бөліну реакциясы деп, нейтрондардың (немесе басқа бөлшектердің) әсерінен ауыр ядроның бірнеше жеңіл ядроларға бөлінуін айтады. Ауыр атом ядроларының (уран) бөлінуі кезінде өте үлкен энергия (шамамен 200 Мэ. В) және 23 нейтрон шығады. Бұл шығарылған нейтрондар және де уран ядроланын бөлуі мүмкін. Сонымен, нейтрондардың мөлшері және бөлінетін ядролардың мөлшері үздіксіз өседі. Тізбекті ядролық реакция пайда болады.

Бөлінудің тізбекті реакциясын сипаттау үшін нейтрондардың көбею коэффициенті k деп аталатын түсінік енгізіледі. Көбею коэффициенті осы буындағы нейтрондар санының бұдан алдыңғы буындағы нейтрондар санына қатынасына тең. Тізбекті реакция дамуы үшін k >1 болуы керек. Егер k=1 болса, онда уақыт өткен сайын нейтрондар саны өзгермейді, ол реакция өзін қолдаушы деп аталады. Егер k<1 болса, онда нейтрондардың уақыт бойынша бөліну саны кемиді. Реакция өшетін реакция деп аталады. Тізбекті реакция басқарылатын және басқарылмайтын болып бөлінеді. Атом бомбасының жарылуы – басқарылмайтын реакция. Басқарылатын тізбекті реакция ядролық реакторларда іске асады.

Атомдық ядролардың синтез реакциясы Жеңіл атом ядроларында өте жоғары температураларда (107 К және одан да жоғары) өтетін ауыр ядролардағы синтез реакциясы термоядролық реакция деп аталады. Синтез реакциясы кезінде бір нуклонға бөлінетін энергия ауыр ядроның бөліну кезіндегі ядродан едәуір артық болады. Мысалы, уран-235 ядросының бөлінуі кезінде 1 нуклонға бөлінетін энергия шамамен 0, 84 Мэ. В-қа тең болады, ал синтез реакциясында бұл шама 2, 5 Мэ. В-ті құрайды.

Элементар бөлшектердің өзара әсері 4 негізгі топқа бөлінеді. 1. Бірінші топқа бір ғана фотон бөлшегі жатады, немесе электромагниттік өрістің кванты жатады. Фотондар электромагниттік өзара әсерлесуге қатысады. 2. Екінші топқа күшті өзара әсерлесуге қатысатын жеңіл бөлшектер – лептондар жатады. Бұл топқа электрондар (е-, е+), электронды нейтрино ( е, ), мюондар ( -, +) және мюонды нейтрино ( , ) жатады. Зарядталған лептондар сонымен қатар электромагниттік өзара әсерлесуге де қатысады. 3. Үшінші топ мезондарды құрайды – олар, күшті өзара әсерлерге қатысушы тұрақсыз бөлшектер. Барлық мезондар үшін спин нөлге тең. Мезондар массасы өте ірі бөлшектер болып табылады.

4. Төртінші топқа кіретіндер нуклондар (p, n) және массалары нуклондардың массасынан артық болатын, массасы тұрақсыз гиперондарды ( , +, -, о, -) қосатын бариондар болып табылады. Барлық бариондар күшті өзара әсерлерге қатысады. Барлық бариондардың спині 1/2 -ге тең. Бөлшектер мен антибөлшектердің қосылуы кезінде бұл бөлшектердің екі еселенген тыныштық энергиясына тең энергиясымен бөлінетін олардың аннигиляциясы болады.

КВАРК 1964 жылы Гелл-Манн кварктер туралы гипотеза ұсынды; бұл гипотеза бойынша барлық элементар бөлшектер, кварктер деп аталатын үш бөлшектердің комбинациясынан тұрады. Әдетте, кварктерді P, N, әріптерімен белгілейді және оларға +2/3, -1/3 бөлшектік электрлік зарядтар жазылады, бұлар әрбір кварктерге сәйкес келеді. Бұдан басқа, әрбір кваркке сәйкес антикварктері болады. Мезондар кварк-антикварк қосағынан құралады. Бариондар үш үштен алынған кварктерден құралады. Әрбір кваркке кв бірдей магниттік момент келеді. Әрбір кварк үш түрлі түсте пайда болуы мүмкін: қызыл, сары және көгілдір. Бұл үшті біріктіргенде нөлдік ақ түс шығады.
Fizika-2_Atom_fizikasy[1].pptx