 АТОМ ВОДОРОДА Вступление Опыты Резерфорда. Ядерная модель атома Постулаты Бора. Боровская теория атома водорода Квантовая теория атома водорода Смысл Боровских орбит Квантовые числа
АТОМ ВОДОРОДА Вступление Опыты Резерфорда. Ядерная модель атома Постулаты Бора. Боровская теория атома водорода Квантовая теория атома водорода Смысл Боровских орбит Квантовые числа
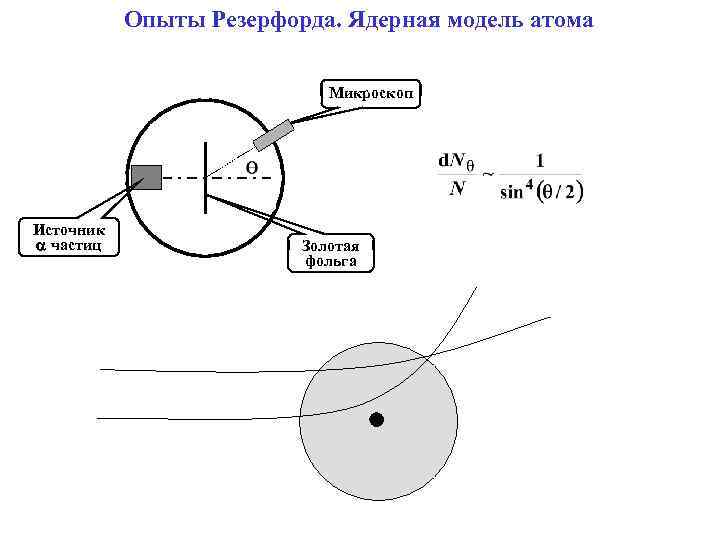 Опыты Резерфорда. Ядерная модель атома Микроскоп Источник a частиц Золотая фольга
Опыты Резерфорда. Ядерная модель атома Микроскоп Источник a частиц Золотая фольга
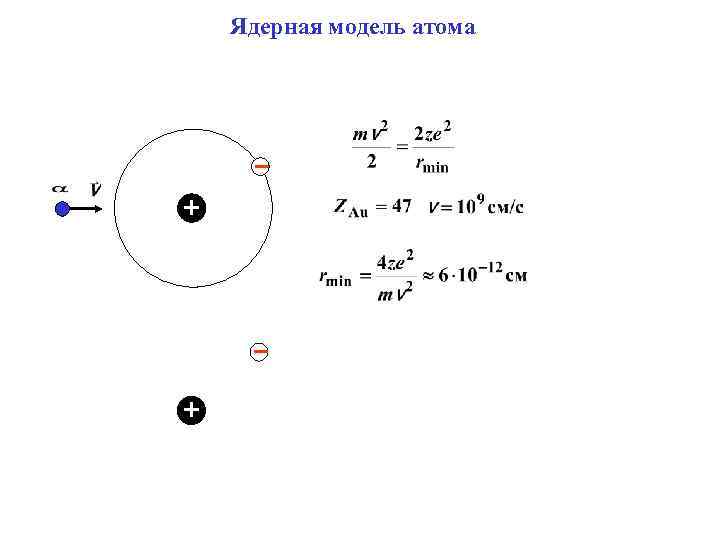 Ядерная модель атома
Ядерная модель атома
 Постулаты Бора 1. Из бесконечного множества электронных орбит, возможных с точки зрения классической механики, реализуются в действительности только некоторые дискретные орбиты, удовлетворяющие определенным квантовым условиям. Такие орбиты называются стационарными. Находясь на стационарных орбитах электроны не излучают электромагнитных волн не смотря на то, что движутся с ускорением. 2. Излучение испускается или поглощается в виде светового кванта энергии при переходе электрона из одного стационарного состояния в другое. Правило квантования круговых орбит: Излучаемая или поглощаемая энергия:
Постулаты Бора 1. Из бесконечного множества электронных орбит, возможных с точки зрения классической механики, реализуются в действительности только некоторые дискретные орбиты, удовлетворяющие определенным квантовым условиям. Такие орбиты называются стационарными. Находясь на стационарных орбитах электроны не излучают электромагнитных волн не смотря на то, что движутся с ускорением. 2. Излучение испускается или поглощается в виде светового кванта энергии при переходе электрона из одного стационарного состояния в другое. Правило квантования круговых орбит: Излучаемая или поглощаемая энергия:
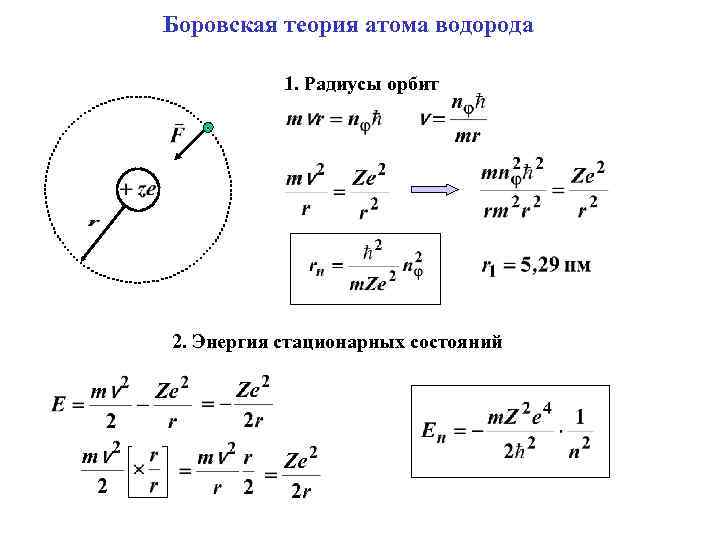 Боровская теория атома водорода 1. Радиусы орбит 2. Энергия стационарных состояний
Боровская теория атома водорода 1. Радиусы орбит 2. Энергия стационарных состояний
 Квантовая теория атома водорода Квантование момента импульса Момент импульса как вектор не определен z Lz |L| l - азимутальное квантовое число ml - магнитное квантовое число
Квантовая теория атома водорода Квантование момента импульса Момент импульса как вектор не определен z Lz |L| l - азимутальное квантовое число ml - магнитное квантовое число
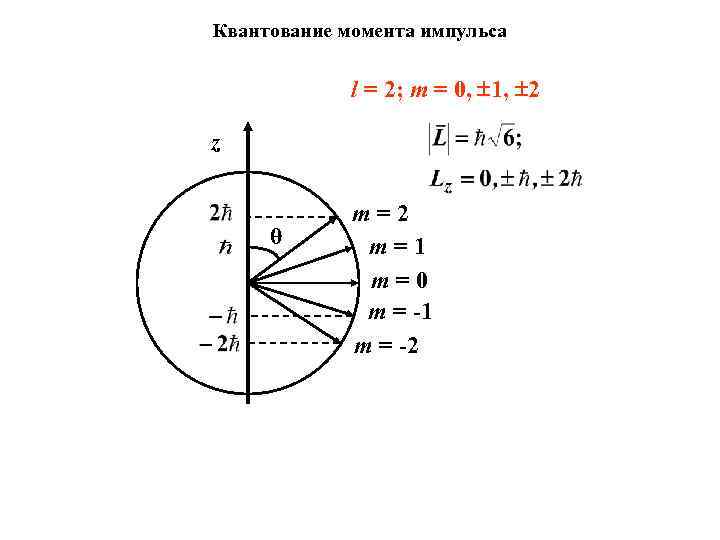 Квантование момента импульса l = 2; m = 0, 1, 2 z θ m=2 m=1 m=0 m = -1 m = -2
Квантование момента импульса l = 2; m = 0, 1, 2 z θ m=2 m=1 m=0 m = -1 m = -2
 Угловая часть волновой функции |m| • ψ(θ, φ)=c. Pl cos(θ)eimφ |m| • Ylm(θ, φ) = c. Pl cos(θ)eimφ - шаровая функция l = 0, m = 0 Y 00(θ, φ) = Момент импульса равен нулю
Угловая часть волновой функции |m| • ψ(θ, φ)=c. Pl cos(θ)eimφ |m| • Ylm(θ, φ) = c. Pl cos(θ)eimφ - шаровая функция l = 0, m = 0 Y 00(θ, φ) = Момент импульса равен нулю
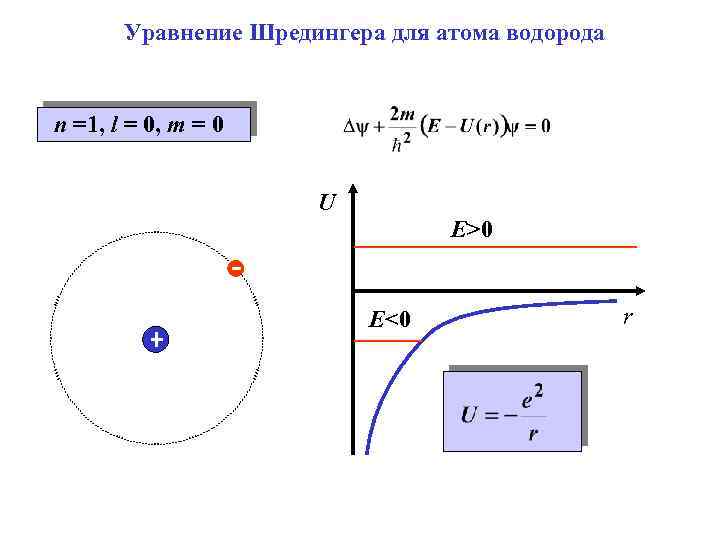 Уравнение Шредингера для атома водорода n =1, l = 0, m = 0 U E>0 E<0 r
Уравнение Шредингера для атома водорода n =1, l = 0, m = 0 U E>0 E<0 r
 n=1, l=0, m=0
n=1, l=0, m=0
 Смысл Боровских орбит z r r + dr y x плотность вероятности
Смысл Боровских орбит z r r + dr y x плотность вероятности
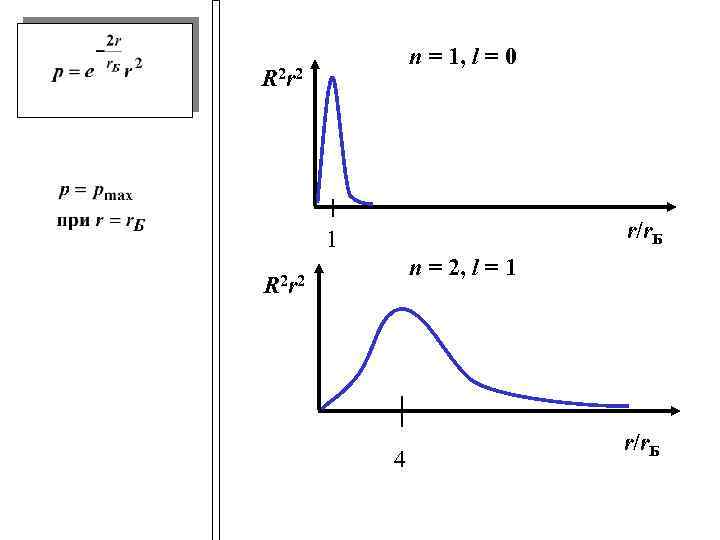 n = 1, l = 0 R 2 r 2 r/r. Б 1 n = 2, l = 1 R 2 r 2 4 r/r. Б
n = 1, l = 0 R 2 r 2 r/r. Б 1 n = 2, l = 1 R 2 r 2 4 r/r. Б
 Квантовые числа n = 1, 2, 3, …. … - главное квантовое число l = 0, 1, 2…. , n-1 - азимутальное m = 0, 1, 2, …, l - магнитное
Квантовые числа n = 1, 2, 3, …. … - главное квантовое число l = 0, 1, 2…. , n-1 - азимутальное m = 0, 1, 2, …, l - магнитное