 Атом водорода в квантовой механике (50. 1) (50. 2) 1. Энергия (50. 3)
Атом водорода в квантовой механике (50. 1) (50. 2) 1. Энергия (50. 3)
 2. Квантовые числа (50. 4) (50. 5) (50. 6) (50. 7) (50. 8)
2. Квантовые числа (50. 4) (50. 5) (50. 6) (50. 7) (50. 8)
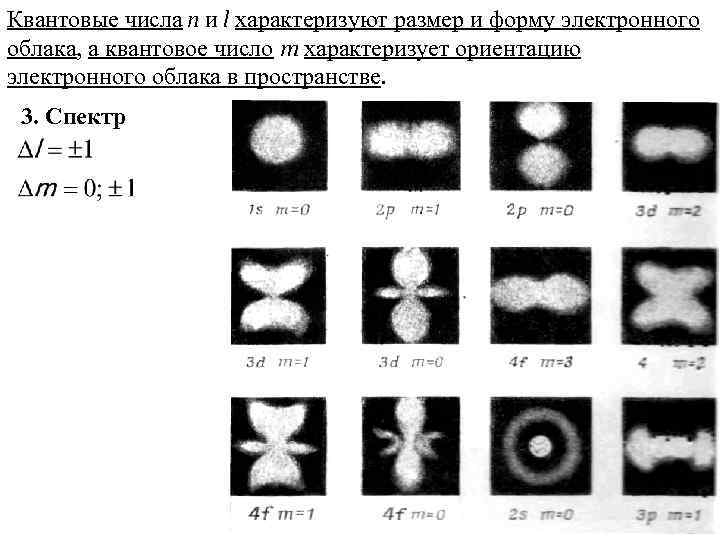 Квантовые числа n и l характеризуют размер и форму электронного облака, а квантовое число m характеризует ориентацию электронного облака в пространстве. 3. Спектр (50. 9)
Квантовые числа n и l характеризуют размер и форму электронного облака, а квантовое число m характеризует ориентацию электронного облака в пространстве. 3. Спектр (50. 9)
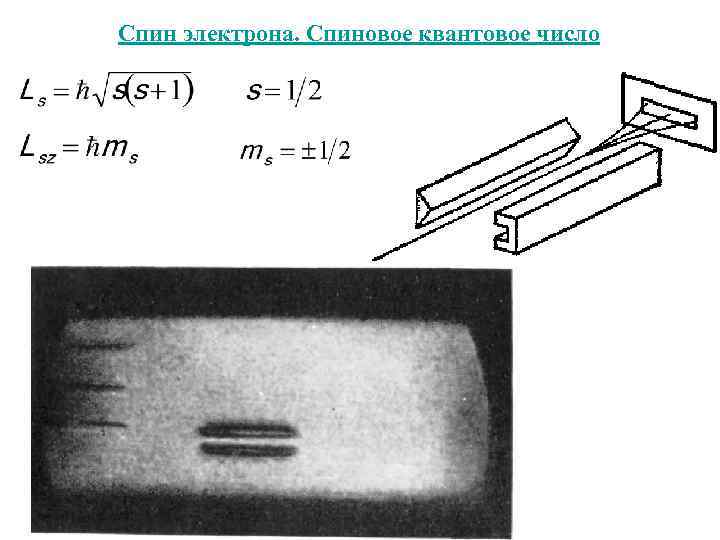 Спин электрона. Спиновое квантовое число
Спин электрона. Спиновое квантовое число
 Принцип неразделимости тождественных частиц. Фермионы и бозоны Принцип неразделимости тождественных частиц состоит в том, что невозможно экспериментально различить тождественные частицы. (53. 1) Если при перемене частиц местами волновая функция не меняет знака, то она называется симметричной, если меняет – антисимметричной. Частицы с полуцелым спином (электроны, протоны, нейтроны) описываются антисимметричными волновыми функциями и подчиняются статистике Ферми- Дирака; эти частицы называются фермионами. Частицы с нулевым или целочисленным спином (π-мезоны, фотоны) описываются симметричными функциями и подчиняются статистике Бозе-Эйнштейна; эти частицы называются бозонами.
Принцип неразделимости тождественных частиц. Фермионы и бозоны Принцип неразделимости тождественных частиц состоит в том, что невозможно экспериментально различить тождественные частицы. (53. 1) Если при перемене частиц местами волновая функция не меняет знака, то она называется симметричной, если меняет – антисимметричной. Частицы с полуцелым спином (электроны, протоны, нейтроны) описываются антисимметричными волновыми функциями и подчиняются статистике Ферми- Дирака; эти частицы называются фермионами. Частицы с нулевым или целочисленным спином (π-мезоны, фотоны) описываются симметричными функциями и подчиняются статистике Бозе-Эйнштейна; эти частицы называются бозонами.
 § 54 Принцип Паули. Распределение электронов в атоме по состояниям Принцип Паули: в системе одинаковых фермионов любые два из них не могут одновременно находится в одном и том же состоянии. Совокупность электронов в многоэлектронном атоме, имеющих одно и тоже главное квантовое число n, называют электронной оболочкой.
§ 54 Принцип Паули. Распределение электронов в атоме по состояниям Принцип Паули: в системе одинаковых фермионов любые два из них не могут одновременно находится в одном и том же состоянии. Совокупность электронов в многоэлектронном атоме, имеющих одно и тоже главное квантовое число n, называют электронной оболочкой.
 § 56 Молекулярные спектры В зависимости от того, изменение каких видов энергии обуславливает испускание молекулой фотона, различают три вида полос: 1) вращательные, 2) колебательно-вращательные, 3) электронно-колебательные.
§ 56 Молекулярные спектры В зависимости от того, изменение каких видов энергии обуславливает испускание молекулой фотона, различают три вида полос: 1) вращательные, 2) колебательно-вращательные, 3) электронно-колебательные.
 Комбинационное рассеяние света (57. 1) Каждому красному (стоксовскому) спутнику (т. е. спутнику, смещенному в сторону больших длин волн) с частотой соответствует фиолетовый (антистоксовский) спутник с частотой. При обычных температурах интенсивность фиолетовых спутников значительно меньше, чем красных. С повышением температуры интенсивность фиолетовых спутников быстро растет.
Комбинационное рассеяние света (57. 1) Каждому красному (стоксовскому) спутнику (т. е. спутнику, смещенному в сторону больших длин волн) с частотой соответствует фиолетовый (антистоксовский) спутник с частотой. При обычных температурах интенсивность фиолетовых спутников значительно меньше, чем красных. С повышением температуры интенсивность фиолетовых спутников быстро растет.