Atom.ppt
- Количество слайдов: 57
 Атом Устойчивая микросистема элементарных частиц, состоящая из положительно заряженного ядра и электронов, движущихся в околоядерном пространстве
Атом Устойчивая микросистема элементарных частиц, состоящая из положительно заряженного ядра и электронов, движущихся в околоядерном пространстве
 • Ядро атома состоит из протонов и нейтронов • Число протонов в ядре равно атомному номеру элемента и числу электронов в атоме • Атом - электронейтрален
• Ядро атома состоит из протонов и нейтронов • Число протонов в ядре равно атомному номеру элемента и числу электронов в атоме • Атом - электронейтрален
 Свойства элементарных частиц Частица поло- заряд масса жение (у. е. ) Протон (p) ядро +1 1, 00728 Нейтрон (n) ядро 0 1, 00867 Позитрон (е) ядро +1 0, 00055 Электрон(е) обо-1 0, 00055 лочка
Свойства элементарных частиц Частица поло- заряд масса жение (у. е. ) Протон (p) ядро +1 1, 00728 Нейтрон (n) ядро 0 1, 00867 Позитрон (е) ядро +1 0, 00055 Электрон(е) обо-1 0, 00055 лочка
 A=Z+N A – массовое число атома Z – заряд ядра (число протонов) N – число нейтронов А Z Э
A=Z+N A – массовое число атома Z – заряд ядра (число протонов) N – число нейтронов А Z Э
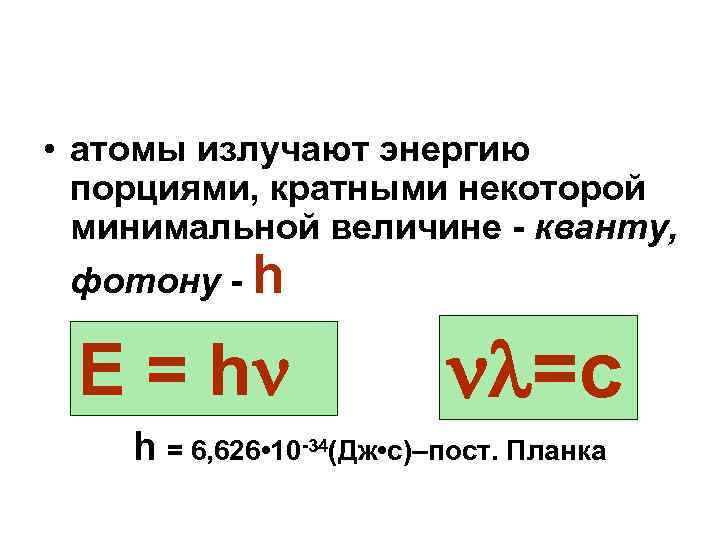 • атомы излучают энергию порциями, кратными некоторой минимальной величине - кванту, фотону - h Е = h =c h = 6, 626 • 10 -34(Дж • c)–пост. Планка
• атомы излучают энергию порциями, кратными некоторой минимальной величине - кванту, фотону - h Е = h =c h = 6, 626 • 10 -34(Дж • c)–пост. Планка
 Принцип корпускулярно-волнового дуализма • При движении электронов проявляются их волновые свойства • При взаимодействии с веществом – корпускулярные • волновые и корпускулярные свойства присущи электронам одновременно
Принцип корпускулярно-волнового дуализма • При движении электронов проявляются их волновые свойства • При взаимодействии с веществом – корпускулярные • волновые и корпускулярные свойства присущи электронам одновременно
 Принцип неопределенности • Движение электрона в атоме не может быть описано определённой траекторией • Положение и скорость движения электрона в атоме можно найти лишь с определенной долей точности
Принцип неопределенности • Движение электрона в атоме не может быть описано определённой траекторией • Положение и скорость движения электрона в атоме можно найти лишь с определенной долей точности


 Квантовые представления • Положение электрона характеризуется вероятностью пребывания частицы в конкретной области пространства • Область наиболее вероятного пребывания электрона в атоме называют атомной орбиталью - АО • Вероятность обнаружения электрона определяется квадратом волновой функцией - 2
Квантовые представления • Положение электрона характеризуется вероятностью пребывания частицы в конкретной области пространства • Область наиболее вероятного пребывания электрона в атоме называют атомной орбиталью - АО • Вероятность обнаружения электрона определяется квадратом волновой функцией - 2
 Квантовые числа • Уравнение Шредингера - трехмерно. Соответственно - три набора квантовых чисел. Каждой координате свое квантовое число. • Размер, энергия, форма и ориентация электронного облака изменяются в атоме скачками (квантами)
Квантовые числа • Уравнение Шредингера - трехмерно. Соответственно - три набора квантовых чисел. Каждой координате свое квантовое число. • Размер, энергия, форма и ориентация электронного облака изменяются в атоме скачками (квантами)
 Главное квантовое число(n) • n - 1, 2, 3, … , определяет энергию электрона в атоме • Энергетический уровень - состояние электронов в атоме с тем или иным значением n • Основное состояние атома - min энергия электронов • Возбужденное состояние – более высокие значения энергии электронов
Главное квантовое число(n) • n - 1, 2, 3, … , определяет энергию электрона в атоме • Энергетический уровень - состояние электронов в атоме с тем или иным значением n • Основное состояние атома - min энергия электронов • Возбужденное состояние – более высокие значения энергии электронов

 Орбитальное квантовое число (l) характеризует форму электронного облака l = 0, 1, 2, 3…. n-1 Подуровень: s, p, d, f, g, h Т. е. энергетический уровень (n) содержит совокупность энергетических подуровней, отличающихся по энергиям (в многоэлектронном атоме)
Орбитальное квантовое число (l) характеризует форму электронного облака l = 0, 1, 2, 3…. n-1 Подуровень: s, p, d, f, g, h Т. е. энергетический уровень (n) содержит совокупность энергетических подуровней, отличающихся по энергиям (в многоэлектронном атоме)
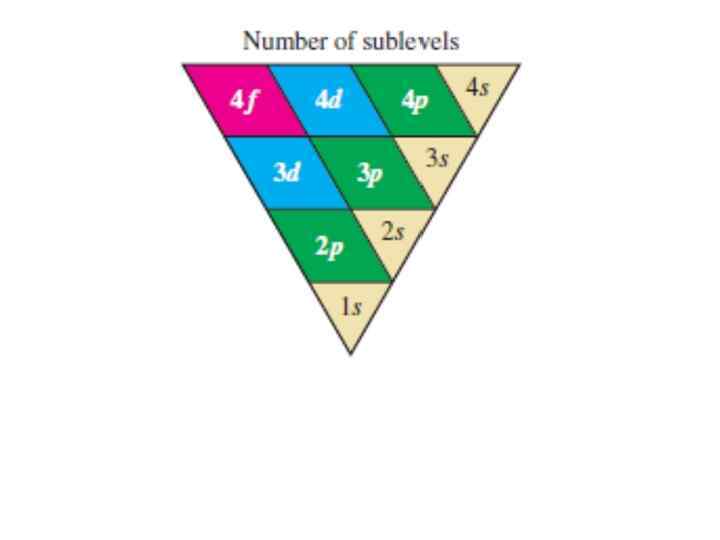
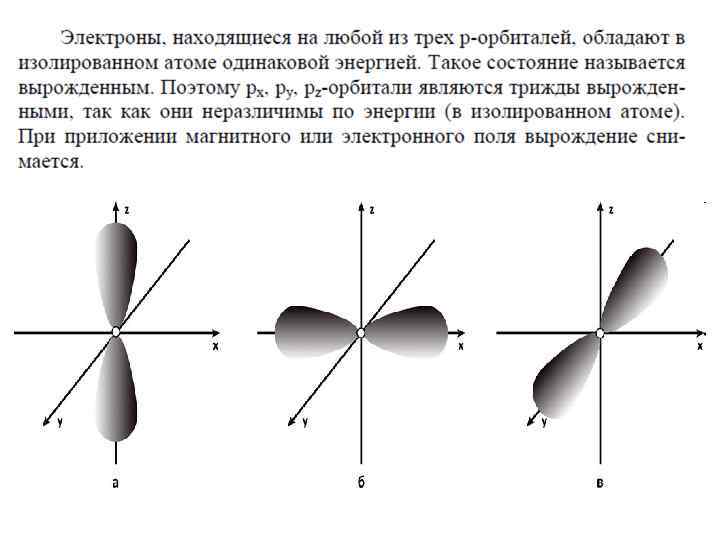
 Магнитное квантовое число (ml) характеризует ориентацию электронных облаков в пространстве ml меняется от –l до +l, = 2 l + 1 значений Например: l = 0 (s); ml = 0 а всего l = 1 (p); ml = 0, +1, -1
Магнитное квантовое число (ml) характеризует ориентацию электронных облаков в пространстве ml меняется от –l до +l, = 2 l + 1 значений Например: l = 0 (s); ml = 0 а всего l = 1 (p); ml = 0, +1, -1
 • Спиновое квантовое число (ms) характеризует собственный магнитный момент электрона, который или совпадает с ориентацией орбитального момента, или направлен в противоположную сторону. • ms имеет значения: +1/2 или -1/2
• Спиновое квантовое число (ms) характеризует собственный магнитный момент электрона, который или совпадает с ориентацией орбитального момента, или направлен в противоположную сторону. • ms имеет значения: +1/2 или -1/2
 • это состояние электрона в атоме, которое описывается волновой функцией с набором из трех квантовых чисел n, l, ml s Условное изображение АО • АО обозначают с помощью кв. чисел Например: 1 s (n = 1, l = 0, ml = 0) 2 p (n = 2, l = 1, ml = -1, 0, +1)
• это состояние электрона в атоме, которое описывается волновой функцией с набором из трех квантовых чисел n, l, ml s Условное изображение АО • АО обозначают с помощью кв. чисел Например: 1 s (n = 1, l = 0, ml = 0) 2 p (n = 2, l = 1, ml = -1, 0, +1)
 • Принцип наименьшей энергии: электрон размещается на АО c min энергией • Принцип Паули: в атоме не может быть двух электронов с одинаковым набором 4 -х кв. чисел
• Принцип наименьшей энергии: электрон размещается на АО c min энергией • Принцип Паули: в атоме не может быть двух электронов с одинаковым набором 4 -х кв. чисел

 • Правила Гунда: (1) на одном подуровне сумма спинов электронов максимальна, (2) сумма магнитных кв-х чисел максимальна.
• Правила Гунда: (1) на одном подуровне сумма спинов электронов максимальна, (2) сумма магнитных кв-х чисел максимальна.
 Правила Клечковского • Ниже по энергии находится та орбиталь для которой сумма (n + l) минимальна • Если сумма (n + l) для двух подуровней одинакова , то сначала эл-ны заполняют АО с меньшим n
Правила Клечковского • Ниже по энергии находится та орбиталь для которой сумма (n + l) минимальна • Если сумма (n + l) для двух подуровней одинакова , то сначала эл-ны заполняют АО с меньшим n

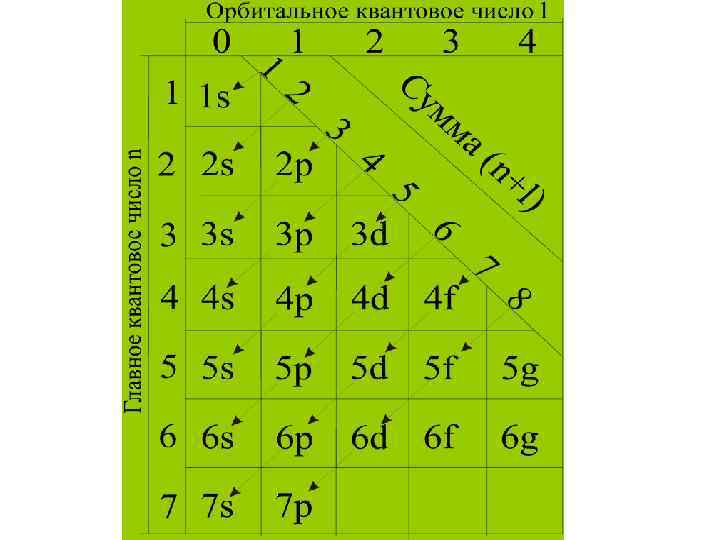
 Последовательность заполнения АО по правилам Клечковского 1 sι 2 s 2 pι 3 s 3 pι 4 s 3 d 4 pι 5 s 4 d 5 pι 6 s 4 f 5 d 6 pι 7 s 5 f 6 d 7 p
Последовательность заполнения АО по правилам Клечковского 1 sι 2 s 2 pι 3 s 3 pι 4 s 3 d 4 pι 5 s 4 d 5 pι 6 s 4 f 5 d 6 pι 7 s 5 f 6 d 7 p
 Способы изображения электронных структур • Электронная формула • Графическая структура • Энергетическая диаграмма
Способы изображения электронных структур • Электронная формула • Графическая структура • Энергетическая диаграмма
 Примеры электронных структур Полная электронная формула Se - 1 s 22 p 63 s 23 p 64 s 23 d 104 p 4 Краткая формула Se - 4 s 24 p 4 Электронно-графическая формула Ti 4 3 2 1
Примеры электронных структур Полная электронная формула Se - 1 s 22 p 63 s 23 p 64 s 23 d 104 p 4 Краткая формула Se - 4 s 24 p 4 Электронно-графическая формула Ti 4 3 2 1
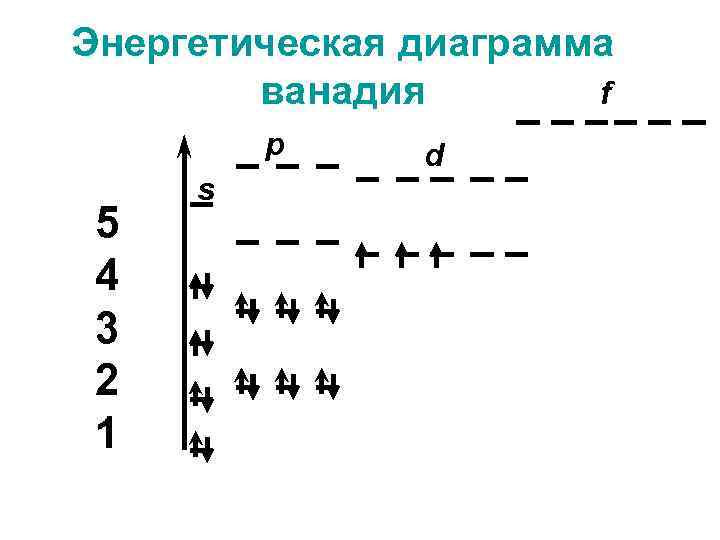 Энергетическая диаграмма f ванадия p 5 4 3 2 1 s d
Энергетическая диаграмма f ванадия p 5 4 3 2 1 s d
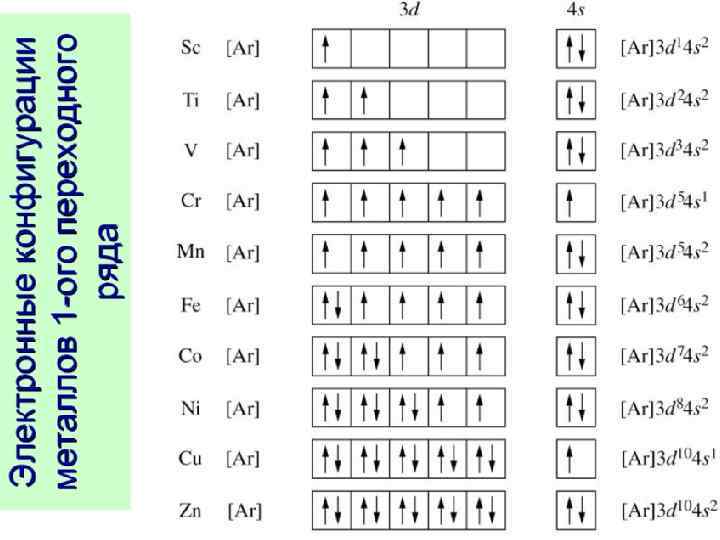
 Проскок электрона Пример: z = 24; Cr Ожидаемая: 22 s 22 p 63 s 23 p 64 s 23 d 4 1 s Действительная: 22 s 22 p 63 s 23 p 64 s 13 d 5 1 s
Проскок электрона Пример: z = 24; Cr Ожидаемая: 22 s 22 p 63 s 23 p 64 s 23 d 4 1 s Действительная: 22 s 22 p 63 s 23 p 64 s 13 d 5 1 s
 Пример: z = 29; Cu Ожидаемая: 22 s 22 p 63 s 23 p 64 s 23 d 9 1 s Действительная: 22 s 22 p 63 s 23 p 64 s 13 d 10 1 s
Пример: z = 29; Cu Ожидаемая: 22 s 22 p 63 s 23 p 64 s 23 d 9 1 s Действительная: 22 s 22 p 63 s 23 p 64 s 13 d 10 1 s
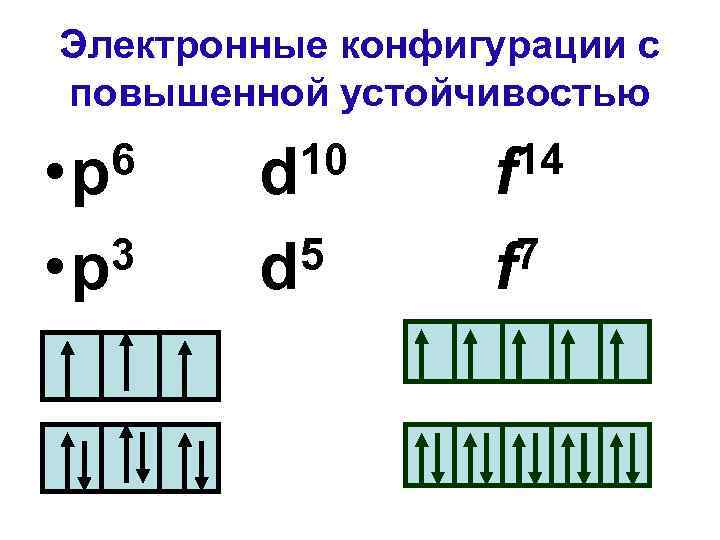 Электронные конфигурации с повышенной устойчивостью 6 • p 10 d 14 f 3 • p 5 d 7 f
Электронные конфигурации с повышенной устойчивостью 6 • p 10 d 14 f 3 • p 5 d 7 f
 Постройте энергетическую диаграмму и запишите электронную конфигурацию атома фосфора Фосфор — 15 элемент Периодической системы. Число электронов равно атомному номеру, то есть 15. Для того, чтобы построить энергетическую диаграмму проведем вертикальную ось и отложим на ней (приблизительно) энергии 1 s, 2 p, 3 s и 3 p атомных орбиталей фосфора. Электроны распределяются по АО согласно принципу наименьшей энергии, принципу Паули и правилу Хунда. На первом энергетическом уровне имеется одна орбиталь s-типа, на которой может находиться два электрона. На втором уровне два типа орбиталей: s и p, причем p-орбиталей три. На каждой орбитали второго уровня находится по два электрона, всего 8. Оставшиеся 5 электронов заполняют 3 s-орбиталь (2 электрона), и 3 pорбитали (3 электрона). На 3 p-орбиталях электроны располагаются по одному на каждой орбитали так, чтобы суммарный спин был максимальным. Валентными являются 5 электронов внешнего энергетического уровня (3 s 23 p 3), что соответствует положению фосфора в Периодической системе.
Постройте энергетическую диаграмму и запишите электронную конфигурацию атома фосфора Фосфор — 15 элемент Периодической системы. Число электронов равно атомному номеру, то есть 15. Для того, чтобы построить энергетическую диаграмму проведем вертикальную ось и отложим на ней (приблизительно) энергии 1 s, 2 p, 3 s и 3 p атомных орбиталей фосфора. Электроны распределяются по АО согласно принципу наименьшей энергии, принципу Паули и правилу Хунда. На первом энергетическом уровне имеется одна орбиталь s-типа, на которой может находиться два электрона. На втором уровне два типа орбиталей: s и p, причем p-орбиталей три. На каждой орбитали второго уровня находится по два электрона, всего 8. Оставшиеся 5 электронов заполняют 3 s-орбиталь (2 электрона), и 3 pорбитали (3 электрона). На 3 p-орбиталях электроны располагаются по одному на каждой орбитали так, чтобы суммарный спин был максимальным. Валентными являются 5 электронов внешнего энергетического уровня (3 s 23 p 3), что соответствует положению фосфора в Периодической системе.
 • Что общего в строении атомов и химических свойствах серы и хрома? • Электронная конфигурация атома серы: 16 S 1 s 22 p 63 s 23 p 4 • Электронная конфигурация атома хрома: 24 Cr 1 s 22 p 63 s 23 p 43 d 44 s 2 • Валентные электроны подчеркнуты. И у атома серы, и у атома хрома их шесть. Поэтому максимальная степень окисления, которую эти элементы проявляют в своих соединениях +6, например SO 3 и Cr. O 3, K 2 SO 4 и K 2 Cr. O 4. Оксиды серы и хрома в высших степенях окисления являются кислотными, им обоим соответствуют сильные кислоты.
• Что общего в строении атомов и химических свойствах серы и хрома? • Электронная конфигурация атома серы: 16 S 1 s 22 p 63 s 23 p 4 • Электронная конфигурация атома хрома: 24 Cr 1 s 22 p 63 s 23 p 43 d 44 s 2 • Валентные электроны подчеркнуты. И у атома серы, и у атома хрома их шесть. Поэтому максимальная степень окисления, которую эти элементы проявляют в своих соединениях +6, например SO 3 и Cr. O 3, K 2 SO 4 и K 2 Cr. O 4. Оксиды серы и хрома в высших степенях окисления являются кислотными, им обоим соответствуют сильные кислоты.
 • Атом какого элемента имеет электронную конфигурацию • 1 s 22 p 63 s 23 p 63 d 104 s 24 p 64 d 105 s 25 p 1? • Решение. • Количество электронов в оболочке нейтрального атома составляет 49. Поэтому его заряд ядра и, следовательно, порядковый номер, также равны 49. В периодической системе Д. И. Менделеева находим, что этот элемент – индий.
• Атом какого элемента имеет электронную конфигурацию • 1 s 22 p 63 s 23 p 63 d 104 s 24 p 64 d 105 s 25 p 1? • Решение. • Количество электронов в оболочке нейтрального атома составляет 49. Поэтому его заряд ядра и, следовательно, порядковый номер, также равны 49. В периодической системе Д. И. Менделеева находим, что этот элемент – индий.
 Периодическая система элементов Свойства элементов, а также формы и свойства их соединений находятся в периодической зависимости от их
Периодическая система элементов Свойства элементов, а также формы и свойства их соединений находятся в периодической зависимости от их
 Неясные моменты • В чем причина периодичности? • Почему элементы одной группы имеют одинаковую валентность и образуют одинаковые соединения? • Почему число элементов в периодах не одинаковое? • Почему в ПС расположение элементов не всегда соответствует возрастанию атомной массы (Аr –
Неясные моменты • В чем причина периодичности? • Почему элементы одной группы имеют одинаковую валентность и образуют одинаковые соединения? • Почему число элементов в периодах не одинаковое? • Почему в ПС расположение элементов не всегда соответствует возрастанию атомной массы (Аr –
 • Свойства элементов, а также формы и свойства их соединений находятся в периодической зависимости от заряда ядер их атомов
• Свойства элементов, а также формы и свойства их соединений находятся в периодической зависимости от заряда ядер их атомов
 Причина периодичности • Определенная последовательность формирования электронных оболочек (принципы и правила Паули, Хунда, Клечковского) • Периодическое повторение сходных электронных слоёв и их усложнение при увеличении главного квантового числа: периоды начинаются sэлементами, а заканчиваются рэлементами
Причина периодичности • Определенная последовательность формирования электронных оболочек (принципы и правила Паули, Хунда, Клечковского) • Периодическое повторение сходных электронных слоёв и их усложнение при увеличении главного квантового числа: периоды начинаются sэлементами, а заканчиваются рэлементами
 Короткие периоды • 1 период (n=1): (2 n 2) 2 элемента (1 s 2) • 2 период (n=2): (2 n 2) 8 элементов (2 s 22 p 6) • 3 период (n=3): (2 n 2 – 2*5) 8 элементов (3 s 23 p 6)
Короткие периоды • 1 период (n=1): (2 n 2) 2 элемента (1 s 2) • 2 период (n=2): (2 n 2) 8 элементов (2 s 22 p 6) • 3 период (n=3): (2 n 2 – 2*5) 8 элементов (3 s 23 p 6)
 Длинные периоды • 4 период (n=4): (2 n 2 -2*7) 18 элементов (4 s 23 d 104 p 6) • 5 период (n=5): (2 n 2 -2(7 + 9) ) 18 элементов (5 s 24 d 105 p 6) • 6 период (n=6): (2 n 2 -2(9 + 11) ) 32 элемента (6 s 24 f 145 d 106 p 6) • 7 период (n=7): (2 n 2 -2(9 + 11 + 13) ) 32 элемента (7 s 25 f 146 d 107 p 6), незавершенный
Длинные периоды • 4 период (n=4): (2 n 2 -2*7) 18 элементов (4 s 23 d 104 p 6) • 5 период (n=5): (2 n 2 -2(7 + 9) ) 18 элементов (5 s 24 d 105 p 6) • 6 период (n=6): (2 n 2 -2(9 + 11) ) 32 элемента (6 s 24 f 145 d 106 p 6) • 7 период (n=7): (2 n 2 -2(9 + 11 + 13) ) 32 элемента (7 s 25 f 146 d 107 p 6), незавершенный
 • Период горизонтальная последовательность элементов, атомы которых имеют равное число энергетических уровней, частично или полностью
• Период горизонтальная последовательность элементов, атомы которых имеют равное число энергетических уровней, частично или полностью
 • Группа - вертикальная последовательность элементов с однотипной электронной конфигурацией атомов, равным числом внешних электронов, одинаковой max валентностью и похожими химическими свойствами
• Группа - вертикальная последовательность элементов с однотипной электронной конфигурацией атомов, равным числом внешних электронов, одинаковой max валентностью и похожими химическими свойствами
 Периодичность свойств элементов • атомные и ионные радиусы • энергия ионизации • сродство к электрону • электроотрицательность • валентность элементов
Периодичность свойств элементов • атомные и ионные радиусы • энергия ионизации • сродство к электрону • электроотрицательность • валентность элементов
 Атомные и ионные радиусы химических элементов • Орбитальный радиус атома (иона) – это расстояние от ядра до максимума электронной плотности наиболее удаленной орбитали этого атома
Атомные и ионные радиусы химических элементов • Орбитальный радиус атома (иона) – это расстояние от ядра до максимума электронной плотности наиболее удаленной орбитали этого атома

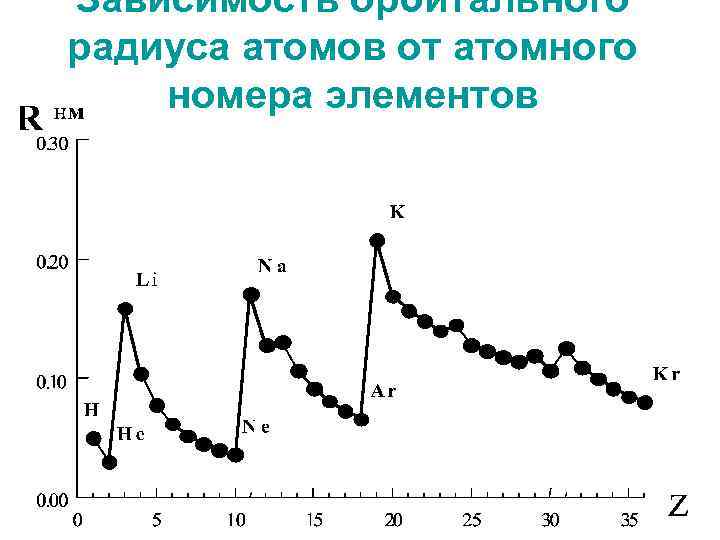 Зависимость орбитального радиуса атомов от атомного номера элементов
Зависимость орбитального радиуса атомов от атомного номера элементов
 Энергия и потенциал ионизации атомов • Энергия ионизации – это энергия, необходимая для отрыва электрона от атома и превращение атома в положительно заряженный ион +, Еион [к. Дж/моль] Э–е=Э • Ионизационный потенциал – это разность потенциалов, при которой происходит ионизация J [э. В/атом]; Еион= 96, 5 • J
Энергия и потенциал ионизации атомов • Энергия ионизации – это энергия, необходимая для отрыва электрона от атома и превращение атома в положительно заряженный ион +, Еион [к. Дж/моль] Э–е=Э • Ионизационный потенциал – это разность потенциалов, при которой происходит ионизация J [э. В/атом]; Еион= 96, 5 • J
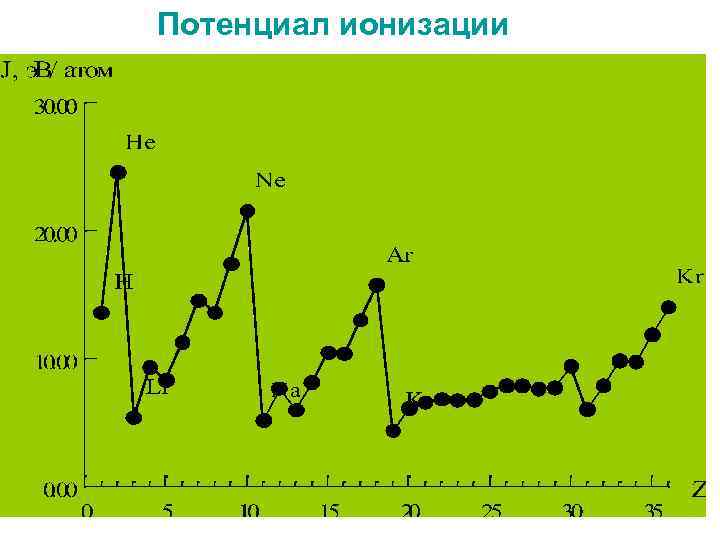 Потенциал ионизации
Потенциал ионизации
 Сродство к электрону • энергия, выделяющаяся или поглощающаяся при захвате электрона атомом или энергия, необходимая для присоединения электрона к атому: Э+е=Э - , F [к. Дж/моль]
Сродство к электрону • энергия, выделяющаяся или поглощающаяся при захвате электрона атомом или энергия, необходимая для присоединения электрона к атому: Э+е=Э - , F [к. Дж/моль]
 Электроотрицательность • - свойство атома притягивать электроны от других атомов, с которыми он образует химическую связь в соединениях • Электроотрицательность выражается в относительных условных единицах
Электроотрицательность • - свойство атома притягивать электроны от других атомов, с которыми он образует химическую связь в соединениях • Электроотрицательность выражается в относительных условных единицах
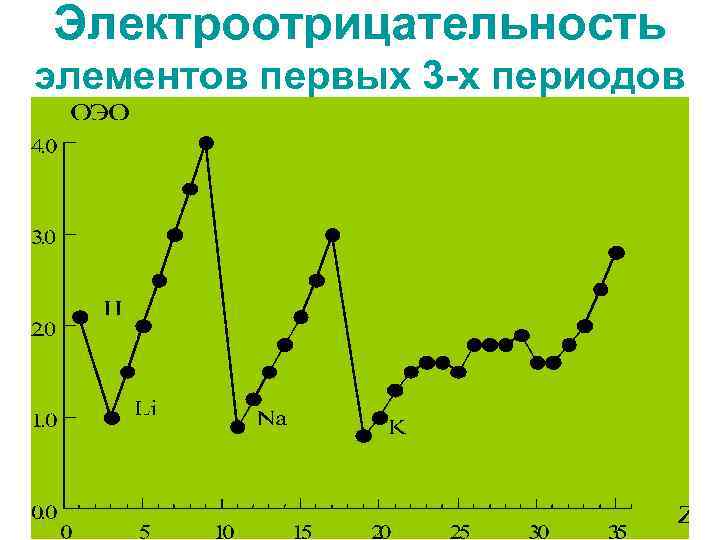 Электроотрицательность элементов первых 3 -х периодов
Электроотрицательность элементов первых 3 -х периодов
 Валентность • Валентность определяется электронами внешнего уровня, поэтому высшая валентность элементов главных подгрупп равна номеру группы
Валентность • Валентность определяется электронами внешнего уровня, поэтому высшая валентность элементов главных подгрупп равна номеру группы
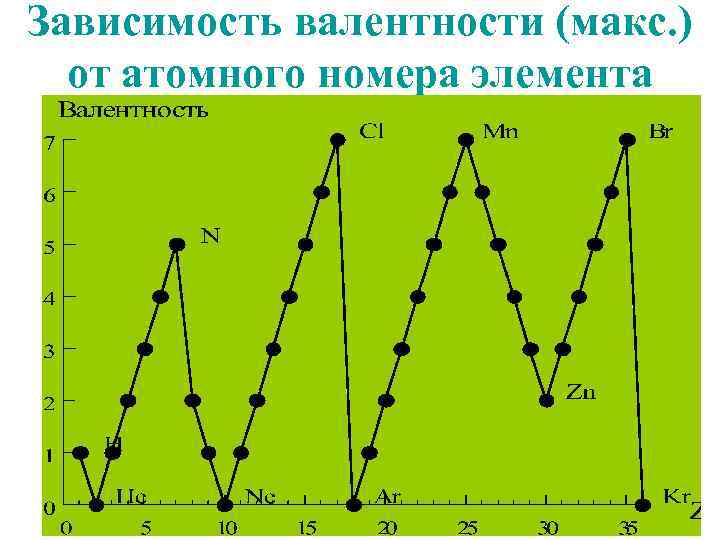 Зависимость валентности (макс. ) от атомного номера элемента
Зависимость валентности (макс. ) от атомного номера элемента
 Периодические свойства соединений • основно-кислотные свойства оксидов и гидроксидов: • в периодах уменьшаются основные свойства, но увеличиваютяся кислотные свойства этих соединений • в группах основные свойства увся, а кислотные уменьшаются
Периодические свойства соединений • основно-кислотные свойства оксидов и гидроксидов: • в периодах уменьшаются основные свойства, но увеличиваютяся кислотные свойства этих соединений • в группах основные свойства увся, а кислотные уменьшаются