Атмосфера.ppt
- Количество слайдов: 57

Атмосфера

Общие сведения Толщина атмосферы ≈ 2000— 3000 км от поверхности Земли. Суммарная масса воздуха ≈ (5, 1— 5, 3)· 1018 кг. Масса сухого воздуха ≈ 5, 1352 ± 0, 0003· 1018 кг, Общая масса водяных паров ≈ 1, 27· 1016 кг. M чистого сухого воздуха ≈ 28, 966 г/моль, ρ поверхности моря ≈ 1, 2 кг/м 3. P(0 °C на уровне моря) ≈ 101, 325 к. Па; Критическая температура — − 140, 7 °C; Критическое давление — 3, 7 МПа; Cp при 0 °C — 1, 0048· 103 Дж/(кг·К), Cv — 0, 7159· 103 Дж/(кг·К) (при 0 °C). Растворимость воздуха в воде (по массе) при 0 °C — 0, 0036 %, при 25 °C — 0, 0023 %. Н. У. у поверхности Земли: ρ=1, 2 кг/м 3, P= 101, 35 к. Па, t=+20 °C и относительная влажность 50 %.
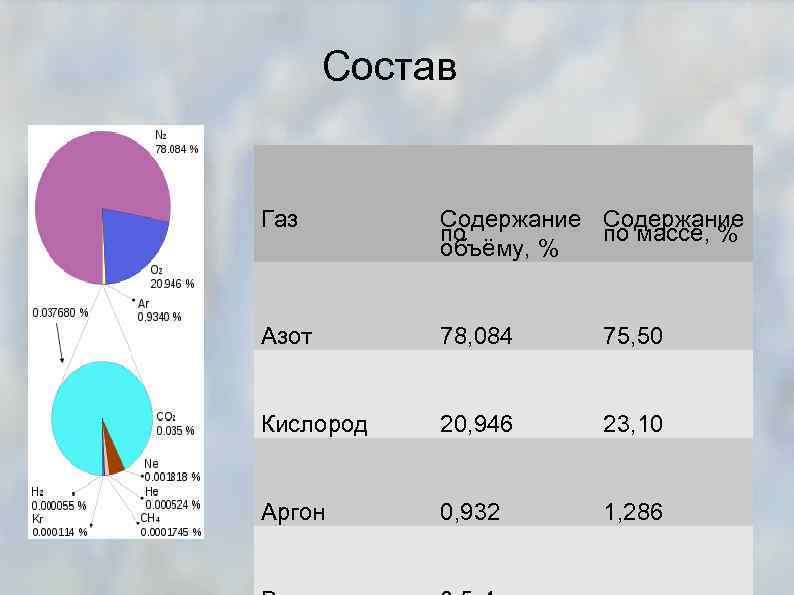
Состав Газ Содержание по по массе, % объёму, % Азот 78, 084 75, 50 Кислород 20, 946 23, 10 Аргон 0, 932 1, 286
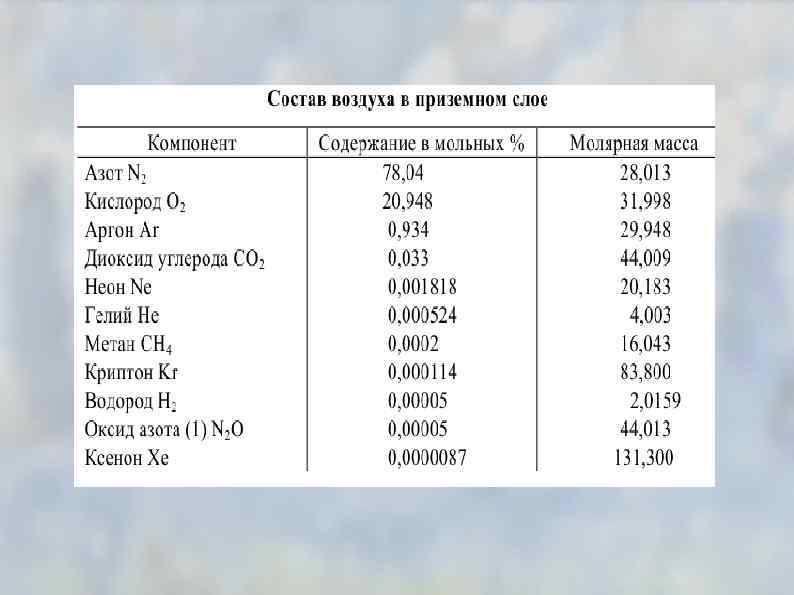
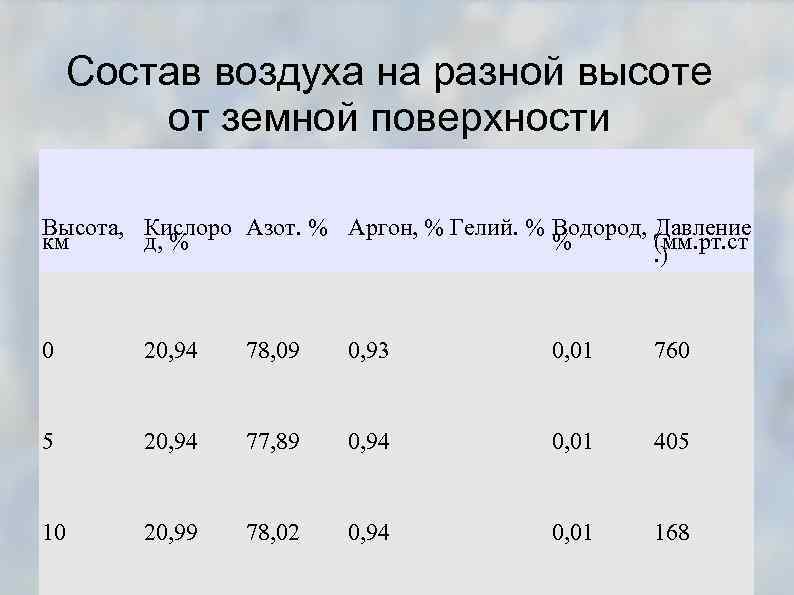
Состав воздуха на разной высоте от земной поверхности Высота, Кислоро Азот. % Аргон, % Гелий. % Водород, Давление км д, % % (мм. рт. ст. ) 0 20, 94 78, 09 0, 93 0, 01 760 5 20, 94 77, 89 0, 94 0, 01 405 10 20, 99 78, 02 0, 94 0, 01 168
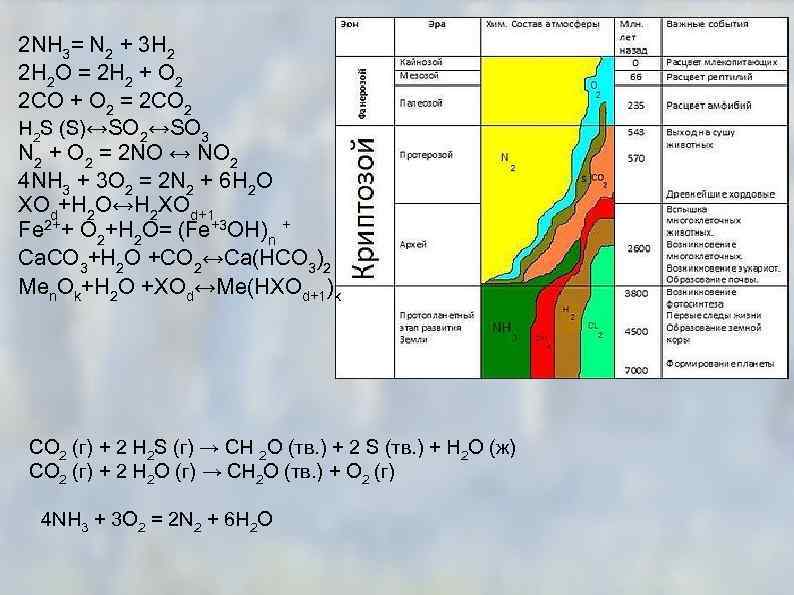
2 NH 3= N 2 + 3 H 2 2 H 2 O = 2 H 2 + O 2 2 CO + O 2 = 2 CO 2 H 2 S (S)↔SO 2↔SO 3 N 2 + O 2 = 2 NO ↔ NO 2 4 NH 3 + 3 O 2 = 2 N 2 + 6 H 2 O XOd+H 2 O↔H 2 XOd+1 Fe 2++ O 2+H 2 O= (Fe+3 OH)n + Ca. CO 3+H 2 O +CO 2↔Ca(HCO 3)2 Men. Ok+H 2 O +XOd↔Me(HXOd+1)k CO 2 (г) + 2 H 2 S (г) → CH 2 O (тв. ) + 2 S (тв. ) + Н 2 О (ж) CO 2 (г) + 2 H 2 O (г) → CH 2 O (тв. ) + О 2 (г) 4 NH 3 + 3 O 2 = 2 N 2 + 6 H 2 O

Основные события истории живого вещества и развития атмосферы и гидросферы. Заштрихованная площадь представляет относительное количество видов организмов. Звездочками обозначены ископаемые, возраст которых установлен калий-аргоновым методом. (Составлено по различным источникам. )
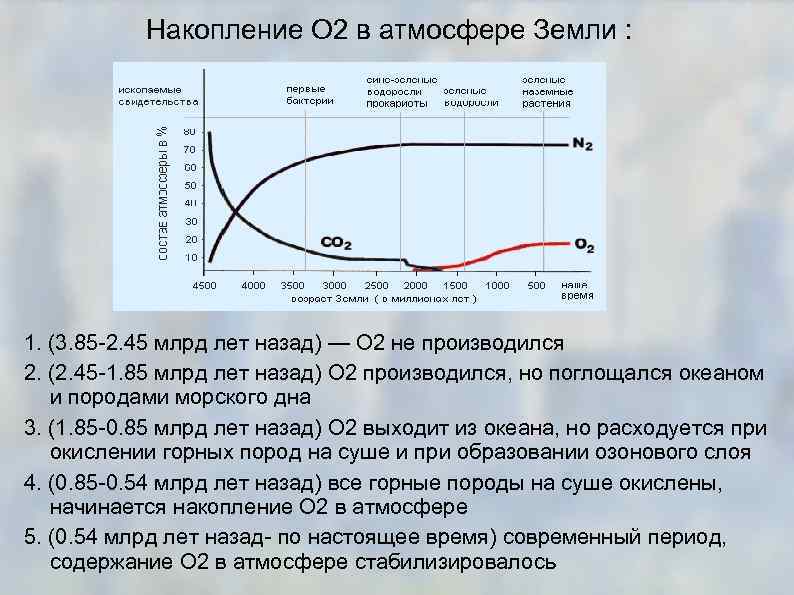
Накопление O 2 в атмосфере Земли : 1. (3. 85 -2. 45 млрд лет назад) — O 2 не производился 2. (2. 45 -1. 85 млрд лет назад) O 2 производился, но поглощался океаном и породами морского дна 3. (1. 85 -0. 85 млрд лет назад) O 2 выходит из океана, но расходуется при окислении горных пород на суше и при образовании озонового слоя 4. (0. 85 -0. 54 млрд лет назад) все горные породы на суше окислены, начинается накопление O 2 в атмосфере 5. (0. 54 млрд лет назад- по настоящее время) современный период, содержание O 2 в атмосфере стабилизировалось

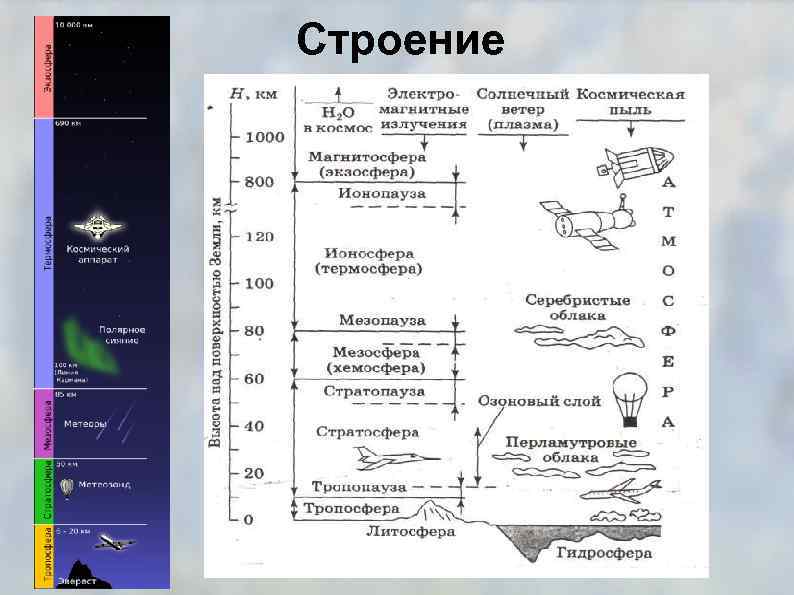
Строение
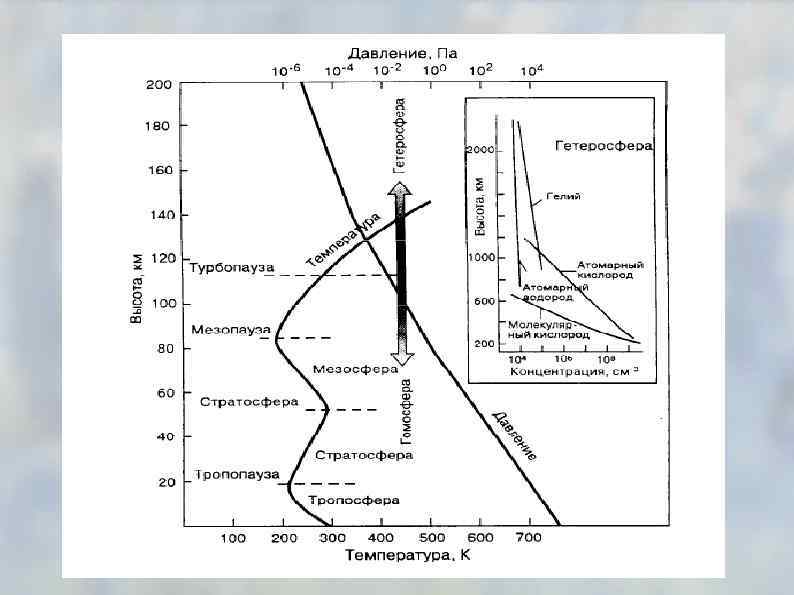
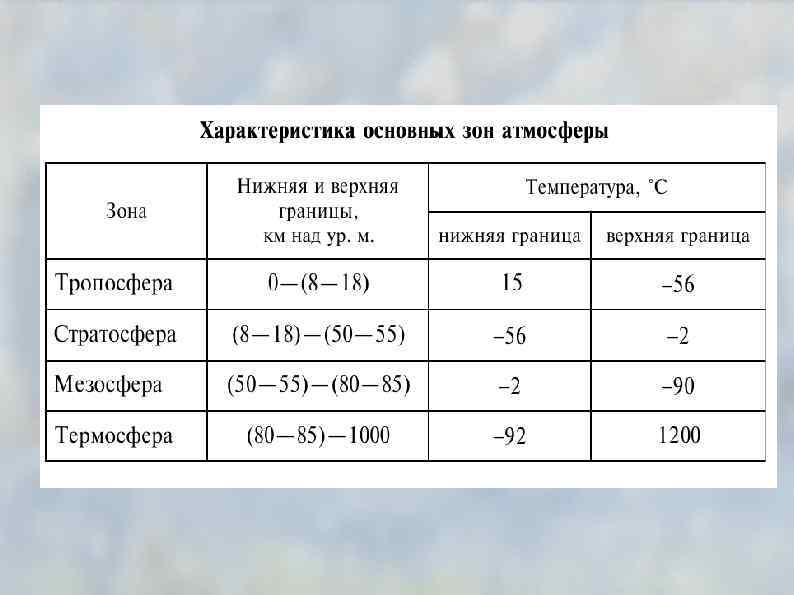

Классификация атмосферных веществ по устойчивости • устойчивые компоненты • неустойчивые компоненты • сильноизменяющиеся компоненты

Источники атмосферных газов биологические антропогенные CO(NH 2) 2 + H 2 O→ 2 NH 3 + CO 2 2 NH 3 + 7 [O] → N 2 O + 3 H 2 O (CH 3)2 S, COS Na. Cl + H 2 SO 4 → HCl + Na. HSO 4 SO 2, CO 2, HCl, HF — вулканы K 40 →Ar 40 + γ Ra 226 → Rn 222 + α U 238 →Th 234 + α геохимические

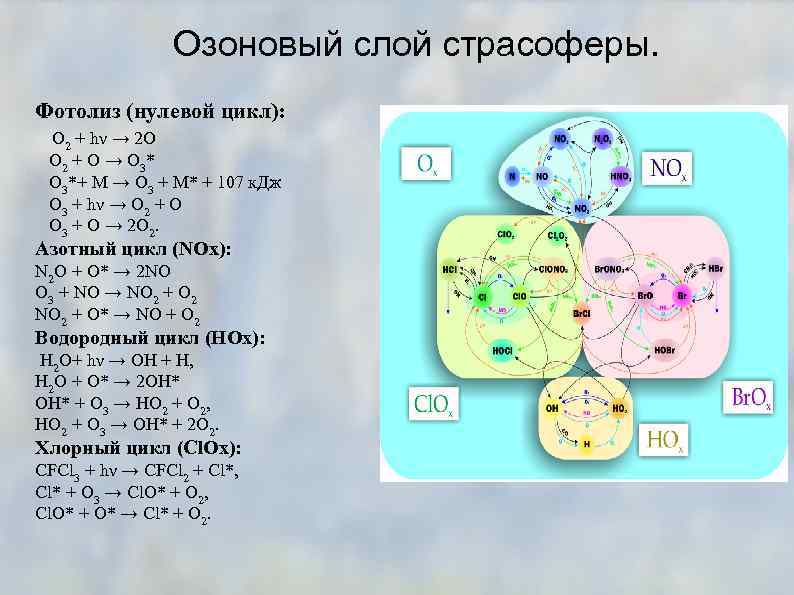
Озоновый слой страсоферы. Фотолиз (нулевой цикл): О 2 + hν → 2 О О 2 + O → О 3 * O 3*+ M → O 3 + M* + 107 к. Дж О 3 + hν → О 2 + О О 3 + O → 2 О 2. Азотный цикл (NOx): N 2 O + O* → 2 NO О 3 + NO → NO 2 + О 2 NO 2 + О* → NO + О 2 Водородный цикл (HOx): Н 2 O+ hν → OH + H, Н 2 O + O* → 2 OH* ОН* + О 3 → НО 2 + О 2, НО 2 + О 3 → ОН* + 2 О 2. Хлорный цикл (Cl. Ox): CFCl 3 + hν → CFCl 2 + Cl*, Cl* + O 3 → Cl. O* + O 2, Cl. O* + O* → Cl* + O 2.
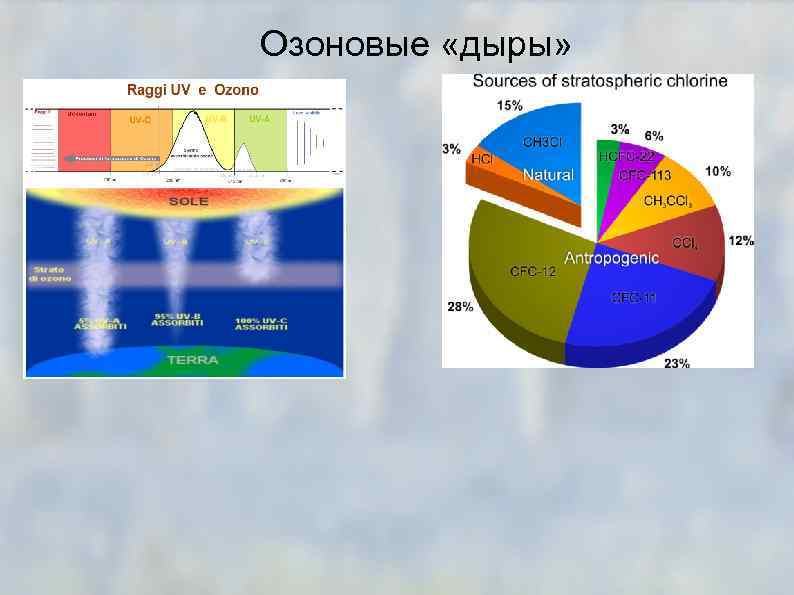
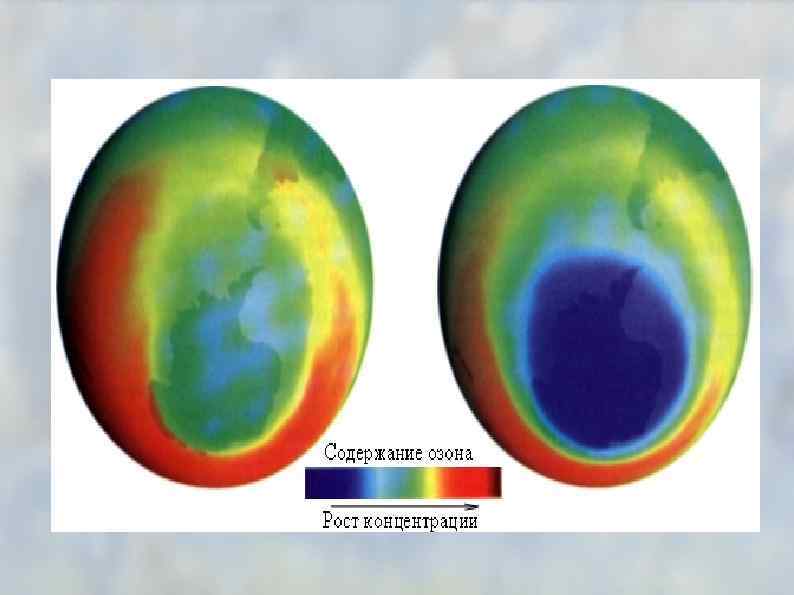
Озоновые «дыры»

Тропосфера Гетеролитический распад + K : A = K + : A - Гомолитический распапад . +. A K : A = K

Образование гидроксильного радикала NO 2 +hν → NO* + O* (λ< 400 нм) O* + O 2 + M → O 3 + M* О 3 + hν → О 2 + О*, (λ =310 нм) О* + Н 2 О → ОН* + ОН* HNO 2 + hν → NO* + OH*, (λ< 400 нм) HNO 3 + hν → NO 2* + OH*, (λ< 330 нм) H 2 O 2 + hν → 2 OH*, (λ< 330 нм)
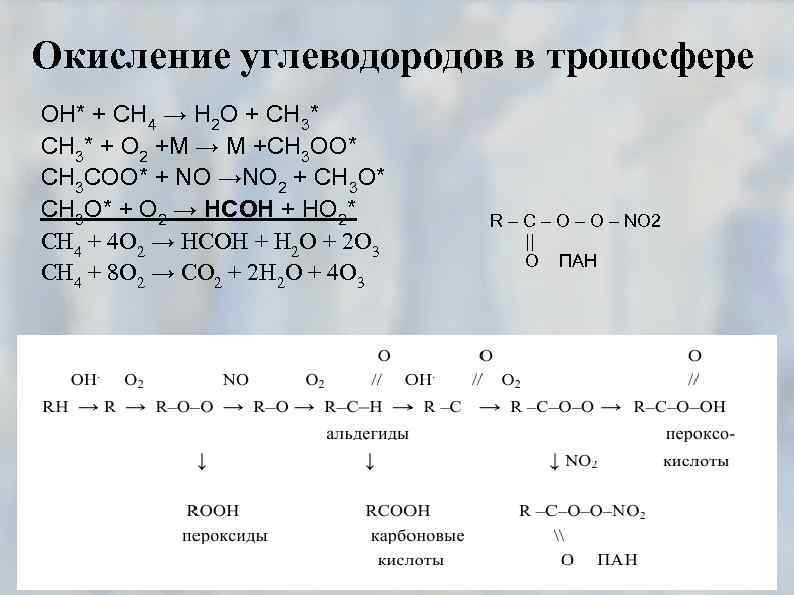
Окисление углеводородов в тропосфере ОН* + СН 4 → Н 2 О + СН 3* СH 3* + O 2 +M → M +CH 3 OO* CH 3 COO* + NO →NO 2 + CH 3 O* + O 2 → HCOH + HO 2* CH 4 + 4 O 2 → HCOH + H 2 O + 2 O 3 СH 4 + 8 O 2 → CO 2 + 2 H 2 O + 4 O 3 R – C – O – NO 2 || O ПАН
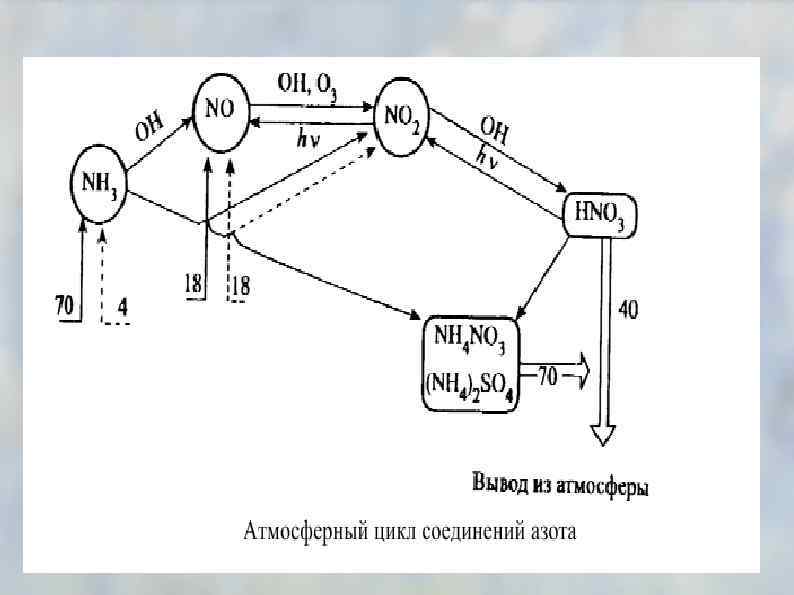
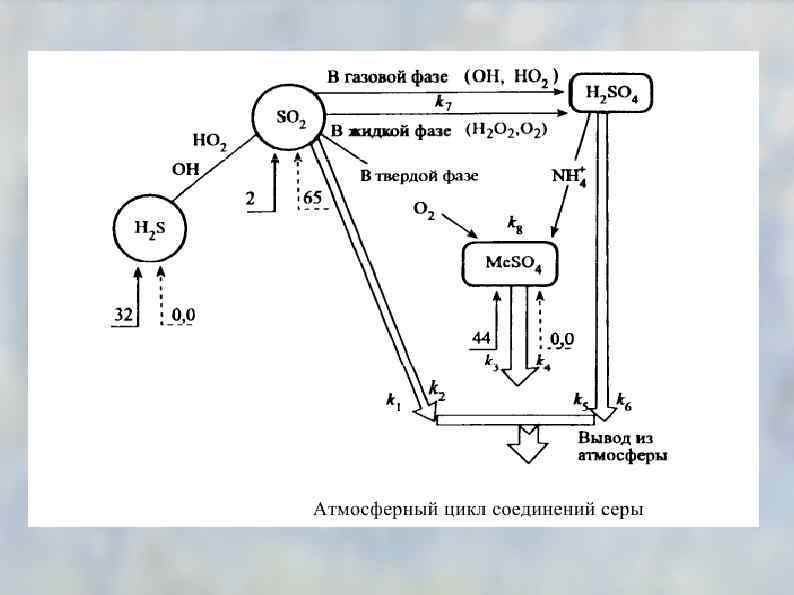

Самоочищение атмосферы Перемещение воздушных масс Осадки и оседание Химическое взаимодействие Биологическое поглощение (пр. фотосинтез) Самоочищение атмосферы приводит к загрязнению других частей биосферы.

Виды смога Влажный смог лондонского типа Ледяной смог аляскинского типа Радиационный туман Сухой смог Лос-анджелесского типа Фотохимический смог

Смог NO 2 + hν → O + NO, O + O 2 + M → O 3 + M, М - третье вещество, принимающее избыток энергии. вий на основе соединений азота в тропосфере дополняет O 3 + NO → O 2 + NO 2 OH* + CH 4 → H 2 O + CH 3 O 2, CH 3 O 2 + NO → CH 3 O + NO 2, CH 3 O + O 2 → HCHO + HO 2 + NO → NO 2 + OH* 4 NO 2 + 2 H 2 O + O 2 → 4 HNO 3 + R–CH=CH–R → RCHO + RO* + HCO*, CO* - свободные радикалы. ПАН
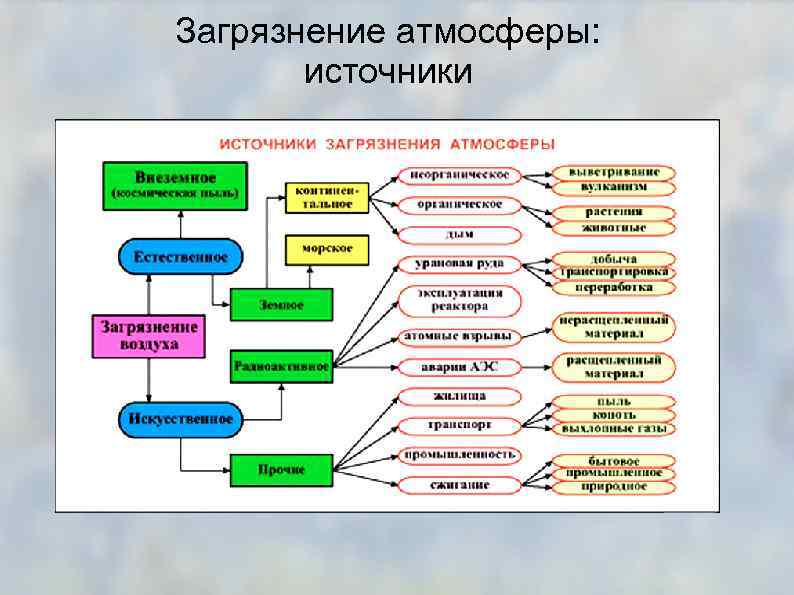
Загрязнение атмосферы: источники

ЗАГРЯЗНЕНИЕ АТМОСФЕРЫ Основной параметр, характеризующий взвешенные частицы, – это их размер. Закон Стокса: где F – сила трения, r – радиус частицы, V – ее скорость и – вязкость среды. Буферная ёмкость экосистемы - способность экосистемы противостоять загрязнению.
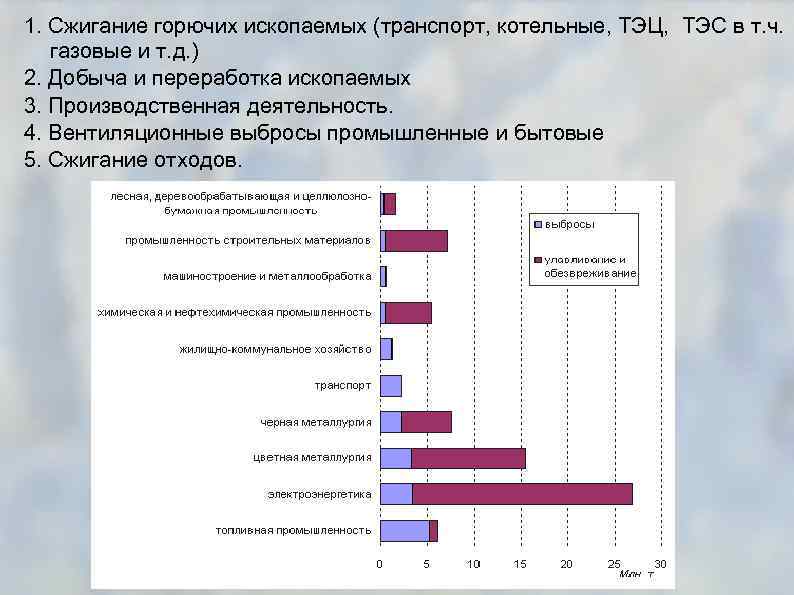
1. Сжигание горючих ископаемых (транспорт, котельные, ТЭЦ, ТЭС в т. ч. газовые и т. д. ) 2. Добыча и переработка ископаемых 3. Производственная деятельность. 4. Вентиляционные выбросы промышленные и бытовые 5. Сжигание отходов.


Основные загрязнители: Оксиды углерода Соединения серы ( оксиды, гидрид, углеводородные) Оксиды азота, аммиак, органические соединения Углеводороды (в т. ч. полициклические ароматические соединения) Альдегиды Тяжёлые металлы (Pb, Cu, Zn, Cd, Cr) Соединения галогенов Атмосферная пыль
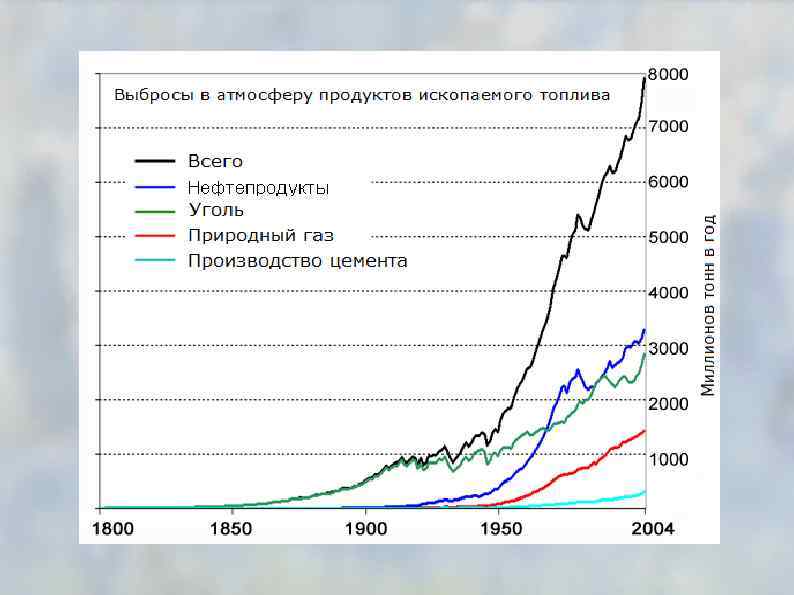
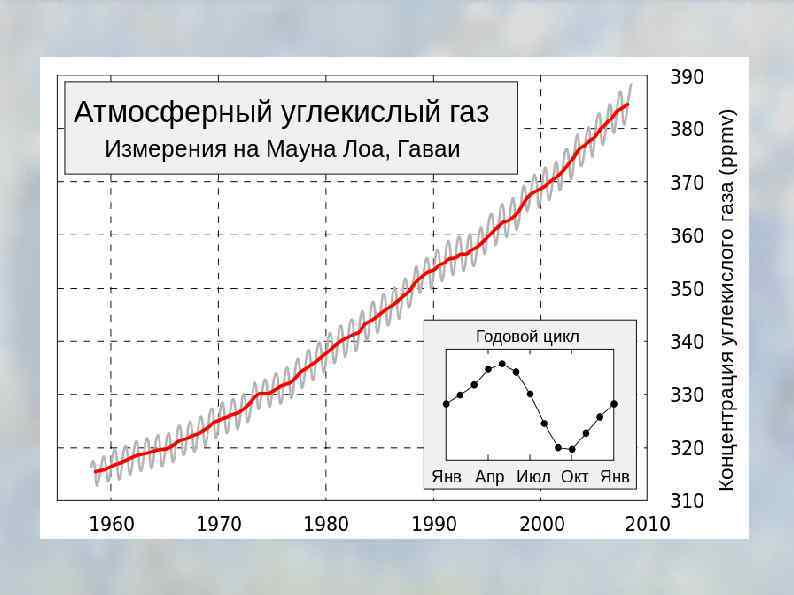

Выбросы в атмосферу при сжигании различных видов топлива: • нетоксичные: углекислый газ, водяной пар (парниковые газы). • вредные вещества: оксид углерода (II), оксиды серы, азота, соединения свинца, сажа, углеводороды, бенз(а)пирен (С 20 Н 12), несгоревшие частицы топлива и т. п.

Горение топлива Идеальная ситуация: Реальная ситуация:

Горение топлива - СО связывает гемоглобин в 210 раз эффективнее О 2

Горение топлива - Промышленные выбросы SO 2 – 200 Мт/год - Природные источники – 300 Мт/год (Эткинс, 1991)

Горение топлива - Промышленные выбросы SO 2 – 200 Мт/год - Природные источники – 300 Мт/год (Эткинс, 1991)
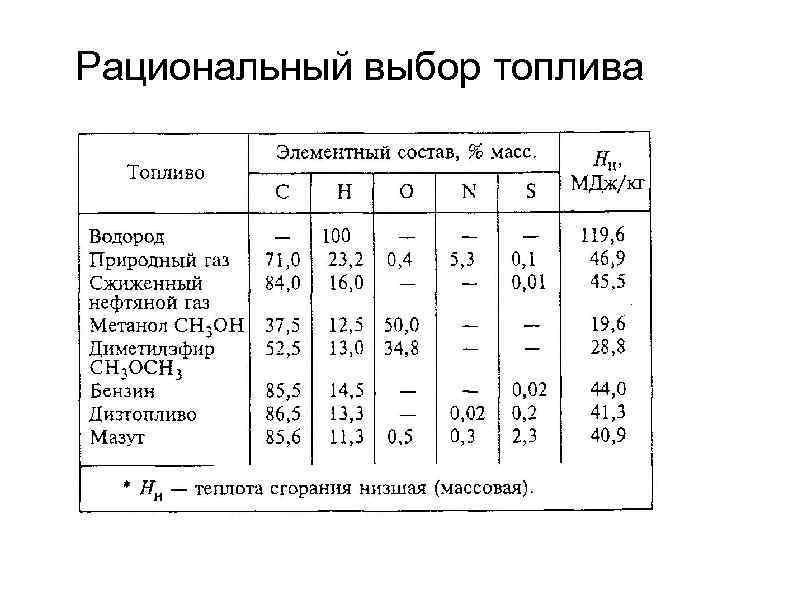
Рациональный выбор топлива
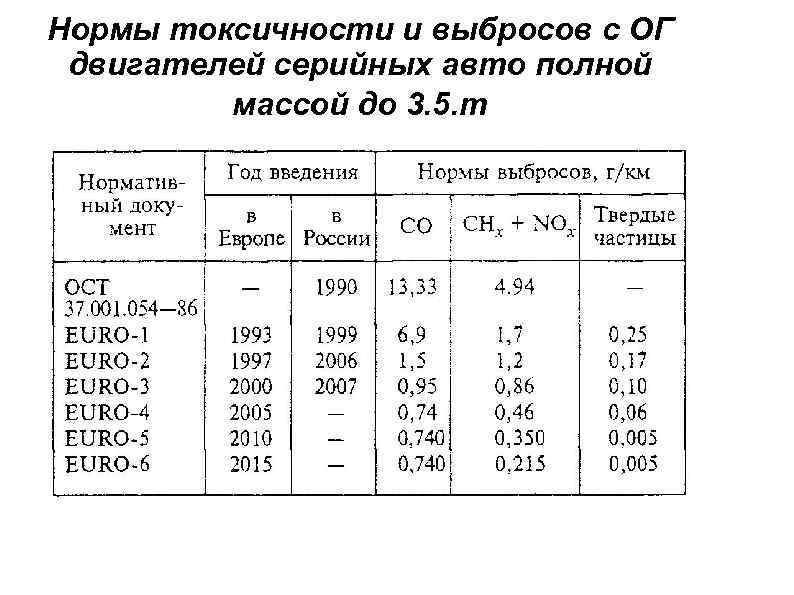
Нормы токсичности и выбросов с ОГ двигателей серийных авто полной массой до 3. 5. т
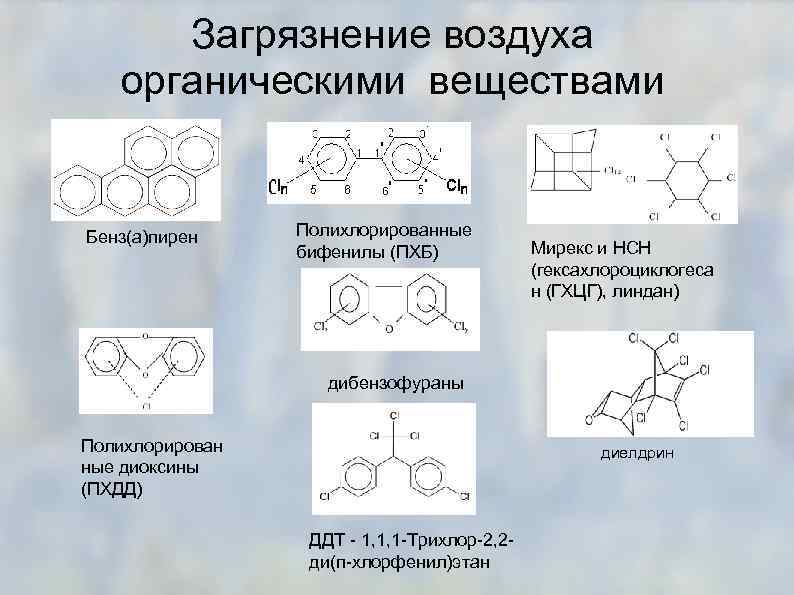
Загрязнение воздуха органическими веществами Бенз(а)пирен Полихлорированные бифенилы (ПХБ) Мирекс и НСН (гексахлороциклогеса н (ГХЦГ), линдан) дибензофураны Полихлорирован ные диоксины (ПХДД) диелдрин ДДТ - 1, 1, 1 -Трихлор-2, 2 ди(п-хлорфенил)этан

Результат загрязнения атмосферы: Локальные Смог Местное отравление почвы, водоёмов Глобальные «Кислотные дожди» «Озоновые дыры» Повышение заболеваемости «Глобальное потепление» Вымирание биоты Снижение прозрачности атмосферы Изменение состава атмосферы

Продукты горения топлива вызывают появление вторичного загрязнения Общая схема образования фотохимического смога в упрощенном виде:

Продукты горения топлива вызывают появление вторичного загрязнения Общая схема образования фотохимического смога в упрощенном виде:

Некоторые составляющие фотохимического смога

Кислотные дожди все виды метеорологических осадков — дождь, снег, град, туман, дождь со снегом, при котором наблюдается понижение p. H дождевых осадков из-за загрязнений воздуха кислотными оксидами (обычно — оксидами серы, оксидами азота) 4 NO 2 + 2 H 2 O + O 2 → 4 HNO 3 CO 2 + H 2 O → H 2 CO 3 SO 2 + H 2 O → H 2 SO 3 + H 2 O → H 2 SO 4 Лес после кислотного дождя
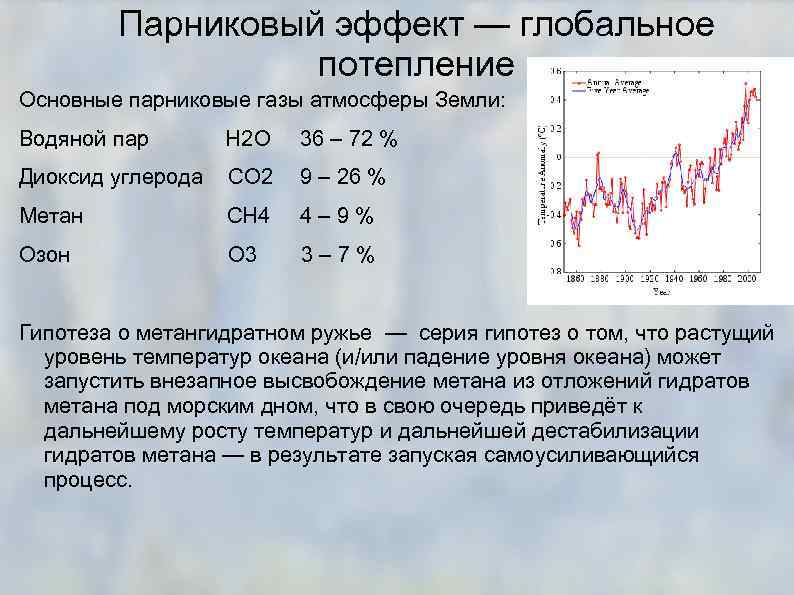
Парниковый эффект — глобальное потепление Основные парниковые газы атмосферы Земли: Водяной пар H 2 O 36 – 72 % Диоксид углерода CO 2 9 – 26 % Метан CH 4 4 – 9 % Озон O 3 3 – 7 % Гипотеза о метангидратном ружье — серия гипотез о том, что растущий уровень температур океана (и/или падение уровня океана) может запустить внезапное высвобождение метана из отложений гидратов метана под морским дном, что в свою очередь приведёт к дальнейшему росту температур и дальнейшей дестабилизации гидратов метана — в результате запуская самоусиливающийся процесс.


выброс углекислого газа, 109 т в год, в атмосферу Фотосинтез растений (чистая продукция). . . . — 77, 61 Фотосинтез растений на суше. . . . . — 52, 86 В том числе фотосинтез в лесах. . . . . — 33, 25 Фотосинтез растений в океане. . . . — 24, 75 Окисление микроорганизмами и животными, лесные и степные пожары. . . . +78 Средняя скорость роста атмосферного СО 2 за период с 1958 по 1976 гг. . . . . +2, 134 Современная скорость роста атмосферного СО 2. . . +2, 3 Выделение СО 2 промышленностью. . . . +5 Выделение СО 2 при уничтожении лесов: . . . . оценка по лесохозяйственным данным ФАО. . . . +1 оценка по росту культурных земель за 1950— 1970 гг. . +1, 3 оценка по сгоранию древесины и окислению гумуса. . . +1, 9 Поглощение СО 2 океаном и биосферой. . . — 4 Выделение СО 2 вулканами. . . +0, 04 Средняя за историю Земли скорость накопления карбонатных осадков. . . . -0, 01 Современная скорость захоронения углерода в донных осадках. . . . . — 0, 085 Выветривание карбонатных и силикатных пород. . . — 0, 01

Глобальное затемнение Последствия: Общее охлаждение планеты Уменьшение испаряемости Перераспределение тепла на планете Усиление глобального потепления вскоре после того, как значительная часть антропогенных выбросов затемняющих веществ прекратится. При этом такое усиление, вероятно, может запустить более мощные процессы, усиливающие глобальное потепление: самопроизвольный выброс десятков миллиардов тонн метана из-под мелководий Арктики и вечных мерзлот.

Нормирование примесей в атмосферном воздухе (мг/м 3) Среднесуточная ПДК Максимально разовая ПДК рабочей зоны ПДК санитарно — защитной зоны Предельно допустимый выброс (ПДВ) (г/с) Временно допустимые концентрации (ВДК) или Ориентировочно безопасный уровень воздействия (ОБУВ).
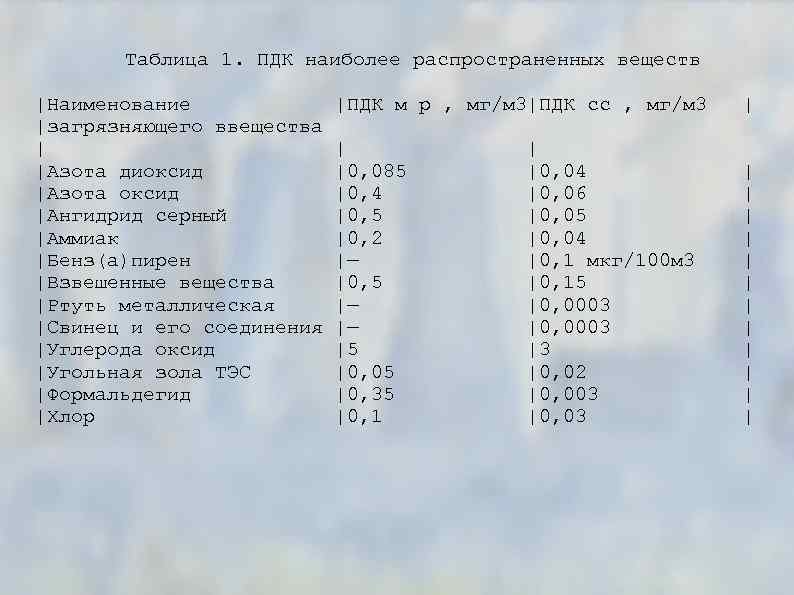
Таблица 1. ПДК наиболее распространенных веществ |Наименование |загрязняющего ввещества | |Азота диоксид |Азота оксид |Ангидрид серный |Аммиак |Бенз(а)пирен |Взвешенные вещества |Ртуть металлическая |Свинец и его соединения |Углерода оксид |Угольная зола ТЭС |Формальдегид |Хлор |ПДК м р , мг/м 3|ПДК сс , мг/м 3 | | |0, 085 |0, 4 |0, 5 |0, 2 |— |0, 5 |— |— |5 |0, 05 |0, 35 |0, 1 | | | |0, 04 |0, 06 |0, 05 |0, 04 |0, 1 мкг/100 м 3 |0, 15 |0, 0003 |3 |0, 02 |0, 003 |0, 03

Условие безразмерной суммарной концентрации при одновременном присутствии в атмосферном воздухе нескольких вредных веществ, обладающих однонаправленным действием (суммацией) Максимальное значение приземной концентрации для горячих точечных источников где Н – высота трубы, м; М – расход выбрасываемого в атмосферу вещества (мощность выбросов), г/с; Тг и Тв – температуры выбрасываемых газов и атмосферного воздуха соответственно; V 1 – полный объем выбрасываемых газов на срезе трубы, м 3/с; А – коэффициент, учитывающий рассеивающие свойства атмосферы, которые определяются климатической зоной (для Московской области А=140); F – коэффициент, учитывающий скорость оседания вредных веществ в атмосфере; m, n – коэффициенты, учитывающие условия выхода газовоздушной среды из устья источника выброса.

Шприцы больших объемов для забора проб воздуха Четырехканальный пробоотборник ОП 4 -42 У Testo-435. Насос-аспиратор Сигнализаторы и анализаторы воздуха
Атмосфера.ppt