(Химия ОС) атмосфера.pptx
- Количество слайдов: 33

Атмосфера – газовая оболочка Земли, связанная с ней силой тяжести и принимающая участие в ее суточном и годовом вращении. Атмосфера – это смесь молекулярных, диссоциированных и ионизированных газов, находящихся на различных высотах, между которыми происходят постоянные реакции, обусловливающие возникновение как более легких, так и тяжелых частиц. Все это приводит к «перемешиванию» атмосферы и к постоянству ее основного состава. Параметры атмосферы: масса 5, 15. 1015 т, высота – 50– 55 км – стратосфера, 2000– 3000 км – экзосфера.

Образование атмосферы
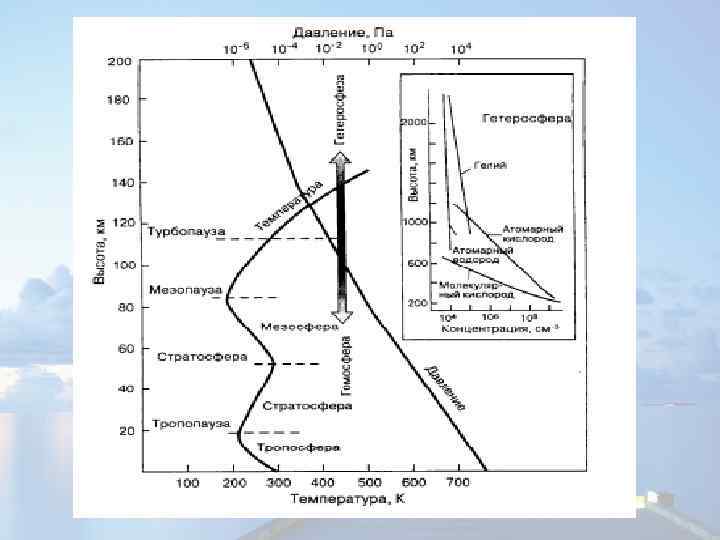

По химическому составу вся атмосфера Земли подразделяется на Øнижнюю – гомосферу (до 100 км), имеющую состав, сходный с приземным воздухом, Øверхнюю – гетеросферу, неоднородного химического состава. Гетеросфера находится настолько высоко (сотни километров), что давление здесь крайне низкое. Граница, которая разделяет эти две части, называется турбопаузой. По физическим свойствам атмосфера имеет ярко выраженное слоистое строение и подразделяется на несколько сфер: ТРОПОСФЕРА – это нижняя часть атмосферы, в которой сосредоточено более 75 % массы всей атмосферы (5. 1018 кг). Ее высота определяется интенсивностью вертикальных (восходящих или нисходящих) потоков воздуха, вызванных нагреванием земной поверхности. На экваторе она простирается до высоты 16– 18 км, в умеренных широтах – до 10– 11 км, а на полюсах – до 8 км. Понижение температуры воздуха с высотой – в среднем на 0, 6 °С на каждые 100 м. Высота 11, 8 км принимается за среднюю границу тропосферы, называемую тропопаузой, которая находится на экваторе на высоте 16– 18 км, над умеренными широтами – до 10– 12 км, а на полюсах – 8– 10 км.
Стратосфера – располагается выше тропосферы до высоты 50– 55 км. В стратосфере находится 20 % всей массы атмосферы. Температура у ее верхней границы повышается, что связано с наличием здесь пояса озона на высотах 20– 30 км в зависимости от широты. Наличие озонового слоя имеет исключительное значение для живых организмов Земли. Мезосфера – верхняя граница этого слоя располагается до высоты 80 км. Главная ее особенность – резкое понижение температуры до – 75– 90 °С у ее верхней границы. Здесь фиксируются серебристые облака, состоящие из ледяных кристаллов. Верхней границей мезосферы является мезопауза, в зоне которой температура достигает ~190 К (– 83 °С). Ионосфера (термосфера) – располагается до высоты 800 км, для нее характерно значительное повышение температуры (более 1000 °С). Под действием ультрафиолетового излучения Солнца газы находятся в ионизированном состоянии. Ионосфера обладает способностью многократно отражать радиоволны, что обеспечивает дальнюю радиосвязь на Земле. Экзосфера – располагается выше 800 км и простирается до 2000– 3000 км. Здесь температура превышает 2000 °С. Скорость движения газов приближается к критической величине 11, 2 км/с. Господствуют атомы водорода и гелия, которые образуют вокруг Земли корону, простирающуюся до высоты 20 тыс. км.

Уравнение баланса между источником газа для атмосферы и его стоком где Fвх. , Fвых – потоки вещества; А – общее количество газа в атмосфере, τ – время пребывания газа в атмосфере 1. вещества с большим временем пребывания могут накапливаться в относительно больших концентрациях; 2. при высоком значении времени пребывания вследствие эффективности перемешивания проявляется высокое постоянство концентрации газа в атмосфере по всему земному шару

Компоненты атмосферы следует разделить на группы: Ø Постоянные (устойчивые компоненты, время пребывания до нескольких тысяч лет): N 2, O 2, Аr и др. Содержание этих составных частей практически не зависит от того, в каком месте взята проба воздуха. Ø Переменные (неустойчивые компоненты, время пребывания порядка 4 -25 лет): СО 2, СH 4, N 2 O. Ø Случайные (сильноизменяющиеся компоненты, время пребывания порядка 2 -10 суток): СО 2, NO, H 2 S, NH 2, НСl и др. Определяются местными условиями (например, около металлургических комбинатов – диоксид серы, в местах разложения органических соединений – аммиак)
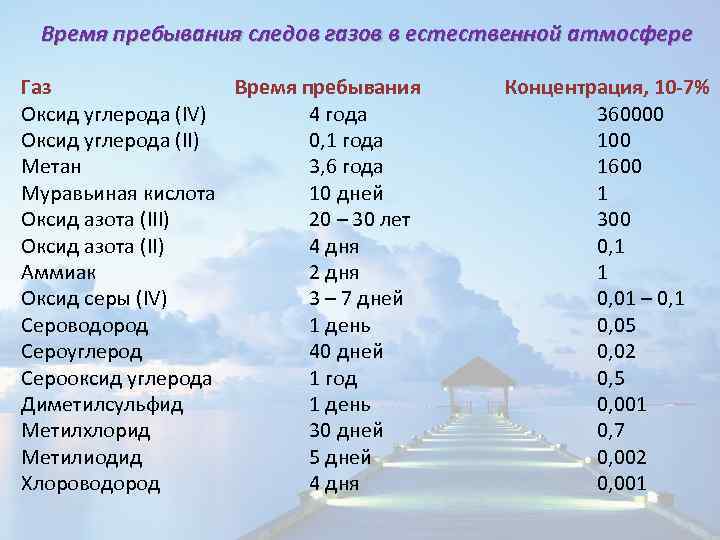
Время пребывания следов газов в естественной атмосфере Газ Время пребывания Оксид углерода (IV) 4 года Оксид углерода (II) 0, 1 года Метан 3, 6 года Муравьиная кислота 10 дней Оксид азота (III) 20 – 30 лет Оксид азота (II) 4 дня Аммиак 2 дня Оксид серы (IV) 3 – 7 дней Сероводород 1 день Сероуглерод 40 дней Серооксид углерода 1 год Диметилсульфид 1 день Метилхлорид 30 дней Метилиодид 5 дней Хлороводород 4 дня Концентрация, 10 -7% 360000 1600 1 300 0, 1 1 0, 01 – 0, 1 0, 05 0, 02 0, 5 0, 001 0, 7 0, 002 0, 001

Источники атмосферных газов Ø геохимические, Ø биологические, Ø антропогенные. ГЕОХИМИЧЕСКИЕ ИСТОЧНИКИ Почвенная эрозия и выветривание горных пород частицы почвы и пород в виде пыли. твердые Капельный унос влаги с поверхности океана растворенные в морской воде соли. Характеризуются довольно высокой реакционной способностью, в частности, являясь одним из источников атмосферного хлороводорода: Вулканическая деятельность частицы вулканической пыли и вулканических газов, содержащих SO 2, CO 2, HCl, HF. В атмосферу с поверхности Земли поступают газообразные продукты радиоактивного распада элементов горных пород – радиоактивных изотопов калия, радия, урана.

БИОЛОГИЧЕСКИЕ ИСТОЧНИКИ (за исключением лесных пожаров) Живой лес играет важную роль в атмосферном звене круговорота газов: кислород и углекислый газ вовлечены в процессы дыхания и фотосинтеза. Лесами выделяется большое количество следовых органических веществ (терпены, органические кислоты, альдегиды и др. ). Лесные пожары являются источником твердых частиц сажи. Мощным источником газов является деятельность микроорганизмов. Процессы микробиологического разложения органического вещества в анаэробных условиях (влажные почвы, пищевой тракт животных) продуцируют метан. Гидролиз мочевины, накапливаемой в почвах, дает аммиак и углекислый газ В результате биохимического окисления аммиака микроорганизмами выделяется оксид азота: 2 Также источники поступления в атмосферу оксида азота (II), свободного азота, аммиака. Результатом деятельности океанических микроорганизмов являются такие соединения, как диметилсульфид (CH 3)2 S и карбонилсульфид COS, хлористый метил, бром- и йодсодержащие органические соединения.
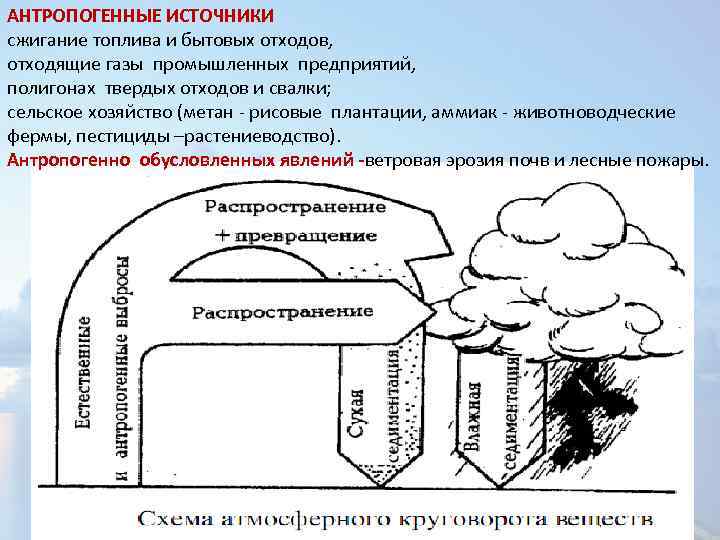
АНТРОПОГЕННЫЕ ИСТОЧНИКИ сжигание топлива и бытовых отходов, отходящие газы промышленных предприятий, полигонах твердых отходов и свалки; сельское хозяйство (метан - рисовые плантации, аммиак - животноводческие фермы, пестициды –растениеводство). Антропогенно обусловленных явлений -ветровая эрозия почв и лесные пожары.

Функции атмосферы – ДЫХАТЕЛЬНАЯ ФУНКЦИЯ – атмосфера содержит кислород, который необходим для дыхания всего живого на планете. – ТЕПЛОРЕГУЛИРУЮЩАЯ ФУНКЦИЯ – газовая оболочка предохраняет Землю от чрезмерного остывания и нагревания. Лучистая энергия Солнца частично поглощается атмосферой. Достигшая поверхности Земли энергия частично поглощается почвой и водоемами, а частично отражается в атмосферу. – РАСПРЕДЕЛЕНИЕ СВЕТА – воздух атмосферы разбивает солнечные лучи на миллион мелких лучей, рассеивает их и создает равномерное освещение. Наличие воздушной оболочки придает нашему небу голубой цвет. – ЗАЩИТНАЯ ФУНКЦИЯ – газовая оболочка спасает все живое на Земле от губительных ультрафиолетовых, рентгеновских и космических лучей. Верхние слои атмосферы частично поглощают, частично рассеивают эти лучи. Защита от крупных и мелких метеоритов. – Обеспечивает ЗВУКОПРОВОДИМОСТЬ – наличие воздуха обеспечивает распространение звука. Без атмосферы не Земле царила бы тишина, не возможна была бы даже человеческая речь.

РЕАКЦИИ, ОБУСЛОВЛИВАЮЩИЕ ЗАЩИТНЫЕ СВОЙСТВА АТМОСФЕРЫ Фотодиссоциация – это диссоциация молекул с образованием свободных радикалов в результате поглощения фотона – нейтральной элементарной частицы, переносчика электромагнитного излучения. Фотон способен произвести химическое воздействие на встретившуюся ему молекулу или атом только в том случае, если обладает достаточной энергией. Например, для фотодиссоциации молекул кислорода требуется 495 к. Дж/моль Фотодиссоциация воды Ионизация – образование ионов из молекул и атомов под действием солнечного излучения (фотоионизация), в меньшей мере – под действием потоков электронов и протонов, идущих от Солнца.

РЕАКЦИИ ИОНОВ В АТМОСФЕРЕ Диссоциативная рекомбинация – реакция иона с электроном с образованием нейтральной молекулы, которая в разреженных условиях верхней атмосферы быстро диссоциирует Перенос заряда – реакции молекулярного иона с нейтральной частицей, сопровождающиеся переносом электрона. Идет только в том случае, если энергия ионизации молекулы, теряющей электрон, меньше энергии ионизации молекулы, образующейся в результате переноса заряда, например: Реакции обмена сопровождаются разрывом химической связи.

Диссоциация кислорода с образованием атомарного кислорода в верхних слоях атмосферы: где O (1 D) – атом кислорода в возбужденном состоянии; O (3 P) – атом кислорода в основном состоянии. В ионосфере на высотах 90 – 200 км основными первичными ионами являются ионы N 2+, O+

Химические реакции в ионосфере

Высота менее 50 км Максимум скорости образования озона - 15 – 35 км. Нулевой цикл озона

Водородный цикл – реакции разложения озона с участием гидроксильных радикалов, которые образуются при фотохимическом разложении молекул воды под действием излучения с длиной волны менее 240 нм: Взаимодействие молекул воды и метана с атомом кислорода: Реакции водородного цикла: Реакции азотного цикла

Хлорный цикл Бромный цикл Общая масса озона в атмосфере составляет 3, 3 · 109 т. Суммарное содержание озона в атмосфере над той или иной территорией обычно приводится в единицах Добсона (е. Д. ) - количество озона в столбе атмосферного воздуха (приведенного к нормальным условиям) единичной площади сечения, соответствующее высоте слоя озона в данном столбе воздуха, равной 10 -5 м. По характеру сезонных колебаний и высотному профилю концентраций озона выделяют три зоны: § полярная зона – характеризуется наибольшими значениями среднегодового общего содержания (около 400 е. Д. ) и концентраций озона, наибольшими сезонными колебаниями; §тропическая зона – среднегодовые значения общего содержания озона невелики (около 265 е. Д. ), сезонные колебания не превышают 10 – 15 %; §средние широты – занимают промежуточное положение, сезонные изменения составляют 30 – 40 % от средних значений.

ХИМИЧЕСКИЕ ПРОЦЕССЫ В ТРОПОСФЕРЕ с участием свободных радикалов ОН-радикал, стимулирующий протекание химических реакций. Этот радикал (ОН·) образуется в результате фотохимически инициируемой реакции разложения озона. При фотолизе О 3 образуется атомарный кислород в электронно-возбужденном состоянии по реакции: ОН-радикал образуется в тропосфере и в результате реакций фотохимического разложения азотсодержащих соединений (HNО 2, НNО 3) и пероксида водорода (Н 2 О 2): Радикалы ОН· участвуют преимущественно в реакциях с оксидами азота, углерода и углеводородами. При взаимодействии радикалов ОН· с оксидами азота образуются азотистая и азотная кислоты:

РЕАКЦИИ ОКИСЛЕНИЯ УГЛЕВОДОРОДОВ Окисление СН 4 под действием ОН· радикалов с последующим протеканием реакций В результате брутто-реакция окисления СН 4 в присутствии NO как катализатора и при воздействии солнечного света с длиной волны 300– 400 нм запишется в виде:

Образующийся при окислении метана формальдегид далее окисляется радикалами ОН· до оксида углерода (II): Оксид углерода (II) является вторичным загрязнителем атмосферы и сравним по количеству с поступлением СО от процессов неполного сгорания природного углеводородного топлива. Оксид серы (IV) в тропосфере, подвергаясь фотохимическому превращению, трансформируется в возбужденные молекулы SO 2* с временем жизни 8 мс: Дальнейшее окисление SO 2* кислородом воздуха ведет к образованию SОЗ К образованию SO 3 приводит также окисление SO 2 под действием НО 2· радикалов:

ГИДРОПЕРОКСИДНЫЙ РАДИКАЛ НО 2· Образуется при взаимодействии атомарного водорода (который образуется при окислении СО до СО 2) с кислородом Образуются также при взаимодействии ОН· с озоном и пероксидом и играют важную роль в химии атмосферы Радикал НО 2· эффективно взаимодействует с оксидом азота с образованием ОН· радикала: Процесс рекомбинации НО 2 · радикалов является основным источником образования атмосферного пероксида водорода:

УЧАСТИЕ ВОДЫ В ХИМИЧЕСКИХ ПРОЦЕССАХ АТМОСФЕРЫ Растворимость SО 2 будет повышаться вследствие взаимодействия его с водой с последующей диссоциацией сернистой кислоты Аналогично повышенная растворимость NО 2 связана с протеканием следующих реакций Растворение формальдегида: Жидкофазное окисление SО 2 под действием пероксида водорода, в присутствии ионов железа и марганца протекает по реакции с образованием серной кислоты

Фотокаталитические реакции компонентов атмосферы можно разделить на две группы: 1) реакции основных компонентов атмосферы, приводящие к образованию следовых соединений; 2) реакции следовых компонентов, приводящие к их удалению из атмосферы. Из ожидаемых фотокаталитических реакций основных компонентов атмосферы можно выделить следующие процессы: 1. Восстановление азота до аммиака и гидразина 2. Окисление азота водой и кислородом воздуха

3. Разложение воды на кислород и водород 4. Окисление воды кислородом с образованием перекиси водорода: 5. Восстановление СО 2 с образованием различных органических соединений, например

Для следовых атмосферных соединений можно ожидать протекания фотокаталитических реакций следующих основных типов: 1. Реакции полного окисления (минерализации) углеводородов, например: 2. Реакции полного окисления (минерализации) галогенсодержащих углеводородов, например

3. Реакции полного окисления (минерализации) кислородсодержащих органических соединений, например, спиртов, фенолов, кислот, кетонов, альдегидов, ПАВ и др. 4. Реакции разложения Н 2 S и NOx 5. Реакция окисления SO 2 6. Другие более сложные реакции, например, селективное окисление некоторых летучих органических веществ:

Цикл азота в атмосфере N 2 O + hν → N 2 + O 2 ( λ ≤ 250 нм) N 2 O + O → N 2 + O 2 или N 2 O + O → 2 NO NO + HO 2 → NO 2 + OH NO + O 3 → NO 2 + O 2 NO 2 + O 3 → NO 3+O 2 NO 2 + hν → NO + O NO 2 + OH → HNO 3+ NO 2 → N 2 O 5 HNO 3 + hν → OH. + NO 2 HNO 3 + OH. → H 2 O + NO 3 HNO 3 + NH 3 → NH 4 NO 3 N 2 O 5 + H 2 O → 2 HNO 3
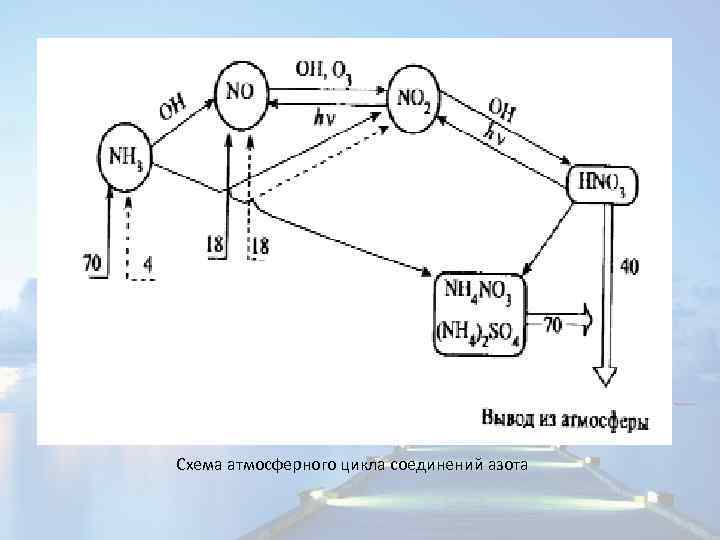
Схема атмосферного цикла соединений азота

Цикл серы в атмосфере H 2 S + OH → H 2 O + HS HS + O 2 → OH + SO SO + HO 2 → SO 2. + OH SO 2 + hν → SO 2* (λ < 400 нм) SO 2* + O 2 → SO 3 + O SO 2 + OH + M → HSO 3 + M HSO 3 + HO 2 → SO 3 + 2 OH SO 2 + HO 2 → SO 3 + OH SO 2 + CH 3 O 2 → SO 3 + CH 3 O SO 2 + O + M → SO 3 + M SO 3 + H 2 O → H 2 SO 4 В результате реакций с аммиаком и ионами металлов серная кислота в атмосфере частично переходит в сульфаты – (NH 4)2 SO 4, Na 2 SO 4, Ca. SO 4. SO 2 + H 2 O = H 2 SO 3 = H+ + HSO 3 - + 2 H+ + SO 32 SO 2 + Ca. O → Ca. SO 3 SO 2 + Mg → Mg. SO 3 Ca. SO 3 + ⅟ 2 O 2 → Ca. SO 4 Mg. SO 3 + ⅟ 2 O 2 → Mg. SO 4
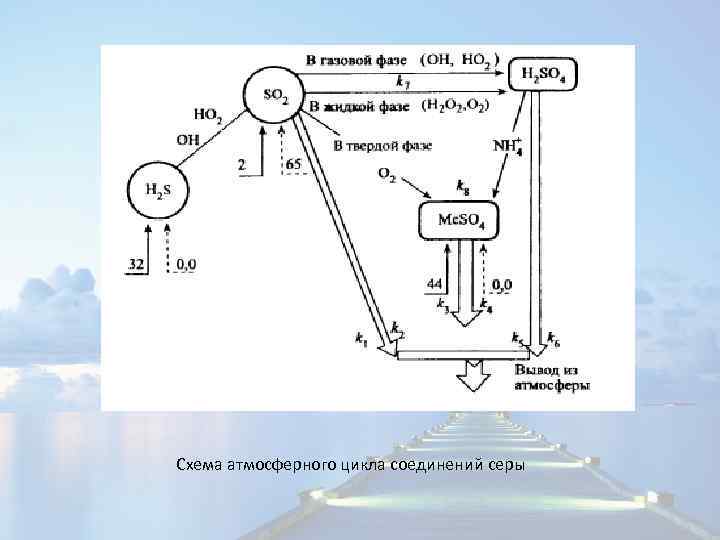
Схема атмосферного цикла соединений серы

КИСЛОТНЫЕ ДОЖДИ http: //grandhdcns. net/smotretvideo/164489300 -50351478/
(Химия ОС) атмосфера.pptx